PEMANFAATAN KEMBALI ZEOLIT ALAM SETELAH MENGALAMI PROSES REGENERASI SEBAGAI PENYERAP LOGAM Cu (TEMBAGA) DAN
Zn (SENG) DI DALAM AIR LIMBAH INDUSTRI PERTAMBANGAN EMAS
SKRIPSI
FASMA RIANA SARAGIH 080802066
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PEMANFAATAN KEMBALI ZEOLIT ALAM SETELAH MENGALAMI PROSES REGENERASI SEBAGAI PENYERAP LOGAM Cu (TEMBAGA) DAN
Zn (SENG) DI DALAM AIR LIMBAH INDUSTRI PERTAMBANGAN EMAS
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana sains
FASMA RIANA SARAGIH 080802066
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PEMANFAATAN KEMBALI ZEOLIT ALAM SETELAH
MENGALAMI PROSES REGENERASI SEBAGAI PENYERAP LOGAM Cu (TEMBAGA) DAN Zn (SENG) DI DALAM AIR
LIMBAH INDUSTRI PERTAMBANGAN EMAS
Kategori : SKRIPSI
Nama : Fasma Riana Saragih
NIM : 080802066
Program studi : SARJANA (S-1) KIMIA Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA)
UNIVERSITAS SUMATERA UTARA
Diluluskan di,
Medan, Juli 2013
Komisi Pembimbing :
Dosen Pembimbing 2 Dosen Pembimbing 1
Prof. Dr. Zul Alfian Prof. Dr. Harlem Marpaung
NIP. 195504051983031002 NIP. 194804141974131001
Diketahui/Disetujui oleh,
Departemen kimia FMIPA USU
Ketua,
Dr. Rumondang Bulan, MS
PEMANFAATAN KEMBALI ZEOLIT ALAM SETELAH MENGALAMI PROSES REGENERASI SEBAGAI PENYERAP LOGAM Cu (TEMBAGA) DAN
Zn (SENG) DI DALAM AIR LIMBAH INDUSTRI PERTAMBANGAN EMAS
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa
kutipan dan ringkasan-ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2013
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus, atas berkat dan kasih
karunia-Nya sehingga penyusunan skripsi ini dapat selesai dengan baik.
Rasa terimakasih yang begitu besar penulis sampaikan kepada orangtua terkasih,
ayahku tersayang Lesmar Saragih dan ibuku tercinta Kemerlina br. Purba atas doa dan
kasih sayang yang tak henti-hentinya diberikan kepada penulis selama ini, juga untuk
saudaraku terkasih abang Saud Daniel Saragih, serta adik-adikku Abdi Leonardo
Saragih dan Dina Febrina Saragih untuk dukungan semangat yang telah diberikan.
Ucapan terimakasih juga penulis sampaikan kepada bapak Prof. Dr. Harlem Marpaung
selaku pembimbing 1 dan kepada bapak Prof. Dr. Zul Alfian selaku pembimbing 2
yang telah mau meluangkan waktunya untuk memberikan bimbingan dan saran yang
sangat membantu kepada penulis selama penelitian dan proses penyelesaian skripsi ini.
Dan juga ucapan terimakasih kepada bapak Prof. Dr. Basuki Wiryosentono selaku
dosen wali yang telah membantu penulis selama mengikuti perkuliahan, serta ucapan
terimakasih kepada ibu Dr. Rumondang Bulan, MS dan bapak Drs. Albert Pasaribu
selaku ketua dan sekretaris Departemen Kimia FMIPA USU.
Dan juga tidak lupa ucapan terimakasih untuk seluruh rekan-rekan seperjuangan
stambuk 2008 terkhusus Christiana, Samaria, Pelita, Nurmaya, Julianti, Jontinus,
Rizal, Christou, Oktavianus, dan Paulus yang telah menjadi sahabat selayaknya
saudara. Dan rasa terimakasih juga penulis sampaikan untuk asisten laboratorium
Kimia Analitik (Bella, Indah, Rehmalem, Roiman, Desta, Emilia, dan Juliana) yang
telah banyak membantu selama penulis melakukan penelitian. Serta tak lupa ucapan
terimakasih untuk adik-adik asisten laboratorium kimia Anorganik (Louis, Fantoso,
Nabila, Mars, Tio, Suwandi dan Rahel) untuk semua keceriaan yang diberikan.
Pemanfaatan zeolit alam Sarulla yang telah mengalami aktivasi dengan penambahan HCl 15% dan dilanjutkan dengan pemanasan pada suhu 300oC selama 3 jam sebagai penyerap logam Cu dan Zn di dalam air limbah industri pertambangan emas yang berasal dari daerah Tapanuli Selatan telah dilakukan. Zeolit alam aktif yang telah dipakai untuk menyerap logam Cu dan Zn di dalam air limbah industri pertambangan emas dipakai kembali sebagai penyerap setelah dilakukan proses regenerasi dan ditentukan besarnya penyerapan yang terjadi. Proses regenerasi yang dilakukan sama dengan proses aktivasi. Hasil yang diperoleh menunjukkan bahwa penyerapan zeolit alam terhadap logam Cu setelah diregenerasi pada kisaran 81,59% - 83,91% dan Seng pada kisaran 77,64% - 83,28%. Dimana setelah 3 kali pemakaian penyerapan zeolit alam terhadap logam Cu sebesar 81,59% dan Zn sebesar 77,64%.
Dari penelitian ini dapat disimpulkan bahwa zeolit alam sebelum dan setelah penggunaan kembali sampai 3 kali pemakaian tidak menunjukkan perbedaan yang jauh.
ABSTRACT
The use of natural zeolite of sarulla from North Tapanuli after undergoing activation proccess by addition of HCl 15% and heated 300oC for 3 hours to remove Copper and Zink in the waste water of gold mining of South Tapanuli has been studied. The used of the zeolite was applied again to remove those metals to determined the amount of metals remove. It was found that the zeolite removed Copper in the range of 81,59% – 83,91% and Zink in the range of 77,64% - 83,28%. Wheres after three times used the Copper was removed 81,59 and Zink of 77,64%.
DAFTAR ISI
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak v
Abstract vi
Daftar Isi vii
Daftar Tabel x
Daftar Gambar xi
BAB I. PENDAHULUAN
1.1 Latar Belakang 1
1.2 Permasalahan 3
1.3 Pembatasan Masalah 4
1.4 Tujuan Penelitian 4
1.5 Manfaat Penelitian 4
1.6 Lokasi Penelitian 5
1.7 Metodologi Penelitian 5
BAB II. TINJAUAN PUSTAKA
2.1 Zeolit Alam 6
2.1.1 Aktivasi Zeolit Alam 8
2.1.2 Zeolit Sebagai Adsorben 10
2.2 Adsorpsi 11
2.2.1 Jenis-jenis Adsorpsi 11
2.2.2 Isoterm Adsorpsi 12
2.3 Pencemaran Lingkungan akibat Limbah Industri 13
2.5 Toksisitas Logam Berat 15
2.5.1 Tembaga (Cu) 16
2.5.2 Seng (Zn) 17
2.6 Spektrofotometer Serapan Atom 18
2.6.1 Prinsip Dasar Spektrofotometer Serapan Atom 18
2.6.2 Cara Kerja Spektrofotometer Serapan Atom 19
2.6.3 Keuntungan Penggunaan metode Spektrofotometer
Serapan Atom 19
BAB III. Metodologi Penelitian
3.1 Alat 20
3.2 Bahan 21
3.3 Prosedur Penelitian
3.3.1 Pembuatan Larutan HCl 15% 21
3.3.2 Penyediaan Zeolit Alam 21
3.3.3 Pengaktifan Zeolit Alam 21
3.3.4 Pembuatan Larutan Standar Cu 22
3.3.5 Pembuatan Larutan Standar Zn 22
3.3.6 Pembuatan Kurva Kalibrasi 23
3.3.7 Penyerapan Kandungan Cu dan Zn di dalam air
limbah industri oleh Zeolit Alam Teraktivasi 23
3.3.8 Regenerasi Zeolit Alam 24
3.3.9 Penyerapan Kandungan Cu dan Zn di dalam air
limbah industri oleh Zeolit Alam Teregenerasi 24
3.4 Bagan Penelitian
3.4.1 Penyediaan Zeolit Alam 26
3.4.2 Pengaktifan Zeolit 26
3.4.3 Pembuatan Kurva Kalibrasi Cu 27
3.4.4 Pembuatan Kurva Kalibrasi Zn 28
3.4.5 Penyerapan Logam Cu dan Zn oleh Zeolit Alam
3.4.7 Penyerapan Logam Cu dan Zn oleh Zeolit Alam
Teregenerasi 31
BAB IV. Hasil Dan Pembahasan
4.1 Hasil Penelitian 32
4.1.1 Penentuan Logam Cu 33
4.1.2 Penentuan Logam Zn 38
4.2 Pembahasan 44
BAB V. Kesimpulan Dan Saran
5.1 Kesimpulan 48
5.2 Saran 48
DAFTAR PUSTAKA 49
DAFTAR TABEL
TABEL 4.1.Data Absorbansi dari larutan seri standar Cu 33
TABEL 4.2.Penurunan Persamaan Garis Regresi untuk
Penentuan Konsentrasi Cu 34
TABEL 4.3.Data Absorbansi dari Larutan Seri Standar Zn 38
TABEL 4.4.Penurunan Persamaan Garis Regresi untuk
Penentuan Konsentrasi Zn 39
TABEL 1. Data Absorbansi Cu di dalam 100 mL Sampel Air
Limbah Sebelum dan Sesudah Penambahan Zeolit Alam
Aktif dan Zeolit Alam Yang Telah Diregenerasi
dengan Variasi Berat Zeolit 52
TABEL 2. Data Konsentrasi Cu di dalam 100 mL Sampel Air
Limbah Setelah Penambahan Zeolit Alam Aktif dan
Zeolit Alam yang Telah Diregenerasi dengan Variasi
Berat Zeolit 53
TABEL 3. Data Persentase Cu yang Terserap Setelah
Penambahan Zeolit Alam Aktif dan Zeolit Alam
yang Telah Diregenerasi 54
TABEL 4. Data Absorbansi Zn di dalam 100 mL Sampel Air
Limbah Sebelum dan Sesudah Penambahan Zeolit Alam
Aktif dan Zeolit Alam yang Telah Diregenerasi dengan
Variasi Berat Zeolit 55
TABEL 5. Data Konsentrasi Zn di dalam 100 mL Sampel Air
Limbah Setelah Penambahan Zeolit Alam Aktif dan
Zeolit Alam yang Telah Diregenerasi dengan Variasi
Berat Zeolit 56
TABEL 6. Data Persentase Zn yang Terserap Setelah
Penambahan Zeolit Alam Aktif dan Zeolit Alam
Gambar 4.1. Kurva kalibrasi larutan seri standar Cu 33
ABSTRAK
Pemanfaatan zeolit alam Sarulla yang telah mengalami aktivasi dengan penambahan HCl 15% dan dilanjutkan dengan pemanasan pada suhu 300oC selama 3 jam sebagai penyerap logam Cu dan Zn di dalam air limbah industri pertambangan emas yang berasal dari daerah Tapanuli Selatan telah dilakukan. Zeolit alam aktif yang telah dipakai untuk menyerap logam Cu dan Zn di dalam air limbah industri pertambangan emas dipakai kembali sebagai penyerap setelah dilakukan proses regenerasi dan ditentukan besarnya penyerapan yang terjadi. Proses regenerasi yang dilakukan sama dengan proses aktivasi. Hasil yang diperoleh menunjukkan bahwa penyerapan zeolit alam terhadap logam Cu setelah diregenerasi pada kisaran 81,59% - 83,91% dan Seng pada kisaran 77,64% - 83,28%. Dimana setelah 3 kali pemakaian penyerapan zeolit alam terhadap logam Cu sebesar 81,59% dan Zn sebesar 77,64%.
Dari penelitian ini dapat disimpulkan bahwa zeolit alam sebelum dan setelah penggunaan kembali sampai 3 kali pemakaian tidak menunjukkan perbedaan yang jauh.
The use of natural zeolite of sarulla from North Tapanuli after undergoing activation proccess by addition of HCl 15% and heated 300oC for 3 hours to remove Copper and Zink in the waste water of gold mining of South Tapanuli has been studied. The used of the zeolite was applied again to remove those metals to determined the amount of metals remove. It was found that the zeolite removed Copper in the range of 81,59% – 83,91% and Zink in the range of 77,64% - 83,28%. Wheres after three times used the Copper was removed 81,59 and Zink of 77,64%.
1.7 Metodologi Penelitian
1. Penelitian ini merupakan riset laboratorium yang bersifat purposif.
2. Zeolit diambil dari daerah Sarulla Kecamatan Pahae, Kabupaten Tapanuli Utara,
sedangkan sampel air limbah industri diambil dari Industri Pertambangan Emas,
di Kabupaen Tapanuli Selatan.
3. Zeolit diaktivasi secara kimia menggunakan HCl 15%, dan diikuti dengan
aktivasi fisika melalui pemanasan pada suhu 300oC.
4. Zeolit diregenerasi menggunakan perlakuan yang sama dengan proses aktivasi
yaitu dengan penambahan HCl 15%, dan diikuti dengan pemanasan pada suhu
300oC.
5. Zeolit diregenerasi sebanyak 2 (dua) kali berturut-turut dengan menggunakan
perlakuan yang sama.
6. Lamanya waktu aktivasi dan regenerasi menggunakan HCl 15% adalah 24 jam,
dan lamanya waktu pemanasan pada suhu 300oC adalah 3 jam.
7. Penentuan kandungan logam Cu dan Zn di dalam sampel air limbah limbah
sebelum dan sesudah penambahan zeolit aktif dan regenerasinya dilakukan
BAB 2
TINJAUAN PUSTAKA
Indonesia merupakan negara yang dikenal memiliki jumlah yang cukup besar dan
beragam berbagai sumberdaya mineral dan tersebar di beberapa provinsi. Salah satu
sumberdaya mineral yang patut diperhatikan adalah zeolit alam dan juga logam mulia
emas dan perak. Dalam bab ini akan dibicarakan secara singkat materi yang berkaitan
dengan penelitian.
2.1 ZEOLIT ALAM
Zeolit adalah mineral kristal alumina silika tetrahidrat berpori yang mempunyai
struktur kerangka tiga dimensi, terbentuk oleh tetrahedral [SiO4]4- dan [AlO4]5- yang
saling terhubungkan oleh atom-atom oksigen sedemikian rupa, sehingga membentuk
kerangka tiga dimensi terbuka yang megandung kanal-kanal dan rongga-rongga, yang
di dalamnya terisi oleh ion-ion logam, biasanya adalah ogam-logam alkali atau alkali
tanah dan molekul air yang dapat bergerak bebas (Lestari, 2010).
Rumus umum zeolit adalah :
Mx/n[(AlO2)x(SiO2)y].mH2O
Dimana M adalah kation bervalensi n, (AlO2)x(SiO2)y adalah kerangka zeolit yang
bermuatan negatif, H2O adalah molekul air yang terhidrat dalam kerangka zeolit.
Zeolit banyak ditemukan dalam batuan. Kerangka dasar struktur zeolit terdiri
dari unit-unit tetrahedral AlO45- dan SiO44- yang saling berhubungan melalui atom O
struktur kristal sedangkan logam alkali atau alkali tanah merupakan sumber kation
yang dapat dipertukarkan. Kerangka struktur tiga dimensi senyawa alumina silikat
terdiri atas dua bagian, yaitu bagian netral dan bagian bermuatan. Bagian netral
sematamata dibangun oleh silikon dan oksigen dan jenisnya bervariasi antara SiO4
4-sampai SiO2 dengan perbandingan Si:O dari 1:4 sampai 1:2. Bagian bermuatan
dibangun oleh ion aluminium yang kecil dan oksigen. Dalam bagian ini terjadi
penggantian ion pusat silikon bervalensi empat dengan kation aluminium yang
bervalensi tiga, sehingga setiap penggantian ion silikon dan ion aluminium
memerlukan satu ion logam alkali atau alkali tanah yang monovalen atau setengah ion
logam divalen, seperti : Na+, K+, Ca2+, Mg2+, Ba2+, Sr2+, dan lain-lain untuk
menetralkan muatan listriknya (Lestari, 2010).
Zeolit mempunyai sifat fisika dan kimia yang unik, sehingga zeolit dijadikan
sebagai mineral serba guna. Sifat-sifat unik tersebut meliputi dehidrasi, adsorben dan
penyaring molekul, katalisator, dan penukar ion. Zeolit mempunyai
sifat dehidrasi (melepaskan molekul H2O) apabila dipanaskan. Pada umumnya struktur
kerangka zeolit akan menyusut. Tetapi kerangka dasarnya tidak mengalami perubahan
secara nyata. Disini molekul H2O seolah-olah mempunyai posisi yang spesifik dan
dapat dikeluarkan secara reversibel. Sifat zeolit sebagai adsorben dan penyaring
molekul, dimungkinkan karena struktur zeolit yang berongga, sehingga zeolit mampu
menyerap sejumlah besar molekul yang berukuran lebih kecil atau sesuai dengan
ukuran rongganya. Selain itu kristal zeolit yang telah terdehidrasi merupakan adsorben
yang selektif dan mempunyai efektivitas adsorpsi yang tinggi. Zeolit juga mempunyai
kemampuan sebagai katalis berkaitan dengan tersedianya pusat-pusat aktif dalam
saluran antar zeolit. Pusat-pusat aktif tersebut terbentuk karena adanya gugus fungsi
asam tipe Bronsted maupun Lewis. Perbandingan kedua jenis asam ini tergantung pada
proses aktivasi zeolit dan kondisi reaksi. Pusat-pusat aktif yang bersifat asam ini
selanjutnya dapat mengikat molekul-molekul basa secara kimiawi. Sedangkan sifat
zeolit sebagai penukar ion karena adanya kation logam alkali dan alkali tanah. Kation
tersebut dapat bergerak bebas didalam rongga dan dapat dipertukarkan dengan kation
logam lain dengan jumlah yang sama. Akibat struktur zeolit berongga, anion atau
molekul berukuran lebih kecil atau sama dengan rongga dapat masuk dan terjebak.
Di Indonesia, jumlah zeolit sangat melimpah dan tersebar di berbagai daerah
baik di pulau Jawa, Sumatera, dan Sulawesi. Pemanfaatan zeolit Indonesia untuk
penggunaan secara langsung belum dapat dilakukan, karena zeolit Indonesia banyak
mengandung campuran (impurities) sehingga perlu dilakukan pengolahan terlebih
dahulu untuk menghilangkan atau memisahkannya dari pengotor-pengotor. Pada
penelitian ini zeolit alam yang digunakan berasal dari daerah Sarulla, Kecamatan
Pahae, kabupaten Tapanuli Tengah.
2.1.1 Aktivasi Zeolit Alam
Peningkatan mutu zeolit alam melalui proses aktivasi dan modifikasi dimaksudkan
untuk memperbesar kemampuan zeolit baik dari segi daya katalis, adsorben, maupun
pertukaran kation. Proses aktivasi zeolit alam dapat dikelompokkan ke dalam dua cara,
yaitu aktivasi secara fisika dan aktivasi secara kimia (Fatimah, 2000).
Pada zeolit alam, adanya molekul air dalam pori dan oksida bebas di
permukaan seperti Al2O3, SiO2, CaO, MgO, Na2O, K2O dapat menutupi pori-pori atau
situs aktif dari zeolit sehingga dapat menurunkan kapasitas adsorpsi maupun sifat
katalisis dari zeolit tersebut. Inilah alasan mengapa zeolit alam perlu diaktivasi terlebih
dahulu sebelum digunakan. Aktivasi secara fisika dapat dilakukan dengan pemanasan
pada suhu 300 - 400oC dengan udara panas atau dengan sistem vakum untuk
melepaskan molekul air. Sedangkan aktivasi secara kimia dilakukan melalui pencucian
zeolit dengan larutan asam-asam organik seperti HF, HCl dan H2SO4 atau Na2EDTA
untuk menghilangkan oksida-oksida pengotor yang menutupi permukaan pori.
Aktivasi dengan perlakuan asam menyebabkan terjadinya dealuminasi dan
dekationasi. Aktivasi dengan HCl menyebabkan keluarnya Al dan kation-kation (Mn+)
dalam kerangka menjadi Al dan kation-kation non kerangka. Begitu pula dengan
HNO3, H2SO4, dan H3PO4 juga mengalami dealuminasi dan dekationisasi pada
kerangka zeolit. Zeolit dapat terdealuminasi dengan perlakuan asam menggunakan
dealuminasi terbesar pada konsentrasi 4-10 N dengan berkurangnya sebagian besar
alumunium kerangka. Terjadinya proses dealuminasi akan menyebabkan
bertambahnya luas permukaan zeolit karena berkurangnya logam pengotor yang
menutupi pori-pori zeolit. Dengan bertambahnya luas permukaan tersebut maka akan
mengakibatkan proses penyerapan yang terjadi semakin besar(Heraldy, 2003).
Menurut penelitian yang dilakukan oleh Rivan (2011) terhadap pengaruh
konsentrasi HCl dan H2SO4 terhadap daya adsorpsi zeolit alam, menunjukkan bahwa
kapasitas adsorpsi zeolit alam yang paling optimum sebagai adsorben logam Co dan
Ni di dalam larutan standar terjadi pada penambahan HCl 4 N, dan pada penambahan
H2SO4 2 N. Sedangkan penelitian yang dilakukan oleh Vera (2011) menunjukkan
bahwa zeolit alam yang aktivasi secara fisika dengan pemanasan pada suhu 300oC
merupakan suhu aktivasi yang paling optimum, dimana pada suhu aktivasi di atas
300oC zeolit mengalami destruksi sehingga kehilangan sifat-sifatnya.
Penelitian yang dilakukan oleh Heraldy (2003) juga menunjukkan bahwa
aktivasi zeolit alam yang paling efektif sebagai adsorben logam Zn dalam limbah
elektroplating adalah dengan penambahan HCl. Dimana aktivasi dengan perlakuan
asam akan meningkatkan karakter rasio Si/Al, keasaman, luas permukaan, dan
pengurangan sebagian komposisi logamnya. Tingkat keasamandari suatu adsorben
akan menunjukkan banyaknya H+ yang terikat pada struktur zeolit. Hasil analisis
keasaaman menunjukkan bahwa pengaruh aktivasi dengan perlakuan asam akan
meningkatn keasaman dari zeolit alam. Semakin besar keasaman akan meningkatkan
situs aktif dari adsorpsi. Hal ini dibuktikan dengan bertambahnya konsentrasi Zn yang
tersadsorpsi oleh zeolit alam aktif.
Pada penelitian ini proses aktivasi dan regenerasi dilakukan dengan
menggunakan metode yang sama yaitu dengan penambahan HCl 15% dan dilanjutkan
Zeolit yang terdehidrasi akan mempunyai struktur pori terbuka dengan internal surface
area yang besar sehingga kemampuan mengadsorpsi molekul selain air semakin
tinggi. Ukuran cincin dari jendela yang menuju rongga menentukan ukuran molekul
yang dapat teradsorpsi. Sifat ini yang menjadikan zeolit mempunyai kemampuan
penyaringan yang sangat spesifik yang dapat digunakan untuk pemurnian dan
pemisahan. Pada penelitian ini zeolit alam yang telah diaktivasi dan diregenerasi
diaplikasikan secara langsung sebagai adsorben logam Cu dan Zn di dalam air limbah
industri pertambangan emas.
Kapasitas yang tinggi sebagai penyerap menyebabkan zeolit dapat memisahkan
molekul-molekul berdasarkan ukuran dan konfigurasi dari molekul. Mekanisme
adsorpsi yang mungkin terjadi adalah adsorpsi fisika (melibatkan gaya Van der Walls),
adsorpsi kimia (melibatkan gaya elektrostatik), ikatan hidrogen dan pembentukan
kompleks koordinasi (Poerwadio, A.D, 2004).
Penelitian yang dilakukan oleh Rivan (2011) menunjukkan bahwa kapasitas
adsorpsi yang paling optimum terhadap penyerapan logam Co dan Ni oleh zeolit alam
yang diaktivasi dengan HCl berada pada konsentrasi 4 N yaitu sebesar 93,26% dan
93,70% dan kapasitas adsorpsi yang paling optimum terhadap penyerapan logam Co
dan Ni oleh zeolit alam yang diaktivasi menggunakan H2SO4 berada pada konsentrasi
2 N yaitu sebesar 95,02% dan 96,18%. Sedangkan penelitian yang dilakukan oleh Vera
(2011) menunjukkan bahwa kapasitas adsorpsi zeolit alam terhadap logam Cu dan Fe
di dalam limbah cair industri sarung tangan yang paling optimum terjadi pada
penambahan zeolit aktif yang diaktivasi pada suhu 300oC dengan dosis zeolit 100 g
dalam 100 mL larutan sampel yaitu sebesar 79,55% dan 87,40%.
2.2 Adsorpsi
Adsorpsi adalah proses dimana satu atau lebih unsur-unsur pokok dari suatu larutan
fluida akan lebih terkonsentrasi pada permukaan suatu padatan tertentu (adsorbent).
dari satu atau lebih larutan antara fasa cair dan partikel. Permukaan adsorben pada
umumnya secara fisika maupun kimia heterogen dan energi ikatan sangat mungkin
berbeda antara satu titik dengan titik lainnya.
Salah satu metode yang digunakan untuk menghilangkan zat pencemar dari air
limbah adalah adsorpsi.zat yang teradsorpsi merupakan fase teradsorpsi (adsorbat) dan
zat yang mengadsorpsi disebut adsorben. Adsorben pada umumnya adalah zat padat
yang berongga, seperti zeolit (Agustiningtyas, 2012).
Terdapat dua metode adsorpsi yaitu tumpak (batch) dan lapik tetap (fixed bed).
Pada metode tumpak larutan contoh dicampurkan dan dikocok dengan bahan penyerap
sampai tercapai kestimbangan. Sedangkan metode lapik tetap merupakan metode
adsorpsi dengan menempatkan adsorben dalam kolom sebagai lapik dan adsorbat
dialirkan ke dalam kolom tersebut sebagai influen. Larutan yang keluar dari kolom
merupakan sisa larutan yang tidak teradsorpsi yang disebut efluen (Agustiningtyas,
2012).
2.2.1 Jenis-jenis adsorpsi
Jenis adsorpsi yang umum dikenal adalah adsorpsi kimia (kemisorpsi) dan adsorpsi
fisika (fisisorpsi). Adsorpsi kimia (Kemisorpsi) merupakan Adsorpsi yang terjadi
karena adanya gaya kimia dan diikuti oleh reaksi kimia. Adsorpsi jenis ini
menyebabkan terbentuknya ikatan secara kimia. Maka adsorpsi jenis ini akan
menghasilkan produksi reaksi berupa senyawa yang baru. Ikatan kimia yang terjadi
pada kemisorpsi sangat kuat mengikat molekul gas atau cairan dengan permukaan
padatan sehingga sangat sulit untuk dilepaskan (irreversibel). Sedangkan Adsorpsi
fisika (Fisisorpsi) adalah Adsorpsi yang terjadi karena adanya gaya-gaya fisika.
Molekul-molekul yang diadsorpsi secara fisika tidak terikat kuat pada permukaan, dan
biasanya terjadi proses balik yang cepat (reversibel), sehingga mudah untuk diganti
dengan molekul yang lain. Adsorpsi fisika didasarkan pada gaya Van Der waals dan
dapat terjadi pada permukaan yang polar dan non polar. Adsorpsi juga mungkin terjadi
akan mengikat ion-ion yang diadsorpsi dengan ikatan secara kimia, tetapi ikatan ini
mudah dilepaskan kembali untuk dapat terjadinya pertukaran ion (Atkins P.W, 1978).
2.2.2 Isoterm Adsorpsi
Isoterm adsorpsi adalah hubungan yang menunjukkan distribusi adsorben antara fasa
teradsorpsi pada permukaan adsorben dengan fasa ruah saat kesetimbangan pada
temperatur tertentu. Ada tiga jenis hubungan matematik yang umumnya digunakan
untuk menjelaskan isoterm adsorpsi.
1. Isoterm Brunauer, Emmet, and Teller (BET)
Isoterm ini berdasarkan asumsi bahwa adsorben mempunyai permukaan yang
homogen. Dan molekul-molekul adsorbat bisa membentuk lebih dari satu lapisan
adsorbat di permukaannya.
2. Isoterm Langmuir
Isoterm ini hampir sama dengan isoterm BET hanya saja yang membedakan adalah
pada isoterm ini hanya membentuk satu lapisan adsorbat di permukaannya.
3. Isoterm Freundlich
Isoterm ini berasumsi bahwa adsorben mempunyai permukaan yang heterogen dan
tiap molekul mempunyai potensi penyerapan yang berbeda-beda. Dari isoterm ini,
2.3 Pencemaran Lingkungan akibat Limbah Industri
Pencemaran atau polusi adalah suatu kondisi yang telah berubah dari bentuk asal
kekeadaan yang lebih buruk. Pergeseran bentuk tatanan dan kondisi asal pada kondisi
yang buruk ini dapat terjadi sebagai akibat masuknya bahan-bahan pencemar atau
polutan. Bahan polutan tersebut pada umumnya mempunyai sifat racun (toksik) yang
berbahaya bagi organisme hidup. Toksisitas atau daya racun dari polutan itulah yang
kemudian menjadi pemicu terjadinya pencemaran (Palar, 2004).
Suatu lingkungan hidup dikatakan tercemar apabila telah terjadi
perubahan-perubahan dalam tatanan lingkungan itu sehingga tidak sama lagi dengan bentuk
asalnya. Perubahan yang terjadi itu memberikan dampak yang buruk terhadap
organisme yang sudah ada. Dan pada tingkat lanjut dalam arti jika lingkungan sudah
tercemar dalam tingkat tinggi, dapat membunuh bahkan memusnahkan satu atau lebih
jenis organisme. Jadi pencemaran lingkungan adalah terjadinya perubahan dalam
tatanan lingkungan dari bentuk asli ke arah yang lebih buruk (Palar, 2004).
Perkembangan ekonomi di Indonesia menitikberatkan pada pembangunan di
sektor industri. Di satu sisi pembangunan akan meningkatkan kualitas hidup manusia
dengan meningkatnya pendapatan masyarakat. Di sisi lain, pembangunan juga bisa
menurunkan kesehatan masyarakat dikarenakan pencemaran yang berasal dari limbah
industri (Widowati, 2008).
Proses industri pada akhirnya akan menghasilkan limbah, baik dalam bentuk
padat maupun cair. Limbah dikatakan berbahaya jika menimbulkan dampak yang
negatif bagi kesehatan manusia. Logam berat pada limbah industri dapat berasal dari
bahan baku maupun dari bahan pendukung pada proses industri.
Pencemaran yang disebabkan oleh buangan industri baik dalam bentuk unsur
maupun persenyawaan logam berat merupakan toksikan yang mempunyai daya racun
yang sangat tinggi. Polutan ini akan mencemari lingkungan, baik melalui udara, tanah,
Logam emas merupakan logam yang paling mulia, artinya tidak teroksidasi di udara
terbuka, hanya dapat larut di dalam larutan akuaregia, dan didalam larutan encer
NaCN. Terdapat dua metode yang dapat diterapkan dalam pengolahan emas, yaitu
amalgamasi dan sianidasi. Amalgasi adalah proses ekstraksi emas dengan cara
mencampurkan bijih emas dengan merkuri (air raksa), namun cara ini jarang
digunakan pada industri karena berisiko terjadinya pencemaran oleh merkuri. Sianidasi
adalah proses pelarutan bijih emas menggunakan larutan sianida. Dalam skala industri,
metode sianidasi merupakan yang paling ekonomis dan banyak diterapkan pada
banyak pabrik pengolahan emas di seluruh dunia.
Beberapa mineral pengotor dapat dipisahkan dari butiran emas pada tahap awal
pengolahan bijih (mineral dressing atau mineral processing) yaitu proses/operasi
dimana bijih diolah dengan mempergunakan sifat fisika/ kimia sehingga menghasilkan
produk yang dapat dijual (konsentrat) dan produk yang tidak berharga (disebut tailing)
dengan tidak mengubah sifat fisika dan kimia mineral yang diolah. Produk dari tahap
pengolahan bijih disalurkan ke tahap ekstraksi metalurgi yang mencakup tahap
pirometalurgi (bekerja pada temperatur 1000oC) dan tahap hidrometalurgi (Sudarsono,
2003).
Dasar-dasar proses hidrometalurgi mencakup pelindian (leaching), pemurnian
(purification) dan perolehan produk akhir (product recovery) logam berharga dari
larutannya. Pelindian adalah proses pelarutan mineral berharga dari suatu bijih
sedemikian rupa sehingga logam-logam berharga bisa terlarutkan dalam suatu pelarut.
Pemurnian larutan merupakan tahapan setelah pelindian dengan tujuan untuk
membersihkan larutan dari pengotor yang tidak diinginkan yang ikut terlarut pada
proses pelindian. Pengotor dapat dibersihkan dengan cara presipitasi, ekstraksi pelarut,
ion exchange dan sementasi. Tahap akhir dari suatu rangkaian ekstraksi hidrometalurgi
adalah perolehan produk akhir, dimana umumnya logam berharga diperoleh dengan
cara elektrowinning dari larutannya, sehingga logam mengendapkan di katoda
Pada proses pelarutan endapan emas, mineral sulfida seperti pyrit, galena, dan
kalkopirit juga akan ikut terlarut. Pada proses ini, ion sulfida yang terbentuk akan
bereaksi dengan oksigen membentuk sulfat sehingga menyebabkan larutan bersifat
asam dan berpotensi menghasilkan air asam tambang. Hal ini dapat dicegah dengan
penambahan garam – garam Timbal atau kapur Ca(OH)2 sebelum proses sianidasi
yang akan mengendapkan ion sulfida. Larutan kemudian dipisahkan dari limbah koloid
sampai diperoleh larutan pregnant yang jernih. Butiran karbon dipakai untuk
menangkap logam emas yang telah larut dan kemudian emas diendapkan dengan
penambahan bubuk Zn. Sedangkan logam kompleks lainnya termasuk logam emas
yang tidak dapat tertangkap akan terbawa bersama didalam lumpur residu sebagai
tailing (Sudarsono, 2003).
2.5 Toksisitas Logam Berat
Logam berat mempunyai kriteria yang sama dengan logam-logam lain. Perbedaanya
terletak pada pengaruh yang dihasilkan oleh logam berat ini jika berikatan atau masuk
ke dalam tubuh organisme hidup, sehingga akan menimbulkan pengaruh-pengaruh
buruk terhadap fungsi fisiologis tubuh.
Kerja utama logam adalah menghambat kerja enzim. Efek ini timbul akibat
interaksi antara logam dengan gugus SH pada enzim. Fungsi enzim juga dapat
terhambat oleh logam toksik melalui penggusuran kofaktor logam yang penting dari
enzim (Frank C.Lu, 1994).
Umumnya, efek toksik logam merupakan akibat dari reaksi antara logam dan
komponen intrasel. Setelah masuk ke dalam sel, logam dapat mempengaruhi berbagai
organel seperti retikulum endoplasma yang mengandung berbagai jenis enzim.
Logam-logam toksik ini akan mengacaukan struktur dari enzim dan menghambat
Tembaga (Cu) adalah logam berwarna merah muda yang lunak, dapat ditempa, dan
liat. Tembaga mempunyai berat molekul 63,5 dan melebur pada suhu 1038oC (Vogel,
1990).
Unsur tembaga di alam dapat ditemukan dalam bentuk logam bebas, akan
tetapi lebih banyak ditemukan dalam bentuk persenyawaan atau senyawa padat dalam
bentuk mineral. Pada badan perairan laut tembaga dapat ditemukan dalam bentuk
persenyawaan ion seperti CuCO3+ dan CuOH+ (Palar, 2004).
Pada proses pengolahan emas, umumnya endapan emas berasosiasi atau
berikatan dengan dengan mineral sulfida seperti pirit, sphalerit, dan kalkopirit,
sehingga pada saat pelarutan, logam-logam lain juga akan ikut terlarut, maka di dalam
larutan selain logam emas, juga akan terdapat logam-logam Perak, Tembaga, Besi, dan
Seng (Sudarsono, 2003).
Pada manusia, Tembaga dikelompokkan ke dalam metalloenzim. Logam ini
dibutuhkan untuk sistem enzim oksidatif seperti enzim askorbat oksidase. Tembaga
juga dibutuhka manusia sebagai kompleks Cu-protein yang mempunyai fungsi tertentu
dalam pembentukan haemoglobin, kolagen, dan pembuluh darah. Selain itu, Tembaga
juga terlibat dalam proses pembentukan energi untuk metabolisme. Namun demikian,
meski sangat dibutuhkan, logam Tembaga akan berbalik menjadi bahan racun untuk
manusia bila masuk dalam jumlah berlebihan (Palar, 2004).
Bentuk Tembaga yang paling beracun adalah debu-debu Cu yang dapat
mengakibatkan kematian pada dosis 3,5 mg/kg. Pada manusia, efek keracunan utama
yang ditimbulkan akibat terpapar oleh debu atau uap logam Tembaga adalah terjadinya
gangguan pada jalur pernafasan sebelah atas (Palar, 2004).
Gejala yang timbul pada manusia yang keracunan Cu akut: mual, muntah, sakit
perut, hemolisis, netrofisis, kejang, dan dapat menyebabkan kematian. Pada keracunan
tertimbunnya H2O2 dalam sel darah merah sehingga terjadi oksidasi dari lapisan sel
yang mengakibatkan sel menjadi pecah. Defesiensi suhu dapat menyebabkan anemia
dan pertumbuhan terhambat (Darmono, 1995).
2.5.2 Seng
Seng (Zn) merupakan logam berwarna putih kebiruan yang cukup mudah ditempa dan
liat pada suhu 110-150oC. Unsur ini melebur pada suhu 410oC (Vogel, 1990).
Seng merupakan komponen alam yang terdapat di kerak bumi. Unsur ini tika
terdapat dalam keadaan bebas di alam, tetapi dalam bentuk terikat dengan unsur lain
berupa mineral seperti kalamin, franklinit, smithsonit, willenit, dan zinkit serta
sphalerit. Kelimpahan seng di dunia menempati urutan ke-27 sebagai unsur penyusun
kerak bumi.
Seng banyak digunakan pada pelapisan baja dan besi untuk mencegah korosi
dan juga sebagai bahan pembuatan alloy. Sedangkan pada industri pengolahan bijih
emas, Seng dalam bentuk serbuk digunakan pada proses sementasi emas atau
presipitasi yang dikenal sebagai proses Merill-Crowe (Sudarsono, 2003).
Seng merupakan unsur yang sangat penting untuk pertumbuhan manusia.
Metabolisme sel dipengaruhi dan ditentukan oleh Seng. Seng berperan dalam fungsi
syaraf dan reproduksi. Seng juga berperan dalam menstabilisasi struktur protein.
Selain itu, Seng juga dibutuhkan dalam sintesis DNA, replika DNA, transkripsi RNA,
pertumbuhan dan aktivasi sel, pertumbuhan dan perkembangan normal selama hamil,
masa pertumbuhan anak dan pertumbuhan remaja, menjaga kesehatan kulit dan daya
tahan terhadap infeksi, serta merupakan aktifator enzim dan juga berperan dalam
metabolisme karbohidrat dan energi (Widowati, 2008).
Logam seng merupakan unsur esensial dan mempunyai banyak fungsi, namun
dalam dosis tinggi Seng dapat berbahaya dan bersifat toksik. Dalam keadaan sebagai
kadar Cu, pengubahan fungsi Fe, pengurangan imunitas tubuh, serta pengurangan
kadar high density lipoprotein (HDL). Komsumsi Seng sebesar 2 g atau lebih akan
menyebabkan mual, muntah, dan demam (Widowati, 2008).
2.6 Spektrofotometer Serapan Atom
Spektrofotometer Serapan Atom adalah suatu metode pengukuran kuantitatif suatu
unsur yang terdapat dalam suatu cuplikan berdasarkan penerapan cahaya pada panjang
gelombang tertentu oleh atom-atom bentuk gas dalam keadaan dasar. Jika cahaya
dengan panjang gelombang resonansi dilewatkan nyala yang mengandung atom-atom
yang bersangkutan, maka sebagian cahaya itu akan diserap dan jauhnya penyerapan
akan berbanding lurus dengan atom keadaan dasar yang berada dalam nyala. Metode
ini digunakan untuk penetapan sejumlah unsur, kebanyakan logam, dan berbagai
sampel (Mulja M, 1995).
2.6.1 Prinsip Dasar Spektrofotometer Serapan Atom
Jika cahaya dengan panjang gelombang resonansi dilewatkan nyala yang mengandung
atom-atom yang bersangkutan, maka sebagian cahaya akan diserap, dan jauhnya
penyerapan akan berbanding lurus dengan banyaknya atom keadaan dasar yang berada
dalam nyala. Hal ini merupakan dasar penentuan kuantitatif logam-logam dengan
2.6.2 Cara Kerja Spektrofotometer Serapan Atom
Spektrofotometer Serapan atom terdiri atas tiga komponen berikut:
1. Unit atomisasi
2. Sumber radiasi
3. Sistem pengukur fotometrik
Cara kerja spektrofotometer serapan atom mengikuti hukum Lambert-Beer,
yaitu banyaknya sinar yang diserap berbanding lurus dengan kadar zat. Persamaan
garis lurus dengan koefisien arah positif Y = ax + b. Dengan memasukkan nilai
absorbansi larutan contoh ke dalam persamaan garis dari larutan standar, maka kadar
logam berat dalam contoh dapat diketahui.
Oleh karena yang mengabsorbansi sinar adalah atom, maka ion/senyawa logam
berat dalam contoh harus diubah menjadi bentuk atom. Perubahan bentuk ion/senyawa
menjadi bentuk atom biasanya dilakukan pada suhu tinggi (2000oC) melalui
pembakaran (asetilen-udara) atau dengan energi listrik.
2.6.3 Keuntungan Penggunaan Metode Spektrofotometer Serapan Atom
Analisis dilakukan dengan metode Spektrofotometer Serapan Atom (SSA) dengan
pertimbangan bahwa:
1. Metode analisis SSA dapat menentukan hampir keseluruhan unsur logam.
2. Metode analisis SSA dapat menentukan logam dalam skala kualitatif karen
lampunya 1 (satu) untuk setiap 1 logam.
3. Analisis unsur logam langsung dapat ditentukan walau sampel dalam bentuk
campuran.
4. Analisis unsur logam dengan metode SSA didapat hasil kuantitatif
BAB 3
METODOLOGI PENELITIAN
3.1. Alat-alat
-Spektrofotomere Serapan Atom Shimadzu AA - 6300
-Hot plate
-spatula
-Tanur Sibata
-Oven
-Termometer
-Neraca analitik
-Cawan porselen
-Beaker gelas Pyrex
-Labu takar Pyrex
-Gelas ukur Pyrex
-Erlenmeyer Pyrex
-Corong
-Desikator
-Siever (Ayakan) Schichemco
-Alu dan lumpang
-Pipet volume Pyrex
-Kertas saring No. 42 Whatman
-Pipet tetes
3.2. Bahan-bahan
-Zeolit alam
-Air Limbah industri pertambangan emas
-Akuades
-HNO3(p) p.a (E. Merck)
-HCl(p) p.a (E. Merck)
-Larutan induk Tembaga (Cu) 1000 mg/L p.a (E. Merck)
-Larutan induk Seng (Zn) 1000 mg/L p.a (E. Merck)
3.3. Prosedur Penelitian
3.3.1 Pembuatan Larutan HCl 15 %
Sebanyak 40,54 mL larutan Cl(p) dimasukkan ke dalam labu takar 100 mL, diencerkan
dengan akuades hingga garis tanda lalu dihomogenkan.
3.3.2 Penyediaan Zeolit Alam
Zeolit alam dihaluskan dan dibuat ukuran partikelnya 120 mesh. Kemudian
dikeringkan pada suhu 110oC.
3.3.3 Pengaktifan Zeolit Alam
Ke dalam 150 gram zeolit alam 120 mesh ditambahkan 500 mL HCl 15 %, diaduk
menggunakan magnetik stirer selama 3 jam sambil dipanaskan pada suhu 60oC dan
didiamkan selama 24 jam. Kemudian disaring menggunakan kertas saring. Lalu dibilas
dengan akuades hingga pH netral. Kemudian diaktivasi dengan pemanasan pada suhu
3.3.4.1Pembuatan Larutan Standar Cu 100 mg/L
Sebanyak 10 mL larutan induk Cu 1000 mg/L dimasukkan ke dalam labu takar 100
mL, kemudian diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
3.3.4.2Pembuatan Larutan Standar Cu 10 mg/L
Sebanyak 10 mL larutan standar Cu 100 mg/L dimasukkan ke dalam labu takar 100
mL, kemudian diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
3.3.4.3Pembuatan Larutan seri standar Cu 0,2; 0,4; 0,6; 0,8; dan 1,0 mg/L
Sebanyak 2, 4, 6, 8, dan 10 mL larutan standar Cu 10 mg/L dimasukkan
masing-masing ke dalam labu takar 100 mL, kemudian diencerkan dengan akuades hingga
garis tanda dan dihomogenkan.
3.3.5 Pembuatan Larutan Standar Zn
3.3.5.1Pembuatan Larutan Standar Zn 100 mg/L
Sebanyak 10 mL larutan induk Zn 1000 mg/L dimasukkan ke dalam labu takar 100
mL, kemudian diencerkan dengan akuades hingga garis tanda dan dihomogenkan
3.3.5.2Pembuatan Larutan Standar Zn 10 mg/L
Sebanyak 10 mL larutan standar Zn 100 mg/L dimasukkan ke dalam labu takar 100
3.3.5.3Pembuatan Larutan seri standar Zn 0,2; 0,4; 0,6; 0,8; dan 1,0 mg/L
Sebanyak 2, 4, 6, 8, dan 10 mL larutan standar Zn 10 mg/L dimasukkan
masing-masing ke dalam labu takar 100 mL, kemudian diencerkan dengan akuades hingga
garis tanda dan dihomogenkan.
3.3.6 Pembuatan Kurva Kalibrasi 3.3.6.1Pembuatan Kurva Kalibrasi Cu
Masing-masing larutan seri standar Cu diukur absorbansinya dengan Spektrofotometer
Serapan Atom pada λspesifik = 324,8 nm. Pengukuran dilakukan sebanyak 3 kali untuk
setiap larutan seri standar. Perlakuan yang sama dilakukan terhadap akuades bebas Cu
sebagai blanko.
3.3.6.2Pembuatan Kurva Kalibrasi Zn
Masing-masing larutan seri standar Zn diukur absorbansinya dengan Spektrofotometer
Serapan Atom pada λspesifik = 213,9 nm. Pengukuran dilakukan sebanyak 3 kali untuk
setiap konsentrasi larutan seri standar. Prosedur yang sama dilakukan terhadap akuades
bebas Zn sebagai blanko.
3.3.7 Penyerapan Kandungan Cu dan Zn dalam limbah cair oleh Zeolit Alam Teraktivasi
Sebanyak 100 mL larutan limbah dimasukkan ke dalam beaker glass, ditambahkan 25
gram zeolit aktif. Diaduk dengan magnetik stirer selama 3 jam, kemudian disaring
dengan kertas saring Whatman No. 42 dan filtratnya ditampung.
Sebanyak 25 mL filtrat dipipet dan dimasukkan ke dalam labu erlenmeyer, lalu
ditambahkan 3 mL HNO3(p). Dipanaskan hingga setengah volume awal dan
didinginkan. Disaring dengan kertas saring Whatman No. 42. Filtrat dimasukkan ke
dalam labu takar 25 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan. Diukur absorbansi Cu dengan Spektrofotometer Serapan Atom pada
oleh Zeolit aktif dengan dosis 50 dan 75 g.
3.3.8 Regenerasi Zeolit Alam
Zeolit alam yang telah terpakai dicuci dengan akuades, lalu dikeringkan. Ditambahkan
HCl 15 % lalu diaduk menggunakan magnetik stirer selama 3 jam sambil dipanaskan
pada suhu 60oC dan didiamkan selama 24 jam. Kemudian disaring menggunakan
kertas saring. Lalu dibilas dengan akuades hingga pH netral. Kemudian diaktivasi
dengan pemanasan pada suhu 300oC selama 3 jam. Didinginkan dan disimpan di
dalam desikator.
Catatan: Setiap proses Regenerasi dilakukan setelah zeolit digunakan sebagai penyerap
logam Cu dan Zn di dalam air limbah.
3.3.9 Penyerapan Kandungan Cu dan Zn di dalam limbah cair oleh Zeolit Alam Teregenerasi
Sebanyak 100 mL larutan limbah dimasukkan ke dalam beaker glass, ditambahkan 25
gram zeolit alam yang telah diregenerasi. Diaduk dengan magnetik stirer selama 3 jam
dan didiamkan selama 24 jam. Kemudian disaring dengan kertas saring Whatman No.
42 dan filtratnya ditampung.
Sebanyak 25 mL filtrat dipipet dan dimasukkan ke dalam labu erlenmeyer, lalu
ditambahkan 3 mL HNO3(p). Dipanaskan hingga setengah volume awal dan
didinginkan. Disaring dengan kertas saring Whatman No. 42. Filtrat dimasukkan ke
dalam labu takar 25 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan. Kemudian diukur absorbansi Cu dengan Spektrofotometer Serapan
Atom pada λspesifik = 324,8 nm dan absorbansi Zn pada λspesifik = 213,9 nm.
Dilakukan perlakuan yang sama untuk penyerapan logam Cu dan Zn dalam air limbah
3.4 Bagan Penelitian
3.4.1 Penyediaan Zeolit Alam
dihaluskan
diayak120 mesh
dikeringkan dalam oven pada suhu 110oC selama 2 jam
3.4.2 Pengaktifan Zeolit
dimasukkan ke dalam beaker glass
ditambahkan 500 mL HCl 15 %
diaduk dengan magnetik stirer selama 3 jam sambil
dipanaskan di atas hot plate pada suhu 60oC
disaring
dibilas dengan akuades hingga pH = 7
diaktivasi pada suhu 300oC selama 3 jam
didinginkan
disimpan di dalam desikator Zeolit berwarna
Filtra Resid
Zeolit
Zeolit Alam
dipipet sebanyak 10 mL
dimasukkan ke dalam labu takar 100 mL
diencerkan dengan akuades hingga garis tanda
diaduk hingga homogen
\
dipipet sebanyak 10 mL
dimasukkan ke dalam labu takar 100 mL
diencerkan dengan akuades hingga garis tanda
diaduk hingga homogen
dipipet sebanyak 2; 4; 6; 8; dan 10 mL
dimasukkan masing-masing ke dalam labu takar 100
mL
diencerkan dengan akuades hingga garis tanda
diaduk hingga homogen
diukur absorbansinya dengan Spektrofotometer
Serapan Atom pada λspesifik = 324,8 nm
Hasil
Larutan Standar Cu 1000
Larutan Standar Cu 100
Larutan Standar Cu 10
Larutan Seri Standar Cu 0,2; 0,4; 0,6;
3.4.4 Pembuatan Kurva Kalibrasi Zn
dipipet sebanyak 10 mL
dimasukkan ke dalam labu takar 100 mL
diencerkan dengan akuades hingga garis tanda
diaduk hingga homogen
\
dipipet sebanyak 10 mL
dimasukkan ke dalam labu takar 100 mL
diencerkan dengan akuades hingga garis tanda
diaduk hingga homogen
dipipet sebanyak mL 2; 4; 6; 8; dan 10 mL
dimasukkan masing-masing ke dalam labu takar 100
mL
diencerkan dengan akuades hingga garis tanda
diaduk hingga homogen
diukur absorbansinya dengan Spektrofotometer
Serapan Atom pada λspesifik = 213,9 nm
Hasil
Larutan Standar Zn 1000
Larutan Standar Zn 100
Larutan Standar Zn 10
Larutan Seri Standar Zn 0,2; 0,4; 0,6; 0,8;
dimasukkan ke dalam labu erlenmeyer
ditambahkan 25 gram Zeolit Alam teraktivasi diaduk dengan menggunakan magnetik stirer selama 3 jam
disaring dengan kertas saring whatman No.42
dipipet sebanyak 25 mL
dimasukkan ke dalam erlenmeyer ditambahkan 3 mL HNO3(p)
didinginkan dipanaskan hingga setengah volume awal disaring dengan kertas saring whatman No.42
dimasukkan ke dalam labu takar 25 mL diencerkan dengan akuades sampai garis tanda
diukur absorbansi Cu pada λspesifik = 324,8 nm dan absorbansi Zn pada λspesifik = 213,9 nm.
Dilakukan perlakuan yang sama terhadap penyerapan logam Cu dan Zn di
dalam air limbah dengan penambahan zeolit aktif dengan dosis 50 dan 75 gram.
Filtrat Endap
100 mL air limbah
Filtrat Resid
3.4.6 Regenerasi Zeolit Alam
ditambahkan 500 mL HCl 15 %
diaduk dengan magnetik stirer selama 3 jam
sambil dipanaskan di atas hot plate pada suhu
60oC
disaring
dibilas dengan aquadest hingga pH = 7
dipanaskan pada suhu 300oC selama 3 jam
didinginkan
disimpan di dalam desikator
Catatan: Setiap proses Regenerasi dilakukan setelah zeolit digunakan sebagai
penyerap logam Cu dan Zn di dalam air limbah. Filtra Resid
Zeolit alam
dimasukkan ke dalam labu erlenmeyer
ditambahkan 25 gram Zeolit Alam yang
telah diregenerasi
diaduk dengan menggunakan magnetik stirer selama 3 jam
disaring dengan kertas saring whatman No.42
dipipet sebanyak 25 mL
dimasukkan ke dalam erlenmeyer ditambahkan 3 mL HNO3(p)
didinginkan dipanaskan hingga setengah volume awal disaring dengan kertas saring whatman No.42
dimasukkan ke dalam labu takar 25 mL diencerkan dengan akuades sampai garis batas
diukur absorbansi Cu pada λspesifik = 324,8 nm dan absorbansi Zn pada λspesifik = 213,9 nm.
Dilakukan perlakuan yang sama terhadap penyerapan logam Cu dan Zn dalam air
limbah oleh zeolit alam yang telah diregenerasi dengan dosis 50 dan 75 gram.
Filtrat Residu
100 mL air limbah
Filtrat Resid
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
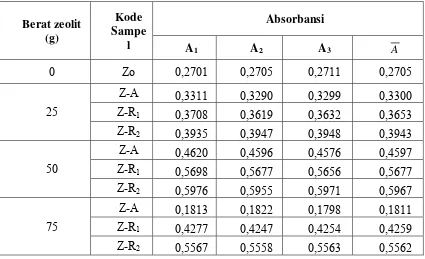
Data hasil pengukuran absorbansi dari suatu larutan seri standar Cu dengan
menggunakan Spektrofotometer Serapan Atom terdapat pada TABEL 4.1, sedangkan
kurva kalibrasi terdapat pada Gambar 4.1. Data hasil pengukuran absorbansi Cu pada
air limbah industri pertambangan emas, baik sebelum maupun sesudah penambahan
zeolit alam aktif dan zeolit alam yang telah diregenerasi dicantumkan pada lampiran
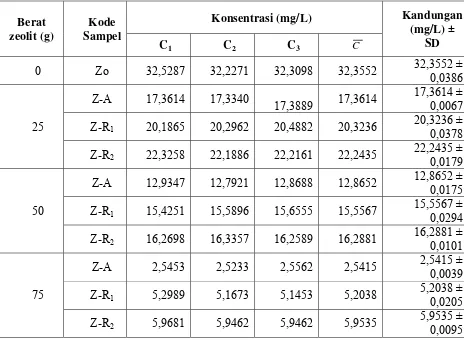
TABEL 1. Data konsentrasi Cu sebelum dan sesudah penambahan zeolit alam aktif
dan zeolit alam yang telah diregenerasi dicantumkan pada lampiran TABEL 2. Dan
data persentase Cu yang terserap setelah penambahan zeolit alam aktif dan zeolit alam
yang telah diregenerasi dicantumkan pada lampiran TABEL 3.
Data hasil pengukuran absorbansi dari suatu larutan seri standar Zn dengan
menggunakan Spektrofotometer Serapan Atom terdapat pada TABEL 4.3, sedangkan
kurva kalibrasi terdapat pada gambar 4.2. Data hasil pengukuran absorbansi Zn pada
air limbah industri pertambangan emas, baik sebelum maupun sesudah penambahan
zeolit alam aktif dan zeolit alam yang telah diregenerasi dicantumkan pada lampiran
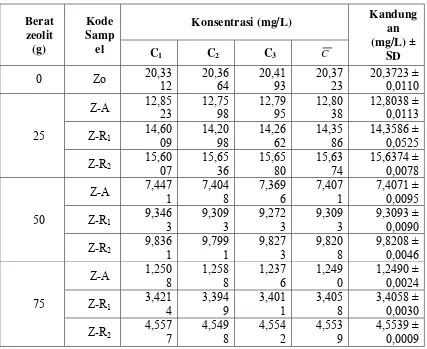
TABEL 4. Data konsentrasi Zn sebelum dan setelah penambahan zeolit alam aktif dan
zeolit alam yang telah diregenerasi dicantumkan pada lampiran TABEL 5. Dan data
persentase Zn yang terserap setelah penambahan zeolit alam aktif dan zeolit alam yang
Data absorbansi yang diperoleh dari suatu larutan seri standar logam Cu diplotkan
terhadap konsentrasi larutan seri standar, sehingga diperoleh suatu kurva kalibrasi
[image:42.595.106.293.250.373.2]berupa garis linear seperti pada Gambar 4.1 di bawah ini.
TABEL 4.1. Data Absorbansi dari Larutan Seri Standar Cu
Konsentrasi (mg/L)
Absorbansi Rata-rata
0,2 0,0392
0,4 0,0766
0,6 0,1149
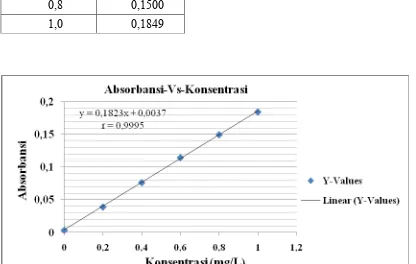
0,8 0,1500
[image:42.595.107.523.340.604.2]1,0 0,1849
Gambar 4.1. Kurva kalibrasi larutan seri standar Cu
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan
menggunakan metode Least Square, dimana konsentrasi dinyatakan sebagai xi dan
absorbansi dinyatakan sebagai yi seperti pada TABEL 4.2 berikut:
No xi yi (xi-x ) (yi-y ) (xi-x )2 (yi-y )2 (xi-x )(yi-y )
1. 0,2 0,0392 -0,4 -0,0739 0,16 0,005446 0,0296
2. 0,4 0,0766 -0,2 -0,0365 0,04 0,001332 0,0073
3. 0,6 0,1149 0,0 0,0018 0,00 0,000003 0,0000
4. 0,8 0,1500 0,2 0,0369 0,04 0,001362 0,0073
5. 1,0 0,1849 0,4 0,0718 0,16 0,005155 0,0287
xi 3,0 yi 0,5656 0,0 0,0001 0,40 0,013298 0,0729x 0,6 y 0,1131
4.1.1.1Penurunan Persamaan Garis Regresi
b
ax
y
Dimana:
a
= slopeb
= intersept0037 , 0 1094 , 0 1131 , 0 ) 6 , 0 )( 1823 , 0 ( 1131 , 0 1823 , 0 4 , 0 0729 , 0 ) ( ) )( ( 2
b b b x a y b b ax y x x y y x x a i i iMaka persamaan garis regresi adalah:
0,07293 0,99958 07290 , 0 0053192 , 0 07290 , 0 ) 013298 , 0 )( 4 , 0 ( 07290 , 0 ) ( . ) ( ) )( ( 2 1 2 2
y y x x y y x x r i i i i4.1.1.3Penentuan Cu di Dalam Sampel Sebelum dan Sesudah Penambahan Zeolit Aktif dan Zeolit yang Telah Mengalami Regenerasi
Contoh perhitungan:
Untuk sampel air limbah sebelum penambahan zeolit aktif (Zo), dengan metode
destruksi basah diperoleh absorbansi (A) sebagai berikut:
A1 = 0,1223
A2 = 0,1212
A3 = 0,1215
Dengan mensubstitusikan nilai y kepersamaan regresi:
Maka diperoleh konsentrasi Cu (FP = 50):
x1 = 32,5287
x2 = 32,2271
x3 = 32,3098
Dengan demikian konsentrasi Cu adalah:
(x1 - x )2 = (32,5287 – 32,3552)2 = 0,0301
(x2 - x )2 = (32,2271 – 32,3552)2 = 0,0164
(x3 - x )2 = (32,3098 – 32,3552)2 = 0,0020
2)
(xi x = 0,0485
Maka : 0,1557
2 0485 , 0 1 ) ( 2
n x x S iDidapat harga 0,0898
3 1557 , 0 n S Sx
Dari hasil data distribusi t student untuk n = 3, derajat kebebasan (dk) = n-1 = 2, untuk
derajat kepercayaan 95% (p = 0,05), nilai t = 4,30.
Maka: d = t ( p . dk) Sx
= 4,30 (0,05 . 2) 0,0898
= 0,0386
Dengan demikian konsentrasi total Cu di dalam air limbah sebelum penambahan
zeolit adalah: 32,3552 ± 0,0386 mg/L.
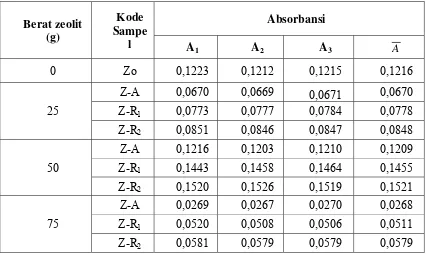
Untuk sampel air limbah setelah penambahan zeolit aktif dengan berat zeolit 25 g (Z-A), dengan metode destruksi basah diperoleh absorbansi (A) sebagai berikut:
A1 = 0,0670
A2 = 0,0669
A3 = 0,0671
Dengan mensubstitusikan nilai y kepersamaan regresi:
x1 = 17,3614
x2 = 17,3341
x3 = 17,3889
Dengan demikian konsentrasi Cu adalah:
(x1 - x )2 = (17,3614 – 17,3614)2 = 0,00000
(x2 - x )2 = (17,3341 – 17,3614)2 = 0,00074
(x3 - x )2 = (17,3889 – 17,3614)2 = 0,00075
2)
(xi x = 0,00149
Maka : 0,0272
2 00149 , 0 1 ) ( 2
n x x S iDidapat harga 0,0157
3 0272 , 0 n S Sx
Dari hasil data distribusi t student untuk n = 3, derajat kebebasan (dk) = n-1 = 2, untuk
derajat kepercayaan 95% (p = 0,05), nilai t = 4,30.
Maka: d = t ( p . dk) Sx
= 4,30 (0,05 . 2) 0,0157
= 0,0067
Dengan demikian konsentrasi total Cu dalam air limbah sebelum penambahan zeolit
4.1.1.4Perhitungan Jumlah Cu yang Terserap dan Persentase Penyerapan dari Zeolit Alam
Jumlah Cu yang terserap dihitung dengan persamaan:
[Cu]terserap = [Cu]awal - [Cu]sisa
Hasil dari persamaan di atas digunakan untuk menghitung persentase [%] penyerapan
dari zeolit alam terhadap logam Cu, dengan menggunakan persamaan:
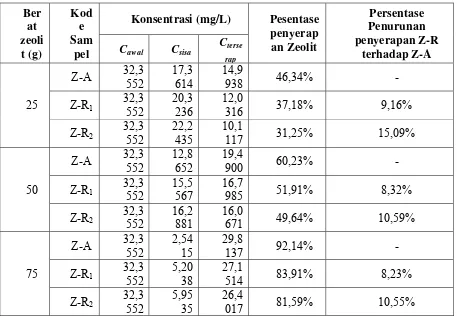
Persentase penyerapan dari zeolit alam terhadap logam Cu serta persentase penurunan
penyerapan zeolit alam yang telah diregenerasi terhadap zeolit alam aktif dicantumkan
pada lampiran tabel 3.
4.1.2 Penentuan Seng (Zn)
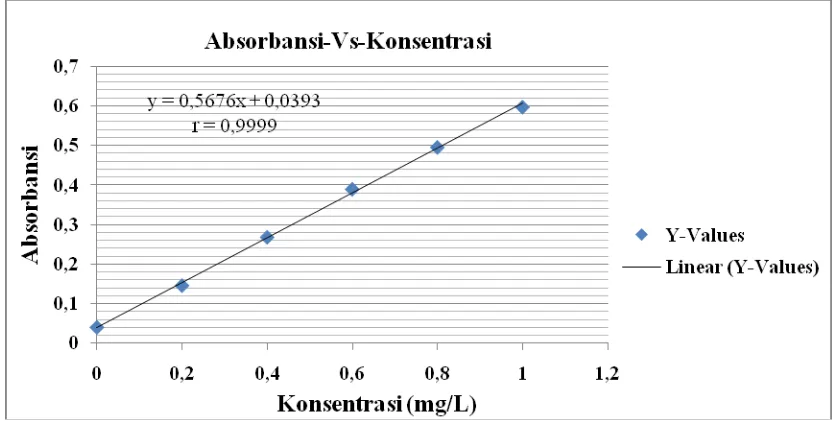
Data absorbansi yang diperoleh dari suatu larutan seri standar logam Zn diplotkan
terhadap konsentrasi larutan seri standar, sehingga diperoleh suatu kurva kalibrasi
[image:47.595.108.301.633.760.2]berupa garis linear seperti pada Gambar 4.2 di bawah ini.
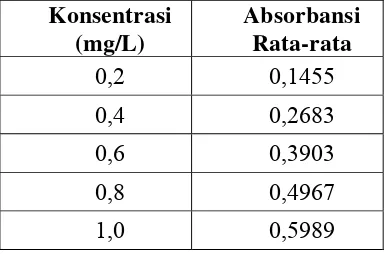
TABEL 4.3. Data Absorbansi dari Larutan Seri Standar Zn
Konsentrasi (mg/L)
Absorbansi Rata-rata
0,2 0,1455
0,4 0,2683
0,6 0,3903
0,8 0,4967
1,0 0,5989
100 %] [
] [
% x
Cu Cu
Gambar 4.2. Kurva kalibrasi larutan seri standar Zn
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan
menggunakan metode Least Square, dimana konsentrasi dinyatakan sebagai xi dan
absorbansi dinyatakan sebagai yi seperti pada TABEL 4.4 berikut:
TABEL 4.4. Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi Zn
No xi yi (xi-x ) (yi-y ) (xi-x )2 (yi-y )2 (xi-x )(yi-y )
1. 0,2 0,1455 -0,4 -0,2344 0,16 0,0549 0,09376
2. 0,4 0,2683 -0,2 -0,1116 0,04 0,0124 0,02232
3. 0,6 0,3903 0,0 0,0104 0,00 0,0001 0,00000
4. 0,8 0,4967 0,2 0,1168 0,04 0,0136 0,02336
5. 1,0 0,5989 0,4 0,2190 0,16 0,0479 0,08760
xi 3,0 yi 1,8997 0,0 0,0000 0,40 0,1289 0,227044.1.2.1Penurunan Persamaan Garis Regresi
b
ax
y
Dimana:
a
= slopeb
= intersept03938 , 0 34056 , 0 37994 , 0 ) 6 , 0 )( 5676 , 0 ( 37994 , 0 5676 , 0 4 , 0 22704 , 0 ) ( ) )( ( 2
b b b x a y b b ax y x x y y x x a i i iMaka persamaan garis regresi adalah:
4.1.2.1Menghitung Koefisien Korelasi (r)
0,22706 0,9999122704 , 0 05156 , 0 22704 , 0 ) 1289 , 0 )( 4 , 0 ( 22704 , 0 ) ( . ) ( ) )( ( 2 1 2 2
x x y yAktif dan Zeolit yang Telah Mengalami Regenerasi
Contoh perhitungan :
Untuk sampel air limbah sebelum penambahan zeolit aktif (Zo), dengan metode
destruksi basah diperoleh absorbansi (A) sebagai berikut:
A1 = 0,2701
A2 = 0,2705
A3 = 0,2711
Dengan mensubstitusikan nilai y kepersamaan regresi:
Maka diperoleh konsentrasi Zn (FP = 50) :
x1 = 20,3312
x2 = 20,3664
x3 = 20,4193
Dengan demikian konsentrasi Zn adalah:
(x1 - x )2 = (20,3312 – 20,3723)2 = 0,00172
(x2 - x )2 = (20,3664 – 20,3723)2 = 0,00003
(x3 - x )2 = (20,4193– 20,3723)2 = 0,00220
2)
(xi x = 0,00395
0393 , 0 5676 ,
0
x y
3723 , 20 3
1169 ,
61
n x
Maka : 0,0444 2 00395 , 0 1 ) ( 2
n x x S iDidapat harga 0,0256
3 0444 , 0 n S Sx
Dari hasil data distribusi t student untuk n = 3, derajat kebebasan(dk) = n-1 = 2, untuk
derajat kepercayaan 95% (p = 0,05), nilai t = 4,30.
Maka: d = t ( p . dk) Sx
= 4,30 (0,05 . 2) 0,0256
= 0,0110
Dengan demikian konsentrasi total Zn dalam air limbah sebelum penambahan zeolit
adalah: 20,3723 ± 0,0110 mg/L.
Untuk sampel air limbah setelah penambahan zeolit aktif dengan berat zeolit 25 g
(Z-A), dengan metode destruksi basah diperoleh absorbansi (A) sebagai berikut:
A1 = 0,3311
A2 = 0,3290
A3 = 0,3299
Dengan mensubstitusikan nilai y kepersamaan regresi:
Maka diperoleh konsentrasi Zn (FP = 25) :
x1 = 12,8523
x2 = 12,7598
x3 = 12,7995
Dengan demikian konsentrasi Zn adalah:
8038 , 12 3 4116 , 38
n x x i(x1 - x )2 = (12,8523 – 12,8038)2 = 0,00235
(x2 - x )2 = (12,7598 – 12,8038)2 = 0,00193
(x3 - x )2 = (12,7995 – 12,8038)2 = 0,00001
2)
(xi x = 0,00429
Maka : 0,0463
2 00429 , 0 1 ) ( 2
n x x S iDidapat harga 0,0267
3 0463 , 0 n S Sx
Dari hasil data distribusi t student untuk n = 3, derajat kebebasan(dk) = n-1 = 2, untuk
derajat kepercayaan 95% (p = 0,05), nilai t = 4,30.
Maka: d = t ( p . dk) Sx
= 4,30 (0,05 . 2) 0,0267
Dengan demikian konsentrasi total Zn dalam air limbah setelah penambahan zeolit
aktif dengan berat zeolit 25 g adalah: 12,8038 ± 0,0114 mg/L.
4.1.2.3Perhitungan Jumlah Zn yang Terserap dan Kapasitas Adsorpsi dari Zeolit [%Zn]
Jumlah Zn yang terserap dihitung dengan persamaan:
[Zn]terserap = [Zn]awal - [Zn]sisa
Hasil dari persamaan di atas digunakan untuk menghitung kapasitas adsorpsi dari
zeolit alam terhadap logam Zn [%Zn], dengan menggunakan persamaan:
%
100
]
[
]
[
[%]
x
Zn
Zn
awal terserap
Persentase penyerapan dari zeolit alam terhadap logam Zn serta persentase penurunan
penyerapan zeolit alam yang telah diregenerasi terhadap zeolit alam aktif dicantumkan
pada lampiran TABEL 6.
4.2. Pembahasan
Telah dilakukan penelitian mengenai pemanfaatan kembali zeolit alam yang telah
diregenerasi sebagai penyerap logam Cu dan Zn di dalam air limbah industri
pertambangan emas. Dimana zeolit aktif yang telah dipakai sebagai adsorben logam
Cu dan Zn di dalam air limbah industri dipakai kembali sebagai adsorben pada sampel
yang sama setelah mengalami proses regenerasi. Zeolit alam yang dipakai pada
penelitian ini adalah campuran jenis Anortit dan Monmorilonit, yang diambil dari
daerah Sarulla, kecamatan Pahae, Kabupaten Tapanuli Tengah, sedangkan sampel air
limbah diambil dari industri pertambangan emas di daerah KabupatenTapanuli
mesh, sedangkan variasi berat zeolit yang ditambahkan adalah 25 g, 50 g, dan 75 g.
Proses regenerasi sama dengan proses aktivasi yaitu dengan penambahan HCl 15%
dan dilanjutkan dengan pemanasan pada suhu 300oC selama 3 jam. Pada proses
aktivasi, penambahan HCl 15% dimaksudkan untuk membersihkan permukaan pori,
membuang pengotor-pengotor (impurities) yang menempel (terikat) pada struktur
zeolit, sehingga di dapat pori-pori zeolit yang lebih bersih dan aktif (Fatimah, 2000),
sedangkan pada proses regenerasi penambahan HCl 15% dimaksudkan untuk
menghilangkan kembali logam-logam atau molekul-molekul yang telah terserap dan
terikat dalam struktur zeolit, sehingga dapat kembali dihasilkan zeolit yang diharapkan
mempunyai kemampuan tukar kation yang sama dengan zeolit aktif. Sementara itu,
pemanasan yang dilakukan pada suhu 300oC, baik pada proses aktivasi maupun pada
proses regenerasi dimaksudkan untuk memperbesar pori-pori zeolit dengan terlepasnya
molekul air dari dalam pori, sehingga luas permukaan internal pori meningkat
(Fatimah, 2000).
Metode yang digunakan untuk mendestruksi sampel air limbah, baik sebelum
maupun sesudah penambahan zeolit alam adalah metode destruksi basah dengan
penambahan HNO3(p). Penentuan kandungan logam Cu dan Zn di dalam sampel air
limbah industri pertambagan emas dilakukan menggunakan spektrofotometer serapan
atom (SSA). Dimana panjang gelombang maksimum untuk logam Cu adalah 324,8 nm
dan panjang gelombang maksimum untuk logam Zn adalah 213,9 nm.
Penentuan kandungan Cu di dalam sampel air limbah dilakukan dengan
menplotkan data absorbansi yang diperoleh dari suatu larutan seri standar logam Cu
terhadap konsentrasi larutan seri standar, sehingga diperoleh suatu kurva kalibrasi
berupa garis linear. Persamaan garis regresi untuk kurva kalibrasi ini diturunkan
dengan menggunakan metode Least Square, dimana konsentrasi dinyatakan sebagai xi
dan absorbansi dinyatakan sebagai yi.
Sedangkan penentuan kandungan Zn di dalam sampel air limbah dilakukan
dengan menplotkan data absorbansi yang diperoleh dari suatu larutan seri standar
kalibrasi berupa garis linear. Persamaan garis regresi untuk kurva kalibrasi ini
diturunkan dengan menggunakan metode Least Square, dimana konsentrasi dinyatakan
sebagai xi dan absorbansi dinyatakan sebagai yi.
4.2.1.Tembaga (Cu)
Pada Lampiran TABEL 3, dicantumkan persentase penyerapan dari zeolit alam aktif
dan zeolit alam yang di regenerasi terhadap kandungan logam Cu di dalam air limbah
industri pertambangan emas dengan variasi berat zeolit 25 gram; 50 gram; dan 75
gram.
Dari hasil penelitian yang dilakukan diperoleh bahwa konsentrasi Cu pada
sampel air limbah industri pertambangan emas menurun setelah dilakukan
penambahan zeolit alam aktif dan zeolit alam yang telah diregenerasi. Persentase
penyerapan dari zeolit alam terhadap kandungan Cu yang paling optimum terjadi pada
penambahan zeolit alam dengan dosis 75 gram dengan persentase penyerapan untuk
zeolit alam yang mengalami 1 (satu) kali proses regenerasi yaitu 83,91% dan 2 (dua)
kali proses regenerasi yaitu 81,59%. Pada penambahan zeolit alam yang telah diregenerasi dengan dosis di bawah 75 gram di dapat bahwa penyerapan kandungan
Cu belum maksimal. Dibandingkan dengan penyerapan zeolit alam aktif yang sebesar
92,14%, zeolit alam yang telah mengalami 1 (satu) dan 2 (dua) kali proses regenerasi
penyerapannya menurun berturut-turut sebesar 8,23% dan 10,55%. Menurunnya
penyerapan dari zeolit alam yang telah diregenerasi kemungkinan besar terjadi karena
tidak semua molekul yang telah teradsorpsi oleh zeolit alam dapat dilepaskan kembali
dengan penambahan HCl 15%. Namun dari hasil penelitian dapat disimpulkan bahwa
zeolit alam yang telah diregenerasi sebanyak 2 kali masih dapat digunakan sebagai
penyerap logam Cu di dalam air limbah industri pertambangan emas.
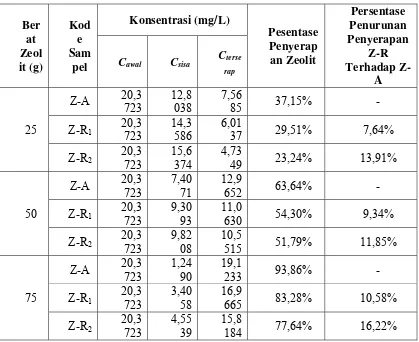
Pada Lampiran TABEL 6, dicantumkan persentase penyerapan dari zeolit alam aktif
dan zeolit alam yang di regenerasi terhadap kandungan logam Zn di dalam air limbah
industri pertambangan emas dengan variasi berat zeolit 25 gram; 50 gram; dan 75
gram.
Dari hasil penelitian yang dilakukan diperoleh bahwa konsentrasi Zn pada
sampel air limbah industri pertambangan emas menurun setelah dilakukan
penambahan zeolit alam aktif dan zeolit alam yang telah diregenerasi. Persentase
penyerapan dari zeolit alam terhadap kandungan Zn yang paling optimum terjadi pada
penambahan zeolit alam dengan dosis 75 gram dengan persentase penyerapan untuk
zeolit alam yang mengalami 1 (satu) kali proses regenerasi yaitu 83,28% dan 2 (dua)
kali proses regenerasi yaitu 77,64%. Pada penambahan zeolit alam yang telah diregenerasi dengan dosis di bawah 75 gram di dapat bahwa penyerapan kandungan
Zn belum maksimal. Dibandingkan dengan penyerapan zeolit alam aktif yang sebesar
93,86%, zeolit alam yang telah mengalami 1 (satu) dan 2 (dua) kali proses regenerasi
penyerapannya menurun berturut-turut sebesar 10,58% dan 16,22%. Menurunnya
penyerapan dari zeolit alam yang telah diregenerasi kemungkinan besar terjadi karena
tidak semua molekul yang telah teradsorpsi oleh zeolit alam dapat dilepaskan kembali
dengan penambahan HCl 15%. Namun dari hasil penelitian dapat disimpulkan bahwa
zeolit alam yang telah diregenerasi sebanyak 2 kali masih dapat digunakan sebagai
penyerap logam Zn di dalam air limbah industri pertambangan emas.
Penelitian sebelumnya juga telah ada yang melakukan tekhnik regenerasi
seperti yang telah dilakukan oleh Martini dkk (2009) menunjukkan bahwa regenerasi
adsorben surfaktan kationik berpenyangga Zeolit alam jenis Monmorilonit Boyolali
sebagai penyerap polutan organik dan logam berat, dimana regenerasi adsorben
dilakukan dengan tekhnik pencucian menggunakan H2O2 5%, KH2PO4 0,01 M, NaOH
0,1 M, dan Na2CO3 0,28 M, dihasilkan reagen regenerasi yang paling efektif dalam
proses regenerasi adalah menggunakan H2O2 5% dengan kapasitas adsorpsi sebesar
30,7%, diikuti dengan KH2PO4 0,01 M sebesar 26,8%. Sedangkan penelitian yang
mengalami kejenuhan sebagai penyerap NH3 dalam larutan, dimana tekhnik regenerasi
hanya dilakukan dengan pemanasan pada suhu 550oC selama 1 jam menunjukkan
bahwa kapasitas adsorpsi zeolit alam hasil regenerasi mengalami penurunan yang
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
- Zeolit alam yang telah diregenerasi dapat dimanfaatkan kembali sebagai
penyerap logam Cu dan Zn di dalam air limbah industri pertambangan emas.
- Penyerapan optimum dari zeolit alam terhadap logam Cu dan Zn di dalam 100
mL air limbah industri pertambangan emas terjadi pada penambahan zeolit alam
sebesar 75 g. Persentase penyerapan dari zeolit alam sebelum dan setelah
diregenerasi sebanyak 1 dan 2 kali terhadap logam Cu berturut-turut sebesar
92,14%, 83,91%, dan 81,59%. Dan persentase penyerapan dari zeolit alam
sebelum dan setelah diregenerasi sebanyak 1 dan 2 kali terhadap logam Zn
berturut-turut sebesar 93,86%, 83,28%, dan 77,64%.
5.2 Saran
Pada penelitian ini, regenerasi zeolit alam hanya dilakukan sampai 2 kali dan
menggunakan metode yang sama dengan proses aktivasi. Oleh karena itu perlu
dilakukan penelitian lebih lanjut terhadap pemakaian zeolit alam yang diregenerasi
diatas 2 kali sampai diketahui batas optimum proses regenerasi yang masih dapat
DAFTAR PUSTAKA
Atkins, P.W., 1978. Physical Chemistry. San Francisco: W. H. Freeman and
Company.
Darmono., 1995. Logam Dalam Sistem Biologi Makhluk Hidup. Jakarta: UI-Press.
Eckenfelder, W. E., 20