LAMPIRAN 1
DATA PENELITIAN
1.1 BILANGAN IODIN ADSORBEN KULIT JENGKOL
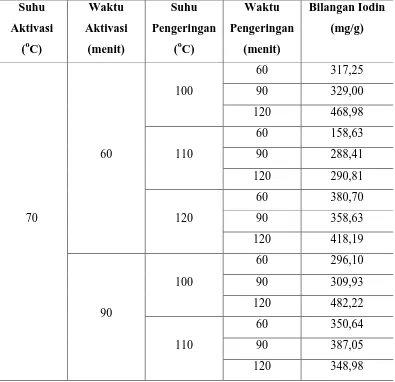
Dari modifikasi adsorben kulit jengkol yang dilakukan dengan memvariasikan suhu aktivasi sebesar 70, 80 dan 90 oC, waktu aktivasi selama 60, 90 dan 120 menit, suhu pengeringan sebesar 100, 110 dan 120 oC, waktu pengeringan selama 60, 90 dan 120 menit, serta rasio kulit jengkol : asam nitrat (b/v) sebesar 20:0,5; 20:1 dan 20:2 (mg/ml), diperoleh bilangan iodin masing-masing adsorben seperti pada Tabel L1.1, Tabel L1.2 dan Tabel L1.3 di bawah ini. Bilangan iodin adsorben kulit jengkol sebelum diaktivasi adalah 374,36 mg/g.
Tabel L1.1 Bilangan Iodin Adsorben Kulit Jengkol untuk Setiap Variasi Suhu dan Waktu
Suhu Aktivasi
(oC)
Waktu Aktivasi
(menit)
Suhu Pengeringan
(oC)
Waktu Pengeringan (menit) Bilangan Iodin (mg/g) 70 60 100
60 317,25
90 329,00
120 468,98
110
60 158,63
90 288,41
120 290,81
120
60 380,70
90 358,63
120 418,19
90
100
60 296,10
90 309,93
120 482,22
110
60 350,64
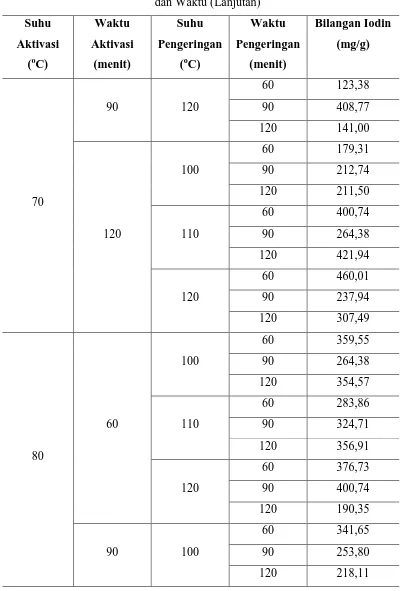
Tabel L1.1 Bilangan Iodin Adsorben Kulit Jengkol untuk Setiap Variasi Suhu dan Waktu (Lanjutan)
Suhu Aktivasi
(oC)
Waktu Aktivasi
(menit)
Suhu Pengeringan
(oC)
Waktu Pengeringan (menit) Bilangan Iodin (mg/g) 70
90 120
60 123,38
90 408,77
120 141,00
120
100
60 179,31
90 212,74
120 211,50
110
60 400,74
90 264,38
120 421,94
120
60 460,01
90 237,94
120 307,49
80
60
100
60 359,55
90 264,38
120 354,57
110
60 283,86
90 324,71
120 356,91
120
60 376,73
90 400,74
120 190,35
90 100
60 341,65
90 253,80
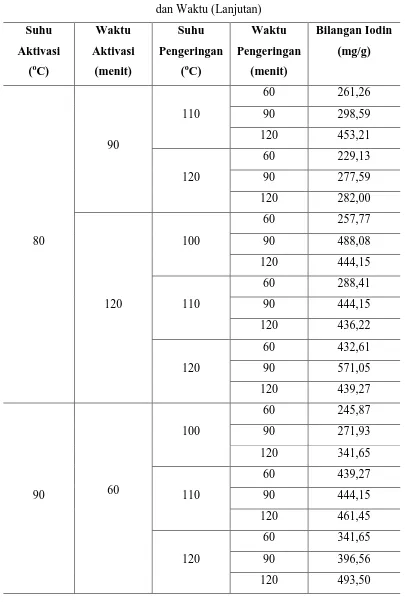
Tabel L1.1 Bilangan Iodin Adsorben Kulit Jengkol untuk Setiap Variasi Suhu dan Waktu (Lanjutan)
Suhu Aktivasi
(oC)
Waktu Aktivasi
(menit)
Suhu Pengeringan
(oC)
Waktu Pengeringan (menit) Bilangan Iodin (mg/g) 80 90 110
60 261,26
90 298,59
120 453,21
120
60 229,13
90 277,59
120 282,00
120
100
60 257,77
90 488,08
120 444,15
110
60 288,41
90 444,15
120 436,22
120
60 432,61
90 571,05
120 439,27
90 60
100
60 245,87
90 271,93
120 341,65
110
60 439,27
90 444,15
120 461,45
120
60 341,65
90 396,56
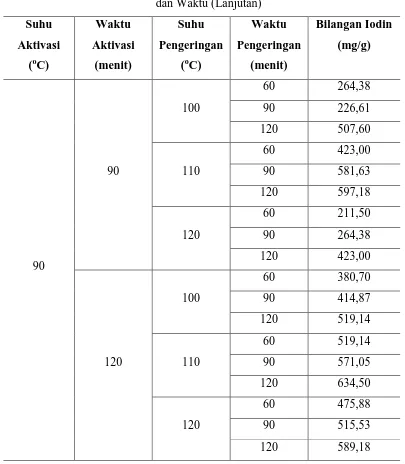
Tabel L1.1 Bilangan Iodin Adsorben Kulit Jengkol untuk Setiap Variasi Suhu dan Waktu (Lanjutan)
Suhu Aktivasi
(oC)
Waktu Aktivasi
(menit)
Suhu Pengeringan
(oC)
Waktu Pengeringan (menit) Bilangan Iodin (mg/g) 90 90 100
60 264,38
90 226,61
120 507,60
110
60 423,00
90 581,63
120 597,18
120
60 211,50
90 264,38
120 423,00
120
100
60 380,70
90 414,87
120 519,14
110
60 519,14
90 571,05
120 634,50
120
60 475,88
90 515,53
120 589,18
Tabel L1.2 Bilangan Iodin Adsorben Kulit Jengkol untuk Setiap Variasi Rasio Kulit Jengkol : Asam Nitrat
Rasio Kulit Jengkol : Asam Nitrat (mg/ml)
Bilangan Iodin (mg/g)
20 : 0,5 291,87
20 : 1 634,50
1.2 KAPASITAS ADSORPSI LOGAM Cd (II)
Kapasitas adsorpsi adalah banyaknya logam yang diserap pada rentang massa adsorben yang digunakan. Melihat proses adsorpsi yang digunankan dengan membandingkan dengan literatur yang ada, maka dapat dilihat kecendrungan pada proses adsorpsi fisika, karena menggunakan energi yang lebih rendah, suhu yang lebih rendah, dan proses cepat dan setimbang (reversibel). Limbah cair yang digunakan dalam penelitian ini sebelum dilakukan proses adsorpsi memiliki konsentrasi logam Cd (II) sebesar 20,35 ppm. Dari proses adsorpsi yang dilakukan dengan memvariasikan massa adsorben sebesar 0,5; 1 dan 1,5 diperoleh kapasitas adsorpsi logam Cd (II) yang ditunjukkan pada tabel L1.4 dibawah ini.
Tabel L1.3 Kapasitas Adsorpsi Ion Cd (II) pada Limbah Cair Pelapisan Logam untuk Setiap Variasi Massa Adsorben
Massa Adsorben (g) Absorbansi Konsentrasi (ppm)
Kapasitas Adsorpsi (mg/g)
0,5 0,219 7,090 1,326
1 0,282 9,269 0,554
LAMPIRAN 2
CONTOH PERHITUNGAN
2.1 PERHITUNGAN BILANGAN IODIN ADSORBEN
ilangan Iodin mgg 1 -VxN1N
W x W1xFp (30)
Dimana,
V = volume natrium tiosulfat yang diperlukan (ml) N1 = normalitas natrium tiosulfat (N)
N2 = normalitas iodin (0,1 N)
W1 = jumlah iodin untuk setiap 1 ml larutan natrium tiosulfat 0,1 N (12,69 mg/ml)
W2 = massa sampel (g) Fp = faktor pengenceran (5)
Misalnya untuk adsorben setelah diaktivasi pada suhu 80 oC dan waktu 120 menit dan dikeringkan pada suhu 110oC dan waktu 120 menit dan rasio adsorben : asam nitrat sebesar 20:1 (mg/mL), diketahui :
V = 9 ml N1 = 0,1 N W2 = 0,1 g Maka :
ilangan Iodin (mgg ) 1 9
x ,1 ,1
,1 x 1 ,69 x 5
= 634,50 mg/g
2.2 PERHITUNGAN KAPASITAS ADSORPSI ION Cd (II) qe Co- Ce V
W [7]
Dimana,
Ce = Konsentrasi akhir Cd (II) (mg/L) V = Volume sampel yang digunakan (L) W = Berat adsorben yang digunakan (g)
Misalnya untuk adsorpsi dengan menggunakan massa adsorben 0,5 g, diketahui :
Co = 20,35 mg/L Ce = 7,09 mg/L V = 0,05 L W = 0,5 g Maka :
Kapasitas Pen erapan ,35 7, 9 ,5
LAMPIRAN 3
FOTO PERCOBAAN PENELITIAN
3.1 FOTO PERCOBAAN ADSORPSI LOGAM KADMIUM DALAM LIMBAH CAIR ELEKTROPLATING
Gambar L3.1 Rangkaian Alat Percobaan Adsorpsi 1
2
3
4
Keterangan gambar : 1. Elenmeyer 2. Magnetic Stirrer 3. Hot Plate
DAFTAR PUSTAKA
[1] Elysa, “Uji Efek Ekstrak etanol Biji Jengkol (Pithecellobium Lobatum Benth.)
Terhadap Penurunan Kadar Glukosa Darah Tikus Putih Jantan Galur Wistar Yang
Diinduksi Aloksan” Jurnal Sains, 2011: hal 1
[ ] Kementerian Pertanian. “Statistik Produksi Hortiikultura Tahun 14”. Jurnal
Sains. 2015: Hal. 76-208.
[3] Sihombing, Sintong Parsaoran. Studi Pemanfaatan Ekstrak Kulit Jengkol (Pithecellobium Jiringa) Sebagai Antioksidan Alami. Jurnal Sains, 2012: hal 1
[4] Lay A, 9. “Pembuang Kulit Jengkol sedang Diintai”, http://www.borneotribu
ne.com/pontianak-kota/pembuang-kulit-jengkol-sedang-diintai.html.
[5] Putri Isnaini, Rahmiana Zein, Dan Edison Munaf, “Penyerapan Ion Cd II Dan Zn (II) Dalam Air Limbah Menggunakan Kulit Jengkol (Pithecellobium Jiringa Prain. ”, Jurusan Kimia Fmipa, Universitas Andalas. Padang : Jurnal Kimia Unand, 2(3) 2011: hal 1-7.
[6] Gusnidar, Yulnafatmawita Rosa Nofianti, “Pengaruh Kompos Asal Kulit Jengkol (Phitecolobium jiringa Jack Prain ex King) Terhadap Ciri Kimia Tanah Sawah dan
Produksi Tanaman Padi”, : Jurnal Kimia Unand, 2011: hal 2.
[7] Iffatunniswah Suhud, Vanny M. A. Tiwow, dan Baharuddin Hamzah. Adsorpsi Ion Kadmium(Ii) Dari Larutannya Menggunakan Biomassa Akar Dan Batang Kangkung Air (Ipomoea Aquatica Forks ”, Jurnal Sains, 2012: hal 1
[8] Suprihatin, Erriek A, “ ioabsorpsi Logam Cu II dan Cr VI Pada Limbah Elektroplating dengan Menggunakan iomassa Phanerochaete Chrysosporium”,
Jurnal Sains, 4(1) 2009: hal 1
[9] Charles Manurung, “Pengaruh Kuat Arus Terhadap Ketebalan Lapisan Dan Laju
Korosi Mpy Hasil Elektroplating aja Karbon Rendah Dengan Pelapis Nikel”, Jurnal Sains, 2011: hal 2
[1 ] Mario Hendro K, Ratih Sulastiningrum, “Pemisahan Kromium dan Nikel dari
Limbah Cair Elektroplating dengan Proses Ultrafiltrasi,” Jurnal Sains, 2014: hal. 2.
[11] Rumahlatu a. D. Corebima, M. Amin, F. Rachman, “Kadmium Dan Efeknya Terhadap Ekspresi Protein Metallothionein Pada Deadema Setosum (Echinoidea;
Echinodermata ”, Jurnal Sains 1(1) 2012: 26-35.
[13] Mohammed ali, Al-hashimi, Manar M. Al-safar “Removal Of Cadmium From
Synthetic Water y Using Agricultural Wastes” Jurnal Sains, 2013: hal. 1.
[14] Darwin, “Perbedaan Percepatan Penyembuhan Luka akar Dari Ekstrak Kulit Buah Jengkol (Pithecellobium Lobatum Benth.) Dalam Bentuk Sediaan Salep Dan Gel Secara Praklinis Pada Tikus Putih Jantan Galur Wistar”, Jurnal Sains, 11: hal 1.
[15] Donald G. MD. Barceloux, Djenkol Bean [Archidendron jiringa (Jack) I. C.
Nielsen]” Jurnal Sains, 9: hal. -3
[16] Hutauruk, J.E. Isolasi Senyawa Flavonoida Dari Kulit Buah Tanaman Jengkol
(Pithecellobium lobatum Benth.), Skripsi, 2010: hal. 2-3.
[17] Sancaya rini, Sugiarti, melani kurnia riswati. “Pesona Warna Indonesia”, Jurnal
Pertanian. 2011: hal 18.
[18] Nickel Institute, “Nickel Plating Handbook”. Brussels, Belgium. 2014
[19] Santhosh, sridevi. “A Lab-Scale Study On Reduction Of Heavy Metals From
Electroplating Effluent Using Conventional Chemical Precipitatio”,. Journal of
environmental research and development. 8(1) 2013: hal. 3-7
[20] Sitinaimah, Rahyani Ermawati, “Efektifitas Fotokatalis Tio Yang Dikompositkan Dengan Karbon Aktif Dan Precipitated Calcium Carbonat Dalam Menurunkan Chrom Dari Limbah Industri Elektroplating, Juurnal Sains, 2011: hal. 3
[ 1] Suwari, “Model Pengendalian Pencemaran Air Pada Wilayah Kali Surabaya”,
Tesis, 2010: hal. 247
[ ] Peraturan Kementrian Lingkungan Hidup Nomor 3 tahun 1 “ aku Mutu Air Limbah agi Kawasan Industri”
[23] Tjandra Setiadi, Fransisca I, Partiwi, Irma I, Widyarsa, “Pengolahan Limbah Cair Industri Tekstil yang Mengandung Zat Warna Azo Reaktif dengan Proses
Gabungan Anaerob dan Aerob,” Jurnal Sains, 1 : hal. -3.
[24] Cindy Rianti Priadi, Anita, Putri Nilam Sari, Setyo Sarwanto Moersidik,
“adsorpsi logam Seng dan Timbal Pada Limbah Cair Industri Keramik Oleh Limbah
Tanah Liat”, Jurnal Sains, 15 1 14: hal .
[25] Darmono, Lingkungan Hidup dan Pencemaran, Penerbit UI Press, Jakarta. 2001. Hal. 234-240
[26] Stumm,w. And morgan j.j, Aquatic Chemistry, An Introduction Emphasizing
Chemical Equibria In Natural Water, (John Wiley & Sons, New york 1991).
[28] Lidya Fernanda “Studi Kandungan Logam erat Timbal Pb , Nikel Ni , Kromium (Cr) Dan Cadmium (Cd) Pada Kerang Hijau (Perna Viridis) Dan Sifat Fraksionasinya Pada Sedimen Laut’, Skripsi. Fakultas matematika dadn ilmu pengetahuan alam departemen kimia, Depok, 2012, hal 35
[29] Mahdi gharabaghi, mehdi irannajad, amir reza azadmehr. “Optimization Of Cadmium Dissolution From A Hazardous Waste By Statistical Design Of
Experiments,” Environmental engineering and management journal. 13(12) 2014:
hal. 1-2
[30] Husin a, Muhammad, “Adsorpsi Dan Desorpsi Gas Metana Pada Bejana ertekanan Vessel Dengan Kenaikan Tekanan Secara ertahap”, Skripsi, Fakultas teknik, UI, Depok, 2012, hal. 6-27
[31] Edward Tandy, Ismail Fahmi Hasibuan, Hamidah Harahap, “Kemampuan Adsorben Limbah Lateks Karet Alam Terhadap Minyak Pelumas Dalam Air”, Jurnal Sains, 1(2) 2012: hal. 34-34
[3 ] Endah Retno D, Agus P, arkah Rizki S, Nurul Wulandari, “Pembuatan
Ethanol Fuel Grade Dengan Metode Adsorbsi Menggunakan Adsorbent Granulated Natural Zeolite Dan Cao,” Jurnal Sains, 2012: hal. 1-2.
[33] Haniffudin Nurdiansah, Diah Susanti, “Pengaruh Variasi Temperatur Karbonisasi dan Temperatur Aktivasi Fisika dari Elektroda Karbon Aktif Tempurung Kelapa dan Tempurung Kluwak Terhadap Nilai Kapasitansi Electric Double Layer
Capacitor EDLC ”, Jurnal Sains, 1 13: hal. 1-2
[34] Muhammad Turmuzi, Arion Syaputra, “Pengaruh Suhu Dalam Pembuatan Karbon Aktif Dari Kulit Salak (Salacca Edulis) Dengan Impregnasi Asam Fosfat H3PO4 ”, Jurnal Sains, 4 1 Maret 15: hal 3.
[35] Standar Nasional Indonesia. 1995. Arang Aktif Teknis (SNI 06-370-1995). Jakarta: Badan Standardisasi Nasional Indonesia.
[36] Lisanti Emelda, Suhardini Martiana Putri, Simparmin Br. Ginting, “Utilization of Activated Natural Zeolites for Chromium Adsorption” Jurnal Sains, 4 4 13: hal. 2
[37] Reza Mulyawan, Asep Saefumillah, Foliatin, “Biosorpsi Timbal Oleh Biomassa Daun Ketapang”, Jurnal Sains, 1 1 15: hal. 1.
[38] Agus Mangiring Siburian dan Agnes Sartika Doharma Pardede, “Pemanfaatan Adsorben dari Biji Asam Jawa untuk Menurunkan Bilangan Peroksida pada CPO (Crude Palm Oil ”, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
Air Kelapa Muda di andung,” Skripsi, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Jenderal Achmad Yani, Cimahi, 2010.
[40] ASTM, “Standard Test Method for Determination of Iodine Number of Activated Carbon,” American Society for Testing and Material, Philadelphia, 1999.
[41] Nailul Fauziah, “Pembuatan Arang Aktif Secara Langsung dari Kulit Acacia Mangium Wild dengan Aktivasi Fisika dan Aplikasinya Sebagai Adsorben,” Skripsi, Program Sarjana Fakultas Kehutanan IPB, Bogor, 2009, hal. 6 -10.
[42] Siti Jamilatun, Martomo Setyawan, “Pembuatan Arang Aktif dari Tempurung Kelapa dan Aplikasinya untuk Penjernihan Asap Cair,” Spektrum Industri, 12(1)
2014 : hal. 78 - 79.
[43] Amalia Aisha Noer, Awitdrus, Usman Malik, “Pembuatan Karbon Aktif dari Pelepah Kelapa Sawit Menggunakan Aktivator H2O Sebagai Adsorben,” JOM
FMIPA, 1(2) 2014 : hal. 42 - 46.
[44] Hayan Mao, Dingguo Zhou, Zaher Hashisho, Sunguo Wang, Heng Chen,
Haiyan Helena Wang, “Preparation of Pinewood and Wheat Straw-Based Activated
Carbon Via A Microwave-Assisted Potassium Hydroxide Treatment and An Analysis of The Effects of The Microwave Activation Conditions,” Bioresources,
10(1) 2015 : hal 809 - 817.
[45] Allwar, Ahmad in Md Noor, Mohd Asri in Mohd Nawi, “Textural Characteristics of Activated Carbons Prepared from Oil Palm Shells Activated with ZnCl2 and Pyrolysis Under Nitrogen and Carbon Dioxide,” Journal of Physical Science, 19(2) 2008 : hal. 93 - 100.
[46] Suqin Li, Liingling Zhang, aiyi Pan, Guohong Xiong, Daqiang Cang, “Study on Preparation and Charaterization of The Adsorbents With Sewage Sludge,”
Srcosmos, 2010, hal. 1 - 3.
[47] Sarifah Fauziah Syed Draman, Norzila Mohd, Nor Hafiza Izzati Wahab, Nurul Syahirah Zulkfli, Nor Fatin Adila Abu akar, “Adsorption of Lead II Ions In Aqueous Solution Using Selected Agro-Waste,” ARPN Journal of Engineering and Applied Sciences, 10(1) 2015, hal. 297 - 299.
[48] Jamal A. Abudaia, Muhamed O. Sulyman, Khalad Y. Elazaby, Salah M. Ben-Ali, “Adsorption of Pb II dan Cu II from Aqueous Solution onto Activated
Carbon Prepared from Dates Stones,” International Journal of Environmental
Science and Development, 4(2) 2013, hal. 191 - 194.
[50] Barbara Stuart, Infrared Spectroscopy: Fundamentals and Applications (John Wiley & Sons Ltd,1999), hal. 71 - 86.
[51] John Coates, Interpretation of Infrared Spectra, A Practical Approach (John Wiley & Sons Ltd, 2000), hal. 1 - 15.
[52] Roozbeh Hoseinzadeh Hesas, Arash Arami-Niya, Wan Mohd Ashri Wan Daud,
J.N. Sahu, “Preparation and Characterization of Activated Carbon from Apple Waste
by Microwave-Assisted Phosporic Acid Activation: Application in Methylene Blue
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilakukan di Laboratorium Operasi Teknik Kimia dan Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara dan Laboratorium Penelitian, Fakultas Farmasi, Universitas Sumatera Utara. Penelitian ini dilaksanakan selama kurang lebih 5 bulan.
3.2 BAHAN DAN PERALATAN 3.2.1 Bahan
Pada penelitian ini bahan-bahan yang digunakan antara lain :
1. Limbah Cair dari salah satu Industri Pelapisan Logam di sekitar Kawasan Industri Medan (KIM)
2. Kulit Jengkol (Pithecellobium jiringa Prain) yang dikumpulkan dari pajak Simpang Limun
3. Aquadest (H2O)
5. Asam Nitrat (HNO3) 4N 6. Asam Klorida (HCl)
7. Natrium Hidroksida (NaOH) 8. Natrium Tiosulfat (Na2S2O3) 0,1 N 9. Iodin (I2) 0,1 N
10. Indikator Amilum 1%
3.2.2 Peralatan
Pada penelitian ini peralatan yang digunakan antara lain: 1. Atomic Absorption Spectroscopy (AAS)
2. Spektrofotometer FTIR 3. Corong gelas
4. Termometer
5. Hot plate dan magnetic stirrer
7. Beaker glass
8. Tabung reaksi 9. Erlenmeyer 10. Oven
11. Alat-alat titrasi 12. Gelas ukur
13. Ayakan 100 mesh 14. Lumpang dan alu 15. Ball mill
16. Stopwatch
17. Timbangan digital 18. Batang pengaduk 19. Penjepit tabung 20. pH meter 21. Desikator
3.3 PROSEDUR PERCOBAAN 3.3.1 Pembuatan Adsorben
1. Kulit Jengkol dicuci dengan air lalu dikeringkan di bawah sinar matahari selama 7 hari.
2. Kulit Jengkol dihaluskan hingga berbentuk serbuk berukuran 100 mesh.
3. Kulit Jengkol diaktifkan dengan larutan asam nitrat (HNO3) 4 N dengan rasio bahan baku : asam nitrat adalah 20:0,5 mg/mL dan dipanaskan selama 60 menit pada suhu 70 oC, lalu didinginkan.
4. Setelah dingin, dilanjutkan dengan pencucian beberapa kali menggunakan
aquadest untuk menghilangkan pengotor terlarut.
5. Adsorben dimasukkan ke dalam oven selama 60 menit pada suhu 100 oC. 6. Prosedur diulangi untuk suhu aktivasi 80 dan 90 oC, waktu aktivasi 90 dan 120
3.3.2 Analisa Bilangan Iodin pada Adsorben
1. Timbang 1 gram adsorben dan keringkan pada suhu 115 oC selama 1 jam [39]. 2. Lakukan pendinginan dalam desikator.
3. Selanjutnya tambahkan 50 ml larutan iod 0,1 N dan diaduk dengan magnetic
stirer selama 15 menit.
4. Saring dan diambil sebanyak 10 ml filtrat. Titrasi dengan larutan Na2S2O3 0,1 N sampai warna kuning berkurang.
5. Selanjutnya tambahkan beberapa tetes indikator amilum 1% dan dititrasi kembali sampai larutan tidak berwarna
6. Catat volume Na2S2O3 0,1 N yang terpakai. Titrasi juga dilakukan untuk larutan blanko. Bilangan iodin dihitung dengan menggunakan persamaan:
ilangan Iodin ቀmggቁ 1 -VxN1
N
W x W1xFp [40]
Dimana,
V = volume natrium tiosulfat yang diperlukan (ml) N1 = normalitas natrium tiosulfat (N)
N2 = normalitas iodin (0,1 N)
W1 = jumlah iodin untuk setiap 1 ml larutan natrium tiosulfat 0,1 N (12,69 mg/ml)
W2 = massa sampel (g) Fp = faktor pengenceran (5) (40)
3.3.3 Analisa Karakteristik Gugus Fungsi dengan Spektrofotometri FTIR 1. Siapkan sampel yang akan diuji.
2. Lakukan pengukuran dengan alat FTIR dan amati grafik yang terbentuk.
3. Simpan data yang dihasilkan dan lakukan pembahasan terhadap puncak-puncak yang terbentuk
3.3.4 Prosedur Adsorpsi Batch
1. Diukur 50 ml sampel limbah cair pelapisan logam dan dimasukkan ke dalam beaker glass.
2. Diatur pH sebesar 5 dengan penambahan larutan 0,1 M HNO3 atau 0,1 M NaOH. Karena proses adsorpsi Cd (II) optimum pada pH 5.
3. Ditambahkan adsorben kulit jengkol berukuran 100 mesh dengan massa 0,5 g. 4. Campuran diaduk menggunakan magnetic stirrer dengan kecepatan 150 rpm
dan dipertahankan selama 15 menit.
5. Campuran disaring dengan corong gelas dan kertas saring Whatman No.1 6. Ulangi percobaan untuk variasi massa kulit jengkol 1 dan 1,5 g.
3.3.5 Prosedur Analisa Konsentrasi Ion Logam Cd (II)
Untuk menentukan dan melihat konsentrasi Cd (II) pada limbah cair, maka setiap sampel yang diuji, dianalisa menggunakan Atomic Adsorption Spectrofotometri (AAS). Perbedaan konsentrasi logam Cd (II) mula-mula atau
sebelum dan sesudah perlakuan merupakan jumlah ion logam Cd (II) yang terserap adsorben. Pengujian dilakukan dengan mengukur nilai serapannya pada panjang gelombang 228,8 nm. Kemudian dari data tersebut, akan dicari kapasitas adsorpsi ion logam Cd (II) dengan persamaan :
qe Co - Ce V
W [5] Dimana,
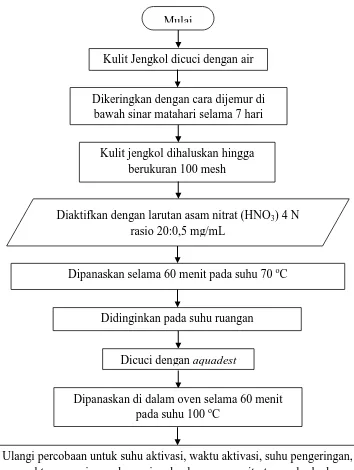
3.4 FLOWCHART PENELITIAN 3.4.1 Pembuatan Adsorben Kulit Jengkol
Alur proses pembuatan adsorben kulit Jengkol dapat digambarkan melalui
flowchart pada Gambar 3.1.
Gambar 3.1 Flowchart Pembuatan Adsorben Kulit Jengkol Mulai
Kulit jengkol dihaluskan hingga berukuran 100 mesh
Dikeringkan dengan cara dijemur di bawah sinar matahari selama 7 hari
Didinginkan pada suhu ruangan
Dicuci dengan aquadest
Selesai
Diaktifkan dengan larutan asam nitrat (HNO3) 4 N rasio 20:0,5 mg/mL
Dipanaskan selama 60 menit pada suhu 70 oC
Dipanaskan di dalam oven selama 60 menit pada suhu 100 oC
Ulangi percobaan untuk suhu aktivasi, waktu aktivasi, suhu pengeringan, waktu pengeringan dan rasio adsorben : asam nitrat yang berbeda
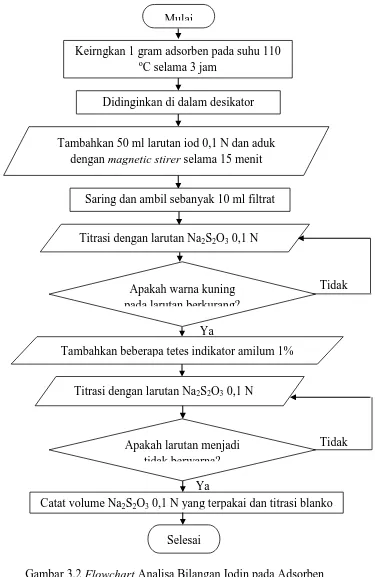
Ya 3.4.2 Analisa Bilangan Iodin pada Adsorben
Alur proses analisa bilangan iodin adsorben dapat digambarkan melalui
flowchart pada Gambar 3.3.
Gambar 3.2 Flowchart Analisa Bilangan Iodin pada Adsorben Mulai
Keirngkan 1 gram adsorben pada suhu 110 o
C selama 3 jam
Didinginkan di dalam desikator
Tambahkan 50 ml larutan iod 0,1 N dan aduk dengan magnetic stirer selama 15 menit
Saring dan ambil sebanyak 10 ml filtrat
Titrasi dengan larutan Na2S2O3 0,1 N
Tidak Apakah warna kuning
pada larutan berkurang?
Tambahkan beberapa tetes indikator amilum 1% Ya
Titrasi dengan larutan Na2S2O3 0,1 N
Tidak Apakah larutan menjadi
tidak berwarna?
Catat volume Na2S2O3 0,1 N yang terpakai dan titrasi blanko
3.4.3 Analisa Karakteristik Gugus Fungsi pada Adsorben
Alur proses analisa karakteristik gugus fungsi pada adsorben dapat digambarkan melalui flowchart pada Gambar 3.2.
Gambar 3.3 Flowchart Analisa Karakteristik Gugus Fungsi pada Adsorben
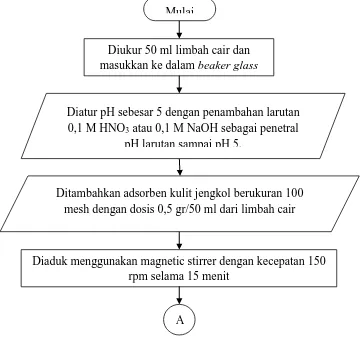
3.4.4 Proses Adsorpsi Batch
Alur proses adsorpsi dapat digambarkan melalui flowchart pada Gambar 3.5. Mulai
Diukur 50 ml limbah cair dan masukkan ke dalam beaker glass
Diatur pH sebesar 5 dengan penambahan larutan 0,1 M HNO3 atau 0,1 M NaOH sebagai penetral
pH larutan sampai pH 5.
Ditambahkan adsorben kulit jengkol berukuran 100 mesh dengan dosis 0,5 gr/50 ml dari limbah cair
Diaduk menggunakan magnetic stirrer dengan kecepatan 150 rpm selama 15 menit
Disiapkan sampel adsorben kulit jengkol yang akan diuji
Lakukan pengukuran dengan alat FTIR dan amati grafik yang terbentuk
Selesai Mulai
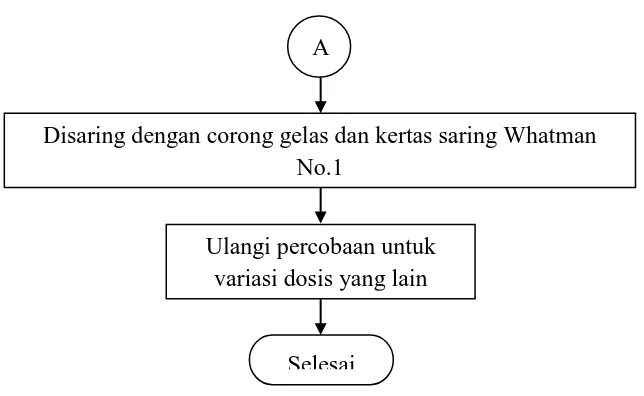
Gambar 3.4 Flowchart Prosedur Adsorpsi Batch Disaring dengan corong gelas dan kertas saring Whatman
No.1
Ulangi percobaan untuk variasi dosis yang lain
BAB IV
HASIL DAN PEMBAHASAN
4.1 BILANGAN IODIN ADSORBEN KULIT JENGKOL
Pada penelitian ini, adsorben dari bahan baku kulit jengkol diaktivasi secara kimia dengan aktivator asam nitrat (HNO3) 4 N dan dioptimasi dengan memvariasikan suhu aktivasi 70, 80 dan 90 oC, waktu aktivasi 60, 90 dan 120 menit, suhu pengeringan 100, 110 dan 120 oC dan waktu pengeringan 60, 90 dan 120 menit. Setelah diperoleh hasil yang optimum dari variasi tersebut, adsorben dioptimasi lagi menggunakan variasi rasio adsorben : asam nitrat sebesar 20:0,5; 20:1 dan 20:2 (mg/ml). Sebelum dan setelah diaktivasi, dilakukan analisa bilangan iodin terhadap adsorben (mg I2/g adsorben). Sebelum aktivasi, bilangan iodin adsorben kulit jengkol adalah 374,36 mg/g. Nilai ini sedikit lebih rendah daripada bilangan iodin adsorben biji asam jawa yaitu sebesar 379,81 mg/g [29]. Perbedaan hasil ini mungkin disebabkan karena perbedaan jumlah pengotor pada adsorben yang dihasilkan sebelum aktivasi dilakukan. Berdasarkan data Standar NasionaI Indonesia (1995), standar kualitas karbon aktif untuk daya serap terhadap iodin yaitu minimal 750 mg/g [35]. Dalam hal ini adsorben kulit jengkol tidak memenuhi standar karbon aktif berdasarkan SNI karena bilangan iodin yang diperoleh secara keseluruhan masih dibawah 750 mg/g.
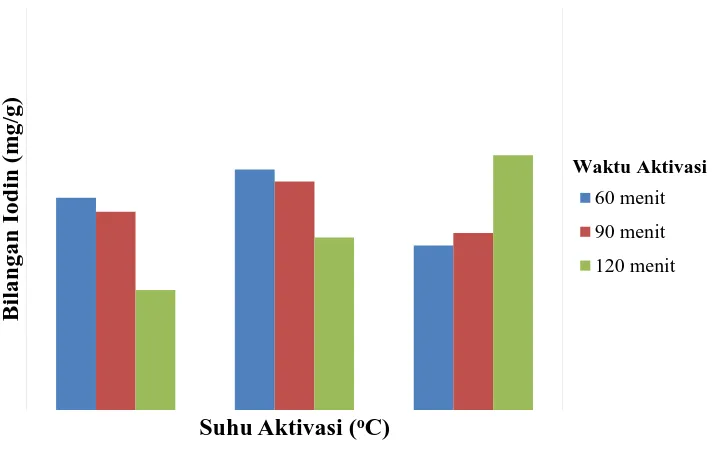
4.1.1 Pengaruh Suhu Aktivasi (oC), Waktu Aktivasi (menit), Suhu Pengeringan (oC) dan Waktu Pengeringan (menit) terhadap Bilangan Iodin Adsorben Kulit Jengkol
Gambar 4.1 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 100oC dan Waktu Pengeringan 60 menit
Gambar 4.2 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 100oC dan Waktu Pengeringan 90 menit
B
il
an
gan
Iod
in
(m
g/g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
120 menit
B
il
an
gan
Iod
in
(m
g/g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
Gambar 4.3 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 100oC dan Waktu Pengeringan 120 menit
Dari Gambar 4.1, 4.2 dan 4.3 diatas dapat dilihat pengaruh suhu aktivasi, waktu aktivasi, suhu pengeringan dan waktu pengeringan terhadap bilangan iodin adsorben kulit jengkol pada suhu pengeringan 100oC untuk waktu pengeringan 60, 90 dan 120 menit.
Pada Gambar 4.1 yaitu pada waktu aktivasi 60 dan 90 menit bilangan iodin meningkat dengan meningkatnya suhu aktivasi dari 70oC ke 80oC namun setelah itu mengalami penurunan pada suhu 90oC. Namun pada waktu aktivasi 120 menit, bilangan iodin terus meningkat dengan meningkatnya suhu aktivasi. Pada Gambar 4.2, bilangan iodin mengalami variasi peningkatan dan penurunan yang tidak beraturan pada ketiga grafik dengan meningkatnya suhu aktivasi. Pada Gambar 4.3 bilangan iodin menunjukkan variasi peningkatan dan penurunan juga namun pada waktu aktivasi 120 menit, bilangan iodin terus meningkat dimana sebelumnya ditunjukkan juga pada Gambar 4.1 pada waktu aktivasi yang sama.
Menurut teori, peningkatan suhu memperluas permukaan adsorben yang ditandai dengan meningkatnya bilangan iodin [42]. Adanya kesesuaian teori secara berulang yang hanya terdapat pada waktu 120 menit yaitu pada Gambar 4.1 dan 4.3 menunjukkan bahwa waktu aktivasi 120 menit merupakan waktu yang optimum
B
il
an
ga
n
Io
d
in
(m
g/
g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
dalam aktivasi adsorben kulit jengkol selama 90 menit dengan bilangan iodin tertinggi pada Gambar 4.3 sebesar 519,14 mg/g.
Pada Gambar 4.1 dan 4.2 dapat dilihat bilangan iodin yang dihasilkan secara keseluruhan lebih rendah daripada Gambar 4.3. Hal ini menunjukkan dari ketiga grafik, suhu pengeringan optimum pada suhu 100 oC dengan waktu pengeringan optimum pada waktu 120 menit.
Gambar 4.4 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 110oC dan Waktu Pengeringan 60 menit
B
il
an
ga
n
Io
d
in
(m
g/
g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
Gambar 4.5 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 110oC dan Waktu Pengeringan 90 menit
Gambar 4.6 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 110oC dan Waktu Pengeringan 120 menit
Dari Gambar 4.4, 4.5 dan 4.6 diatas dapat dilihat pengaruh suhu aktivasi, waktu aktivasi, suhu pengeringan dan waktu pengeringan terhadap bilangan iodin
B
il
an
gan
Iod
in
(m
g/g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
120 menit
B
il
an
gan
Iod
in
(m
g/g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
adsorben kulit jengkol pada suhu pengeringan 110oC untuk waktu pengeringan 60, 90 dan 120 menit.
Pada Gambar 4.4 yaitu pada waktu aktivasi 90 dan 120 menit bilangan iodin menurun dengan meningkatnya suhu aktivasi dari 70oC ke 80oC namun setelah itu mengalami peningkatan pada suhu 90oC. Namun pada waktu aktivasi 60 menit, bilangan iodin terus meningkat dengan meningkatnya suhu aktivasi. Pada Gambar 4.5 yaitu pada waktu aktivasi 60 dan 120 menit bilangan iodin terus meningkat dengan meningkatnya suhu aktivasi. Namun pada waktu aktivasi 90 menit, bilangan iodin menurun dengan peningkatan suhu dari 70 sampe 80oC kemudian naik pada suhu 90oC. Pada Gambar 4.6 bilangan iodin terus meningkat dengan meningkatnya suhu untuk setiap variasi waktu aktivasi.
Menurut teori, peningkatan suhu memperluas permukaan adsorben yang ditandai dengan meningkatnya bilangan iodin [42]. Pada Gambar 4.4 dan 4.5 terdapat kesesuaian teori pada waktu aktivasi 60 menit untuk masing-masing grafik. Namun Gambar 4.6 menunjukkan kesesuaian teori pada ketiga grafik, yaitu meningkatnya bilangan iodin dengan meningkatnya suhu aktivasi. Hal ini menunjukkan bahwa suhu pengeringan 110 dan waktu pengeringan 120 menit merupakan suhu dan waktu yang optimum dengan bilangan iodin 634,50 mg/g untuk suhu aktivasi 110 menit dan waktu aktivasi 120 menit.
Gambar 4.7 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin
B
il
an
gan
Iod
in
(m
g/g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
Gambar 4.8 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 120oC dan Waktu Pengeringan 90 menit
Gambar 4.9 Pengaruh Suhu Aktivasi dan Waktu Aktivasi terhadap Bilangan Iodin Pada Suhu Pengeringan 120oC dan Waktu Pengeringan 120 menit
Dari Gambar 4.7, 4.8 dan 4.9 diatas dapat dilihat pengaruh suhu aktivasi, waktu aktivasi, suhu pengeringan dan waktu pengeringan terhadap bilangan iodin
B
il
an
gan
Iod
in
(m
g/g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
120 menit
B
il
an
ga
n
Io
d
in
(m
g/
g)
Suhu Aktivasi (oC)
Waktu Aktivasi
60 menit
90 menit
adsorben kulit jengkol pada suhu pengeringan 120oC untuk waktu pengeringan 60, 90 dan 120 menit.
Pada Gambar 4.7 pada tiap waktu aktivasi bilangan iodin mengalami variasi kenaikan dan penurunan dengan meningkatnya suhu aktivasi. Pada Gambar 4.8 yaitu pada waktu aktivasi 60 dan 120 menit bilangan iodin meningkat dengan meningkatnya suhu aktivasi dari suhu 70 ke 80oC kemudian turun pada suhu 90oC. Namun pada waktu aktivasi 90 menit, bilangan iodin terus menurun dengan meningkatnya suhu aktivasi. Pada Gambar 4.9 bilangan iodin meningkat dengan meningkatnya suhu untuk waktu aktivasi 90 dan 120 menit. Namun pada waktu 60 menit bilangan iodin menurun kemudian naik lagi dengan meningkatnya suhu aktivasi.
Menurut teori, peningkatan suhu memperluas permukaan adsorben yang ditandai dengan meningkatnya bilangan iodin [42]. Pada Gambar 4.9 adanya kesesuaian teori pada grafik yaitu pada waktu 90 dan 120 menit. Hal ini menunjukkan bahwa dari ketiga grafik suhu pengeringan 120oC dan waktu pengeringan 120 menit yang paling dengan bilangan iodin tertinggi 589,18 pada suhu aktivasi 90oC dan waktu 120 menit.
Dari keseluruhan grafik, bilangan iodin cenderung meningkat seiring bertambahnya suhu aktivasi, suhu pengeringan, suhu pengeringan dan waktu pengeringan. Hal ini menunjukkan semakin tinggi suhu dan waktu maka daya serap adsorben juga semakin meningkat. Namun pada grafik tertentu bilangan iodin mengalami penurunan dengan meningkatnya suhu serta waktu pada kedua proses. Hal ini dapat disebabkan karena beberapa kemungkinan. Pertama, kadar air sulit dikontrol sebelum dilakukan penyerapan senyawa iodin. Kedua, ketidak merataan adsorben dalam wadah saat proses aktivasi dilakukan sehingga asam nitrat tidak efektif dalam memodifikasi adsorben kulit jengkol. Bilangan iodin yang optimum diperoleh pada suhu aktivasi 90 oC, waktu aktivasi 120 menit, suhu pengeringan 110oC dan waktu pengeringan 120 menit sebesar 634,50 mg/g.
terjadi ditandai dengan meningkatnya bilangan iodin [42]. Waktu aktivasi yang semakin lama dapat meningkatkan bilangan iodin suatu adsorben yang dapat ditandai dengan meningkatnya kandungan karbon dalam adsorben tersebut [43]. Meningkatnya waktu pengeringan dapat menyebabkan terbukanya mesopori dan mikropori yang meningkatkan ukutan pori adsorben [44]. Namun pada pemanasan yang berlebihan dapat terjadi pengurangan mesopori dan mikropori pada adsorben tersebut [38] serta menyebabkan kerusakan struktur dan dinding pori yang dapat menghambat pertumbuhan pori [45].
Dengan membandingkan teori dan hasil yang diperoleh dari penelitian, dapat disimpulkan bahwa kondisi yang paling baik untuk menghasilkan adsorben dari kulit jengkol dengan bilangan iodin yang paling optimum pada suhu aktivasi 90 oC, waktu aktivasi 120 menit, suhu pengeringan 110oC dan waktu pengeringan 120 menit adalah sebesar 634,50 mg/g.
4.1.2 Pengaruh Rasio Kulit Jengkol : Asam Nitrat terhadap Bilangan Iodin Adsorben
[image:30.595.132.508.524.690.2]Pada penelitian ini dapat dilihat kapasitas adsorpsi adsorben yang paling baik dari berbagai variasi rasio kulit jengkol : asam nitrat tertentu yang dinyatakan sebagai bilangan iodin (mg/g), yaitu jumlah mg iodin yang dapat diserap oleh setiap 1 gram adsorben, sebagaimana digambarkan melalui grafik pada Gambar 4.10 di bawah ini.
Gambar 4.10 Pengaruh Rasio Kulit Jengkol : Asam Nitrat terhadap Bilangan Iodin Adsorben
B
il
an
gan
Iod
in
(m
g/g)
Dari grafik pada Gambar 4.10 di atas dapat dilihat bahwa bilangan iodin semakin meningkat seiring dengan semakin tingginya rasio kulit jengkol : asam nitrat. Bilangan iodin paling besar diperoleh pada rasio 20:2.
Pada rasio 20:0,5 ; 20:1 dan 20:2 (mg/ml), bilangan iodin terus meningkat. Bilangan iodin meningkat dari rasio 20:0,5 ke 20:1. Namun pada rasio 20:2, peningkatan yang ada tidak terlalu besar, sehingga dapat dianggap bahwa rasio 20:1 merupakan rasio kulit jengkol : asam nitrat yang paling optimum dalam menyerap senyawa iodin. Hal ini disebabkan oleh jumlah aktivator yang digunakan pada rasio 20:1 sudah cukup untuk memodifikasi adsorben dari kulit jengkol yang digunakan.
Secara teori, semakin meningkatnya rasio kulit jengkol : aktivator yang digunakan maka daya serap adsorben akan semakin meningkat. Hal ini disebabkan adanya dehidrasi kimia serta kondensasi yang semakin kuat sehingga menghasilkan struktur pori yang besar [46].
Dengan membandingkan teori dan hasil yang diperoleh dari penelitian, dapat disimpulkan bahwa kondisi rasio kulit jengkol : asam nitrat yang paling optimum dalam menyerap senyawa iodin yaitu sebesar 20:1 dengan bilangan iodin 634,50 mg/g.
Berdasarkan data Standar NasionaI Indonesia (1995), standar kualitas karbon aktif untuk daya serap terhadap iodin yaitu minimal 750 mg/g [33]. Dalam hal ini adsorben kulit jengkol belum memenuhi standar karbon aktif berdasarkan SNI karena bilangan iodin yang optimum yaitu sebesar 634,50 mg/g masih dibawah standar karbon aktif SNI. Hal ini dapat disebabkan karena aktivasi tidak dilakukan dengan cara karbonisasi.
4.2 ADSORPSI LOGAM Cd (II) PADA LIMBAH CAIR INDUSTRI PELAPISAN LOGAM
Limbah cair yang digunakan dalam penelitian ini adalah limbah cair yang berasal dari salah satu industri pelapisan logam di sekitar Kawasan Industri Medan (KIM). Kandungan logam Cd (II) awal dalam limbah cair sebelum dilakukan proses adsorpsi dengan adsorben adalah sebesar 20,35 ppm.
Pada penelitian ini dapat dilihat kemampuan adsorpsi adsorben yang paling baik dari variasi massa adsorben tertentu yang dinyatakan sebagai kapasitas adsorpsi (mg/g), sebagaimana digambarkan melalui grafik pada Gambar 4.4. Konsentrasi logam Cd (II) dalam limbah cair sebesar 20,35 ppm dengan adsorbansi 0,487.
Gambar 4.11 Pengaruh Massa Adsorben terhadap Kapasitas Adsorpsi Adsorben
Dari grafik pada Gambar 4.11 di atas dapat dilihat bahwa kapasitas adsorpsi cenderung menurun seiring dengan semakin banyaknya massa adsorben. Kapasitas adsorpsi yang paling besar diperoleh pada massa adsorben 0,5 gram yaitu sebesar 1,32 mg/g dengan adsorbansi 0,219.
Pada massa adsorben 0,5; 1 dan 1,5 gram, kapasitas adsorpsi terus menurun. Pada massa adsorben 0,5 g konsentrasi Cd (II) berkurang menjadi 7,09 ppm dengan kapasitas adsorpsi 1,32 mg/g. Pada massa adsorben 1 g dengan konsentrasi Cd (II) 9,26 ppm diperoleh kapasitas adsorpsi 0,55 mg/g. Pada massa adsorben 1,5 g dengan konsentrasi 11,96 ppm diperoleh kapasitas adsorpsi 0,27 mg/g. Hal ini dapat terjadi karena pada dosis lebih dari 0,5 adsorben membentuk gumpalan-gumpalan yang menyebabkan berkurangnya luas permukaan adsorben [5] dan perpindahan massa yang terjadi saat proses adsorpsi berlangsung menjadi kurang baik.
Secara teori, semakin meningkatnya dosis adsorben yang digunakan maka kapasitas adsorpsi juga akan semakin meningkat. Hal ini disebabkan situs atau luas permukaan adsorpsi meningkat bersamaan dengan berat dari adsorben, sehingga
-0.1 0.1 0.3 0.5 0.7 0.9 1.1 1.3 1.5
0.5 1 1.5
K
ap
asitas
Adso
rp
si
(m
g/g)
memberikan hasil kapasitas adsorpsi yang lebih besar pada massa adsorben yang lebih besar [47]. Kapasitas adsorpsi dapat berkurang dengan meningkatnya massa adsorben dapat disebabkan oleh terbentuknya gumpalan yang menyebabkan menurunnya luas permukaan keseluruhan [48]. Hal ini juga bisa disebabkan oleh kendala-kendala teknis seperti pola pengontakan, perbandinagn luas wadah dengan mixer, dan juga penggunaan magnetic stirrer yang memungkinkan lengketnya logam-logam berat pada saat adsorpsi berlangsung.
Dengan membandingkan teori dan hasil yang diperoleh dari penelitian, dapat disimpulkan bahwa massa yang paling optimum dalam menjerap logam Cd (II) yaitu sebesar 0,5 yang dinyatakan dengan kapasitas adsorpsi sebesar 1,32 mg/g. Rendahnya kapasitas penyerapan logam Cd pada adsorben dapat terjadi karena adanya logam-logam lain seperti krom (Cr), tembaga (Cu), seng (Zn), nikel (Ni) dan Timbal (Pb) dalam limbah cair industri pelapisan logam sehingga terjadi kompetisi di dalam proses adsorpsi logam berat.
Berdasarkan Peraturan Mentri Lingkungan Hidup, kandungan Cd (II) yang diperbolehkan dibuang ke lingkungan untuk limbah cair industri pelapisan logam adalah sebesar 0,1 ppm. Namun konsentrasi Cd (II) yang paling rendah dalam limbah cair pada penelitian ini adalah sebesar 7,09 ppm. Kadar tersebut masih jauh dengan baku mutu lingkungan hidup. Hal ini dapat disebabkan karena beberapa kemungkinan. Pertama, limbah cair yang digunakan berasal dari inlet buangan yang memiliki konsentrasi ion Cd (II) yang masih tinggi. Kedua proses adsorpsi merupakan pengolahan tingkat ke-3, dimana ada 2 proses pengolahan limbah yang dilakukan di industri pelapisan logam terlewati.
4.3 KARAKTERISTIK GUGUS FUNGSI PADA ADSORBEN KULIT JENGKOL DENGAN SPEKTROFOTOMETRI FTIR
39
[image:34.595.115.527.213.491.2]menunjukkan pita absorpsi energi yang unik dalam analisa FTIR dan hal ini berguna untuk mengidentifikasi adanya gugus-gugus fungsional dari adsorbent [49]. Gugus-gugus fungsional yang terbentuk disimpulkan dengan membandingkannya dengan literatur yaitu Tabel karakteristik pita IR berbagai senyawa [50] dan Tabel frekuensi berbagai gugus-gugus fungsi [51]. Adapun hasil yang diperoleh dapat dilihat pada Gambar 4.5, 4.6 dan 4.7 berikut.
Gambar 4.12 Hasil Spektrofotometri FTIR Adsorben Kulit Jengkol Sebelum Aktivasi
547,78 cm-1 : gugus S-S (senyawa sulfur) 1612,49 cm-1 : gugus C=C (alkena) 1045,42 cm-1 : gugus C-H (alkena aromatik) 2349,30 cm-1 : gugus CO2
1219,01 cm-1 : gugus P-O (senyawa fosfor) (karbondioksida) 1338,60 cm-1 : gugus C-H (alkana) 2939,52 cm-1 : gugus C-H (alkana) 1519,91 cm-1 : gugus NO2 (senyawa nitro) 3394,72 cm
-1
[image:34.595.112.511.620.802.2]Gambar 4.13 Hasil Spektrofotometri FTIR Adsorben Kulit Jengkol Sesudah Aktivasi
Gambar 4.14 Hasil Spektrofotometri FTIR Adsorben Kulit Jengkol Sesudah Adsorpsi
Dari Gambar 4.12, 4.13 dan 4.14 di atas dapat dibandingkan gugus-gugus fungsi yang terdapat pada adsorben sebelum dan sesudah aktivasi serta sesudah adsorpsi. Dari grafik pada Gambar 4.12, yaitu adsorben sebelum aktivasi terlihat gugus fungsional hidroksil termasuk ikatan hidrogen [regangan O-H (3700-3200 cm -1
)], yang semakin tidak tampak pada Gambar 4.13 dan 4.14 yaitu adsorben sesudah aktivasi dan sesudah adsorpsi. Reduksi dari ikatan hidrogen ini menunjukkan asam nitrat sebagai agen pengdehidrasi, bereaksi dengan bahan baku setelah kedua substansi tercampur. Pergeseran pita pada 2939,52 sebelum diaktivasi menjadi
2924,09 cm-1 yang merupakan regangan C-H juga menunjukkan adanya pelepasan sejumlah hidrogen secara signifikan. Pada adsorben sebelum diaktivasi terdapat regangan pada 1045,42 cm-1 yang merupakan regangan alkena aromatik C-H. Pita ini tidak terdapat pada adsorben sesudah aktivasi, sehingga dapat disimpulkan aktivasi kimia melepaskan banyak ikatan pada senyawa aromatik dan mengeliminasi banyak substrat-substrat ringan dan volatil [52].
Pada Gambar 4.12, yaitu adsorben sebelum aktivasi juga terlihat regangan pada 2349,30 cm-1 yang menunjukkan regangan CO2 yang tidak tampak pada adsorben sesudah aktivasi pada Gambar 4.13. Adanya regangan pada 1612,49 cm-1 yang merupakan rengangan C=C (ikatan alkena) bergeser menjadi 1635,64 cm-1 dan berkurang ketajamannya pada adsorben yang diaktivasi. Adanya regangan pada 1519,91 (regangan NO2) pada adsorben sebelum aktivasi yang menunjukkan senyawa nitro tidak tampak lagi pada adsorben setelah aktivasi. Pelepasan gugus CO2 menunjukkan aktivasi kimia melepas sejumlah oksigen yang terperangkap dalam adsorben. Pembentukan gugus sulfonil pada adsorben yang terjadi akibat pergeseran pita pada 547,78 cm-1 (pada Gambar 4.12) menjadi 470,63 cm-1 (Gambar 4.13) yaitu regangan S-S (senyawa sulfur) yang menunjukkan terjadinya pengikatan oksigen oleh sulfur setelah aktivasi memperlihatkan kemungkinan peningkatan daya adsorpsi oleh adsorben karena gugus sulfonil terlibat pada proses adsorpsi di penjelasan selanjutnya.
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang dapat diambil dari penelitian ini adalah:
1. Bilangan iodin adsorben yang paling besar adalah 634,50 mg/g yang diperoleh pada aktivasi dengan suhu 90 oC dan waktu 120 menit dan pada pengeringan dengan suhu 110 oC dan waktu 120 menit serta rasio kulit jengkol : asam nitrat 20:1 (mg/mL).
2. Adsorpsi terbaik terhadap ion logam Cd (II) diperoleh pada massa adsorben 1 gr/50 mL limbah cair dengan kapasitas penyerapan 1,32 mg/g
3. Dari hasil spektofotometri IR adsorben dapat disimpulkan bahwa aktivasi kimia pada adsorben dapat mereduksi ikatan hidrogen, melepas senyawa aromatik dan mengeliminasi berbagai substrat yang ringan dan volatil serta pada prosesnya, adsorpsi logam Cd (II) melibatkan gugus hidroksil, sulfonil, fosfor dan merkaptan.
4. Pada proses adsorpsi, konsentrasi ion Cd (II) yang paling rendah adalah 7,09 ppm belum memenuhi baku mutu lingkungan hidup yaitu sebesar 0,1 ppm.
5.2 SARAN
Adapun saran yang dapat diberikan kepada peneliti selanjutnya, yaitu:
1. Dilakukan uji perbandingan dengan adsorben dengan variasi tetap dan berubah yang sama, namun diaktivasi dengan cara karbonisasi untuk mengetahui perbedaan bilangan iodin yang dihasilkan.
2. Dilakukan analisa SEM dan BET pada adsorben untuk melihat topografi dan komposisi permukaan adsorben kulit jengkol.
BAB II
TINJAUAN PUSTAKA
2.1 JENGKOL
2.1.1 Pengertian Kulit Jengkol
Jengkol atau Jering atau Pithecellobium jiringa Jack. atau Pithecellobium
lobatum Benth. adalah tumbuhan khas di wilayah Asia Tenggara, termasuk yang
[image:39.595.111.525.344.500.2]digemari di Malaysia, Thailand dan Indonesia terutama di wilayah Jawa Barat yang seharinya dikonsumsi 100 ton [14]. Sementara potensi tumbuhan jengkol di Indonesia dapat di lihat pada Tabel 2.1 dibawah ini:
Tabel 2.1 Pertumbuhan Luas panen, dan rata-rata hasil jengkol di Indonesia tahun 2009 – 2014 [2].
Tahun Luas Panen (ha) Rata-rata Hasil (Ton/ha)
2009 7.631 8,19
2010 6.943 7,24
2011 7.907 8,33
2012 7.407 8,40
2013 6.838 8,94
2014 6.678 8,04
Kulit jengkol adalah bagian terluar dari Jengkol yang berwarna coklat yang melapisi daging buah kulit jengkol dan Kulit jengkol merupakan sampah pertanian yang bisa dijadikan sebagai biosorben dengan biaya yang sangat murah [5]. Jengkol mengandung sulfur dan asam amino dengan rumus molekul C11H23N3S3O6 dengan berat basah 0,3-1,3g/100g dengan komponen cysteine thioacetal formaldehid.
[image:39.595.187.475.649.728.2]Jengkol merupakan salah satu tumbuhan dengan ukuran pohon yang tinggi yaitu ± 20 m , tegak bulat berkayu, licin, percabangan simpodial, cokelat kotor. Bentuk majemuk, lonjong, berhadapan , panjang 10 - 20 cm, lebar 5 - 15 cm, tepi rata, ujung runcing, pangkal membulat, pertulangan menyirip, tangkai panjang 0,5 – 1 cm, warna hijau tua. Struktur majemuk, berbentuk seperti tandan, diujung dan ketiak daun, tangkai bulat, panjang ± 3 cm , berwarna ungu kulitnya, bentuk buah menyerupai kelopak mangkok, benang sari kuning, putik silindris, kuning mahkota lonjong, putih kekuningan. Bulat pipih berwarna coklat kehitaman, berkeping dua dan berakar tunggang. Pohon Jengkol sangat bermanfaat dalam konservasi air disuatu tempat hal ini dikarenakan ukuran pohonnya yang sangat tinggi.
Klasifikasi ilmiah jengkol adalah sebagai berikut : Divisi : Spermatophyta
Sub divisi : Angiospermae Kelas : Dicotyledonae Bangsa : Rosales Suku : Fabacceae Genus : Pithecellobium
Spesies : Pithecellobium jiringa (Jack) Prain [16]
2.1.2 Kandungan Dalam Kulit Jengkol
[image:40.595.183.459.618.752.2]Kandungan kulit jengkol merupakan hal yang sangat penting, karena sangat menentukan dalam pemanfaatan kulit jengkol, terutama pemanfaatan kulit jengkol untuk penyerapan logam berat. Kandungan kulit jengkol dapat di lihat pada Tabel 2.1
Tabel 2.2 Kandungan dalam kulit Jengkol [6] Kadar unsur hara Kandungan (%)
Kadar Air 65,56
N-total 1,82
P-total 0,32
K-total 2,10
Mg-total 0,25
C-total 44,02
C/N 24,19
Dari Tabel kandungan kulit jengkol unsur karbon merupakan nilai persen kedua tertinggi, hal ini yang memungkinkan kulit jengkol dapat dijadikan adsorben.
2.1.3 Pemanfatan Tumbuhan Jengkol
Hampir seluruh bagian tanaman bermanfaat. Kayunya untuk bangunan rumah, peti mati dan kayu bakar. Daun mudanya untuk obat luka, rebusan dari babakannya dapat menurunkan kadar glukosa darah. Dinding polong yang di tumbuk dimanfaatkan untuk mencuci rambut. Bijinya dapat dikonsumsi namun pada orang yang memakannya air seninya akan berbau keras. Selain itu, di beberapa tempat di buat makanan ringan seperti keripik. Bagian yang dimanfaatkan untuk pewarna: Daunnya digunakan untuk memberikan warna hitam pengganti sumba. Bagian yang mengandung zat warna adalah kulit buah, kulit biji dan kulit batang. Menurut laporan, zaman dahulu di sepanjang pantai Kalimantan Barat kulit dan daun jengkol digunakan untuk member warna hitam pada bahan anyaman [17]. Sementara kulit jengkol baru dimanfaatkan sebagai bioherbisida dan biolarvasida. Padahal dalam kulit jengkol terkandung alkaloid, flavonoid, glikosida antrakinon, tannin, triterpenoid/steroid, dan saponin dan senyawa unsur kimia seperti N, P, K, Ca, Mg, C, dan C/N.
2.2 INDUSTRI PELAPISAN LOGAM
2.2.1 Pengertian Industri Pelapisan Logam (Elektroplating)
atau tegangan diterapkan antara elektroda ion ini bermigrasi ke arah elektroda dengan muatan yang berlawanan - bermuatan positif ion ke katoda dan ion bermuatan negatif untuk anoda. Hal ini menyebabkan transfer elektron, yang merupakan aliran arus, antara elektroda - sehingga menyelesaikan sirkuit listrik [18].
[image:42.595.160.447.204.367.2]Skema sel elektropalating dapat di lihat dari Gambar 2.2 di bawah ini.
Gambar 2.2 Sekema sel elektropalating [18]
Industri elektroplating menghasilkan produk samping berupa limbah cair dengan unsur logam yang sangat tinggi seperti uranium, kadmium, merkuri, nikel, kromium dan tembaga. Limbah yang di hasilkan ini berdampak buruk pada lingkungan, karena biasanya limbah industri pelapisan logam sering di buang ke sungai. Unsur - unsur ini dikenal sebagai unsur B3 (Beracun dan Berbahaya), karena unsur ini bersifat karsinogenik [19].
2.2.2 Potensi dan Keadaan Industri Elektroplating di Indonesia
limbah logam berat yaitu rata-ratanya: 358.22 m3/hari. Hal ini diyakini sangat berdampak besar pada pencemaran lingkungan [21]. Sifat karakteristik limbah industri elektroplating yaitu: pH 2; Cr 311,09 ppm; Ni 2,7 ppm; Cd 12-24 ppm; Zn 31,85; Fe 44,64; TDS 306 ppm; COD 777,54 ppm [10]. Sedangkan mengacu pada peraturan menteri negara lingkungan hidup nomor 03 tahun 2010 baku mutu air limbah bagi kawasan industri dapat dilihat pada Tabel 1.1 dibawah ini:
Tabel 2.3 Baku Mutu Air Limbah Bagi Kawasan Industri Elektroplating [22].
No Parameter Satuan Kadar Maksimum
1 Sulfida (H2S) mg/L 1
2 Amonia (NH3) mg/L 20
3 Fenol (C6H6O) mg/L 1
4 Kadmium (Cd) mg/L 0,1
5 Krom (Cr) mg/L 1
6 Tembaga (Cu) mg/L 2
7 Timbal (Pb) mg/L 1
8 Nikel (Ni) mg/L 0,5
9 Seng (Zn) mg/L 10
Melihat dari karakteristik dan kadar maksimum peraturan mentri Negara lingkungan hidup tentunya membrikan pebandingan yang sangat jauh, sehingga kondisi seperti ini dapat dikategorikan sebagai permasalahan semua pihak dan harus diatasi secara bersama-sama.
2.2.3 Pengolahan Limbah Industri Elektroplating di Indonesia
Teknologi pengolahan limbah cair merupakan kunci dalam memeliharan kelestarian lingkungan. Apapun teknologi pengolahan limbah cair industri yang dibangun harus dapat dioperasikan dan dipelihara oleh perusahana setempat. Berbagai teknik pengolahan limbah cair untuk menyisihkan bahan polutannya telah dicoba dan dikembangkan selama ini. Teknik-teknik pengolahan air buangan yang telah dikembangkan tersebut secara umum terbagi menjadi 3 metode pengolahan:
untuk suatu jenis air buangan tertentu, ketiga metode pengolahan tersebut dapat diaplikasikan secara sendiri-sendiri atau secara kombinasi. Pengolahan air buangan dapat dilakukan secara fisika, kimia dan biologi, atau gabungan biologi-kimia dan kimia-biologi. Cara fisika memisahkan sebagian dari beban pencemaran yang berupa bahan-bahan tersuspensi dengan cara adsorpsi, sedimentasi, dan filtrasi. Adsorpsi dilakukan dengan memanfaatkan karbon aktif sebagai adsorbannya, namun kendala yang timbul adalah mahalnya harga karbon aktif. Cara kimia yang umumnya digunakan adalah koagulasi, flokulasi dan penetralan. Masalah dalam pengolahn limbah kimiawi adalah banyaknya endapan lumpur yang dihasilkan sehingga perlu penangana lebih lanjut [23].
Berbagai macam teknologi telah dikembangkan untuk menyisihkan logam berat dari air limbah. Teknik konvensional yang biasanya digunakan adalah proses fisik-kimiawi, seperti presipitasi, oksidasi, reduksi, ekstraksi pelarut, ekstraksi elektrolisis, penguapan, osmosis, pertukaran ion dan adsorpsi. Reverse osmosis meskipun sangat efektif, merupakan proses yang membutuhkan biaya yang besar. Presipitasi kimia tidak cocok digunakan jika polutan yang hadir dalam jumlah banyak dan juga akan menghasilkan banyak lumpur dalam proses ini. Proses adsorpsi merupakan salah satu metode yang paling sering dilakukan untuk penyisihan logam beracun dalam air limbah. Adsorpsi merupakan proses fisik-kimiawi dimana adsorbat, dalam hal ini pencemar, terakumulasi di permukaan padatan yang disebut adsorben. Proses adsorpsi cocok untuk air limbah dengan logam konsentrasi rendah dan industri dengan keterbatasan biaya [24].
2.3 LOGAM KADMIUM (CD) 2.3.1 Pengertian Logam Kadmium
berbagai bidang industri kimia tersebut karena sifat kadmium yang lunak dan tahan korosi [25].
2.3.2 Sumber Kadmium (Cd)
Logam Kadmium merupakan bahan alami yang terdapat dalam kerak bumi, berwarna putih, ditemukan dalam bentuk senyawa gabungan seperti kadmium oksida, kadmium klorida, dan kadmium sulfida . Kadmium masuk ke dalam air bersih dari sumber yang berasal dari industri. Air sungai dan irigasi untuk pertanian yang mengandung kadmium akan terjadi pengendapan pada sedimen dan lumpur. Sebagian besar kadmium dalam tanah berpengaruh pada pH, larutan material organik, logam yang negandung oksida, tanah liat dan zat organik, maupun anorganik [26].
2.3.3 Sifat-Sifat Logam Kadmium 1. Sifat Fisik
a. Logam berwarna putih keperakan dan mengkilat b. Kalor penguapan 99.87 kJ·mol−1
c. Titik didih 1413 °F, 767 °C, 1040 K d. Titik lebur 594.22 K, 609.93 °F 321.07 °C e. Massa jenis (mendekati suhu kamar) 8.65 g·cm−3
f. Mengalami kerusakan bila terkena uap amonia dan sulfur hidroksida. 2. Sifat Kimia
a. Kadmium tidak larut dalam basa
b. Larut dalam H2SO4 encer dan HCl encer Cd + H2SO4 → CdSO4 + H2 c. Bereaksi dengan halogen dan nonlogam seperti S, Se, P
d. Kadmium adalah logam yang cukup aktif
e. Dalam udara terbuka, jika dipanaskan akan membentuk asap coklat CdO f. Memiliki ketahanan korosi yang tinggi [27].
2.3.4 Manfaat dan Kerugian dari Logam Kadmium
pencampuran logam. Beberapa gram kadmium seperti sulfida, karbonat dan oksida, tidak larut dalam air. Namun dapat berubah menjadi larut dalam air garam di alam bawah pengaruh oksigen. Kadmium merupakan komponen campuran logam yang memiliki titik lebur terendah.Unsur ini dugunakan dalam campuran logam poros dengan koefisen gesek yang rendah dan tahan lama. Logam ini juga banyak digunakan dalam aplikasi sepuhan listrik electroplating [28].
Kadmium adalah logam berat beracun yang ditemukan sebagai konstituen minor dari bijih seng. Kadmium biasanya diproduksi sumber daya primer dan skunder seperti basis konsentrat logam, limbah baterai Ni-Cd, listrik debu tanur, surya sel, dan bahan fluorescent. Adapun dampak negatif logam Cd dalam tubuh manusia yaitu dapat menghambat kerja paru-paru, bahkan mengakibatkan kanker paru-paru, mual, muntah, diare, kram, anemia, kerusakan ginjal dan hati [29].
2.4 ADSORBSI
2.4.1 Pengertian Adsorbsi
Adsorpsi adalah fenomena fisik yang terjadi antara molekul-molekul fluida (gas atau cair) yang dikontakkan dengan suatu permukaan padatan. Adsorpsi adalah proses dimana molekul- molekul fluida menyentuh dan melekat pada permukaan padatan [30]. Berdasarkan gaya yang bekerja, proses adsorpsi dibagi menjadi dua, yaitu adsorpsi fisika dan adsorpsi kimia. Pada adsorpsi fisika, gaya utama bekerja adalah gaya gaya Van der Waals. Gaya ini relatif lemah dengan energi yang terlibat sekitar 20 kkal/mol. Sementara pada adsorpsi kimia, terdapat proses perpindahan elektron yang sama dengan pembentukan ikatan kimia antara permukaan padatan dengan zat terjerap. Adsorpsi kimia biasanya terjadi pada proses-proses katalitik heterogen. Aktivasi kimia pada adsorben pada umumnya digunakan industri yang umumnya lebih efisien dalam penghilangan impurities (kotoran). Pada adsorpsi fisika terjadi proses cepat dan setimbang (reversibel) sedangkan adsorpsi kimia berlangsung lambat tetapi ireversibel [31].
2.4.2 Jenis dan Sumber Adsorben
1. Zeolit
Zeloid merupakan material berpori dan memiliki beberapa kandungan mineral dominan (SiO4 dan AlO4). Kapasitas adsorpsinya dapat ditingkatkan dengan aktivasi larutan asam kuat atau basa kuat. Zeolit memiliki bentuk kristal yang sangat teratur dengan rongga yang saling berhubungan ke segala arah yang menyebabkan luas permukaan zeolit sangat besar [32].
2. Karbon aktif
Karbon aktif merupakan suatu bentuk arang yang telah melalui aktifasi dengan menggunakan gas CO2, uap air atau bahan-bahan kimia sehingga pori-porinya terbuka dan dengan demikian daya absorpsinya menjadi lebih tinggi terhadap zatwarna dan bau. Karbon aktif mengandung 5 sampai 15 persen air, 2 sampai 3 persen abu dan sisanya terdiri dari karbon. Karbon yang sekarang banyak digunakan berbentuk butiran (granular) dan berbentuk bubuk (tepung). Besarnya daya serap karbon aktif sangat dipengaruhi oleh keadaan pori-pori yang terbentuk. Pori-pori pada karbon aktif memiliki beberapa jenis sebagai berikut :
a. Mikropori dengan ukuran dibawah 40 Angstrom b. Mesopori dengan ukuran antara 40 - 5000 Angstrom c. Makropori dengan ukuran diatas 5000 Angstrom
pada bahan baku yang berbeda dan perlakuan yang berbeda maka dominasi pori-pori yang terbentuk juga berbeda. Pada karbon aktif dengandominasi mikropori sangat sesuai untuk digunakan sebagai penyerap molekul-molekus kecil seperti molekul gas dan dengan tingkat kontaminan rendah. Sedangkan karbon aktif dengan dominasi makropori sesuai untuk menyerap molekul yang lebih besar seperti molekul cairan dan sangat cocok untuk decolorizing. Pembuatan karbon aktif terdiri dari tiga tahap yaitu:
a. Dehidrasi: proses penghilangan air. Bahan baku dipanaskan sampai temperatur 170 °C.
b. Karbonisasi: pemecahan bahan-bahan organik menjadi karbon. Karbonasi dilakukan pada suhu 400-900ºC
dengan uap atau CO2 sebagai activator. Akitivasi biasanya ada dua yaitu aktivasi fisika (suhu tinggi) dan aktivasi kimia (menggunakan bahan kimia basa pada suhu rendah) [33].
Sifat karbon aktif yang paling penting adalah daya serap. Dalam hal ini, ada beberapa faktor yang mempengaruhi daya serap adsorbsi, yaitu: sifat adsorben, sifat serapan, dan temperatur. Karbon aktif yang merupakan adsorben adalah suatu padatan berpori, yang sebagian besar terdiri dari unsur karbon bebas dan masing- masing berikatan secara kovalen. Dengan demikian, permukaan karbon aktif bersifat non polar. Selain kompisisi dan polaritas, struktur pori juga merupakan faktor yang penting diperhatikan. Struktur pori berhubungan dengan luas permukaan, semakin kecil pori-pori karbon aktif, mengakibatkan luas permukaan semakin besar. Dengan demikian kecepatan adsorbsi bertambah. Untuk meningkatkan kecepatan adsorbsi, dianjurkan agar menggunakan karbon aktif yang telah dihaluskan. Banyak senyawa yang dapat diadsorbsi oleh karbon aktif, tetapi kemampuannya untuk mengadsorbsi berbeda untuk masing- masing senyawa. Adsorbsi akan bertambah besar sesuai dengan bertambahnya ukuran molekul serapan dari sturktur yang sama, seperti dalam deret homolog. Adsorbsi juga dipengaruhi oleh gugus fungsi, posisi gugus fungsi, ikatan rangkap, struktur rantai dari senyawa serapan [32].
[image:48.595.130.480.602.753.2]Pada penelitian ini yang menjadi standar kualitas karbon aktif dengan menentukan besar bilangan iodin dimana jumlah milligram iodin yang teradsorpsi oleh satu gram karbon aktif. pori-pori karbon aktif akan terbuka sehingga penyerapan karbon aktif terhadap larutan iodin semakin besar, apabila suhu dinaikan akan terjadi dekomposisi sampel menjadi abu [34]. Kualitas karbon aktif dapat dinilai berdasarkan persyaratan (SNI) 06–3730-1995 pada Tabel 2.4.
Tabel 2.4 Standarisasi Karbon Aktif (SNI) 06–3730-1995 [35]
Jenis Persyaratan Parameter
Kadar Air Mak. 15 %
Kadar Abu Mak. 10 %
Kadar Zat Menguap Mak. 25 %
Kadar Karbon Terikat Min. 65 %
3. Silika gel
Slika gel adalah substansi-substansi yang digunakan untuk menyerap kelembaban dan cairan partikel dari ruang yang berudara/bersuhu. Silika gel yang siap untuk digunakan berwarna biru. Ketika silica gel telah menyerap banyak kelembaban, ia akan berubah warnanya menjadi pink (merah muda). Ketika ia berubah menjadi warna pink (merah muda), ia tidak bisa lagi menyerap kelembaban. Ia harus meregenerasi. Hal ini dapat dilakukan dengan menghangatkannya di dalam mesin oven. Panas nya mengeluarkan kelembaban, lalu ia akan berubah warnanya menjadi biru dan kembali bisa digunakan [36].
4. Biosorpsi
Biosorpsi menggunakan adsorben dari biomassa sebagai penyerap ion logam yang terkandung dalam limbah sehingga kandungan ion logam dalam air limbah menjadi turun. Contohnya: alga, limbah hasil pertanian, dan lumut [37].
2.4.3 Faktor- Faktor yang Mempengaruhi Adsorbsi
Dalam menentukan proses tingginya penyerapan proses adsorpsi ada beberapa faktor yang mempengaruhi diantaranya:
1. Ukuran molekul adsorbat
Ukuran molekul yang sesuai merupakan hal penting agar proses adsorpsi dapat terjadi, karena molekul yang dapat di adsorpsi adalah molekul-molekul yang diameternya leih kecil atau sama dengan diameter pori adsorben. 2. Kepolaran zat
Apabila berdiameter sama, molekul-molekul polar lebih kuat diadsorpsi daripada molekul molekul tidak polar. Molekul-molekul yang lebih polar dapat menggantikan molekul-molekul yang kurang polar yang terlebih dahulu teradsorpsi.
3. Kemurnian adsorben
Sebagai zat untuk mengadsorpsi, maka adsorben yang lebih murni lebih diinginkan karena kemampuan adsorpsi lebih baik.
Jumlah molekul adsorbat yang teradsorp meningkat dengan bertambahnya luas permukaan dan volume pori adsorben.
5. Temperatur absolute (T)
Temperatur yang di maksud adalah temperatur adsorbat. Pada saat molekul-molekul gas atau adsorbat melekat pada permukaan adsorben akan terjadi pembaebasan sejumlah energi yang dinamakan peristiwa eksotermis. Berkurangya temperatur akan menambah jumlah adsorbat yang teradsorpsi demikian juga untuk peristiwa sebaliknya.
6. Tekanan (P)
Tekanan yang dimaksut adalah tekanan adsorbat. Kenaikan tekanan adsorbat dapat menaikkan jumlah yang di adsorpsi.
7. Interaksi Potensial (E)
Interaksi potensial antara adsorbat dengan dinding adsorben sangat bervariasi, tergantung dari sifat adsorbat-adsorben.
8. pH medium
Memiliki dampak yang signifikan terhadap penyerapan adsorbat oleh perbedaan adsorben. Hal ini disebabkan oleh fakta bahwa hidrogen ion itu sendiri adalah adsorbat bersaing kuat, dan sebagian karena spesiasi kimia ion logam di bawah pengaruh pH larutan [30].
2.5 DESKRIPSI PROSES
120 menit. Variasi waktu ini berdekatan dengan waktu aktivasi yang dilakukan oleh Hamzah [12].
Adsorben yang dihasilkan kemudian dianalisa kemampuan adsorpsinya terhadap iodin yang dinyatakan dengan bilangan iodin. Adsorben yang memiliki bilangan iodin tertinggi selanjutnya akan digunakan sebagai adsorben dalam mengurangi kadar logam Cd (II) dalam limbah cair industri pelapisan logam.
Pada proses adsorpsi, digunakan adsorben yang melewati ayakan 100 mesh, volume limbah cair 50 mL, kecepatan pengadukan 150 rpm, waktu kontak 15 menit yang diadopsi dari penelitian Isnaini [5] pada kondisi optimum yang diperoleh. Pada proses ini dijaga pH 5 yang diadopsi dari jurnal yang ditulis oleh Muhammed dkk. [13], dimana proses adsorpsi Cd (II) optimum pada pH 5 berdasarkan beberapa penelitian terdahulu. Pada proses ini dilakukan variasi dosis adsorben sebesar 0,5 ; 1 dan 1,5 gr per 50 mL limbah cair untuk mengetahui jumlah adsorben yang optimum dalam mengurangi kandungan logam Cd (II) dalam industri pelapisan logam.
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Tumbuhan jengkol adalah tumbuhan khas di wilayah Asia Tenggara. Bijinya digemari di Malaysia, Thailand, dan Indonesia sebagai bahan pangan. Tumbuhan ini juga banyak ditemukan di Malaysia dan Thailand. Namun, asal-usul tanaman jengkol tidak diketahui dengan pasti. Di Sumatera, Jawa Barat, dan Jawa Tengah, tumbuhan jengkol banyak ditanam di kebun atau pekarangan secara sederhana [1]. Jengkol merupakan bagian dari 3 komponen utama yaitu: daging buah, kulit ari dan kulit jengkol. Bagian Kulit jengkol sebesar 30-40% berat jengkol. Menurut data statistik produksi holtikultura tumbuhan jengkol pada tahun 2014 Luas panen di Indonesia memiliki luas 6.678 ha dengan potensi rata-rata hasil 8,04 Ton/ha, sementara untuk daerah sumatera Utara memiliki potensi 333 Ha dengan hasil rata-rata 10,71 ton/ha, dimana jumlah tersebut lebih besar dari rata-rata potensi semua provinsi di Indonesia sebesar 8,04 Ton/ha. Bila dihitung potensi pencemaran limbah kulit jengkol di daerah Sumatera Utara mencapai 4,28 ton/ha atau 1.398,6 ton/tahun [2]. Kulit Jengkol (Pithecellobium jiringa Prain) selama ini tergolong limbah organik yang berserakan di pasar tradisional dan tidak memberikan manfaat. Sebagai contoh sampah organik ini mengotori lingkungan dan parahnya turut memberi kontribusi pada banjir yang terjadi di daerah Medan [3]. Tidak hanya di propinsi Sumatera Utara, di propinsi lain juga sampah organik ini tidak dimanfaatkan. Bahkan pemerintah daerah Pontianak mengeluarkan peraturan untuk menangkap masyarakat yang membuang kulit jengkol sembarangan [4].
memiliki unsur karbon sebesar 44,02%, yang diyakini unsur paling penting dapat dijadikannya kulit jengkol sebagai adsorben [6].
Beberapa metode yang dapat digunakan untuk menurunkan konsentrasi ion logam dalam limbah cair ataupun industri pelapisan logam diantaranya adalah adsorpsi, pengendapan, penukar ion dengan menggunakan resin, dan filtrasi. Diantara metode-metode tersebut, adsorpsi merupakan metode yang paling umum dipakai karena memiliki konsep yang lebih sederhana dan ekonomis [7]. Proses adsorpsi merupakan bagian dari pengolahan limbah dimana biasanya dilakukan pada tahap filtrasi dengan menggunakan beberapa adsorben seperti pelet, zeolite, karbon aktif, gel slika,