EKSPRESI p53 PADA ENDOMETRIOMA DIBANDINGKAN
KARSINOMA OVARIUM TIPE 1
TESIS
OLEH:
ALFRED HARA SINUHAJI
DEPARTEMEN OBSTETRI DAN GINEKOLOGI
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA RSUP. H. ADAM MALIK
PENELITIAN INI DI BAWAH BIMBINGAN TIM 5
PEMBIMBING:
dr. Aswar Aboet, MKed(OG), SpOG.K
dr. Deri Edianto, MKed(OG), SpOG.K
PENYANGGAH :
dr. Hotma Partogi Pasaribu, MKed(OG), SpOG
dr. Yostoto B. Kaban,SpOG.K
dr. Sarah Dina, MKed(OG), SpOG.K
Diajukan Untuk Melengkapi Tugas Dan Memenuhi
Salah Satu Syarat Untuk Mencapai Keahlian
KATA PENGANTAR
Segala Puji dan Syukur saya panjatkan ke hadirat Tuhan Yesus, karena atas
Berkat dan Karunia-Nya lah penulisan tesis ini dapat saya selesaikan dengan
baik.
Tesis ini disusun untuk melengkapi tugas-tugas dan memenuhi salah satu syarat
untuk menyelesaikan program pendidikan spesialis dalam bidang Obstetri dan
Ginekologi. Sebagai manusia biasa, saya menyadari bahwa tesis ini masih
memiliki banyak kekurangan dan masih jauh dari sempurna, namun demikian
besar harapan saya kiranya tulisan ini dapat bermanfaat dalam menambah
perbendaharaan bacaan khususnya tentang:
“ EKSPRESI P53 PADA ENDOMETRIOMA DIBANDINGKAN KARSINOMA OVARIUM TIPE 1”
Dengan selesainya laporan penelitian ini, perkenankanlah saya menyampaikan
rasa terima kasih dan penghargaan yang setinggi-tingginya kepada yang
terhormat :
Rektor Universitas Sumatera Utara Prof.Dr.dr.Syahril Pasaribu, DTM&H,
MSc (CTM), SpA(K) dan Dekan Fakultas Kedokteran Universitas Sumatera
memberikan kesempatan kepada saya untuk mengikuti Program Pendidikan
Dokter Spesialis di Fakultas Kedokteran USU Medan.
Prof.dr.Delfi Lutan, MSc, SpOG(K), Kepala Departemen Obstetri dan
Ginekologi FK-USU Medan ; dan DR. dr. M. Fidel Ganis Siregar, Mked(OG),
SpOG(K), Sekretaris Departemen Obstetri dan Ginekologi FK-USU Medan;
DR. dr Henry Salim Siregar, SpOG(K), Ketua Program Studi Pendidikan
Dokter Spesialis Obstetri dan Ginekologi FK-USU Medan ; dr. M. Rhiza Z.
Tala, MKed(OG), SpOG(K), Sekretaris Program Studi Pendidikan Dokter
Spesialis Obstetri dan Ginekologi FK-USU Medan ; dr. Makmur Sitepu,
MKed(OG), SpOG(K), Ketua divisi Fetomaternal SMF Kebidanan dan
Penyakit Kandungan RSHAM; dr. Ichwanul Adenin, MKed(OG), SpOG(K),
Ketua divisi Fertilisasi Endokrinologi dan Reproduksi SMF Kebidanan dan
Penyakit Kandungan RSHAM; Prof. dr. M. Fauzie Sahil, SpOG(K), Ketua
divisi Onkologi SMF Kebidanan dan Penyakit Kandungan RSHAM; Prof. dr.
R. Haryono Roeshadi, SpOG(K); Prof. dr. M. Jusuf Hanafiah, SpOG(K) ;
Prof. dr. Hamonangan Hutapea, SpOG(K) ; Prof. DR. dr. M. Thamrin
Tanjung, SpOG(K) ; Prof. dr. Djafar Siddik, SpOG(K) ; Prof. dr. T.M.
Hanafiah, SpOG(K) ; Prof. dr. Budi R. Hadibroto, SpOG(K) ; Prof. dr. Daulat
H. Sibuea, SpOG(K) dan Prof. dr. M. Fauzie Sahil, SpOG(K) yang telah
bersama-sama berkenan menerima saya untuk mengikuti Program
Pendidikan Dokter Spesialis di Departemen Obstetri dan Ginekologi di
Kepada dr. Aswar Aboet, MKed(OG), SpOG(K) sebagai Pembimbing Utama
Tesis saya ,bersama-sama dengan dr. Deri Edianto, MKed(OG), SpOG K
yang juga sebagai pembimbing tesis saya yang telah dengan sabar
meluangkan waktu dan pikiran yang sangat berharga dan juga sebagai nara
sumber untuk membimbing, mengkoreksi, dan melengkapi penulisan dan
penyusunan tesis ini hingga dapat diselesaikan dengan baik.
Kepada dr. Hotma Partogi Pasaribu , MKed(OG), SpOG; dr.Yostoto B.
Kaban, SpOG(K) ; dan dr. Sarah Dina, MKed(OG), SpOG(K), sebagai
penyanggah tesis saya, yang juga merupakan nara sumber yang telah
dengan penuh kesabaran meluangkan waktu yang sangat berharga untuk
membimbing, memeriksa, dan melengkapi penulisan tesis ini hingga dapat
diselesaikan dengan baik.
Terimakasih kepada dr. Putri C. Eyanoer, MPH yang telah dengan penuh
kesabaran meluangkan waktu dan pikiran untuk membimbing dan
membantu saya dalam penyelesaian analisis statistik tesis ini.
Saya juga mengucapkan terima kasih yang sebesarnya kepada divisi
onkologi atas kesempatan yang diberikan kepada saya untuk dapat
Terima kasih kepada dr. Makmur Sitepu, MKed(OG), SpOG. K sebagai
pembimbing Refarat Fetomaternal saya dengan judul “Imunologi
Preeclampsia”; Kepada dr. M. Oky Prabudi, MKed(OG), SpOG sebagai pembimbing Refarat Fertilitas Endokrinologi dan Reproduksi dengan judul
“Terapi Operatif pada Adenomiosis untuk Fertility Sparing, kepada dr. John S Khoman, SpOG(K) sebagai pembimbing Refarat Onkologi saya
dengan judul “PET Scan pada Kanker Serviks”.
Kepada dr.T.M. Ichsan, SpOG, selaku Bapak Angkat saya ,selama saya
menjalani masa pendidikan di Departemen Obstetri dan Ginekologi FK-USU,
yang telah banyak mengayomi, membimbing dan memberikan
nasehat-nasehat yang bermanfaat kepada saya dalam menghadapi masa-masa sulit
selama masa pendidikan.
Para Guru yang saya hormati,seluruh Staf Pengajar Departemen Obstetri
dan Ginekologi FK-USU Medan / RSUP H.Adam Malik / RSUD Dr.Pirngadi
Medan, yang secara langsung telah banyak membimbing dan mendidik saya
sejak awal hingga akhir pendidikan. Semoga Tuhan membalas budi baik
guru-guru saya tersebut.
Direktur RSUP. H. Adam Malik Medan; dan Ketua SMF Kebidanan dan
Penyakit Kandungan RSUP H.Adam Malik, beserta seluruh staf, para Bidan
serta bantuan kepada saya untuk bekerja selama mengikuti pendidikan dan
selama saya bertugas di SMF Kebidanan dan Penyakit Kandungan RSUP
H.Adam Malik Medan.
Direktur RSUD Dr. Pirngadi Medan dan Wakil Direktur Pelayanan RSUD Dr.
Pirngadi Medan, dr Rushakim Lubis, Mked(OG), SpOG beserta Ketua SMF
Kebidanan dan Penyakit Kandungan RSUD Dr.Pirngadi Medan, dr. Syamsul
Arifin Nasution, Mked(OG), SpOG(K); sekretaris SMF Kebidanan dan
Penyakit Kandungan RSUD Dr.Pirngadi Medan; Koordinator Pendidikan
dokter spesialis SMF Kebidanan dan Penyakit Kandungan RSUD
Dr.Pirngadi Medan, dr. Sanusi Piliang, SpOG; Koordinator penelitian SMF
Kebidanan dan Penyakit Kandungan RSUD Dr.Pirngadi Medan, dr. Fadjrir,
Mked(OG), SpOG, Koordinator pelayanan SMF Kebidanan dan Penyakit
Kandungan RSUD Dr.Pirngadi Medan, dr. Jenius L. Tobing, Mked(OG),
SpOG; Ketua divisi Fetomaternal SMF Kebidanan dan Penyakit Kandungan
RSUD Dr.Pirngadi Medan, dr. Christoffel Tobing, Mked(OG), SpOG(K);
Ketua divisi Fertilisasi Endokrinologi dan Reproduksi SMF Kebidanan dan
Penyakit Kandungan RSUD Dr.Pirngadi Medan, dr. Aswar Aboet,
Mked(OG), SpOG(K); Ketua divisi Onkoginekologi SMF Kebidanan dan
Penyakit Kandungan RSUD Dr.Pirngadi Medan, dr. Roy Yustin
Simanjuntak, SpOG(K) dan dr. John S. Khoman, SpOG(K) beserta seluruh
staff, para Bidan dan seluruh paramedis yang telah memberikan
mengikuti pendidikan Spesialis Obstetri dan Ginekologi di Departemen
Obstetri dan Ginekologi.
.
Direktur RS Haji Mina Medan dan Kepala SMF Kebidanan dan Penyakit
Kandungan RS Haji Mina Medan dr. Muslich Peranging-angin, SpOG
beserta seluruh staff, para Bidan dan seluruh paramedis yang telah
memberikan kesempatan dan sarana serta membantu saya untuk bekerja
selama bertugas di Rumah Sakit tersebut.
Direktur RS Sundari Medan dan Kepala SMF Kebidanan dan Penyakit
Kandungan RS Sundari Medan, dr. M Haidir, MHA, SpOG, dr. Ali Akbar
Hasibuan, Mked(OG), SpOG, dr. Juni Hardi Tarigan, SpOG dan Ibu
Hj.Sundari,Amkeb, beserta para Bidan dan seluruh paramedis yang telah
memberikan kesempatan dan sarana kepada saya untuk bekerja selama
bertugas di Rumah Sakit tersebut.
Ka. RUMKIT Tk. II KesDam II / Bukit Barisan ” Puteri Hijau” dan Kepala
SMF Kebidanan dan Penyakit Kandungan di RUMKIT Tk.II KesDam II / Bukit
Barisan beserta seluruh staff, para Bidan dan seluruh paramedis di RUMKIT
Tk.II KesDam II / Bukit Barisan ”Puteri Hijau” yang telah memberikan
kesempatan dan sarana serta bantuan kepada saya untuk bekerja selama
Kepada Direktur RSUD Gunung Tua beserta seluruh staf medis, paramedis
maupun non medis-paramedis. Terimakasih atas segala kesempatan,
sarana serta bantuan yang diberikan selama saya bertugas di RSUD
Gunung Tua.
Kepada Laboratorium Patologi Anatomi RSUP H Adam Malik Medan, dr
Jamaluddin, Sp.PA, dr. Sumondang Pardede, Sp.PA, beserta staf yang telah
membantu saya dalam menyelesaikan penelitian ini.
Kepada Almarhumah Ibu Hj. Asnawati Hasibuan; beserta Ibu Hj.
Sosmalahayati; Ibu Zubaedah; Ibu Sudarmawan; Ibu Bani; Rahmi, Amd;
Vina, Amd; Anggi, Amd; kak Asih, kak Dewi, dan seluruh pegawai di
lingkungan Departemen Obstetri dan Ginekologi RSUP H. Adam Malik
Medan dan RSUD dr. Pirngadi Medan, terima kasih atas bantuan dan
dukungannya.
Kepada seluruh Teman Sejawat PPDS, sejawat senior, seangkatan dan
junior yang tidak dapat saya sebutkan satu persatu, terima kasih atas
kebersamaan, dorongan semangat dan doa yang telah diberikan .
Seluruh Teman Sejawat Asisten Ahli dari departemen lain, Dokter Muda,
para Bidan, seluruh Paramedis, serta para pasien di Departemen Obstetri
dan RS Jejaring yang daripadanya saya banyak memperoleh pengetahuan
baru, terima kasih atas kerja sama dan saling pengertian yang baik, yang
diberikan kepada saya selama ini, sehingga saya dapat sampai pada akhir
program pendidikan ini.
Sembah sujud, hormat dan terima kasih yang tiada terhingga dari lubuk hati
sanubari yang paling dalam, saya sampaikan kepada kedua Orang Tua saya
yang saya cintai dan saya sayangi, Papa Alm. Andy Ronald Sinuhaji, BA dan
Mama Inganna br Sembiring, AmKeb, tiada kata terindah yang dapat saya
ucapkan melainkan rasa syukur dan terimakasih saya yang tidak terhingga
kepada Tuhan, karena telah menitipkan saya kepada orangtua yang telah
membesarkan, membimbing, mendoakan, serta mendidik saya dengan penuh
kasih sayang dari sejak saya kecil hingga saat ini, memberi contoh yang baik
dalam menjalani hidup ,serta memberikan motivasi dan semangat serta
dukungan kepada saya selama saya mengikuti pendidikan ini. Semoga Tuhan
Yesus melindungi dan memberkati kita semua.
Kepada kakak kandung saya Margaretha Emagda Bybyna Sinuhaji, AmKeb dan
keluarga. Terima kasih atas semua dorongan semangat serta doa yang diberikan
Kepada kekasih tersayang, Mega Tryanastasia Sembiring Milala, SKed
terimakasih atas bantuan doa dan dukungan kepada saya selama penyelesaian
tesis ini.
Kepada seluruh pihak yang saya sebutkan maupun tidak tersebut sebelumnya,
saya mohon maaf atas segala kekhilafan yang saya lakukan selama ini, baik
yang disadari maupun tidak. Semoga kita semua selalu menjadi orang yang
rendah hati, ikhlas, bersyukur, serta selalu dalam ampunan, kemudahan, dan
kasih sayang dari Tuhan Yang Maha Esa, Tuhan memberkati.
Semoga Tuhan Yang Maha Esa senantiasa memberikan berkah-Nya kepada kita
semua.
Medan, Maret 2015
i
1.1. Latar Belakang Penelitian...
1.2. Rumusan Masalah...
1.3. Hipotesa Penelitian...
1.4. Tujuan Penelitian ...
1.5. Manfaat Penelitian...
2.2.1 Inisiasi Apoptosis Jalur Intrinsik
(Mitokondria) ………
2.2.2 Inisiasi Apoptosis Jalur Ekstrinsik
(Inisiasi Reseptor Kematian)………..
2.2.3 Disregulasi Apoptosis ……….
2.3 Genetik dari Endometriosis...
2.4. Konsep Biokimia dari Endometriosis...
ii
2.6. Persamaan Molekular Endometriosis dan
Karsinoma Ovarium……...
3.6. Kriteria Inklusi dan Eksklusi Penelitian...
iii
BAB IV
BAB V
3.8. Cara Kerja dan Pengumpulan Data ………
3.9. Prosedur Pemeriksaan Imunohistokimia …………
3.9.1 Alat Penelitian ………..
3.9.2. Bahan Penelitian………...
3.9.3. Cara Kerja ……….
3.9.4. Instrumen Penelitian ………
3.10. Defenisi Operasional...
3.11. Rancangan Analisis...
3.12. Alur Penelitian ……….
HASIL PENELITIAN DAN PEMBAHASAN...
Tabel 4.1. Karakteristik Subjek Penelitian...
Tabel 4.2. Ekspresi p53 pada Karsinoma Ovarium tipe 1
iv
DAFTAR GAMBAR
Gambar 1. Representasi Skematik Struktur p53...… 7 Gambar 2. Protein p53 pada Persimpangan Jalur
Hubungan Kompleks ……… 8
Gambar 3 Hubungan Antara Inisiasi Apoptosis Jalur Ekstrinsik
Dengan Jalur Intrinsik ……….. 12 Gambar 4 Mekanisme Perubahan Apoptosis dan Proses
Karsinogenesis ………. 14
Gambar 5 Transfer dari Normal Tuba Epitelium ke Ovarium ……. 24 Gambar 6 Skematik untuk Perkembangan dari Kanker Serosum
Grade Rendah dan Tinggi ………. 25
Gambar 7 Perkembangan yang Diusulkan dari Endometrioid
Derajat Rendah dan Karsinoma Clear sel ……….. 25
v
DAFTAR TABEL
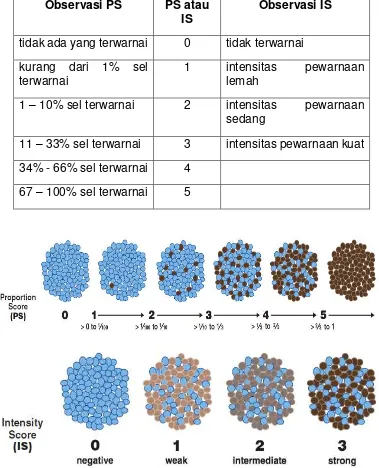
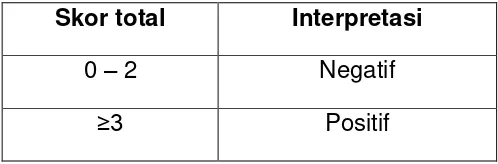
Tabel 1 Penilaian Proporsi skor dan
Intensitas Skor ……….………. 38
vi
DAFTAR SINGKATAN
BAX BCL-2 associated X Protein
TSG Tumor Supressor Gen
FasL Fas Ligand
DISC Death Inducing Signaling
SNPs Single Nucleotide Polymorphisms
VEGF Vascular Endothelial Growth Factor
BAK BCL-2 antagonist/killer-1
DNA Deoksiribo Nucleic Acid
FADD Fas-associated death domain
EKSPRESI P53 PADA ENDOMETRIOMA DIBANDINGKAN KARSINOMA OVARIUM TIPE 1
Sinuhaji AH, Aboet A, Edianto D Pasaribu HP, Kaban YB, Dina S
Departemen Obstetri dan Ginekologi Fakultas Kedokteran Universitas Sumatera Utara
RSUP H Adam Malik Medan
ABSTRAK
Latar belakang: Endometrioma adalah endometriosis yang berkembang pada ovarium. Walaupun endometriosis adalah lesi yang jinak, namun data menunjukkan bahwa endometriosis dapat menjadi lesi prekusor untuk terjadinya beberapa subtipe dari kanker ovarium, terutama kanker ovarium tipe 1. Hal ini disebabkan karena endometriosis memiliki kesamaan karakteristik biomolekular dengan kanker yang salah satunya adalah kemampuannya dalam bertahan (resistensi) terhadap proses apoptosis yang dapat dilihat dari overekspresi dari Bcl-2 ( anti-apoptosis), ekspresi yang rendah dari pro-apoptosis ( Bax ) dan inaktivasi dari p53 (pro-apoptosis). Hal ini yang menjadi alasan bagi peneliti untuk melihat apakah terdapat perbedaan ekspresi p53 pada jaringan endometrioma dibandingkan dengan karsinoma ovarium tipe 1.
Tujuan: Untuk mengetahui apakah ada perbedaan ekspresi protein p53 antara endometriosis (endometrioma) dan karsinoma ovarium tipe 1.
Metode: Penelitian ini adalah penelitian deskriptif observasional dengan pendekatan cross sectional. Subjek penelitian adalah blok parafin penderita endometrioma dan karsinoma ovarium tipe1 dengan jumlah sampel masing-masing sebanyak 25 sampel dan dilakukan pemeriksaan ekspresi secara imunohistokimia terhadap p53. Data yang terkumpul ditabulasi dan kemudian dianalisa dengan test Mann-Whitney.
Hasil: Endometrioma paling sering terjadi pada wanita usia < 40 tahun sebesar 15 sampel ( 60%) dan wanita nulipara 19 sampel (76%). Sedangkan karsinoma ovarium paling sering terjadi pada wanita usia > 40 tahun sebesar 18 sampel ( 72%) dan wanita multipara 11 sampel ( 44%). Ada perbedaan bermakna skor ekspresi p53 (mean + SD) antara endometrioma ( 0,36 + 0,86) dengan karsinoma ovarium tipe 1 ( 3,08 + 3,16) dengan nilai p = 0,0001.
Kesimpulan: Penelitian ini menunjukkan bahwa ada perbedaan bermakna ekspresi p53 pada endometrioma bila dibandingkan dengan karsinoma ovarium tipe 1..
EXPRESSION OF P53 IN ENDOMETRIOMA COMPARED WITH KARSINOMA OVARIUM TYPE 1
Sinuhaji AH, Aboet A, Edianto D Pasaribu HP, Kaban YB, Dina S
Obstetrics dan Gynaecology Departement Faculty of Medicine University of Sumatera Utara
Adam Malik General Hospital Medan
ABSTRACT
Introduction : Endometrioma is one type of endometriosis that located on the ovarium. Although endometriosis considered as a benign lesion, but it shown that endometriosis can be as a precursor lesion for occurrence of several subtypes of ovarian cancer, especially ovarian cancer type 1. This is due to biomolecular characteristics of the endometriosis in common with cancer, one of which is the ability in defense (resistance) against apoptosis which can be seen from the overexpression of Bcl-2 (anti-apoptotic), low expression of pro-apoptotic (Bax) and inactivation of p53 (pro-apoptotic). This is the reason for researchers to see whether there are difference in p53 expression in endometrioma tissue compared with ovarian carcinoma type 1.
Objective:To determine whether there are difference in p53 protein expression between endometriomas and ovarian carcinoma type 1.
Methods : This study is a descriptive observational study with cross sectional approach. The subjects were paraffin blocks from ovarian carcinoma type 1 and endometriomas patients from Adam Malik Hospital. The number of each group are 25 samples and the sample was examined by immunohistochemistry for p53 expression. The data was collected and tabulated and then analyzed with the Mann-Whitney test.
Result Endometrioma is most common in women with aged <40 years with 15 samples (60%), and nuliparous women with 19 samples (72%). While ovarian carcinoma type 1 is most common in women at aged > 40 years for 18 samples (72%) and multiparous women 11 samples (44%). The difference was significant for expresion of p53 ( mean+SD) between endometrioma (0.36 + 0.86) with ovarian carcinoma type 1 (3.08 + 3.16) with p value = 0.0001.
Conclusion This study shows that there was a significant difference of ekspresion of p53 between endometrioma and ovarian carcinoma type 1.
EKSPRESI P53 PADA ENDOMETRIOMA DIBANDINGKAN KARSINOMA OVARIUM TIPE 1
Sinuhaji AH, Aboet A, Edianto D Pasaribu HP, Kaban YB, Dina S
Departemen Obstetri dan Ginekologi Fakultas Kedokteran Universitas Sumatera Utara
RSUP H Adam Malik Medan
ABSTRAK
Latar belakang: Endometrioma adalah endometriosis yang berkembang pada ovarium. Walaupun endometriosis adalah lesi yang jinak, namun data menunjukkan bahwa endometriosis dapat menjadi lesi prekusor untuk terjadinya beberapa subtipe dari kanker ovarium, terutama kanker ovarium tipe 1. Hal ini disebabkan karena endometriosis memiliki kesamaan karakteristik biomolekular dengan kanker yang salah satunya adalah kemampuannya dalam bertahan (resistensi) terhadap proses apoptosis yang dapat dilihat dari overekspresi dari Bcl-2 ( anti-apoptosis), ekspresi yang rendah dari pro-apoptosis ( Bax ) dan inaktivasi dari p53 (pro-apoptosis). Hal ini yang menjadi alasan bagi peneliti untuk melihat apakah terdapat perbedaan ekspresi p53 pada jaringan endometrioma dibandingkan dengan karsinoma ovarium tipe 1.
Tujuan: Untuk mengetahui apakah ada perbedaan ekspresi protein p53 antara endometriosis (endometrioma) dan karsinoma ovarium tipe 1.
Metode: Penelitian ini adalah penelitian deskriptif observasional dengan pendekatan cross sectional. Subjek penelitian adalah blok parafin penderita endometrioma dan karsinoma ovarium tipe1 dengan jumlah sampel masing-masing sebanyak 25 sampel dan dilakukan pemeriksaan ekspresi secara imunohistokimia terhadap p53. Data yang terkumpul ditabulasi dan kemudian dianalisa dengan test Mann-Whitney.
Hasil: Endometrioma paling sering terjadi pada wanita usia < 40 tahun sebesar 15 sampel ( 60%) dan wanita nulipara 19 sampel (76%). Sedangkan karsinoma ovarium paling sering terjadi pada wanita usia > 40 tahun sebesar 18 sampel ( 72%) dan wanita multipara 11 sampel ( 44%). Ada perbedaan bermakna skor ekspresi p53 (mean + SD) antara endometrioma ( 0,36 + 0,86) dengan karsinoma ovarium tipe 1 ( 3,08 + 3,16) dengan nilai p = 0,0001.
Kesimpulan: Penelitian ini menunjukkan bahwa ada perbedaan bermakna ekspresi p53 pada endometrioma bila dibandingkan dengan karsinoma ovarium tipe 1..
EXPRESSION OF P53 IN ENDOMETRIOMA COMPARED WITH KARSINOMA OVARIUM TYPE 1
Sinuhaji AH, Aboet A, Edianto D Pasaribu HP, Kaban YB, Dina S
Obstetrics dan Gynaecology Departement Faculty of Medicine University of Sumatera Utara
Adam Malik General Hospital Medan
ABSTRACT
Introduction : Endometrioma is one type of endometriosis that located on the ovarium. Although endometriosis considered as a benign lesion, but it shown that endometriosis can be as a precursor lesion for occurrence of several subtypes of ovarian cancer, especially ovarian cancer type 1. This is due to biomolecular characteristics of the endometriosis in common with cancer, one of which is the ability in defense (resistance) against apoptosis which can be seen from the overexpression of Bcl-2 (anti-apoptotic), low expression of pro-apoptotic (Bax) and inactivation of p53 (pro-apoptotic). This is the reason for researchers to see whether there are difference in p53 expression in endometrioma tissue compared with ovarian carcinoma type 1.
Objective:To determine whether there are difference in p53 protein expression between endometriomas and ovarian carcinoma type 1.
Methods : This study is a descriptive observational study with cross sectional approach. The subjects were paraffin blocks from ovarian carcinoma type 1 and endometriomas patients from Adam Malik Hospital. The number of each group are 25 samples and the sample was examined by immunohistochemistry for p53 expression. The data was collected and tabulated and then analyzed with the Mann-Whitney test.
Result Endometrioma is most common in women with aged <40 years with 15 samples (60%), and nuliparous women with 19 samples (72%). While ovarian carcinoma type 1 is most common in women at aged > 40 years for 18 samples (72%) and multiparous women 11 samples (44%). The difference was significant for expresion of p53 ( mean+SD) between endometrioma (0.36 + 0.86) with ovarian carcinoma type 1 (3.08 + 3.16) with p value = 0.0001.
Conclusion This study shows that there was a significant difference of ekspresion of p53 between endometrioma and ovarian carcinoma type 1.
1
BAB I PENDAHULUAN
1.1 Latar Belakang Penelitian
Endometriosis adalah kelainan ginekologi dengan karakteristik
adanya implantasi jaringan endometrium di lokasi ektopik, misal:
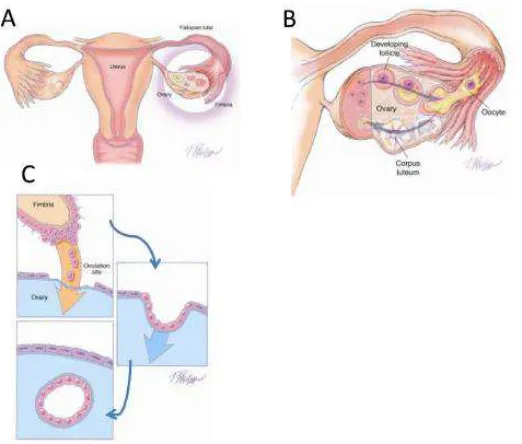
peritoneum panggul, ovarium dan saluran cerna.1 Banyak teori yang
menjelaskan patofisiologi dari endometriosis, namun teori Sampson2
mengenai retrograde menstruasi menjadi deskripsi teori dari endometriosis
yang paling banyak dipakai.
Prevalensi endometriosis belum diketahui secara pasti. Hal ini
disebabkan karena diagnosisnya memerlukan intervensi pembedahan dan
bergantung dari tampilan klinis yang sangat bervariasi.3 Namun prevalensi
dari endometriosis pada wanita usia reproduksi diperkirakan sekitar
6%-10%, dan sekitar 2%-5% pada wanita postmenopause.4
Walaupun endometriosis tidak dapat disebut sebagai kondisi
premalignant, namun secara epidemiologis, histopatologis dan data
molekular menunjukkan bahwa endometriosis dapat bertransformasi
menjadi proses keganasan dari beberapa subtipe kanker ovarium.5
Sebenarnya perubahan keganasan dari endometriosis pertama kali telah
diperkirakan oleh Sampson pada tahun 1925.
Pada penelitian oleh Oral dkk, 6 melakukan penelitian retrospektif
terhadap 160 keganasan dan 23 borderline tumor ovarium selama periode
2
kanker ovarium berkisar 7,65%. Banyak penelitian lain yang dilakukan
untuk menemukan hubungan antara kanker ovarium dengan
endometriosis. Berdasarkan data oleh Nishida, dkk 7 melakukan penelitian
terhadap 147 kasus kista endometriosis dan menemukan bahwa
perubahan keganasan dari endometriosis berkisar 7%.
Penelitian kohort retrospektif di Swedia terhadap 20.686 wanita yang
dirawat dikarenakan endometriosis, Brinton dkk melakukan follow up
selama 11,4 tahun dan menemukan peningkatan resiko untuk kanker
ovarium 1,9 (1,3-2,8).8 Melin dkk kemudian melaporkan bahwa adanya
peningkatan resiko relatif terhadap pasien dengan kista ovarium
endometriosis namun tidak pada pasien dengan adenomiosis 9. Dan
berdasarkan penelitian Deligdisch dkk,10 ditemukan adanya lesi
endometriosis pada 40 kasus dari 76 kasus kanker ovarium tipe 1.
Penelitian Bulun, Kitawaki, Wieser dan Arvaniti menunjukkan sifat
endometriosis dalam tingkat molekuler bahwa endometrioma cenderung
mengalami penurunan aktivitas penghambatan siklus sel, mampu menahan
apoptosis, memiliki sifat angiogenik, mampu menginvasi jaringan sekitar.
11,12,13 Sifat dari endometrioma tersebut diatas sesuai dengan ciri-ciri suatu
keganasan dikemukakan oleh Hannahan (2000)14 yang disebut dengan
Hallmark of Cancer. Hallmark dari kanker itu sendiri melibatkan enam
kemampuan biologis untuk perkembangan dari tumor pada manusia.
Hallmark tersebut merupakan prinsip dasar dari perkembangan keganasan.
Termasuk sinyal proliferasi yang berkelanjutan, kemampuan menghindari
3
kematian sel (resistensi terhadap suatu apoptosis), kemampuan untuk
bereplikasi tanpa henti, dapat mencetuskan angiogenesis dan kemampuan
invasi dan metastasis.
Resistensi terhadap suatu apoptosis ditunjukkan dengan adanya
overekspresi dari protein anti apoptosis (Bcl-2), ekspresi yang kurang dari
protein pro-apoptosis (Bcl-2 assosiated x protein, BAX) dan inaktivasi dari
gen p53 (p53 merupakan tumour suppressor gene (TSG) yang merupakan
pro apoptosis yang tidak aktif melalui proses mutasi.15 Jejas endometriotik
mempunyai kesamaan di dalam perkembangannya melalui strategi
menghindari diri dari apoptosis dengan (1) meningkatnya ekspresi Bcl-2,
(2) penurunan BAX.16 (3) Peningkatan Fas Ligand (FasL) yang terlarut dan
Interleukin (IL-8) pada cairan peritoneum yang memicu apoptosis dari
limfosit T yang memungkinkan sel endometriotik menghindar dari kematian
sel.15 (4) tidak aktifnya gen p53 akibat mengalami mutasi.18,19
Sehingga dapat disimpulkan gagalnya suatu apoptosis pada
endometriosis dan karsinoma ovarium dipengaruhi oleh 4 hal penting yaitu
Bcl-2(antiapoptosis), FasL, p53 (tumour suppresor gene) dan
BAX(pro-apoptosis). Dan dalam banyak penelitian disebutkan bahwa gangguan
pada salah satu regulator secara ototomatis mempengaruhi regulator yang
lain. Penelitian oleh Meresman dkk, mengamati bahwa pada sel
endometrium pada endometriosis memperlihatkan peningkatan ekspresi
faktor anti apoptosis dan penurunan ekspresi faktor pro apoptosis.16
Dari berbagai sifat molekular endometrioma di atas akan diambil satu
4
antara endometrioma dengan karsinoma ovarium yang dalam hal ini adalah
dengan melakukan evaluasi ekspresi dari pro-apoptosis p53 pada jaringan
endometrioma yang dibandingkan dengan kanker ovarium tipe 1.
1.2. Rumusan Masalah
Walaupun endometriosis adalah lesi yang jinak, namun secara
epidemiologis dan molekular telah menunjukkan bahwa endometriosis
dapat menjadi lesi prekusor untuk terjadinya beberapa subtipe dari kanker
ovarium. Hal ini disebabkan karena endometriosis memiliki kesamaan
karakteristik biomolekular dengan kanker yang salah satunya adalah
kemampuannya dalam bertahan terhadap proses apoptosis. Resistensi
apoptosis diperlihatkan dengan adanya overekspresi dari Bcl-2 (
anti-apoptosis), ekspresi yang rendah dari pro-apoptosis ( Bax ) dan inaktivasi
dari p53 (pro-apoptosis). Oleh karena itu dirumuskan masalah apakah
terdapat perbedaan ekspresi p53 pada jaringan endometrioma
dibandingkan dengan karsinoma ovarium tipe 1?
1.3. Hipotesa Penelitian
Hipotesa penelitian ini adalah ada perbedaan ekspresi p53 pada
5
1.4. Tujuan Penelitian
Untuk mengetahui perbedaan ekspresi protein p53 antara
endometrioma dan karsinoma ovarium tipe 1.
1.5. Manfaat Penelitian 1.5.1. Manfaat Teoritis
Dapat diketahui bagaimana ekspresi protein P53 pada jaringan
endometrioma dengan karsinoma ovarium tipe 1.
1.5.2. Manfaat Aplikatif
Mengubah pandangan terhadap endometrioma yang memiliki ciri-ciri
keganasan yang sama dengan karsinoma ovarium tipe 1 sehingga
memberikan landasan penanganan yang lebih spesifik pada
6
BAB 2
TINJAUAN PUSTAKA
2.1. Protein p53
Protein p53 pertama kali diidentifikasi pada tahun 1979 sebagai
transformation-related protein dan protein yang terakumulasi pada inti sel
kanker serta berikatan kuat dengan antigen T simian virus 40 (SV40). Akan
tetapi, sepuluh tahun kemudian, para peneliti mendapatkan bahwa ternyata
protein tersebut merupakan mutasi dari bentuk awal p53/wild-type p53 (wt
p53) dan sifat onkogenik p53 sebenarnya merupakan hasil dari mutasi p53
(Bai & Zhu, 2006). Gen p53 merupakan tumor suppressor gene yang
multifungsi dan sering mengalami alterasi pada kanker ovarium dan jenis
kanker lainnya. Pada kondisi normal, p53 berinteraksi dengan berbagai
jenis protein yang terlibat dalam regulasi transkripsional, repair DNA, siklus
sel, apoptosis, dan degradasi protein yang dimediasi oleh proteosom 22
Dalam kondisi normal, jaringan p53 dalam kondisi tidak aktif,
biasanya diaktifkan oleh semacam stress seluler yang dapat mengubah
siklus pertumbuhan sel normal atau menginduksi mutasi genom yang
kemudian mengarah pada tranformasi onkogenik. Protein p53 yang aktif
dapat menghentikan siklus sel atau menghidupkan jalur apoptosis dan
memaksa sel-sel rusak dan mengandung mutasi melakukan bunuh diri
sehingga mencegah perbanyakan dan pertumbuhan selular yang
abnormal. Oleh karena itu, protein p53, sebagai guardian of genom, adalah
7
gen ini menjadi paling sering bermutasi dalam penyakit kanker pada
manusia23 .
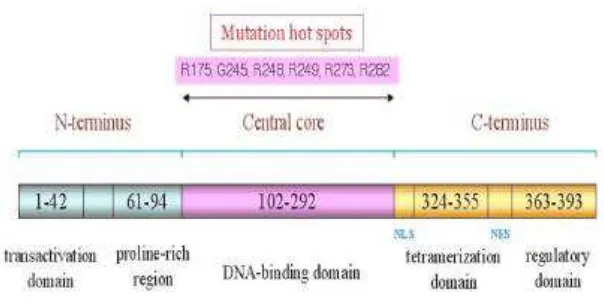
2.1.1. Struktur protein p53
Gen p53 terletak pada bagian lengan pendek dari kromosom 17
(17p13.1), merupakan suatu nuklear phospoprotein yang memiliki berat
molekul sebesar 53 kilo Dalton (kDa). Gen p53 ini dikode oleh 20 kilobasa
(kb) yang terdiri dari 11 ekson dan 10 29 intron. Gen p53 ini termasuk di
dalam kelompok gen pelindung sel, yang memiliki dua anggota lainnya
yaitu, p63 dan p73. Protein p53wild type (wt p53), mengandung sebanyak
393 asam amino dan terdiri dari tiga domain fungsional yaitu N-terminal
activation domain, DNA binding domain dan C-terminal tetramerization
domain (Gambar 1). Selain itu, terdapat sebuah daerah domain inti sentral
atau central core, yaitu pada residu 102 sampai 292 dan daerah domain
C-terminal, yaitu pada residu 324 sampai 393 22.
8
2.1.2. Peran protein p53
Protein p53 memiliki aktivitas biokimia sebagai faktor transkripsi dan
peran biologi sebagai tumor suppressor yang sangat kuat. Sebagai faktor
transkripsi multitarget, p53 mengontrol berbagai jenis gen dengan fungsi
yang berbeda-beda. Sebagai penekan tumor, p53 sangat penting untuk
mencegah proliferasi sel yang menyimpang serta mempertahankan
integritas genom akibat stress genotoksik10.
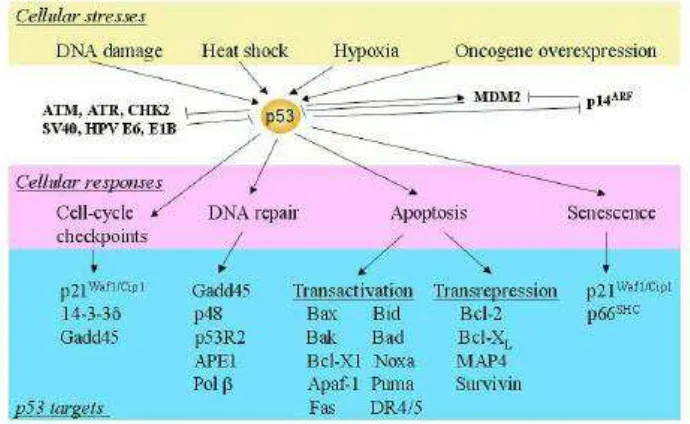
Gambar 2. Protein p53 pada Persimpangan Jalur Hubungan Kompleks Respon Sel terhadap Stress 22
Sebagai penekan tumor,p53 sangat penting dalam mencegah
proliferasi yang salah dari sel dan menjaga integritas gen yang diakibatkan
oleh stress genotoksik. Dengan adanya stimulus yang beragam yang dapat
berasal dari luar dan dalam sel, seperti kerusakan DNA (disebabkan radiasi
9
panas, hypoksia, kemoterapi , akan mengaktifkan wt p53 yang akan
berfungsi sebagai pengatur protein yang memicu perubahan respon
biologis sel. Aktivasi p53 tersebut akan menyebabkan pengaktifan gen
target p53. Sebagai contoh, sebagai respon kerusakan DNA akan
menyebabkan putusnya rantai ganda DNA , ATM (ataxia-telangiectasia
mutated) protein kinase yang akan mengaktifkan Chk2 kinase. ATM dan
Chk2 bersama-sama akan memfosforilasi p53 yang menyebabkan
berhentinya siklus sel atau apoptosis. 22
Pada kondisi yang normal, wt p53 ada pada kadar yang rendah
dengan bentuk laten inaktif. Selama perlembangan sel, kadar rendah dari
wt p53 ini diatur secara cermat, dan half-lifenya hanya terbatas pada
hitungan menit. Namun dengan adanya stress atau agen yang merusak
DNA, half-life tersebut menjadi diperpanjang menjadi hitungan jam.
Peningkatan kadar dari protein p53 diatur dengan perpanjangan dari
half-life tersebut, dan bergantung kepada stimulus di dalam dan di luar sel. 22
2.2 Apoptosis
Sebagai penjaga sel, salah satu tugas dari p53 adalah untuk
mengawasi stress dari sel dan menginduksi apoptosis. Pada jaringan yang
mengalami stress dan kerusakan, p53 akan menginisiasi apoptosis yang
akan menghancurkan sel yang rusak tersebut. 22
Produk hasil gen apoptosis yang diinduksi oleh p53 termasuk
didalamnya adalah Bax (Bcl-2 associated protein), DR5/KILLER (death
p53-10
inducible gen), Puma (p53-upregulated modulator of apoptosis), Noxa,
PIDD (p53-induced protein with death domain), PERP (p53 apoptotis
effector related to PMP-22),Apaf-1 (apoptotic protease-activating factor-1),
Scotin, p53AIP1 (p53-regulated apoptosis-inducing protein 1), dll. 22
Proses apoptosis dapat dibagi menjadi tahap inisiasi, dimana
terdapat beberapa caspases yang menjadi katalis aktif, serta tahap
eksekusi atau pelaksanaan, dimana caspases lainnya memicu degradasi
komponen seluler. Inisiasi apoptosis terjadi oleh karena sinyal dari dua jalur
yang berbeda. Jalur intrinsik atau mitokondria dan ekstrinsik atau kematian
reseptor. Jalur ini diinduksi oleh stimulus yang berbeda dan melibatkan set
protein yang berbeda, walaupun terdapat beberapa persilangan jalur
diantaranya. Kedua jalur bertemu untuk mengaktifkan caspases, yang
merupakan mediator sebenarnya kematian sel. 24
2.2.1 Inisiasi apoptosis jalur intrinsik (mitokondria)
Sesuai dengan namanya, jalur intrinsik berlangsung di dalam sel.
Jalur apoptosis intrinsik akan menghasilkan peningkatan permeabilitas
mitokondria dan pelepasan dari molekul pro-apoptosis (death inducers) ke
dalam sitoplasma . Mitokondria mengandung protein seperti sitokrom c
yang penting bagi kehidupan, tetapi bila beberapa protein yang serupa
terlepas ke dalam sitoplasma (merupakan indikasi bahwa sel tersebut tidak
sehat), akan menginisiasi program “bunuh diri” dari apoptosis. Pelepasan
protein mitokondria ini dikontrol secara seimbang melalui anggota keluarga
11
pertama protein pro-apoptosis (Bax, Bak, Bad, Bcl-X, Bid, Bik, Bim, dan Hrk
) dan uang kedua adalah anti-apoptosis ( Bcl-2, Bcl-xl, Bcl-W, Bcl-1 dan
Mcl-1). 24,25
Ketika protein anti-apoptosis mengatur apoptosis dengan cara
menghambat pengeluaran sitokrom, sedangkan protein pro-apoptosis
melakukan yang sebaliknya. Keseimbangan antara pro dan anti apoptosis
akan menentukan apakah sel tersebut akan mati atau tidak. Faktor
apoptosis lain yang dilepaskan oleh mitokondria ke sitoplasma yaitu :
apoptosis inducing factor (AIF),-derived second mitochondria
Bindingderived activator of caspase (Smac), direct IAP binding protein with
low pl (DIABLO) dan Omi/high temperature requirement protein A (HtrA2).
Sitoplasma melepaskan sitokrom c akan mengaktifkan caspase 3 melalui
pembentukan kompleks protein yang disebut dengan apoptosome (terdiri
dari sitokrom c, Apaf-1 dan caspase 9. Dilain pihak, Smac/DIABLO atau
Omi/HtrA2 ) akan menyebabkan pengaktifan caspase dngan melekat pada
protein penghambat apoptosis (IAPs) yang akan merusak interaksi IAPs
dengan caspase 3 atau 9. 24,25
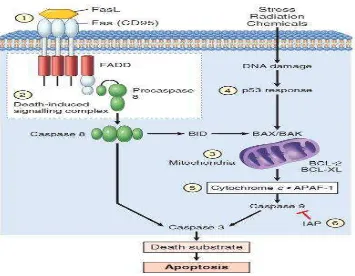
2.2.2 Inisiasi apoptosis jalur ekstrinsik (inisiasi reseptor kematian)24 Jalur ini diawali melalui keterlibatan ligan kematian yang akan
berikatan dengan reseptor kematian. Walaupun beberapa reseptor
kematian telah banyak diketahui, namun reseptor kematian yang paling
12
dengan Fas (CD 95) dan ligand mereka yang disebut dengan TNF dan Fas
ligand (FasL).
Dengan berikatannya ligan kematian dengan reseptornya akan
membentuk suatu kompleks yang disebut dengan death inducing signaling
complex (DISC) yang akan mengaktifkan pro-caspase 8. Caspase ini
merupakan suatu kaspase pencetus terhadap apoptosis. 24,25
Alur apoptosis ini dapat dihambat oleh protein yang dinamakan FLIP,
yang dapat mengikat pro-caspase-8. Beberapa virus dan sel normal
memproduksi FLIP dan menggunakan inhibitor ini untuk melindungi dirinya
dari apoptosis yang dimediasi oleh Fas. 25
13
2.2.3 Disregulasi Apoptosis,24,25,26
Apoptosis dan gen yang mengontrolnya mepunyai efek yang besar
pada fenotip keganasan. Gangguan regulasi pada program apoptosis akan
menyebabkan mortalitas sel. Mutasi onkogenik yang apoptosis
mempengaruhi inisiasi tumor, progresifitas tumor dan metastase. Kanker
merupakan hasil dari perubahan genetik dimana sel normal berubah
menjadi ganas, dimana penghentian kematian sel sementara merupakan
salah satu perubahan penting yang menyebabkan suatu transformasi
kearah keganasan.
Pada awal 1970 Kerr dkk telah mengaitkan apoptosis untuk
menghapus sel yang berpotensi ganas , sel yang mengalami hiperplasi dan
perkembangan tumor. Oleh karena itu, pengurangan peran apoptosis dan
resistensinya memainkan peran penting dalam karsinogenesis. Ada benyak
cara sel menjadi tumor atau mengalami keganasan melalui proses
pengurangan apoptosis dan rsistensi apoptosis. Umumnya, mekanisme
perubahan apoptosis yang bisa meyebabkan kanker atau tumor dapat
dibagi atas 3 bagian besar, yaitu
1. Gangguan keseimbangan protein proapotosis dan protein
antiapoptosis
2. Berkurangnya fungsi caspase
14
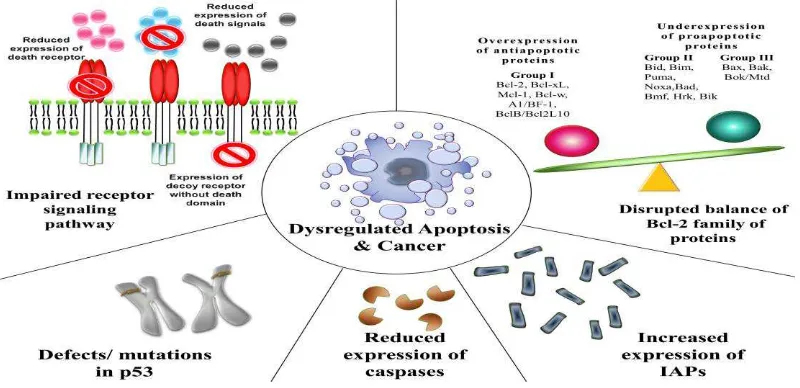
Gambar 4 Mekanisme perubahan Apoptosis dan proses Karsinogenesis25
Pada proses apoptosis dapat terjadi kegagalan pada jalur , yang
akan menyebabkan terjadinya kanker. Kegagalan ini lebih sering terjadi
pada jalur intrinsik dibandingkan jalur ekstrinsik, karena jalur ekstrinsik ini
lebih sensitif dan paling sering disebabkan oleh mutasi dari gen p53. Gen
p53 ini merupakan tumor supresor gen yang terakumulasi bila DNA
mengalami kerusakan. Fungsi dari p53 ini yaitu mencegah replikasi sel
pada sel yang rusak secara genetik melalui penghentian siklus sel pada
fase G1 atau interface, sehingga sel mempunyai waktu untuk repair. Selain
itu gen ini juga berfungsi untuk mencetuskan apoptosis bila kerusakan sel
cukup luas dan terjadi kegagalan repair.
Bila terjadi mutasi pada gen p53 dapat mengakibatkan disregulasi
gen ini sehingga terjadi kegagalan apoptosis dan sel yang rusak terus
15
Faktor lain yang berperan pada karsinogenesis adalah
keseimbangan antara proapotosis dan anti apoptosis dari kelompok Bcl2.
Pada sel tumor, mutasi dari gen Bcl2 dapat meyebabkan peningkatan
ekspresi yang dapat menekan fungsi normal dari protein proapotosis,
seperti Bax dan Bak. Jika terjadi mutasi pada gen Bax dan Bak dapat
meyebabkan penurunan regulasi, sehingga sel kehilangan kemampuan
untuk regulasi apoptosis yang dapat menimbulkan kanker.
2.3. Genetik dari Endometriosis
Komponen yang dimiliki oleh endometriosis telah banyak diketahui
walaupun gen spesifik yang berkaitan dengan endometriosis masih banyak
diteliti. Analisa terhadap gen yang berhubungan dengan 1100 keluarga
dengan dua atau lebih keterlibatan dari saudara kandung telah dilakukan
dan didapatkan adanya lokus pada kromosom 10q26 dan 7-13-15.24
Penelitian terhadap berbagai hubungan antara gene dengan proses yang
terlibat pada endometriosis termasuk didalamnya sinyal steroid, matrix
degradasi, inflamasi dan detoksifikasi seperti yang dilaporkan, telah
dilakukan review terhadap penelitian tersebut. Untuk mendapatkan
hubungan gen dengan penyakit ini, penelitian kohort terhadap wanita
dengan dan tanpa endometriosis adalah memiliki genotip SNPs (Single
Nucleotide Polymoprhisms).27 Penelitian terbaru terhadap 1900 wanita
dengan endometriosis dengan memakai kontrol sebanyak 5300 wanita
16
pada kromosom 9p21 dan gen WNT4 pada kromosom 1p36 pada
peritoneum endometriosis.28
Pada level transkripsi gen, ditemukan adanya perbedaan ekspresi
gen pada endometrioum ektopik pada wanita dengan dan tanpa
endometriosis perbedaan tersebut memperlihatkan adanya abnormalitas
yang diturunkan ataupun yang didapat pada endometrium yang
memberikan ketahanan hidup yang berbeda dan implantasi terhadap
pembentukan dari lesi endometriosis. 1
2.4. Konsep Biokimia dari endometriosis
Konsep yang ada mengenai endometriosis adalah kelainan yang
berkaitan dengan esterogen. Pada saat ini, endometriosis memiliki
hubungan dengan proses inflamasi, penurunan fungsi progesteron pada
level endometrium dan neuroangiogenesis. 1
2.4.1. Inflamasi
Endometriosis sangat menarik dan dianggap sebagai kondisi yang
merupakan inflamasi kronik. Lingkungan peritonum dari endometriosis
mempunyai karakterisik dengan adanya peningkatan makrofag yang aktif
dan peningkatan kadar sitokin inflamasi, kemokin, faktor pertumbuhan dan
prostaglandin. Analisa terhadap endometrium eutopik dan ektopik
menunjukkan adanya peningkatan yang tinggi terhadap phospoliphase A2
17
Faktor nuklear kappaB (NF-kB) ternyata memiliki peranan yang
penting dalam memediasi kunci biokimia dari endometriosis. faktor tersebut
diaktivasi oleh proinflamasi sitokin dan stres oksidatif dan meningkat pada
tipe lesi endometriosis merah. Sebagai faktor transkripsi, pengaktifan dari
(NF-kB) akan meningkatkan ekspresi dari beberapa gen yang terlibat dalam
inflamasi, termasuk didalamnya interleukin 1 (IL-1), IL-6, IL-8, dan
sikooksigenase 2. Pada endometriosis ditemukan adanya aktifasi abnormal
terhadap (NF-kB). 1,29,30
Sebagai tambahan terhadap kaskade dari inflamasi, (NF-kB)
mengatur gen yang terkait dengan antiapoptosis, invasi jaringan, proliferasi
sel dan angiogenesis yang merupakan langkah penting dalam patogenesis
dari endometriosis.1
2.4.2. Penurunan Fungsi Progesteron
Sebagai tambahan dari adanya ketergantungan dengan esterogen,
peningkatan temuan terhadap adanya penurunan dari fungsi progesteron
pada endometrium pada patofisiologi dari endometrium telah banyak
ditemukan.1 Penelitian terhadap ekspresi gen menunjukkan adanya
penurunan respon endometrium terhadap progesteron pada fase sekretori
pada endometriosis dibandingkan dengan kelompok kontrol normal.
Dengan adanya efek dari anti inflamasi oleh progesteron, sehingga jika
terjadi penurunan fungsinya pada endometrium dapat menghasilkan
peningkatan proinflamasi pada uterus yang menyebabkan uterus tidak
18
2.4.3.Neuroangiogenesis
Perkembangan dari vaskularisasi mempunyai peranan yang penting
juga pada perkembangan implantasi endometriosis pada rongga
peritoneum. Lesi peritoneum, terutama tipe vesikular merah,
memperlihatkan adanya tampilan kongesti dari neovaskular pada
laparoskopi.1 Beberapa faktor angiogenesis seperti faktor pertumbuhan
(VEGF), meningkat pada cairan peritoneum wanita endometriosis.
penurunan lesi dari endometriosis dengan menggunakan pengobatan
dengan antiangiostatik pada tikus juga menunjukkan adanya peranan
angiogenesis pada perkembangan penyakit ini. Yang paling penting adalah
angiogenesis dan pertumbuhan syaraf adalah kejadian yang saling
berkaitan dan saling terencana pada penyakit ini yang disebut dengan
neuroangiogenesis.32
Dasar dari pemahaman terhadap patofisiologi rasa sakit yang
berhubungan dengan endometriosis adalah dengan adanya penelitian
terhadap inervasi lesi endometriosis pada tikus. Penelitian tersebut
menunjukkan adanya peningkatan 14 kali lipat terhadap densitas syaraf
pada lesi endometriosis bila dibandingkan dengan kelompok kontrol. Dan
tingkat keparahan rasa nyeri sangat berhubungan dengan adanya
19
2.5. Kanker Epitel Ovarium
2.5.1 Asal dan Patogenesis dari Kanker Epitel Ovarium
Kanker ovarium merupakan kanker ginekologi yang sangat letal.
Pendekatan diagnostik dan pengobatan kanker ovarium ini masih belum
sempurna karena asal dan patogenesis dari kanker epitel ovarium masih
belum diketahui dengan jelas. Walaupun telah dilakukan berbagai
penelitian, namun hasil yang didapatkan belum memuaskan. Penelitian
mengatakan bahwa kanker epitel ovarium bukan merupakan penyakit
tunggal namun terdiri dari kelompok tumor yang berbeda berdasarkan
morfologi dan genetik molekular. Satu kelompok tumor disebut dengan tipe
1, serous grade rendah, endometrioid grade rendah, clear sel, musinosum
dan kanker transisional (Brenner). Tumor ini biasanya indolen, terbatas
pada ovarium dan genetiknya stabil. Kelompok kedua disebut dengan tipe
2, yang lebih agresif, berkembang cepat dan biasanya tampil dengan
grading yang lebih tinggi. Termasuk didalamnya kanker ovarium serosum
dengan grade tinggi, karsinoma undifferensiasi, karsinosarkoma. Pada 80
kasus memiliki mutasi gen TP53. Penelitian juga menunjukkan bahwa yang
dulunya anggapan bahwa kanker ovarim berasal dari primer ovarium
ternyata berasal dari organ pelvik lain dan melibatkan ovarium secara
sekunder. Tumor serosum berasal dari implantasi epitelium tuba falopi.
Endometrioid dan clear sel telah banyak dihubungkan dengan
endometriosis, yang dianggap sebagai prekusor tumor ini. Data juga
menunjukkan bahwa tumor musinosum dan Brenner berasal dari tipe epitel
20
proses metaplasia. Dengan adanya temuan ini, konsep baru terhadap
pendekatan diagnosa, skrining, pengobatan bahkan pencegahan memiliki
peranan yang besar terhadap penyakit ini. 34
2.5.2. Heterogenisitas Morfologi dan Molekular dari Kanker Epitel Ovarium
Salah satu masalah besar dalam memahami patogenisitas dari
kanker ovarium adalah adanya penyakit yang heterogen yang berhubungan
dengan tipe yang berbeda dari sifat dan klinikopatologi penyakit ini. Telah
diketahui bahwa tipe dari kanker ovarium dibagi menjadi tipe 1 dan tipe 2.
Sebagai kelompok tipe 1, merupakan tumor dengan genetik yang stabil
dibandingkan dengan tipe 2 yang menunjukkan adanya mutasi yang
spesifik. Mutasi dari KRAS, BRAF dan ERBB2 terjadi sekitar duapertiga dari
karsinoma grade rendah dimana mutasi TP53 jarang terjadi pada tumor ini.
Karsinoma grade rendah memiliki hubungan sinyal Wnt termasuk di
dalamnya mutasi dari somatik CTNNB1 (enkode B-catenin), PTEN dan
PIK3CA. Karsinoma musinosum memiliki mutasi KRAS lebih dari 50%
kasus. Karsinoma clear sel sangat unik dengan persentase yang tinggi dari
mutasi PIK3CA. Karsinoma serous grade tinggi sebagai prototipe tipe 2,
mempunyai karakteristik mutasi TP53 (> 80% kasus) dan CCNE1 (enkoding
dari cyclin E1) namun jarang terjadi mutasi dari KRAS,BRAF, PTEN,
CTNNB1 dan PIK3CA. Dengan adanya temuan ini, dapat disimpulkan
bahwa tipe yang berbeda dari kanker ovarium akan memiliki perbedaan
21
2.5.3. Asal Sel Kanker Epitel Ovarium bukan dari Ovarium
Asal sel dari kanker ovarium dan mekanisme perkembangannya
telah lama diperdebatkan. Pandangan tradisional karsinogenesis ovarium
yaitu perbedaan jenis tumor berasal dari permukaan epitel ovarium
(mesotelium) dan terjadi perubahan metastasis yang mengarah kepada
perkembangan berbagai sel yang berbeda (serous, endometrioid, clear sel,
musinosum dan sel transisional (brenner) yang secara morfologis
menyerupai epitel dari tuba falopi, endometrium, saluran cerna atau
endoserviks dan kandung kencing 36. Ovarium yang normal, bagaimanapun
juga tidak memiliki kesamaan dengan tumor ini. Serviks, endometrium dan
tuba falopi berasal dari duktus mullerian sedangkan ovarium berasal dari
epitelium mesodermal pada sinus urogenital yang berbeda. Oleh karena itu,
ada teori yang mengatakan tumor dengan fenotip mullerian (serous,
endometrioid dan sel clear) berasal dari jaringan mullerian. 36 Tipe mullerian
tersebut ( epitel columnar, biasanya bersilia) berasal dari paratuba dan
paraovarium yang biasa disebut dengan “sistem sekunder Mullerian”37.
Ketika tumor semakin membesar, tumor itu menekan ovarium dan
menyumbat ovarium sehingga dapat terlihat kesannya berasal dari
ovarium. Dan teori yang lebih baru mengatakan bahwa kebanyakan kanker
ovarium terutama serous dengan grade tinggi berasal dari tuba falopi yang
menyebar ke ovarium. Pandangan yang berbeda ini mendorong berbagai
penelitian untuk dapat menjelaskan teori yang paling dapat dianggap sesuai
22
Teori yang mengatakan bahwa asal dari kanker ovarium adalah
permukaan epitelium (mesotelium) memiliki beberapa keterbatasan.
Secara histologis, lapisan mesotelium yang melapisi ovarium tidak memiliki
kesamaan terhadap tipe serosum, endometrioid, musinosum, sel clear atau
karsinoma transisional (Brenner). Untuk mendukung teori ini, dianggap
bahwa mesotelium yang ada di permukaan ovarium masuk ke stroma yang
disebut bentuk “kista inklusi kortikal”. Kista ini di bawah pengaruh faktor
lokal, terutama hormon akan mengalami perubahan metaplasia , yang akan
berubah menjadi epitelium tipe Mullerian. Lalu akan berubah menjadi
karsinoma dengan tipe yang berbeda ( serosum, endometrioid dan clear
sel). Walaupun kista inklusi kortikal dilapisi oleh silia ( tipe epitelium
Mullerian) sering dilihat pada kortex ovarium, namun transisi dari kista ini
berubah menjadi kanker belum pernah dilaporkan. Lebih lagi kista inklusi
kortikal yang dilapisi epitel Mullerian untuk berubah menjadi karsinoma
musinosum sangat jarang.35
Keterbatasan kedua dari teori Mullerian adalah lesi prekusor yang
sama dengan kanker serosum, endometrioid dan sel clear sangat jarang,
dan apabila pernah dilaporkan, itupun berasal dari kista paraovarian dan
paratubal. Lebih lagi, tampilan dari berbagai tumor musinous lebih kepada
tipe intestinal dibandingkan dengan tipe endoservikal dan tidak memenuhi
syarart sebagai tumor tipe Mullerian. Kejadian yang lebih tegas juga
ditunjukkan bahwa kanker ovarium primer, khususnya serous, endometrioid
dan karsinoma clear sel, berasal dari tuba falopi dan endometrium, tidak
23
karsinoma tuba dan displasia memiliki kesamaan dengan kanker ovarium
grade tinggi, pada wanita dengan genetik predisposisi kanker ovarium. 38
Implantasi langsung dari epitel tuba pada ovarium membentuk kista
inklusi, yang akan menjadi asal dari kanker ovarium serosum, walaupun
belum dapat didemonstrasikan adalah teori alternative daripada metaplasia
dari mesotelium pada ovarium. Implantasi epitel tuba dari fimbria pada saat
ovulasi ketika permukaan epitel ovarium rusak dapat menjelaskan
terjadinya dari grade rendah dan tinggi kanker ovarium serosum. Pada
kasus karsinoma grade rendah, perkembangan proses berjalan lambat dari
kistaadeoma serous kemudian menjadi tumor serous borderline setelah
mutasi KRAS atau BRAF, dimana terjadi perkembangan cepat dari kanker
serosum grade tinggi.Juga telah diketahui bahwa kedua morfologi dan
penelitian genetik molekular dari grade rendah endometrioid dan kanker
clear sel berkembang dari kista endometriosis (endometrioma) yang
biasanya berhubungan dengan implamtasi endometriosis pada berbagai
tempat. Walaupun asal yang pasti dari endometriosis belum sepenuhnya
diketahui, dan teori sebelumnya mengenai kanker ovarium sangat susah
untuk diteliti. Jika retrograde menstruasi adalah yang sering terjadi pada
endometriosis, menjadi benar bahwa endometrioid dan tumor clear sel
berkembang dari endometriosis (turunan Mullerian) yang berimplantasi ke
ovarium sehingga keterlibatan ovarium adalah sekunder. 34
Pengamatan lanjutan juga menunjukkan bahwa endometrium
eutopik dari penderita endometriosis memperlihatkan kelainan faktor
24
perubahan ini menyebabkan implantasi dari jaringan endometrium,
ketahanan hidup sel dan invasi pada ovarium dan permukaan peritoneum.36
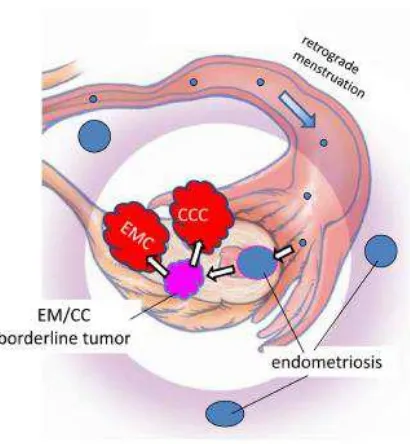
Hipotesis yang mengatakan asal dari endometrioid dan kanker clear sel
berkembang dari jaringan endometrium yang berimplantasi pada ovarium
didukung dengan adanya kejadian efek perlindungan dengan ligasi tuba
yang hanya ada pada endometrioid dan karsinoma clear sel pada ovarium.
39
Gambar 5. Transfer dari normal tuba epitelium ke ovarium. A. Hubungan anatomi dari tuba falopi dengan ovarium pada saat
ovulasi. B. Ovulasi. C. Sel epitelium tuba dari fimbria jatuh dan berimplantasi pada permukaan yang gundul yang membentuk kista
25
Gambar 6. skematik untuk perkembangan dari kanker serosum grade rendah dan grade tinggi.36
26
2.6. Persamaan Molekuler endometriosis dan karsinoma ovarium
Molekuler dan ciri genetik dari hubungan endometriosis dengan
karakteristik kanker di usulkan oelh Hanahan dan Weinberg (2000). Dikenal
dengan The Hallmarks of Cancer, Yaitu (1) Memiliki kemampuan yang
cukup dalam sinyal pertumbuhan , (2) Tidak peka terhadap sinyal anti
proliferasi, (3) Resisten terhadap apoptosis, (4) Potensi replikasi tanpa
batas, (5) Sokongan dari angiogenesis, (6) Kemampuan Invasi dan
metastase ke jaringan (7) Memiliki instabilitas genetik.15
2.6.1. Insufisiensi dalam sinyal pertumbuhan32,40,41
Sama seperti kanker uterus dan payudara, endometriosis memiliki
sifat yang hamper sama dalam hal ketergantungan terhadap esterogen.
Endometriosis secara spesifik tergantung terhadap esterogen didasarkan
pada sinyal : (1) Peningkatan produksi lokal estrogen melalui peningkatan
ekspresi dari aromatse p450 tetapi terjadi kekurangan ekspresi dari 17 β-
hydroxysteroid dehydrogenase type 2 (yang menyebabkan inaktifasi dari
estradiol yang berpoten menjadi estrone yang kurang poten), (2)
Peningkatan respon pada estrogen. Peningkatan reseptor estrogen (ER-α)
ekspresi pada jejas yang aktif (Red lesion) dibanding dengan yang tidak
aktif (Black Lession) endometriosis (3) Mewarisi polimorfisme genetik pada
estrogen dan reseptor progesterone (PRs) merupakan predisposisi dari
endometriosis, (4) Mewarisi polimorfisme genetik pada metabolisme enzim
(CYP1A1,CYP19 dan GSTMI) yang merupakan predisposisi dari
27
2.6.2. Tidak peka terhadap sinyal anti proliferasi32
Pembelahan sel bergantung kepada aktivasi cyclin (mis : D1 cyclin)
yang berikatan dengan cyclin yang bergantung pada kinase (cdk) untuk
menginduksi siklus sel ke fase S dan kemudian menginisiasi mitosis.
Dengan adanya aktifitas cdk yang tidak terkontrol pada sel kanker, fungsi
mereka sangat diregulasi dengan ketat oleh pemghambat cdk (mis : p21
dan p27 Cip/Kip protein). Sebagai contoh : peningkatan ekspresi dari cyclin
D1 dan cdk terjadi pada kanker payudara dan berhubungan dengan hasil
yang jelek. 15
Pada tingkat sel terdapat perbedaan ekspresi dari protein p27 Kip
(cdk inhibitor) antara jejas endometriotik yang aktif dan yang tidak aktif,
bersamaan dengan peningkatan ekspresi p27 antara endometrioma dan
karsinoma ovarium data tersebut menyimpulkan kenaikan aktivitas cdk
melalui hambatan aktivitas induksi siklus sel, yang pada umumnya tidak
seimbang pada kanker. Hal ini menunjukkan peningkatan aktivitas CDK
melalui penghambatan siklus sel.42
2.6.3. Resisten terhadap apoptosis
Keganasan pada umumnya menunjukkan ekspresi berlebihan dari
antiapoptosis (Bcl-2), dan ekspresi rendah dari proapotosis BAX, gen p53
(p53 adalah tumor supresor gen (TSG) sedangkan protein (TP53) adalah
proapotosis melalui mutasi menjadi tidak aktif. Pada jejas endometriotik
mempunyai strategi untuk menghindar dari apoptosis melalui (1)
28
matrix metalloproteinase (MMPs),43 (3) peningkatan Fas ligand (Fasl) dan
interleukin 8 (IL-8) di dalam zalir peritoneal endometrioma (peningkatan
Fasl dan IL-8) menginduksi apoptosis dari T limfosit dan kemungkinan
endometrioma menghindar dari kematian 41 (4) sel germinal dan sel somatik
yang didapat menyebabkan tidak aktifnya mutasi gen p53.
2.6.4. Potensi replikasi tanpa batas
Pada setiap siklus replikasi sel, telomerase (pengulangan DNA pada
setiap kromosom) menjadi lebih pendek dan menghasilkan kematian.
Tumor pada umumnya mengekspresi enzim telomerase yang memproteksi
telomerase dari pemendekan dan mencegah sel menjadi tua Estrogen dan
progesteron menstimulasi, sedangkan tamoxifen dan wild type (varian
normal) p53 menghambat, aktivitas telomerase pada kanker mamae dan
endometrium belum dipublikasikan penelitian fungsi telomerase
endometriosis, neoplasma yang bergantung pada estrogen mempunyai
potensi rentan terhadap kontrol telomerase.42
2.6.5. Sokongan dari angiogenesis
Patologi angiogenesis, supresor sel imun dan aktivasi sel imun
terdapat pada endometriosis dan proses karsinoma. Transmisi genetik atau
induksi lingkungan (pencemaran dioksin) merubah angigenik dan atau
respon imun yang merupakan predisposisi perempuan pada implantasi
ektopik sel endometrial yang dibawa pada kavum uteri pada saat darah
29
Terdapat kesamaan implikasi mediator inflamtory angiogenesis pada
karsinoma dan endometriosis.Gen pada mediator menunjukkan
polimorfisme genetik merupakan predisposisi pada endometriosis ( eg
intercellular adhesion molecule-1. IL-6,IL-10 gene promoters) maupun
karsinoma (eg IL-6, tumour necrosis factor(TNF)α, NFKB-1 dan peroxisome
proliferator activated receptor –y genes) pengobatan antiangiogenik
menghambat faktor proangiogenik.15
2.6.6 Kemampuan invasi dan metastase ke jaringan
Kemampuan invasi menembus membran basalis merupakan
spesifikasi perubahan dari non ivasif ke kanker inavasif tumor
mengeluarkan protease (eg MMPs) menghancurkan membrana basalis dari
stroma Ekspresi dari MMP-2 dan MMP-9 berkorelasi dengan stadium
kanker. Aktivitas MMP terdapat juga pada jejas endometriotik. 46
Deregulasi dari sinyal perekat sel meliputi intrgrin β karsinomatenin,
E-cadherin dan P-karsinomadherin terlihat pada kejadian dari beberapa
keganasan dan terlihat pada etipatogenesis endomerioma.Mutasi
B-Catenin telah dikenal pada kanker endometrial dan kanker ovarium
endometrioid namun belum dapat dipastikan untuk endometriosis. 47
2.6.7 Memiliki instabilitas genetik
Model klasik dari perubahan keganasan dari sel termasuk di
30
itu sendiri. Biasanya didampingi dengan aktivasi protoonkogen menjadi
onkogen (transformasi dari pertumbuhan sel yang normal, proliferasi dan
diferensiasi gen) dan inaktivasi oleh TSG (gen yang mengkode protein yang
mengatur proliferasi sel dan perubahan keganasan.) 15
Enam mekanisme dasar gen yang berhubungan dengan
ketidakstabilan gen dari kanker , namun hanya tiga yang pertama yang
berhubungan dengan endometriosis:15
i) Mendapatkan aktivitas onkogenik
ii) Inaktivasi oleh TSG
iii) Anomali dari enzyme yang berhubungan dengan perbaikan DNA,
identifikasi oleh instabilitas mikrosatelit (MSI)
iv) Inaktivasi gen yang memonitor instabilitas gen pada saat siklus
sel
v) Disfungsi telomerase
vi) Hipermetilasi
Mekanisme diatas saling sinergis untuk meningkatkan proses
ketidakstabilan gen dan proliferasi dari sel tumor. Sebagai contoh :
defisiensi dari TSG p53 mengurangi respon sel terhadap kerusakan sel
31
2.7. Kerangka Teori
anti-apoptosis pro-apoptosis
Menghambat
Mengaktifkan
P 53
BCL2 BAX Bcl-xL BAK
Caspase 9 Sitokrom c
Apoptosis
Endometrioma Karsinoma ovarium tipe 1
32
2.8. Kerangka Konsep
Endometrioma
33
BAB III
METODOLOGI PENELITIAN
3.1. Rancangan Penelitian
Penelitian ini adalah penelitian deskriptif observasional dengan
pendekatan cross sectional.
3.2. Waktu dan Tempat Penelitian
Tempat penelitian dilakukan di Departemen Obstetri dan Ginekologi
Fakultas Kedokteran Universitas Sumatera Utara-RSUP. H. Adam Malik
Medan sedangkan pemeriksaan imunohistokimia dilakukan oleh
Departemen Patologi Anatomi (PA) Universitas Sumatera Utara Medan.
Penelitian ini dilakukan mulai Januari 2015 sampai dengan Februari
2015.
3.3. Subjek Penelitian
Subjek penelitian adalah blok parafin penderita endometrioma dan
karsinoma ovarium tipe1 yaitu tipe serosum, tipe musinosum, tipe
endometrioid dan tipe clear cell yang berdiferensiasi baik yang dibuktikan
34
3.4. Besar Sampel
Penentuan besar sampel, dilakukan berdasarkan perhitungan
analitik numerik tidak berpasangan.
Besar sampel penelitian dihitung secara statistik berdasarkan rumus :
Dimana :
Zα = Nilai baku normal dari tabel Z yang besarnya bergantung pada nilai α
yang besarnya ditentukan. Nilai α =0,05 Zα = 1,64
Zβ = nilai baku normal dari tabel Z yang besarnya bergantung pada nilai β yang ditentukan. Nilai β = 0,2 Zβ = 0,84
SD = simpangan baku gabungan score ekspresi p53 endometrioma dan
karsinoma ovarium 1,5
X1-X2 = selisih rerata minimal yang dianggap bermakna yang ditentukan
peneliti
Setelah dilakukan perhitungan, didapat besar sampel minimal 22,2 sampel
endometrioma dan 22,2 sampel karsinoma ovarium tipe 1. Pada penelitian
ini diambil 25 sampel endometrioma dan 25 sampel karsinoma ovarium
35
3.5 Teknik sampling
Pengambilan sampling dilakukan dengan cara non random
convenient-sampling pada parafin blok jaringan endometrioma dan pada
paraffin blok jaringan karsinoma ovarium tipe 1 yaitu tipe serosum, tipe
musinosum, tipe endometrioid dan tipe clear cell yang berdiferensiasi baik
di RSUP H. Adam Malik Medan.
3.6. Kriteria Inklusi dan Eksklusi Peneltian
Kriteria inklusi adalah :
Parafin blok jaringan endometrioma dan karsinoma ovarium tipe 1
yaitu tipe serosum, tipe musinosum, tipe endometrioid dan tipe clear
cell yang berdiferensiasi baik yang dibuktikan dengan hasil
pemeriksaan histopatologi
Kriteria eksklusi adalah :
1. Sediaan tidak dapat dianalisa
2. Rekam Medik tidak dijumpai (data tidak lengkap)
3.7. Identifikasi Variabel Variabel bebas
Status penyakit endometrioma dan karsinoma ovarium tipe 1
Variabel tergantung