UJI PENDAHULUAN KAPASITAS ABU SEKAM PADI
DALAM MENGADSORPSI TIMBAL DAN KADMIUM
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk
memperoleh
gelar Sarjana Farmasi pada Fakulta
s FarmasSu
matera
Utar
OLEH:
VINA RAHMAYANI
NIM 091501001
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI PENDAHULUAN KAPASITAS ABU SEKAM PADI
DALAM MENGADSORPSI TIMBAL DAN KADMIUM
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk
memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
VINA RAHMAYANI
NIM 091501001
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI PENDAHULUAN KAPASITAS ABU SEKAM PADI
DALAM MENGADSORPSI TIMBAL DAN KADMIUM
OLEH:
VINA RAHMAYANI
NIM 091501001
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 27 Agustus 2013
Pembimbing I, Panitia Penguji,
Dra. Nurmadjuzita, M.Si., Apt. Dr. Muchlisyam, M.Si., Apt.
NIP 194809041974122001 NIP 195006221980021001
Dra. Nurmadjuzita, M.Si., Apt.
NIP 194809041974122001 Pembimbing II,
Drs. Chairul A. Dalimunthe, M.Sc., Apt. Dra. Tuty Roida Pardede, M.Si., Apt.
NIP 194907061980021001 NIP 195401101980032001
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
Medan, Oktober 2013 Fakultas Farmasi
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan. Skripsi ini disusun
untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada
Fakultas Farmasi Universitas Sumatera Utara, dengan judul Uji Pendahuluan
Kapasitas Abu Sekam Padi Dalam Mengadsorpsi Timbal dan Kadmium.
Pada kesempatan ini dengan segala kerendahan hati penulis
mengucapkan terima kasih yang sebesar-besarnya kepada, Bapak Prof. Dr.
Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU Medan,
yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan
pendidikan. Ibu Dra. Nurmadjuzita, M.Si., Apt., dan Bapak Drs. Chairul Azhar
Dalimunthe, M.Sc., Apt., yang telah membimbing dan memberikan petunjuk
serta saran-saran selama penelitian hingga selesainya skripsi ini. Bapak Dr.
Muchliysam, M.Si., Apt., Ibu Dra. Tuty Roida Pardede, M.Si., Apt., dan Ibu
Dra. Sudarmi, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik,
saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan
Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik selama
perkuliahan dan Bapak Drs. Saiful Bahri, M.S., Apt., selaku penasehat
akademik yang selalu memberikan bimbingan, perhatian dan motivasi kepada
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada
terhingga kepada Ayahanda Ahmad Yani dan Ibunda Yarnis yang telah
memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun,
pengorbanan baik materi maupun motivasi serta doa yang tulus yang tidak
pernah berhenti. Adikku tercinta Yumi Rahmayani, Nanang Maulana, Agil
Ahmad Maulana dan Maenek Tk. Nazarudin serta seluruh keluarga yang selalu
mendoakan dan memberikan semangat. Serta teman-teman Farmasi angkatan
09 yang selalu memberikan dukungan, semangat dan motifasi.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini
masih jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati,
penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya,
penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Juli 2013 Penulis,
UJI PENDAHULUAN KAPASITAS ABU SEKAM PADI DALAM MENGADSORPSI TIMBAL DAN KADMIUM
ABSTRAK
Tingginya tingkat pencemaran logam timbal dan kadmium di perairan umumnya dihasilkan oleh limbah industri (seperti industri cat, batrai). Karena bersifat toksik, diperlukan suatu upaya pengurangan kadar logam tersebut seperti menggunakan metode adsorpsi dengan adsorben abu sekam padi. Abu sekam padi berasal dari sekam padi yang merupakan hasil samping penggilingan padi sehingga harganya murah, mudah didapatkan, dan
mengandung silika (SiO2) yang merupakan material berpori sehingga cocok
untuk dijadikan adsorben timbal dan kadmium. Tujuan penelitian ini adalah sebagai penelitian pendahuluan untuk mengetahui kapasitas sekam padi yang diabukan selama 5 jam dan 15 jam untuk mengadsorpsi logam timbal dan kadmium.
Pada penelitian ini, adsorbennya adalah sekam padi yang diabukan pada suhu 500°C selama 5 jam dan 15 jam. Adsorbatnya berupa larutan baku
timbal dan kadmium 10 µg/ml sebanyak 25 ml. Kadar timbal dan kadmium
setelah penambahan adsorben ditentukan dengan metode spektrofotometri serapan atom pada panjang gelombang 283,3 nm untuk timbal dan 228,8 untuk kadmium dengan atomisasi menggunakan nyala udara-asetilen.
Hasil penelitian menunjukan bahwa terdapat perbedaan kemampuan adsorpsi sekam padi yang diabukan selama 5 jam dan 15 jam terhadap logam timbal dan kadmium. Sekam padi yang diabukan selama 5 jam lebih baik dalam mengadsorpsi logam timbal dan kadmium. Kadar timbal dan kadmium yang diadsorpsi oleh sekam padi yang diabukan selama 5 jam adalah 0,9134 ± 0,0532 mg/g dan 0,5022 ± 0,0244 mg/g. Sedangkan kadar timbal dan kadmium yang diadsorpsi oleh sekam padi yang diabukan selama 15 jam adalah 0,6359 ± 0,0548 mg/g dan 0,4433 ± 0,0402 mg/g.
PRELIMINARY TEST OF RICE HUSK ASH CAPASITY IN ADSORPTION OF LEAD AND CADMIUM
ABSTRACT
High pollution of lead and cadmium in water aregenerally produced by industrial waste (such as paint and battery industries). Because of their toxicity, an effort is require to reduce those heavy metals level, such as using adsorption method with rice husk ash as adsorbent. Rice husk ash made from rice husk, a byproduct of rice milling, which is low cost, widely available, and high amount of silica contains (SiO2) which is a porous material and can be used as adsorbent of lead and cadmium. The aim of this study is as preliminary test of rice husk ash capacity in adsorption of laed and cadmium.
In this study, rice husk was furnace at 500°C for 5 hours and 15 hours. The adsorbate was 10 µg/ml in 25 ml aqueous solution of lead and cadmium. Quantitative analysis of lead and cadmium after adsorbent added was done by atomic absorption spectrophotometer, with atomization using air-acetylene flame at wavelengths 283.3 nm for lead and 228.8 nm for cadmium.
The result of this study showed that there are differences in adsorption ability between 5 hours and 15 hours furnace of rice husk. Rice husk furnaced for 5 hours has better adsorption of lead and cadmium. The quantitative level of lead and cadmium adsorbed by rice husk which was furnace for 5 hours were 0.9134 ± 0.0532 mg/g and 0.5036 ± 0.0265 mg/g. And quantitative level of lead and cadmium adsorbed by rice husk which furnace for 15 hours were 0.6359 ± 0.0548 mg/g and 0.4439 ± 0.1297 mg/g.
Key word: Rice husk ash, Furnace, Silica, Lead, Cadmium, Adsorbent, Atomic absorption spectrophotometry
DAFTAR ISI
JUDUL ... ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... iv
ABSTRACT ... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Sekam Padi ... 5
2.1.1 Komposisi Sekam Padi dan Abu Sekam Padi ... 6
2.2 Logam Berat dan Pencemaran Lingkungan ... 7
2.2.1 Timbal ... 8
2.2.1.1 Manfaat ... 8
2.2.1.2 Toksisitas ... 8
2.2.2 Kadmium ... 8
2.2.2.1 Manfaat ... 8
2.2.2.2 Toksisitas ... 9
2.3 Adsorpsi ... 9
2.3.1 Pembagian Adsorpsi ... 10
2.3.1.1 Adsorpsi Fisika ... 10
2.3.1.2 Adsorpsi Kimia ... 10
2.3.2 Faktor yang Mempengaruhi Adsorpsi ... 11
2.3.2 Isoterm Adsorpsi ... 12
2.4 Study Pendahuluan Abu Sekam Padi Sebagai Adsorben ... 12
2.5 Spektrofotometri Serapan Atom ... 13
2.4.1 Gangguan pada Spektrofotometri Serapan Atom ... 17
BAB III METODE PENELITIAN ... 18
3.1 Tempat dan Waktu Penelitian ... 18
3.2 Bahan-bahan ... 18
3.2.1 Sampel ... 18
3.2.2 Bahan ... 18
3.3 Alat-alat ... 18
3.4 Prosedur Penelitian ... 19
3.4.1 Pengambilan Sampel ... 19
3.4.2 Pembuatan Adsorben ... 19
3.4.3.1 Pembuatan Kurva Kalibrasi Timbal ... 19
3.4.3.2 Pembuatan Kurva Kalibrasi Kadmium ... 20
3.4.4 Pembuatan Larutan Uji ... 20
3.4.4.1 Pembuatan Larutan Uji Timbal ... 20
3.4.4.2 Pembuatan Larutan Uji Kadmium ... 20
3.4.5 Penetapan Kadar Logam Setelah Penambahan Adsorben 21
3.4.5.1 Timbal ... 21
3.4.5.2 Kadmium ... 21
3.4.6 Analisis Data Secara Statistik ... 22
3.4.6.1 Penolakan Hasil Pengamatan ... 22
3.4.6.2 Pengujian Beda Nilai Rata-rata antar Sampel 22 BAB IV HASIL DAN PEMBAHASAN ... 24
4.1 Analisis Kuantitatif ... 24
4.1.1 Kurva Kalibrasi Timbal dan Kadmium ... 24
4.1.2 Adsorben yang Diperoleh Setelah Pengabuan ... 25
4.1.3 Analisis Timal dan Kadmium yang Diadsorpsi ... 27
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... ... 31
5.2 Saran ……… ... 31
DAFTAR PUSTAKA ……….... .. 32
DAFTAR TABEL
Tabel 1.
Berat Abu Sekam Padi yang Diperoleh Setelah
Pengabuan Sekam Padi pada Suhu 500°C Selama 5 Jam ……….
Berat Abu Sekam Padi yang Diperoleh Setelah
Pengabuan Sekam Padi pada Suhu 500°C Selama 15 jam
Tabel 2.
Kadar Timbal yang Diadsorpsi oleh Sekam adi yang Diabukan pada Suhu 500°C Selama 5 Jam dan 15 Jam ....
Tabel 3.
Kadar Kadmium yang Diadsorpsi oleh Sekam Padi yang Diabukan pada Suhu 500°C Selama 5 Jam dan 15 Jam
Tabel 4.
Kadar Rata-rata Timbal dan Kadmium yang Diadsorpsi
Tabel 5.
Hasil Uji Beda Nilai Rata-rata Logam Timbal dan
Kadmium yang Diadsorpsi ………
Tabel 6.
16
26
26
28
28
29
Halaman
Nyala yang Dapat Digunakan dalam Spektrofotometri Serapan Atom ………
Tabel 7.
DAFTAR GAMBAR
Halaman
Gambar 1.
Kurva K Kurva Kalibrasi Timbal ……….. 24
Gambar 4. Kurva Kalibrasi Kadmium ... 25 Proses Adsorpsi ………...
Gambar 2.
10
Komponen Spektrofotometri Serapan Atom ……... 15
DAFTAR LAMPIRAN
Lampiran 1. Gambar Sekam Padi ... 36
Lampiran 2. Lampiran 3. Lampiran 4. Lampiran 5. Lampiran 6. Lampiran 7. Lampiran 8. Lampiran 9. Lampiran 10.
Adsorben Sekam Padi yang Diabukan pada Suhu
500°C selama 5 jam dan 15 jam ...
Bagan Alir Proses Pembuatan Adsorben ...
Bagan Alir Pengukuran Timbal yang Diadsorpsi ...
Bagan Alir Pengukuran Kadmium yang Diadsorpsi ...
Data Hasil Pengukuran Absorbansi Larutan Baku Timbal dan Kadmium ...
Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ...
Contoh perhitungan persentase abu dan karbon yang tersisa setelah pengabuan sekam padi ...
Hasil Analisis Kadar Timbal dan Kadmium yang Diadsorpsi oleh Adsorben yang Diabukan Selama 5 jam ...
Contoh Perhitungan Kadar Timbal dan Kadmium yang Diadsorpsi oleh Sekam Padi yang Diabukan Selama 5 jam ...
Perhitungan Statistik Kadar Timbal dan Kadmium yang diadsorpsi oleh Sekam Padi yang Diabukan
Selama 5 jam ...
Hasil Analisis Kadar Timbal dan Kadmium yang diadsorpsi oleh Adsorben yang diabukan selama 15 jam ...
Contoh Perhitungan Kadar Timbal dan Kadmium yang Diadsorpsi oleh Sekam Padi yang Diabukan Selama 15
Lampiran 14
Lampiran 15
Perhitungan Statistik Kadar Timbal dan Kadmium yang Diadsorpsi oleh Sekam Padi yang Diabukan selama 15 jam ...
Pengujian Beda Nilai Rata-rata Kadar Timbal dengan menggunakan Sekam Padi yang Diabukan masing-masing 5 jam dan 15 jam ...
55
59
Pengujian Beda Nilai rata-Rata Kadar Kadmium dengan menggunakan Sekam Padi yang Diabukan masing-masing 5 jam dan 15 jam ………
Gambar Atomic Absorption Spectrophotometer (AAS) Hitachi Z-2000 dan mini orbital shaker ……...
Tabel Distribusi t ……...
Tabel Distribusi F ……...
61
63
64
65
n 18
3.
Lampiran 16.
Lampiran 17.
UJI PENDAHULUAN KAPASITAS ABU SEKAM PADI DALAM MENGADSORPSI TIMBAL DAN KADMIUM
ABSTRAK
Tingginya tingkat pencemaran logam timbal dan kadmium di perairan umumnya dihasilkan oleh limbah industri (seperti industri cat, batrai). Karena bersifat toksik, diperlukan suatu upaya pengurangan kadar logam tersebut seperti menggunakan metode adsorpsi dengan adsorben abu sekam padi. Abu sekam padi berasal dari sekam padi yang merupakan hasil samping penggilingan padi sehingga harganya murah, mudah didapatkan, dan
mengandung silika (SiO2) yang merupakan material berpori sehingga cocok
untuk dijadikan adsorben timbal dan kadmium. Tujuan penelitian ini adalah sebagai penelitian pendahuluan untuk mengetahui kapasitas sekam padi yang diabukan selama 5 jam dan 15 jam untuk mengadsorpsi logam timbal dan kadmium.
Pada penelitian ini, adsorbennya adalah sekam padi yang diabukan pada suhu 500°C selama 5 jam dan 15 jam. Adsorbatnya berupa larutan baku
timbal dan kadmium 10 µg/ml sebanyak 25 ml. Kadar timbal dan kadmium
setelah penambahan adsorben ditentukan dengan metode spektrofotometri serapan atom pada panjang gelombang 283,3 nm untuk timbal dan 228,8 untuk kadmium dengan atomisasi menggunakan nyala udara-asetilen.
Hasil penelitian menunjukan bahwa terdapat perbedaan kemampuan adsorpsi sekam padi yang diabukan selama 5 jam dan 15 jam terhadap logam timbal dan kadmium. Sekam padi yang diabukan selama 5 jam lebih baik dalam mengadsorpsi logam timbal dan kadmium. Kadar timbal dan kadmium yang diadsorpsi oleh sekam padi yang diabukan selama 5 jam adalah 0,9134 ± 0,0532 mg/g dan 0,5022 ± 0,0244 mg/g. Sedangkan kadar timbal dan kadmium yang diadsorpsi oleh sekam padi yang diabukan selama 15 jam adalah 0,6359 ± 0,0548 mg/g dan 0,4433 ± 0,0402 mg/g.
PRELIMINARY TEST OF RICE HUSK ASH CAPASITY IN ADSORPTION OF LEAD AND CADMIUM
ABSTRACT
High pollution of lead and cadmium in water aregenerally produced by industrial waste (such as paint and battery industries). Because of their toxicity, an effort is require to reduce those heavy metals level, such as using adsorption method with rice husk ash as adsorbent. Rice husk ash made from rice husk, a byproduct of rice milling, which is low cost, widely available, and high amount of silica contains (SiO2) which is a porous material and can be used as adsorbent of lead and cadmium. The aim of this study is as preliminary test of rice husk ash capacity in adsorption of laed and cadmium.
In this study, rice husk was furnace at 500°C for 5 hours and 15 hours. The adsorbate was 10 µg/ml in 25 ml aqueous solution of lead and cadmium. Quantitative analysis of lead and cadmium after adsorbent added was done by atomic absorption spectrophotometer, with atomization using air-acetylene flame at wavelengths 283.3 nm for lead and 228.8 nm for cadmium.
The result of this study showed that there are differences in adsorption ability between 5 hours and 15 hours furnace of rice husk. Rice husk furnaced for 5 hours has better adsorption of lead and cadmium. The quantitative level of lead and cadmium adsorbed by rice husk which was furnace for 5 hours were 0.9134 ± 0.0532 mg/g and 0.5036 ± 0.0265 mg/g. And quantitative level of lead and cadmium adsorbed by rice husk which furnace for 15 hours were 0.6359 ± 0.0548 mg/g and 0.4439 ± 0.1297 mg/g.
Key word: Rice husk ash, Furnace, Silica, Lead, Cadmium, Adsorbent, Atomic absorption spectrophotometry
BAB I PENDAHULUAN
1.1 Latar Belakang
Pencemaran air yang disebabkan karena zat anorganik seperti logam
berat menjadi masalah serius yang dihadapi oleh berbagai daerah di Indonesia
(Mulia, 2005). Pembangunan yang berbasis industri menjadi salah satu faktor
penyebab meningkatnya pencemaran perairan tersebut sehingga dapat
menurunkan kualitas air dan tidak layak digunakan sesuai dengan
peruntukannya (Hamid dan Pramudyanto, 2007; Soegianto, 2004). Industri
yang menghasilkan limbah khususnya yang mengandung logam berat, harus
diberikan perlakuan khusus untuk mengurangi kadar logam sebelum dibuang
ke perairan (Farooq, et al., 2010).
Beberapa jenis logam seperti timbal dan kadmium, dengan konsentrasi
yang relatif kecil sudah dapat membahayakan makhluk hidup. Logam
merupakan zat yang sangat persisten sehingga dapat masuk melalui rantai
makanan dan terkonsentrasi dalam tubuh makhluk hidup melalui proses
bioakumulasi (Mulia, 2005).
Mengingat dampak yang ditimbulkan oleh kedua logam tersebut, maka
diperlukan suatu upaya untuk mengurangi kadarnya. Adsorpsi merupakan
salah satu metode yang dapat digunakan untuk mengurangi kadar timbal dan
kadmium dalam air atau perairan. Keuntungan menggunakan metode tersebut
dibandingkan dengan metode lain, seperti pengendapan secara kimia, membran
murah; tidak menimbulkan efek samping beracun dan efektif pada konsentrasi
logam yang rendah (Igwe dan Abia, 2007); selain itu jenis adsorben yang
digunakan juga banyak dan beragam (El-Said, et al., 2012) seperti kitosan.
Penggunaan adsorben tersebut membutuhkan proses pembuatan yang lebih
lama, cenderung menggunakan bahan kimia dan mahal (Igwe dan Abia, 2007),
sehingga diperlukan alternatif lain yang lebih murah, bahan dasarnya mudah
diperoleh (El-Said, et al., 2012), serta tidak membutuhkan proses pembuatan
yang lama dan tidak memerlukan banyak perlakuan dalam pembuatannya
(Ngah dan Hanafiah, 2008). Salah satunya adalah sekam padi yang merupakan
limbah dari penggilingan padi (Tarley dan Arruda, 2004; Ngah dan Hanafiah,
2008).
Menurut Badan Pusat Statistik pada tahun 2011, Indonesia
menghasilkan 65,75 juta ton gabah kering, dan 18-28% terdiri atas sekam padi.
Sekam padi jika diarangkan akan menguraikan unsur-unsur organiknya. Dan
jika dilanjutkan akan berubah menjadi abu. Pengabuan sekam padi
menghasilkan 18-20% abu. Sekitar 87-97% dari kandungan utama abu sekam
padi tersebut adalah silika (SiO2) (Hsu dan Luh, 1980). Menurut Kolasinski
(2008), silika pada abu sekam padi merupakan material berpori sehingga dapat
digunakan sebagai adsorben logam timbal dan kadmium.
Penggunaan abu sekam padi sebagai adsorben akan meningkatkan
nilainya, karena biasanya pada sentra-sentra penggilingan padi, sekam padi
hanya dibakar menjadi abu kemudian dibiarkan begitu saja, atau pun
Mengingat tidak mungkin untuk menggunakan langsung air limbah
karena banyaknya zat lain yang dapat mempengaruhi adsorpsi, maka
digunakan larutan baku untuk mengetahui kapasitas adsorpsi abu sekam padi
terhadap logam timbal dan kadmium.
Berdasarkan uraian di atas, peneliti tertarik untuk meneliti kapasitas
adsorpsi abu sekam padi terhadap logam timbal dan kadmium , yang diujikan
terhadap larutan baku masing-masing logam tersebut. Sekam padi diabukan
pada suhu 500°C dengan variasi waktu pengabuan yaitu 5 jam dan 15 jam.
Timbal dan kadmium yang tersisa pada larutan baku ditentukan secara
spektrofotometri serapan atom. Pemilihan metode spektrofotometri serapan
atom karena pelaksanaannya relatif sederhana, memiliki kepekaan yang tinggi,
dan interferensinya sedikit (Gandjar dan Rohman, 2008), jika dibandingkan
1.2 Perumusan Masalah
a. Apakah sekam padi yang diabukan selama 5 jam dan 15 jam pada suhu
500°C dapat menyerap logam timbal dan kadmium dari larutan baku.
b. Apakah perbedaan waktu pengabuan pada suhu 500°C dapat
mempengaruhi kemampuan abu sekam padi sebagai adsorben logam
timbal dan kadmium.
1.3 Hipotesis
a. Penggunaan sekam padi yang diabukan selama 5 jam dan 15 jam
dengan suhu 500°C dapat digunakan sebagai adsorben untuk
mengurangi kadar logam timbaldan kadmium dari larutan baku.
b. Variasi waktu pengabuan sekam padi pada suhu 500°C akan
mempengaruhi daya adsorbsinya terhadap logam timbal dan kadmium.
1.4 Tujuan
a. Untuk mengetahui kapasitas adsorpsi sekam padi yang diabukan pada
suhu 500°C selama 5 jam dan 15 jam terhadap timbal dan kadmium.
b. Untuk membandingkan kemampuan adsorpsi dari sekam padi yang
diabukan selama 5 jam dan 15 jam pada suhu 500°C terhadap logam
timbal dan kadmium.
1.5 Manfaat
Sebagai informasi yang dapat digunakan untuk penelitian selanjutnya
BAB II
TINJAUAN PUSTAKA
2.1 Sekam Padi
Menurut Badan Pusat Statistik (2011), Indonesia memiliki sawah seluas
12,84 juta hektar yang menghasilkan padi sebanyak 65,75 juta ton. Limbah
sekam padi yang dihasilkan sebanyak 8,2 sampai 10,9 ton. Potensi limbah yang
besar ini hanya sedikit yang baru dioptimalkan. Secara tradisional, sekam padi
biasanya hanya digunakan sebagai bahan bakar konvensional (Danarto, et al.,
2010).
Sekam padi merupakan bagian pelindung terluar dari padi (Oryza
sativa). Dari proses penggilingan dihasilkan sekam sebanyak 20-30%, dedak
8-12% dan beras giling 52% bobot awal gabah (Hsu dan Luh, 1980). Pada proses
penggilingan padi, sekam akan terpisah dari butiran beras dan menjadi bahan
sisa atau limbah penggilingan. Karena bersifat abrasif, nilai nutrisi rendah, bulk
density rendah, serta kandungan abu yang tinggi membuat penggunaan sekam
padi terbatas. Diperlukan tempat penyimpanan sekam padi yang luas sehingga
biasanya sekam padi dibakar untuk mengurangi volumenya. Jika hasil
pembakaran sekam padi ini tidak digunakan, akan menimbukan masalah
lingkungan (Hsu dan Luh, 1980).
Salah satu proses alternatif untuk meningkatkan manfaat sekam padi
adalah dengan pirolisis. Pirolisis merupakan proses dekomposisi suatu zat/
berupa char mengandung karbon dan silika dengan komposisi tergantung pada
kondisi pirolisis (Danarto, et al., 2010).
Sekam padi mempunyai bulk density 96 sampai 160 kg/m3.
Penggilingan sekam padi dapat meningkatkan bulk density dari 192 menjadi
384 kg/m3 Dengan pembakaran pada kondisi tertentu dapat menghasilkan abu
sekam padi yang lebih mudah dihaluskan (Hsu dan Luh, 1980).
2.1.1 Komposisi Sekam Padi dan Abu Sekam Padi
Sekam padi terdiri unsur organik seperti selulosa, hemiselulosa, dan
lignin. Selain itu, sekam padi juga mengandung unsur anorganik, berupa abu
dengan kandungan utamanya adalah silika 94-96%. Selain itu, juga terdapat
komponen lain seperti Kalium, Kalsium, Besi, Fosfat, dan Magnesium (Hsu
dan Luh, 1980). Komposisi anorganik dari abu sekam padi berbeda, tergantung
dari kondisi geografis, tipe padi, dan tipe pupuk yang digunakan (Shukla,
2011).
Material karbon yang mempunyai pori disebut juga karbon aktif.
Pengaktifan dapat dilakukan dengan dua cara, yakni dengan cara fisika dan
kimia. Biasanya, pengaktifan secara fisika dengan cara karbonisasi terhadap
bahan dasar, karbonisasi dan aktifasi terjadi secara bersamaan dan pada
temperatur yang rendah. Dengan aktifasi, pori baru terbentuk tapi pada saat
yang bersamaan ukuran pori meningkat menjadi lebih besar sehingga
menghasilkan luas area permukaan yang tinggi, sekitar 1500 m2/g. Karbon
aktif diketahui mempunyai struktur pori yang beragam, menurut IUPAC,
< 25 nm) dan makropori (d > 50 nm). Mikro dan mesopori dari karbon aktif
mempunyai kapasitas yang baik sebagai adsorben (Mdoe dan Mkayula, 2002).
Abu sekam padi berwarna putih keabuan, yang mengandung silika
(Si2O) dengan kisaran 86,9-97,3% (Widwiastuti, et al., 2013). Merupakan
oksida berpori, bersifat inert, dan area permukaan yang luas (Kolasinski,
2008). Luas area permukaan dari silika adalah 50-430 m2/g (Widwiastuti, et
al., 2013)
2.2 Logam berat dan pencemaran lingkungan
Logam berat dapat mencemari lingkungan udara, tanah maupun air.
Masuknya logam berat ke dalam badan air dapat melalui proses alami maupun
diakibatkan oleh perbuatan manusia (Mulia, 2005). Logam berat dapat
menyebabkan pencemaran lingkungan dan berpengaruh pada kesehatan
manusia karena bersifat toksik, dapat terakumulasi pada rantai makanan dan
bersifat persisten (Igwe dan Abia, 2007). Beberapa jenis logam seperti timbal
dan kadmium dengan konsentrasi relatif kecil dapat membahayakan makhluk
hidup (Mulia, 2005).
Logam terbagi dua, yakni logam berat yang mempunyai berat 5 gram
atau lebih untuk tiap cm3 dan logam ringan yang beratnya kurang dari 5 gram
tiap cm3. Ada istilah logam trace yakni logam yang dalam keadaan alami
2.2.1 Timbal 2.2.1.1 Manfaat
Timbal (plumbum atau timah hitam) sering digunakan sebagai bahan
pelapis atau coating karena sifatnya yang tahan terhadap peristiwa korosi.
Penggunaan timbal adalah untuk produksi baterai pada kendaraan bermotor,
kabel, amunisi, dan industri percetakan tinta (Darmono, 1995).
2.1.1.2 Toksisitas
Gejala yang khas dari keracunan timbal adalah gastroenteritiss,
merupakan reaksi rangsangan garam timbal terhadap mukosa saluran cerna.
Selain itu, juga dapat menyebabkan anemia, karena timbal dapat berikatan
dengan eritrosit sehingga sel darah merah mudah pecah dan berpengaruh
terhadap sintesis Hb Disamping itu, dapat menyebabkan encefalopati, yakni
kerusakan sel endotel kapiler darah otak sehingga protein dapat masuk ke
dalam otak (Darmono, 1995).
Di dalam tubuh, timbal bersirkulasi dalam darah setelah diabsorbsi dari
usus, kemudian didistribusikan dalam jaringan lunak seperti tubulus ginjal dan
sel hati. Timbal terdeposit dalam tulang, rambut, gigi. Di mana 90% terdeposit
dalam tulang (Darmono, 2001).
2.2.2 Kadmium 2.2.2.1 Manfaat
Kadmium bersifat tahan terhadap korosi sehingga banyak digunakan
sebagai penstabil dalam pembuatan polivinil klorida. Selain itu, mempunyai
sifat yang tahan panas sehingga bagus untuk campuran dalam pembuatan
pencegahan korosi (Darmono, 1995). Kebanyakan kadmium merupakan
produk samping dari pengecoran seng, timah atau tembaga. Kadmium banyak
digunakan pada industri pelapisan logam, pigmen, batrai, dan plastik
(Darmono, 2001). Sehingga, limbah industri yang mengandung kadmium
sering mencemari perairan.
2.2.2.3 Toksisitas
Kadmium dapat menyebabkan resiko terhadap kerusakan pembuluh
darah. Beberapa efek yang ditimbulkan oleh kadmium adalah kerusakan ginjal,
liver, sistem imunitas, sistem susunan saraf dan darah. Kadmium dapat masuk
ke dalam tubuh melalui inhalasi maupun pencernaan. Setelah kadmium
diabsorbsi maka akan terakumulasi dalam hati dan ginjal. Hati dan ginjal
merupakan tempat deposit 50% dari total kadmium yang masuk ke dalam
tubuh. Waktu paruh kadmium dalam jaringan sekitar 5-10 tahun dalam hati,
sedangkan waktu paruhnya 16-33 tahun dalam ginjal (Darmono,1995).
2.3 Adsorpsi
Adsorpsi merupakan suatu proses dimana komponen pindah dari suatu
fase ke fase lainnya dengan melintasi beberapa pembatas. Atau perpindahan zat
dari pelarut menuju penyerapnya (LaGrega, et al., 2001). Menurut Benjamin
(2002), adsorpsi adalah akumulasi dari suatu substansi pada atau didekat
permukaan. Substansi yang terserap disebut dengan adsorbat, sedangkan bahan
yang menyerap disebut dengan adsorben. Perpindahan bahan organik atau
tranpor bulk fluid, film transport, difusi intrapartikel, physical attachment
Menurut LaGrega, et al., (2001), proses adsorpsi dapat dilihat pada Gambar 1.
2.3.1 Pembagian Adsorpsi 2.3.1.1Adsorpsi fisika
Dalam adsorpsi fisika, melibatkan gaya van der waals yang
menyebabkan molekul adsorbat terikat secara lemah dengan permukaan
adsorben, dan proses ini berlangsung cepat dan bersifat refersibel (Madan dan
Tuli, 2007). Proses adsorpsi fisika terjadi tanpa memerlukan energi aktivasi
(energi untuk bereaksi), sehingga proses tersebut membentuk banyak lapisan
(multilayer) pada permukaan adsorben. Kecepatan adsorpsi tergantung dari
kecepatan difusi dari adsorbat terhadap permukaan adsorben dan tidak
tergantung dari sisi spesifik adsorben (Selwood, 1962).
2.3.1.2Adsorpsi kimia
Adsorpsi kimia terjadi karena adanya reaksi kimia antara
molekul-molekul adsorbat dengan permukaan adsorben dan berlangsung lambat,
bersifat ireversibel dan hanya membentuk satu lapisan (monolayer) (Madan
dan Tuli 2007). Adsorpsi kimia (chemisorptions) selalu disertai dengan
pertukaran elektron pada adsorben dan tergantung terhadap temperatur
(Selwood, 1962).
2.3.2 Faktor yang mempengaruhi adsorpsi
Menurut Al-Anber (2011), beberapa faktor yang mempengaruhi adsorpsi,
yakni:
− Luas permukaan adsorben, semakin luas area permukaan adsorben,
maka kapasitas adsorpsinya juga semakin meningkat.
− Ukuran partikel adsorben, semakin kecil ukuran partikel adsorben maka
akan memperlambat difusi internal.
− Waktu kontak, semakin lama waktu kontak maka proses adsoprsi akan
semakin baik.
− Kelarutan adsorbat dalam air atau limbah, adsobat yang kurang larut
dalam limbah akan semakin mudah untuk diserap oleh adsorben.
− Afinitas pelarut terhadap adsorben, jika permukaan adsorben bersifat
kurang polar, maka substansi yang kurang polar akan lebih mudah
diadsorpsi.
− Ukuran molekul adsorbat dan ukuran pori adsorben, molekul adsorbat
yang berukuran besar jika masuk ke dalam pori adsorben yang ukuran
lebih kecil, maka akan menurunkan kapasitas adsorpsi.
− Kemampuan ionisasi adsorbat
− pH, ionisasi adsorbat tergantung pada pH, sehingga dapat
− Efek konsentrasi awal adsorbat, dengan konsentrasi tinggi, kemampuan
adsorsi lebih sedikit, hal ini berhubungan dengan proses kompetitif
difusi adsorbat terhadap pori adsorben yang tersedia
− Efek dosis adsorben, adsorpsi akan semakin efektif jika adsorben yang
digunakan semakn banyak
Total zat yang teradsorpsi adsorben disebut dengan densitas adsorbsi,
dengan symbol q. Densitas adsorpsi dapat berupa masa zat yang terserap per
luas area (mg/m2) atau per masa adsorben (mg/g) (Benjamin, 2002).
2.3.3 Isoterm adsorpsi
Isoterm adsorpsi merupakan hubungan kesetimbangan antara
konsentrasi pada fase cair dan konsentrasi pada partikel adsorben pada suhu
tertentu. Model isotherm Langmuir dan Freudlich umum digunakan pada
adsorpsi cairan dengan konsentrasi rendah. Isotherm Langmuir berdasarkan
sisi ikatan yang terdistribusi secara homogen diseluruh permukaan adsorben,
dimana adsorpsi terjadi pada satu lapisan (monolayer), serta adsorpsinya
bersifat refersibel (LaGrega, et al., 2001). Sedangkan isotherm Freudlich
berdasarkan adsorpsi pada banyak lapisan (fisisorpsi) Model isotherm ini
mengasumsikan bahwa adsorpsi terjadi secara fisika (Sembodo, 2005).
2.4 Study Pendahuluan Abu Sekam Padi Sebagai Adsorben
Penelitian terdahulu yang memanfaatkan abu sekam padi sebagai
itu, penelitian tentang penggunaan abu sekam padi sebagai adsorben logam
tembaga juga pernah dilakukan oleh Astuti, et al., (2011).
2.5 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom didasarkan pada penyerapan energi
sinar oleh atom-atom netral, dan sinar yang diserap biasanya sinar tampak atau
sinar ultraviolet (Gandjar dan Rohman, 2008).
Prinsip dari spektrofotometer serapan atom adalah atom-atom pada
keadaan dasar mampu menyerap cahaya pada panjang gelombang tertentu,
yang umumnya adalah panjang gelombang pada radiasi yang akan dipancarkan
atom-atom itu bila kembali ke keadaan dasar dari keadaan eksitasi. Jika cahaya
pada panjang gelombang tertentu dilewatkan nyala yang mengandung
atom-atom yang bersangkutan maka sebagian cahaya itu akan diserap dan banyaknya
penyerapan akan berbanding lurus dengan banyaknya atom pada keadaan dasar
yang berada dalam nyala. Lampu yang digunakan disebut dengan lampu
katode rongga dan katode tersebut dilapisi dengan logam yang akan dianalisis.
Kerugian teknik ini adalah lampu harus diganti setiap unsur yang akan dianlisis
berbeda dan hanya satu unsur yang dapat dianalis pada satu waktu (Watson,
2005).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit
(ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu
sampel dan tidak tergantung pada bentuk molekul logam dalam sampel
kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaanya relatif
sederhana, dan interferensinya sedikit (Gandjar dan Rohman, 2008).
Metode spektrofotometri serapan atom berprinsip pada absorpsi cahaya
oleh atom. Atom-atom menyerap cahaya pada panjang gelombang tertentu,
tergantung pada sifat unsurnya. Cahaya pada panjang gelombang ini
mempunyai cukup energi untuk mengubah tingkat elektronik suatu atom.
Transisi elektronik suatu unsur bersifat spesifik. Dengan absorpsi energi,
berarti memperoleh lebih banyak energi, suatu atom pada keadaan dasar
dinaikkan tingkat energinya ke tingkat eksitasi (Khopkar, 1985).
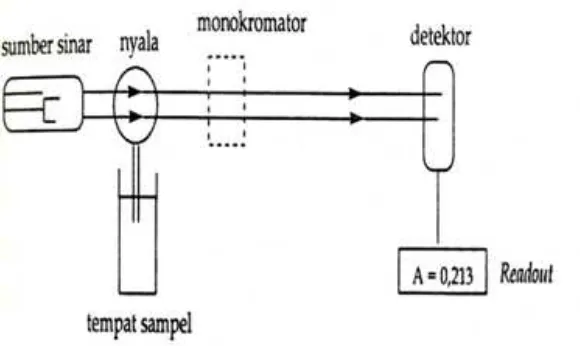
Bagian instrumentasi spektrofotometer serapan atom adalah sebagai
berikut:
a. Sumber Sinar
Sumber sinar yang digunakan adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi
dengan logam tertentu (Gandjar dan Rohman, 2008).
b. Tempat Sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang
akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam
keadaan azas.
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih
dari sekian banyak spektrum yang dihasilkan lampu katoda berongga (Gandjar
dan Rohman, 2008).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Gandjar dan Rohman, 2008).
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima
dari detektor sehingga dapat dibaca alat pencatat hasil (Readout) (Gandjar dan
Rohman, 2008).
f. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan
sebagai pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva
yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman,
2008). Menurut Watson, (2005), komponen spektrofotometer serapan atom
dapat dilihat pada Gambar 2.
[image:31.595.151.441.520.693.2]Ada berbagai macam alat yang digunakan untuk mengubah sampel
menjadi uap atom-atomnya, yaitu:
1. Dengan nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi
bentuk uap dan untuk proses atomisasi. Suhu yang dapat dicapai oleh nyala
tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara
suhunya sebesar 2200°C. Sumber nyala asetilen-udara ini merupakan sumber
nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai
bahan pembakar, sedangkan udara sebagai bahan pengoksidasi (Gandjar dan
Rohman, 2008).
Menurut Khopkar (1985), beberapa contoh nyala yang digunakan
[image:32.595.111.497.456.654.2]dalam spektrofotometri serapan atom dapat dilihat pada Tabel 1:
Tabel 1. Nyala yang Dapat Digunakan dalam Spektrofotometri Serapan Atom
Komposisi Gas °C
Hidrokarbon (methane, propane) – Udara
Udara – Asetilen
Hidrogen – Oksigen
Asetilen – Dinitrogen oksida
Asetilen – Oksigen
Propana – Oksigen
1950
2200
2780
2955
3050
2800
2.Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Untuk mencapai
2000-3000°K (1700 - 2700°C) dalam beberapa detik. Sejumlah sampel diambil
sedikit (hanya beberapa µL), lalu diletakkan dalam tabung grafit, kemudian
tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan
arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis
berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu
sinar yang berasal dari lampu katoda berongga sehingga terjadilah proses
penyerapan energi sinar yang memenuhi kaidah analisis kuantitatif (Gandjar
dan Rohman, 2008). Tanpa nyala sering digunakan untuk logam-logam yang
tidak tahan panas, seperti timbal, kadmun, raksa (Khopkar, 1985).
2.4.1Gangguan-gangguan pada Spektrofotometri Serapan Atom
Gangguan-gangguan (interference) pada Spektrofotometri Serapan
Atom adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi
unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai
dengan konsentrasinya dalam sampel (Gandjar dan Rohman, 2008). Secara
luas dapat dikategorikan menjadi dua kelompok, yakni interferensi spektral dan
interferensi kimia (Khopkar, 1985).
Interferensi spektral disebabkan karena tumpangasuh absorpsi antara
spesies pengganggu dan spesies yang diukur. Interfernsi kimia disebabkan
adanya reaksi kimia selama atomisasi, sehingga mengubah sifat absorpsi
(Khopkar, 1985).
Contoh gangguan kimia adalah terdapatnya senyawa refragtorik (sukar
diuraikan dengan nyala api), dengan adanya senyawa ini maka akan
mengurangi jumah atom netral yang terdapat dalam nyala (Ganjar dan
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara pada bulan Januari - Maret 2013.
3.2 Bahan–bahan 3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah sekam padi yang
diambil dari kilang padi IDAMA 88 Jalan Jendral Sudirman Km 23 Simpang
Bandar Tinggi, Indrapura.
3.2.2 Bahan
Bahan yang digunakan dalam penelitian ini berkualitas pro analisis
keluaran E. Merck yaitu asam nitrat 65% b/v, larutan baku timbal 1000 µg/ml
dan larutan baku kadmium 1000 µg/ml; kecuali akuabides (PT. Ika
Pharmindo).
3.3 Alat–alat
Spektrofotometer serapan atom Hitachi Z-2000 lengkap dengan lampu
katoda timbal dan kadmium, kertas saring Whatman No. 42, neraca analitik,
3.4 Prosedur Penelitian 3.4.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposife
yang dikenal juga sebagai pengambilan sampel dengan pertimbangan dimana
sampel yang diambil dapat mewakili populasi (Budiarto, 2004).
3.4.2 Pembuatan Adsorben
Sekam padi dicuci dengan air, kemudian dicuci lagi dengan akuades.
Setelah itu, diangin-anginkan dan dikeringkan menggunakan oven selama 24
jam pada suhu 110°C. Kemudian sekam padi dihaluskan dengan blender,
sehingga diperoleh berupa serbuk sekam padi.
Serbuk sekam padi ditimbang seksama kurang lebih 3,3 gram untuk
masing-masing kurs porselen sebanyak enam kurs porselen. Setelah itu,
diabukan masing-masing selama 5 jam dan 15 jam pada suhu 500°C kemudian
digerus dan diayak dengan ayakan mesh 100.
3.4.3 Pembuatan Kurva Kalibrasi
3.4.3.1 Pembuatan Kurva Kalibrasi Timbal
Larutan baku timbal dengan konsentrasi 1000 µg/ml dipipet sebanyak 1
ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis
tanda dengan akuabides. Diperoleh konsentrasi larutan timbal 10 µg/ml.
Larutan untuk kurva kalibrasi timbal dibuat dengan memipet (2,5; 5,0;
7,5; 10; 12,5 dan 15) ml larutan baku 10 µg/ml, dimasukan ke dalam labu
tentukur 25 ml dan dicukupkan hingga garis tanda dengan akuabides.
secara spektrofotometri serapan atom dengan nyala udara-asetilen pada
panjang gelombang 283,3 nm.
3.4.3.2 Pembuatan Kurva Kalibrasi Kadmium
Larutan baku kadmium dengan konsentrasi 1000 µg/ml dipipet
sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan
hingga garis tanda dengan akuabides. Diperoleh konsentrasi larutan kadmium
10 µg/ml.
Larutan untuk kurva kalibrasi kadmium dibuat dengan memipet
sebanyak (1,5; 2,5; 5,0; 7,5 dan 10) ml dari larutan 10 µg/ml, dan dimasukan
ke dalam labu tentukur 25 ml kemudian dicukupkan hingga garis tanda dengan
akuabides. Diperoleh kosentrasi (0,6; 1,0; 2,0; 3,0 dan 4,0) µg/ml dan
ditentukan secara spektrofotometri serapan atom dengan nyala udara-asetilen
pada panjang gelombang 228,8 nm.
3.4.4 Pembuatan Larutan Uji
3.4.4.1 Pembuatan Larutan Uji Timbal 10 µg/ml
Larutan baku timbal dengan konsentasi 1000 µg/ml dipipet sebanyak 1
ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis
tanda dengan akuabides. Diperoleh konsentrasi larutan timbal 10 µg/ml
3.4.4.1 Pembuatan Larutan Uji Kadmium 10 µg/ml
Larutan baku kadmium denangan konsentrasi 1000 µg/ml dipipet
sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan
hingga garis tanda dengan akuabides. Diperoleh konsentrasi larutan kadmium
3.4.5 Penetapan Kadar Logam Setelah Penambahan Adsorben 3.4.5.1 Penetapan Kadar Timbal
Larutan uji timbal dengan konsentrasi 10 µg/ml dipipet sebanyak 25
ml, kemudian dimasukkan ke dalam erlenmeyer 100 ml. Ditambahkan
adsorben sebanyak 0,2 gram, diaduk menggunakan mini orbital shaker selama
60 menit dengan kecepatan 150 rpm. Setelah itu disaring dengan menggunakan
kertas Whatman No. 42, kadar timbal yang tersisa ditentukan secara
spektrofotometri serapan atom.
3.4.5.2 Penetapan Kadar Kadmium
Larutan uji kadmium dengan konsentrasi 10 µg/ml dipipet sebanyak 25
ml, kemudian dimasukkan ke dalam erlenmeyer 100 ml. Ditambahkan
adsorben sebanyak 0,4 gram, diaduk menggunakan mini orbital shaker selama
60 menit dengan kecepatan 150 rpm. Setelah itu disaring dengan menggunakan
kertas Whatman No. 42, kadar logam kadmium yang tersisa ditentukan secara
spektrofotometri serapan atom.
Menurut LaGrega, et al., (2001) dan El-Said, (2010), perhitungan kadar
logam timbal dan kadmium yang diadsorpsi setelah penambahan adsorben
dapat dihitung dengan rumus sebagai berikut:
w V ) Ce -Co ( ) / (mg g =
Kadar
Keterangan: Co = Konsentrasi awal logam (larutan uji) (µg/ml)
Ce = Konsentrasi logam yang tersisa setelah penambahan adsorben (µg/ml)
3.4.6 Analisis Data Secara Statistik 3.4.6.1 Penolakan Hasil Pengamatan
Kadar timbal dan kadmium yang diadsorpsi, diperoleh dari hasil
pengukuran masing-masing keenam larutan sampel, kemudian diuji secara
statistik dengan uji t.
Menurut Sudjana (2005), untuk mencari t hitung digunakan rumus:
t hitung =
n SD
X Xi
/ −
Menurut Sudjana (2005), rumus untuk menghitung stándar deviasi (SD)
sebagai berikut:
SD =
(
)
1 -n
X
-Xi 2
∑
Keterangan : Xi = Kadar sampel
−
X = Kadar rata-rata sampel n = Jumlah perlakuan
Data ditolak jika t hitung > t tabel.
Menurut Sudjana (2005), untuk menentukan kadar logam yang dapat
diadsorpsi oleh adsorben dengan interval kepercayaan 99%, α = 0,01, dk =
n-1, dapat digunakan rumus:
Kadar Logam : µ = X ± (t(α/2, dk) x SD / √n )
Keterangan :
−
X = Kadar rata-rata sampel
SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1) α = Interval kepercayaan
3.4.6.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Menurut Sudjana (2005), sampel yang dibandingkan adalah independen
dan jumlah pengamatan masing-masing lebih kecil dari 30 dan variansi (σ)
tidak diketahui sehingga dilakukan uji F untuk mengetahui apakah variansi
kedua populasi sama (σ1 = σ2)atau berbeda (σ1 ≠ σ2) dengan menggunakan
rumus:
Fo = 2 2 2 1
S S
Keterangan : Fo = Beda nilai yang dihitung
S2 = Standar deviasi sampel 2
S1 = Standar deviasi sampel 1
Menurut Sudjana (2005), apabila dari hasilnya diperoleh Fo tidak melewati
nilai kritis F maka dilanjutkan uji dengan distribusi t dengan rumus:
(X1 – X2)
to =
s √1/n1 + 1/n2
Keterangan : X1 = Kadar rata-rata sampel 1 n 1 = Jumlah perlakuan sampel 1
X2 = Kadar rata-rata sampel 2 n 2 = Jumlah perlakuan sampel 2
S = Standar deviasi sampel
jika Fo melewati nilai kritis F, dilanjutkan uji dengan distribusi t dengan rumus:
(X1 – X2)
to =
√S12/n1 + S22/n2
Keterangan : X1 = Kadar rata-rata sampel 1
X2 = Kadar rata-rata sampel 2
S1 = Standar deviasi sampel 1
S2 = Standar deviasi sampel 2
n1 = Jumlah perlakuan sampel 1
BAB IV
HASIL DAN PEMBAHASAN
4.1 Kurva Kalibrasi
4.1.1 Kurva Kalibrasi Larutan Timbal dan Kadmium
Kurva kalibrasi timbal dan kadmium diperoleh dengan cara mengukur
absorbansi dari larutan baku timbal dan kadmium secara spektrofotometri
serapan atom, dengan nyala udara-asetilen pada panjang gelombang
masing-masing. Hasil pengukuran kurva kalibrasi untuk kedua logam tersebut
diperoleh persamaan garis regresi yaitu Y = 0,00637X + 0,0000528571 untuk
timbal dan Y = 0,0872X + 0,01305 untuk kadmium.
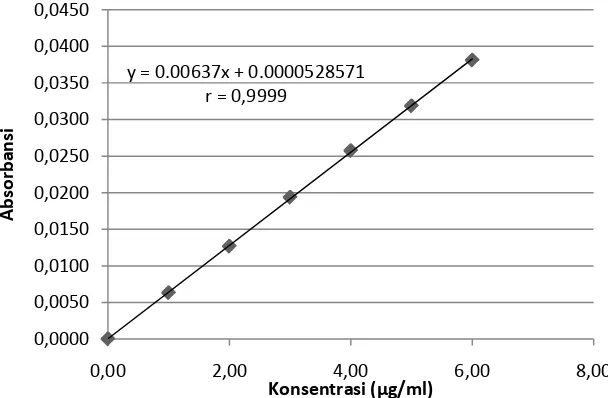
Kurva kalibrasi larutan baku timbal dapat dilihat pada Gambar 3 dan
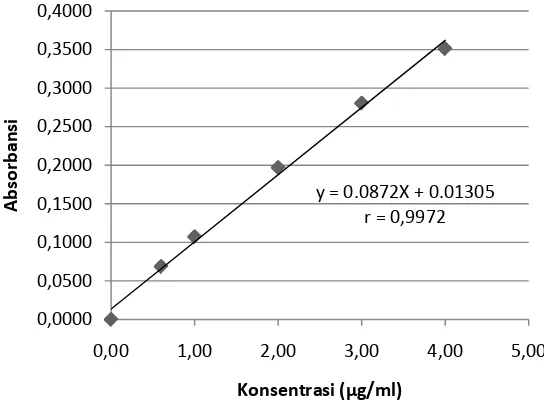
[image:40.595.154.458.466.665.2]kadmium pada Gambar 4.
Gambar 3. Kurva Kalibrasi Larutan Baku Timbal Keterangan:
X = Konsentrasi (µg/ml) Y = Absorbansi
y = 0.00637x + 0.0000528571 r = 0,9999
0,0000 0,0050 0,0100 0,0150 0,0200 0,0250 0,0300 0,0350 0,0400 0,0450
0,00 2,00 4,00 6,00 8,00
A
bso
rba
nsi
Keterangan:
X = Konsentrasi (µg/ml) Y = Absorbansi
Berdasarkan kurva di atas, diperoleh hubungan yang linear antara
konsentrasi dengan absorbansi. Dengan koefisien korelasi (r) timbal sebesar
0,9999 dan kadmium sebesar 0,9972. Nilai r ≥ 0,97 menunjukkan adanya
korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan
Y (absorbansi) (Miller, 2005). Data hasil pengukuran absorbansi larutan baku
timbal dan kadmium, perhitungan persamaan garis regresi serta koefisien
korelasi dapat dilihat pada Lampiran 6, halaman 41dan Lampiran 7, halaman
42-43.
4.1.2 Adsorben Yang Diperoleh Setelah Pengabuan
Sekam padi diabukan pada suhu 500°C masing-masing selama 5 jam
dan 15 jam. Berat abu sekam padi yang diperoleh dapat dilihat pada Tabel 2
dan 3.
y = 0.0872X + 0.01305 r = 0,9972
0,0000 0,0500 0,1000 0,1500 0,2000 0,2500 0,3000 0,3500 0,4000
0,00 1,00 2,00 3,00 4,00 5,00
A
bso
rba
nsi
[image:41.595.161.433.113.314.2]Konsentrasi (µg/ml)
Tabel 2. Berat abu sekam padi yang diperoleh setelah pengabuan sekam padi pada suhu 500°C selama 5 jam
No. Berat awal sekam
padi (gram) Berat abu sekam padi yang diperoleh
1. 3,330 0,6910
2. 3,330 0,6933
3. 3,330 0,6840
4. 3,340 0,6932
5. 3,348 0,7014
6. 3,421 0,7169
−
X 3,3498 0,6966
% Rata-rata campuran abu yang diperoleh= 20,80%
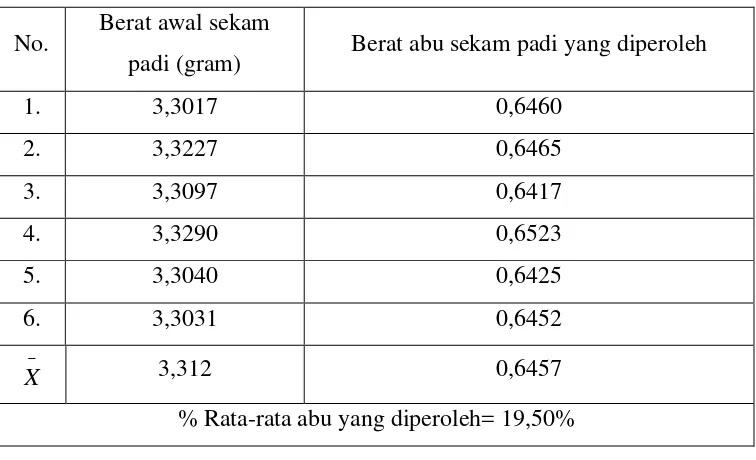
Tabel 3. Berat abu sekam padi yang diperoleh setelah pengabuan sekam padi pada suhu 500°C selama 15 jam
No. Berat awal sekam
padi (gram) Berat abu sekam padi yang diperoleh
1. 3,3017 0,6460
2. 3,3227 0,6465
3. 3,3097 0,6417
4. 3,3290 0,6523
5. 3,3040 0,6425
6. 3,3031 0,6452
−
X 3,312 0,6457
% Rata-rata abu yang diperoleh= 19,50%
Dari data di atas, diketahui bahwa berat rata-rata abu sekam padi yang
diperoleh dengan waktu pengabuan selama 5 jam adalah 20,80%, diperoleh
[image:42.595.119.497.426.656.2]adalah 1,3%. Sedangkan pengabuan selama 15 jam diperoleh rata-rata abu
sekam padi sebanyak 19,50%. Contoh perhitungan dapat dilihat pada Lampiran
8, halaman 44-45.
4.1.3 Analisis Timbal dan Kadmium Yang Diadsorpsi
Adsorben yang telah diperoleh kemudian dihaluskan dan diayak
menggunakan mesh 100, hal ini bertujuan untuk meningkatkan luas area
permukaan adsorben. Semakin luas area permukaan, maka makin banyak
tempat interaksi antara adsorben dan logam, ukuran dari adsorben akan
mempengaruhi kecepatan dari adsorpsi. Waktu kontak antara adsorben dan
adsorbat dilakukan selama 60 menit, hal ini berdasarkan bahwa kesetimbangan
adsorpsi logam degan berbagai adsorben tercapai setelah 60 menit
(Purwaningsih, 2009).
Berdasarkan orientasi yang telah dilakukan, diketahui bahwa adsorben
yang digunakan untuk mengadsorpsi logam kadmium lebih banyak dari pada
timbal. Pada penggunaan adsorben 0,2 gram terhadap larutan baku timbal dan
kadmium 10 µg/ml sebanyak 25 ml, kemampuan adsorbsi terhadap timbal
lebih besar dari pada kadmium; dan konsentrasi kadmium yang tersisa setelah
penambahan adsorben tidak memenuhi terhadap rentang konsentrasi dari
kurva kalibrasi. Maka adsorben yang pakai untuk mengadsorbsi logam timbal
sebanyak 0,2 gram, sedangkan kadmium sebanyak 0,4 gram.
Konsentrasi logam timbal dan kadmium tersebut ditentukan
berdasarkan persamaan garis regresi kurva kalibrasi larutan baku
masing-masing logam. Contoh perhitungan kadar yang diadsorpsi dapat dilihat pada
Kadar (mg/g) yang diadsorbsi oleh adsorben dapat dilihat pada Tabel 4
[image:44.595.121.498.192.409.2]dan Tabel 5.
Tabel 4. Kadar timbal yang diadsorpsi oleh sekam padi yang diabukan pada suhu 500°C selama 5 jam dan 15 jam.
Timbal
Sekam padi dengan pengabuan 5
jam
Sekam padi dengan pengabuan 15
jam
Kadar (mg/g) Kadar (mg/g)
0,9223 0,5919
0,8705 0,6649
0,9325 0,6105
0,9208 0,6721
0,8792 0,6578
0,9548 0,6179
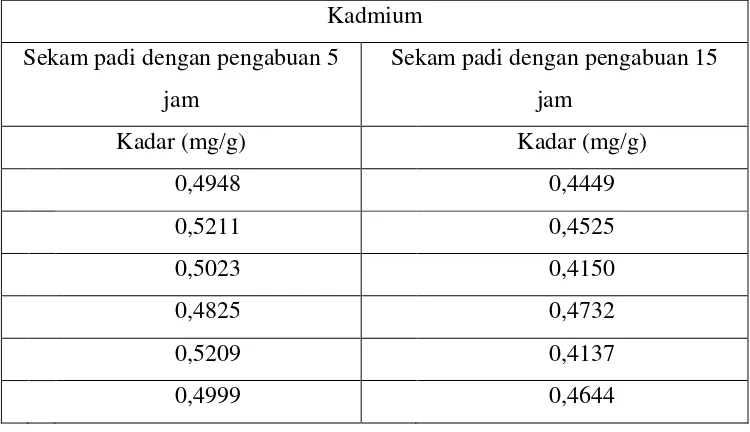
Tabel 5. Kadar kadmium yang diadsorpsi oleh sekam padi yang diabukan pada suhu 500°C selama 5 jam dan 15 jam.
Kadmium
Sekam padi dengan pengabuan 5
jam
Sekam padi dengan pengabuan 15
jam
Kadar (mg/g) Kadar (mg/g)
0,4948 0,4449
0,5211 0,4525
0,5023 0,4150
0,4825 0,4732
0,5209 0,4137
0,4999 0,4644
Analisis dilanjutkan dengan perhitungan kadar rata-rata timbal dan
[image:44.595.122.497.463.679.2]Lampiran 11, halaman 49-52 dan Lampiran 14, halaman 55-58). Kadar
[image:45.595.114.505.195.278.2]rata-rata timbal dan kadmium yang diadsorpsi dapat dilihat pada Tabel 6.
Tabel 6. Kadar rata-rata timbal dan kadmium yang diadsorpsi.
No. Adsorben Kadar Timbal
(mg/g)
Kadar Kadmium (mg/g)
1. SPD-5 jam 0,9134 ± 0,0532 0,5022 ± 0,0224
2. SPD-15 jam 0,6359 ± 0,0548 0,4433 ± 0,0402
Keterangan:
SPD-5 jam : Sekam padi yang diabukan selama 5 jam SPD-15 jam : Sekam padi yang diabukan selama 15 jam.
Data yang didapat kemudian diuji statistik untuk mengetahui beda nilai
rata-rata logam timbal dan kadmium yang diadsorpsi (Perhitungan dapat dilihat
pada Lampiran 15, halaman 59-60 dan Lampiran 16, halaman 61-62). Hasil
perhitungan statistik dapat dilihat pada Tabel 7.
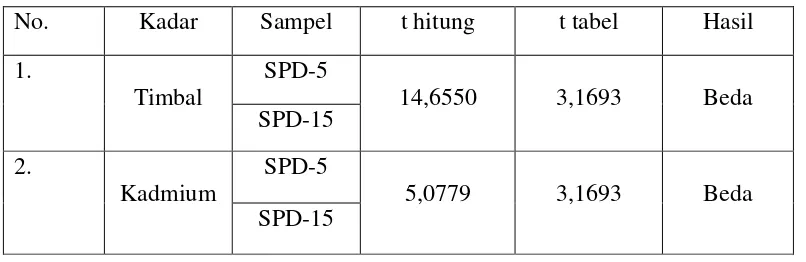
Tabel 7. Hasil uji beda nilai rata-rata logam timbal dan kadmium yang diadsorpsi.
No. Kadar Sampel t hitung t tabel Hasil
1.
Timbal
SPD-5
14,6550 3,1693 Beda
SPD-15
2.
Kadmium
SPD-5
5,0779 3,1693 Beda
SPD-15
Keterangan:
SPD-5 jam : Sekam padi yang diabukan selama 5 jam SPD-15 jam : Sekam padi yang diabukan selama 15 jam
Berdasarkan Tabel 7, diketahui bahwa terdapat perbedaan yang
[image:45.595.112.515.493.624.2]500°C selama 5 jam dan 15 jam terhadap kedua logam. Sekam padi yang
diabukan pada suhu 500°C selama 5 jam memiliki kemampuan adsorpsi yang
lebih baik.
Sekam padi yang diabukan pada suhu 500°C selama 5 jam
menghasilkan campuran berupa abu (berupa silika) dan karbon. Karbon yang
dihasilkan dapat bertindak sebagai adsorben. Silika bersifat inert, mempunyai
area permukaan yang luas (Kolasinski, 2007). Karbon yang diperoleh pada
pengabuan selama 5 jam, merupakan karbon yang teraktifasi secara fisik,
mempunyai kemampuan adsorpsi terhadap logam timbal dan kadmium. Jika
dibandingkan dengan persentase karbon aktif yang diperoleh hanya sebanyak
1,3%, tapi mempunyai kemampuan adsorpsi yang lebih baik jika dibandingkan
dengan adsorben yang mengandung silika saja.
Pemanasan adsorben dapat meningkatkan kemampuan penyerapan
terhadap larutan logam. Pemanasan dilakukan untuk memperbesar pori-pori
adsorben sehingga dapat meningkatkan efesiensi penyerapan. Sedangkan untuk
pemanasan yang lebih lama maka efesiensinya akan menurun. Pengabuan
sekam padi selama 15 jam menghasilkan menjadi abu (silika) secara
keseluruhan. Menurut Ramezanianpour, et al., (2009), bahwa lamanya waktu
pengabuan dapat mempengaruhi efektifitas dari silika. Dari hasil penelitian ini
diperoleh bahwa semakin lama waktu pengabuan, maka daya adsorpsi abu
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Kadar timbal serta kadmium yang diadsorpsi oleh abu sekam padi yang
diabukan selama 5 jam adalah 0,9134 mg/g dan 0,5022 mg/g.
Sedangkan kadar timbal dan kadmium yang diadsorpsi oleh sekam padi
yang diabukan selama 15 jam adalah 0,6359 mg/g dan 0,4433 mg/g.
b. Sekam padi yang diabukan pada suhu 500°C selama 5 jam mempunyai
kemampuan lebih baik dalam mengadsorpsi logam timbal dan
kadmium bila dibandingkan dengan sekam padi yang diabukan pada
suhu 500°C selama 15 jam.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk melanjutkan penelitian
penggunaan abu sekam padi sebagai adsorben logam timbal dan kadmium
DAFTAR PUSTAKA
Al-Anber, M.A. (2011). Thermodynamics Approach in the Adsorption of Heavy Metal. Dalam: Thermodynamics - Interaction Studies- Solid, Liquid and Gases. Editor: Juan Carlos Moreno Pirajain.
Astuti, A.D., Hadiwidodo, M., Oktiawan, W., dan Wahyudi, J. (2011). Penggunaan Abu Sekam Padi Sebagai Adsorben Limbah Logam Tembaga (Cu+2). Teknologi Indonesia. 34(2): 111.
Badan Pusat Statistik. (2012). Produksi Padi Indonesia
Diakses 12 Januari 2013.
Benjamin, M.M. (2002). Water Chemistry. New York: The McGraw Hill. Hal.
553-554.
Budiarto, E. (2004). Metodologi Penelitian Kedokteran. Jakarta: Penerbit Buku Kedokteran EGC. Hal. 46.
Danarto, Y.C., Nur, A., Setiawan, D.P., dan Kuncoro, N.D. (2010). Pengaruh Waktu Operasi Terhadap Karakterstik Char Hasil Pirolisis Sekam Padi Sebagai Bahan Pembuatan Nano Struktur Supermikrosporous Carbon.
Prosiding Seminar Nasional Teknik Kimia Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia. Yogyakarta. Hal. 1-2.
Darmono. (1995). Logam Dalam Sistem Biologi Makhluk Hidup. Jakarta: UI
Press. Hal. 5-7.
Darmono. (2001). Lingkungan Hidup dan Pencemaran, Hubungan dengan Toksikologi Senyawa Logam. Jakarta: UI Press. Hal. 137-146.
El-Said, A.G. (2010). Biosorption of Pb(II) Ion from Aqueous Solution Onto Rice Husk and Its Ash. Journal of American Science. 6(10): 144.
El-Said, A.G., Badawy, N.A., dan Garamon, S.E. (2012). Adsorption of Cadmium (II) and Mercury (II) onto Natural Adsorbent Rice Husk Ash (RHA) from aqueous Solution: Study in Singel and Binary System.
Farooq, U., Kozinski, J.A., Khan, M.A., dan Athar, M. (2010). Biosorption of Heavy Metal Ion Using Wheat Based Biosobent- A Review of the Recent Liteeature. Biosource Teghnology. 110: 5043-5045.
Gandjar, I.G., dan Rohman, A. (2008). Kimia Farmasi Analisis. Cetakan III. Yogyakarta: Pustaka Pelajar. Hal. 298, 305-307, 305-312, 319.
Hamid, H., dan Pramudyanto, B. (2007). Pengawasan Industri Dalam
Pengendalian Pencemaran Lingkungan. Jakarta: Granit. Hal. 1.
Hsu, H.W., dan Luh, B.S. (1980). Rice Hull. Dalam Rice Produck And
Utilization. Editor: Bor Shiun Luh. New York: Avi Publishing Company Inc. Hal. 736-740.
Igwe, J.C., dan Abia, A.A. (2007). Adsorption Isotherm Studies of Cd(II), Pb(II), and Zn(II) on Bioremediation from Aqueous Solution Using Unmodified and EDTA-Modified Maize Cob. Ecletica. 32(I): 33-34.
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry.
Penerjemah: Asmuwahyu Saptorahardjo. (2008). Konsep Dasar Kimia
Analitik. Jakarta: UI-Press. Hal. 275-277, 285.
Kolasinski, K.W. (2008). Surface Science: Foundation of Catalysis and
Nanoscience. Edisi ke-2. London: John Wiley & Sons Ltd. Hal. 22-23, 27.
LaGrega, M.D., Buckingham, P.L., dan Evans, J.C. (2001). Hazardous Waste
Mangement. Edisi ke-2. New York: McGraw Hill. Hal. 117, 196, 202, 478-479.
Madan, R.I., dan Tuli, G.D. (2007). Physical Chemistry. Edisi ke-4 Revisi. New Delhi: Rajendra Ravindra Printers (Pvt.) Ltd. Hal. 146.
Mdoe, J.E.G., dan Mkayula, L.L. (2002). Preparation And Characteritation Of Activated Carbon From Rice Husks And Shells Of Palm Fruits. Tanz. J. Sci: 28(2): 131-132.
Miller, J.H.M. (2005). System Suitability Test. Dalam: Method Validation in Pharmaceutical Analysis. Editor: Joachim Ermer dan John H. McB. Miller. Weinheim: Willey-Vch Verlag GmbH & Co. KGaA. Hal. 171.
Ngah, W.S., dan Hanafiah, M.A.K.M. (2008). Removal of Heavy Metal Ion from Waste Water by Chemical Modified Plants Wastes as Adsorbent: A review. Science Direct Bioresource Technology. 99: 3936.
Purwaningsih, D. (2009). Adsorpsi Multi Logm Ag (I), Pb(II), Cr (III), Cu (II) dan Ni (II) Pada Hibrida Etilendiamono-Silika Dari Abu Sekam Padi.
Jurnal Penelitian Saintek. 14(1): 6.
Ramezanianpour, A.A., Khani, M.M., dan Ahmadibeni, G. (2009). The Effect of Rice Husk Ash on Mechanical Properties and Durability of Sustainable Concrete. International Journal of Civil Engineering. 7(2): 86.
Selwood, P.W. (1962). Adsorption and Collective Paramagnetism. New York:
Academic Press. Hal. 1-2.
Sembodo, B.S.T. (2005). Isoterm Kesetimbangan Adsorsi Timbal Abu Sekam Padi. Ekuilibrium. 4(2): 101.
Shukla, S.P. (2011). Investigation In to Tribo Potential of Rice Husk (RH) Char Reinforced Epoxy Composite. Thesis. Rourkela: National Institute of Technology Rourkela.
Soegianto, A. (2004). Metode Pendugaan Pencemaran Perairan Dengan
Indikator Biologi. Cetkan I. Surabaya: Air Langga Press. Hal. 1.
Sonmezay, A., Salim, O.M., dan Nihal, B. (2012). Adsorption of Lead and Cadmium Ions From Aqueous Solution Using Manganoxide Minerals.
ScienceDirect: Trans. Nonferrous Met. Soc. China. 22(4): 3136.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Hal. 93, 168, 239, 241, 249.
Tarley, C.R.T., dan Arruda, M.A.Z. (2004). Biosorption of Heavy Metal Using Rice Milling By-Produck, Characterisation and Application for Removal of Metal from Aqueos Effluents. Elsevier Chemosphere. 54: 988.
Watson, G. (2005). Pharmaceutical Analysis: A Textbook for Pharmacy
Students and Pharmaceutical Chemists. Penerjemah: Winny R. Syarief.
(2010). Analisis Farmasi. Jakarta: Penerbit Buku Kedokteran EGC.
Widwiastuti, H., Mulyasuryani, A., dan Sabarudin, A. (2013). Extraction of
Pb+2 Using Silica From Rice Husk Ash (RHA) – Chitosan As Solid
Lampiran 1. Gambar sekam padi
Gambar sekam padi
Lampiran 2. Adsorben sekam padi yang diabukan pada suhu suhu 5000C selama 5 jam dan 15 jam
Gambar Sekam Padi Setelah Pengabuan 5 jam Pada Suhu 5000C
[image:53.595.202.429.428.618.2]Lampiran 3. Bagan alir proses pembuatan adsorben Sekam Padi
Ditimbang sebanyak 3,3 gram
Diabukan dengan temperatur awal 100◦C dan
perlahan – lahan temperatur dinaikkan hingga
suhu 500◦C dengan interval 25◦C setiap 5
menit
Digerus
Diayak dengan ayakan mesh 100
Hasil
Dilakukan selama 5 jam dan 15 jam
Abu
Dicuci dengan air Dibilas dengan akuades
Dikeringkan di udara terbuka dan dioven selama 24 jam pada suhu 1100 C
Dihaluskan dengan blander
Lampiran 4. Bagan alir proses pengukuran logam timbal yang tersisa setelah penambahan adsorben
Larutan Uji Logam Timbal 10 µg/ml
Dipipet sebanyak 25 ml
Dimasuk kan ke dalam erlemeyer 100 ml
Dipindahkan ke dalam labu tentukur 50 ml, dibiladibila
Ditambahkan Adsorben sebanyak 0,2 gram
Diaduk dengan mini orbital shaker dengan kecepatan 150 rpm selama 60 menit
Filtrat
Disaring dengan kertas Whatman no. 42 dan dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan pengukuran kadar timbal yang tersisa dengan spektrofotometer serapan atom pada panjang gelombang 283,3 nm
Lampiran 5. Bagan alir proses pengukuran logam kadmium yang tersisa setelah penambahan adsorben
Larutan Uji Logam Kadmium 10 ppm
Dipipet sebanyak 25 ml
Dimasuk kan ke dalam erlemeyer 100 ml
Dipindahkan ke dalam labu tentukur 50 ml, dibiladibila
Ditambahkan Adsorben sebanyak 0,4 gram
Diaduk dengan mini orbital shaker dengan kecepatan 150 rpm selama 60 menit
Filtrat
Disaring dengan kertas Whatmen no. 42 dan dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan pengukuran kadar Kadmium yang tersisa dengan spektrofotometer serapan atom pada panjang gelombang 228,8 nm
Lampiran 6. Data hasil pengukuran absorbansi larutan standar timbal dan kadmium
A. Larutan standar timbal
No. Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1. 0,0000 0,00003
2. 1,0000 0,00633
3. 2,0000 0,01269
4. 3,0000 0,01938
5. 4,0000 0,02574
6. 5,0000 0,03185
7. 6,0000 0,03812
B. Larutan standar kadmium
No. Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1. 0,0000 -0,0001
2. 0,6000 0,0686
3. 1,0000 0,1073
4. 2,0000 0,1969
5. 3,0000 0,2804
Lampiran 7. Perhitungan persamaan garis regresi dan koefisien korelasi (r)
A. Timbal
No. X Y XY X2 Y2
1. 0,0000 0,00003 0,0000 0,0000 9,0000 X 10-10
2. 1,0000 0,00633 0,00633 1,0000 4,0068 X 10-5
3. 2,0000 0,01269 0,02538 4,0000 1,6103 X 10-4
4. 3,0000 0,01938 0,05814 9,0000 3,7558 X 10-4
5. 4,0000 0,02574 0,10296 16,000 6,6254 X 10-4
6. 5,0000 0,03185 0,15925 25,000 1,0144 X 10-3
7. 6,0000 0,03812 0,22872 36,000 1,4531 X 10-3
∑ 21,0000 0,13414 0,58078 91,0000 3,7068 X 10-3
X = 3,0000
Y=
0,019162857
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)
(
21,0000)
/7 0000 , 91 7 / ) 13414 , 0 ( 0000 , 21 58078 , 0 2 − − = 0,00637Y = a X + b
b = Y − aX
= 0,019162857 – (0,00637)(3,0000)
= 0,0000528571
Maka persamaan garis regresinya adalah: Y = 0,00637X + 0,0000528571
=
(
)(
)
(
)
B. Kadmium
No. X Y XY X2 Y2
1. 0,0000 -0,0001 0,00000 0,0000 0,00000001
2. 0.6000 0,0686 0,04116 0.3600 0,00470596
4. 1,0000 0,1073 0,10730 1,0000 0,01151329
5. 2,0000 0,1969 0,39380 4,0000 0,03876961
6. 3,0000 0,2804 0,84120 9,0000 0,07862416
7. 4,0000 0,3509 1,40360 16,000 0,12313081
∑ 10.6 1,0031 2,78706 30,36 0,256745
X = 1,76666 Y=0,16718
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)(
)
(
10,6000)
/6 3600 , 30 6 / 0031 , 1 600 , 10 78706 , 2 2 − − = 0,0872Y = a X + b
b = Y − aX
= 0,16718 – (0,0872)( 1,76666) = 0,01305
Maka persamaan garis regresinya adalah: Y = 0,0872X + 0,01305
=
(
)(
)
(
)
Lampiran 8. Contoh perhitungan jumlah abu dan karbon yang tersisa setelah pengabuan sekam padi
Berat abu sekam padi yang diperoleh setelah pengabuan sekam padi pada suhu 500°C selama 5 jam
No. Berat awal sekam padi
(gram) Berat abu sekam padi yang diperoleh
1. 3,330 0,6910
2. 3,330 0,6933
3. 3,330 0,6840
4. 3,340 0,6932
5. 3,348 0,7014
6. 3,421 0,7169
−
X 3,3498 0,6966
% Rata-rata campuran abu yang diperoleh= 20,80 %
% Rata-rata kehilangan bobot sekam padi
= (Berat awal sekam padi – Berat abu sekam padi setelah pengabuan) X 100 %
Berat awal sekam padi
= 100%
3498 , 3
6966 , 0 3498 , 3
× −
= 79,20 %
% Abu yang diperoleh
=100 % - 79,20%
Berat abu sekam padi yang diperoleh setelah pengabuan sekam padi pada suhu 500°C selama 15 jam
No. Berat awal sekam padi
(gram) Berat abu sekam padi yang diperoleh
1. 3,3017 0,6460
2. 3,3227 0,6465
3. 3,3097 0,6417
4. 3,3290 0,6523
5. 3,3040 0,6425
6. 3,3031 0,6452
−
X 3,312 0,6457
% Rata-rata abu yang diperoleh= 19,50 %
% Kehilangan berat sekam padi
= Berat awal sekam padi – Berat abu sekam padi setelah pengabuan X 100 %
Berat awal sekam padi
= 100%
312 , 3
6457 , 0 312 , 3
× −
= 80,50 %
% Abu rata-rata yang diperoleh
= 100 % - 80,50 %
= 19, 50 %
% Karbon yang terdapat dari sisa pengabuan
= % Abu sekam padi selam 5 jam - % Abu sekam padi selama 15 jam
= 20,50 % - 19,50 %