SKRIPSI
MODIFIKASI PENGASAMAN KIMIAWI DALAM PEMBUATAN TEMPE YANG DIDASARKAN PADA ASPEK CITARASA
oleh
MARIA DEWI P. T. GUNAWAN P. F24101125
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Maria Dewi Puspitasari Tirtaningtyas Gunawan Putri. F24101125. Modifikasi Pengasaman Kimiawi dalam Pembuatan Tempe yang Didasarkan pada Aspek Citarasa. Di bawah bimbingan Hanny Wijaya dan Harsi D. Kusumaningrum.
RINGKASAN
Pengasaman merupakan salah satu tahap penting dalam pembuatan tempe yang dilakukan untuk menghambat pertumbuhan mikroba pembusuk dan patogen serta memberikan kondisi optimum pertumbuhan kapang. Pengasaman alami dilakukan dengan perendaman kedelai dalam air selama semalam. Air rendaman kedelai hasil pengasaman alami sering menimbulkan masalah lingkungan yang cukup serius. Pengasaman alami dapat digantikan dengan pengasaman kimiawi, namun penggunaan asam dalam bahan pangan mempengaruhi citarasa. Penelitian ini bertujuan untuk mencari metode pengasaman kimiawi untuk menggantikan metode pengasaman tradisional tanpa menurunkan kualitas citarasa tempe yang dihasilkan.
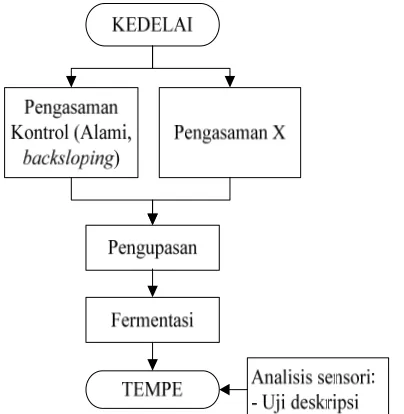
Penelitian ini terdiri atas empat tahap yaitu seleksi awal metode pengasaman kimiawi, modifikasi proses pengasaman, modifikasi jenis pengasam, dan perbaikan citarasa metode pengasaman kimiawi terpilih. Seleksi awal memilih metode pengasaman terbaik dari metode-metode pengasaman yang sudah pernah dilakukan oleh peneliti lain. Berdasarkan skor kesukaan dan hasil pengamatan subjektif, metode pengasaman terpilih adalah pengasaman yang dilakukan dengan perebusan kedelai di dalam asam laktat 0.85% selama 30 menit. Karakterisasi citarasa tempe pengasaman laktat menunjukkan perlunya pengembangan metode pengasaman untuk menekan atribut rasa asam.
Modifikasi proses pengasaman pada dasarnya merupakan usaha untuk mereduksi residu asam laktat pada akhir pengasaman. Modifikasi proses pengasaman yang terpilih adalah pengasaman yang dilakukan dengan perebusan kedelai di dalam asam laktat 0.85% selama 30 menit dilanjutkan dengan perebusan kedelai dalam air bersih selama 20 menit. Pengamatan subjektif, uji afektif, dan uji deskriptif menunjukkan bahwa citarasa tempe yang dihasilkan dari pengasaman ini kurang memuaskan sehingga dilakukan pengembangan metode pengasaman lebih lanjut dengan modifikasi jenis pengasam.
Modifikasi jenis pengasam pada dasarnya merupakan substitusi asam laktat dengan bahan pengasam lain yang memiliki rasa lebih netral. Bahan pengasam yang diuji adalah asam fosfat, asam malat, bahan pengasam X serta kombinasi dari asam laktat, asam asetat, dan asam sitrat. Berdasarkan karakteristik visual dan citarasa hasil pengamatan subjektif, tempe yang terpilih pada tahap modifikasi jenis pengasam adalah tempe pengasaman X. Tempe pengasaman X termasuk dalam kelompok tempe dengan skor kesukaan paling tinggi dan karakter citarasa keseluruhan tidak berbeda nyata dengan tempe kontrol.
MODIFIKASI PENGASAMAN KIMIAWI DALAM PEMBUATAN TEMPE YANG DIDASARKAN PADA ASPEK CITARASA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
MARIA DEWI P. T. GUNAWAN P. F24101125
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
BOGOR
FAKULTAS TEKNOLOGI PERTANIAN
MODIFIKASI PENGASAMAN KIMIAWI DALAM PEMBUATAN TEMPE YANG DIDASARKAN PADA ASPEK CITARASA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
MARIA DEWI P. T. GUNAWAN P. F24101125
Dilahirkan pada tanggal 6 Juli 1984 di Semarang
Tanggal Lulus: ...
Menyetujui
Bogor, 2006
Dr. Ir. Harsi D. Kusumaningrum, MSc. Dosen Pembimbing II
Prof. Dr. Ir. C. Hanny Wijaya, MAgr. Dosen Pembimbing I
Diketahui
Dr. Ir. Dahrul Syah, MSc.
RIWAYAT HIDUP
Penulis dilahirkan di Semarang pada tanggal 6 Juli 1984 sebagai putri ketiga dalam tiga bersaudara dari ayah Drs. Ranu Gunawan Uripwibowo, MBA dan ibu Emmy Susanti Widjajanti. Penulis lulus dari SMU Kolese Loyola Semarang pada tahun 2001 dan pada tahun yang sama lulus Ujian Masuk Perguruan Tinggi Negeri IPB untuk jurusan Teknologi Pangan dan Gizi yang kemudian dikenal dengan nama Departemen Ilmu dan Teknologi Pangan.
Penulis terlibat dalam beberapa kegiatan organisasi selama masa studi di IPB, yaitu Kemaki 2002, NSPC 2004, dan kepanitiaan lainnya. Pada tahun 2003, penulis memenangkan The 2nd National Student Paper Competition IPB sebagai juara II dan pada tahun 2004 memperoleh beasiswa untuk mengikuti program Hokkaido University Short Term Exchange Program selama 11 bulan di kota Sapporo, Hokkaido, Jepang.
PRAKATA
Penulis memanjatkan rasa syukur kepada Allah Bapa di surga atas segala rahmat-Nya selama penulis menyelesaikan skripsi ini. Skripsi ini disusun berdasarkan penelitian yang dilakukan di laboratorium ITP, laboratorium SEAFAST, dan pengrajin tempe Warung Jambu selama lima bulan, yaitu dari Mei 2006-September 2006
Penulis menyadari bahwa penelitian ini dapat diselesaikan karena bantuan, kerja sama, dan dukungan banyak pihak. Penulis ingin mengucapkan terima kasih kepada:
1. Prof. Dr. Ir. C. Hanny Wijaya, MAgr. dan Dr. Ir. Harsi D. Kusumaningrum, MSc. selaku pembimbing yang telah memberikan banyak masukan, pencerahan, dan dukungan terhadap penulis.
2. Ir. Budi Nurtama, MAgr. selaku dosen penguji atas waktu yang diberikan untuk mendiskusikan rancangan percobaan dan pengolahan data.
3. Para pengrajin tempe Sukasari yang telah mengijinkan penulis untuk mendapatkan pengetahuan dan pengalaman produksi tempe serta masukan yang telah diberikan termasuk ide yang melandasi penelitian ini.
4. Fierminich dan Dio atas bantuan flavor yang diberikan.
5. Bu Tati atas pertemanan, konsultasi, sikap keibuan yang telah diberikan selama pengujian bersama.
6. CAMO Software Asia Pvt. Ltd. atas ijin penggunaan perangkat lunak The
Unscrambler® 8.0.
7. Inggrid, Pretty, Karen, Steisi, Fenni, Shinta, Eva, Randy, Mumus, Herold, Uli, Inda sebagai panelis terlatih dan panelis-panelis tidak terlatih lain yang bersedia meluangkan waktu dan tenaga dalam begitu banyak uji-uji organoleptik.
8. Pak Rozak, Mas Edi, Pak Mul, Mbak Sri, Mbak Ari, Pak Koko, Pak Wachid, Pak Taufik, Teh Ida, Pak Solikin, Pak Sobirin atas segala bantuan, keramahan, dan canda tawa di laboratorium.
penelitian. Terutama ooh yang selalu memberikan kata-kata positif dan dukungan serta menjadi tempat mengeluh kala-kala mati lampu saat mengetik. 10. Pustakawan di perpustakaan Fateta dan perpustakaan PAU atas segala layanan
literatur dan fotokopian.
11. Teman-teman kost di Perwira 12, terutama Inge, Felis, Hadi, Kak Sapto, Kak Nona, dan Kak Meis.
12. Herold, Aponk, Vivi, Maya atas kebersamaan kita dalam penelitian dan bimbingan.
13. Inggrid, Pretty, Karen, Steisi, Herold, Tukep, Mel, Fenni atas waktu-waktu yang menyenangkan di L2.
14. Para pendamping yang telah memberikan banyak doa dan dukungan selama penelitian.
15. Seluruh pihak lain yang terlibat dalam memberikan dukungan dalam penyelesaian karya ilmiah ini.
Semoga skripsi ini menjadi salah satu karya ilmiah yang bermanfaat.
DAFTAR ISI
PRAKATA ... iii
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
I. PENDAHULUAN A. LATAR BELAKANG ... 1
B. TUJUAN PENELITIAN ... 3
II. TINJAUAN PUSTAKA A. TEMPE ... 4
B. TEKNOLOGI PEMBUATAN TEMPE ... 5
C. CITARASA TEMPE ... 8
D. PENGASAMAN ALAMI ... 9
E. LIMBAH INDUSTRI TEMPE ... 12
F. PENGASAMAN KIMIAWI ... 14
G. ANALISIS SENSORI ... 19
1. Uji Diskriminatif ... 20
2. Uji Deskriptif ... 23
3. Uji Afektif ... 25
H. PRINCIPAL COMPONENT ANALYSIS (PCA) ... 26
III. METODOLOGI PENELITIAN A. ALAT DAN BAHAN ... 28
B. METODE PENELITIAN ... 28
1. Seleksi Awal Metode Pengasaman Kimiawi ... 30
2. Modifikasi Proses Pengasaman ... 31
3. Modifikasi Jenis Pengasam ... 33
4. Reduksi Atribut Aroma Langu Tempe Pengasaman X ... 34
C. ANALISIS SENSORI ... 35
1. Uji Afektif ... 35
3. Uji Deskripsi ... 36
a. Persiapan panelis terlatih ... 36
b. Pengujian produk ... 38
c. Pengolahan data ... 39
IV. HASIL DAN PEMBAHASAN A. TEKNOLOGI PEMBUATAN TEMPE ... 41
B. SELEKSI AWAL METODE PENGASAMAN KIMIAWI ... 44
C. MODIFIKASI PROSES PENGASAMAN ... 47
D. MODIFIKASI JENIS PENGASAM ... 51
E. REDUKSI ATRIBUT AROMA LANGU TEMPE PENGASAMAN X ... 55
F. KARAKTERISTIK CITARASA TEMPE PENGASAMAN KIMIAWI TERPILIH ... 59
V. KESIMPULAN DAN SARAN A. KESIMPULAN ... 63
B. SARAN ... 64
DAFTAR TABEL
Tabel 1. Komposisi rata-rata air rendaman kedelai... 13 Tabel 2. Bahan pengasam yang digunakan sebagai bahan tambahan
pangan dan karakteristiknya ... 19 Tabel 3. Larutan sampel dalam penentuan rasa dasar ... 37 Tabel 4. Deskriptor yang digunakan dalam pengenalan aroma standar ... 38 Tabel 5. Standar citarasa yang digunakan dalam pengujian akhir QDA .... 39 Tabel 6. Hasil pengamatan subjektif pada tahap seleksi pengasaman
kimiawi ... 45 Tabel 7. Hasil pengamatan subjektif pada tahap modifikasi proses
pengasaman ... 49 Tabel 8. Bahan pengasam yang digunakan untuk modifikasi jenis
pengasam ... 52 Tabel 9. Hasil pengamatan subjektif pada tahap modifikasi jenis
pengasam ... 53 Tabel 10. Hasil pengamatan subjektif pada tahap reduksi aroma langu
DAFTAR GAMBAR
Gambar 1. Beberapa metode pembuatan tempe tradisional ... 7
Gambar 2. Bagan alir teknologi pembuatan tempe pengrajin tempe Sukasari ... 29
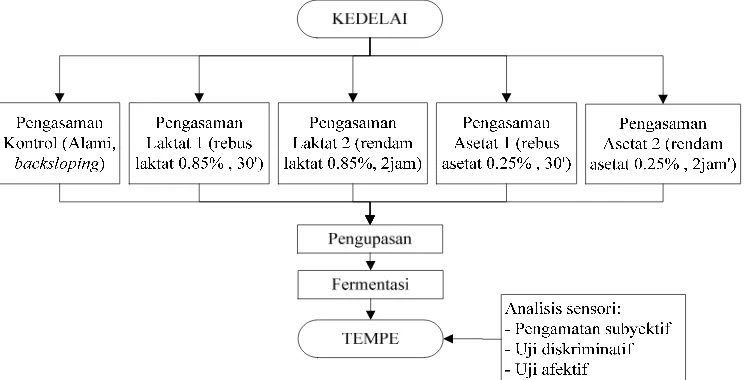
Gambar 3. Seleksi awal metode pengasaman kimiawi ... 31
Gambar 4. Karakterisasi citarasa tempe laktat 1 ... 31
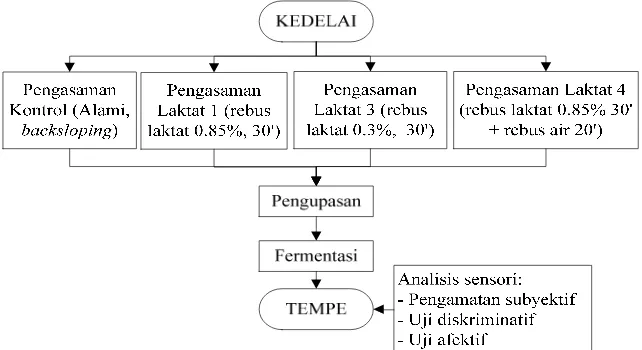
Gambar 5. Seleksi modifikasi proses pengasaman ... 32
Gambar 6. Karakterisasi citarasa tempe laktat 4 ... 32
Gambar 7. Seleksi modifikasi jenis pengasam ... 33
Gambar 8. Karakterisasi citarasa tempe pengasaman X ... 34
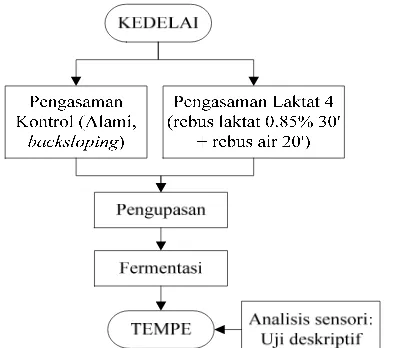
Gambar 9. Pengolahan untuk reduksi aroma langu tempe pengasaman X ... 35
Gambar 10. Air rendaman usia 22 jam dan kedelai prefermentasi ... 42
Gambar 11. Pembuangan limbah cair tempe pengrajin tempe Gg. Wahir ... 43
Gambar 12. Spider web tempe laktat 1 dan tempe kontrol ... 47
Gambar 13. Spider web tempe laktat 4, tempe laktat 1, dan tempe kontrol .... 50
Gambar 14. Spider web tempe pengasaman X dan tempe kontrol ... 54
Gambar 15. Spider web tempe pengolahan X2, pengolahan X1, dan tempe kontrol ... 56
Gambar 16. Spider web tempe pengolahan X3, pengolahan X1, dan tempe kontrol ... 57
Gambar 17. Grafik residual variance komponen utama citarasa tempe pengasaman kimiawi terpilih ... 60
Gambar 18. Grafik plot scores PC1 dan PC2 ... 60
Gambar 19. Grafik plot x-loading PC1 dan PC2 ... 61
DAFTAR LAMPIRAN
Lampiran 1. Contoh formulir uji kesukaan ... 69
Lampiran 2. Contoh formulir simple different test ... 70
Lampiran 3. Contoh formulir uji penentuan rasa dasar ... 71
Lampiran 4. Contoh formulir uji segitiga rasa... 72
Lampiran 5. Contoh formulir uji deskripsi aroma ... 73
Lampiran 6. Contoh formulir uji segitiga aroma ... 74
Lampiran 7. Contoh formulir pengenalan standar aroma ... 75
Lampiran 8. Contoh formulir pelatihan penskalaan ... 76
Lampiran 9. Contoh formulir pelatihan intensitas rasa ... 77
Lampiran 10. Contoh formulir pelatihan intensitas aroma ... 78
Lampiran 11. Contoh formulir quantitative descriptive analysis rasa ... 79
Lampiran 12. Contoh formulir quantitative descriptive analysis aroma ... 80
Lampiran 13. Contoh formulir quantitative descriptive analysis tekstur ... 81
Lampiran 14. Data uji simple different test pada tahap seleksi pengasaman kimiawi ... 82
Lampiran 15. Analisis data uji simple different test pada tahap seleksi pengasaman kimiawi ... 83
Lampiran 16. Data uji kesukaan pada tahap seleksi pengasaman kimiawi ... 84
Lampiran 17. Analisis data uji kesukaan pada tahap seleksi metode pengasaman kimiawi ... 85
Lampiran 18. Data uji simple different test pada tahap modifikasi proses pengasaman ... 87
Lampiran 19. Analisis data uji simple different test pada tahap modifikasi proses pengasaman ... 88
Lampiran 20. Data uji kesukaan pada tahap modifikasi proses pengasaman ... 89
Lampiran 21. Analisis data uji kesukaan pada tahap modifikasi proses pengasaman ... 90
Lampiran 22. Data uji simple different test pada tahap modifikasi jenis pengasam ... 92
Lampiran 23. Analisis data uji simple different test pada tahap modifikasi jenis pengasam ... 93
Lampiran 26. Data uji kesukaan pada tahap reduksi atribut aroma langu tempe
pengasaman X ... 97
Lampiran 27. Analisa data uji kesukaan pada tahap reduksi atribut aroma langu tempe pengasaman X ... 98
Lampiran 28. Data QDA tempe kontrol ... 100
Lampiran 29. Data QDA tempe laktat 1 ... 101
Lampiran 30. Data QDA tempe laktat 4 ... 102
Lampiran 31. Data QDA tempe pengasaman X/pengolahan X1 ... 103
Lampiran 32. Data QDA tempe pengolahan X2 ... 104
Lampiran 33. Data QDA tempe pengolahan X3 ... 105
I. PENDAHULUAN
A. LATAR BELAKANG
Tempe didefinisikan sebagai suatu massa hasil fermentasi kapang
dengan bahan baku biji-bijian yang terikat bersama oleh miselium kapang
tersebut (Nout dan Kiers, 2005). Pada umumnya tempe Indonesia terbuat dari
kedelai sehingga orang cenderung menyebut tempe kedelai dengan tempe saja
(Yeong, 1999).
Teknologi pembuatan tempe seperti halnya teknologi pembuatan
makanan tradisional lainnya berkembang secara turun temurun, dari mulut ke
mulut dan berubah karena pengalaman. Meskipun demikian, ada hal-hal dasar
yang diterapkan oleh semua pengrajin, salah satunya adalah pentingnya
pengasaman kedelai sebelum inokulasi kultur starter (Hermana & Karmini,
1996).
Pengasaman kedelai dalam pembuatan tempe memberikan kontribusi
terhadap keamanan dan penerimaan tempe yang dihasilkan. Fungsi utama
proses pengasaman adalah mendukung pertumbuhan kapang dan menghambat
pertumbuhan beberapa bakteri patogen dan pembusuk (Kuswanto, 2004).
Pengasaman kedelai di Indonesia umumnya dilakukan secara alami
dengan perendaman kedelai selama semalam pada suhu 28-31oC, yang merupakan suhu ruang di negara tropis, sampai air rendaman berbusa dan
berbau asam (Yeong et al., 1999). Proses pengasaman alami merupakan
proses biologis yang mengubah komponen dalam kedelai serta mempengaruhi
citarasa, daya cerna, nilai gizi dan daya simpan tempe yang dihasilkan
(Hermana & Karmini, 1996).
Bakteri asam laktat (BAL) yang mendominasi selama pengasaman
alami menghasilkan asam-asam organik yang menghambat pertumbuhan
patogen dan mikroba pembusuk pada tempe. Proses perendaman juga
menurunkan zat-zat inhibitor pertumbuhan kapang sehingga memberikan
kondisi pertumbuhan kapang yang lebih baik (Kuswanto, 2004).
Permasalahan yang sering timbul dalam proses pembuatan tempe
alami seringkali menyebabkan masalah lingkungan yang cukup serius. Hal ini
terutama karena sampai saat ini pembuangannya dilakukan begitu saja oleh
sebagian besar pengrajin tempe (Yeong et al., 1999). Limbah cair hasil
perendaman bersifat asam (Liu, 1997), mempunyai bau yang asam serta
banyak mengandung bahan-bahan organik terlarut dan bakteri penghasil asam
laktat seperti Lactobacillus sp. serta bakteri lain seperti bakteri pembusuk
(Yeong et al., 1999).
Survei di empat pengrajin tempe di daerah Bogor (Sukasari, Cimanggu,
Caringin, dan Warung Jambu) menunjukkan bahwa limbah cair industri tempe
yang berasal dari air rendaman hasil pengasaman alami dicirikan sebagai
larutan kental, kuning keruh, berbuih yang memiliki bau asam yang tajam.
Karena pengolahan limbah belum diterapkan di keempat pengrajin tempe
tersebut, beberapa dari para pengrajin tersebut mengakui bahwa masyarakat
sekitar masih mengeluhkan kualitas air yang dicemari oleh limbah cair
industri tempe tersebut.
Steinkraus et al. (1965) serta Nout dan Kiers (2005) menyatakan bahwa
pengasaman alami dapat digantikan dengan pengasaman kimiawi. Seperti
limbah cair hasil perendaman alami, limbah hasil pengasaman kimiawi
memiliki keasaman yang tinggi sehingga bersifat korosif dan dapat
menyebabkan pengkaratan pada pipa-pipa besi (Fardiaz, 1992). Namun
demikian limbah hasil pengasaman kimiawi dapat digunakan kembali sebagai
bahan pengasam untuk proses pengasaman berikutnya. Selain itu, limbah hasil
pengasaman kimiawi tidak mengandung bahan organik dan mikroorganisme
sebanyak limbah cair hasil perendaman alami (Yeong et al., 1999) yang
menghabiskan oksigen terlarut dalam air. Suplai oksigen yang menurun akan
mengganggu keseimbangan ekologi air (Jenie dan Rahayu, 1989).
Pengasaman kimiawi ini pada mulanya dikembangkan untuk pembuatan
tempe di negara beriklim sub tropis (Liu, 1997). Di negara beriklim subtropis,
karena suhu lingkungan yang terlalu rendah untuk memicu aktivitas
fermentasi BAL, pengasaman alami selama perendaman ini tidak terjadi atau
berlangsung sangat lambat (Liu, 1997). Pengasaman kimiawi menguntungkan
hingga 2-3 jam bila dibandingkan dengan cara tradisional yang membutuhkan
waktu perendaman 20-30 jam (Hermana dan Karmini, 1996).
Steinkraus et al. (1965) mengemukakan tentang proses pengasaman
kimiawi yang dilakukan dengan perendaman dalam larutan asam laktat 0.85%
selama 2 jam pada suhu 25oC dan 30 menit pada suhu 100oC. Sedangkan Nout dan Kiers (2005) menyatakan bahwa asam asetat hingga konsentrasi 0.25%
juga umum digunakan dalam pengasaman kimiawi.
Doores (1983) mengemukakan bahwa penggunaan bahan pengasam
dapat mempengaruhi citarasa bahan pangan. Citarasa didefinisikan sebagai
persepsi yang diterima oleh alat indera dari produk yang terletak di dalam
mulut. Berdasarkan definisi tersebut, yang termasuk di dalamnya adalah
aroma, rasa, faktor stimulasi kimia dan mouthfeel (Meilgaard et al., 1999;
Civille dan Lyon, 1996).
Bahan pengasam pada umumnya berkontribusi terhadap rasa asam dan
getir dari produk. Bahan pengasam dan hubungannya dengan citarasa
seringkali membatasi penggunaannya dalam bahan pangan. Penggunaan bahan
pengasam harus menyeimbangkan antara kepentingannya sebagai senyawa
antimikroba dengan karakteristik citarasa yang dimilikinya pada suatu
konsentrasi (Doores, 1990).
B. TUJUAN PENELITIAN
Penelitian ini bertujuan untuk mencari metode pengasaman kimiawi
yang mampu menggantikan metode pengasaman alami tanpa menurunkan
II. TINJAUAN PUSTAKA
A. TEMPE
Tempe didefinisikan sebagai suatu massa hasil fermentasi kapang
dengan bahan baku biji-bijian yang terikat bersama oleh miselium kapang
tersebut (Nout dan Kiers, 2005). Tempe juga diklasifikasikan sebagai salah
satu contoh produk fermentasi kacang-kacangan dan/atau serealia yang
menghasilkan protein nabati bertekstur pengganti daging (Steinkraus, 2002).
Tempe dihasilkan dengan pemasakan dan pengupasan kedelai serta
inokulasi beberapa galur Rhizopus yang berbeda (R. oligosporus, R. oryzae,
dan R. stolonifer). Fermentasi tempe merupakan fermentasi kultur padat yang
melibatkan kapang, bakteri, dan khamir (Denter et al., 1998). Tempe yang
baik dicirikan oleh permukaan yang ditutupi oleh miselium kapang secara
merata, kompak dan berwarna putih, antara butiran kacang atau serealia
dipenuhi oleh miselium dengan ikatan yang kuat dan merata sehingga bila
diiris tempe tersebut tidak hancur (Yeong et al., 1999).
Fermentasi pada tempe merupakan jenis fermentasi yang dilakukan
untuk meningkatkan kualitas nilai gizi dan karakter organoleptik (Nout dan
Kiers, 2005). Tempe Indonesia pada umumnya terbuat dari kedelai. Tempe
yang dibahas pada penulisan selanjutnya adalah tempe yang terbuat dari
kacang kedelai.
Brata-Arbai (1996) menyatakan bahwa tempe memiliki beberapa
keunggulan dibandingkan dengan kedelai. Isoflavon kedelai yang dilaporkan
dapat mencegah carcinoma payudara manusia dan sel kanker lambung
meningkat jumlahnya pada tempe (Wang dan Murphy, 1996). Komponen
isoflavon tempe yang lain, asam 3-hidroksiantranilat (HAA), efektif dalam
mencegah autooksidasi kedelai dan memiliki aktivitas antioksidatif yang
tinggi baik di dalam air, alkohol, maupun membran eritrosit. HAA tidak
ditemukan dalam kedelai namun diproduksi selama inkubasi Rhizopus
oligosporus. Tempe sangat stabil terhadap ketengikan. Minyak mentah yang
terhadap oksidasi daripada minyak yang diekstrak dari kedelai (Esaki et al.,
1996).
Fermentasi tempe merombak protein menjadi asam-asam amino bebas
dan meningkatkan kadar peptida sehingga protein tempe memiliki kuantitas
dan kualitas lebih baik serta lebih mudah diserap dibandingkan protein kedelai.
Protein tempe merupakan salah satu alternatif protein hewani yang sangat
memadai (Nout dan Kiers, 2005). Di samping itu tempe juga menghasilkan
antibakteri yang tidak dimiliki kedelai. Fermentasi tempe juga meningkatkan
kualitas dan kuantitas zat-zat gizi kedelai asalnya antara lain vitamin B2,
vitamin B12, niasin, asam pantotenat, asam amino bebas, asam lemak bebas,
fosfor, dan zat besi (Yeong, et al., 1995).
Metabolisme kapang dan bakteri selama fermentasi meningkatkan
kandungan grup vitamin B, terutama riboflavin, niasin, vitamin B6, dan
vitamin B12. Beberapa galur Rhizopus memproduksi betakaroten sehingga
tempe yang difermentasi dengan kultur terseleksi dapat menjadi alternatif
solusi di berbagai negara-negara yang penduduknya mengalami kekurangan
vitamin A. Tempe juga mengandung ergosterol, prekursor vitamin D2, hasil
aktivitas kapang Rhizopus sp. yang tidak terdapat pada kedelai asalnya (Denter
et al., 1998).
Tempe dapat menanggulangi anemia gizi besi dan berpotensi mencegah
kanker (Astuti, 1996a dan Astuti, 1996b). Brata (1999) juga mengemukakan
bahwa tempe mampu mencegah dan menanggulangi hiperkolesterolemia serta
penyakit-penyakit yang terkait seperti penyakit jantung dan atherosclerosis.
Konsumsi tempe yang memiliki sifat anti-infeksi dan merupakan sumber
protein dengan kualitas, kuantitas, dan daya cerna yang tinggi juga telah
terbukti mampu menanggulangi diare (Karmini, 1999).
B. TEKNOLOGI PEMBUATAN TEMPE
Teknologi pembuatan tempe, seperti halnya teknologi pembuatan
makanan tradisional lainnya, berkembang secara turun temurun, dari mulut ke
mulut dan berubah karena pengalaman. Teknologi pembuatan tempe
tahap produksi yang bervariasi, pada perkembangannya terjadi modifikasi
pada setiap tahap produksi tempe. Modifikasi tersebut antara lain waktu dan
teknik perendaman, jenis dan cara penambahan ragi tempe, waktu perebusan
dan tambahan proses pemanasan pada tahap lain, jenis bahan pembungkus dan
cara membungkus, serta waktu dan cara memeram (Hermana dan Karmini,
1996). Perendaman yang dilakukan dalam teknologi pembuatan tempe
tradisional ini dilakukan dengan tujuan pengasaman kedelai secara alami.
Pengasaman ini dapat dilakukan pula secara kimiawi dengan perendaman atau
perebusan kedelai dalam bahan pengasam (Nout dan Kiers, 2005).
Pengelompokan metode pembuatan tempe tradisional dapat dilakukan
berdasarkan asal daerah pengembangannya (Hermana dan Karmini, 1996)
maupun urutan langkah produksi tempe (Kuswanto, 2004). Berbagai metode
pembuatan tempe tradisional dapat dilihat pada Gambar 1. Berdasarkan asal
daerah pengembangannya, metode pembuatan tempe dibagi menjadi teknologi
pembuatan tempe Malang (metode 8), tempe Purwokerto (metode 9), dan
tempe Magelang (metode 10). Urutan langkah produksi tempe yang seringkali
membedakan metode pembuatan tempe tradisional diantaranya adalah
pencucian, perendaman, perebusan, pengupasan, inokulasi, pengemasan, dan
jumlah pemanasan yang diterapkan (metode 1 – 7).
Pembagian metode pembuatan tempe ini juga dapat dilakukan
berdasarkan cara pengupasannya yaitu metode pengupasan basah dan metode
pengupasan kering. Metode pengupasan kering dilakukan untuk produsen dan
industri tempe skala menengah dan besar, sedangkan pengrajin tempe skala
kecil umumnya menggunakan metode pengupasan basah (Yeong et al., 1999).
Kedelai merupakan sumber nutrisi rendah biaya yang kaya protein.
Nilai nutrisi kedelai dibatasi oleh beberapa komponen antinutrisi dan
komponen toksik. Perendaman, pengupasan, dan perebusan secara efektif
meningkatkan nilai nutrisi kedelai. Pemanasan basah menghancurkan tripsin
inhibitor. Pengupasan menghilangkan kandungan tanin. Fermentasi kedelai
dalam pembuatan tempe mereduksi fitat hingga 30.7%. Kombinasi perlakuan
perendaman, pengupasan, pemanasan, dan fermentasi oleh R. oligosporus
menghilangkan hampir semua stakiosa, yaitu oligosakarida kedelai yang
Metode 11) Metode 21) Metode 31) Metode 41) Metode 51) Metode 61) Metode 71) Metode 82) 3) Metode 93) Metode 103)
Kupas Rebus Rendam Rebus Rebus Rendam Rendam Rebus Rebus Rebus
↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓
Cuci Rendam Kupas Rendam Dinginkan Rebus Rebus Kupas Kupas Kupas
↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓
Rebus Kupas Cuci Kupas Kupas Cuci Dinginkan Rendam Rendam Rendam
↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓
Tiriskan Cuci Rebus Cuci Cuci Rebus Kupas Cuci Cuci Cuci
↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓
Dinginkan Tiriskan Tiriskan Rebus Rendam Dinginkan Cuci Rebus Tiriskan Direndam
↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ Bersama
Inokulasi Inokulasi Dinginkan Tiriskan Rebus Kupas Rendam Tiriskan Inokulasi Inokulum
↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓
Kemas Kemas Inokulasi Dinginkan Tiriskan Cuci Rebus Dinginkan Kemas Tiriskan
↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓ ↓
Inkubasi Inkubasi Kemas Inokulasi Dinginkan Tiriskan Tiriskan Inokulasi Inkubasi Kemas
↓ ↓ ↓ ↓ ↓ ↓ ↓
Inkubasi Kemas Inokulasi Inokulasi Dinginkan Kemas Inkubasi
↓ ↓ ↓ ↓ ↓
Inkubasi Kemas Kemas Inokulasi Inkubasi
↓ ↓ ↓
Inkubasi Inkubasi Kemas
↓
Inkubasi
Keterangan: 1)Kuswanto (2004); 2)Winarno (1989); 3)Hermana dan Karmini (1996)
C. CITARASA TEMPE
Fermentasi merupakan salah satu proses pembentukan citarasa dalam
bahan makanan (Heath dan Reineccius, 1994). Kapang Rhizopus oligosporus
yang biasa digunakan dalam pembuatan tempe memiliki kemampuan untuk
tumbuh pesat, menghasilkan enzim-enzim proteolitik dan lipolitik yang
mengubah komponen-komponen kedelai dan menghasilkan aroma yang khas
(Mital dan Garg, 1990).
Salah satu faktor penghambat kedelai sebagai makanan, khususnya
untuk bangsa Barat adalah aroma dan rasa kedelai atau “beany flavor and
taste”. Oleh adanya aktivitas mikroorganisme aroma kedelai diubah menjadi
aroma khas tempe yang lebih dapat diterima (Pawiroharsono, 1996). Peranan
fermentasi tempe dalam pembentukan citarasanya ditunjukkan dengan
perubahan komponen volatil selama fermentasi tempe baik secara kuantitatif
maupun kualitatif (Nurjannah, 1999). Enzim yang dihasilkan kapang tempe
memacu perubahan kimia yang terjadi selama fermentasi tempe (Varzakas,
1998).
Nurkori (1999) dalam penelitiannya menyebutkan bahwa komponen
volatil pada kedelai yang teridentifikasi dengan jumlah cukup tinggi berasal
dari golongan asam karboksilat, senyawa ester alifatik, alkohol alifatik,
aldehid alifatik, terpenoid, hidrokarbon, dan beberapa senyawa pyrazin.
Degradasi komponen volatil tersebut sangat berkontribusi terhadap aroma
tempe yang dihasilkan (Owens et al., 1997) .
Winarno et al. (1986) menyebutkan bahwa tempe segar memiliki
penampakan putih bersih dan tidak memiliki aroma kacang-kacangan seperti
pada kedelai. Tempe tidak umum dikonsumsi dalam bentuk mentah melainkan
setelah mengalami pengolahan. Menurut Mottram (1994), pengolahan panas
mempengaruhi citarasa bahan pangan melalui reaksi Maillard.
Martoyo (2001) dalam penelitiannya menunjukkan bahwa pengolahan
tidak menghilangkan deskripsi rasa asam dan pahit tempe. Tempe mentah dan
tempe rebus tidak bergaram terdapat dalam kelompok atribut rasa yang sama
dan kelompok atribut aroma yang berbeda. Tempe rebus digambarkan dengan
rendah dan aroma rebus lebih dominan (Nurkori, 1999). Hasil deskripsi tempe
oleh panelis terlatih dan tidak terlatih tidak menunjukkan perbedaan yang
nyata (Martoyo, 2001).
D. PENGASAMAN ALAMI
Meskipun teknologi pembuatan tempe sangat beragam, ada hal-hal
dasar yang diterapkan oleh semua pengrajin, salah satunya adalah pengasaman
(Hermana dan Karmini, 1996). Di Indonesia, pengasaman biasanya dilakukan
secara alami yaitu dengan perendaman kedelai beserta kulitnya, sehingga
bakteri yang ada pada kulit kedelai tumbuh dan menghasilkan berbagai asam
seperti asam sitrat, asam laktat, dan asam asetat. Yang penting dalam proses
pengasaman ini adalah proses penurunan pH sehingga keasaman biji kedelai
dan air rendaman mencapai nilai pH 3.5-5 (Yeong et al., 1999).
Proses pembuatan tempe melibatkan tahap perebusan yang
mengeliminasi sebagian besar mikroorganisme, namun demikian
kemungkinan terjadi rekontaminasi tetap ada. Rhizopus oligosporus dapat
menghambat sebagian besar mikroorganisme, namun bakteri patogen tertentu
masih dapat hidup apabila digunakan kultur murni R. oligosporus. Bakteri
asam laktat (BAL) memberikan kontribusi penting dalam proses fermentasi
dan menjamin keamanan tempe yang dihasilkan (Feng et al., 2005).
Selama pengasaman alami berlangsung, terjadi fermentasi asam laktat
yang menghambat pertumbuhan patogen dan mikroba pembusuk pada tempe.
Pada proses pengasaman alami ini jenis mikroorganisme yang umum
ditemukan adalah jenis-jenis bakteri pembentuk asam-asam organik yaitu
bakteri dari kelompok Enterobacillus seperti Lactobacillus sp., L. plantarum
dan sebagainya (Pawiroharsono, 1996).
Penelitian Feng et al. (2005) menunjukkan bahwa Lactobacillus
plantarum dan BAL yang lain menghambat pertumbuhan bakteri patogen
selama fermentasi tempe dan mempunyai efek inhibisi yang lebih tinggi pada
kondisi asam. BAL yang mendominasi selama perendaman ini meningkatkan
Pengasaman kedelai terjadi secara alami selama proses perendaman
pada daerah tropis. Selama periode perendaman pertumbuhan bakteri banyak
berperan dan menurunkan pH hingga mencapai nilai pH 4.5-5.3 (Kuswanto,
2004; Yeong et al., 1999). Fungsi utama pengasaman adalah mendukung
pertumbuhan bakteri dan menghambat pertumbuhan beberapa bakteri patogen
dan pembusuk. Namun demikian, proses pengasaman alami yang dilakukan
dengan perendaman kedelai dalam air selama semalam juga dapat
menurunkan zat-zat inhibitor pertumbuhan kapang (Kuswanto, 2004) dan
mempermudah pencernaan atau hidrolisis protein kedelai pada tahap
fermentasi berikutnya (Hermana dan Karmini, 1996). Proses fermentasi pada
pengasaman alami ini penting dalam menghasilkan tempe dengan flavor, daya
cerna, nilai nutrisi/gizi dan keawetan yang baik (Yeong et al., 1999).
Hal lain yang mendasari pentingnya aplikasi pengasaman terhadap
kedelai yang akan digunakan dalam pembuatan tempe adalah karena kapang
tempe memiliki aktivitas proteolitik yang tinggi. Deaminasi yang mengikuti
hidrolisis melepaskan amonia yang akan meningkatkan nilai pH. Nilai pH
lebih dari 7.0 merupakan kondisi di mana amonia bebas terdapat dalam jumlah
yang cukup untuk membunuh kapang. Nilai pH awal yang lebih rendah
memerlukan waktu fermentasi yang lebih lama sebelum amonia dibebaskan
dalam jumlah yang cukup besar untuk membunuh kapang (Steinkraus, 1996).
Fermentasi bakteri selama perendaman mengubah senyawa isoflavon
kedelai menjadi antioksidan yang lebih aktif. Proses perendaman yang
panjang juga memungkinkan pertumbuhan bakteri-bakteri lain penghasil
vitamin seperti vitamin B2, B6, niasin, biotin, asam folat, asam pantotenat dan
bahkan vitamin B12 (Hermana dan Karmini, 1996), vitamin dengan struktur
molekul sangat kompleks yang umumnya terdapat pada produk-produk
pangan hewani dan jarang ditemukan pada produk pangan nabati (Yeong et
al., 1999).
Kemampuan BAL memproduksi senyawa-senyawa antimikroba telah
lama digunakan dalam pengawetan pangan. Fermentasi oleh BAL mengurangi
jumlah karbohidrat yang tersedia dan menghasilkan komponen organik
(Ouwehand dan Vesterlund, 2004). Asam laktat, salah satu agen inhibisi yang
dihasilkan BAL, merupakan produk akhir utama dari katabolisme karbohidrat.
Karena dari proses konversi sumber karbon ini dihasilkan setidaknya 50%
asam laktat, maka grup bakteri ini dinamakan bakteri asam laktat (De Vuyst
dan Vandamme, 1994).
Fermentasi yang melibatkan BAL dikarakterisasi dengan akumulasi
asam-asam organik yang menyebabkan penurunan pH (De Vuyst dan
Vandamme, 1994). Komponen-komponen tersebut pada umumnya berupa
asam laktat, asam asetat, dan asam propionat (Ouwehand dan Vesterlund,
2004). Prinsip pengawetan dari fermentasi asam laktat terutama hasil dari
aktivitas antimikroba asam-asam organik yang dihasilkan selama metabolisme
BAL (De Vuyst dan Vandamme, 1994). Pengasaman dan efek inhibisi yang
lain dari BAL menekan mikroflora alami seperti koliform, Klebsiella
pneumoniae, dan khamir sehingga dengan demikian memperpanjang masa
simpan tempe (Nout dan Kiers, 2005).
Fermentasi asam laktat pada dasarnya terbagi menjadi dua yaitu
homofermentasi dan heterofermentasi. Homofermentasi memproduksi asam
laktat sedangkan heterofermentasi memproduksi asam laktat, asam asetat,
karbondioksida, dan/atau etanol (Ouwehand dan Vesterlund, 2004).
Selama pembuatan tempe pada iklim tropika seperti di Indonesia,
heterofermentasi asam laktat berlangsung sangat aktif. Hal ini ditandai dengan
terbentuknya buih dari gas CO2 (Yeong et al., 1999). Karbondioksida (CO2) terbentuk sebagai hasil heterofermentasi BAL terhadap heksosa. Gas CO2 memiliki efek antimikroba ganda karena selain memiliki aktivitas
antimikroba, gas CO2 juga memberikan kondisi lingkungan anaerobik yang menghambat pertumbuhan mikroba aerofilik.
Dalam kondisi aerobik, BAL mampu membentuk hidrogen peroksida.
Apabila dalam media tidak tersedia heme, BAL tidak akan memproduksi
katalase untuk menghilangkan hidrogen peroksida dan dengan demikian
menyebabkan akumulasi hidrogen peroksida. Efek bakterisidal dari hidrogen
memiliki grup sulfihidril, dan struktur lipid membran sel (Ouwehand dan
Vesterlund, 2004).
Menurut Sparringa dan Owens (1999) asam organik utama yang
ditemukan setelah tahap perendaman adalah asam laktat yaitu sekitar 80% dari
seluruh asam organik yang ditemukan dalam air rendaman. Demikian pula
menurut Nout dan Kiers (2005) setelah perendaman selama 24 jam pada suhu
30oC, asam organik utama yang ditemukan dalam air rendaman kedelai hasil pengasaman alami teknologi backsloping adalah asam laktat (2.1% w/v air
rendaman), sedangkan asam asetat (0.3% w/ v air rendaman) dan asam sitrat
(0.5% w/ v air rendaman) ditemukan pula dalam jumlah lebih sedikit.
Pengasaman alami dengan perendaman kedelai tidak mempengaruhi
citarasa tempe yang dihasilkan karena kapang Rhizopus memproduksi amonia
dalam jumlah yang cukup untuk menetralisir asam (Yeong et al., 1999).
Namun demikian Nout dan Kiers (2005) menyarankan proses pemasakan
dalam air (kedelai : air = 1 : 6.5) setelah perendaman untuk menurunkan
konsentrasi asam laktat dan asam asetat hingga 45% dan 51%.
E. LIMBAH INDUSTRI TEMPE
Limbah industri pangan dapat menimbulkan masalah karena
mengandung sejumlah besar nutrisi sehingga dapat bertindak sebagai sumber
makanan untuk pertumbuhan mikroba. Umumnya limbah industri pangan
tidak membahayakan kesehatan masyarakat, karena tidak terlibat langsung
dalam perpindahan penyakit. Akan tetapi limbah industri pangan dapat
berperan sebagai pasokan makanan yang berlimpah bagi mikroorganisme,
yang bila berkembang biak dengan cepat akan mereduksi oksigen terlarut
dalam air dan menimbulkan bau yang tidak diinginkan (Jenie dan Rahayu,
1989).
Berdasarkan data yang diperoleh oleh Yeong et al. (1999), konsumsi
kedelai yang diolah menjadi tempe di Kabupaten Bogor sekitar 13 ton per
tahun. Dari jumlah ini limbah padat yang dihasilkan sekitar 9.36 ton per tahun
Limbah padat berupa kulit kedelai dihasilkan pada tahap pengupasan,
sedangkan limbah cair dihasilkan pada tahap perebusan, perendaman
(pengasaman alami), dan pencucian (Yeong et al., 1999). Limbah padat
industri tempe telah mulai dimanfaatkan sebagai medium fermentasi dan
makanan ternak yang baik dan ekonomis karena nilai proteinnya (Murti dan
Nasution, 1996). Limbah cair yang merupakan limbah utama industri tempe
dibuang secara langsung ke saluran yang ada atau ke sungai, kolam, maupun
danau (Yeong et al., 1999).
Limbah cair hasil pengasaman alami berupa air rendaman kedelai
mempunyai bau yang asam (Yeong et al., 1999) sehingga tidak jarang limbah
produksi tempe ini menjadi sumber protes masyarakat sekitar pabrik (Murti
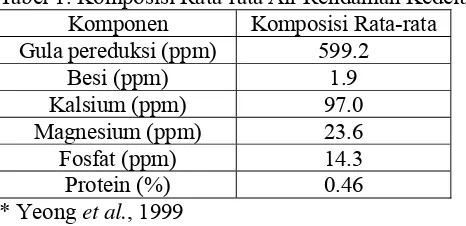
dan Nasution, 1996). Air limbah rendaman kedelai banyak mengandung
bahan-bahan organik terlarut seperti gula dan protein (Tabel 1). Air limbah
rendaman kedelai mengandung bakteri penghasil asam laktat seperti
Lactobacillus sp. dan bakteri lain seperti bakteri pembusuk yang secara alami
terdapat dalam air rendaman (Yeong et al., 1999).
Kandungan bahan organik dan mikroorganisme dalam air limbah
rendaman kedelai meningkatkan nilai BOD (Biological Oxygen Demand) dan
menghabiskan oksigen terlarut dalam air. Apabila suplai oksigen terus
menurun, keseimbangan ekologi air terganggu bahkan dapat menyebabkan
kematian ikan dan biota perairan lainnya (Jenie dan Rahayu, 1989).
Tabel 1. Komposisi Rata-rata Air Rendaman Kedelai*
Komponen Komposisi Rata-rata
Gula pereduksi (ppm) 599.2
Besi (ppm) 1.9
Kalsium (ppm) 97.0
Magnesium (ppm) 23.6
Fosfat (ppm) 14.3
Protein (%) 0.46
* Yeong et al., 1999
Air limbah rendaman kedelai juga bersifat asam (pH 3.5-5.2), karena
pada tahap perendaman terjadi proses pengasaman (Liu, 1997). Peningkatan
bersifat korosif dan dapat menyebabkan pengkaratan pada pipa-pipa besi
(Fardiaz, 1992).
Konsep perlindungan lingkungan yang dianut oleh industri selama ini
adalah penanganan dan pembuangan limbah yang disebut konsep End of Pipe
Treatment (EOPT). Konsep EOPT memiliki kelemahan yaitu kebutuhan akan
biaya yang tinggi dan teknologi yang canggih sehingga sulit untuk diterapkan
di industri kecil dan menengah (Suprihatin, 1999).
Suprihatin (1999) mengemukakan kemungkinan konsep alternatif yang
lebih murah dan relatif lebih mudah yang disebut konsep teknologi produksi
bersih. Konsep teknologi produksi bersih mencegah pencemaran lingkungan
sejak pada sumber asalnya. Menurut Modak (1995), keberhasilan penerapan
teknologi produksi bersih dapat dicapai dengan lima jalur yaitu penerapan
house keeping yang baik, modifikasi peralatan, substitusi, bahan baku,
modifikasi produk, dan inovasi teknologi. Pengasaman kimiawi dapat
digolongkan dalam usaha aplikasi teknologi bersih dengan cara inovasi
teknologi sebagai alternatif solusi untuk masalah lingkungan yang ditimbulkan
pengasaman alami.
Bahan pengasam juga memiliki keasaman yang tinggi sehingga bersifat
korosif dan dapat menyebabkan pengkaratan pada pipa-pipa besi (Fardiaz,
1992). Namun demikian limbah hasil pengasaman kimiawi dapat digunakan
kembali sebagai bahan pengasam untuk proses pengasaman berikutnya. Selain
itu, limbah hasil pengasaman kimiawi tidak mengandung bahan organik dan
mikroorganisme sebanyak limbah cair hasil perendaman alami (Yeong et al.,
1999). Bahan organik dan mikroorganisme menghabiskan oksigen terlarut
dalam air dan meningkatkan BOD sehingga mengganggu kehidupan biota air
(Jenie dan Rahayu, 1989).
F. PENGASAMAN KIMIAWI
Keunggulan nutrisi dan sifat fungsional tempe telah menarik perhatian
dunia sehingga permintaan akan tempe di dunia internasional juga semakin
sangat mudah rusak mendorong negara industri, seperti Jepang untuk memulai
produksi tempe di negaranya sendiri (Kozaki, 2004).
Di negara beriklim subtropis, pengasaman alami selama perendaman
tidak selalu terjadi atau sangat lambat (Liu, 1997; Yeong et al., 1999). Pada
kondisi suhu yang cukup dingin, fermentasi asam laktat pada umumnya
kurang dapat berjalan dengan baik, sehingga untuk mencapai pH yang
diinginkan perlu dilakukan pengasaman kimiawi dengan penambahan bahan
pengasam (Yeong et al., 1999).
Berkembangnya proses pengasaman kimiawi didasarkan pada tujuan
utama pengasaman kedelai dalam proses pembuatan tempe yaitu menghambat
pertumbuhan bakteri patogen dan pembusuk dan memberikan kondisi
lingkungan yang sesuai untuk pertumbuhan kapang (Kuswanto, 2004). Hal ini
dapat dicapai dengan menambahkan bahan pengasam yang merupakan bahan
tambahan pangan (BTP) yang diperbolehkan oleh peraturan (Doores, 1983).
Efek antimikroba asam tidak hanya diperoleh dari penurunan pH
(Doores, 1990). Aktivitas antimikroba dari asam organik ditentukan oleh nilai
pH, konstanta disosiasi (pKa) dan konsentrasi asam (De Vuyst dan Vandamme, 1994). Penggunaan asidulan secara efektif tergantung pKa atau pH dimana 50% dari total asam terdisosiasi. Pada umumnya, asam-asam
organik memiliki pKa 3-5 (Doores, 1983). Oleh karena itu asam organik umumnya memiliki aktivitas antimikroba yang lebih kuat pada pH rendah
daripada pH netral (Ouwehand dan Vesterlund, 2004).
Asam dapat dikelompokkan menjadi dua yaitu asam lipofilik dan asam
karboksilat. Asam lipofilik seperti asam asetat dan turunannya, asam
propionat, asam laktat, dan asam kaprilat merupakan komponen yang relatif
nonpolar. Komponen ini umumnya ditambahkan ke dalam bahan pangan
karena properti antimikroba yang dimilikinya. Asam karboksilat lebih polar
daripada asam lipofilik dan umumnya digunakan karena efek secondary (rasa,
pengkelat ion logam, reaksi sinergis dengan antioksidan, mengkontrol
pembentukan gel pektin, mencegah pencoklatan) daripada efek
Efek antimikroba dari asam sangat bergantung pada pH dan pada bentuk
tidak terdisosiasi asam tersebut (Doores, 1990). Bagian yang tidak terdisosiasi
dari suatu molekul dipercaya merupakan faktor yang bertanggungjawab
terhadap efek antimikroba (Doores, 1983; Ouwehand dan Vesterlund, 2004).
Bentuk terdisosiasi asam lemah, tidak dapat menembus dinding sel
mikroorganisme. Bentuk tidak terdisosiasi dari asam lemah dapat menembus
bagian dalam sel dengan cepat karena kelarutannya dalam lemak sehingga
mampu berdifusi melewati plasma membran dan berdisosiasi di dalam sel
(Doores, 1990).
Asam lipofilik dalam bentuk tidak terdisosiasi dapat menembus sel
mikroba, dan pada pH intaseluler yang lebih tinggi, terdisosiasi memproduksi
ion hidrogen, dan menggangu fungsi metabolisme esensial seperti translokasi
substrat dan fosforilasi oksidatif, serta menurunkan pH intraseluler mikroba
(De Vuyst dan Vandamme, 1994). Oleh karena itu penggunaan asam yang
bertujuan untuk pengawetan lebih baik digunakan pada nilai pH yang
mendekati pKa (Doores, 1983). Pada suatu nilai pH, asam yang memiliki nilai pKa tertinggi, akan memiliki bentuk tidak terdisosiasi lebih banyak dan dengan demikian memiliki aktivitas antimikroba yang lebih tinggi (De Vuyst
dan Vandamme, 1994).
Selama ini asam laktat merupakan pilihan utama sebagai bahan
pengasam dalam pembuatan tempe. Jika tidak mungkin memperoleh asam
laktat, asam cuka dapat digunakan (Hermana dan Karmini, 1996). Jumlah
asam yang ditambahkan beragam tergantung suhu dan nilai pH akhir kedelai
prefermentasi (Yeong et al., 1999).
Penggunaan bahan pengasam menambah biaya produksi namun
mempersingkat waktu produksi tempe. Pengasaman kimiawi menguntungkan
untuk produksi tempe skala industri karena hanya membutuhkan waktu 2-3
jam bila dibandingkan dengan cara tradisional yang membutuhkan waktu
20-30 jam (Hermana dan Karmini, 1996).
Steinkraus (1965) mengemukakan bahwa di negara-negara subtropis
pengasaman ini dapat dilakukan dengan perendaman dalam larutan asam
Asam laktat merupakan inhibitor bakteri pembentuk spora pada pH 5.0. Asam
laktat tidak efektif terhadap khamir dan kapang sehingga penggunaannya
untuk mengasamkan kedelai tidak menggangu fermentasi kapang dalam
pembuatan tempe (Doores, 1983). Selain menurunkan pH, asam laktat
meningkatkan permeabilitas membran dan dengan demikian memicu aktivitas
komponen antimikroba lain (Ouwehand dan Vesterlund, 2004). Berdasarkan
status regulasinya, asam laktat dinyatakan sebagai bahan tambahan pangan
(BTP) Generally Recognized as Safe (GRAS) untuk penggunaan umum dan
lain-lain (21 CFR 182.1061). Nilai asupan harian yang dapat diterima untuk
asam laktat tidak dibatasi (Doores, 1983).
Nout danKiers (2005) menyatakan bahwa perendaman kimiawi dengan
asam asetat (< 0.25%) juga umum digunakan untuk menggantikan metode
pengasaman alami, meskipun menurut De Reu, Rombouts, dan Nout (1995)
asam asetat menunjukkan efek inhibisi terhadap pertumbuhan kapang. Asam
asetat merupakan antimikroba spektrum luas dengan properti bakterisidal dan
mikosidal. Aksi antimikroba asam asetat dicapai pada pH yang lebih tinggi
dibandingkan HCl (Doores, 1983).
Penggunaan utama asam asetat adalah untuk membatasi pertumbuhan
bakteri dan khamir daripada kapang, namun pada pH 3.5 mempunyai aktivitas
antifungal yang biasa digunakan untuk mencegah pertumbuhan kapang roti
(Doores, 1983). Dalam kondisi dimana asam laktat dan asam asetat terdapat
bersamaan, asam laktat berperanan menurunkan pH sedangkan asam asetat
dalam bentuk tidak terdisosiasinya berperan sebagai antimikroba aktual
(Ouwehand dan Vesterlund, 2004). Karakteristik rasa asam asetat seringkali
membatasi penggunaannya (Doores, 1990). Berdasarkan status regulasinya,
asam asetat dinyatakan sebagai BTP GRAS untuk penggunaan umum dan
lain-lain (21 CFR 182.1005). Nilai asupan harian yang dapat diterima untuk
asam asetat tidak dibatasi (Doores, 1983)
Asam sitrat merupakan salah satu asam yang ditemukan dalam jumlah
cukup tinggi pada air rendaman kedelai hasil pengasaman alami (Nout dan
Kiers, 2005). Asam sitrat merupakan komponen asam utama pada kebanyakan
secara alami sehingga nilai asupan harian yang dapat diterima tidak dibatasi.
Asam sitrat dinyatakan sebagai BTP GRAS untuk penggunaan umum dan
lain-lain (21 CFR 182.1033). Asam sitrat memiliki efek inhibisi paling baik
pada salmonellae sehingga umum digunakan dalam pengawetan daging
(Doores, 1983).
Asam malat merupakan asam nonhigroskopik dengan rasa asam yang
terasa secara perlahan-lahan namun persisten, tidak menyengat seperti
kebanyakan bahan pengasam lain. Asam malat dinyatakan sebagai BTP
GRAS untuk penggunaan umum dan lain-lain (21 CFR 182.1069). Efek
antimikroba asam malat terhadap khamir dan bakteri diperkirakan merupakan
efek langsung dari manipulasi pH yang ditimbulkannya. Asam malat
umumnya digunakan sebagai flavoring (Doores, 1983).
Asam anorganik seperti asam fosfat dapat pula digunakan sebagai bahan
pengasam. Asam fosfat memiliki rasa datar, berbeda dengan rasa tart yang
tajam kebanyakan asam organik. Asam fosfat dapat menyebabkan iritasi kulit
sehingga memerlukan penanganan yang hati-hati (Reineccius, 1994).
Bahan pengasam X merupakan senyawa anorganik yang juga umum
digunakan sebagai BTP dan memiliki status regulasi GRAS. Keamanan
penggunaan bahan pengasam X telah terbukti secara empiris pada produk
pangan lain. Pengasam X ini ditemukan dalam tubuh manusia dan dapat
diperoleh dari fermentasi bahan pangan.
Penggunaan utama dari bahan pengasam adalah sebagai antimikroba
untuk mencapai keamanan pangan (Doores, 1990). Bahan pengasam yang
umum digunakan sebagai BTP dapat dilihat pada Tabel 2. Pemilihan bahan
pengasam yang digunakan selain bergantung pada efek antimikrobanya juga
harus mempertimbangkan status regulasi dan efeknya terhadap citarasa bahan
pangan (Doores, 1983).
Bahan pengasam berkontribusi terhadap rasa asam dan getir dari produk
(Doores, 1983). Tingkat keasaman yang diperlukan untuk mencapai tujuan
pengawetan dapat mempengaruhi citarasa bahan pangan. Bahan pengasamdan
hubungannya dengan citarasa ini seringkali menjadi batasan penggunaan asam
Tabel 2. Bahan pengasam yang digunakan sebagai bahan tambahan pangan dan karakteristiknya*
No Nama Asam Struktur pKa Bentuk fisik Kelarutan
(g/100ml air) 1 Asam asetat C2H4O2 4.75 Cairan bening jernih Sangat larut
2 Asam adipat C6H10O4 4.43
5.41
Bubuk kristal 1.9g (20oC) 83g (90oC) 3 Asam askorbat C6H8O6 4.17
11.57
4 Asam kaprilat C8H16O2 4.89 Cairan bening jernih
5 Asam sitrat C6H8O7 3.14
4.77 6.39
Bubuk kristal 181g (25oC)
208g (25oC)
6 Asam fumarat C4H4O4 3.03
4.44
Granula atau bubuk kristal
0.5g (20oC) 9.8g (100oC) 7 Asam laktat C3H6O3 3.08 Cairan atau bubuk
kering
Sangat larut
8 Asam malat C4H6O5 3.40
5.11
Bubuk kristal 62g (25oC)
9 Asam fosfat 2.12
7.21 12.67
Cair Sangat larut
dalam air panas 10 Asam tartarat C4H6O6 2.98
4.34
Bubuk kristal 147g (25oC)
11 Asam propionat C3H6O2 4.87 Oily liquid Sangat larut
12 Asam sorbat Kristal putih Sedikit larut
13 Asam suksinat C4H6O4 4.16 5.61 *Doores, 1983; Doores, 1990; Reineccius, 1994
G. ANALISIS SENSORI
Analisis sensori didefinisikan sebagai disiplin ilmu yang digunakan
untuk memunculkan, mengukur, menganalisis, dan menginterpretasi persepsi
terhadap produk yang diterima oleh indera penglihatan, penciuman,
pendengaran, perasa, dan peraba. Atribut sensori yang dianalisis dengan
penginderaan ini antara lain adalah penampilan, aroma, tekstur dan konsistensi,
citarasa, serta suara (Meilgaard et al., 1999).
Citarasa didefinisikan sebagai persepsi yang diterima oleh alat indera
dari produk yang terletak di dalam mulut. Berdasarkan definisi tersebut, yang
termasuk di dalamnya adalah aroma, rasa, faktor stimulasi kimia dan
[image:32.612.153.550.104.459.2]karakteristik sensori produk pangan hanya dapat diukur dengan baik, lengkap,
dan berarti bila menggunakan manusia sebagai subjek pengukuran. Dalam
bahasa analisis sensori, subjek manusia biasa disebut panelis (Poste et al.,
1991).
Panelis analisis sensori ini dapat dikelompokkan menjadi empat macam
yaitu kelompok expert yang sangat terlatih, panelis terlatih skala laboratorium,
panelis penerimaan skala laboratorium, dan panelis konsumen skala besar.
Expert yang sangat terlatih (1-3 orang) digunakan untuk evaluasi kualitas yang
membutuhkan derajat ketepatan yang tinggi seperti anggur, teh, dan kopi.
Panelis terlatih (8-20 orang) digunakan untuk evaluasi perubahan karakteristik
produk tanpa instrumentasi yang lengkap. Analisis sensori oleh panelis
penerimaan skala laboratorium (25-50 orang) digunakan untuk prediksi reaksi
konsumen terhadap produk. Panelis konsumen skala besar (lebih dari 100
orang) digunakan menetukan reaksi konsumen terhadap produk (Poste et
al.,1991 dan Meilgaard et al., 1999).
Berbagai metode analisis sensori telah dikembangkan dengan
keuntungan dan kelemahan masing-masing. Situasi yang berbeda
membutuhkan metode berbeda. Tidak ada satu metode yang dapat selalu
digunakan secara umum. Sebelum digunakan, penguji harus menentukan
tujuan dari suatu pengujian dan informasi yang ingin dilihat dari pengujian
tersebut (Poste et al., 1991).
Pada dasarnya, jenis analisis sensori terbagi menjadi tiga kelompok
besar yaitu uji diskriminatif atau uji beda, uji deskriptif, dan uji afektif (Poste
et al., 1991; Meilgaard et al. 1999). Uji diskriminatif digunakan untuk
menentukan apakah terdapat perbedaan diantara sampel-sampel yang diujikan.
Uji deskriptif digunakan untuk menentukan karakter dan intensitas perbedaan
tersebut. Uji afektif didasarkan pada evaluasi preferensi atau penerimaan
untuk menentukan preferensi relatif (Poste et al., 1991).
1. Uji Diskriminatif
Analisis sensori seringkali dilakukan untuk menentukan ada
1991). Secara umum uji diskriminatif terbagi menjadi uji diskriminatif
keseluruhan (overall difference test) dan uji diskriminatif atribut tertentu
(attribute difference test).
Uji diskriminatif keseluruhan seperti uji segitiga dan uji duo-trio,
dirancang untuk menunjukkan apakah panelis dapat mendeteksi perbedaan
yang terdapat pada sampel. Uji diskriminatif keseluruhan dapat dilakukan
dengan berbagai metode diantaranya uji segitiga, uji duo-trio, uji two out
of five, simple different test, uji A bukan A, uji different from control
(Poste et al., 1991, Meilgaard et al., 1999).
Kelima metode pertama yang disebutkan memiliki tujuan untuk
menentukan apakah terdapat perbedaan karakteristik sensori akibat
perubahan bahan baku, pengolahan, pengemasan, dan penyimpanan serta
untuk menentukan apakah terdapat perbedaan karakteristik sensori secara
keseluruhan dimana tidak ada atribut spesifik yang diketahui telah berubah
(Meilgaard et al., 1999).
Uji different from control dilakukan untuk menentukan ada tidaknya
perbedaan diantara satu atau beberapa sampel dengan kontrol. Namun
demikian uji ini juga dapat digunakan untuk memperkirakan seberapa jauh
perbedaan tersebut. Uji segitiga dan uji two out of five dapat dilakukan
untuk menyeleksi dan melatih kemampuan panelis dalam memilah
perbedaan yang ada dalam sampel. Simple different test merupakan
metode yang paling sederhana dan paling sering digunakan untuk
menentukan keberadaan perbedaan karakteristik sensori di antara pasangan
sampel yang disajikan (Meilgaard et al., 1999).
Uji diskriminatif atribut tertentu meminta panelis untuk
berkonsentrasi pada satu atau beberapa atribut tertentu saja sementara
atribut sensori yang lain tidak dihiraukan. Yang perlu diperhatikan dalam
pengujian ini adalah tidak adanya perbedaan suatu atribut diantara
sampel-sampel yang diujikan tidak menunjukkan bahwa diantara sampel-sampel tersebut
juga tidak ada perbedaan atribut sensori secara keseluruhan. Metode
yang diuji yaitu paired comparison design dan multisample difference test
(Meilgaard et al., 1999).
Metode pengujian yang termasuk paired comparison design
diantaranya adalah directional difference test dan pairwise ranking test.
Directional difference test merupakan bentuk lain simple different test dan
uji preferensi pasangan untuk analisis perbedaan atribut tertentu suatu
produk pangan. Pairwise ranking test merupakan metode yang
membandingkan atribut tertentu dari semua pasangan sampel yang
mungkin dengan menggunakan panelis tidak terlatih (Meilgaard et al.,
1999).
Multisample difference test umumnya dilakukan dengan
membandingkan 3-6 sampel yang disajikan sekaligus. Namun demikian,
pengujian dengan jumlah sampel yang terlalu banyak bila disajikan
sekaligus dapat menggunakan rancangan pengujian balanced incomplete
block. Pengujian ini merupakan rancangan penyajian dimana seorang
panelis hanya menerima sebagian sampel yang diujikan, namun semua
sampel mendapatkan jumlah evaluasi panelis yang sama (Meilgaard et al.,
1999).
Metode pengukuran respon dalam uji diskriminatif multisample
difference test yang umum digunakan adalah ranking atau rating. Ranking
pada dasarnya merupakan pengembangan dari pengujian paired
comparison. Panelis menerima tiga sampel atau lebih kemudian diminta
untuk mengurutkan sampel berdasarkan intensitas atribut sensori tertentu.
Metode ini umumnya digunakan bukan untuk menguji semua sampel
melainkan untuk memilih satu atau dua sampel dari suatu kelompok
sampel. Data uji ranking tidak menunjukkan besar perbedaan diantara
sampel-sampel yang diuji (Poste et al., 1991).
Rating merupakan salah satu bentuk dalam teknik penskalaan
(scaling). Penskalaan adalah pengukuran respon evaluasi sensori yang
menggunakan angka atau kata-kata untuk menunjukkan intensitas atau
teknik penskalaan dikelompokkan menjadi skala kategorial (rating), skala
garis (skoring), dan skala magnitude estimation (ratio scaling).
Rating merupakan metode yang menggunakan kata-kata untuk
menunjukkan intensitas atribut sampel. Skoring meminta panelis untuk
memberikan tanda pada suatu garis horisontal sehubungan dengan
intenstitas atribut yang dirasakan. Ratio scaling merupakan teknik
penskalaan dimana panelis diminta memberikan nilai secara bebas pada
suatu produk (Meilgaard, 1998).
2. Uji Deskriptif
Analisis sensori deskriptif merupakan identifikasi, deskripsi, dan
kuantifikasi parameter sensori suatu produk dengan instrumen manusia
yang telah mengalami pelatihan (Einstein, 1991). Hasil aplikasi uji
deskripsi dapat memetakan atribut citarasa produk yang diuji (Meilgaard et
al., 1999).
Uji deskriptif hanya menggunakan lima sampai sepuluh panelis
untuk produk dengan variasi tinggi seperti produk pertanian. Panelis
dengan jumlah yang lebih banyak digunakan pula untuk uji deskriptif
produk yang diproduksi secara massal di mana perbedaan yang sangat
sedikit sangat penting (Meilgaard et al., 1999).
Panelis merupakan instrumen analisis dalam analisis sensori.
Kualitas dari instrumen ini bergantung pada objektivitas, presisi dan
kemampuan repetisi dari panelis itu sendiri. Sebelum seorang panelis
dapat digunakan, kemampuan seorang panelis untuk membuat penilaian
harus ditentukan terlebih dahulu. Panelis untuk pengujian deskripsi harus
terlebih dahulu diseleksi dan dilatih (Poste et al., 1991).
Menurut Poste et al. (1991) seleksi panelis dilakukan berdasarkan
karakter personal dan kemampuan panelis. Kemampuan panelis yang
dimaksud antara lain status kesehatan, minat, ketersediaan waktu,
kemampuan menepati waktu, dan kemampuan verbal. Pelatihan panelis
mengingat panelis untuk memberikan pengukuran sensori yang tepat,
konsisten, dan terstandarisasi.
Panelis uji deskriptif terseleksi harus melalui pelatihan sehingga
memiliki kemampuan untuk mendeteksi perbedaan karakteristik atau
intensitas, kemampuan menggambarkan karakteristik secara verbal dan
skala intensitasnya, serta kemampuan untuk mengingat reference (Einstein,
1995).
Uji deskriptif dapat digunakan untuk mendefinisikan properti
sensori dari produk target dalam pengembangan produk baru atau kontrol
untuk aplikasi quality assurance, quality control, atau riset dan
pengembangan. Uji deskriptif dapat pula digunakan untuk melacak
perubahan sensori selama penyimpanan. Sebelum dilakukan uji konsumen,
deskriptif dapat membantu menseleksi atribut sensori yang perlu
dimasukkan dalam kuesioner kepada konsumen dan membantu
menjelaskan hasil yang diperoleh dari uji konsumen tersebut (Meilgaard et
al., 1999).
Uji deskriptif yang umum digunakan antara lain Flavor Profile
Method, Texture Profile Method, Quantitative Descriptive Analysis
(QDA)® Method, SpectrumTM Descriptive Analysis Method, Time-Intensity
Descriptive Analysis, Free Choice Profiling (Meilgaard et al., 1999).
Flavor Profile Method merupakan analisis karakteristik aroma dan
flavor, intensitas, penampilan, dan aftertaste suatu produk hasil penilaian
4-6 panelis terlatih. Texture Profile Method dikembangkan untuk menilai
atribut spesifik deskriptor produk-produk seperti pangan semi-solid,
minuman, dan produk-produk yang diperuntukkan untuk kulit, serta bahan
kain dan kertas. SpectrumTM Descriptive Analysis Method pada prinsipnya
meminta panelis untuk memberikan skor terhadap intensitas stimulasi
yang diterima bila dibandingkan referensi yang memiliki skala intensitas
absolut dan telah dipelajari sebelumnya. Free Choice Profiling merupakan
teknik baru yang mengijinkan panelis untuk menciptakan dan
mendeskripsikan karakteristik sensori sampel yang diujikan (Meilgaard et
al., 1999).
Time-Intensity Descriptive Analysis adalah analisis deskripsi
produk-produk tertentu dimana persepsi yang diterima dapat bervariasi
seiring dengan periode waktu penginderaan. Contoh penggunaan metode
ini adalah untuk mengukur intensitas warna lipstik setelah beberapa jam
penggunaan, efek pahit dari bir, atau aftertaste yang ditinggalkan pemanis
(Meilgaard et al., 1999).
Metode QDA menggambarkan karakteristik sensori secara
matematis (Zook and Pearce, 1988) sehingga analisis statistik pada data
yang diperoleh dapat diinterpretasikan lebih baik. Data QDA diolah secara
sistematik dan hasilnya harus dapat ditampilkan dalam bentuk yang mudah
dimengerti (Zook and Pearce, 1988). Hasil QDA umumnya dilaporkan
dalam bentuk spiderweb dengan nilai nol pada titik pusat untuk setiap
atribut (Meilgaard et al., 1999).
3. Uji Afektif
Uji afektif digunakan untuk mengevaluasi kecenderungan subjektif
suatu produk berdasarkan properti sensorinya. Hasil uji afektif
mengindikasikan pilihan, kesukaan, atau penerimaan suatu produk. Uji
afektif umumnya dilakukan menggunakan responden tidak terlatih dalam
jumlah besar untuk mengetahui indikasi daya tarik suatu produk
dibandingkan produk lainnya (Poste et al., 1991).
Secara umum terdapat dua macam uji afektif yaitu uji afektif
kualitatif dan uji afektif kuantitatif. Metode uji afektif kualitatif terdiri dari
focus group, focus panel, dan wawancara personal. Sedangkan metode uji
afektif kuantitatif terdiri dari uji kesukaan atau uji hedonik dan uji
penerimaan (Meilgaard, 1998).
Uji afektif kualitatif mengukur respon subjektif panelis terhadap
properti sensori suatu produk dengan menanyakan perasaan mereka
terhadap sampel dalam wawancara atau suatu kelompok kecil. Salah satu
praduga terhadap konsep atau prototipe suatu produk (Meilgaard et al.,
1999).
Kata hedonik didefinisikan sebagai “terkait dengan kesenangan”.
Uji kesukaan yang disebut juga uji preferensi ini merupakan metode
pengujian yang paling umum dilakukan untuk mengukur kesukaan suatu
sampel bila dibandingkan sampel lain (Poste et al., 1991). Sedangkan uji
penerimaan merupakan metode uji afektif kuantitatif untuk menentukan
status kesukaan suatu produk yaitu sejauh mana produk tersebut disukai
oleh konsumen.
H. PRINCIPAL COMPONENT ANALYSIS (PCA)
PCA adalah suatu analisis peubah jamak yang dapat mengurangi data
yang komplek menjadi data yang mudah diinterpretasikan. Prinsipnya adalah
transformasi berbagai dimensi ke dalam sistem koordinat dengan dimensi
yang lebih kecil (Esbensen et al., 1994). Masing-masing dimensi baru harus
memaksimalkan jumlah keragaman yang dijelaskan (Carpenter et al., 2000).
Tujuan PCA adalah menentukan komponen-komponen utama untuk
menerangkan keragaman data semaksimal mungkin. Komponen utama yang
diperoleh diurutkan berdasarkan penurunan keragamannya. Komponen utama
pertama (PC1) adalah komponen utama dengan keragaman terbesar yang
paling informatif dan paling berpengaruh. Bila informasi dari variabel yang
di-input dianalisis kembali akan muncul komponen utama pelengkap dengan
keragaman kedua terbesar setelah PC1, disebut PC2, dan demikian seterusnya
(Afifi dan Clark, 1996).
Tahapan dasar dalam analisis ini adalah mentransformasikan variabel
asli yang kurang berhubungan ke dalam variabel baru yang disebut komponen
utama. Variabel baru tersebut merupakan kombinasi linear dari variabel
aslinya. Setiap komponen dalam model PCA mempunyai tiga set karakteristik
atribut yaitu keragaman, loadings, dan skor (Esbensen et al., 1994).
Keragaman memberikan informasi-informasi untuk digunakan pada
komponen utama yang dapt dinyatakan dengan residual variance dan
sedangkan scores menggambarkan sampel. Gabungan plot loadings dan
scores merupakan hasil analisis berupa grafik biplot yang menggambarkan
hubungan antara variabel dan sampel secara keseluruhan (Esbensen et al.,
III. METODOLOGI PENELITIAN
A. ALAT DAN BAHAN
Bahan-bahan yang digunakan dalam pembuatan tempe adalah adalah
kacang kedelai putih Finna, laru LIPI, asam laktat, asam asetat, asam sitrat,
asam fosfat, asam malat, bahan pengasam X, dan bahan pengemas plastik PP.
Bahan-bahan yang digunakan dalam pengujian tempe yang dihasilkan adalah
air, akuades, propilenglikol (PG), glukosa, NaCl, kafein, MSG, flavor meaty,
hexanal, asam oktanoat.
Alat-alat yang digunakan dalam penelitian ini adalah panci, baskom,
tampah, saringan, ember, alat uji organoleptik, gelas ukur, toples kaca, pipet
Mohr, pipet tetes, gelas piala, sealer, dan pHmeter.
B. METODE PENELITIAN
Secara umum penelitian ini terbagi menjadi empat tahap. Tahap pertama
merupakan seleksi metode pengasaman kimiawi dari metode-metode
terdahulu yang bervariasi dalam hal perlakuan (perebusan 30 menit atau
perendaman 2 jam dalam bahan pengasam) maupun jenis asam (asam asetat
dan asam laktat). Metode pengasaman kimiawi terpilih dalam seleksi awal,
yaitu perebusan kedelai dalam asam laktat 0.85% selama 30 menit
(pengasaman laktat 1), dikarakterisasi citarasanya untuk menentukan arah
modifikasi yang akan dilakukan.
Penelitian tahap kedua merupakan modifikasi proses pengasaman dari
pengasaman laktat 1. Metode pengasaman yang diuji pada tahap ini adalah
pengasaman laktat 1 dengan pengurangan konsentrasi asam laktat menjadi
0.3% (pengasaman laktat 3) dan pengasaman laktat 1 yang diikuti perebusan
dalam air bersih selama 20 menit (pengasaman laktat 4). Karakterisasi citarasa
dilakukan terhadap metode pengasaman kimiawi terpilih dalam modifikasi
proses pengasaman, yaitu pengasaman laktat 4. Karakterisasi citarasa tempe
dilakukan modifikasi jenis pengasam yang digunakan pada penelitian tahap
berikutnya.
Tahap ketiga merupakan seleksi metode pengasaman kimiawi yang
telah dimodifikasi bahan pengasamnya (asam fosfat, asam malat, bahan
pengasam X, serta kombinasi asam laktat, asam asetat, dan asam sitrat).
Karakterisasi citarasa dilakukan terhadap metode pengasaman kimiawi terpilih
dalam modifikasi jenis pengasam, yaitu pengasaman X. Tahap keempat hanya
merupakan finishing atau perbaikan proses pengolahan kedelai sebelum
pengupasan dalam pembuatan tempe menggunakan pengasaman X supaya
produk tempenya memiliki citarasa yang lebih mendekati kontrol.
Teknologi pembuatan tempe tradisional yang menjadi basis metode
pembuatan tempe secara umum pada penelitian ini adalah teknologi
pembuatan tempe yang dilakukan oleh pengrajin tempe Sukasari, Bogor.
Tempe yang dihasilkan dari teknologi ini disebut tempe Bogor atau tempe
Magelang. Secara umum teknologi pembuatan tempe ini digambarkan dalam
bagan alir Gambar 2.
Proses pencucian dilakukan dengan merendam kedelai kering dalam
wadah yang berisi air bersih kemudian mengaduknya dengan tangan
berulang-ulang sampai air pencuci menjadi bening. Pemanasan awal dilakukan dengan
memanaskan kedelai dalam air berlebih sampai mendidih, kemudian tetap
dipanaskan dengan api kecil selama 10 menit, dan dibiarkan dalam air rebusan
tersebut selama 1 jam.
Tahap pengasaman kedelai dilakukan hingga keasaman biji kedelai dan
air rendaman turun mencapai nilai pH antara 3.5 sampai 5. Pengasaman yang
dilakukan di pengrajin Sukasari dilakukan secara alami teknologi backsloping
yaitu perendaman kedel