PENGARUH PEMBERIAN PAKAN TEPUNG DAN MINYAK
IKAN LELE, SERTA PROBIOTIK
E. faecium
IS-27526
TERHADAP PROFIL DARAH
Macaca fascicularis
BETINA USIA TUA
NOVIA AKMALIYAH HARJANI
DEPARTEMEN GIZI MASYARAKAT FAKULTAS EKOLOGI MANUSIA
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul pengaruh pemberian pakan tepung dan minyak ikan lele, serta probiotik E. faecium IS-27526 terhadap profil darah Macaca fascicularis betina usia tua adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
NOVIA AKMALIYAH HARJANI. Pengaruh Pemberian Pakan Tepung dan Minyak Ikan Lele, serta Probiotik E. faecium IS-27526 terhadap Profil Darah Macaca fascicularis Betina Usia Tua. Dibimbing oleh CLARA M. KUSHARTO.
Penelitian ini bertujuan menganalisis pengaruh pemberian pakan tepung ikan lele, minyak ikan lele, serta probiotik E. faecium IS-27526 terhadap profil darah monyet ekor panjang (MEP) betina usia tua. Desain penelitian yang digunakan adalah experimental study selama 90 hari. Contoh dalam penelitian ini berjumlah 9 ekor MEP yang telah mengalami masa adaptasi selama 45 hari. Peneliti membagi contoh ke dalam tiga perlakuan, yaitu kelompok tepung ikan lele (A1), kelompok tepung ikan lele + probiotik (A2), dan kelompok tepung ikan lele + probiotik + minyak ikan (A3). Hasil uji sidik ragam menunjukkan bahwa terdapat perbedaan yang nyata (p<0.05) antara perlakuan dengan perubahan kadar eritrosit, hemoglobin, dan hematokrit. Namun, tidak terdapat perbedaan yang nyata (p>0.05) antara perlakuan terhadap perubahan nilai MCV, MCH, MCHC, leukosit, dan trombosit. Lama intervensi dan interaksi perlakuan dengan lama intervensi juga tidak berpengaruh nyata terhadap profil darah monyet ekor panjang.
Kata kunci: profil darah, tepung ikan lele, minyak ikan lele, probiotik, Macaca fascicularis
ABSTRACT
NOVIA AKMALIYAH HARJANI. Effect of Catfish Flour, Catfist Oil, and Probiotic E. faecium IS-27526 Based Feed on Blood Profile of Aged Female Long-tailed Monkeys. Supervised by CLARA M. KUSHARTO.
The aim of this study was to analyze the effect of catfish flour, catfish oil, and probiotic E. faecium IS-27526 based on blood profile of aged female long-tailed monkeys. Experimental design was applied for this study. Feeding trial was conducted in 90 days. Nine monkeys had been conditined on 45 days before this study begun and they were divided into 3 groups of treatment: catfish flour (A1), catfish flour + probiotic (A2), and catfish flour + probiotic + catfish oil (A3). The statistical analysis using ANOVA test showed that significant difference exist (p<0.05) between treatment to the change level of erythrocytes, hemoglobin, and hematocrit. However, no significant difference (p>0.05) were observed between treatment to the change level of MCV, MCH, MCHC, leukocytes, and thrombocytes. The result also showed that the duration of intervention and intervention treatment vs duration of intervention had no significant difference on blood profile of the samples.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Gizi
dari Program Studi Ilmu Gizi pada Departemen Gizi Masyarakat
PENGARUH PEMBERIAN PAKAN TEPUNG DAN MINYAK
IKAN LELE, SERTA PROBIOTIK
E. faecium
IS-27526
TERHADAP PROFIL DARAH
Macaca fascicularis
BETINA USIA TUA
NOVIA AKMALIYAH HARJANI
DEPARTEMEN GIZI MASYARAKAT FAKULTAS EKOLOGI MANUSIA
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Pengaruh pemberian pakan tepung dan minyak ikan lele, serta probiotik E. faecium IS-27526 terhadap profil darah Macaca fascicularis betina usia tua.
Nama : Novia Akmaliyah Harjani NIM : I14100062
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga penelitian dan penulisan naskah skripsi ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilakukan di Pusat Studi Satwa Primata Institut Pertanian Bogor (PSSP-IPB) ini adalah tentang pengaruh intervensi produk tepung ikan lele terhadap profil darah Macaca fascicularis betina usia tua, dengan judul pengaruh pemberian pakan tepung dan minyak ikan lele, serta probiotik E. faecium IS-27526 terhadap profil darah Macaca fascicularis betina usia tua. Penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Prof Dr drh Clara M. Kusharto, M Sc selaku komisi pembimbing yang senantiasa memberi bimbingan, arahan, masukan, dan saran yang membangun kepada penulis.
2. Dr Rimbawan dan Dr Berry Juliandi, S Si, M Si selaku dosen penguji luar komisi yang telah memberikan saran dan penyempurnaan penyusunan naskah skripsi ini.
3. Program Hibah Kompetensi (HIKOM) DIKTI yang telah memberi sponsor pelaksanaan penelitian sebagian bagian dari penelitian utama dengan
judul: ”Makanan fungsional kaya protein, mineral, dan minyak by-product
tepung ikan lele sebagai nutritious dan emergency food untuk lansia”.
4. PT Bimana Indomedical dan PT Carmelitha Lestari atas bantuan dalam sarana dan prasarana penelitian.
5. Kedua orangtua, Ayah Sarjono dan Ibu Anik Sunarni, abang Aditya Tirta Pratama, serta keluarga yang selalu mendoakan, memberikan dukungan dan selalu memberikan semangat penulis selama menyelesaikan penelitian.
6. Marlita Jayanti yang berjuang bersama-sama, saling memberikan dukungan dan motivasi untuk menyelesaikan penelitian ini.
7. Teman-teman Keluarga besar Gizi Masyarakat 47 (April, Lidya, Tina, Icha, Rotua, Emir, Ifdal, Nizaf, Kaka) yang telah memberikan bantuan dan motivasi selama penulis melangsungan studi di Departemen Gizi Masyarakat IPB.
8. Temen-temen A12 Messanger, Ikatan Lembaga Mahasiswa Gizi Indonesia (Septian, Gati, Feni, Desy Prima, Desy Dwi, Nandika, Dini, Hanum, Ari, Aji, Nicol, Tiwi, Siska, Faishal), ILMAGI IPB, A3/280 (Indah, Laras, Icha Prima), Pondok Al-hikmah (Windita, Deti).
9. Seluruh pihak yang telah membantu, baik secara langsung maupun tidak langsung, yang tidak dapat penulis sebutkan satu per satu.
Penulis menyadari bahwa penulisan penelitian ini masih banyak kekurangan. Oleh karena itu, kritik serta saran dari pembaca yang sifatnya membangun sangat penulis harapkan demi perbaikan selanjutnya. Semoga penelitian ini dapat memberikan manfaat.
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 3
Hipotesis 3
Manfaat Penelitian 3
METODE 4
Desain, Waktu dan Tempat 4
Bahan dan Alat 4
Materi 4
Pemeriksaan Darah 7
Rancangan Percobaan dan Analisis Data 8
HASIL DAN PEMBAHASAN 9
Penelitian Pendahuluan 9
Penelitian Utama 10
Sel Darah Merah (Eritrosit) 12
Sel Darah Putih (Leukosit) 20
Platelet (Trombosit) 21
SIMPULAN DAN SARAN 22
Simpulan 22
Saran 22
DAFTAR PUSTAKA 22
LAMPIRAN 27
DAFTAR TABEL
1 Hasil analisis proksimat kandungan gizi pakan monkey chow 5
2 Komposisi pakan perlakuan 6
3 Hasil analisis proksimat kandungan gizi pakan perlakuan 9 4 Rata-rata dan presentasi konsumsi pakan selama intervensi 10
5 Nilai profil darah awal monyet ekor panjang 11
6 Rata-rata nilai profil darah monyet ekor panjang selama perlakuan 12 7 Rata-rata perubahan kadar eritrosit monyet ekor panjang 13 8 Rata-rata perubahan kadar hemoglobin monyet ekor panjang 14 9 Rata-rata perubahan kadar hematokrit monyet ekor panjang 16 10 Rata-rata perubahan kadar MCV monyet ekor panjang 17 11 Rata-rata perubahan kadar MCH monyet ekor panjang 18 12 Rata-rata perubahan kadar MCHC monyet ekor panjang 19 13 Rata-rata perubahan kadar leukosit monyet ekor panjang 20 14 Rata-rata perubahan kadar trombosit monyet ekor panjang 21
DAFTAR GAMBAR
1 Alat Analisis Darah merek Nihon Kohden, Celltac 7
2 Diagram Alir Prosedur Penelitian 8
3 Grafik Kadar Eritrosit Monyet Ekor Panjang Selama Perlakuan 12 4 Grafik Kadar Hemoglobin Monyet Ekor Panjang Selama Perlakuan 14 5 Grafik Kadar Hematokrit Monyet Ekor Panjang Selama Perlakuan 15 6 Grafik MCV Monyet Ekor Panjang Selama Perlakuan 17 7 Grafik MCH Monyet Ekor Panjang Selama Perlakuan 18 8 Grafik MCHC Monyet Ekor Panjang Selama Perlakuan 19 9 Grafik Kadar Leukosit Monyet Ekor Panjang Selama Perlakuan 20 10 Grafik Kadar Trombosit Monyet Ekor Panjang Selama Perlakuan 21
DAFTAR LAMPIRAN
1 Gambar Kandang Monyet Ekor Panjang 27
2 Gambar Pakan Perlakuan 27
3 Gambar Proses Pengambilan Darah pada Monyet Ekor Panjang 27 4 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
eritrosit monyet ekor panjang 28
5 Hasil uji lanjut Duncan perlakuan terhadap perubahan kadar eritrosit
monyet ekor panjang 28
6 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
hemoglobin monyet ekor panjang 28
7 Hasil uji lanjut Duncan perlakuan terhadap perubahan kadar
hemoglobin monyet ekor panjang 28
8 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
9 Hasil uji lanjut Duncan perlakuan terhadap perubahan kadar hematokrit
monyet ekor panjang 29
10 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
MCV monyet ekor panjang 29
11 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
MCH monyet ekor panjang 29
12 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
MCHC monyet ekor panjang 30
13 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
leukosit monyet ekor panjang 30
14 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
trombosit monyet ekor panjang 30
PENDAHULUAN
Latar Belakang
Proses menua adalah sebuah proses yang mengubah orang dewasa sehat menjadi rapuh disertai dengan menurunnya semua sistem fisiologis dan meningkatnya resiko penyakit dan kematian (Darmono 1999). Menurut UU No.13 Tahun 1998 tentang Kesejahteraan Lansia, yang dimaksud dengan kelompok lansia adalah seseorang yang telah mencapai usia 60 tahun atau lebih. Prevalensi lansia di Indonesia terus meningkat, yaitu sebesar 20.5 juta (9%) penduduk Indonesia dan diproyeksikan akan menjadi 11.3% atau sebesar 28.8 juta jiwa pada tahun 2020 (Wirakusumah 2000).
Lansia sangat rentan terhadap berbagai jenis penyakit akibat daya tahan tubuhnya yang melemah. Salah satu masalah kesehatan yang sering dialami lansia yaitu anemia. Anemia terjadi ketika tidak cukupnya sel darah merah yang sehat dalam tubuh (Ulfa 2012). Kondisi ini dapat dideteksi ketika ada angka hemoglobin dalam darah dibawah normal yang sesuai dengan jenis kelamin. Batasan anemia yang telah ditetapkan WHO yaitu untuk wanita apabila konsentrasi hemoglobinnya di bawah 12 gr/dl dan untuk pria apabila konsentrasi hemoglobinnya di bawah 13 gr/dl (Kyriazi 2011). Ada beberapa mekanisme untuk terjadinya anemia, yaitu: kehilangan darah, menurunnya umur hidup sel darah merah (eritrosit), kelainan pada pembentukan sel darah merah (eritrosit), berkumpul dan dihancurkannya eritrosit di dalam limpa yang membesar, dan meningkatnya volume plasma.
Prevalensi anemia pada pria lanjut usia adalah 6-30%, sedangkan pada wanita lanjut usia adalah 10-12%. Akan tetapi, prevalensi tersebut meningkat secara signifikan setelah usia 75 tahun. Pada lansia penderita anemia, berbagai penyakit penyerta lebih mudah timbul dan penyembuhannya akan semakin lama. Prevalensi dan akumulasi penyakit kronik yang meningkat pada lansia, sering memberikan gejala yang mengaburkan sehingga anemia seringkali tidak mendapat perhatian (Bakta 2006).
Menurut hasil studi NHANES III (National Health and Nutrition Examination Study), terdapat 3 penyebab utama anemia pada usia lanjut, yaitu defisiensi gizi/kehilangan darah, inflamasi/penyakit kronik, dan anemia yang tidak dapat dijelaskan (unexplained) (Prasetyo 2008). Proses menua akan berjalan searah dengan menurunnya kapasitas fungsional yang membuat lansia sulit untuk memelihara kestabilan status fisik. Lansia secara progresif akan kehilangan daya tahan terhadap infeksi dan akan makin banyak distorsi metabolik dan struktural yang juga akan menimbulkan gangguan terhadap sistem homopoeisis (Darmono 1999).
2
keunggulan dibandingkan sumber protein lainnya (Adawyah 2007). Ngadiarti et al. (2013) menyatakan ikan lele sebagai produk perikanan unggulan Indonesia yang perlu didukung dan dikembangkan. Tetapi ikan ini mudah rusak karena kandungan airnya yang tinggi (80%). Oleh karena itu diperlukan pengolahan yang sesuai untuk menambah nilainya.
Tepung ikan merupakan salah satu produk hasil olahan ikan. Saat ini penggunaan tepung ikan belum dilakukan secara maksimal. Pembuatan tepung ikan berbahan dasar ikan lele dapat menjadi alternatif bahan pangan. Hal ini yang mendorong dilakukan modifikasi formula makanan bergizi diperkaya tepung dan minyak ikan lele, serta probiotik. Tepung lele telah terbukti dapat membantu meningkatkan status gizi dan kesehatan balita rawan gizi (Kusharto et al. 2008; Adi 2010). Proses pengolahan ikan lele menghasilkan limbah berupa cairan yang mengandung rendemen minyak. Hasil pemurnian dan karakterisasi menunjukkan bahwa minyak ikan lele mempunyai kandungan lemak esensial yang cukup tinggi yaitu 17.79% asam lemak linoleat (C18:2) (omega 6) dan 1,21% asam lemak linolenat (C18:3) (omega 3) (Srimiati 2011). Asam lemak esensial yang terkandung dalam biskuit ikan lele tersebut teruji mempunyai efek anti inflamasi dan anti aterosklerosis (Nugraha 2013). Penambahan probiotik ditujukan untuk meningkatkan status gizi lansia, kesehatan saluran pencernaan, dan respon imun hormonal. Probiotik dapat bertahan hidup dalam saluran cerna, mampu menempel pada epitel usus, kolonisasi mikroba yang menguntungkan dalam saluran cerna, mencegah perkembangan bakteri patogen sehingga teruji secara klinis menguntungkan bagi kesehatan (Salminen et al. 2004).
Pengembangan formula makanan fungsional berbasis tepung dan minyak ikan lele, serta probiotik diusulkan untuk mengoptimalkan hasil penelitian sebelumnya dan membantu menyediakan makanan bergizi siap santap untuk memenuhi kecukupan gizi pada lansia. Selain itu melihat pengaruh makanan fungsional tersebut terhadap kadar profil darah pada lansia untuk mencegah terjadinya anemia. Penelitian ini menggunakan uji pre-klinis pada hewan uji, yaitu monyet ekor panjang (Macaca fascicularis) (MEP), karena primata ini memiliki banyak kemiripan dengan manusia baik dalam hal anatomi maupun fisiologi (Roth et al. 2004).
Perumusan Masalah
Lansia mengalami penurunan sistem fisiologis dalam tubuhnya. Penurunan sistem fisiologis ini salah satunya berhubungan dengan menurunnya kemampuan mencerna vitamin B12, vitamin D, dan kalsium, menurunnya produksi asam
3 Penurunan kemampuan menyerap dan mencerna zat gizi pada lansia menyebabkan lansia rentan mengalami defisiensi zat gizi, sehingga diperlukan makanan fungsional yang dapat dikonsumsi oleh lansia untuk mempertahankan status gizi dan meningkatkan kualitas hidup pada lansia. Salah satunya dengan memberikan makanan fungsional berbasis tepung dan minyak ikan lele serta probiotik.
Tujuan Penelitian
Tujuan Umum
Secara umum penelitian ini bertujuan untuk menganalisis pengaruh pemberian pakan tepung ikan lele, minyak ikan lele, dan probiotik E. faecium IS-27526 terhadap profil darah pada MEP betina usia tua.
Tujuan Khusus
Tujuan khusus dari penelitian ini antara lain:
1. Melakukan pengukuran profil darah MEP betina usia tua.
2. Menganalisis pengaruh pakan tepung dan minyak ikan lele serta probiotik terhadap profil darah MEP betina usia tua.
3. Menganalisis pengaruh lama intervensi terhadap profil darah MEP betina usia tua.
4. Menganalisis pengaruh interaksi perlakuan dengan lama intervensi terhadap profil darah MEP betina usia tua.
Hipotesis
Hipotesis pada penelitian ini antara lain:
1. Pemberian pakan tepung dan minyak ikan lele serta probiotik berpengaruh nyata terhadap profil darah MEP betina usia tua.
2. Lama intervensi berpengaruh nyata terhadap profil darah MEP betina usia tua. 3. Interaksi perlakuan dengan lama intervensi berpengaruh nyata terhadap profil
darah MEP betina usia tua.
Manfaat Penelitian
4
METODE
Desain, Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan April - Juli 2013 yang merupakan bagian dari penelitian Hibah Kompetensi DIKTI berjudul: Makanan Fungsional Kaya Protein, Mineral, dan Minyak by Product Tepung Ikan Lele sebagai Nutritious and Emergency Food untuk Lansia, sehingga terdapat data yang sama dengan penelitian lain yang juga merupakan bagian dari penelitian ini. Penelitian ini dilakukan di Pusat Konservasi dan Studi Primata untuk pemeliharaan dan pemberian perlakuan, Laboratorium Patologi untuk pengujian profil darah MEP, Pusat Studi Satwa Primata-IPB (PSSP-IPB) di Jalan Lodaya II No. 5, Bogor. Pembuatan pakan monyet dilakukan di PT. Carmelitha Lestari Bogor.
Bahan dan Alat
Bahan yang digunakan antara lain yaitu kultur E. faecium IS-27526, minyak ikan lele, bahan pembuatan pakan (tepung daging lele, tepung kepala lele, tepung ubi jalar, isolat kedelai, butter, telur dan gula), bahan pengambilan darah (ketamin 10 mg/kg dan alkohol swap), bahan analisis darah (antikoagulen EDTA).
Peralatan yang digunakan dalam penelitian adalah peralatan untuk kultivasi biomassa probiotik dan analisis mikrobiologi meliputi: shaker-incubator, fermentor, laminar flow, inkubator, autoklaf, mikropipet, bunsen, tabung reaksi, timbangan, cawan petri, centrifuge. Pembuatan pakan diperlukan hand-blender, sendok, timbangan digital, dan panci. Pengambilan dan analisis darah menggunakan syringe 5 ml, tabung vacum dengan larutan EDTA (merek Vacuette Purple Tube 3 ml), kotak pendingin, dan alat analisis darah dengan prinsip volumetric impendance (merek Nihon Kohden, Celltac).
Materi
Hewan Percobaan
Setiap perlakuan menggunakan 3 ekor hewan coba (unit percobaan), sehingga keseluruhan menggunakan 9 ekor hewan coba. Pengambilan sampel 9 ekor digunakan rumus Federer yaitu :
(T-1) (n-1) > 15 (3-1) (n-1) > 15 (3-1) (n-1) > 15 2n > 15+2 = 17 n = 9
Seharusnya jumlah sampel setiap kelompok adalah 9 ekor sehingga jumlah keseluruhan hewan coba 27 ekor. Akan tetapi yang dilakukan pada penelitian hanya sepertiga dari jumlah seharusnya yaitu 3 ekor tiap kelompok (9 ekor jumlah keseluruhan) sehingga dikategorikan pilot study.
5 badan berkisar antara 2–4 kg. Hewan coba telah diovariektomi untuk menghentikan fase bulanan MEP guna mensimulasi menopause pada manusia. Seluruh MEP yang digunakan bebas dari penyakit tuberkulosis (TBC) dan simian retrovirus (SRV). Perlakuan yang melibatkan hewan percobaan dilakukan berdasarkan peraturan yang telah ditentukan oleh Animal Care and Use Commitee (ACUC) yaitu Komisi Kesejahteraan Hewan Percobaan dari Pusat Studi Satwa Primata-IPB (PSSP-IPB) dengan nomor P01.13-IR.
Kandang
Kandang yang digunakan adalah kandang individu stainless steel (squeeze back cage) untuk mempermudah dalam pemeliharaan dan pengendalian dengan ukuran 0.6 x 0.6 x 0.9 m. Hewan dikandangkan dalam kandang yang ditempatkan pada posisi agar antar individu dapat berinteraksi secara audiovisual (Choliq et al. 2013). Setiap kandang dilengkapi dengan tempat pakan dan tempat air minum berupa mangkuk yang terbuat dari logam anti karat. Air minum disediakan secara ad libitum. Pakan yang diberikan sebelum perlakuan berupa pakan komersil (monkey chow) berbentuk pakan padat, kering dan agak keras dengan kandungan gizi pada Tabel 1 dibawah ini.
Tabel 1 Hasil analisis proksimat kandungan gizi pakan monkey chow
No Zat Gizi Kandungan
Penelitian ini fokus pada penggunaan produk pangan fungsional dari tepung dan minyak ikan lele dan probiotik pada MEP. Parameter yang diamati adalah profil darah monyet meliputi sel darah merah (eritrosit), hemoglobin, hematokrit, Mean Corpuscular Volume (MCV), Mean Corpuscular Hemoglobin (MCH), Mean Corpuscular Hemoglobin Concentration (MCHC), sel darah putih (leukosit), dan platelet (trombosit). Tahap ini terdiri dari tiga bagian, yaitu masa persiapan bahan intervensi, masa adaptasi dan masa perlakuan.
a. Persiapan bahan intervensi
6
Pada komposisi pakan juga dilakukan penambahan tepung ubi jalar untuk meningkatkan kandungan serat dalam pakan yang diberikan. Ambarsari et al. (2009) menyatakan bahwa kadar serat tepung ubi jalar Indonesia mencapai 3.93%. Ubi jalar juga mengandung senyawa stakiosa dan rafinosa yang berperan sebagai prebiotik karena tahan terhadap hidrolisis, difermentasi oleh mikrobiota usus, dan menstimulus pertumbuhan probiotik (Nugraha 2013). Minyak ikan lele diberikan sebagai substitusi terhadap butter. Berikut komposisi pakan perlakuan pada Tabel 2 di bawah ini.
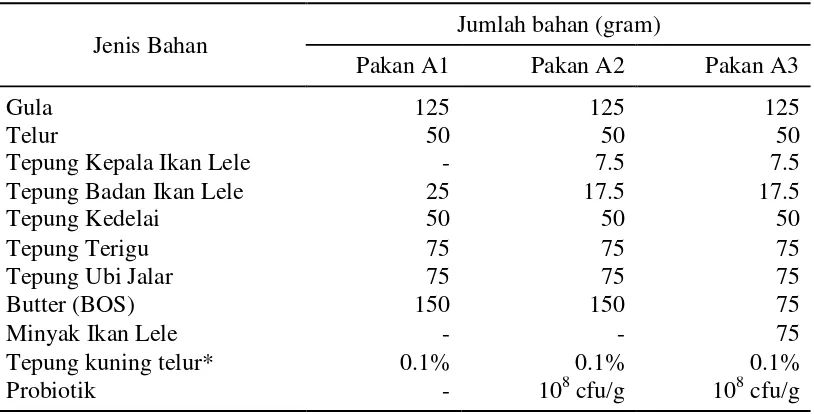
Tabel 2 Komposisi pakan perlakuan
Jenis Bahan Jumlah bahan (gram)
Pakan A1 Pakan A2 Pakan A3
Keterangan : * persentase terhadap jumlah pakan total Sumber : Kusharto et al. (2012)
b. Masa adaptasi
Tahap persiapan pada penelitian utama adalah menyiapkan hewan coba. Hal yang pertama dilakukan adalah mengkarantina hewan untuk memberikan waktu adaptasi kandang selama 30 hari. Selain adaptasi kandang, juga dilakukan adaptasi pakan selama 15 hari, dimana pakan monkey chow dikombinasikan dengan pakan perlakuan dengan perbandingan pakan perlakuan dengan pakan monkey chow 25:75, 50:50, dan 100:0. Adaptasi kandang dan adaptasi pakan bertujuan untuk menghindari terjadinya stres pada hewan coba. Pada H-0 setelah adaptasi, dilakukan pengambilan data dasar yang meliputi kadar eritrosit, hemoglobin, hematokrit, MCV, MCH, MCHC, leukosit, dan trombosit.
c. Masa perlakuan
Pada masa perlakuan, ketiga kelompok hewan akan diberi pakan yang berbeda. Kelompok pertama diberikan pakan tepung ikan lele (pakan standar). Kelompok kedua akan diberikan pakan standar dengan probiotik. Kelompok ketiga diberikan pakan standar yang ditambah dengan minyak ikan lele dan probiotik.
A1 = pakan standar
A2 = pakan standar + probiotik
7 Pakan diberikan dalam bentuk pelet sebanyak 100 gram/hari diberikan dua kali sehari pada pagi dan siang hari. Pertimbangan jumlah pakan yang diberikan sesuai kebutuhan energi MEP yaitu sebesar 120 kkal/kg BB (Bennet et al. 1996). Selain mendapat pakan di atas, MEP juga mendapat pakan tambahan berupa buah-buahan selain pisang karena pisang mengandung inulin, dan untuk menarik minat monyet mengkonsumsi pakan formulasi maka dilakukan pengkayaan lingkungan (environmental enrichment) dengan cara diberi tambahan buah jeruk, apel dan jambu biji sebanyak satu buah perhari.
Pemeriksaan Darah
Pengambilan contoh darah dan analisis darah dilakukan selama empat kali, yaitu pada hari ke-0, 30, 60, dan 90 hari penelitian. Sebelum darah diambil, monyet dibius terlebih dahulu dengan ketamin 10 mg/kg secara intramusculer (Fortman et al. 2001). Darah diambil di daerah vena femoralis menggunakan syringe 5 ml dan dimasukan ke dalam tabung vakum yang berisi antikoagulan EDTA. Bahan yang digunakan dalam pengambilan darah yaitu ketamin 10 mg/kg dan alkohol swap. Bahan yang digunakan dalam analisis darah adalah contoh darah. Alat yang digunakan adalah syringe 5 ml, tabung vacum dengan larutan EDTA (merk vacuette purple tube), kotak pendingin, dan alat analisis darah dengan prinsip volumetric impendance (merek Nihon Kohden, Celltac) dapat dilihat pada Gambar 1.
Gambar 1 Alat Analisis Darah merek Nihon Kohden, Celltac
Perhitungan jumlah sel darah merah (×106/µl), konsentrasi hemoglobin (g/dl), nilai hematokrit (%), sel darah putih (×106/ml), dan trombosit (×103) dilakukan dengan alat analisis darah secara bersamaan. Sampel darah dari tabung vacuette purple tube diuji satu per satu. Hasil dari pembacaan akan tampil pada layar dan tersimpan di memory alat. Nilai MCV, MCH, dan MCHC dihitung dengan menggunakan rumus menurut McGill Virtual Lab (2009):
MCV (fl) = Hematokrit (%) x 10 . Jumlah sel darah merah (ml)
MCH (ρg) = Hemoglobin (g/dl) x 10 .
Jumlah sel darah merah (ml) MCHC (g/dl) = Hemoglobin (g/dl) x 100
8
- adaptasi kandang 30 hari
- adaptasi pakan 10 hari- baseline (titik 0) analisis profil darah - penelitian pendahuluan
Keterangan:
: Variabel yang akan diukur : Variabel yang tidak akan diukur : Hubungan yang diteliti
: Hubungan yang tidak diteliti
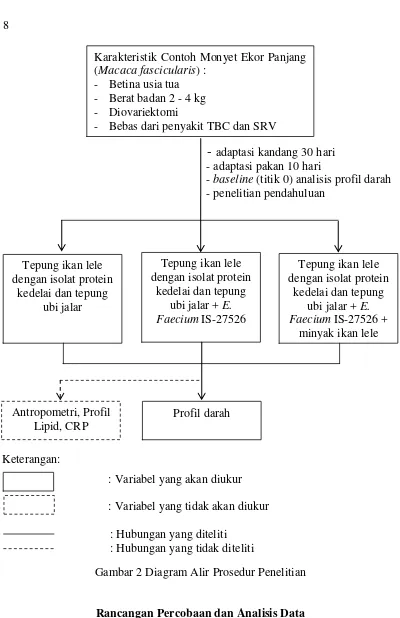
Gambar 2 Diagram Alir Prosedur Penelitian
Rancangan Percobaan dan Analisis Data
Rancangan Percobaan
Rancangan percobaan yang digunakan adalah Rancangan Acak Faktorial (RAF) dengan faktor pengacak kelompok perlakuan dan lama waktu intervensi. Model matematis dari rancangan ini adalah sebagai berikut:
9 ABij : Interaksi antara Faktor A dengan Faktor B Analisis Data
Data diolah dan dianalisis menggunakan program Microsoft Excel 2010 dan Statistical Program for Social Science (SPSS) versi 16.0 for Windows. Tahapan pengolahan data dimulai dari proses entry dan analisis. Pengaruh perlakuan terhadap profil darah MEP dianalisis dengan uji statistik menggunakan Analysis of Variance (ANOVA) dengan uji lanjut Duncan. Analisis statistik dilakukan pada masing-masing parameter pengamatan, yaitu eritrosit, hemoglobin, hematokrit, MCV, MCH, MCHC, leukosit, dan trombosit.
HASIL DAN PEMBAHASAN
Penelitian Pendahuluan
Pakan yang diberikan pada penelitian ini adalah modifikasi formula tepung ikan lele, probiotik, dan minyak ikan lele. Berikut hasil analisis proksimat kandungan gizi pakan perlakuan pada Tabel 3 dibawah ini.
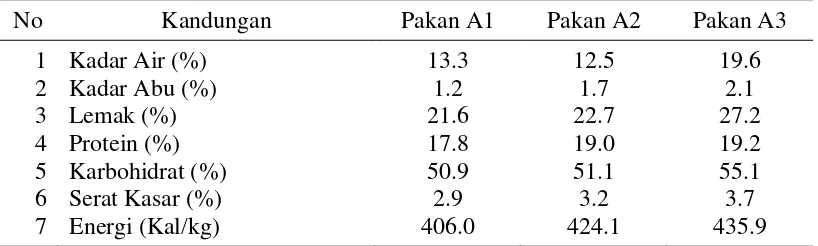
Tabel 3 Hasil analisis proksimat kandungan gizi pakan perlakuan
No Kandungan Pakan A1 Pakan A2 Pakan A3
Keterangan: Jumlah % dalam berat basah. Hasil analisis proksimat Laboratorium Terpadu Institut Pertanian Bogor 2013.
10
senyawa sederhana seperti asam amino, sehingga kebutuhan akan protein dalam pembentukan sel-sel darah dapat terpenuhi (Ali et al. 2013).
Minyak ikan yang berasal dari air tawar (ikan lele, gabus, dan mas) dapat dijadikan sebagai sumber asam lemak omega 6 (Srimiati 2011). Zat gizi utama yang terkandung dalam minyak ini adalah asam lemak tidak jenuh yang sebagian besar berupa asam lemak linoleat (Pudjiadi 1997). Strategi yang dapat digunakan untuk memenuhi kebutuhan asam lemak esensial adalah dengan mengonsumsi minimal 2 ikan setiap minggu (Gebauer et al. 2006).
Ketiga pakan formulasi yang diberikan memiliki kandungan gizi yang tidak jauh berbeda. Pakan A3 yang ditambahkan probiotik dan minyak ikan lele memiliki kadar air, kandungan lemak dan energi yang lebih tinggi dibandingkan pakan lainnya. Sementara kandungan protein pakan yang diberikan tidak jauh berbeda, padahal pakan A1 lebih banyak tepung badan ikan daripada pakan A2 dan A3 yang ditambahkan tepung kepala ikan. Hal ini diduga disebabkan karena pada bagian kepala ikan yang digunakan untuk pembuatan tepung, daging dalam jumlah kecil yang menempel pada kepala tidak dipisahkan, sehingga kandungan proteinnya tidak jauh berbeda. Mervina et al. (2012) menyatakan bahwa kadar protein tepung badan ikan sebesar 63.83% bk, sedangkan kadar protein tepung kepala ikan sebesar 56.04% bk.
Hewan coba mengkonsumsi pakan formulasi selama tiga bulan, tetapi konsumsi pakan MEP selama intervensi menunjukkan respon yang berbeda-beda. Hal ini dikarenakan jenis pakan dan daya terima MEP terhadap pakan yang diberikan selama intervensi. Tabel 4 di bawah ini menggambarkan rata-rata dan persentase konsumsi pakan selama intervensi.
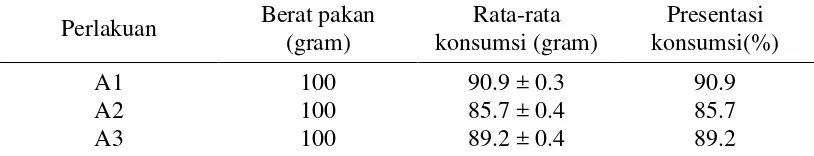
Tabel 4 Rata-rata dan presentasi konsumsi pakan selama intervensi Perlakuan Berat pakan
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Rata-rata konsumsi MEP terhadap ketiga jenis pakan cukup baik, karena mencapai lebih dari 80%. Konsumsi tertinggi pada pakan A1 (90.9%), sedangkan konsumsi terendah pada pakan A2 (85.7%). Perbedaan rata-rata konsumsi dipengaruhi oleh daya terima MEP terhadap pakan yang diberikan. Menurut Bennet et al. (1996), faktor yang dapat mempengaruhi daya terima primata terhadap makanan adalah jenis nutrisi, palatabilitas, bentuk, dan bahan makanan.
Penelitian Utama
11 mempertahankan tubuh terhadap infeksi dan invasi mikroorganisme, serta memelihara keseimbangan asam basa (Mccanca et al. 2010).
Darah akan menghasilkan dua fraksi yang berpisah apabila disentrifusi yaitu fraksi padatan yang disebut butir-butir darah dan fraksi cairan (plasma). Harper et al. (1979) menyatakan bahwa butir darah dapat digolongkan menjadi 3 komponen penting yaitu eritrosit, leukosit dan trombosit. Tabel 5 di bawah ini merupakan kondisi profil darah awal sebelum perlakuan terhadap MEP.
Tabel 5 Nilai profil darah awal monyet ekor panjang
Parameter (Satuan) A1 A2 A3 Nilai
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
*sumber : Fortman et al. 2001
Tabel 5 di atas menunjukkan bahwa hewan coba yang akan diberi pakan A1 memiliki nilai eritrosit, hemoglobin, hematokrit, MCH, dan MCHC yang lebih rendah dibandingkan MEP yang akan diberi pakan A2 dan A3. Profil darah MEP ini menunjukkan bahwa hewan coba mengalami anemia yang ditandai dengan nilai hemoglobin dan hematokrit di bawah nilai normal. Secara umum nilai hemoglobin dan hematokrit digunakan untuk memantau derajat anemia (Kemenkes 2011). Hewan coba yang akan diberi pakan A2 dan A3 memiliki status normal, karena nilai hemoglobin MEP berada pada nilai normal.
Jika melihat nilai leukosit MEP sebelum perlakuan, diketahui bahwa MEP yang akan diberi pakan A1 memiliki nilai yang normal, sedangkan MEP yang akan diberi pakan A2 dan A3 memiliki nilai yang lebih rendah. Hal ini mengindikasikan hewan coba mengalami infeksi virus. Nilai leukosit yang rendah juga dapat disebabkan karena hewan coba mengalami stres (Kemenkes 2011). Nilai trombosit MEP berada di bawah nilai normal mengindikasikan terjadi trombositopenia. Hal ini berhubungan dengan idiopatik trombositopenia purpura (ITP), anemia hemolitik, aplastik, dan pernisiosa (Kemenkes 2011).
12
Tabel 6 Rata-rata nilai profil darah monyet ekor panjang selama perlakuan
Parameter (Satuan) A1 A2 A3 Nilai
Rata-rata Eritrosit (× 106/µl) 3.8±0.9 4.2±0.7 4.5±0.3 4.2±0.3 Hemoglobin (g/dl) 10.8±1.9 11.9±1.8 12.1±0.7 11.6±0.7 Hematokrit (%) 26.4±6.2 29.3±4.9 30.6±2.3 28.7±2.1
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Rata-rata nilai profil darah MEP yang diberi pakan A3 lebih tinggi pada eritrosit, hemoglobin, hematokrit, dan trombosit dibandingkan MEP dengan pakan A1 dan A2, sedangkan MCV, MCH, MCHC, dan leukosit MEP tertinggi pada MEP dengan pakan A1. Apabila dibandingkan dengan nilai normal, nilai profil darah MEP masih belum sesuai pada eritrosit, hematokrit, MCV, MCH, MCHC, dan trombosit. Hal ini diduga disebabkan karena nilai profil darah MEP pada awal intervensi belum menunjukkan nilai yang optimal pada ketiga jenis perlakuan.
Sel Darah Merah (Eritrosit)
Sel darah merah atau eritrosit merupakan jenis sel darah paling umum, berbentuk lempengan bikonkaf dan terpulas merah muda dengan pewarna eosin (Eroschenko 2000). Eritrosit dibentuk di dalam sumsum tulang dengan jangka hidup normal eritrosit pada hewan adalah 115-120 hari. Sel darah merah tua akan hancur dalam limpa, sumsum tulang, dan hati (Mitruka & Rawnsley 2001). Jumlah eritrosit dipengaruhi oleh umur, jenis kelamin, keadaan gizi, masa laktasi, kehamilan, temperatur lingkungan dan ketinggian (Mccance et al. 2010).
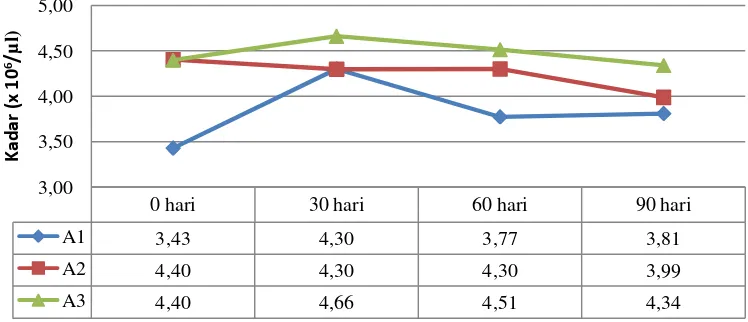
Keterangan: A1= Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 3 Grafik Kadar Eritrosit Monyet Ekor Panjang Selama Perlakuan
13 Jumlah rata-rata eritrosit monyet ekor panjang yang diberi pakan perlakuan sebesar 4.2±0.5(x106/µl). Nilai ini menunjukkan hasil yang tidak jauh berbeda dengan penelitian Soma et al. (2011) yang menyatakan bahwa kadar eritrosit monyet ekor panjang betina antara 3.9±0.5(x106/µl), tetapi hal ini berbeda dengan Fortman et al. (2001) yang menyatakan bahwa nilai normal eritrosit pada monyet ekor panjang adalah 5.3-6.3(x106/µl).
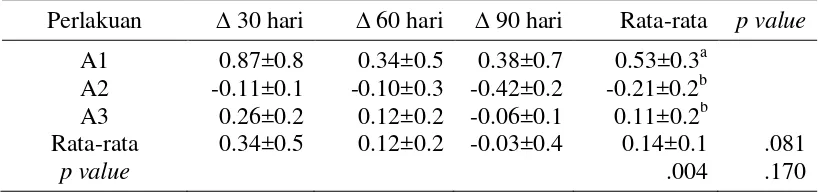
Tabel 7 Rata-rata perubahan kadar eritrosit monyet ekor panjang
Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Berdasarkan Tabel 7 di atas diketahui bahwa rata-rata perubahan eritrosit bulan pertama sebesar 0.34±0.5 (×106/µl) dan mengalami penurunan pada bulan kedua dan ketiga. Hasil analisa sidik ragam menunjukkan bahwa perubahan kadar eritrosit MEP berbeda nyata (p<0.05) antara perlakuan, namun tidak berbeda nyata (p>0.05) terhadap lama intervensi, baik pada bulan pertama, kedua, maupun ketiga, serta tidak berbeda nyata (p>0.05) terhadap interaksi perlakuan dengan lama intervensi. Pemberian pakan A1 dan A3 menunjukkan bahwa terjadi peningkatan nilai eritrosit pada titik 30 hari dan menurun di titik 60 dan 90 hari, sedangkan pemberian pakan A2 menunjukkan terjadi penurunan kadar eritrosit pada titik 30, 60, dan penurunan terbesar terjadi pada titik 90 hari. Perubahan nilai eritrosit pada MEP didasarkan pada pencapaian nilai optimum, sehingga pemberian perlakuan bertujuan untuk mencapai nilai optimum pada kadar eritrosit. Bukan semata-mata hanya meningkatkan nilai eritrosit dalam darah.
Hasil uji lanjut Duncan menunjukkan bahwa perubahan nilai eritrosit MEP perlakuan pakan A1 berbeda nyata dengan perlakuan pakan A2 dan A3. Pakan standar (A1) meningkatkan kadar eritrosit dalam darah, sedangkan pakan A2 dan A3, peningkatan kadar eritrosit dalam darah cenderung lebih sedikit. Hal ini berbeda dengan penelitian Ali et al. (2013) yang menyatakan bahwa pemberian probiotik dalam pakan tambahan dapat menguntungkan bagi ternak, dimana probiotik menyeimbangkan mikroflora usus, meningkatkan ketersediaan nutrient ternak, meningkatkan imun tubuh dan dapat memperbaiki profil darah (jumlah eritrosit, kadar hemoglobin dan hematokrit).
Pembentukan eritrosit memerlukan dua faktor, yaitu faktor ekstrinsik yang ditemukan dalam daging, ragi, hati, dedak, telur, dan susu, serta faktor intrinsik yang dihasilkan oleh mukosa lambung, dan mukosa duodenum. Sitokin, faktor pertumbuhan, hormon, interaksi sel stroma dengan sumsum tulang dan elemen, seperti zat besi (Fe), folat, dan vitamin B12 juga berperan dalam mekanisme proses
14
Proses eritropoeisis tidak dapat berlangsung jika tidak ada vitamin-vitamin, terutama B12, asam folat, B6, riboflavin, asam pantotenat, niasin, asam askorbat,
dan vitamin E, serta zat besi untuk pembentukan hemoglobin dan tembaga sebagai katalisator. Vitamin B12 adalah molekul utama yang dibutuhkan untuk mensekresi
protein (Mccance et al. 2010). Pakan A1 mengandung 25 gram tepung badan ikan lele yang merupakan sumber kalsium (Ca) dan phospor (P), serta mengandung trace element seperti seng (Zn), yodium (I), besi (Fe), mangan (Mn) dan kobalt (Co) (Moeljanto 1982) serta protein yang cukup untuk proses eritropoeisis.
Hemoglobin
Warna merah pada darah disebabkan karena adanya hemoglobin. Hemoglobin dalam eritrosit merupakan besi heme yang mengandung protein (Elliott 2008). Adanya hemoglobin membuat darah dapat mengikat oksigen dalam bentuk oksihemoglobin (HbO2) dan karbondioksida dalam bentuk
karboksihemoglobin HbCO2. Semakin banyak jumlah molekul hemoglobin yang
terkandung dalam sel darah merah, semakin banyak oksigen yang dapat diikat (Frandson 1986).
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 4 Grafik Kadar Hemoglobin Monyet Ekor Panjang Selama Perlakuan Hewan coba yang diberi pakan perlakuan memiliki kadar hemoglobin rata-rata antara 10.8-12.1 g/dl. Hal ini sesuai dengan Fortman et al. (2001) yang menyatakan kadar hemoglobin normal pada MEP adalah 11.0-12.4 g/dl. Sama halnya dengan perubahan nilai eritrosit, perubahan nilai hemoglobin pada MEP juga didasarkan pada pencapaian nilai optimum, yaitu mencapai 11.0-12.4 g/dl.
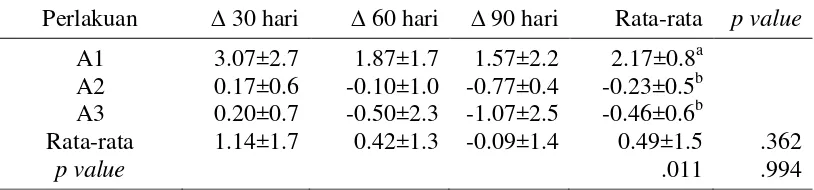
Tabel 8 Rata-rata perubahan kadar hemoglobin monyet ekor panjang Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
15 Tabel 8 di atas menunjukkan perubahan kadar hemoglobin MEP selama tiga bulan perlakuan. Berdasarkan tabel tersebut, diketahui bahwa rata-rata perubahan kadar hemoglobin berbanding lurus dengan perubahan kadar eritrosit. Hasil uji sidik ragam menunjukkan bahwa terdapat perbedaan yang nyata (p<0.05) antara perubahan kadar hemoglobin dengan perlakuan, namun tidak terdapat perbedaan yang nyata (p>0.05) terhadap lama intervensi, dan interaksi perlakuan dengan lama intervensi. Kadar hemoglobin MEP yang diberi pakan A1 mengalami peningkatan selama tiga bulan perlakuan mencapai rata-rata 2.17 g/dl. Hal ini sesuai dengan penelitian Gera et al. (2012) yang menyebutkan bahwa saus ikan memiliki bioavaibilitas heme zat besi yang tinggi, dan fortifikasi Fe pada makanan signifikan meningkatkan Hb (0.42 g/dl).
Hasil uji lanjut Duncan menunjukkan bahwa perubahan kadar hemoglobin perlakuan pakan A1 berbeda nyata dengan pakan A2 dan A3. Kadar hemoglobin meningkat setelah diberi pakan A1, sedangkan pakan A2 dan A3 menurunkan nilai kadar hemoglobin MEP. Hal ini diduga disebabkan karena MEP dengan pakan A1 memiliki nilai hemoglobin yang belum mencapai nilai optimum pada awal perlakuan, sedangan MEP dengan pakan A2 dan A3 sudah mencapai nilai optimum, sehingga MEP dengan pakan A1 lebih banyak menyerap zat gizi yang diberikan karena hewan coba mengalami kekurangan. Hal tersebutlah yang menyebabkan zat gizi lebih banyak terserap dan peningkatan nilai hemoglobin lebih tinggi dibandingkan pakan lain.
Kandungan zat besi dalam tepung ikan lele berperan dalam sintesis hemoglobin, sehingga pemberian perlakuan berperan dalam meningkatkan nilai hemoglobin dalam darah. Selain zat besi, mangan yang terkandung dalam tepung ikan lele berperan dalam metabolisme asam amino, sedangkan kobalt merupakan bagian yang penting dari vitamin B12 untuk membantu mencegah anemia dan
merangsang produksi eritrosit (Marliyati dan Kustiyah 2008). Peningkatan status hemoglobin berkorelasi positif dengan peningkatan status riboflavin. Powers et al. (2011) menyatakan bahwa defisiensi riboflavin pada hewan dapat menurunkan penyerapan.
Hematokrit
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 5 Grafik Kadar Hematokrit Monyet Ekor Panjang Selama Perlakuan
16
Menurut Wijayakusuma dan Sikar (1986), hematokrit adalah persentase sel darah merah dalam 100 ml darah. Pada hewan normal nilai hematokrit sebanding dengan jumlah sel darah merah dan kadar hemoglobin. Kebanyakan hewan mempunyai nilai hematokrit antara 38-48% dengan rataan 40%. Pada hewan percobaan, nilai Hematokrit berkisar antara 26.4-30.6%. Hal ini masih dibawah nilai normal menurut Soma et al. (2011) yang menyatakan kadar hematokrit MEP betina dewasa sebesar 32.1±4.1%. Hematokrit abnormal menunjukkan adanya masalah pada sirkulasi darah merah (Tortora dan Anagnostakos 1990).
Tabel 9 Rata-rata perubahan kadar hematokrit monyet ekor panjang
Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Hasil uji sidik ragam menunjukkan terdapat perbedaan yang nyata (p<0.05) antara perubahan kadar hematokrit MEP dengan perlakuan, namun lama intervensi dan interaksi perlakuan dengan lama intervensi tidak menunjukkan perbedaan yang nyata (p>0.05). Rata-rata kadar hematokrit MEP setelah satu bulan perlakuan mengalami peningkatan sebesar 2.30±3.3% dan cenderung mengalami penurunan pada bulan berikutnya. Perubahan kadar hematokrit ini berbanding lurus dengan kadar eritrosit, yaitu pemberian pakan A1 dan A3 menunjukkan bahwa terjadi peningkatan nilai hematokrit pada titik 30 hari dan menurun di titik 60 dan 90 hari, sedangkan pemberian pakan A2 menunjukkan terjadi penurunan kadar hematokrit pada titik 30, 60, dan penurunan terbesar terjadi pada titik 90 hari.
Hasil uji lanjut Duncan menunjukkan bahwa pakan A1 berbeda nyata dengan pakan A2, namun tidak berbeda nyata dengan pakan A3. Pakan A1 meningkatkan kadar hematokrit MEP, sedangkan pakan A2 cenderung menurunkan kadar hematokrit MEP. Hal ini diduga disebabkan karena MEP dengan pakan A2 sudah memiliki kadar hematokrit yang cukup baik, sehingga asupan makanan yang diberikan tidak terlalu menunjukkan perubahan. Selain itu diduga disebabkan karena status hidrasi MEP baik, sehingga tidak meningkatkan nilai hematokrit. Baldy (1995) menyatakan bahwa hematokrit juga berfungsi untuk menilai status dehidrasi tubuh. Kondisi dehidrasi karena kekurangan cairan, penurunan pasokan cairan, redistribusi dari plasma ke jaringan akibat cidera akan meningkatkan nilai hematokrit.
Mean Corpuscular Volume
17
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 6 Grafik MCV Monyet Ekor Panjang Selama Perlakuan
Gambar 6 menunjukkan bahwa ukuran rata-rata sel darah merah pada MEP adalah 68.6±0.3fl, hal ini lebih dari ukuran normal menurut Fortman et al. (2001) yang menyatakan bahwa nilai MCV pada MEP adalah 59.0-66.0 fl. Nilai MCV akan naik bila ukuran sel darah merah lebih besar dari ukuran normal (macrocytic), contohnya pada anemia yang disebabkan oleh defisiensi vitamin B12
(AACC 2009).
Tabel 10 Rata-rata perubahan kadar MCV monyet ekor panjang
Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Tabel 10 di atas menunjukkan bahwa tidak terdapat perbedaan antara nilai MCV pada pakan perlakuan dan waktu. Hasil uji beda juga menunjukkan bahwa nilai MCV tidak berbeda nyata (p>0.05) terhadap perlakuan, lama intervensi, dan interaksi perlakuan dengan lama intervensi. Setelah diberi pakan perlakuan, nilai MCV MEP cenderung mengalami penurunan, yang berarti ukuran sel semakin kecil, biasanya terjadi karena defisiensi zat besi (AACC 2009). Namun pada percobaan kali ini, penurunan nilai MCV diduga bukan karena defisiensi zat besi, melainkan karena pakan yang diberikan mencoba untuk mencapai nilai optimum untuk kadar MCV pada MEP, dimana pada awal intervensi nilai MCV pada MEP cenderung lebih tinggi dari batas nilai optimum.
Mean Corpuscular Hemoglobin
Mean Corpuscular Hemoglobin (MCH) menunjukkan rata-rata jumlah oksigen terikat hemoglobin yang terdapat dalam satu sel darah merah. Rata-rata
18
nilai MCH MEP yang diberi perlakuan A1, A2, dan A3 berturut-turut adalah 28.5±3.1, 28.0±2.0, 27.0±1.3. Nilai rata-rata MCH MEP tidak terlalu berbeda antara ketiga perlakuan.
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 7 Grafik MCH Monyet Ekor Panjang Selama Perlakuan
Hewan coba dengan perlakuan A3 lebih rendah dibandingkan yang lain. Namun nilai ini lebih tinggi dari nilai normal MCH MEP menurut Fortman et al. (2001) yang mengatakan bahwa rata-rata MCH pada MEP adalah sebesar 19.0-21.0 pg. MCH biasanya akan meningkat dalam keadaan anemia macrocytic yang berhubungan dengan defisiensi vitamin B12 dan asam folat (AACC 2009).
Tabel 11 Rata-rata perubahan kadar MCH monyet ekor panjang
Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Tabel 11 di atas menunjukkan perubahan kadar MCH MEP setelah diberi perlakuan selama tiga bulan. Berdasarkan hasil tersebut diketahui bahwa pemberian perlakuan meningkatkan kadar MCH. Hasil uji sidik ragam menunjukkan bahwa tidak terdapat hubungan yang signifikan (p>0.05) antara perlakuan, lama intevensi, dan interaksi perlakuan dengan lama intevensi terhadap perubahan nilai MCH. Pemberian pakan A1 meningkatkan kadar MCH lebih tinggi dibandingkan yang lain. Peningkatan tertinggi terjadi pada titik ke 60. Pemberian pakan A3 menunjukkan peningkatan kadar MEP yang stabil.
19 Mean Corpuscular Hemoglobin Concentration
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 8 Grafik MCHC Monyet Ekor Panjang Selama Perlakuan
Mean Corpuscular Hemoglobin Concentration (MCHC) merupakan konsentrasi hemoglobin rata-rata pada setiap sel darah merah. Nilai rata-rata MCHC MEP dengan tiga perlakuan tidak jauh berbeda. Nilai MCHC tertinggi pada MEP yang diberi pakan A1, namun nilai MCHC ini masih diatas batas normal menurut Fortman et al. (2001). Penurunan nilai MCHC (hypochromia) terlihat pada kondisi hemoglobin dalam sel darah merah yang encer. Hal ini dapat terjadi karena anemia defisiensi zat besi dan thalasemia. Peningkatan nilai MCHC (hyperchromia) terlihat pada kondisi hemoglobin dalam sel darah merah yang pekat. MCHC dapat turun saat nilai MCV turun, sedangkan peningkatannya terbatas hanya sampai pada jumlah hemoglobin yang layak dalam kapasitas tampung sebuah sel darah merah (AACC 2009).
Tabel 12 Rata-rata perubahan kadar MCHC monyet ekor panjang
Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Uji sidik ragam menunjukkan bahwa tidak terdapat perbedaan yang signifikan (p>0.05) antara nilai MCHC dengan perlakuan, lama intevensi, dan interaksi perlakuan dengan lama intevensi yang diberikan. Perubahan nilai MCHC sama dengan perubahan nilai MCH, yaitu MCHC MEP yang diberi pakan A1 memiliki perubahan yang paling tinggi, diikuti dengan pakan A3 dan A2.
20
Sel Darah Putih (Leukosit)
Sel darah putih (leukosit) merupakan sel yang berfungsi untuk mempertahankan tubuh terhadap mikroorganisme yang menyebabkan infeksi dan berperan dalam sistem kekebalan tubuh (Mccance et al. 2010).
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 9 Grafik Kadar Leukosit Monyet Ekor Panjang Selama Perlakuan Penyimpangan persentase jumlah dari diferensiasi sel darah putih menunjukkan kondisi patologis yang serius, misalnya infeksi, demam dan influenza, alergi, serta serangan virus (Benson et al. 1999). Rata-rata nilai leukosit MEP dengan perlakuan A1 lebih tinggi dibandingkan A2 dan A3.
Tabel 13 Rata-rata perubahan kadar leukosit monyet ekor panjang
Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Hasil sidik ragam pengaruh perlakuan terhadap perubahan kadar leukosit monyet ekor panjang menunjukkan bahwa tidak terdapat perbedaan yang signifikan (p>0.05) antara perlakuan, lama intevensi, dan interaksi perlakuan dengan lama intevensi. Pemberian pakan perlakuan terhadap MEP meningkatkan kadar leukosit dalam darah yang berarti meningkatkan daya tahan terhadap infeksi. Peningkatan terbesar terjadi pada MEP yang diberi pakan A3, kemudian pakan A2, sedangkan peningkatan terendah terjadi pada MEP yang diberi pakan A1.
Pakan A2 dan A3 mengandung probiotik yang berperan dalam mempertahankan dan memperbaiki saluran cerna, serta berperan dalam respon imun. Rieuwpassa (2004) menunjukkan bahwa pemberian biskuit berbasis tepung ikan teri dan krim probiotik E. faecium IS-27526 pada balita dapat meningkatkan
21 respon imun tubuh. Mekanisme pertahanan intestinal oleh probiotik salah satunya dengan merangsang respon sel imun dan mengaktivasi respon kekebalan dan inflamasi (Lu dan Walker 2001).
Platelet (Trombosit)
Platelet (trombosit) tidak berbentuk sel, tetapi menyerupai cakram sitoplasma yang penting dalam proses pembekuan darah (Mccance et al. 2010). Nilai normal kadar trombosit pada manusia antara 150-400 (× 103), namun kemoterapi, radioterapi, demam berdarah, hepatitis kronis, infeksi virus atau ketidakseimbangan dalam sistem kekebalan tubuh dapat menyebabkan jumlah trombosit abnormal. Sayuran berdaun hijau, seperti brokoli, bayam, dan kangkung kaya akan vitamin dan mineral yang penting untuk pembekuan darah dan terbentuknya trombosit (Dutt 2013).
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Gambar 10 Grafik Kadar Trombosit Monyet Ekor Panjang Selama Perlakuan Rata-rata trombosit MEP yang diberi perlakuan A1, A2, dan A3 berturut-turut adalah 228.3±57.0, 242.9±60.0, dan 268.8±37.3 (× 103). Rata-rata ini masih dibawah kadar normal menurut Fortman et al. (2001), yaitu 300.0-512.0 (× 103).
Tabel 14 Rata-rata perubahan kadar trombosit monyet ekor panjang
Perlakuan ∆ 30 hari ∆ 60 hari ∆ 90 hari Rata-rata p value
Keterangan: A1 = Pakan standar; A2 = Pakan standar + probiotik; A3 = Pakan standar + probiotik + minyak ikan lele
Hasil uji sidik ragam menunjukkan bahwa tidak terdapat perbedaan yang signifikan (p>0.05) antara perubahan trombosit dengan perlakuan yang diberikan,
22
lama intevensi, dan interaksi perlakuan dengan lama intevensi. Perubahan kadar trombosit MEP pakan A1 mengalami penurunan dengan nilai rata-rata sebesar 14.0 (× 103). Peningkatan kadar trombosit tertinggi terjadi pada MEP dengan pakan A3, yaitu mencapai 35.0 (× 103). Hal ini diduga karena pakan A3 mengandung asam lemak omega 3 yang dapat meningkatkan jumlah trombosit yang rendah (Dutt 2013). Asam lemak esensial yang terkandung pada pakan A3 juga teruji mempunyai efek anti inflamasi (Nugraha 2013).
SIMPULAN DAN SARAN
Simpulan
Profil darah MEP yang diukur meliputi eritrosit, hemoglobin, hematokrit, MCV, MCH, MCHC, leukosit, dan trombosit dengan nilai rata-rata berturut-turut adalah 4.2±0.3 (× 106/µl), 13.3±3.5 (g/dl), 28.7±2.1 (%), 68.6±0.3 (fl), 27.9±0.8 (pg), 40.6±1.0 (× 106/ml), dan 247±20 (× 103). Hasil pengukuran profil darah MEP betina usia tua menunjukkan bahwa rata-rata nilai profil darah masih belum mencapai nilai optimum.
Hasil uji ragam menunjukkan bahwa terdapat perbedaan yang signifikan (p<0.05) antara perlakuan dengan nilai eritrosit, hemoglobin, dan hematokrit. Namun tidak terdapat perbedaan yang signifikan (p>0.05) antara perlakuan dengan nilai MCV, MCH, MCHC, leukosit, dan trombosit. MEP yang diberi pakan A1 memberikan perubahan kadar eritrosit, hemoglobin, dan hematokrit lebih tinggi dari pada MEP dengan pakan A2 dan A3. Hal ini diduga disebabkan karena MEP dengan pakan A1 memiliki nilai eritrosit, hemoglobin, dan hematokrit yang lebih rendah daripada pakan lain sebelum perlakuan serta belum mencapai nilai optimum, sehingga penyerapan kandungan gizi lebih maksimal untuk mencapai nilai optimum. Lama intevensi serta interaksi perlakuan dengan lama intevensi tidak memberikan perbedaan yang signifikan (p>0.05) terhadap profil darah MEP betina usia tua.
Saran
Sebaiknya sebelum melakukan analisis profil darah, kondisi kesehatan MEP harus dalam kondisi yang sama sebelum perlakuan, sehingga penyerapan zat gizi antar perlakuan dapat sama dan dapat diketahui pengaruh pakan perlakuan terhadap profil darah.
DAFTAR PUSTAKA
23 Adawyah R. 2007. Pengelohan dan Pengawetan Ikan. Jakarta (ID): Bumi Aksara. Adi AC. 2010. Efikasi pemberian makanan tambahan (PMT) biscuit diperkaya dengan tepung protein ikan lele dumbo (Clarias gariepinus) isolate protein kedelai dan probiotik Enterococcus faecium IS-27526 yang dimikroenkapsulasi pada balita (2-5 tahun) berat badan rendah [disertasi]. Bogor (ID): Institut Pertanian Bogor.
Ali AS, Ismoyowati, dan Indrasanti D. 2013. Jumlah eritrosit, kadar hemoglobin dan hematokrit pada berbagai jenis itik lokal terhadap penambahan probiotik dalam ransum. Jurnal Ilmu Peternakan. 1(3): 1001-1013.
Ambarsari I, Sarjana, Choliq A. 2009. Rekomendasi dalam penetapan standar mutu tepung ubi jalar. Jurnal Standardisasi. 11(3): 212-219.
Bakta IM. 2006. Pendekatan terhadap pasien anemia. Dalam: Sudoyo AW, Setyohadi B, Alwi I, Simadibrata KM, Setiyati S, ed. Buku Ajar Ilmu Penyakit Dalam. Jakarta (ID): Universitas Indonesia.
Baldy CM. 1995. Patofisiologi Konsep Klinis Proses-Proses Penyakit. Jakarta (ID): EGC.
Barrow PA. 1992. Probiotics the Scientific Basic. 1st Ed. London (UK): Chapman and Hall.
Bennet BT, Abee CR, Henrickson R. 1996. Non Human Primates in Biomedical Research: Biology and Management. New York (US): Academic Press Inc.
Benson HJ, Gunstream SE, Tolaro A, Tolaro KP. 1999. Anatomy and Physiology Laboratory Textbook. Boston (US): Mc-Graw Hill.
Choliq C, Suparto IH, Iriani S, Sajuthi D. 2013. Bobot badan, indeks massa tubuh, dan glukosa darah monyet ekor panjang (macaca fascicularis) yang diberi pakan berenergi tinggi dan nikotin cair. Acta Veterinaria Indonesiana. 1(1): 20-26.
Collado CM, Surono I, Meriluoto J, Salminen S. 2007. Indigenous dadih lactic acid bacteria: cell-surface properties and interaction with phatogens. Journal of Food Science. 72(3):89-93.
Darmono B. 1999. Demografi dan Epidemiologi Populasi Lanjut Usia. Jakarta (ID): Universitas Indonesia.
Departemen Perdagangan 1982. dalam Mervina. 2009. Formulasi biskuit dengan substitusi tepung ikan lele dumbo (Clarias gariepinus) dan isolat protein kedelai (Glycine max) sebagai makanan potensial untuk anak balita gizi kurang [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Dharmawan SN. 2002. Pengantar Patologi Klinik Veteriner. Bukit Jimbaran (ID): Udayana Press.
Dutt S. 2013. Those with a low platelet count benefit from a healthy diet [internet]. [diakses pada 2014 Juli 22]. Tersedia dari http://scmp.com/lifestyle/health/ article/1234646/those-low-platelet-count-benefit-healthy-diet.
24
Eroschenko PV. 2000. Di Fiores Atlas of Histology with Functional Correlations. Mascow (RU): Academic Press Inc.
Fortman JD, Hewett TA, Bennett BT. 2001. The Laboratory Nonhuman Primates. London [UK]: CRC Press.
Frandson RD. 1986. Anatomi Fisiologi Ternak. Edisi ke-4. Yogjakarta (ID): Universitas Gadjah Mada.
Gebauer SK, Psota TL, Harris WS, Kris-Etherton PM. 2006. n-3 Fatty acid dietary recommendations and food sources to achieve essentiality and cardiovascular benefits. Am J Clin Nutr. 83: 1526S-35S.
Gera T, Sachdev HS, Boy E. 2012. Effect of iron-fortified foods on hematologic and biological outcomes: systematic review of randomized controlled trials. Am J Clin Nutr. 96: 309-24
Harper HA, Rodwell VW, Mayes PA. 1979. Diterjemahkan oleh: Martin Muliawan. Biokimia [Review of Physiological Chemistery] 17th Edition. Canada (CA): Lange Medical Publications.
[KEMENKES] Kementrian Kesehatan Republik Indonesia. 2011. Pedoman Interpretasi Data Klinik. Jakarta (ID).
Khomsan A. 2004. Peran Pangan dan Gizi untuk Kualitas Hidup. Jakarta (ID): PT. Grasindo.
Kusharto CM, Marliyati SA, Surono IS, Amalia, Astawan M, Dewi M. 2008. Makanan fungsional berbasis protein ikan dan probiotik untuk meningkatkan daya tahan tubuh anak balita rawan gizi. Bogor (ID): Institut Pertanian Bogor.
__________________________________, Dainy N. 2012. Makanan fungsional biskuit Clarias kaya protein, mineral dan serat, dengan penambahan minyak ikan lele sebagai nutritious and emergency food untuk lansia. Bogor (ID): Institut Pertanian Bogor
Kyriazi VI. 2011. A holistic approach of erythropoiesis and iron anemia. Health Science Journal. 5(3): 176-181.
Lu L & Walker WA. 2001. Phatologic and physiologic interactions of bacteria with the gastrointestinal ephitelium. Am J Clin Nutr. 73: 1124S-1130S. Marliyati SA, Kustiyah L. 2008. Diktat Mata Kuliah Ilmu Gizi Dasar. Bogor [ID]:
Institut Pertanian Bogor.
25 Mervina, Kusharto CM, Marliyati SA. 2012. Formulasi biskuit dengan substitusi tepung ikan lele dumbo (Clarias gariepinus) dan isolat protein kedelai (Glycine max) sebagai makanan potensial untuk anak balita gizi kurang. J. Teknol. dan Industri Pangan. 23(1)
Mitruka BM & Rawnsley HM. 2001. Clinical Biochemical and Hematological Reference Values in Normal Experimental Animals. New York (US): Masson.
Moeljanto. 1982. Pengolahan Hasil-Hasil Samping Ikan. Jakarta (ID): PT Penebar Swadaya.
Ngadiarti I, Kusharto CM, Briawan D, Marliyati SA, Sayuthi D. 2013. Kandungan asam lemak dan karakteristik fisiko-kimia minyak ikan lele dan minyak ikan lele terfermentasi. Journal Gizi dan Makanan. 36(1): 82-90. Nugraha EAS. 2013. Pengaruh probiotik Enterococcus faecium is-27526 dan
minyak ikan lele (Clarias gariepinus) dalam biskuit fungsional yang diperkaya dengan tepung ikan lele dan tepung ubi jalar (Ipomoea sp.) terhadap profil mikrobiota fekal monyet ekor panjang (Macaca fascicularis) betina usia tua [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Ohta M. 2009. Management of Anemia in the elderly. Journal of the Japan Medical Association. 52(4): 219-223.
Powers HJ, Hill MH, Mushtaq S, Dianty JR, Majsak-Newman G, Williams EA. 2011. Correcting a marginal riboflavin deficiency improves hematologic status in young women in the United Kingdom (RIBOFEM). Am J Clin Nutr. 93: 1274-84.
Prasetyo YF. 2008. Hubungan usia terhadap anemia pada pasien geriatri dengan penyakit kronik [skripsi]. Semarang (ID): Universitas Diponegoro.
Pudjiadi. 1997. Ilmu Gizi Klinis pada Anak. Jakarta [ID]: Universitas Indonesia Rieuwpassa F. 2004. Biskuit konsentrat ikan dan probiotik sebagai makanan
tambahan untuk meningkatkan antibodi igA dan status gizi balita [disertasi]. Bogor (ID): Institut Pertanian Bogor.
Rifqi MA. 2014. Pengaruh pemberian pakan berbasis tepung, minyak ikan lele (Clarias gariepinus) dan probiotik terhadap berat badan, profil lipid, dan C-reactive protein monyet ekor panjang betina usia tua [tesis]. Bogor: Institut Pertanian Bogor.
Roth GS, Mattison JA, Ottinger MA, Chachich ME, LAne MA, Ingram DK. 2004. Aging in rhesus monkey: relevance to human health intervention. Science 305: 1423-1426.
Russell RM. 2000. The aging process as a modifier of metabolism. Am J Clin Nutr. 72: 529S-32S.
26
Sari DD. 2009. Profil darah monyet ekor panjang (Macaca fascicularis) yang diberi pakan berenergi tinggi pada periode obesitas empat bulan kedua [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Soma IG, Wandia IN, Putra IGAA, Silta R. 2011. Profile of whole blood wild long tail monkey (Macaca fascicularis) in nature habitat. Kongres Asosiasi Farmakologi dan Farmasi Veteriner Indonesia, Denpasar 26 Maret.
Srimiati M. 2011. Pemurnian minyak hasil samping penepungan ikan lele dumbo (Clarias gariepinus) sebagai alternatif sumber asam lemak omega 6 [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Suparto IH, Oktarina R, Astuti D, Mansjoer SS, Sajuthi D. 2010. Profil lipid darah pada monyet ekor panjang (Macaca fascicularis) yang diinduksi diet tinggi lemak. Bogor (ID): Institut Pertanian Bogor.
Surono. 2004. Probiotik Susu Fermentasi dan Kesehatan. Jakarta (ID): YAPMMI. Tortora GJ, Anagnostakos NP. 1990. Principles of Anatomy and Physiology. New
York (US): Harper and Row Publisher.
Ulfa M. 2012. Profil anemia pada lansia di Panti Sosial Tresna Werdha Budhi Luhur dan hubungannya dengan faktor-faktor resikonya [skripsi]. Yogyakarta (ID): Universitas Muhammadiyah Yogyakarta.
Wijayakusuma R, Sikar SHS. 1986. Fisiologi Hewan Jilid II. Kumpulan Materi Kuliah. Bogor [ID]: Institut Pertanian Bogor.
27
LAMPIRAN
Lampiran 1 Gambar Kandang Monyet Ekor Panjang
Lampiran 2 Gambar Pakan Perlakuan
28
Lampiran 4 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar eritrosit monyet ekor panjang
Sumber JK Db KT F Sig.
Model 3.363 8 .420 2.574 .046
Intersep .558 1 .558 3.414 .081
Perlakuan 2.489 2 1.245 7.621 .004
Waktu .639 2 .320 1.957 .170
Perlakuan*Waktu .235 4 .059 .359 .834
Galat 2.940 18 .163
Total 6.860 27
Lampiran 5 Hasil uji lanjut Duncan perlakuan terhadap perubahan kadar eritrosit monyet ekor panjang
Perlakuan N Subset untuk α = 0.05
1 2
Pakan kontrol + probiotik 9 -2089
Pakan kontrol + probiotik + minyak ikan 9 .1078
Pakan kontrol 9 .5322
Sig. .114 1.000
Lampiran 6 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar hemoglobin monyet ekor panjang
Sumber JK Db KT F Sig.
Model 45.639 8 5.705 1.775 .148
Intersep 6.551 1 6.551 2.039 .170
Perlakuan 38.056 2 19.028 5.922 .011
Waktu 6.912 2 3.456 1.075 .362
Perlakuan*Waktu .670 4 .168 .052 .994
Galat 57.840 18 3.213
Total 110.030 27
Lampiran 7 Hasil uji lanjut Duncan perlakuan terhadap perubahan kadar hemoglobin monyet ekor panjang
Perlakuan N Subset untuk α = 0.05
1 2
Pakan kontrol + probiotik + minyak ikan 9 -.4556
Pakan kontrol + probiotik 9 -.2333
Pakan kontrol 9 2.1667
29 Lampiran 8 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar
hematokrit monyet ekor panjang
Sumber JK Db KT F Sig.
Model 161.843 8 20.230 2.400 .059
Intersep 17.120 1 17.120 2.031 .171
Perlakuan 115.659 2 57.829 6.861 .006
Waktu 35.645 2 17.823 2.114 .150
Perlakuan*Waktu 10.539 4 2.635 .313 .866
Galat 151.727 18 8.429
Total 330.690 27
Lampiran 9 Hasil uji lanjut Duncan perlakuan terhadap perubahan kadar hematokrit monyet ekor panjang
Perlakuan N Subset untuk α = 0.05
1 2
Pakan kontrol + probiotik 9 -1.6222
Pakan kontrol + probiotik + minyak ikan 9 .5778 .5778
Pakan kontrol 9 3.4333
Sig. .125 .051
Lampiran 10 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar MCV monyet ekor panjang
Sumber JK Db KT F Sig.
Model 1.400 8 .175 .191 .989
Intersep 3.630 1 3.630 3.955 .062
Perlakuan .009 2 .004 .005 .995
Waktu 1.342 2 .671 .731 .495
Perlakuan*Waktu .049 4 .012 .013 1.000
Galat 16.520 18 .918
Total 21.550 27
Lampiran 11 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar MCH monyet ekor panjang
Sumber JK Db KT F Sig.
Model 9.765 8 1.221 .648 .728
Intersep 57.495 1 57.495 30.528 .000
Perlakuan 6.005 2 3.003 1.594 .230
Waktu .723 2 .361 .192 .827
Perlakuan*Waktu 3.037 4 .759 .403 .804
Galat 33.900 18 1.883
30
Lampiran 12 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar MCHC monyet ekor panjang
Sumber JK Db KT F Sig.
Model 21.079 8 2.635 .810 .603
Intersep 147.935 1 147.935 45.467 .000
Perlakuan 11.645 2 5.823 1.790 .196
Waktu 3.525 2 1.763 .542 .591
Perlakuan*Waktu 5.908 4 1.477 .454 .768
Galat 58.567 18 3.254
Total 227.580 27
Lampiran 13 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar leukosit monyet ekor panjang
Sumber JK Db KT F Sig.
Model 40.652 8 5.081 .889 .545
Intersep 98.231 1 98.231 17.192 .001
Perlakuan 13.352 2 6.676 1.168 .333
Waktu 20.447 2 10.224 1.789 .196
Perlakuan*Waktu 6.853 4 1.713 .300 .874
Galat 102.847 18 5.714
Total 241.730 27
Lampiran 14 Hasil uji sidik ragam 2 arah (univariate ANOVA) perubahan kadar trombosit monyet ekor panjang
Sumber JK Db KT F Sig.
Model 15163.630 8 1895.454 .293 .959
Intersep 2205.037 1 2205.037 .341 .567
Perlakuan 10724.963 2 5362.481 .829 .453
Waktu 2457.852 2 1228.926 .190 .829
Perlakuan*Waktu 1980.815 4 495.204 .077 .988
Galat 116495.333 18 6471.963
31
32
RIWAYAT HIDUP
Penulis merupakan putri bungsu dari dua bersaudara pasangan ayah Sarjono dan ibu Anik Sunarni yang dilahirkan di Sangatta pada tanggal 13 November 1991. Penulis menyelesaikan pendidikan di SMA Negeri 1 Sangatta Utara, Kalimantan Timur pada tahun 2010 kemudian melanjutkan pendidikan di Institut Pertanian Bogor melalui Undangan Seleksi Masuk IPB (USMI) dan diterima di Departemen Gizi Masyarakat, Fakultas Ekologi Manusia, IPB.