ABSTRAK
PERILAKU OKSIDASI BAJA AISI 4130 PADA TEMPERATUR 850 °C Oleh
INDRA IRAWAN
Baja AISI 4130 merupakan baja karbon rendah yang memiliki keuletan tinggi dan mudah dibentuk, namun kekerasannya rendah. Produk baja ini biasanya berbentuk pipa dengan permukaan halus (seamless steel). Pemilihan baja AISI 4130 untuk sistem perpipaan pada pembangkit tenaga panas bumi, pembuatan kapal dan sistem perpipaan pada boiler merupakan aspek yang sangat penting dan perlu mendapatkan perhatian khusus. Baja ini rentan terhadap korosi terutama bila berada pada temperatur tinggi, dan lingkungan yang mengandung unsur-unsur kimia seperti klor dan sulfur. Untuk menunjang kemampuan material baja AISI 4130 penting dilakukan penelitian terhadap perilaku oksidasi baja AISI 4130 pada temperatur 850 °C.
Pengujian dilakukan untuk melihat pertambahan berat terhadap waktu lamanya oksidasi, dan menganalisa produk oksidasi yang dilakukan dengan metode X-RD, SEM/EDS, dan OM. Proses pengujian spesimen diuji dengan dioksidasi pada temperatur 850 °C dengan periode waktu yang digunakan 1, 4, 9, 25, 49, dan 72 jam.
Dari hasil pengujian laju oksidasi baja AISI 4130 yang dioksidasi pada temperatur 850 °C menunjukan bahwa temperatur tinggi dapat meningkatkan laju korosi lebih cepat dibandingkan dengan udara biasa, karakteristik pembentukan oksida besi yang tumbuh pada permukaan logam, serta fasa yang terbentuk berupa lapisanhematite(Fe2O3),magnetite(Fe3O4), dan lapisanwustite(FeO).
ABSTRACT
OXIDATION BEHAVIOR OF AISI 4130 STEEL AT A TEMPERATURE 850 °C needs special attention. Steel is susceptible to corrosion, especially when it is at high temperature, and environment containing chemical elements such as chlorine and sulfur. To support the ability of AISI 4130 steel material, important to study the oxidation behavior of AISI 4130 steel at a temperature of 850 ° C.
Tests performed to show the weight of the time duration of oxidation, and the oxidation product analyzes performed by the method of X-RD, SEM / EDS, and OM. The process of testing the specimens tested with oxidized at a temperature of 850 ° C with the time period used 1, 4, 9, 25, 49, and 72 hours.
From the test results of AISI 4130 steel oxidation rate is oxidized at a temperature of 850 ° C showed that high temperatures can increase the rate of corrosion faster than normal air, the characteristics of the formation of iron oxide that grows on the surface of the metal, as well as the phase that forms a layer of hematite (Fe2O3) , magnetite (Fe3O4), and a layer of wustite (FeO).
P
✗ ✘IL
✙KU OKSI
✚✙SI
✛ ✙J
✙✙ISI 4
✜3
✢P
✙✚ ✙T
✗✣P
✗✘✙TUR 85
✢°
✤
O✥✦✧
IN★R✩ IR✩✪✩N
S✫r✬ps✬
S✦bagai Salah Satu Syarat Untuk Mencapai Gelar SARJANA TEKNIK
Pada
JurusanTeknikMesin
FakultasTeknikUniversitas Lampung
FAKULTAS TEKNIK
UNIVERSITAS LAMPUNG
✭✮✯✰✱✰✲✳ ✮ ✴✵✶
✷✸✹ ✺✻✼✽ ✾✼✻ ✿❀✼❁❂ ✿✹ ✾✼ ✷❁✼✹ ❃✽ ✸❄ ✺ ❅ ✿✾✿ ❆ ✿✹❃ ❃ ✿✻ ❇❈ ❉ ✿❁✸❆ ❇❊❊ ❋ ✽ ✸●✿❃ ✿✼ ✿✹✿❂ ❅✸❁ ❆ ✿❍✿ ✾ ✿❁✼ ❆✼❃✿ ●✸❁✽ ✿✺✾✿❁ ✿, ✾ ✿❁✼ ❅✿✽ ✿✹ ❃ ✿✹✷ ✺■✼❏ ✿❁❆❑✹ ❑✾ ✿✹▲✼❆✼ ▲✿✻ ✿❍✿❀▼
✷✸✹✾ ✼✾✼❂✿✹ ▲✸❂ ❑✻ ✿❀ ◆ ✿✽ ✿❁ ❖✸❃✸❁ ✼ ❇ P ✺✻ ✺✹ ❃ ✿❃ ✺✹ ❃ ✾ ✼✽ ✸✻✸✽ ✿✼❂✿✹ ❅✿✾ ✿ ❆ ✿❀ ✺✹ ◗❋❋❇, ▲✸❂❑ ✻ ✿❀ ❘ ✿✹ ■✺❆ ✿✹ P ✼✹❃❂✿❆ ✷✸❁❆ ✿❍✿❖✸❃✸❁ ✼ ❇❙ ✿✾✼✹ ❃❚✸ ■❑ ✾✼✽ ✸✻✸✽ ✿✼❂ ✿✹❅✿✾ ✿ ❆ ✿❀ ✺✹ ◗❋ ❋❈, ▲✸❂❑ ✻ ✿❀❉✸✹✸✹ ❃ ✿❀ ❯❆ ✿✽ ❖✸❃ ✸❁✼ ❇ ❙ ✿✾✼✹ ❃ ❚✸ ■❑ ✾ ✼✽✸✻✸✽ ✿✼❂✿✹ ❅✿✾ ✿ ❆ ✿❀✺✹ ◗❋ ❋ ❱,✾✿✹ ❅✿✾ ✿ ❆ ✿❀✺✹ ◗❋❋❱ ❅ ✸✹ ✺✻✼✽ ❆✸❁ ✾ ✿❲❆ ✿❁ ✽ ✸●✿❃✿✼ ❉✿❀✿✽ ✼✽ ❄ ✿ P✸❂ ✹✼❂ ❉✸✽ ✼✹ ❳✿❂ ✺✻❆ ✿✽ P✸❂✹ ✼❂ ❨✹ ✼❩✸❁ ✽✼❆ ✿✽ ❘ ✿❍❅ ✺✹❃❍✸ ✻ ✿✻ ✺✼■✿✻ ✺❁ ▲✸✻✸❂ ✽ ✼✷✸✹✸❁ ✼❍✿✿✹❉✿❀ ✿✽ ✼✽❄ ✿❬✿❁✺(▲✷ ❉❬)▼
▲✸✻ ✿❍✿ ❍✸✹ ■✿✾ ✼ ❍✿❀✿✽ ✼✽ ❄ ✿, ❅ ✸✹ ✺✻✼✽ ✿❂ ❆✼ ❲ ✾ ✼ ❑ ❁❃✿✹✼✽ ✿✽ ✼ ❏✼❍❅✺✹✿✹ ❉✿ ❀✿✽ ✼✽❄ ✿ P ✸❂✹ ✼❂ ❉✸✽ ✼✹ (❏ ❭ ❉❯P ❪ ❉)▼ ✷✸✹✺✻✼✽ ■✺❃ ✿❅ ✸❁✹✿❀❍✸✻ ✿❂ ✺❂ ✿✹❂ ✸❁ ■✿❅ ❁ ✿❂ ❆✸❂ ✾✼ ✷P ▼ ✷✸❁❆ ✿❍✼✹ ✿ ✷✸❁✽ ✸❁❑ ◆✸❅ ❑❆ ✷ ✿✹■✿✹❃ ❅✿✾ ✿ ❆ ✿❀ ✺✹ ◗❋❇ ❇▼ ✷ ✿✾✿ ❆ ✿❀✺✹ ◗❋❇◗ ❅ ✸✹ ✺✻✼✽ ❍✸✻ ✿❂ ✺❂ ✿✹ ❅✸✹ ✸✻✼❆✼ ✿✹ ✾ ✸✹ ❃ ✿✹ ■✺✾ ✺✻ Perilaku Oksidasi Baja AISI 4130 Pada
❫❴ ❵❛❴ ❜ ❝❞❡ ❞❢
Dengan kerendahan hati meraih Ridho Illahi Robbi
Kupersembahkan karya kecilku ini untuk Orang-Orang
Yang Aku Sayangi
Ibunda dan Ayahandaku
Atas segala pengorbanan yang tak terbalaskan, doa, kesabaran,
keikhlasan, cinta dan kasih sayangnya
Kedua Adinda Ku
Sumber inspirasi, semangat dan kebanggaan dalam hidupku
Keluarga Besar
Penyemangat, pemberi motivasi dan seluruh dukungan
baik moril dan materil serta banyak wejangan bermanfaat
Sahabat Mesin 07
Yang turut memberikan dukungan moril untuk terus ada disampingku
ketika harapan mulai redup
MOTTO
Gelar tidak menentukan masa depan. Tujuan hidup pun tidak berawal
dari gelar. Tapi gelar menjadi identitas, agar rizki tidak salah tujuan
(Penulis)
Seseorang bisa hidup menjadi baik atau tidak baik, dan seseorang bisa
memilih untuk menjadi baik.
(Spiderman)
Kepedihan tidak pasti berawal dari hal menyakitkan, tapi kesuksesan
bisa datang setalah kepedihan yang menyakitkan
❣❤✐❥❤❦❤✐❤
Assalamu alaikum Wr. Wb.
Dengan mengucapkan lafas ❧ ♠♥ ♠♦ham penulis panjatkan puji syukur kehadirat Allah SWT yang telah memberikan rahmat, taufik, dan hidayah-Nya. Shalawat serta salam tidak lupa penulis panjatkan kepada junjungan nabi besar Muhammad SAW yang telah membimbing dan mengantarkan kita menuju zaman yang lebih baik seperti sekarang, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul Perilaku Oksidasi Baja AISI 4130 Pada Temperatur 850°C . Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Teknik di Jurusan Teknik Mesin Fakultas Teknik Universitas Lampung.
Dalam pelaksanaan dan penyusunan skripsi ini, penulis banyak mendapatkan bantuan dan sumbangan pikiran dari berbagai pihak, oleh karena itu penulis mengucapkan terima kasih kepada:
1. Dr. Ir. Lusmeilia Afriani, D.E.A selaku Dekan Fakultas Teknik Universitas Lampung.
3. Bapak Dr. Mohammad Badaruddin selaku Pembimbing Utama Tugas Akhir atas kesediaan dan keikhlasannya untuk memberikan dukungan, bimbingan, saran, dan kritik dalam proses penyelesaian skripsi ini.
4. Bapak Harnowo Supriadi, S.T., M.T. selaku Pembimbing Pendamping atas kesediaan dan keikhlasannya untuk memberikan bimbingan, motivasi dan saran untuk penyelesaian skripsi ini.
5. Bapak Zulhanif, S.T., M.T. selaku dosen Pembahas yang telah memberikan masukan dalam penulisan laporan ini.
6. Ibu Novri Tanti, S.T., M.T., selaku dosen Pembimbing Akademik.
7. Seluruh Dosen Pengajar Jurusan Teknik Mesin yang banyak memberikan ilmu selama penulis melaksanakan studi, baik berupa materi perkuliahan maupun tauladan dan motivasi sehingga dapat kami jadikan bekal untuk terjun ke tengah-tengah masyarakat.
8. Bapak, ibu, adik-adikku, dan seluruh saudara ku yang terus menerus tiada hentinya memberikan kasih sayang serta doa dan dorongan selalu, dengan ikhlas mensupport dan mendukung penulis baik materi maupun non materi yang merupakan kekuatan yang tiada batas dari arti cinta yang luhur.
9. Teman seperjuangan Joni Yanto yang telah bersama-sama jatuh bangun dalam menyelesaikan skripsi ini.
11. Sahabat-sahabat terbaikku Khoirul Hidayat, Wisnu Virgiawan, Ryan Septiawan dan Ali Rasyid yang terus memberikan motivasi untuk terus memupuk semangat juang ku dalam mengejar cita-cita.
12. Ucapan yang mendalam atas banyaknya jerih susah payah untuk mendukung setiap langkah ku dalam menyelesaikan skripsi ini yaitu untuk seluruh teman yang kompak di Himpunan Pemuda Tulung Rejo (HaPeTuo).
13. Semua pihak yang tidak mungkin penulis sebutkan namanya satu persatu, yang telah ikut serta membantu dalam penyelesaian Tugas Akhir ini.
Penulis telah berusaha semaksimal mungkin dalam penulisan laporan Tugas Akhir ini untuk mencapai suatu kelengkapan dan kesempurnaan. Penulis juga mengharapkan kritik dan saran yang bersifat membangun dari semua pihak. Akhirnya dengan segala kerendahan hati penulis berharap laporan ini memberi manfaat, baik kepada penulis khususnya maupun kepada pembaca pada umumnya.
Bandar Lampung, 30 September 2014 Penulis
♣qrs qt✉ ✈✉
✇① ②① ③① ④
✉ ⑤ ⑥⑦⑧♣q✇⑨⑩ ⑨q⑧
❶❷ ❶ ❸❹❺❹❻❼❽❾ ❹❿ ❹➀ ➁❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ❶ ❶❷➂ ➃➄➅➄❹➀➆❽ ➀❽❾➇❺➇❹➀❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➂ ❶❷ ➈ ❼ ❹❺❹➉ ❹➀➊ ❹➉ ❹❾ ❹➋❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➂ ❶❷➌ ➍➇➉ ❺❽➎❹❺➇❿❹➆❽ ➀➄❾➇➉ ❹➀❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➈
✉ ✉ ⑤ s ✉ ⑧➏q ⑨q⑧⑥⑨✈sq ➐q
➂❷ ❶ ❼ ❹➅❹❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➑ ➂❷➂ ❼ ❹➅❹➒ ➓➍ ➓➌❶ ➈➔❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ❶❶ ➂❷ ➈ →➣ ❻➣➉➇ ❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ❶➂ ➂❷➌ ↔❿ ➉➇ ↕❹➉➇ ❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ❶➙ ➂❷ ➑ ↔❿ ➉➇ ↕❹➉➇ ➆❹↕❹➃❽➎➛❽ ❻❹❺➄❻➃➇➀➁ ➁➇ ❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➂➂ ➂❷➜ →➇➀❽ ❺➇❿ ❹↔❿ ➉➇ ↕❹➉➇ ❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➂➈ ➂❷ ➝ ➍➞➊➟➠ ➡➢➤ ➤➥➤ ➦➧➨➩➡➫➭ ➯➤➲➥➡➭ ➯➳➡ ➯➵ ➸➺ ❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➂➙ ➂❷➙ ➻➼➽➟➾➚➭ ➢ ➸➪➥➶➭ ➢ ➡➫➥ ➯➤ ➺❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷❷❷❷ ❷ ➈➔
✉✉ ✉ ⑤ ➹ ⑦s➘♣ ➘⑩ ➘➴✉⑥⑦⑧ ⑦ ⑩✉ s ✉q⑧
➷➬ ➷ ➮➱✃❐ ❒❮ ❰ ➱➮❒ Ï❒ÐÑÒÑÓ Ï➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬ ➷Ô ➷➬Ô ÕÑÓÖ➱Ó×ØÐÑ ➱➮❒ Ï❒ÐÑÒÑÓ Ï ➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬ ➷Ù
Ú ÛÜ ÝÞßÚ àáÞ âãä åæ Þ ÝÞßÞ â
Ô ➬ ç èÓ❐ ÑÐéê❐Ñ❮ Ó❐ ÑëÓ ìÓØíîíÔç➷ï ➮Ó❮ Óð❒×ñ❒ ➱ÓÒ ❰➱òóïôõ ➬➬ ➬➬➬➬ ➬ ➷ò Ô ➬ö ÷Ñ Ï❒ÒÑ êÓéê❐ Ñ❮Ó❐ Ñë Ó ìÓØíîíÔ ç ➷ï ➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬ Ôï Ô ➬ ➷ ÷Ó ➱Ó êÒ❒ ➱Ñ❐ Ó❐ Ñîñ ❒❐Ñ×❒ Ïë Ó ìÓØÑ❐ ÑÔç➷ïî❒Ò❒ÐÓ øÕÑ ✃ ê❐ Ñ❮ Ó❐Ñ ➬➬ ➬ Ôö
ÛÜ ßÚ åãùàÞ âáÞ âßÞúÞ â
ó ➬ ç îÑ×ñ ❰ÐÓ Ï➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬ óö ó ➬ö îÓ ➱Ó Ï➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬➬➬➬ ➬ ó ➷
þÿ ✁ÿ✂ ✁ÿ✄ ☎ ✆
✁✝ ✞✟✠ ✡✝ ✠✝ ☛✝ ☞
✌✍ ✎ ✏✑✒✓✔ ✕✖ ✗✘✙✑ ✗✚✛✜✙✢✓ ✚✣✤✥✓ ✚✦✙✣ ✏ ✚✓ ✥✓ ✚✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍ ✧ ★ ✩✍ ✎ ✏✑✒✓✔ ✕✖ ✗✘✙✑ ✗✚✢✓ ✚✣✦✙✣✏✚✓ ✥✓ ✚✛✚✪✏ ✥✫✓ ✘✙ ✚✣✬✫✓ ✘✙ ✚✣
✭✗✚✣ ✏✜✙✓ ✚✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍✍✍✍ ✍ ✧ ★ 3. ✭✮✗✘ ✗✚✪✓ ✘✗✯✏✓ ✚✪✙✪✓✪✙✰✗✱✒ ✗✑ ✗✚✢✓ ✚✣✲✗✮✥✓ ✚✳✏ ✚✣✭✓✳✓✴✓ ✜✓✤✵✕✵
✻✼✽✾ ✼✿❀ ✼❁❂ ✼✿
❀❃ ❄❅ ❃❆ H❃❇ ❃❄ ❃❈
1. ❉❊❋ ❊● ❍■❊❏❑▲ F▼ D❑◆❖ ▼❋P ◗❑❘❙▼◆ ❚❑ ❯❍ O❱● ❍❯❑◆ ❲❑ ... 13
2. ■❑❳ ❍●❑◆❨❱● ❍❯❑❖ ▼❋ ❳ ❊❋ ❍ ... 19
3. ■❑❳ ❍●❑◆❨❱● ❍❯❑ T❍❯❑❱❖▼❋ ❳ ❊❋ ❍ ... 20
4. ■❑❳ ❍●❑◆❨❱● ❍❯❑ T❍❯❑❱❖▼❋ ❳ ❊❋ ❍ ... 21
5. ❉P❋❩❑ P▼◆❑▲◗❑❘ ❑◆❖ ▼❋❑ ❬ T▼❋❘❑ ❯❑❳❭❑❱❬P❪❑ ❯❑❫P ❱P ▲ ❉❍◆ ▼❬❍❱ ❑ U◆❬P❱❨❱● ❍❯❑■❊❏❑▲ ... 23
6. ❴❵❑ ❬ U❚❍ SE❙❛❜❝❞ ❡❡ ❢❡ ❣❤ ✐❥❝ ❦❧♠❡♥❢❝ ❧♠ ♦❝♠ ♣q r... 28
7. S❱▼▲❑❴❵❑ ❬ U❚❍ SE❙... 33
8. ❖ ❑❚❑❴sSs 4130 ... 32
9. TP◆❏❱P❛t✉❧❡❞ ❝ ❥r... 33
10. ❙▼● ❍◆✈ ▼❋ ❍◆❯❑ ... 33
11. ❙❍●❬❑❋❯❑◆✇❑◆ ❏❱❑ S❊❋ ❊◆ ❏ ... 33
12. ❙▼● ❍◆❖❊❋ ... 34
13. ❉❑①❑ ❬ S❬❑❍◆❵▼● ●... 34
14. D❍❑ ❏❋❑▲❴❵❍❋ P▼◆▼❵❍❬❍❑◆ ... 37
15. S❳▼●❍▲▼◆②▼◗▼❵P ▲ D❍ ❊❱●❍❯❑●❍... 38
18. P⑥⑦⑧⑨ ⑩⑧ ⑦❶ P⑥❷⑨ ❸ ❹⑧⑧ ⑦T⑥❷ ❺ ⑥⑦❻❸❹⑦ ❼⑧ O❹❽❾❿⑧➀ ⑥❽❾ P⑧❿ ⑧➀⑧➁⑧ ➂➃S➃ 4130 S⑥❻⑥➄⑧➅➆❾➇❹❽❾❿⑧ ❽❾ P⑧❿ ⑧ T⑥⑨⑩⑥❷ ⑧ ❻❸❷ 850
OC ... ➈ ➉ ➊➋ ➌ ➍➇ ➄⑧ D❾➎⑧ ❹ ❽❾r ➏⑧ ❽❾➄➐➑D ➍⑧❿⑧➍⑥⑨ ❸ ❹⑧⑧ ⑦r B⑧➁⑧ A➃➒➃➈➊➓➔→⑧ ⑦ ❶
D❾➇❹❽❾❿⑧ ❽❾➍⑧❿ ⑧ T⑥⑨⑩⑥❷ ⑧ ❻❸❷ 850C... ➈➓
➉➔ ➌ ➒E➣➍⑥⑦⑧⑨⑩⑧ ⑦ ❶➍⑥r⑨❸ ❹⑧⑧ ⑦➀⑧➁⑧ A➃➒➃➈➊ ➓➔→⑧ ⑦ ❶ D❾➇❹❽❾❿⑧ ❽❾ ➒ ⑥➄⑧⑨ ⑧↔ ➣⑥⑦❾t D⑧ ⑦➍⑥⑨ ⑥t⑧⑧ ⑦↕➆➒➐ -r⑧ Ey ➄⑥⑨⑥⑦ ❻➙, Cr, F⑥ D⑧ ⑦
➣➇➍⑧❿ ⑧➙ ❹❽❾❿ ⑧Y⑧ ⑦ ❶ T⑥❷ ❺⑥⑦ ❻❸ ❹ ... 44 21. SE➣S❻❷❸❹❻❸ ❷ O❹ ❽❾❿ ⑧ Y⑧ ⑦ ❶ T⑥❷ ❺⑥⑦ ❻❸ ❹➍⑧❿ ⑧➀⑧➁ ⑧➂➃S➃ 4130 Y⑧ ⑦ ❶
D❾➇❹❽❾❿⑧ ❽❾ S⑥➄⑧ ⑨⑧ 60➣⑥⑦❾ ❻ D⑧ ⑦➍⑥⑨⑥❻⑧⑧ ⑦↕DS ➐-r⑧y E➄⑥⑨⑥⑦❻➙,
F⑥❿ ⑧ ⑦➛r ... ➈↔
➉ ➉➌ ➒E➣➜ ➇⑩➇❶⑧➎❾r ➍⑥⑨ ❸ ❹⑧⑧ ⑦r ➀⑧➁ ⑧ A➃➒➃➈➊ ➓➔→⑧ ⑦ ❶ D❾➇❹❽❾❿ ⑧ ❽❾ ➍⑧❿⑧
T⑥⑨ ⑩⑥❷ ⑧ ❻❸❷ 850C (⑧) ❽ ⑥➄⑧⑨ ⑧➊➁⑧⑨, (❺) ➉↔➁⑧⑨❿ ⑧ ⑦(➝) ➈➋➁ ⑧⑨ ... ➈➞
➉➓➌ ➟⑧➎❾ ❹r ➂ ⑦⑧➄❾ ❽❾s ➠❸⑧➄❾t⑧❾➎t ➀⑧➁⑧ A➃➒➃➈➊ ➓➔→⑧ ⑦ ❶➆❾➇❹❽❾❿ ⑧ ❽❾➍⑧❿ ⑧
➜⑥⑨p⑥⑧rtur 8↔ ➔ ➛ (⑧) ❽ ⑥➄⑧⑨ ⑧↔⑨ ⑥⑦❾t, (❺)➓➔⑨ ⑥⑦❾t❿⑧ ⑦(➝) 7➉➁⑧⑨ ➈➋ ➉ ➈➌ ➒↕➣➍⑥⑨❸❹⑧⑧ ⑦r ➀⑧➁⑧ A➃ ➒➃➈➊ ➓➔→⑧ ⑦ ❶➆❾➇❹❽❾❿ ⑧ ❽❾ ➍⑧❿⑧ ➜⑥⑨⑩⑥⑧rtur
BAB ➡
➢E➤DA➥ ➦➧ ➦A➤
1➨ ➩ ➧➫ ➭➫ ➯➲➳➵➫ ➸➫ ➺➻
Baja AISI 4130 merupakan baja paduan rendah ➼➽➾➚➪ ➶➹➘ ➴➼ yang
mengandung kromium dengan kandungan karbon 0,30%. Sedangkan unsur
pembentuk lain dari baja AISI 4130 yaitu (0,28-0,33)% C; (0,40-0,60)% Mn;
0,035% P; 0,04% S;(0,15-0,30)% Si; (0,80-1,10)% Cr; (0,15-0,25)% Mo.
Baja paduan rendah merupakan baja paduan yang memiliki kadar karbon
sama seperti baja karbon, tetapi ada sedikit unsur paduan. Dengan
penambahan unsur paduan, kekuatan dapat dinaikkan tanpa mengurangi
keuletannya, kekuatanfatik, daya tahan terhadap korosi, aus dan panas.
Aplikasi baja AISI 4130 banyak digunakan pada kapal, jembatan, roda kereta
api, ketel uap, tangki gas, pipa gas dan sebagainya. Korosi merupakan
penurunan mutu logam akibat reaksi elektrokimia dengan lingkungannya.
Dalam penggunaanya baja paduan ini akan mengalami degredasi atau
2
Proses oksidasi temperatur tinggi berawal dari adsorpsi oksigen yang
kemudian membentuk oksida pada permukaan bahan. Selanjutnya, terjadi
proses nukleasi oksida dan pertumbuhan lapisan untuk membentuk proteksi.
Dengan terjadinya oksidasi temperatur tinggi maka akan didapatkan laju
korosi sehingga dapat dilakukan perkiraan masa pakai atau umur baja
tersebut.
Sehubungan dengan uraian di atas maka perlu dilakukan penelitian tentang
baja AISI 4130 terhadap temperatur tinggi. Oleh karena itu penulis
mengambil sebuah judul untuk penelitian yaitu ➷➬➮ ➱✃ ❐ ❒❮❰ Ï ❮Ð✃ Ñ ❒Ð✃
Ò❒Ó❒❒✃ Ð✃Ô ÕÖ ×➬ ❒Ñ ❒Ø➮Ù➬➮➱ ❒Ø❰➱Ú Û × ÜÝ Þ.
Õßà Øáâáã ä➬å äåæçèçã ä
Adapun tujuan dari pelaksanaan dan penulisan laporan tugas akhir ini adalah :
a. Menentukan laju oksidasi (kp) baja AISI 4130 pada temperature 850 C
b. Mengetahui karakteristik baja setelah dioksidasi
ÕßÖ Òãèã é ã ä Ùã éã æã ê
Berdasarkan latar belakang dan perumusan masalah di atas agar proses yang
dilakukan bisa berjalan dengan sesuai maka peneliti membatasi masalah
penelitiannya sebagai berikut :
1. Spesimen uji adalah baja pa
2. duan rendah (AISI 4130) dengan dimensi panjang 20 mm, lebar 10 mm,
3
3. Korosi oksidasi dilakukan pada temperatur 850 C dengan variasi waktu
oksidasi adalah 1 sampai 72 jam.
4. Pengujian foto mikro, makro, SEM, EDS, dan X-RD dilakukan untuk
mengetahui karakteristik baja AISI 4130 setelah dioksidasi.
1ë ì íîï ðñò óðî ôóõñ ö÷øîï óö
Penulisan Tugas Akhir ini disusun menjadi lima Bab. Adapun sistematika
penulisannya adalah sebagai berikut :
ù úùûõü ýþúÿ ✁ úý
Pada bab ini menguraikan latar belakang penelitian tugas akhir, tujuan
penelitian tugas akhir, batasan masalah dan sistematika penulisan.
ù úùû û✂ û ý✄ ú úýõ í ✂ú☎ ú
Pada bab ini menguraikan tinjauan pustaka yang dijadikan sebagai landasan
teori untuk mendukung penelitian ini.
ù úùû û û✆ ü ✂✝ þ✝ ✁✝ ✞ ûõü ýü✁ û ✂ ûúý
Pada bab ini menjelaskan metode tentang langkah-langkah, Alat dan bahan
yang dilakukan untuk mencapai hasil yang diharapkan dalam penelitian ini.
ù úùû ✟ ÿúí û✁þúýúýú✁ûí ú
Pada bab ini menguraikan hasil dan membahas yang diperoleh dari penelitian
4
BAB ✠✡☛ ☞✌✍✎A✏ DA✏✡A✑A✏
Pada bab ini menyimpulkan dari hasil dan pembahasan sekaligus memberikan
saran yang dapat menyempurnakan penelitian ini.
DAF✒A✑✌✍✡✒A✓A
Berisikan literatur-literatur atau referensi yang diperoleh penulis untuk
mendukung penyusunan laporan ini.
✎A☞✌☛ ✑A✏
✔✕ ✔✖✖
✗✖✘✙✕✚✕✘✛✚ ✜✗✕✢✕
✣✤✥ ✔✦ ✧✦
★ ✩j✩ ✩✪✩l✩h l✫✬ ✩m ✭✩✪ ✮ ✩n ✪ ✯✰✬✩n ✱✯si ✲✯✱✩✬✩i unsur ✪✩✲ ✩r ✪ ✩n ✳ ✩r✱✫✰ ✲✯✱✩✬ ✩i unsur ✭ ✩✪✮✩n ut✩m✩ny✩✴ ✵ ✩✰ ✪ ✮✰✬✩n✳✩r✱ ✫✰ ✪ ✩l✩m✱✩j✩ ✱ ✯rki✲ ✩r
✩nt✩r✩ ✶✴✷✸ hin✬✬✩ ✷ ✴✹% ✱✯r✩t ✲ ✯✲ ✮✩i ✺✻ ✼ ✽✾✿n✩✴y Fungsi karbon dalam baja adalah sebagai unsur pengeras. Unsur paduan lain yang biasa ditambahkan
selain karbon adalah mangan (❀✼ ❁✺ ✼❁ ✾ ❂✾), krom (❃❄✻ ❅❀❆❇❀), vanadium, dan
nikel. Dengan memvariasikan kandungan karbon dan unsur paduan lainnya,
berbagai jenis kualitas baja bisa didapatkan. Penambahan kandungan karbon
pada baja dapat meningkatkan kekerasan (❄✼✻ ✽❁ ✾ss ) dan kekuatan tariknya
(t✾❁❂❆ ❈✾ st✻ ✾❁✺ ❉ ❄ ), namun di sisi lain membuatnya menjadi getas (❊✻ ❆tt❈✾ ) serta
menurunkan keuletannya (✽❇ ❃❆ ❈❆t ty).
Pengaruh utama dari kandungan karbon dalam baja adalah pada kekuatan,
kekerasan, dan sifat mudah dibentuk. Kandungan karbon yang besar dalam
baja mengakibatkan meningkatnya kekerasan tetapi baja tersebut akan rapuh
6
Baja karbon rendah memiliki kandungan karbon dibawah
0,3%. Baja karbon rendah sering disebut dengan baja ringan
(♠♥♦♣ stqq♦ ) atau baja perkakas. Jenis baja yang umum dan
banyak digunakan adalah jenis r ✐♦♣ ❣ ✐♦♦ stqq♦ dengan
kandungan karbon 0,08% 0,30% yang biasa digunakan
untuk❤✐♣skendaraan [Sack, 1997].
b. Baja Karbon Sedang
Baja karbon sedang merupakan baja yang memiliki
kandungan karbon 0,30% - 0,60%. Baja karbon sedang
7
paduan didefinisikan sebagai suatu baja yang dicampur dengan
satu atau lebih unsur campuran seperti nikel, mangan,
molybdenum, kromium, vanadium dan wolfram yang berguna
untuk memperoleh sifat-sifat baja yang dikehendaki seperti
8
↕➙ ↕➙r➛p➛ unsur y➛n➜ ↕➙r↕➙➝ ➛ m➙m↕➙➞ ➛ri n si➟ ➛t k➠ ➛s ➝ ➛ri ↕ ➛j➛➡
➢➤➥➛lny➛ ↕ ➛j➛ y➛➜n ➝➤➦➛➝➧ ➝ ➙➜ ➛n n Ni dan Cr akan
menghasilkan baja yang mempunyai sifat keras dan ulet.
Berdasarkan kadar paduannya baja paduan dibagi menjadi tiga
macam yaitu:
a. Baja Paduan Rendah (➨ow ➩ ➫➫oy ➭➯➲➲ ➫ )
Baja paduan rendah merupakan baja paduan yang elemen
paduannya kurang dari 2,5% wt misalnya unsur Cr, Mn, Ni,
S, Si, P, dan lain-lain. Memiliki kadar karbon sama seperti
baja karbon, tetapi ada sedikit unsur paduan. Dengan
penambahan unsur paduan, kekuatan dapat dinaikkan tanpa
mengurangi keuletannya, kekuatan fatik, daya tahan
terhadap korosi, aus dan panas. Aplikasinya banyak
digunakan pada kapal, jembatan, roda kereta api, ketel uap,
tangki gas, pipa gas dan sebagainya.
b. Baja Paduan Menengah (➳➲➵➸➺ ➻➩ ➫➫oy ➭➯➲➲ ➫ )
Baja paduan menengah merupakan baja paduan yang
elemen paduannya 2,5%-10% wt misalnya unsur Cr, Mn,
Ni, S, Si, P, dan lain-lain.
c. Baja Paduan Tinggi (➼➸➽ ➾➩ ➫➫oy ➭➯➲➲ ➫ )
Baja paduan tinggi merupakan baja paduan yang elemen
paduannya lebih dari 10% wt misalnya unsur Cr, Mn, Ni, S,
Si, P, dan lain-lain. Contohnya baja tahan karat, baja
9
1. Keuletan yang tinggi tanpa pengurangan kekuatan tarik
2. Tahan terhadap korosi dan keausan yang tergantung pada jenis
paduannya
3. Tahan terhadap perubahan suhu, ini berarti bahwa sifat fisisnya tidak
banyak berubah
4. Memiliki butiran yang halus dan homogen
Menurut Muhd. Amin Nasution (2008), pengaruh unsur-unsur paduan
dalam baja adalah sebagai berikut:
1. Unsur karbon (C)
Karbon merupakan unsur terpenting yang dapat meningkatkan
kekerasan dan kekuatan baja. Kandungan karbon di dalam baja
sekitar 0,1%-1,7%, sedangkan unsur lainnya dibatasi sesuai dengan
kegunaan baja. Unsur paduan yang bercampur di dalam lapisan baja
adalah untuk membuat baja bereaksi terhadap pengerjaan panas dan
menghasilkan sifat-sifat yang khusus. Karbon dalam baja dapat
meningkatkan kekuatan dan kekerasan tetapi jika berlebihan akan
10
Ù Ú Unsur Mangan (Mn)
Semua baja mengandung mangan karena sangat dibutuhkan dalam
proses pembuatan baja. Kandungan mangan kurang lebih 0,6% tidak
mempengaruhi sifat baja, dengan kata lain mangan tidak
memberikan pengaruh besar pada struktur baja dalam jumlah yang
rendah. Penambahan unsur mangan dalam baja dapat menaikkan
kuat tarik tanpa mengurangi atau sedikit mengurangi regangan,
sehingga baja dengan penambahan mangan memiliki sifat kuat dan
ulet.
3. Unsur Silikon (Si)
Silikon merupakan unsur paduan yang ada pada setiap baja dengan
kandungan lebih dari 0,4% yang mempunyai pengaruh untuk
menaikkan tegangan tarik dan menurunkan laju pendinginan kritis.
Silikon dalam baja dapat meningkatkan kekuatan, kekerasan,
kekenyalan, ketahanan aus, dan ketahanan terhadap panas dan karat.
Unsur silikon menyebabkan sementit tidak stabil, sehingga
memisahkan dan membentuk grafit. Unsur silikon juga merupakan
pembentuk ferit, tetapi bukan pembentuk karbida, silikon juga
cenderung membentuk partikel oksida sehingga memperbanyak
pengintian kristal dan mengurangi pertumbuhan akibatnya struktur
11
Û Ü Unsur Nikel (Ni)
Nikel mempunyai pengaruh yang sama seperti mangan, yaitu
memperbaiki kekuatan tarik dan menaikkan sifat ulet, tahan panas,
jika pada baja paduan terdapat unsur nikel sekitar 25% maka baja
dapat tahan terhadap korosi. Unsur nikel yang bertindak sebagai
tahan karat (korosi) disebabkan nikel bertindak sebagai lapisan
penghalang yang melindungi permukaan baja.
5. Unsur Kromium (Cr)
Sifat unsur kromium dapat menurunkan laju pendinginan kritis
(kromium sejumlah 1,5% cukup meningkatkan kekerasan dalam
minyak). Penambahan kromium pada baja menghasilkan struktur
yang lebih halus dan membuat sifat baja dikeraskan lebih baik
karena kromium dan karbon dapat membentuk karbida. Kromium
dapat menambah kekuatan tarik dan keplastisan serta berguna juga
dalam membentuk lapisan pasif untuk melindungi baja dari korosi
serta tahan terhadap suhu tinggi.
ÝÞ Ý ß àá àâã äãå æç è
Dalam penelitian ini jenis material yang digunakan yaitu baja AISI 4130 yang
merupakan baja paduan rendah éêëì íîï ð éy yang mengandung kromium
dengan kandungan karbon 0,30%. Baja AISI 4130 mempunyai komposisi
kimia (0,28-0,33)% C; (0,40-0,60)% Mn; 0,035% P; 0,04% S; (0,15-0,30)%
12
ñòó ôõ öõ ÷ ø
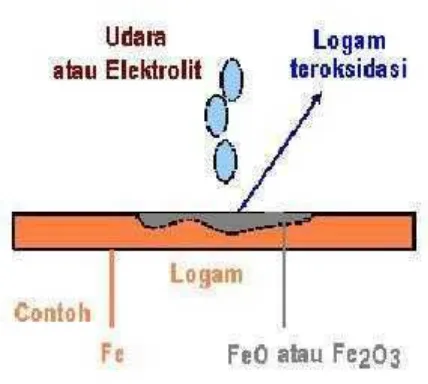
ùrosi oúûúúlhüýú üúrus núútuûý þ ÿúû úsi loþ úmúkiút rýúksi rýû ✁ ü✂ úúntúr
✂✄útu l✁þúmû ýnþún ýrúþúi zat di lingkungannya yang menghasilkan
senyawa-senyawa yang tidak dikehendaki. Dalam bahasa sehari-hari korosi
disebut perkaratan. Contoh korosi yang paling lazim adalah perkaratan besi.
Pada peristiwa korosi, logam mengalami oksidasi, sedangkan oksigen (udara)
mengalami reduksi. Karat logam umumnya adalah berupa oksida atau
karbonat. Rumus kimia karat besi adalah Fe2O3.nH2O, suatu zat padat yang
berwarna coklat-merah.
Korosi dapat juga diartikan sebagai serangan yang merusak logam karena
logam bereaksi secara kimia atau elektrokimia dengan lingkungan. Ada
definisi lain yang mengatakan bahwa korosi adalah kebalikan dari proses
ekstraksi logam dari bijih mineralnya. Contohnya, bijih mineral logam besi di
alam bebas ada dalam bentuk senyawa besi oksida atau besi sulfide, setelah
diekstraksi dan diolah, akan dihasilkan besi yang digunakan untuk pembuatan
baja atau baja paduan. Selama pemakaian, baja tersebut akan bereaksi dengan
lingkungan yang menyebabkan korosi (kembali menjadi senyawa besi
13
Gambar 1. Korosi logam Fe dan berubah menjadi oksidanya
Korosi dapat terjadi oleh air yang mengandung garam, karena logam akan
bereaksi secara elektrokimia dalam larutan garam (elektrolit). Faktor yang
mempengaruhi proses korosi meliputi potensial elektrodanya yang negative
lebih mudah mengalami korosi. Demikian pula dengan logam yang potensial
elektrodanya positif sukar mengalami korosi.
Untuk mencegah terjadinya korosi, beberapa teknik atau cara diusahakan.
Dalam industri logam, biasanya zat pengisi (campuran) atau ☎✆✝ ✞✟☎☎✠t s
diusahakan tersebar merata di dalam logam. Logam diusahakan agar tidak
kontak langsung dengan oksigen atau air, dengan cara mengecat permukaan
logam dan dapat pula dengan melapisi permukaan logam tersebut dengan
logam lain yang lebih mudah mengalami oksidasi. Cara lain yang juga sering
dipergunakan adalah galvanisasi atau perlindungan katoda. Proses ini
14
m
✡m☛✡ntuk l☞pi✌ ☞nZnO. Lapisan inilah yang akan melindungi besi dari
oksidator.
✍ ✎✏ ✎✑ ✒✓ ✔tor ✕✖✓✔tor y✓ ✗✘✙✚ ✙✛ ✚✗✘✓ ✜ ✢ ✣✤✔✥✜ ✥ ✦✤
Secara umum faktor-faktor yang mempengaruhi korosi dibagi menjadi
dua yaitu, faktor internal dan faktor eksternal. Faktor internal meliputi
keragaman struktur, perlakuan panas, pendinginan dan perlakuan
permukaan. Sedangkan yang termasuk faktor eksternal ialah fenomena
korosi yang merupakan interaksi elektrokimia antara logam dengan
lingkungannya. Adapun kondisi lingkungan yang mempengaruhi
korosi logam yaitu:
Temperatur berperan mempercepat seluruh proses yang terlibat
selama korosi terjadi. Titik optimum dari temperatur yang
menyebabkan korosi adalah sekitar rentang 328-353 K.
c. pH larutan
Faktor lain yang mempengaruhi laju korasi di dalam media larutan
adalah pH, pH dapat mempengaruhi laju korosi suatu logam
15
r
✧★ ✩✪h✪✪nt✪r pH 7 sampai 12. Sedangkan pada pH <7 dan pH>12 laju korosinya meningkat.
d. Padatan terlarut
Garam klorida, khususnya ion-ion klorida menyerang lapisan ✫✬✭✮
st
✯✯✭ dan st✰✬✱✭✯ss st✯✯✭✲ Ion-ion ini menyebabkan terjadinya ✳✬tt✬✱✴ ✵✶✷✯v✬✶✯✶✸✷ ✷ ✸ ✹ ✬✸✱ dan pecahnya paduan logam.
✺✲✻✲✺ ✼ ✭✰✹ ✬✽✬✾✰✹✬✾✸✷ ✸ ✹ ✬
Korosi diklasifikasikan melalui banyak cara. Ada metode yang
membagi korosi menjadi korosi pada temperatur rendah dan
temperatur tinggi. Metode lainnya memisahkan korosi menjadi
kombinasi langsung (atau oksidasi) dan korosi elektrokimia [M.G.
Fontana, 1986]. Klasifikassi yang lebih disukai adalah korosi basah
✿w✯t ✶✸ ✷ ✷✸✹✬✸✱ ❀ dan korosi kering ✿✮✷❁ ✶orros✬✸✱❀ ✲ Korosi basah terjadi ketika adanya cairan, biasanya melibatkan larutan yang
mengandung air atau elektrolit. Contoh yang paling umum adalah
korosi pada baja yang disebabkan oleh air. Korosi kering terjadi ketika
tidak adanya fasa cair atau ketika di atas titik embun lingkungan.
Korosi kering paling sering dihubungkan dengan temperatur tinggi.
Contohnya korosi baja pada tungku perapian gas.
✺✲✻✲✻ ❂ ✯✱ ❁✯❃ ✰❃✾✸✷ ✸✹✬ t✯✫✳✯✷✰tur t✬✱✴ ✴ ✬
16 hidrokarbon lainnya. Penguraian C ke permukaan logam
mengakibatkan penggetasan dan degradasi sifat mekanik lainnya.
c. Nitridasi
Terjadi pada lingkungan yang mengandung ammonia, terutama
pada potensial oksigen yang rendah. Penyerapan nitrogen yang
berlebihan akan membentuk presipitat nitride di batas butir dan
menyebabkan penggetasan.
d. Korosi oleh halogen
Senyawa halide akibat penyerapan halogen oleh logam, dapat
bersifat mudah menguap atau mencair pada temperatur rendah.
17
❱❲ ❳ul❨❩❬i si
❭❱❬ ❩❪rj ❩❬❬lm li❫❴kun❴❬n y❬❴n m❱❴❬❫❩❵ ❫❴n ❛❬h❬n❛❬❜❬r ❬t❬u❝❬sil ❞❱m❛❬❜❬r❬n y❬❴nm❱❴❬❫❩❵❫❴n sul❨❲ru❡❱n❴❬n o❴❱sik n m❱m❛❱ntuk ❳❢❣ ❩❬n❳❢
❤ y
❬n❴ ❛❱r si❨❬t ❞ ❱n❴❩❬siko si y❬n❴ k❬urn❴ ❬❴ ✐❱si❨
❩❪❛❬❫❩❪ ❫❴ ❜❬nH 2S yang bersifat pereduksi, tetapi dapat terjadi efek penguatan dengan adanya Na dan K yang akan membentuk uap
yang kemudian akan mengendap ke permukaan logam pada
temperatur yang lebih rendah dan merusak permukaan.
f. Korosi deposit abu dan garam
Deposit dapat mengakibatkan turunnya aktifitas oksigen dan
menaikkan aktifitas sulfur, sehingga merusak lapisan pasif dan
mempersulit pembentukannya kembali. Deposit biasanya
mengandung S, Cl, Zn, Pb dan K.
g. Korosi karena logam cair
Terjadi pada proses yang mempergunakan logam cair, misalnya
❥ ❦❧♠ t♥❦❧♠ ♦❦ ♣♠ dan ♥❦ qr♣ r♣s t ♥ ✉✈❦ss . Korosi terjadi dalam bentuk pelarutan logam dan oksidanya akan semakin hebat dengan adanya
18
Jika satu materi teroksidasi dan materi yang lain tereduksi maka reaksi
demikian disebut reaksi reduksi-oksidasi, disingkat reaksi redoks (➒❸➀❽x
➒❸❼➔t❻❽ ❹ ). Reaksi redoks terjadi melalui tranfer elektron. Tidak semua
reaksi redoks melibatkan oksigen. Akan tetapi semua reaksi redoks
melibatkan transfer elektron dari materi yang bereaksi. Jika satu materi
kehilangan elektron, materi ini disebut teroksidasi⑨ Jika satu materi
memperoleh elektron, materi ini disebut tereduksi.
Dalam reaksi redoks, satu reagen teroksidasi yang berarti menjadi
reagen pereduksi dan reagen lawannya terreduksi yang berarti menjadi
reagen pengoksidasi. Kecenderungan metal untuk bereaksi dengan
oksigen didorong oleh penurunan energi bebas yang mengikuti
pembentukan oksidanya. Lapisan oksida di permukaan metal bisa
berpori (dalam kasus natrium, kalium, magnesium) bisa pula rapat tidak
19
→ ➣↔ ➣→↕ ➙➛ ➙➜ ➝➞ ➝➛➞ ➝➟➠➡ ➝➛➢ ➤➡ ➠ ➥ ➝
➦➧➨➧ umumny➧ l➧➩➧pi n oksi➨➧ y➧➫n t➭rj➧➨ ➯ ➨➯ ➲➭➳ ➵➧➧rm n m➭➧tl ➸➭➺➨ ➭run➫ m➭➺➭➻➧l➼ ➽➭rikut ini ➻➭➻➭➧ ➲➧r m➭ ➵➧➭nism y➧n➫ mun➫kin
t
➭➧➨ ➯➾rj ➧nt➧r➧ l➧in➚
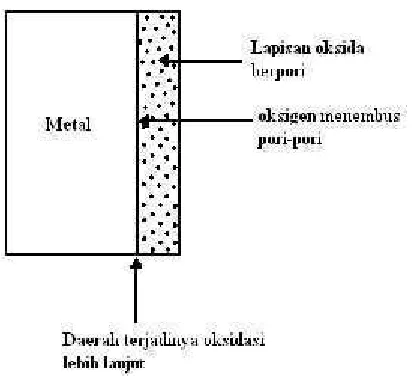
➧➼ Jika lapisan oksida yang pertama terbentuk adalah berpori, maka
molekul oksigen bisa masuk melalui pori-pori tersebut dan kemudian
bereaksi dengan metal di perbatasan metaloksida. Lapisan oksida
bertambah tebal. Lapisan oksida ini bersifat ➛➢ ➛➪prot➙➤t➠➶➹ tidak
memberikan perlindungan pada metal yang dilapisinya terhadap
proses oksidasi lebih lanjut.
Gambar 2. Lapisan oksida berpori.
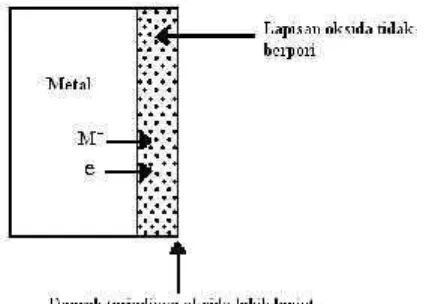
b. Jika lapisan oksida tidak berpori, ion metal bisa berdifusi menembus
lapisan oksida menuju bidang batas oksida-udara, dan di perbatasan
20
l
➘pi➴ ➘n o➷ ➘sik y➘n➬ t➮l➘h➘➷➘➱ ✃❐ ➴➮r s o➷ ➘ksi si ❒➮rl➘njut ➷ ❮ ❰➮Ï Ð➘➘Ñ➱rm Ò➘➘lmÓ➘l ini ➮➮lktron❒ ➮r➬➮r➘k➷ ➮➬ ➘n n➘r➘h y➘➬n s➘m➘
➘➬➘r ❰➮rtuk➘r➘n➮➮lktron➷ ➘l➘m r➮ ➘ksi ini ❒❮➴ ➘ ➮trj➘➷❮ ➱ Jika lapisan oksida tidak berpori, ion metal bisa berdifusi menembus lapisan
oksida menuju bidang batas udara, dan di perbatasan
oksida-udara ini metal bereaksi dengan oksigen dan menambah tebal lapisan
oksida yang telah ada. Proses oksidasi berlanjut di permukaan.
Dalam hal ini elektron bergerak dengan arah yang sama agar
pertukaran elektron dalam reaksi ini bisa terjadi. Ion logam berdifusi
menembus menembus oksida,elektron bermigrasi dari metal ke
permukaan oksida.
Gambar 3. Lapisan oksida tidak berpori
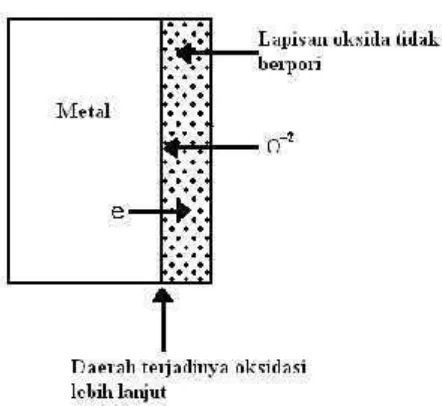
Jika lapisan oksida tidak berpori, ion oksigen dapat berdifusi menuju
bidang batas metal-oksida dan bereaksi dengan metal dibidang batas
21
Ô ÕrÖ Õ×rk kÕ××rhÔ ØÙ×nÖÔ ××ts oÙ×sik Ú Ù×× Ûr ÜrosÕs osikÙ×si ÔÕrl×njut Ù Ø ÝÕÔ ×r ×t×sn mÕ×tl ÞoksiÙ×Û ß oon ksiÖ ÕnÔÕrÙØàusi mÕáÕÔ Úâm oksiÙ×ã
ÕlÕktron Ù×ri mÕ×tl kÕÝÕrmÚä××n oksiÙ×
Gambar 4. Lapisan oksida tidak berpori
Mekanisme lain yang mungkin terjadi adalah gabungan antara reaksi di
mana ion metal dan elektron bergerak ke arah luar sedang ion oksigen
bergerak ke arah dalam. Reaksi oksidasi bisa terjadi di dalam lapisan
oksida. Terjadinya difusi ion, baik ion metal maupun ion oksigen,
memerlukan koefisien difusi yang cukup tinggi. Sementara itu gerakan
elektron menembus lapisan oksida memerlukan konduktivitas listrik
oksida yang cukup tinggi pula. Oleh karena itu jika lapisan oksida
memiliki konduktivitas listrik rendah, laju penambahan ketebalan lapisan
22
m
ånujuæ åç èr èé èt n oksiê è ë ì êèèr yèín êîæ årluïèn ukntuæårtìïèrèn ålåktronê èlèm råèksið
ñòó ô õö ÷dø öi ùøú øûemùeü øû ýüûinþþ÷
Logam yang bereaksi dengan oksigen atau gas lainnya pada suhu tinggi akan
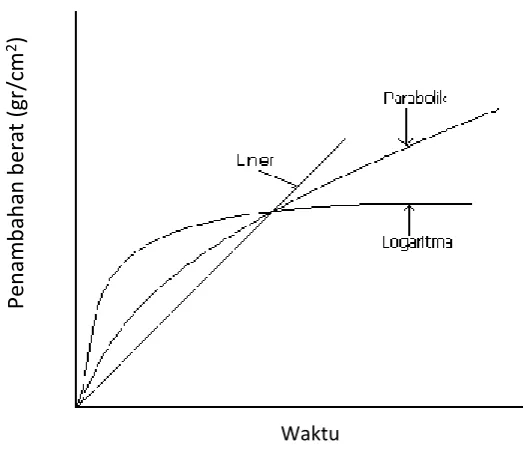
mengalami reaksi kimia. Pada tingkat oksidasi, hukum kinetika parabola,
linier, dan logaritma menggambarkan tingkat oksidasi untuk logam umum
dan paduan. Dalam hal ini oksigen bereaksi untuk membentuk oksida pada
permukaan logam, diukur dengan penambahan berat. Penambahan berat
pada setiap waktu (t) selama oksidasi sebanding dengan ketebalan oksida (x).
Logam tertentu, seperti baja, harus dilapisi untuk pencegahan korosi, karena
memiliki tingkat oksidasi yang tinggi.
Pada tingkat hukum parabola, laju oksidasi temperatur tinggi pada logam
sering mengikuti hukum laju parabolik, yang memerlukan ketebalan (x),
propotional ke waktu (t) yaitu,
xÿ ✁pt
23
Gambar 5. Kurva penambahan berat terhadap waktu pada hukum kinetika
untuk oksidasi logam.
✂✄☎ ✆ine✝i✞✟✠ ✞✡ ☛d✟✡ ☛
Perubahan energi bebas menunjukkan kemungkinan produk reaksi stabil,
tetapi tidak meramalkan laju pembentukan produk. Selama oksidasi, molekul
oksigen pertama yang diabsorpsi permukaan logam berdisosiasi menjadi
komponen atom sebelum membentuk ikatan kimia dengan atom permukaan
logam, proses ini disebut kemisorpsi. Setelah terbentuk beberapa lapisan
absorpsi, oksida bernukleasi secara epitaksial pada butir logam induk di
lokasi yang diutamakan, seperti dislokasi dan atom pengotor. Setiap daerah
nukleasi tumbuh, merasuk satu dengan lainnya sehingga terbentuk lapisan
tipis oksida di seluruh permukaan. Oleh karena itu oksida biasanya terdiri
dari agregat butir individu atau kristal dan menampakkan gejala seperti
24 tipis tidak berpori dan oksida selanjutnya mencakup difusi melalui lapisan
oksida. Apabila terjadi oksida di permukaan oksida oksigen maka ion logam
dan elektron harus berdifusi dalam logam yang berada di bawahnya. Apabila
reaksi oksidasi terjadi antar muka logam-oksida, ion oksigen harus berdifusi
melalui oksida dan elektron berpindah dengan arah berlawanan untuk
menuntaskan reaksi.
Pertumbuhan lapisan oksida dapat diikuti dengan keseimbangan termal
memiliki kepekaan hingga 10-7 g, dan pengurangan dilakukan di lingkungan
pada temperatur yang dikendalikan dengan teliti. Teknik metalografi yang
paling sering diterapkan adalah elipsometri, yang bergantung pada perubahan
di bidang polarisasi berkas cahaya terpolarisasi yang terpantulkan oleh
permukaan oksida, sudut rotasi bergantung tebal oksida. Selain itu juga
digunakan interferometri, tetapi kini lebih sering dipakai replika dan lapisan
tipis di mikroskop transmisi elektron dan mikroskopik scanning elektron.
25
200oC) ketebalan bertambah secara logaritmik dengan waktu (x Ln t) dan
laju oksidasi turun dengan berkurangnya kekuatan medan.
Pada temperatur intermediat (antara 50oC-1000oC untuk Fe) oksidasi
berkembang terhadap waktu mengikuti hukum parabola (x2 t) untuk
hampir semua logam. Di daerah ini pertumbuhan merupakan proses aktivasi
termal dan ion-ion melalui lapisan oksida dengan gerakan termal, dan
kecepatannya bermigrasi bergantung pada jenis cacat struktur dalam kisi
oksida. Tegangan yang besar, baik tekan maupun tarik, sering sekali dialami
lapisan oksida pelindung retak dan lepas. Pengelupasan berulang yang terjadi
pada skala kecil menghalangi pertumbuhan parabolik yang lebih luas dan
oksidasi memiliki laju linier bahkan lebih cepat. Tegangan dalam lapisan
oksida berkaitan dengan rasio ✵ ✶✷✷✶✸✹ ✺✻✼✽ ✾ort✿ (P-B), yaitu rasio volume
molekuler oksida terhadap volume atomik logam yang membentuk oksida.
Apabila rasio lebih kecil dari satu seperti untuk Mg, Na, K oksida yang
terentuk mungkin tidak memberikan perlindungan yang memadai terhadap
oksidasi selanjutnya, sejak tahap awal dan dengan kondisi seperti ini yang
lazim dijumpai pada logam-logam alkali, diikuti hubungan oksidasi linear (x
t). Namun, apabila rasio P-S jauh lebih besar dari satu, seperti pada logam
26
❀❁❂❁ t❃m❄❃❁rtur ti❅❆❆❇i❁l❈❁pi n❉❃❁rt❉ ❁mh❈❃ ❈❊❁i hm luku❁ju❄ ❁r❁❉ ❋●ik (x
2
t). cacat titik berdifusi melalui oksida karena terdapat gradient konsentrasi
yang konstan. Cacat ditiadakan pada salah satu antar muka dan terjadi
pembentukan lokasi kisi yang baru. Khususnya seng oksida bertambah tebal
karena difusi Intertisi seng yang terbentuk di antar muka logam oksida
melalui oksida menuju antar muka oksida logam dan disini menghilang
karena reaksi:
2Zni+++ 4e + O2 2ZnO
Konsentrasi intertisi seng pada antar muka logam/oksida dipertahankan oleh
reaksi:
Zn(logam) Znj+++ 2e
Dengan pembentukan kekosongan dalam kisi seng migrasi cacat intertisi
bermuatan terjadi bersamaan dengan imigrasi elektron, dan untuk lapisan
oksida yang tebal, wajar untuk mengasumsi bahwa konsentrasi kedua spesies
yang bermigrasi adalah konstan pada kedua permukaan oksida, yaitu
permukaan oksida/gas dan oksida logam, konsentrasi dikendalikan oleh
kesetimbangan termodinamika setempat, jadi melintasi oksida terdapat
perbedaan konsentrasi konstan c dan laju transportasi melalui satuan luas
D c/x, dimana D adalah koefisien difusi dan W adalah tebal lapisan. Maka
laju pertumbuhan:
Dx/dt = D c/x .(1)
27
W2= kpt (2)
W = W1-W0 ..(3)
Dimana : kp = konstanta parabolik
W0 = berat awal spesimen
W1 = berat akhir specimen
Wagner menunjukkan proses oksidasi dapat dijabarkan menjadi arus ionic
ditambah arus elektronik, dan mendapatkan persamaan laju oksidasi yang
dinyatakan dalam ekivalen kimia mg2.cm/s, masing-masing mencakup jumlah
transportasi anion dan elektron, konduktivitas oksida, potensial kimia dari ion
yang berdifusi pada antar muka dan ketebalan lapisan oksida. Pada rentang
temperature tertentu berbagai oksida bertambah tebal sesuai hukum parabolik.
Pada temperatur rendah dan untuk lapisan oksida yang tipis, berlaku hukum
logaritmik. Apabila tebal kerak bertambah mengikuti hukum parabolik,
resultan tegangan yang terjadi pada antar muka bertambah dan akhirnya
lapisan oksida mengalami kegagalan perpatahan sejajar dengan antar muka
atau mengalami perpatahan geser atau pematahan tarik melalui lapisan. Di
daerah ini laju oksidasi meningkat sehingga terjadi peningkatan yang
kemudian berkurang lagi akibat perpatahan lokal di kerak oksida. Laju
28
m
❍■ ❏uti hikukum lin❍ ❑i r▲ ▼❍◆❖ ❑P❑r n◗❍❘❍rti ini ❙❚ ◗❍❖◆❯ ❘❑r❑li■❍❑r ❙❑n ❖❚❑ ◗❑❑ny❙❚❘❑jumi ❘❑ ❙❑ oksi❙❑si tit❑nium◗❍t❍l❑h oksi❙❑ m❍■❱❑❘❑i ❲❍❍❖ ❑t ❑ln
k
ritis [M. Daud Pinem, 2005].
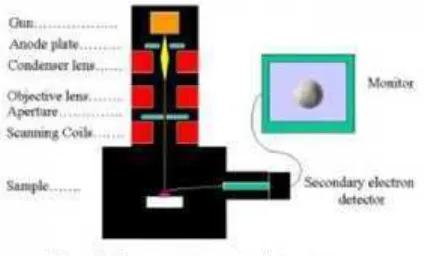
❳❨ ❩ ❬❭ ❪(Scanning Electron Microscopy)
Peralatan SEM ini dapat ditunjukkan seperti pada gambar di bawah ini :
Gambar 6. Alat uji SEM
[http://www.unm.edu/~cmem/nano/facilities/pics/SEM-5200.png]
SEM merupakan alat yang digunakan untuk mengkarakterisasi nanomaterial.
Beberapa hal yang dikarakterisasi yaitu permukaan material tersebut. Jadi,
setelah material diamati dengan SEM ini maka akan diperoleh bagaimana
bentuk permukaan material tersebut. Pada SEM, permukaan material
ditembaki dengan berkas elektron berenergi tinggi. Elektron berenergi tinggi
29
❫ ❴❵❛ ❜n ❝ ❜nj❜❛n ❛❴lom❞ ❜❵❛ ❫❴ ❡❛ro❴❢li ❣r❤✐ ❴s ini m❴❵❛❜❞ ❜ik tk❜n❜❫❜n ❜y ❴l❴ktron y❜n❛ ❫❥❝ ❜ntulk❜n ❜t❜u❫❥❦❜❧❜sil nny❜ ❴l❴nktro✐ ❴❧♠❵❫ ❴❢r ♥♦❴ktron
y
❜ ❛n❫❥❝ ❜ntulk ❜n❫❥t❴rim❜ ol❴h❫ ❴t❴❢ktorLalu hasil yang diterima diolah oleh program dalam komputer. Ada beberapa syarat pada material yang
dikarakterisasi dengan SEM ini. Seperti yang dijelaskan sebelumnya bahwa
detektor mendeteksi elektron yang dipantulkan atau electron sekunder yang
dihasilkan oleh material, maka sifat ini dimiliki oleh material yang berjenis
logam. Jika material yang bersifat isolator dikarakterisasi dengan SEM, maka
hasilnya akan kabur dan mungkin akan hitam.
Hal ini dapat dilakukan dengan melapisi isolator tersebut dengan logam.
Proses pelapisan ini dapat dilakukan dengan beberapa cara, misalnya dengan
proses evaporasi atau proses sputtering. Pada proses evaporasi, logam
dipanaskan lalu menguap. uap logam ini menempel di atas material isolator.
Tebal lapisan diatur dengan mengatur waktu evaporasi. Sedangkan pada
proses sputtering, logam ditembaki dengan ion gas. Hal ini menyebabkan
atom-atom logam menjadi terlepas lalu menempel pada material isolator.
Skema dari SEM dapat ditunjukkan pada gambar berikut :
30 metoda karakterisasi material yang paling tua dan paling sering digunakan
hingga sekarang. Teknik ini digunakan untuk mengidentifikasi fasa kristalin
dalam material dengan cara menentukan parameter struktur kisi serta untuk
mendapatkan ukuran partikel. XRD terdiri dari slit dan film serta
monokromator.
Difraktometer sinar-x merupakan instrumen yang digunakan untuk
mengidentifikasi cuplikan berupa kristal dengan memanfaatkan radiasi
gelombang elektromagnetik sinar-x. Hasil yang diperoleh dari percobaan
adalah intensitas relatif (I/I1) dan sudut hamburan (2 ). Hamburan sinar-x
berasal dari atom-atom yang membentuk bidang kisi kristal dari cuplikan
yang diamati➌
Difraksi sinar-X terjadi pada hamburan elastis foton-foton sinar-X oleh atom
dalam sebuah kisi periodik. Hamburan monokromatis sinar-X dalam fasa
tersebut memberikan interferensi yang konstruktif. Dasar dari penggunaan
difraksi sinar-X untuk mempelajari kisi kristal adalah berdasarkan persamaan
sinar-31
➍ y➎n➏ ➐➑ ➏➒➓ ➎k➎➓ ➔ ➐ ➎➐ ➎l➎h j➎r➎k➎nt➎r➎ ➐➒ ➎ →➑ ➐➎➓➏ kisi➔ a dalah sudut antara sinar datang dengan bidang normal, dan n adalah bilangan bulat yang
disebut sebagai orde pembiasan.
Berdasarkan persamaan Bragg, jika seberkas sinar-X di jatuhkan pada sampel
kristal, maka bidang kristal itu akan membiaskan sinar-X yang memiliki
panjang gelombang sama dengan jarak antar kisi dalam kristal tersebut. Sinar
yang dibiaskan akan ditangkap oleh detektor kemudian diterjemahkan sebagai
sebuah puncak difraksi. Makin banyak bidang kristal yang terdapat dalam
sampel, makin kuat intensitas pembiasan yang dihasilkannya. Tiap puncak
yang muncul pada pola XRD mewakili satu bidang kristal yang memiliki
orientasi tertentu dalam sumbu tiga dimensi. Puncak-puncak yang didapatkan
dari data pengukuran ini kemudian dicocokkan dengan standar difraksi
➣↔ ➣↕ ↕↕
➙ ➛ ➜ ➝➞➝➟➝➠↕➡➛ ➢➛ ➟↕➜↕ ↔➢
3➤ ➥ ➜➦➧ ➨➩➫➡ ➦➭➦➯➲➫➲ ➩➭
➳➵➸➵ ➺➻t➻➼➸ ➻➸ ➻➽ ➻➺➼➾➚ ➾ ➼➸➽➻➪➵ ➪➵r➼p➼ t➵ ➶➹ ➼t ➘➵ ➪ ➼➴ ➼➻➪➵r➻➾➚ ➷➬
➮ ➱ ➳r✃➘ ➵s ➹ ➵ ➶➪➚ ➼t➼➸➘ ➹➵➘ ➻➶➵➸➽ ➼➸➹❐✃➘ ➵s ✃➾➘ ➻➽ ➼➘ ➻➽➻➺➼➾➚➾➼➸ ➽➻➺➼➪✃❐➼tur➻u➶ ❒➼➵tr➻➼➺❮➵ ➾➸➻➾❰ Ï➚➘ ➼➸ur ❮➵ ➾➸ ➻➾❒➵➘ ➻➸Ð➸ ➻Ñ➵➘ ➻r ➼ts Ò ➼➶➹ ➚➸➴ .
2. ➳❐✃➘➵➘➹➵➸➴➚Ó➻➼➸ÔÕÖ➽➻➺➼➾➚➾➼➸➽ ➻Ð➸ ➻Ñ➵❐➘ ➻➷ ➼➘×➘ ➺➼➶Ø➵➴➵❐➻ (Ð× Ø) ➽ ➻
❮➼➸➴➵❐➼➸ ➴.
3. ➳❐✃➘➵➘➹ ➵➸➴➚Ó➻➼➸ÙÚ❒ÛÚÖÙ➽ ➼➸Ü❒➽➻➺➼➾➚➾➼➸ ➽ ➻Ý➼➺➼➻Ý➵➘ ➼❐Þ➵❐➼➶➻➾ (Ò×➳×) ❮➼➸➴➵❐➼➸➴.
3➤ ß ↔➯ ➩➫à ➩➭ ➣➩á ➩➭
â➽ ➼➹ ➚➸ ➪➼ã ➼➸ä➼➸➴➽ ➻➴➚➸➼➾➼➸➹➼➽ ➼➹➵➸ ➵ ➺➻➷ ➻➼➸ ➻➸➻➼➽ ➼➺➼ã➬ 1. Ý➼Ó➼â× Ù× 4130
æ æ
ç è éêë ìíê(îï ðñ òóô)
õöìê ë÷í÷ëêëøêíprùú ûs ü ùøý öp÷þêÿ öëöêÿý ÷ë ✁ùú ûs ùíú öý÷ú öè
✂ è ✄ûú öë☎ûröëý ÷
õöìê ë÷í÷ëêëøêíÿ ûÿùø ùë ìý ÷ëÿ ûë ìü÷þêúí÷ësûú öÿûë ê✆öè
☎÷ÿ✝ ÷✁10. ✄ûú öë☎û✁öëý÷
4. ✄öú ø ÷✁ý÷ë✞÷ëì í÷✟ù ✁ùëì
õöìê ë÷í÷ëêëøêíÿ ûÿ✝ ÷ëøêý ÷þ ÷ÿ ûëì êí ê✁÷ëú ûú öÿ ûëê✆ö. ☎÷ÿ✝ ÷✁ 9. éêë ìí ê(✠ê✁ë÷✡û)
☛ ☞
✌ ✍ ✎✏✑ ✒✓✔ ✕✖
✗✒✘✙✓✚✛ ✚✓✙✓✜ ✙✛✢✏✣ ✙✤ ✚✓✘✒✑✥✏✑ ✒✢✏✓✙✦✒✍
✧✚✢ ✤✚✖ 12. ✎ ✏✑✒✓✔✕✖
6. ★✚✩✚✜✪✜ ✚✒✓✣✏✑ ✑
✗✒✘✙✓✚✛ ✚✓✙✓✜ ✙✛✢✏✓✘ ✘✚✓✜ ✙✓✘✑✥✏✑ ✒✢✏✓✙✦✒.
✧✚✢ ✤✚✖13. ★✚✩✚✜✪✜ ✚✒✓✣✏✑✑
3✫ ✬ ✭✮✯ ✰ ✱✲✳✮✭ ✱✴ ✱✵✶✷✶ ✸✴
✹✺ ✚✥✙✓✥✖✕✑ ✏✺ ✙✖✛✏✖✦ ✚✥ ✚✺✚✥✏✓✏✣✒✜✒✚✓✒✓✒✻ ✚✒✜ ✙✼ 1. ✽✏✖ ✑ ✒✚✥✚✓✪✥✏✑ ✒✢✏✓✾✦✒
✿ ✙✢✣ ✚❀✑✥✏✑ ✒✢✏✓✙✦✒ ✻ ✚✓✘✚✛ ✚✓✺✒✘✙✓✚✛ ✚✓✥ ✚✺✚✥✏✓ ✏✣✒✜✒✚✓✒✓ ✒✑ ✏✤ ✚✓✻ ✚✛18 ✑✥✏✑ ✒✢✏✓ ✍ ✽✚✺ ✚ ✥✏✓ ✏✣✒✜✒✚✓ ✒✓ ✒✺✒✣ ✚✛✙ ✛✚✓✺✚✣ ✚✢✺✙✚ ✤✚ ✘✒✚✓❁✺✏✓✘✚✓ ✙✖✚✒✚✓ ✑ ✏✤✚✘ ✚✒ ✤✏✖ ✒✛ ✙✜ : ✔✚✘✒✚✓ ✥✏✖✜ ✚✢ ✚ ❂ ✚✖ ✒✚✑ ✒ ✩ ✚✛✜ ✙ ✕✛✑ ✒✺ ✚✑ ✒ 1 ✦ ✚✢, 4 ✦✚✢, 9
❡6
❢ ❣ ❤✐❥❦ ❧♠ ❧♥
Yang dimaksud dengan ♦✐❥❦❧♠ ❧ ♥ yaitu pembersihan permukaan logam yang bertujuan untuk menghilangkan kotoran dan membentuk struktur
permukaan spesimen yang baik. Dalam hal ini ada beberapa proses yang
dilakukan antara lain:
a. Proses♣q✐♠r s♠ ❧ ♥
Proses penggosokan pada logam yang menggunakan amplas 200-1200.
b. Proses Pencucian Lemak
Pencucian lemak dengan menggunakan etanol dimaksudkan agar benda
kerja bebas dari lemak atau minyak yang dapat mengganggu daya rekat
hasil pelapisan.
c. Proses Pembilasan
Proses pembilasan dengan menggunakan air yang berfungsi untuk
menghilangkan sisa-sisa etanol yang masih ada pada permukaan benda
kerja.
4. ♣♠♦t✐♠ ❧ ♥
Proses✉♠♦t✐♠ ❧♥adalah proses pembersihan material setelah proses cleaning dengan menggunakan bahan kimia yang mengandung asam.
Dalam hal ini ada beberapa proses yang dilakukan antara lain :
✈ ✇
①② ③④r s ⑤④⑥ ⑦⑧ ⑦⑨⑩⑥ ❶⑨ ❷⑩❸ ⑧❸ ⑩⑥ ⑤⑩❶⑩ p④❹ ⑧❸⑩ ⑩⑥r ❺④⑥❶ ⑩ ❸ ④r❻⑩ y⑩⑥ ❼ ❹⑩ ③⑨❽ ❹④⑥ ❼⑩⑥ ❶ ⑧⑥❼ ❷④❹ ⑩❸ ⑩⑩tu❹ ⑨⑥⑩❸❾y ❿④④⑥ ❶ ⑩❹r ❺④⑥ ❶⑩ ❸④❻⑩r ❸④❶ ⑩ ❷⑩❹ ❷⑩⑩⑥rut ➀⑩ ➁➂+➂3① ➁4+⑩⑨➃ ❶④⑥ ❼⑩⑥ ⑤④➃❺⑩⑥ ❶⑨⑥ ❼ ⑩⑥ 1 : 1 : 1 (❶⑩ ❷⑩❹ ➄②❷⑧❹ ④).
3➅ ➆ ➇➈➉ ➊➋➉ ➌➍➎➈➋
➏⑩❹ ❺⑩➃14. ➐⑨⑩❼➃ ⑩❹⑩ ❷⑨➃ ⑤④⑥④ ❷⑨➑⑨⑩⑥
Mulai
➒ ➓➔ →➣↔➣ ➓↕➙➛ ➓➔➙↕→➛➜➝➔ ➙➞↕ ➟
➠↕➙ ➝➣ ➛ ➡➛➜➢➛ ➤➛ ➜➢➛➥ ➛➡➛ →➔➛➜➙↕➜ →➛ ➤
➠↕➜ ➦➔ ➥ ➣➛ ➜➧➨ ➝➣ →➛➝➣
➒ ➣➩➡➔↔ ➛➜→➛➜➒➛➙➛➜ ➫➜ ➛↔ ➣ ➝➛→➛ ➓➛→➛➜➡↕➩➢➛➤➛ ➝➛ ➜
Selesai Analisa Sampel
➭➛➓➛➯➛ ➝➣ ↔➠↕➜ ➦➔➥ ➣ ➛➜
➵ ➸➵ ➺
➻➼ ➽➾➚➪➸➶➹➸➶➻➸➘➸➶
➴➷➬ ➻➮➱ ✃❐❒❮❰
ÏÐÑ ÒÓ Ô ÕÖ×Ð ØÐÑÐ Ù ÚÐÛ Ò Ñ ÕÛ Ð ÙÜÝÐ ÒÐ Ù ÔÕÙÜÞ ßÒÐ Ù ÚÐ Ù à×Ñ ÕÛ áÐÑ Ò âÐ Ù Ü ã ÕÓÐ Ø ÚÒÓÐÝ ÞÝ Ð ÙÚÐ ÓÐ ÖÔÕÙÕÓÒãÒÐ ÙÒÙÒ, × Õ×ÕÛÐÔ Ð ØÐ ÓâÐ Ù ÜÚÐÔ Ð ãÚÒÑ ÒÖÔÞÓÝÐ Ù, Ñ Õ×ÐÜÐ Ò × ÕÛÒÝ Þ ãä
1. åÐ ßÞ àÝÑ ÒÚÐÑ Ò × Ð ßÐ æçèç 4130 âÐ Ù Ü ÚÒàÝÑ ÒÚÐÑ Ò ÔÐ ÚÐ ãÕÖÔÕÛÐ ãÞ Û éê ë ìí
Ö ÕÖÔÕÛî ÕÔ Ð ã ÔÕÛ ÜÕÛÐÝ Ð Ù Ô ÕÛ ãÕÖÞÐ Ù Òà Ù-ÒàÙ ÚÐ Ù Ð ãàÖ Ñ ÕØ ÒÙÜ ÜÐ Ö ÕÖÔÕÛî ÕÔ Ð ãÔ Û àÑ ÕÑ Ý àÛ àÑ Ò ÚÐ Ù ÖÕÖ× ÕÙ ãÞÝ ÓÐÔ ÒÑ Ð ÙàÝ Ñ ÒÚÐ âÐ Ù ÜÑ ÕÖÐÝÒÙ ãÕÛ ÓÒØÐ ãÑ ÕÒÛ ÒÙ ÜÚ ÕÙ ÜÐ ÙÔ ÕÙÐ Ö× Ð ØÐ ÙïÐÝãÞ àÝ Ñ ÒÚÐÑ Ò.
ð ñ òÕÛ ßÐ ÚÒÙ âÐ Ô ÕÙÐ Ö× Ð ØÐ Ù ×ÕÛÐ ã óô õö÷ø ù ÷ú öûü ÚÒÝ ÐÛ ÕÙÐÝ Ð Ù ÔÕÖ×ÕÙãÞ ÝÐ Ù ÓÐÔÒÑÐ Ù Ð ïÐ Ó âÐ Ù Ü ÝÐâÐ íÛ ÖÕÙ ßÐ ÚÒ ÓÐÔÒÑÐ Ù ÔÛ à ãÕÝãÒý íÛþÿ ÔÐ ÚÐ Ô Û àÑ ÕÑ àÝÑ ÒÚÐÑ Ò âÐ ÙÜ ãÕÛ ßÐ Ú Ò ÔÐÚÐ Ð Ù ãÐÛ ÖÞ Ý Ð ÓàÜÐ Ö ÚÐ Ù Ñ ÕÖÐÝÒÙ Ö ÕÙÒÙ ÜÝ Ð ã Ñ ÕÒÛ ÒÙ ÜÚ ÕÙ ÜÐ ÙÔ ÕÙÐ Ö× Ð ØÐ ÙïÐÝãÞàÝ Ñ ÒÚÐÑ Ò
✆ ✝
✞✟✠ ✡☛ ☞☛ ✌
✩ ✪✫✬ ✪✭✮✯✰✬ ✪✱ ✪
✲✳a✴ ✵✶✷✸✹✺ ✻✴✼ ✻✽ ✾a✴ ✵✶✷✿❀❀ ❀ ✹ Ilmu Bahan. ❁a❂ ✻✽✵a, ❃❄ ✳❅✲❂ ❆a✽a
✲✳ ❆✵ead, ❃.✸✹✷ ✿❀ ❀ ❇ ✹Teknologi Mekanik. ❁a❂✻✽ ✵a, E✽ ❈a✴ ❉❉a
✲❊❋●✴ ✵e✽ ✴ ✻✵❅ ✶✴✻❈, 1993.ASM handbook vol.1:329
Chamberlain J., Trethewey KR.. 1991, KOROSI (Untuk Mahasiswa dan Rekayasawan), PT Gramedia Pustaka Utama, Jakarta.
Dah E N, Tsipas S, Hiero M P, Perez F J., 2007. Study of the cyclic oxidation resistance of Al coated ferritic steels with 9 and 12%Cr, Corrosion science, Vol. 49, pp. 3850-3865.
Davis, Troxell, dan Hauck. 1998. The Testing of Engineering Materials. Edisi 4. Penerbit Mc Graw Hill. New York.
Fontana, M.G., 1986. Corrosion Engineering, 3rd edition. McGraw-Hill Book Company, New York.
❍■❏❑▲, ▼. Da◆❖ P 2005. Korosi dan Rekayasa Permukaan. ❍◗ ❘■❙e❚ ❏■❚❯❑ ❱❑❲ ■ ▼eda❏, ▼eda❏P❳ ■a❚❨e❨❩ada 7 Feb❲ ◆❬❲■ 2012.
❭ac❚❪❫a❴▲ ◗ ❏❖❵. 1997. I Welding: Principles and Prantices . Mc Graw Hill. USA
Townsend, 1992.Surface Engineering ASM Handbook volume 5.ASM International.