PENAPISAN VIRTUAL INTERAKSI SENYAWA FENOLIK, ALKALOID,
DAN SAPONIN DENGAN RESEPTOR ESTROGEN ALFA
ERON TIRTA WIJAYA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Penapisan Virtual Interaksi Senyawa Fenolik, Alkaloid, dan Saponin dengan Reseptor Estrogen Alfa adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, July 2015
Eron Tirta Wijaya
RINGKASAN
ERON TIRTA WIJAYA. Penapisan virtual interaksi senyawa fenolik, Alkaloid, dan Saponin dengan reseptor estrogen alfa. Di bawah bimbingan NURI ANDARWULAN, NANCY DEWI YULIANA dan ARRY YANUAR.
Osteoporosis terjadi pada keadaan ketika resorpsi tulang lebih cepat dibandingkan dengan pembentukan tulang. Hal ini dipicu oleh penurunan produksi hormon estrogen. Penggunaan estrogen sebagai pilihan untuk mengatasi osteoporosis dilaporkan memiliki kemugkinan dapat meningkatkan terjadinya kanker, sehingga penelitian untuk menemukan senyawa anti-osteoporosis yang aman perlu dilakukan. Senyawa fenolik, alkaloid, dan saponin ditemukan berlimpah dalam tumbuhan yang dapat dikonsumsi. Beberapa dari tumbuhan tersebut telah diteliti dan menunjukan aktivitas pencegahan osteoporosis. In silico bearti eksperimen dengan basis komputer
yang dapat digunakan untuk menjelaskan mekanisme dari interaksi protein (misalnya antara resptor dengan ligan) dengan mekanisme penambatan yang mengidentifikasi pose pengikatan ligan dengan tepat saat ligan terikat di dalam reseptor dan untuk memprediksikan energi afinitas (ΔG) antara ligan dengan resptor. Teknik ini digunakan sebagai penghubung ke tahap analisis berikutnya dengan waktu dan biaya yang singkat untuk menemukan efektivitas dari senyawa dibandingkan dengan menggunakan teknik in vitro atau in vivo secara langsung. Penelitian ini bertujuan
untuk menapis kapabilitas ikatan dari beberapa senyawa fenolik, alkaloid, dan saponin pada estrogen reseptor (ER)-α in silico menggunakan beberapa software seperti
Autodock4.2, Ligplot+, dan PyMOL. AutoDock digunakan untuk memperkirakan
afinitas senyawa pada reseptor dengan mengkalkulasikan nilai ΔG. Kemudian,
Ligplot+ dan PyMol digunakan untuk membuat hipotesis bedasarkan visualisasi 2 dan
3 dimensi. Bahan yang digunakan pada penelitian ini adalah sebagai berikut: struktur makromolekul ER-α (1SJ0), 2 kontrol positif (17-b estradiol dan dienestrol) dan 89 ligan. Sampel ligan terdiri dari 32 senyawa fenolik, 40 senyawa alkaloid, dan 17 senyawa saponin.
Hasil penelitian, terdapat beberapa ligan yang memiliki potensi esterogenik. Hal ini dapat dilihat dari nilai ∆G yang berada di bawah nilai ∆G dari kontrol positif diensterol (-9.03 Kkal/mol). Kebanyakan dari ligan terlihat menjanjikan untuk dikembangkan lebih lanjut sebagai fitoestrogen. Semua kelompok yang diuji memiliki ligan yang berpotensi antara lain pinoresinol dan matairesinol dari kelompok fenolik, jurubine, taxol, emetine dan reserpine dari kelompok alkaloid, dan cucurbitacin E, protopanaxadiol, astragaloside III, dan sarsasapogenin dari kelompok saponin. Visualisasi penambatan menunjukan bahwa nilai ∆G dipengaruhi oleh ikatan hidrogen dan interaksi hidrofobik. Bedasarkan visualisasi fenolik, residu dominan dari ikatan hidrogen biasanya terikat pada sisi yang berlawanan, yaitu posisi 2: GLU 353, LEU 387, ARG 394 — posisi 3: MET 421, GLY 521, HIS 524. Senyawa fenolik yang terikat pada posisi 2 dan 3 dengan jarak 10.78±0.65 Å dari masing-masing gugus OH umumnya memiliki potensi esterogenik. Selain itu diperlukan tahap penelitian berikutnya secara in vitro dan in vivo untuk memastikan hasil interaksi ini
menghasilkan efek positif (agonist).
SUMMARY
ERON TIRTA WIJAYA. Virtual Screening of Phenolic, Alkaloid, and Saponin Compound with Estrogen Receptor-α Interaction. Supervised by NURI ANDARWULAN, NANCY DEWI YULIANA and ARRY YANUAR.
Osteoporosis occurs at the situation when bone resorption is faster than bone formation. It is triggered by a decrease in estrogen hormone production. Estrogens intervention as an option to overcome osteoporosis was reported to possibly enhance cancers occurrence, thus research to find safer anti-osteoporosis agent is required. Phenolics, alkaloids and saponins are found abundantly in many edible vegetables. Some of them were reported to show osteoporosis preventive activity.
In silico can be defined as computer based experiment, which can explain the
mechanism of protein interaction (e.g. between receptor and ligand) by docking mechanism which will precisely identify the binding pose of ligand when it is attached on the receptor and to predict the energy affinity (ΔG) between ligand and receptor. This technique was used as the connection to other step of analysis in shorter time and expenses on find out the effectivity of the compound compared to directly use in vitro or in vivo method. The research aimed to screen the binding
caplability of several phenolics, alkaloids, and saponins to the estrogen receptor (ER)-α in silico using Autodock4.2, Ligplot+, and PyMOL software. Autodock was
used to estimate compounds affinity to the receptor by calculating the value of ΔG.
Furthermore, Ligplot+ and PyMol were used to develop hypotheses based on
visualization 2 and 3 dimension. Materials used for this research were as follow: macromolecules ER-α (1SJ0) structure, two positive controls (17-b estradiol and dienestrol), and 89 ligands. The sample ligands consisted of 32 phenolics, 40 alkaloids, and 17 saponins.
As results, there were some ligands that had estrogenic potency. This can be seen from ∆G value which were under ∆G of positive control diensterol (-9.03 Kcal/mol). Most of them seems promising to be developed further as phytoestrogen. All tested groups was found to be potent ER ligands such as pinoresinol and matairesinol from phenolic group, jurubine and taxol, emetine and reserpine from alkaloid group, and cucurbitacin E, protopanaxadiol, astragaloside III, and sarsasapogenin from saponin group. Docking visualization showed that ∆G value were affected by hydrogen bonds and hydrophobic interactions. Based on phenolic visualization, residue of hydrogen bond usually bound to side of the ligand is at position 2: GLU353, LEU387, ARG394 — position 3: MET421, GLY521, HIS524. The phenolic compounds which have bound at position 2 and 3 with length of about 10.78±0.65 Å for each their hydroxyl usually have estrogenic potency. Further in vitro and in vivo studies are needed to ensure the results of these interaction generate
positive effect (agonist)
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Teknologi Industri Pertanian
PENAPISAN VIRTUAL INTERAKSI SENYAWA FENOLIK, ALKALOID,
DAN SAPONIN DENGAN RESEPTOR ESTROGEN ALFA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
Judul Tesis : Penapisan Virtual Interaksi Senyawa Fenolik, Alkaloid, dan Saponin dengan Reseptor Estrogen Alfa
Nama : Eron Tirta Wijaya NIM : F251120141
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala anugrah dan rahmat-Nya sehingga karya tulis yang berjudul Penapisan Virtual Interaksi Senyawa Fenolik, Alkaloid, dan Saponin dengan Reseptor Estrogen Alfa sebagai tugas akhir untuk mendapatkan gelar Magister Sains pada Program Studi Ilmu Pangan, Sekolah Pascasarjana, Insitut Pertanian Bogor berhasil diselesaikan.
Terima kasih penulis ucapkan kepada Ibu Prof. Dr. Ir Nuri Andarwulan M.Si selaku ketua komisi pembimbing, Ibu Dr. Ir. Nancy Dewi Yuliana, M.Sc dan Bapak Dr. Ir. Arry Yanuar, M.Si. Apt. selaku anggota komisi pembimbing yang telah banyak mengarahkan dan memberikan saran selama berjalannya penelitian hingga penulisan karya tulis ini. Penulis juga ingin mengucapkan terima kasih keapada Bapak
Puspo Edi Giriwono, STP., M.Sc, Ph.D dan Ibu. Dr. Ir. Endang Prangdimurti, MSi yang telah meluangkan waktunya untuk menjadi penguji di sidang tesis. Ungkapan terima kasih juga disampaikan kepada seluruh staff dan rekan di laboratorium komputasi biomedik dan rancangan obat, Fakultas Farmasi, Universitas Indonesia, Depok. Keluarga yang selalu mendukung, serta seluruh sahabat dan teman atas segala doa, kasih sayang, dan dukungannya.
Penulis menyadari bahwa karya tulis ini masih jauh dari sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran membangun untuk memperbaiki dan menyempurnakan penulisan karya tulis ini selanjutnya. Akhir kata, penulis berharap karya tulis ini dapat bermanfaat bagi semua pihak yang membutuhkan untuk menjadi pelengkap dalam dunia teknologi pangan untuk menjawab tantangan analisis ke depan dan bagi pengembangan ilmu dan penerapan pembelajaran, khususnya bagi Program Studi Ilmu Pangan, Sekolah Pascasarjana, Institut Pertanian Bogor.
Bogor, July 2015
DAFTAR ISI
DAFTAR TABEL x
DAFTAR GAMBAR x
DAFTAR LAMPIRAN x
1 PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 3
Tujuan Penelitian 3
Manfaat Penelitian 3
Ruang Lingkup Penelitian 3
2 TINJAUAN PUSTAKA 4
3 METODE 8
Bahan 8
Alat 8
Prosedur Penelitian 9
4 HASIL DAN PEMBAHASAN 12
Preparasi Struktur Makromolekul 12
Validasi Metode Penapisann Virtual in silico 12
Penapisan Virtual dan Visualisasi Penambatan Senyawa Fenolik 12 Penapisan Virtual dan Visualisasi Penambatan Senyawa Alkaloid 18 Penapisan Virtual dan Visualisasi Penambatan Senyawa Saponin 20
5 KESIMPULAN DAN SARAN 26
Kesimpulan 26
Saran 26
DAFTAR PUSTAKA 27
LAMPIRAN 36
DAFTAR TABEL
1 Hasil validasi nilai EF1 dan AUC 12
2 Sifat kimia dan sumber pangan pada kelompok fenolik 14 3 Residu asam amino dominan dari ER-α yang berikatan hidrogen 16 4 Sifat kimia dan sumber pangan pada kelompok alkaloid 21 5 Sifat kimia dan sumber pangan pada kelompok saponin 23
DAFTAR GAMBAR
1 Hubungan massa tulang dengan penuaan 4
2 Siklus penghancuran dan pembentukan tulang 5
3 Penurunan hormon estrogen 5
4 Reseptor estrogen-α (1SJ0) 7
5 Boxplot ∆G dengan sub kelas fenolik 13
6 Visualisasi posisi dari residu asam amino dominan dari ER-α yang
berikatan hidrogen 17
7 Penambatan Ligan Quersetin dengan Residu pada Posisi 2 dan 3 18
8 Boxplot ∆G dengan sub kelas alkaloid 19
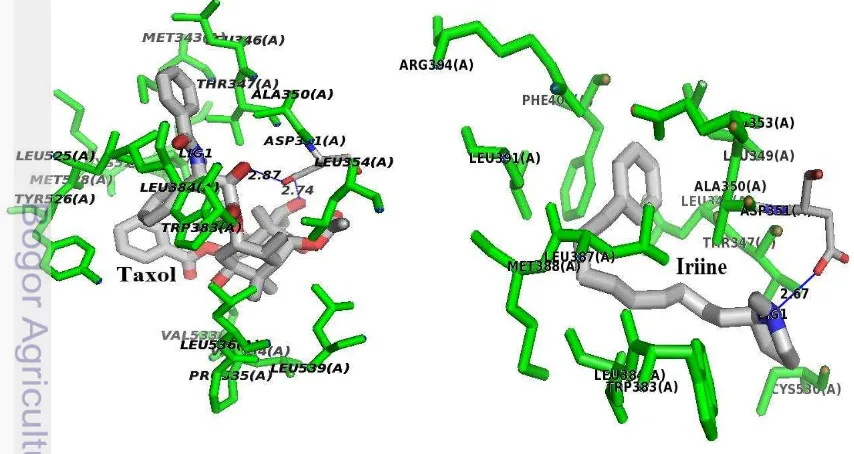
9 Penambatan ligan alkaloid (Taxol dan Iriine) 19
10 Boxplot ∆G dengan sub kelas saponin 20
11 Penambatan ligan saponin (protopanaxadiol dan cucurbitacin) 24
DAFTAR LAMPIRAN
1 Tampilan Situs Protein Data Bank (PDB) 36
2 Tampilan Situs Pub Chem 36
3 Tampilan Program PyRx 37
4 Tampilan Situs A Database of Useful Decoys: Enhanced (DUDE) 37
5 Tampilan Program Open Babel 38
6 Tampilan Program Auto Dock 4.2 38
7 Berkas min.in 39
1
PENDAHULUAN
Latar Belakang
Osteoporosis atau pengeroposan tulang adalah penyakit berkurangnya massa tulang dan adanya perubahan mikroarsitektur (bentuk mikro) jaringan tulang yang mengakibatkan menurunnya kekuatan tulang dan meningkatnya kerapuhan tulang, sehingga menyebabkan tulang menjadi mudah patah. Penyebab utama seseorang mengalami osteoporosis adalah proses resorpsi (penghacuran) tulang oleh osteoklas lebih cepat dibandingkan proses pembentukan tulang oleh osteoblas, sehingga mengakibatkan pengeroposan tulang (Raisz, 2005). Osteoporosis banyak ditemukan pada wanita yang telah mengalami menopause karena pada saat tersebut terjadi penurunan hormon estrogen yang signifikan. Menurut Sipos et al. (2009), penurunan hormon estrogen dapat
menyebabkan menurunnya Reseptor Osteoprotegerin (OPG) dan menurunnya penyerapan kalsium di usus yang menyebabkan meningkatnya Hormon Paratiroid (PTH). Hormon ini menstimulasi pembentukan osteoklas sehingga menyebabkan massa tulang menurun dan menjadi keropos.
Estrogen merupakan molekul steroid, yang berperan utama dalam mengatur metabolisme pada tulang wanita maupun pria. Estrogen pada organ tubuh dimediasi melalui inti dan membran yang berdimerisasi dengan Estrogen Reseptor (ER) untuk mengatur transkripsi gen estrogen responsif. ER adalah molekul protein yang berada di dalam sel, yang menjadi target dari hormon estrogen (NCI, 2010). Estrogen pada manusia bekerja dengan menggunakan 2 tipe reseptor yaitu ER-α dan ER-β (Raisz, 2005). Kedua ER ini memiliki peran yang serupa pada tulang, tetapi menurut Cui et al. (2013), ER-α
adalah satu-satunya mediator yang dapat meningkatkan massa tulang, karena penghilangan ER-β tidak berpengaruh terhadap panjang dan massa tulang (Pearce & Jordan, 2004). Selain itu, Aktivasi ER-α mentransmisikan sinyal untuk memperpanjang hidup osteoblast pada tikus wanita (Imai et al., 2010). Maka dari itu, penelitian kali ini
digunakan ER-α sebagai reseptor jaringan tulang. Pada tulang, estrogen berkaitan langsung dengan osteosit dalam menurunkan aktivitas pembentukan tulang, osteoklas dalam menurunkan perombakan tulang, danosteoblas dalam memelihara pembentukan
tulang(Khosla et al., 2012), sehingga terapi hormon estrogen menjadi salah satu pilihan
dalam mencegah osteoporosis pada lanjut usia.
Menurut Wells et al. (2002), terapi estrogen selama 2 tahun dapat meningkatkan
massa tulang sekitar 7%, namun konsumsi estrogen secara terus-menerus dapat mengindikasikan kanker payudara dan rahim (NCI, 2010 dan Nelson et al., 2013). Hal
tersebut terjadi karena estrogen tidak hanya mendukung terhadap jaringan tulang, melainkan terhadap jaringan payudara dan rahim juga. Dewasa ini telah banyak penemuan senyawa untuk memblokir aksi negatif dari estrogen yaitu Selective Estrogen Reseptor Modulator (SERM) seperti tamoxifen dan raloxifene. Bedasarkan penelitian Love et al.
(1992), SERM tersebut memiliki efek positif dalam meningkatkan massa tulang dan memiliki efek negatif pada payudara. Sedangkan SERM (lasofoxfene dan bazedoxifene) tidak mengindikasikan kanker payudara dan rahim tetapi meningkatkan risiko trombosis dan hot flushes (Cummings et al., 2010; Goldstein et al., 2011; Kulak et al., 2011). Oleh
karena itu, diperlukan suatu senyawa yang dapat berinteraksi dengan ER-α untuk
Fitoestrogen merupakan hormon tanaman yang memiliki potensi estrogenik dan diduga tidak memiliki efek samping dari terapi estrogen. Menurut Cornwell et al. (2004),
Fitoestrogen seperti isoflavonoid, stilbene, lignan, dan coumestan banyak ditemukan pada tumbuhan yang dapat dikonsumsi, serta telah terkait dalam pencegahan kanker, perlindungan kardiovaskular dan pengaturan sistem imun (Watanabe et al., 2002).
Penelitian in vivo pada manusia oleh Yang et al. (2012), menyatakan ekstrak kacang
kedelai yang tinggi isoflavonoid dapat memberikan efek positif pada tulang dengan meningkatkan deoxypyridinoline atau kreatinina sebesar 10.53% (p < 0.05) dan 11.58%
(p < 0.05) dengan pemberian ekstrak kacang kedelai pada dosis 35 mg dan 70 mg selama 6 bulan. Penelitian in vivo lain pada tikus, harmaline (senyawa alkaloid heterosiklik)
meningkatkan pembentukan osteoblas dengan mendorong aktivitas fosfatase alkali dan ekspresi osteocalcin (Yonezawa1 et al., 2011). Selain itu penelitian in vitro, Panax Notoginseng Saponin (PNS) yang kaya akan ginsenoside (senyawa saponin steroidal)
dapat menstimulasi pembentukan sel stroma sumsum tulang dan meningkatkan pembentukan tulang dengan meningkatkan ekspresi dari gen pembuat tulang dan menurunkan ekspresi dari gen pembuat adiposit (Li et al., 2011). Bedasarkan penelitian
tersebut, banyak senyawa fenolik, alkaloid, dan saponin yang memiliki kemiripan struktur dengan isoflavonoid, harmine, atau ginsenosides yang belum diteliti untuk aktivitas pencegahan osteoporosis. Hal ini menjadi dasar pemilihan kelompok ligan yang akan diujikan secara in silico.
In silico dapat didefinisikan sebagai percobaan berbasis komputer, di mana
matematika model dari sistem fisiologis atau farmakologi dikembangkan dan diuji pada komputer (Colquitt et al., 2011). Metode in silico adalah satu dari banyak teknik yang
berpotensi dalam menigkatkan penemuan dan pengembangan obat baru (Ekins et al.,
2007), semenjak in vitro dan in vivo memerlukan waktu yang lebih panjang dan biaya
yang besar. Teknik ini dapat diterapkan dalam bidang kimia untuk menemukan komponen yang baru, menguraikan mekanisme interaksi protein (misalnya antara reseptor dan ligan), dan memprediksi interaksi antara molekul (Cozzini & Luca, 2012). Penguraian mekanisme interaksi protein dapat menggunakan mekanisme penambatan (docking).Penambatan bertujuan untuk mengidentifikasi secara tepat pose ligan ketika
terikat pada makromolekul (reseptor) dan memprediksi afinitas antara ligan dan protein (Krovat et al., 2005). Bila ligan yang diujikan berjumlah banyak atau multiligan, maka
penambatan dilakukan dengan cara penapisan virtual. Penelitian secara in silico dengan
menggunakan penapisan virtual telah juga dilakukan oleh Indrawan (2013), yang memberikan informasi berbagai senyawa fenolik yang berperan dalam meningkatkan air susu ibu dengan mengukur energi ikatan (∆G) antara reseptor dan ligan yang diuji. Semakin rendah ∆G, maka semakin mudah ligan tersebut berinteraksi dengan reseptor (Yuiana et al., 2013).
Bedasarkan potensi alam yang tinggi di Indonesia, maka Indonesia banyak memiliki jenis dan ragam dari sumber daya alam khususnya tumbuhan yang lazim dikonsumsi dengan harapan tumbuhan tersebut berpotensi mengandung ligan yang dapat mencegah osteoporosis seperti permasalahan di atas. Penapisan virtual secara in silico
digunakan sebagai penyambung antara satu tahap ke tahap berikutnya dengan waktu yang singkat dan biaya yang rendah untuk menentukan efektifitas senyawa dibandingkan dengan metode in vitro dan in vivo. Menurut Seifert et al. (2003), metode in silico dapat menghemat 130 juta dollar Amerika serikat dan 0.8 tahun per obatnya, namun teknik ini tidaklah dapat menerangkan hasil seperti in vivo karena sistem biologis makhluk hidup
Perumusan Masalah
Tumbuhan konsumsi yang terdapat di Indonesia umumnya mengandung senyawa fenolik, alkaloid, dan saponin, yang pada senyawa tersebut sangat banyak terdapat macam ligan yang mungkin bersifat estrogenik. Selain itu mekanisme interaksi suatu ligan dengan ER-α belum diketahui, sehingga diperlukan metode untuk memprediksi interaksi antara ligan dengan reseptor. AutoDock merupakan program penambatan yang dapat memprediksi interaksi berdasarkan nilai ∆G antara ligan dan reseptor. Selain itu, penambatan juga dapat dilakukan pada PyRx 0.8 yang dapat melakukan proses penambatan untuk sejumlah ligan dalam waktu yang relatif lebih singkat. Sebagai pelengkap, posisi penambatan divisualisasikan dengan Autodock Tools 1.5.6rc3, PyMOL 1.3 dan Ligplot +1.4.4.
Tujuan Penelitian
Tujuan dari penelitian ini adalah 1) untuk mengidentifikasi senyawa dalam tumbuhan yang mengandung fenolik, alkaloid dan saponin yang dapat berinteraksi spontan dengan makromolekul ER-α secara in silico, 2) memperoleh data nilai ΔG
interkasi ligan terhadap makromolekul, dan 3) menyusun hipotesis interaksi ligan dengan makromolekul berdasarkan hasil visualisasi.
Manfaat Penelitian
Manfaat dari penelitian ini adalah diperolehnya simulasi interaksi antara ligan dari tumbuhan dengan ER-α dalam mencegah osteoporosis dalam waktu yang relatif singkat dan biaya yang jauh lebih murah. Informasi ini dapat digunakan sebagai hipotesis dan penghubung ke tahap penelitian secara in vitro dan in vivo dalam hal penemuan senyawa
yang bersifat estrogenik, serta diperoleh juga berbagai rekomendasi pangan yang dapat digunakan untuk mencegah osteoporosis yang umumnya diderita oleh manula wanita ataupun pria.
Ruang Lingkup Penelitian
Penelitian ini didesain untuk mempelajari interaksi ligan tanaman yang mengandung fenolik, alkaloid, dan saponin dengan ER-α secara in silico. Teknik in silico
2
TINJAUAN PUSTAKA
Mekanisme Terjadinya Osteoporosis
Osteoporosis adalah penyakit berkurangnya massa tulang, sehingga tulang menjadi tipis, rapuh, keropos, dan mudah patah. Bedasarkan penyebabnya osteoporosis dibagi menjadi 2, osteoporosis primer disebabkan berhentinya produksi hormon (khususnya wanita) dengan bertambahnya usia, serta osteoporosis primer sendiri dibagi
menjadi 2 tipe, “pascamenopause” yang terjadi pada wanita dan disebabkan karena
menurunnya hormon estrogen (tipe I) dan “senil” yang terjadi pada wanita ataupun pria,
dan disebabkan karena proses penuaan termasuk disfungsi osteoblas (tipe II) (Sipos et al.,
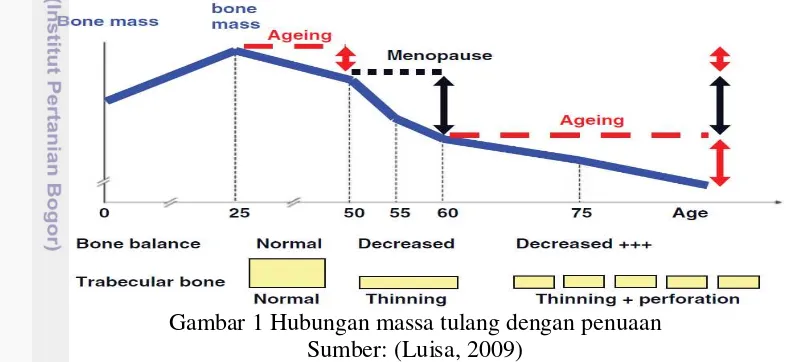
2009), untuk ilustrasi penurunan massa tulang yang disebabkan osteoporosis primer dapat dilihat pada Gambar 1 sedangkan osteoporosis sekunder disebabkan oleh berbagai penyakit tulang (chronic rheumatoid atau artritis), pengobatan steroid dengan jangka
panjang, kelumpuhan otot, ataupun hipertiroid.
Gambar 1 Hubungan massa tulang dengan penuaan Sumber: (Luisa, 2009)
Penyebab utama terjadinya osteoporosis adalah penurunan hormon estrogen. Menurut Sipos et al. (2009), penurunan hormon estrogen berkorelasi dengan menurunnya
OPG dan menurunnya penyerapan kalsium di usus. Kekurangan kalsium pada tubuh menyebabkan meningkatnya PTH yang berhubungan dengan meningkatnya receptor activator of nuclear factor kappa-B Ligand (RANKL). Peningkatan RANKL dan
menurunnya OPG menstimulasi pembentukan osteoklas, meningkatnya osteoklas menyebabkan proses resorpsi tulang. Pada keadaan normal, bila kerja osteoklas atau resorpsi tulang dapat diimbangi oleh kerja osteoblas atau pembentukan tulang, maka tidak akan terjadi penurunan massa tulang, tetapi bila terjadi stimulasi pembentukan osteoklas, maka mengakibatkan massa tulang menurun dan menyebabkan keropos atau osteoporosis. Ilustrasi kerja dari osteoklas danosteoblas sebagai siklus dapat dilihat pada Gambar 2.
Selain dari kekurangan kalium tubuh, peningkatan PTH dapat juga disebabkan oleh menurunnya kadar vitamin D (calcitrol), karena vitamin D tidak hanya berperan dalam mengatur penyerapan kalsium dan fosfor di usus, tetapi menghambat pembentukan PTH (Raisz, 2005). Khosla et al. (2012), menyatakan bahwa terdapatnya hormon estrogen
perombakan tulang oleh osteoklas dan menstimulasi proses pemeliharaan tulang oleh osteoblas, sehingga estrogen bersifat positif pada jaringan tulang atau mencegah osteoporosis. Ilustrasi penurunan estrogen dapat dilihat pada Gambar 3.
Gambar 2. Siklus penghancuran dan pembentukan tulang Sumber: (Luisa, 2009)
Gambar 3: Penurunan hormon estrogen Sumber: (Spios et al., 2009)
Senyawa Fenolik dan Saponin dalam Tumbuhan
Terdapat beberapa anggota senyawa fenolik (minimal memiliki 1 gugus fenol) yang memiliki peran dalam meningkatkan massa tulang atau mencegah osteoporosis. Menurut Kanno et al. (2004), pencegahan osteoporosis dapat terjadi karena sebagian
anggota fenolik memiliki kemiripan struktur dengan 17β-estradiol (estrogen), kemiripan
bekerja sebagai efek positif dari estrogen. Senyawa yang memiliki potensi estrogenik disebut fitoestrogen. Anggota fenolik yang termasukfitoestrogenantara lain isoflavonoid seperti puerarin, genistin, daidzein dan, genistein; stilbenes seperti trans-resveratro; lignan seperti mataresinol; coumestan seperti coumestrol. (Cornwell et al., 2004
Cherdshewasart et al,. 2008; Schilling et al., 2013). Menurut Cassidy (2003), fitoestrogen
memberikan dampak positif seperti mencegah kanker dengan risiko yang tidak berbahaya. Fitoestrogen paling banyak dapat dijumpai kacang-kacangan seperti kacang kedelai, kacang merah, dan kacang kapri (Mazur, 1998; Lee et al., 2005). Bedasarkan
penelitian Yang et al. (2012), ekstrak kacang kedelai yang tinggi akan isoflavon dapat
meningkatkan massa tulang, serta fitoestrogenseperti genistein, daidzein, dan coumestrol dapat mencegah osteoporosis dengan menurunkan aktivitas osteoklas atau penghancuran tulang dengan cara menghambat pembentukan RANKL, di mana coumestrol memiliki efektivitas pencegahan paling tinggi diantara fitoestrogen lain (Kanno et al., 2004).
Selain fitoestrogen terdapat senyawa lain yang memiliki aktivitas estrogenik yaitu saponin. Saponin adalah jenis glikosida yang banyak terdapat ditanaman. Bedasarkan kerangka aglikon saponin dibagi menjadi 2 kelompok, saponin steroid dan triterpenoid (Sparg et al.,2004). Tanaman ginseng (panax notoginseng) atau Tienchi/San-chi dalam
bahasa mandarin memiliki kandungan saponin triterpenoid yang tinggi. Menurut Li et al.
(2011), senyawa saponin dalam panax notoginseng seperti notoginsenoside R1,
ginsenoside Rg1, ginsenoside Re, ginsenoside Rb1, dan ginsenoside Rd dapat meningkatkan massa tulang, serta peneliti lain juga menyatakan hal yang serupa bahwa saponin dari ekstrak ginseng dapat mencegah osteoporosis dengan mengurangi proses resorpsi (penghancuran tulang) oleh osteoklasyaitu, dengan cara meningkatkan OPG dan mengurangi RANKL, sehingga membuat RANKL terikat pada OPG dan mengurangi terjadinya ikatan antara RANKL dengan receptor activator of nuclear factor kappa-B
(RANK) yang mengaktifkan pembentukan osteoklas (Chen et al., 2012; Schilling et al.,
2013).
Estrogen Reseptor (ER)
Estrogen memiliki peran penting dalam pengembangan dan fungsi fisiologis normal dari berbagai sistem jaringan tubuh termasuk tulang baik pada wanita ataupun pria (Khosla et al. 2012). Efek biologis estrogen pada jaringan tertentu seperti tulang
dimediasi melalui interaksi dengan reseptor inti, yang merupakan anggota dari superfamili ligand activated transciption factors. Menurut Cui et al. (2013), terdapat 2
jenis ER yang berperan pada organ manusia yaitu, ER-α (NR3A1) dan ER-β (NR3A2),
keduanya merupakan hormon steroid yang termasuk dalam anggota reseptor inti subfamili 3 (Gibson & Philippa, 2012). Estrogen yang dimediasi oleh ER memiliki 2 sifat yaitu agonis dan antagonis, di mana setiap ER juga memiliki jaringan target yang berbeda-beda. Menurut Ascenzi et al. (2006); Cui et al. (2013); Hertrampf et al. (2007);
Nelson et al. (2013); Timm & Craig (2004), ER-α adalah ER yang bertanggung jawab
terhadap jaringan tulang dengan memberikan efek positif. Imai et al. (2010), menyatakan
Gambar 4: Reseptor estrogen-α (1SJ0)
Sumber: (PDB, 2013) Penambatan Molekuler secara In Silico
Penambatan molekuler atau molecular docking adalah prosedur komputasional
yang digunakan untuk memprediksi ikatan non-kovalen makromolekul seperti ikatan hidrogen atau interaksi hidrofobik antara sebuah molekul besar (reseptor) dan sebuah molekul kecil (ligan). Penambatan molekuler bertujuan untuk memahami dan memprediksi rekognisi molekuler untuk dihasilkanya kecocokan geometris (menemukan mode ikatan yang paling mungkin) dan kecocokan energi (memprediksi energi ikatan) (Yanuar, 2012). Teknik komputasi yang digunakan dalam penambatan molekuler adalah penapisan virtual. Penapisan ini bekerja dengan menapis struktur 3 dimensi semua kemungkinan yang terjadi antara ligan dengan reseptor secara cepat dan praktis dengan memperhatikan nilai ΔG dan jenis interaksi yang terjadi. Penapisan virtual dalam penambatan molekuler disebut dengan teknik in silico, teknik ini dapat menvisualisasi
interaksi yang terjadi antara ligan dengan reseptor dalam penggambaran komputer, sehingga nantinya simulasi komputer ini dapat menggambarkan sistem secara keseluruhan. In silico umumnya diterapkan dalam bidang kimia untuk menemukan
komponen yang baru, menguraikan mekanisme dari ikatan protein dan ligan, memprediksi interaksi antara molekul, dan mempelajari hubungan aktivitas struktur (Cozzini & Luca, 2012).
Aturan Lipinski(The rule of five)
Rule of Five (ROF) adalah aturan untuk obat oral agar dapat larut dan terserap ke
dalam tubuh. ROF dikemukakan oleh Christoper A. Lipinski dan rekan-rekanya saat menganalisis sifat fisiko-kimia lebih dari 2000 obat dan kandidat obat dalam uji klinis. Analisis menyimpulkan bahwa senyawa dalam obat cenderung bersifat membran permeabel (berdifusi pasif) dan mudah diserap oleh tubuh jika memenuhi kriteria seperti (a) berat dari bobot molekuler kurang dari 500 gram/mol (b) koefisien partisi antara air dan 1-oktanol atau Log P kurang dari 5 (c) donor ikatan hidrogen jumlahnya tidak lebih dari 5 (d) akseptor ikatan hidrogen jumlahnya tidak lebih dari 10 (Lipinski et al., 1997;
Lipinski et al., 2012), sehingga bila ligan yang diuji coba dalam penelitian ini mampu
melewati aturan ini maka, diduga kuat senyawa yang mengandung ligan tersebut dapat terserap dengan baik pada tubuh, tetapi penelitian Bickton et al. (2012), menyatakan
3
METODE
Bahan
Bahan-bahan yang digunakan dalam penapisan virtual secara in silico ini antara
lain makromolekul ER-α yang dapat diunduh di (PDB, 2013) dengan kode 1SJ0
(Lampiran 1), 2 kontrol positif (KP) (17-b estradiol dan dienestrol) dan 89 ligan. Struktur tiga dimensi KP dan basis data ligan yang dapat diunduh di Pub Chem Project (PubChem,
2013) (Lampiran 2). Sampel ligan terdiri dari 32 senyawa fenolik, 40 senyawa alkaloid, dan 17 senyawa saponin. Kelompok ligan fenolik dibagi menjadi 12 sub kelas: (1) asam hidroksi sinamat: asam kafeat, asam klorogenat, dan asam ferulat (2) Lignan: sesamin, secoisolariciresinol, pinoresinol, syringaresinol, lariciresinol, dan matairesinol (3) Flavonol: kaempferol, quersetin, dan mirisetin (4) Flavon: apigenin, baicalein, dan luteolin (5) Flavanon : naringenin, naringin, dan hesperitin (6) Flavanol: katekin dan galokatekin (7) Anthocyanidin: pelargonidin, cyanidin, dan malvidin (8) Proanthocyanidins: prodelphinidin dan proanthocyanidin (9) Coumestan : coumestrol (10) Stilbene : resveratrol (11) Isoflavone : daidzein, genistein, dan glycitein (12) Monoterpen fenolik: carvacrol dan thymol. Kelompok ligan alkaloid dibagi menjadi 2 sub kelas: (1) Alkaloid non-heterosiklik: jurubine, taxol, capsaicin, colchine, dopamine, dan ephedrine (2) Alkaloid heterosiklik: emetine dan dehatrine (Isoquinoline); reserpine, vincristine, dan harmaline (Indole); solanidine dan solanine (Steroidal); echimidine dan senecionine (Pyrrolizidine); irniine, broussonetine c, dan hygrine (Pyrrole dan Pyrrolidine); sparteine, 1,3-hydroxylupanine, cytisine, dan norlupinane (Quinolizidine); cinchonine dan quinine (Quinoline); aconine dan aconitine (Terpenoid); cocaine, atropine, dan scopolamine (Tropane); elemicin dan boldine (Aporphine); piperine, nicotine, dan arecoline (Pyridine dan Piperidine); isopilocarpine dan pilocarpine (Imidazole); castanospermine dan swainsonine (Indolizidine); theobromine dan caffeine (Purine). Kelompok ligan saponin dibagi menjadi 2 sub kelas: (1) Saponin triterpenoidal: cucurbitacin_E, saikosaponin_A, asam glycyrrhetinic, dan asam glycyrrhizic (2) Saponin steroidal: protopanaxadiol, astragaloside_III, sarsasapogenin, ruscogenin, diosgenin, protopanaxatriol, cimicifugoside, ginsenoside_Rg1, ginsenoside_Rh2, ginsenoside_Rb1, ginsenoside_Rd, ginsenoside_Re, dan notoginsenoside_R1.
Alat
Alat-alat yang digunakan berupa perangkat keras dan perangkat lunak. Perangkat keras terdiri atas komputer dengan spesifikasi RAM (Random Access Memory) 8 gigabyte, Quad Core Processor (Intel® CoreTM, Amerika), Graphic Card NVIDIA Ge
Force GTX 660M (Amerika), dan sistem operasi Microsoft Windows 7 Professional 64-bit (Microsoft, Amerika). Kelengkapan computer yakni monitor (LG, Korea selatan), CPU (Central Processing Unit) Asus(Amerika), mouse (Logitech, China) dan keyboard
(Logitech, China).Komputer terhubung dengan koneksi internet dan UPS (Uninterupted Power Supply), CPU dengan spesifikasi RAM 32 gigabyte, Graphic Card NVIDIA Ge
Force GTX 680 dual eight Core Xeon E5620 processor (Intel® CoreTM, Amerika).
Perangkat lunak terdiri atas Open Babel-2.3.1, Autodock 4.2 berbantu PyRx 0.8 (The Scripps Research Institute, Amerika) untuk mencari nilai ΔG sekaligus member
(DeLano Scientific LLC, Italia), dan Ligplot+ 1.4.4 (©Roman Lawkowski 2009) untuk
mengobservasi interaksi dengan cara visualisasi baik dua atau tiga dimensi interaksi ligan dengan ER-α.
Tempat dan Waktu Penelitian
Laboratorium Komputasi Biomedik dan Rancangan Obat, Fakultas Farmasi, Universitas Indonesia, Depok. Penelitian dilakukan dalam 6 bulan mulai bulan Desember 2013 hingga Mei 2014.
Prosedur Penelitian
Penelitian ini dilakukan berdasarkan studi literatur, simulasi, dan penapisan virtual dengan tahapan-tahapannya menurut Yanuar (2012):
a. Preparasi struktur makromolekul ER-α
Struktur makromolekul diunduh (kode PDB: 1SJ0) (PDB, 2013)
dalam format *.pdb lalu diubah ke dalam format *.pdbqt melalui program AutoDock 4.2 berbantu PyRx 0.8 (Lampiran 3).
b. Validasi metode penapisan virtual in silico.
Tahap ini dilakukan untuk memastikan paremeter dan ukuran area penambatan pada
ER-α yang akan dilakukan untuk tahap selanjutnya. Validasi metode penapisan virtual dilakukan dengan menambatkan ER-α dengan KP yang disebut ligand dan kontrol negatif
(decoy) yang diunduh dari (DUDE, 2013) (Lampiran 4). Pengunduhan dari DUDE akan
menghasilkan dua berkas yang berisi ligand dengan 627 struktur dan decoy dengan
20.818 struktur dengan format *.sdf, untuk memecah struktur yang berada dalam satu berkas diperlukan akses melalui PuTTY dengan perintah:
Csplit file.sdf -f new file ‘/ZINC/’ ‘{*}’
find -type f -exec mv ‘{}’ ‘{}’.(sdf) \;
Setelah terbentuk sejumlah 627 berkas struktur ligand dan 20.818 berkas struktur decoy
dengan format *.sdf. Selanjutnya, diubah formatnya menjadi format *.pdbqt menggunakan Open Babel (Lampiran 5). Kemudian seluruh berkas dengan format *.pdbqt dilakukan penapisan virtual menggunakan program PyRx 0.8 dengan parameter penambatan diset 10 GA, 250.000 perhitungan, 27.000 generasi 150 populasi dan koordinat penambatan (grid center) yang berasal dari co-kristal 1SJ0 yaitu, x = 30.8850;
y = -1,0670; dan z = 23,4640. Validasi dilakuan dengan 3 variasi ukuran penambatan (grid box) seperti x, y, z (40, 40, 40; 50, 50, 50; dan 60, 60, 60). Hasil dari validasi akan
ditabulasikan dan dianalisis menggunakan Enrichment Factor 1% dari peringkat
pangkalan data (EF1) dan Area Under the Curve (AUC). Nilai EF1 dan AUC terbesar akan
digunakan untuk tahap selanjutnya.
Perhitungan EF1 dan AUC dilakukan dengan cara:
EF1= L a t r l / N1
t tal L a / t tal N (Huang et al., 2006)
Sebagai contoh, protein tertentu dengan 150 ligand (total Ligand) di dalam pangkalan
data 95,000 senyawa (total N), 950 senyawa (N1), jumlah ligand yang terpilih di dalam
AUC didapat dari plot kurva Receiver Operator Characteristic (ROC) oleh sensitivitas
Kurva ROC diplot dengan sumbu x adalah Sp (% decoy terpilih) terhadap sumbu y yaitu, Se (% ligand terpilih). AUC adalah nilai dari Se ketika nilai Sp setengah dari totalnya.
(Triballeau et al., 2005)
c. Preparasi basis data ligan (KP dan sampel).
Sampel yang diuji dan KP didapat dari PubChem (PubChem, 2013) dalam format *.sdf lalu diubah ke dalam format *.pdb menggunakan Open Babel. Selanjutnya dilakukan tahap minimisasi untuk fleksibilitas ligan pada tahap penambatan yang melalui 3 langkah antara lain persiapan ligan, topologi dan koordinat, dan minimisasi ligan.
- Persiapan Ligan
Persiapan ligan dilakukan dengan mengubah berkas 2 dimensi menjadi 3 dimensi, mengubah format *.pdb ke dalam format *.mol2, dan penambahan atom hidrogen. Persiapan ligan dilakukan dengan menggunakan program Open Babel, melalui perintah:
babel -i pdb -fi file.pdb -o mol2 –fo file.mol2 -h
- Topologi dan Koordinat
Pembuatan topologi dan koordinat dilakukan dengan cara, berkas ligan dengan format *.pdb dan *.mol2 diletakan dalam satu folder, selanjutnya struktur dari ligan harus diberikan muatan AM1-BCC menggunakan piranti lunak Antechamber yang diakses melalui PuTTY dengan perintah:
Antechamber -i file.mol2 -fi mol2 -o file mol2. -fo mol2 -c bcc -s 2 &.
Berkas keluaran mol2 hasil antechamber harus dibuat berkas dengan format *. Frcmod (merupakan berkas parameter yang akan dibaca pada tleap) dengan perintah:
Parmchk -i file.mol2 -f mol2 -o file.frcmod.
Berkas yang telah siap dilakukan akan dilakukan permbuatan topologi dan koordinat dengan piranti lunak tLeap dengan perintah:
Tleap -f leaprc.ff99SB
(ff99SB merupakan force field untuk asam amino)
Program LEAP diawali dengan tampilan ”>”
- Minimisasi Ligan
Selain Berkas topologi (prmtop) dan koordinat (inpcrd), tahap minimsasi juga diperlukan berkas min.in (Lampiran 7). Proses minimisasi ini dilakukan dengan piranti lunak sander yang dapat diakses dengan PuTTY dengan perintah:
Sander -O -i min.in -o file_min.out -p file.prmtop –c file.inpcrd -r
file_min.crd &
Perintah -p ditunjukan untuk input file topologi kompleks ligan-makromolekul dalam pelarut air, -c ditunjukan untuk input file koordinat ligan, -o ditunjukan untuk output file yang berisi hasil perhitungan minimisasi ligan, -r ditunjukan untuk output restart file hasil minimisasi. Berkas hasil dari minimisasi dapat dibentuk menjadi format *.pdb kembali dengan perintah:
ambpdb –p file.prmtop < file_min.crd > new file_min.pdb
Selanjutnya pada tahap akhir ligan dengan format *.pdb diubah ke dalam format *.pdbqt dengan menggunakan program AutoDock 4.2 (Lampiran 6). Tahap minimisasi ini penting dilakukan karena untuk menghitung secara rinci energi yang berada pada ligan tersebut, sehingga diharapkan tahap minimisasi akan menghasilkan nilai energi ikatan atau energi Gibs (ΔG) yang akurat dan presisi.
d. Penapisan virtual senyawa fenolik, alkaloid, dan saponin
Penapisan virtual dilakukan dengan program Autodock berbantu PyRx. Ligan akan ditambatkan pada posisi grid center x = 30.8850; y = -1,0670; dan z = 23,4640 dengan
ukuran grid box terbaik 60 x 60 x 60 dan spacing 0,375Å per unit, serta parameter
penambatan ligan dengan ER-α diset 100 GA, 25.000.000 perhitungan, 27.000 generasi, dan 150 populasi. Hasil dari penapisan virtual ini akan menghasilkan nilai ΔG dari masing-masing ligan yang diujikan. Perhitungan ligan dari 100 GA yang memiliki ΔG terendah akan dilanjutkan ke tahap selanjutnya yaitu, visualisasi penambatan.
e. Visualisasi penambatan
4
HASIL DAN PEMBAHASAN
Preparasi Struktur Makromolekul
Kriteria makromolekul ER-α 1SJ0 dipilih bedasarkan tervalidasi oleh situs PDB, DUDE, sebagai reseptor non-mutan, dan memiliki resolusi di bawah 2Å. PDB merupakan kumpulan arsip tunggal mengenai data struktural makromolekul biologi dari seluruh dunia yang telah dideterminasi menggunakan teknik kristalografi X-ray, NMR, dan mikroskop elektron. Sedangkan DUDE adalah situs yang menyediakan kumpulan KP (ligand) dan kontrol negatif (decoy) yang bermanfaat dalam ponolokukuran pada proses
penapisan virtual (Yanuar, 2012). Reseptor yang bersifat non-mutan atau wild type
diperlukan untuk penambatan molekuler karena, ER mutan tidak akan berikatan dengan estradiol yang merupakan kontrol positifnya, serta menurut Cross et al. (2009), resolusi
makromolekul di bawah 2 Å akan memberikan hasil penambatan yang lebih presisi dan akurat. Hal ini menandakan bahwa ER 1SJ0 telah banyak digunakan sebagai ER-α pada penelitian sebelumnya (berada dalam pangkalan data PDB dan DUDE) dan dapat menggambarkan hasil sebuah interaksi reseptor dan ligan dengan baik (bersifat non-mutan dan resolusi di bawah 2 Å).
Validasi Metode Penapisan Virtual in silico
Validasi bertujuan memastikan parameter dan ukuran area penambatan ligan pada ER-α untuk tahap selanjutnya. Validasi dilakukan dengan menggunakan ligand dan decoy
dari DUDE, untuk hasil dari validasi penambatan ligand dan decoy yang telah
ditabulasikan dalam EF1 dan AUC dapat dilihat pada Tabel 1.
Tabel 1. Hasil validasi nilai EF1 dan AUC
Grid box EF1 AUC
40x40x40 17.54 0.776
50x50x50 19.30 0.768
60x60x60 19.30 0.770
Standar (DUDE) 15.4 0.675
Nilai EF1 & AUC mencerminkan kemampuan Penambatandalam membedakan ligand asli di dalam banyak senyawa pengecoh atau decoy. Semakin tinggi nilai EF1 dan
AUC maka, semakin baik performa yang dihasilkan penapisan virtual (Huang et al.,
2006). Nilai AUC yang baik adalah yang mendekati 1 (Triballeau et al., 2005). Parameter
yang digunakan dengan 3 ukuran grid box berbeda menghasilkan nilai EF1 dan AUC yang
lebih tinggi dari standar dengan ukuran grid box terbaik adalah 60 x 60 x 60. Hal tersebut
menandakan bahwa parameter yang digunakan dengan grid box 60 x 60 x 60 dapat
membedakan ligand dan decoy dengan baik, lebih akurat dan presisi dibandingkan
menggunakan grid box 50 x 50 x 50 dan 40 x 40 x 40.
Penapisan Virtual dan Visualisasi Penambatan Senyawa Fenolik
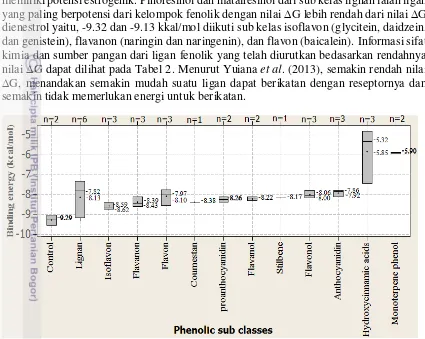
adalah -9.54 dan -9.03 kkal/mol, sementara nilai ∆G dari kelompok fenolik berkisar antara -9.3 — -4.8 kkal/mol (Gambar 5). Ligan fenolik yang memiliki nilai ∆G lebih rendah atau mendekati KP menandakan ligan tersebut dapat berinteraksi spontan dengan ER-α tanpa memerlukan energi ikatan yang besar, sehingga ligan tersebut diduga memiliki potensi estrogenik. Pinoresinol dan matairesinol dari sub kelas lignan ialah ligan yang paling berpotensi dari kelompok fenolik dengan nilai ∆G lebih rendah dari nilai ∆G dienestrol yaitu, -9.32 dan -9.13 kkal/mol diikuti sub kelas isoflavon (glycitein, daidzein, dan genistein), flavanon (naringin dan naringenin), dan flavon (baicalein). Informasi sifat kimia dan sumber pangan dari ligan fenolik yang telah diurutkan bedasarkan rendahnya nilai ∆G dapat dilihat pada Tabel 2. Menurut Yuiana et al. (2013), semakin rendah nilai
∆G, menandakan semakin mudah suatu ligan dapat berikatan dengan reseptornya dan semakin tidak memerlukan energi untuk berikatan.
Gambar 5. Boxplot ∆G dengan sub kelas fenolik
Sub kelas isoflavon, coumestrol, stilbene, dan flavonol memiliki nilai ∆G lebih tinggi dibandingkan KP (-8.74 — -7.79 kkal/mol), namun sebaliknya penelitian Kanno et al. (2004), melaporkan bahwa isoflavonoid dan coumestrol memiliki efek dalam
menghambat pembentukan osteoklas. Penghambatan terjadi dengan menurunkan RANKL yang berinteraksi dengan RANK dalam mengaktifkan pembentukan osteoklas. Selain itu, 30–300 µM kaempferol dari sub kelas flavonol pada calvarial pre-osteoblasts
tikus mendorong pembentukan tulang tergantung dari dosis, bahkan dosis terrendah dari kaempferol memiliki performa lebih baik dari 10 µM estradiol (Guo et al., 2012).
Kemudian, penelitian in vivo pada manusia menyatakan bahwa konsumsi isoflavonoid
sebesar 35mg/hari selama 6 bulan dapat meningkatkan low-density lipoprotein dan total
kolesterol (penigkatan sebesar 4.50% [p < 0.01] dan 4.67% [p < 0.05]) (Yang et al., 2012).
Selanjutnya konsumsi isoflavonoid di atas 17.3 mg/hari selama 2 tahun dapat menurunkan angka kematian dari kanker payudara sebesar 38-36% (Zhang et al., 2012).
Serta, konsumsi isoflavonoid sebesar 107 mg/hari selama 6 bulan dapat menurunkan anti-apoptosis penyebab kanker dan menurunkan insiden kanker prostat (Hamilton-Reeves et al., 2008). Hal ini menandakan bahwa fitoestrogen dianggap aman sebagai pengganti
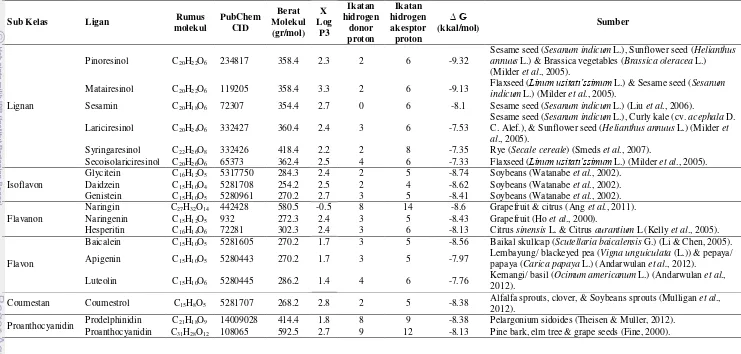
Tabel 2. Sifat kimia dan sumber pangan pada kelompok fenolik
Sesame seed (Sesanum indicum L.), Sunflower seed (Helianthus annuus L.) & Brassica vegetables (Brassica oleracea L.) (Milder et al., 2005).
Matairesinol C20H22O6 119205 358.4 3.3 2 6 -9.13 Flaxseed (indicum L.) (Milder et al., 2005). Linum usitatı´ssimum L.) & Sesame seed (Sesanum
Sesamin C20H18O6 72307 354.4 2.7 0 6 -8.1 Sesame seed (Sesanum indicum L.) (Liu et al., 2006).
Lariciresinol C20H24O6 332427 360.4 2.4 3 6 -7.53
Sesame seed (Sesanum indicum L.), Curly kale (cv. acephala D. C. Alef.), & Sunflower seed (Helianthus annuus L.) (Milder et al., 2005).
Proanthocyanidin Prodelphinidin C21H18O9 14009028 414.4 1.8 8 9 -8.38 Pelargonium sidoides (Theisen & Muller, 2012).
Tabel 2. Sifat kimia dan sumber pangan pada kelompok fenolik lanjutan
Jambu mete/ cashew (Anacardium occidentale L.) & kelor/ horseradish tree (Moringa pterygosperma G.) (Andarwulan et al., 2010 & 2012).
Kaempferol C15H10O6 5280863 286.2 1.9 4 6 -8.06
Kaempferia galanga L., Katuk/ chekkurmanis (Sauropus androgynus (L.) Merr.) & kedongdong cina/ balfour aralia (Polyscias pinnata) (Andarwulan et al., 2010 & 2012; Guo et al., 2012).
Miricetin C15H10O8 5281672 318.2 1.2 6 8 -7.79
Labu siam/chayote (Sechium edule (Jacq.) Swartz) & jambu mete/ cashew (Anacardium occidentale L.) (Andarwulan et al., 2012).
Kedongdong cina/ balfour aralia (Polyscias pinnata) & takokak/ turkey berry (Solanum torvum S.) (Andarwulan et al., 2012).
Caffeic acid C9H8O4 689043 180.2 1.2 3 4 -5.32 Beluntas/ Indian camphorweed (Pluchea indica) & kenikir/ wild cosmos (Cosmos caudatus) (Andarwulan et al., 2012).
Ferulic acid C10H10O4 445858 194.2 1.5 2 4 -4.8
Kedongdong cina/ balfour aralia (Polyscias pinnata) & kelor/ horseradish tree (Moringa pterygosperma G.) (Andarwulan et al., 2012).
Monoterpenephenol Thymol C10H14O 6989 150.2 3.3 1 1 -5.93
Herba timi (Thymus vulgaris), thyme, marjoram, & Oregano (Origanum vulgare) (Al-Bandak & Oreopoulou, 2007; Bhandari & kabra, 2014).
Visualisasi penambatan bertujuan untuk mengetahui mekanisme yang terjadi antara reseptor dengan ligan. Bedasarkan Hernandez & Appu (2006), ikatan hidrogen memiliki energi lebih tinggi dibandingkan interaksi hidrofobik dengan nilai 1-7 kkal/mol banding 1 kkal/mol, namun kedua interaksi tersebut sangat diperhitungkan untuk mengkalkulasi nilai ∆G. Bedasarkan hasil visualisasi, hampir seluruh ligan sampel yang ditambatkan memiliki jenis ikatan hidrogen dan interaksi hidrofobik dengan jumlah dan variasi residu asam amino berbeda-beda. Variasi residu asam amino dominan dari ER-α
yang berikatan hidrogen dengan ligan uji dapat di lihat pada Tabel 3 dan visualasi posisi pada Gambar 6.
Bedasarkan standar PDB, residu asam amino dominan yang berperan pada ikatan hidrogen antara ER-α dengan ligan antara lain ASP 351, GLU 353, LEU 387, ARG 394, GLY 521, dan HIS 524. Angka di belakang asam amino merupakan urutan dari asam amino yang menyusun ER-α, serta ikatan hidrogen yang terjadi umumnya berikatan dengan gugus hidroksil (OH) dan nitrogen (N) pada ligan. Pada Tabel 3, antara ketiga kelompok yang diuji terlihat bahwa residu asam amino dominan pada kelompok fenolik adalah yang paling mirip dengan KP, diikuti kelompok alkaloid dan saponin. Bedasarkan hasil visualisasi penambatan fenolik, nilai ∆G diperoleh dari kontribusi energi ikatan hidrogen dan interaksi hidrofobik. Selain itu bila hasil residu asam amino dominan diposisikan dan dipetakan bedasarkan urutannya maka, residu dapat terbagi menjadi 3 posisi: (1). ASP 351 (2). GLU 353, LEU 387, dan ARG 394 (3). MET 421, GLY 521, dan HIS 524.
Tabel 3. Residu asam amino dominan dari ER-α yang berikatan hidrogen
Sumber Residu ER-α
*Keterangan: Posisi 1, 2, 3 didapat bedasarkan urutan dan posisi dari residu ER-α dominan yang berikatan hidrogen
Gambar 6. Visualisasi posisi dari residu asam amino dominan dari ER-α yang berikatan hidrogen (a) Fenolik, (b) Alkaloid, & (c) Saponin
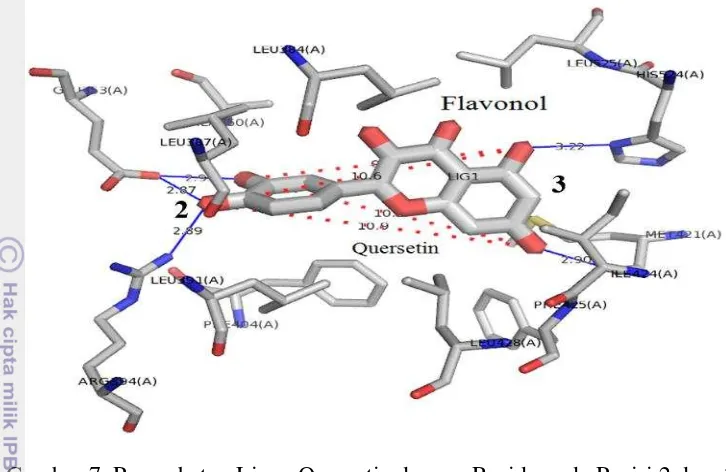
Gambar 7. Penambatan Ligan Quersetin dengan Residu pada Posisi 2 dan 3
Pengujian korelasi digunakan untuk melihat seberapa besar hubungan ∆ G dengan
ke-3 faktor tersebut. Korelasi yang baik adalah yang mendekati -1 atau 1. Bedasarkan
hasil korelasi, ∆ G memiliki hubungan yang cukup erat dengan jarak antara gugus OH pada ligan dan jumlah interaksi hidrofobik (-0.59 dan -0.66). Hal ini menandakan, semakin jauh jarak OH (mendekati 11.65 Å) dan banyak interaksi hidrofobik maka, ∆ G
akan semakin rendah. Sedangkan regresi digunakan untuk memberikan informasi faktor
yang paling berpengaruh. Bedasarkan hasil regresi, ∆ G sangat di pengaruhi oleh jarak
gugus OH (1.48) di bandingkan jumlah interaksi hidrofobik (0.526).
Penapisan Virtual dan Visualisasi Penambatan Senyawa Alkaloid
Penambatan kelompok alkaloid menghasilkan nilai ∆G paling rendah (-11.03 — -4.88 kkal/mol) dibandingkan dengan penambatan kelompok fenolik dan saponin, untuk hasil penambatan ligan alkaloid dapat dilihat pada Gambar 8. 2 ligan non-heterosiklik jurubine dan taxol, dan 2 ligan heterosiklik emetine (sub kelas isoquinoline) dan reserpine (sub kelas indole) ialah ligan yang paling berpotensi dari kelompok alkaloid dengan nilai ∆G lebih rendah dari dienestrol yaitu, -11.03 — -9.25 kkal/mol diikuti kelompok heterosiklik lainnya seperti sub kelas steroids, pyrrolizidine, quinolizidine, quinoline, terpenoid, dan
tropane yang memiliki nilai ∆G lebih tinggi antara -8.94 — -8.06 kkal/mol (Gambar 8). Informasi sifat kimia dan sumber pangan ligan alkaloid yang telah diurutkan bedasarkan rendahnya nilai ∆G dapat dilihat pada Tabel 4.
Salah satu ligan alkaloid, harmine dengan dosis 10 mg/Kg/hari telah dilaporkan dapat menghambat pembentukan osteoklas (osteoclastogenesis) dengan menekan
pembentukan RANKL yang menurunkan ekspresi dari c-Fos dan NFATc1 pada sel RAW264.7 dan tikus ovariectomized (Yonezawa2 et al. 2011). Pada penelitian ini
harmine memiliki nilai ∆G yang lebih tinggi dibandingkan dengan ligan alkaloid yang
telah disebutkan di atas (-7.46 kkal/mol). Hasil ini menarik sebab jurubine, taxol,
emetine, reserpine atau ligan lainnya yang memiliki nilai ∆G lebih rendah belum dikenal
Gambar 8. Boxplot ∆G dengan sub kelas alkaloid
Bedasarkan visualisasi penmbatan alkaloid, nilai ΔG juga diperoleh dari kombinasi energi ikatan hidrogen dan interaksi hidrofobik. Selain itu, residu dominan yang berikatan hidrogen dengan ligan alkaloid memiliki kesamaan dengan residu dominan dari fenolik dan KP (pada posisi 1 dan 2) (Tabel 3 dan Gambar 6). Hal tersebut mungkin terjadi karena ligan alkaloid memiliki kesamaan letak gugus OH atau N dan ukuran ligan, namun kesamaan tersebut tidak sepenuhnya menyerupai ligan KP maka, ligan alkaloid berinteraksi dengan pose yang berbeda yaitu, ligan hanya berikatan hidrogen pada 1 sisinya saja. Sebagai contoh dapat dilihat pada Gambar 9, terlihat ligan taxol dan iriine yang hanya berikatan hidrogen pada posisi 1 saja (ASP 351).
Penapisan Virtual dan Visualisasi Penambatan Senyawa Saponin
Penamabatan ligan kelompok saponin menghasilkan nilai ∆G sebesar -9,44 — -5,25 kkal/mol dengan ligan dari sub kelas triterpenoidal memiliki nilai ∆G lebih rendah (Gambar 10). Ligan yang paling berpotensi dari kelompok alkaloid antara lain cucurbitacin E (saponin triterpenoidal), protopanaxadiol, astragaloside III, dan sarsasapogenin (saponin steroidal) dengan nilai ∆G lebih rendah dari dienestrol yaitu, -9.44 — -9.09 kkal/mol diikuti ligan lain dengan nilai lebih tinggi seperti ruscogenin, diosgenin, protopanaxatriol, saikosaponin, cimicifugoside, dan ginsenoside (-8.91 — -5.25 kkal/mol) sehingga ligan tersebut terlihat kurang berpotensi (Tabel 5).
Meskipun dalam penelitian ini ligan ginsenoside bukan termasuk ligan berpotensi, ligan tersebut telah teruji secara in vitro dan in vivo untuk mencegah osteoporosis dengan
menekan pembentukan RANKL sehingga menurunkan aktivitas dari osteoklas dan meningkatkan pembentukan tulang (Cheng et al., 2012; Gong et al., 2006; He et al., 2012;
Kim1et al., 2011; Kim2et al., 2011; Liu et al., 2009; Siddiqi et al., 2013). Hal ini menarik
untuk dilanjutkan ke tahap berikutnya in vitro atau in vivo untuk mengkonfirmasi
kemungkinan anti-osteoporosis dari ligan saponin yang disebutkan selain ginsenoside.
Gambar 10. Boxplot ∆G dengan sub kelas saponin
Tabel 4. Sifat kimia dan sumber pangan pada kelompok Alkaloid
Taxol C47H51NO14 36314 853.91 2.5 4 14 -10.06 Tabebuia pentaphylla Hemsl and Pacific Yew tree (Taxus brevifolia) (Kathiravan & Vithiyanathan, 2010; Vennila & Muthumary, 2011).
Capsaicin C18H27NO3 1548943 305.41 3.6 2 3 -8.21 Capsicum annuum, C. chinenseand C. frutescens (O'Neill et al. 2012).
Harmaline C13H14N2O 5280951 214.26 1.2 1 3 -7.46 Syrian Rue (Peganum harmala) and Passionflower (Passiflora incarnata) (Allen & Holmstedt, 1980).
Steroidal Solanidine C27H43NO 65727 397.64 6.1 1 2 -8.94 Potato (Solanum tuberosum) & Dioscorea (Minorics et al. 2011).
Cytisine C11H14N2O 10235 190.24 0.2 1 2 -7.03 Lupinus albus, Anagyris foetida L., & Baptisia spp (Przyby & Kubicki, 2011; European Food Safety Authority, 2012).
Tabel 4. Sifat kimia dan sumber pangan pada kelompok Alkaloid lanjutan
Quinine C20H24N2O2 8549 324.42 2.9 1 4 -8.36 Plasmodium falciparum, Plasmodium ovale, Plasmodium knowlesi, & Plasmodium malariae (Jones et al., 2015).
Terpenoid Aconitine C34H47NO11 245005 645.74 0.3 3 12 -8.36
Aconitum carmichaeli D., Aconitum Kusnezoffii R. & Aconitum japonicum (Yang et al., 2013).
Indolizidine Castanospermine C8H15NO4 54445 189.21 -2.2 4 5 -5.84 Castanospermum austral (Machan et al., 2008).
Swainsonine C8H15NO3 51683 173.21 -1.3 3 4 -5.65 Swainsona canescens & Astragalus strictus (Colegate et al., 1979 & Bao-yu et al., 2009).
Purine Theobromine Caffeine CC7H8N4O2 5429 180.16 1 3 0 -4.96 Cacao (Nunez & Macias, 2011).
Tabel 5. Sifat kimia dan sumber pangan pada kelompok Saponin
Water hyssop (Bacopa monnieri), Winter Squash (Cucurbita andreana), & Bitter cucumber (Citrullus colocynthis) (Jayaprakasam et al., 2003; Ayyad et al., 2012).
Saikosaponin_A C42H68O13 167928 780.98 2.5 8 13 -8.21 Bupleurum falcatum (Ashour & Wink, 2011).
Glycyrrhetinic_acid C30H46O4 10114 470.68 6.4 2 4 -7.02 akar manis/ Liquorice (Glycyrrhiza glabra) (Amani et al. 2005).
Glycyrrhizic_acid C42H62O16 128229 822.93 3.7 8 16 -6.45 akar manis/ Liquorice (Glycyrrhiza glabra) (Amani et al. 2005).
Steroidal
Cimicifugoside C37H54O11 128327 674.82 2.6 4 11 -8.09 Cimicifuga racemosa (black cohosh), Cimicifuga simplex (Yawata et al., 2009).
Ginsenoside_Rg1 C42H72O14 441923 801.01 2.7 10 14 -7.82 American ginseng (Panax quinquefolius L.), Panax notoginseng saponins (Li et al., 2011; Wang et al. 2006).
Ginsenoside_Rh2 C36H62O8 119307 622.87 5.6 6 8 -7.2 Ginseng (Panax quinquefolius) (He et al. 2012).
Ginsenoside_Rb1 C54H92O23 9898279 1109.29 0.3 15 23 -7.18 Panax notoginseng saponins (Li et al., 2011).
Ginsenoside_Rd C96H164O36 5458671 1894.31 -- 24 36 -6.48 Panax notoginseng saponins (Li et al., 2011).
Ginsenoside_Re C48H82O18 73149 947.15 1.6 12 18 -5.79 American ginseng (Panax quinquefolius L.), Panax notoginseng saponins (Li et al., 2011; Wang et al. 2006).
Bedasarkan Hernandez & Appu (2006), senyawa dengan ukuran yang besar seperti saponin memperoleh energi besar dari interaksi hidrofobik dan van der walls sehingga
senyawa tersebut sulit terikat dengan reseptor (Yuiana et al., 2013). Bila residu asam
amino dominan yang berikatan hidrogen diurutkan dan diposisikan maka terbentuk posisi yang berbeda dengan penambatan fenolik dan alkaloid (Gambar 6) seperti posisi 1 (ASP 351, THR 347, dan LYS 529) dan posisi 2 (VAL 533, VAL 534, dan LEU 536), tetapi jarak antara kedua posisi tersebut tidak memiliki akurasi yang baik (12.41 ± 1.96 Å). Sebagai contoh (Gambar 11) ligan protopanaxadiol dan cucurbitacin yang memiliki ikatan hidrogen pada posisi 1 dan 2 dengan jarak antara 8.2 ̶ 11.5 Å.
Gambar 11. Penambatan ligan saponin (protopanaxadiol dan cucurbitacin) Residu asam amino dominan yang terlibat dalam interaksi hidrofobik pada penambatan fenolik, alkaloid, dan saponin antara lain LEU 346, THR 347, ALA 350, TRP 383, LEU 387 dan LEU 525. Bedasarkan hasil visualisasi penambatan dari ketiga kelompok, residu asam amino dominan yang muncul untuk berikatan hidrogen antara
ER-α dan ligan dipengaruhi oleh ukuran dari ligan yang diuji. Ligan dengan ukuran kecil (BM < 500 gram/mol) akan melibatkan residu GLU 353, ARG 394, LEU 387, GLY 521, HIS 524, dan ASP 351 pada ikatan hidrogen antara ER-α dan ligan. Pada ligan dengan ukuran besar (BM > 500 gram/mol) kemungkinan terbentuk residu lain, tetapi perbedaan tersebut
tidaklah mempengaruhi nilai ∆G. Nilai ∆G yang dihasilkan tergantung dari jumlah ikatan hidrogen dan interaksi hidrofobik yang terlibat dan jarak dari ikatan hidrogen yang terjadi, semakin banyak interaksi dan semakin dekat jarak ikatan hidrogen yang terjadi pada penambatan molekular maka, semakin rendah nilai ∆G yang diperoleh dan sebaliknya.
Agar lebih memperjelas potensi senyawa (ligan) yang diuji pada ER-α maka, dilakukan klarifikasi ligan dengan kriteria kaidah lipinski (ROF). Menurut Lipinski et al.
(1997 & 2012), suatu senyawa dapat larut terserap ke dalam tubuh jika memenuhi minimal 2 kriteria Role of Five (ROF): (1) berat molekul (BM) < 500 gram/mol, (2) nilai
polar, semakin tinggi koefisien partisi oktanol/air maka senyawa bersifat semakin non polar; donor dan akseptor proton berperan dalam membentuk ikatan hidrogen interaksi antara makromolekul dengan ligannya. Hampir seluruh ligan yang diuji memenuhi syarat dari ROF kecuali, ligan naringin, proanthocyanidin, solanine, dan kelompok saponin. Seperti yang telah disebutkan di atas bahwa saponin memiliki struktur yang besar (BM 400-1800 gram / mol), untuk lebih jelas sifat kimia dan sumber pangan kelompok fenolik termasuk nilai ROF dan Δ G dapat dilihat pada Tabel 2, alkaloid pada Tabel 4, dan saponin pada Tabel 5.
Faktanya, berbagai senyawa tersebut memiliki nilai ∆G yang dekat dengan KP atau mudah berikatan dengan reseptor. Penelitian in vivo pada mencit oleh Choi & kang
(2008), menyatakan 1.5 – 15 mg/kg naringin memiliki absolute bioavailability
(32.8-47.1%) lebih tinggi dibandingkan tamoxifen 10 mg/kg (16.3%). Selanjutnya,
bioavailability dari anthocyanin telah diperhitungkan meski efeknya masih belum jelas,
serta faktor-faktor yang memberikan dampak penting pada bioavailabilitas masih perlu dieksplorisasi (Fernandes et al., 2014). Selain itu, senyawa saponin memiliki penyerapan
yang lambat dan bioavailbilitas yang rendah (Wang et al., 2015), terutama senyawa yang
memiliki BM yang besar. Menurut Ou et al. (2012), Senyawa dengan BM yang besar
memiliki lower aqueous dan penyerapan yang sangat rendah, namun menurut Bickerton et al. (2012), ROF tidak selalu menjadi acuan, karena tidak semua obat oral yang memiliki
5
KESIMPULAN DAN SARAN
Kesimpulan
Kesimpulan dari penelitian ini adalah banyak senyawa dari kelompok fenolik, alkaloid, dan saponin telah ditapis sebagai ligan yang berpotensi untuk ER-α dengan
menggunakan teknik in silico. Bedasarkan nilai ΔG, kebanyakan dari ligan terlihat
menjanjikan untuk dikembangkan lebih lanjut sebagai fitoestrogen. Setiap kelompok yang diuji memiliki ligan yang berpotensi antara lain pinoresinol dan matairesinol dari kelompok fenolik, jurubine, taxol, emetine dan reserpine dari kelompok alkaloid, dan cucurbitacin E, protopanaxadiol, astragaloside III, dan sarsasapogenin dari kelompok saponin. Hasil dari visualisasi penambatan menunjukan bahwa ikatan hidrogen dan interaksi hidrofobik terlibat dalam interaksi ER-α dengan ligan. Pada kasus fenolik, residu dominan dari ikatan hidrogen selalu terjadi pada gugus OH dengan sisi yang berlawanan, yaitu posisi 2: GLU 353, LEU 387, ARG 394 dengan posisi 3: MET 421, GLY 521, HIS 524, bila jarak gugus OH mencapai jarak 10.78±0.65 Å maka, kemugkinan besar ligan fenolik tersebut berpotensi esterogenik. Senyawa yang telah dilaporkan dengan potensi estrogenik banyak dan mudah ditemukan pada tanaman yang umum dikonsumsi sehari-hari seperti biji wijen, kacang kedelai, ginseng, dan pare. Meskipun hasil dari teknik in silico masih merupakan hasil tahapan awal, tetapi mungkin bila senyawa-senyawa
tersebut dikonsumsi maka, osteoporosis dapat dicegah.
Saran
Diperlukan investigasi lebih lanjut mengenai faktor-faktor yang berkontribusi terhadap nilai ∆G. Serta, penelitian secara in vitro atau in vivo untuk memastikan hasil
DAFTAR PUSTAKA
Al-Bandak G, Oreopoulou V. 2007. Antioxidant properties and composition of Majorana syriaca extracts. Eur. J. Lipid Sci. Technol. 109:247-255.
Allen JRF, BR Holmstedt. 1980. The simple b-carboline alkaloids. Phytochemistry. 19:
1573-1582.
Amani M, Mostoufi RSGN, Kashani HAM. 2005. Optimal extraction of glycyrrhetinic acid from licorice root. Journal of Food Technology. 3(4):576-580.
Andarwulan N, Dewi K, Riza AA, Hardianzah R, Anna VR, Bradley WB. 2012. Polypenols, Carotenoids, and Ascorbic Acid in Underutilized Medical Vegetables. Journal of Functional Food. Vol.4:339-347.
Andarwulan N, Ratna B, Diny AS, Bradley B, Hanny W. 2010. Flavonoid Content and Antioxidant Activity of Vegetables from Indonesia.Food Chem. Vol.121:1231-1235.
Ang ESM, Xiaohong Y, Honghui C, Qian L, Ming HZ, Jiake X. 2011. Naringin abrogates osteoclastogenesis and bone resorption via the inhibition of RANKL-induced NF-kB and ERK activation. FEBS Letters. 585:2755-2762.
Ascenzi P, Alessio B, Maria M. 2006. Structure–function relationship of estrogen receptor α and β: Impact on human health. Molecular Aspects of Medicine. 27:299-402.
Ashour ML, Wink M. 2011. Genus Bupleurum: a review of its phytochemistry,
pharmacology and modes of action. Journal of Pharmacy and Pharmacology.
63:305-321.
Ayyad SE, Abdel-Lateff A, Alarif WM, Patacchioli FR, Badria FA, Ezmirly ST. 2012. In vitro and in vivo study of cucurbitacins-type triterpene glucoside from Citrullus
colocynthis growing in Saudi Arabia against hepatocellular carcinoma. Environ Toxicol Pharmacol. 33:245-251.
Azizi SN, Mohammad JC, Parmis S, Ahmadreza B. 2013. Determination of atropine using Mn-doped Zn Squantum dots as novel luminescent sensitizers. Journal of Luminescence. 144:34-40.
Bao-yu Z, Liu Zhong-y, Wang JJ, Sun Li-s, Wang Z-x, Wang Y-c. 2009. Isolation and NMR Study on swainsonine from locoweed, Astragalus strictus. Agricultural Sciences in China. 8(1):115-120.
Bhandari SS , MP Kabra. 2014. To evaluate anti-anxiety activity of thymol. Journal of Acute Disease. Vol.3(2):136-140.
Bickerton GR, Paolini GV, Besnard J, Muresan S, Hopkins AL. 2012. Quantifying the chemical beauty of drugs. Nature Chem. 4: 90-98.
Brimble MA, Jae HP, Carol MT. 2003. Synthesis of the spiroacetal fragment of broussonetine H. Tetrahedron. 59:5861-5868.
Cabello MLR, Sara M, Maria P, Ana IP, Silvia P, Angeles J, Ana MC. 2014. Evaluation of the mutagenicity and genotoxic potential of carvacrol and thymol using the Ames Salmonella test and alkaline, Endo III and FPG-modified comet assays with the human cell line Caco-2. Food and Chemical Toxicology. 72:122-128.
Cao Y, SM Colegate, JA Edgar. 2013. Persistence of echimidine, a hepatotoxic pyrrolizidine alkaloid, from honey into mead. Journal of Food Composition and Analysis.
29:106-109.
Cheng B, Li J, Du J, Lv X, Weng L, Ling C. 2012. Ginsenoside Rb1 inhibits osteoclastogenesis by modulating NF-κB and MAPKs pathways. Food Chem Toxicol.