UJI EFEKTIFITAS EKSTRAK DAUN SIRIH HIJAU
(Piper betle Linn) TERHADAP PERTUMBUHAN BAKTERI
Streptococcus viridans DENGAN METODE DISC DIFFUSION
Laporan penelitian diajukan sebagai salah satu syarat untuk memperoleh gelar SARJANA KEDOKTERAN
Oleh :
Angga Maulana Ibrahim
NIM : 110103000085
PROGRAM STUDI PENDIDIKAN DOKTER
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
v
KATA PENGANTAR
Bismillahirrahmanirrahim.
Assalamu’alaikum Warahmatullahi Wabarakatuh.
Alhamdulillahirabbil’alamin, segala puji saya panjatkan kepada ilahi rabbi, Allah swt. Atas berkat rahmat dan karunia-Nya saya dapat menyelesaikan
laporan penelitian ini,sebagai syarat mendapatkan Gelar Sarjana Kedokteran
(S.Ked). Sepanjang perjalanan penelitian terdapat berbagai macam halangan,
cobaan, dan kesulitan yang didapatkan, namun semua itu sudah dilewati dengan
bantuan, bimbingan dan support dari berbagai pihak. Karena itu saya sebagai peneliti mengucapkan terima kasih kepada :
1.Prof. DR. ( hc ) dr. M.K. Tadjudin, Sp. And sebagai Dekan FKIK UIN Syarif
Hidayatullah Jakarta yang selalu membimbing seluruh mahasiswa FKIK UIN
dan memberikan kesempatan kepada saya untuk menempuh pendidikan di
Program Studi Pendidikan Dokter FKIK UIN Syarif Hidayatullah Jakarta.
2.dr. Witri Ardini, M.Gizi, SpGK sebagai Ketua Program Studi dan untuk
seluruh dosen Program Studi Pendidikan Dokter FKIK UIN Syarif
Hidayatullah Jakarta yang selalu membimbing serta memberikan ilmu kepada
saya selama menjalani masa pendidikan di Program Studi Pendidikan Dokter
FKIK UIN Syarif Hidayatullah Jakarta.
3.Yuliati, S.Si, M.Biomed dan dr. Intan Keumala Dewi, SpMK sebagai
pembimbing yang selalu memberi bantuan serta arahan yang baik dan
menemani saya menyelesaikan penelitian ini.
4.Seluruh anggota keluarga saya yang selalu memberikan dukungan dari semua
aspek untuk menyelesaikan tugas penelitian ini.
5.Tenia Alfitri, Eko Prayoga, Adinda Shofiatunnisa dan Fahri Bangsawan,
sebagai rekan kelompok riset yang telah membantu dalam berbagai hal.
6.Ibu Novi, Pak Bacok, Izkar Ramadhan, Aida Julia Ulfah, Karlina Sari sujana,
Rina Karina, Nida khofia, Diny Febriani Hasanah dan Shidqa Hanif yang telah
membantu dalam proses pengerjaan dan pengambilan data di laboratorium
vi
7.Semua mahasiswa Program Studi Pendidikan Dokter angkatan 2010 yang
memberikan mendukung saya dan menumbuhkan lingkungan yang baik untuk
pendidikan saya..
Demikian laporan ini saya buat, moga bermanfaat bagi saya dan semua
yang membaca. Semua kritik dan saran yang disampaikan sangat diharapkan,
untuk menyempurnakan penelitian ini.
Jakarta, September 2013
vii
ABSTRAK
Angga Maulana Ibrahim. Program Studi Pendidikan Dokter. UJI EFEKTIFITAS EKSTRAK DAUN SIRIH HIJAU (Piper betle Linn) TERHADAP PERTUMBUHAN BAKTERI Streptococcus viridans DENGAN METODE DISC DIFFUSION.
Sirih hijau merupakan tanaman asli kawasan Indo-Cina dan dipercaya mampu mengobati banyak masalah kesehatan. Minyak atsiri ekstrak daun sirih hijau mengandung fenol dan derivatnya seperti euganol dan kavikol yang mampu menghambat pertumbuhan bakteri melalui peningkatan permeabilitas membran bakteri. Streptococcus viridans merupakan penyebab beberapa penyakit seperti faringitis, endokarditis dan lainnya. Penelitian ini bertujuan untuk mengetahui efektifitas ekstrak daun sirih hijau terhadap pertumbuhan Streptococcus viridans. penelitian ini menggunakan metode difusi cakram pada media Agar Darah dengan konsentrasi ekstrak 20%, 30%, 50%, 75% dan 100%. Didapatkan hasil bahwa semakin besar konsentrasi maka semakin besar hambatan terhadap pertumbuhan
Streptococcus viridans (zona hambat yang terbentuk pada konsentrasi 20%; 30%; 50%; 75%; 100%; sebesar 11,67; 14; 17,67; 19; 21,33; mm). Hasil analisis data menggunakan uji One way ANOVA dilanjutkan dengan uji Post hoc menunjukkan terdapat perbedaan yang bermakna (P<0,05) antara berbagai konsentrasi ekstrak daun sirih hijau terhadap pertumbuhan Streptococcus viridans.
Kata kunci : Daun sirih hijau, Streptococcus viridans, difusi cakram.
ABSTRACT
Angga Maulana Ibrahim. Medical Education Department. EFFECTIVITY TEST OF BETEL LEAF (Piper betle Linn) TOWARD GROWTH OF BACTERIA Streptococcus viridans USING DISC DIFFUSION METHOD. Betel leaf is native to Indo-China region and known to have many therapeutic effects. Essential oil of betel leaf contains phenol and its derivatives such as euganol and chavicol, these substances could inhibit bacterial growth by rising membrane permeability. Streptococcus viridans is the cause of some diseases like pharyngitis, endocarditis, etc. the purpose of this study is to determine the effectiveness of betel leaf extract towards the growth of Streptococcus viridans.
This study uses disc diffusion method on agar blood with concentration 20%, 30%, 50%, 75% and 100%. This study shows that the greater concentration of betel leaf extract produces the greater inhibition of Streptococcus viridans growth (inhibition zone at concentration 20%; 30%; 50%; 75%; 100%; at 11,67; 14; 17,67; 19; 21,33; mm). Data analysis using One way ANOVA test followed by Post hoc test shows a significant differences (p<0,05) of inhibiting potential between various concentration of extract towards the growth of Streptococcus viridans.
viii
DAFTAR ISI
LEMBAR PERNYATAAN ... ii
LEMBAR PERSETUJUAN ... iii
LEMBAR PENGESAHAN ... iv
KATA PENGANTAR ... v
ABSTRAK ... vii
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR BAGAN ... xiii
DAFTAR GRAFIK ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
1.3 Tujuan Penelitian ... 2
1.3.1 Tujuan Umum ... 2
1.3.2 Tujuan Khusus ... 3
1.4 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Landasan Teori ... 4
2.1.1. Tanaman Sirih Hijau (Piper betle L.) ... 4
2.1.1.1. Morfologi dan Klasifikasi ... 4
ix
2.1.2. Streptococcus viridans ... 7
2.1.2.1. Morfologi dan Klasifikasi ... 7
2.1.2.2. Patogenesis Streptococcus viridans ... 9
2.1.3. Metode pengujian antimikroba ... 9
2.1.4. Mekanisme Kerja Antibakteri ... 13
2.2 Kerangka Konsep ... 15
3.5 Identifikasi Variabel ... 17
3.5.1 Variabel Bebas ... 17
3.8.1.2 Persiapan dan Determinasi Daun Sirih Hijau ... 19
3.8.1.3 Pembuatan Ekstrak Daun Sirih Hijau (Piper betle.L) ... 19
3.8.1.4 Pembuatan Stok Variabel Konsentrasi ... 19
3.8.1.5 Kultur bakter Streptococcus viridans ... 20
3.8.2 Tahap Pengujian ... 20
x
3.9 Analisis Data ... 20
BAB IV HASIL DAN PEMBAHASAN ... 22
4.1 Hasil ... 22
4.1.1 Ekstrak Daun Sirih Hijau ... 22
4.1.2 Efek Ekstrak Daun Sirih Hijau terhadap Streptococcus viridans ... 23
4.1.3 Uji Kebermaknaan Konsentrasi Ekstrak Daun Sirih Hijau ... 24
4.2 Pembahasan ... 25
BAB V SIMPULAN DAN SARAN ... 28
5.1 Simpulan ... 28
5.2 Saran ... 28
DAFTAR PUSTAKA ... 29
xi
Daftar Tabel
Tabel 2.1. klasifikasi hambatan pertumbuhan bakteri ... 11
Tabel 2.2. Definisi operasional ... 15
xii
Daftar Gambar
Gambar 2.1. Daun sirih hijau ... 4
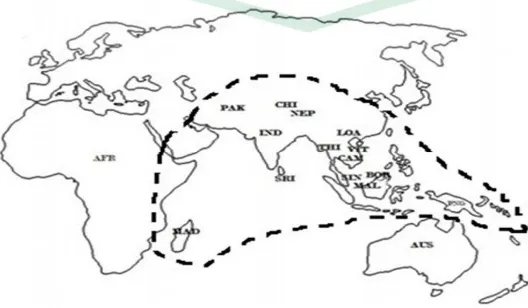
Gambar 2.2. distribusi geografis sirih hijau ... 5
Gambar 2.3. Koloni Streptococcus viridans pada agar darah ... 7
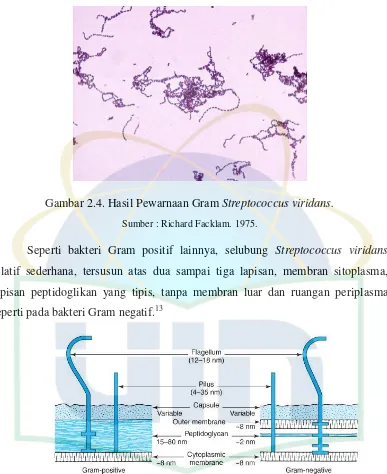
Gambar 2.4. Hasil Pewarnaan Gram Streptococcus viridans ... 8
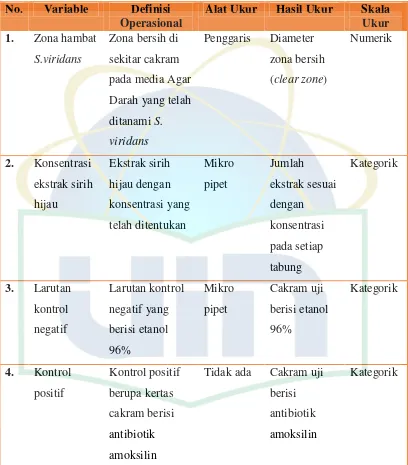
Gambar 2.5. Perbedaan dinding bakteri Gram positif dan Gram negatif ... 8
Gambar 4.1. Hasil ekstraksi Daun Sirih Hijau (Piper betle L.) ... 22
Gambar 4.2. Ekstrak daun sirih hijau (Piper betle L.) pada berbagai konsentrasi ... 22
Gambar 4.3. Efek ekstrak daun sirih hijau terhadap pertumbuhan Streptococcus viridans. ... 23
xiii
Daftar Grafik
xiv
Daftar Lampiran
Lampiran 1. Surat hasil determinasi tumbuhan ... 32
Lampiran 2. Sertifikat pengujian ekstraksi bahan ... 33
Lampiran 3. Hasil uji data statistik ... 34
Lampiran 4. Alat dan bahan ... 37
BAB I PENDAHULUAN
1.1.Latar Belakang
Sirih hijau (Piper Betle Linn) merupakan tanaman asli kawasan Indo-Cina, tanaman ini tumbuh subur di sepanjang Asia tropis hingga Afrika Timur,
menyebar hampir di seluruh wilayah Indonesia, Malaysia, Thailand, Sri lanka,
India, hingga Madagaskar.1 Sirih merupakan salah satu zat psikoaktif yang paling
banyak dikonsumsi, diperkirakan sekitar 600 juta orang mengkonsumsinya setiap
hari. Sirih dikonsumsi luas oleh masyarakat timur Afrika sampai dengan kawasan
Polinesia.2,3 Sirih hijau bersama dengan campuran bahan lainnya sering digunakan
sebagai pencuci mulut di negara Asia tenggara termasuk Indonesia.4
Bangsa Asia telah lama menggunakan sirih hijau sebagai alternatif
pengobatan tradisional.5 Daun, akar dan buah sirih hijau digunakan secara luas
untuk mengobati berbagai penyakit. Daun sirih hijau dipercaya dapat menguatkan
gigi, menyembuhkan luka-luka kecil di mulut, menghilangkan bau mulut, sebagai
obat kumur, pereda batuk, dan menyembuhkan keputihan, daun sirih juga sering
digunakan untuk mengobati radang gusi dan radang tenggorokan 5,6
Efek antibakteri sirih hijau dikarenakan oleh kandungan dari minyak atsiri
daun sirih hijau yang komponen utamanya terdiri atas fenol dan beberapa
derivatnya diantaranya adalah euganol dan kavikol yang berkhasiat sebagai
antibakteri. Fenol memicu kebocoran komponen intraselular termasuk pelepasan
K+ yang merupakan tanda pertama kerusakan membran, euganol sebagai
bakterisida melalui peningkatan permeabilitas membran mikroba dan kavikol
memiliki daya bakterisida lima kali lebih kuat dibandingkan senyawa fenol
lainnya.6,7,8
Sirih hijau memiliki banyak manfaat, yaitu sebagai analgesik, antibakteri,
amebisid, fungisid, antiseptik, immunomodulator dan lainnya.9 Menurut Linchu
(2012) ekstrak kloroform dan etanol sirih hijau memiliki respon hambatan
antibakteri terhadap Streptococcus viridans,10 Penelitian yang lain yang dilakukan
oleh Lidya Pratiwi (2010) menunjukkan bahwa ekstrak etanol 70% sirih hijau
pada konsentrasi 20% dapat mempengaruhi pertumbuhan Streptococcus viridans
dengan konsentrasi hambat minimum lebih dari 15%.11Menurut Maharani (2011)
ekstrak sirih hijau 35% memiliki efek antibakteri yang lebih kuat dibanding
povidone iodine 10%.12
Streptococcus viridans merupakan bakteri Gram positif berbentuk kokus dan tersusun seperti rantai. Walaupun sejatinya bakteri ini flora normal saluran
pernapasan atas, bakteri ini juga merupakan faktor penyebab bagi beberapa
penyakit seperti karies gigi, endokarditis, abses, scarlet fever, radang tenggorokan dan febris puerpuralis.13 Bakteri ini merupakan penyebab 50-70% endokarditis
bakterial pada katup jantung dan faktor penyebab abses lokal yang bisa merusak
rahang, gigi, dan struktur vital lainnya seperti mediastinum, perikardium, dan otot
leher.14
Secara umum metode pengujian antibakteri bisa dilakukan dengan dua
metode, difusi dan dilusi. Metode difusi bisa dilakukan melalui beberapa cara,
yaitu E-test, disc diffusion, ditch plate, cup plate dan gradien plate.15
Berdasarkan hal diatas, penelitian ini bertujuan untuk mengetahui
efektivitas ekstrak daun sirih hijau terhadap pertumbuhan bakteri Streptococcus viridans. Penelitian ini meliputi uji aktivitas antibakteri ekstrak dalam berbagai konsentrasi terhadap bakteri Streptococcus viridans dengan metode disc diffusion menggunakan kertas cakram.
1.2. Rumusan Masalah
Berdasarkan latar belakang di atas, rumusan masalah pada penelitian ini
adalah bagaimana efek ekstrak etanol daun sirih hijau (Piper betle Linn) terhadap pertumbuhan bakteri Streptococcus viridans?
1.3.Tujuan Penelitian
1.3.1. Tujuan umum
1.3.2. Tujuan Khusus
Untuk mengetahui zona hambat berbagai konsentrasi ekstrak sirih
hijau (Piper betle Linn) yang terbentuk pada media Agar Darah yang telah ditanami bakteri Streptococcus viridans.
1.4 Manfaat penelitian
a. Bagi Peneliti
- Menerapkan ilmu pengetahuan yang telah didapatkan selama
menempuh pendidikan di program studi pendidikan dokter
(PSPD) UIN Syarief Hidayatullah, Jakarta.
- Menambah pengetahuan peneliti terhadap penerapan
beberapa ilmu kedokteran terhadap perkembangan dunia
kesehatan.
b. Bagi Institusi
- Menambah informasi dan literatur mengenai keilmuan
mikrobiologi.
- Memajukan UIN Syarif Hidayatullah dan FKIK UIN Syarif
Hidayatullah dengan mempublikasikan penelitian ini.
c. Bagi Keilmuan
- Dapat memberikan informasi mengenai pengaruh ekstrak
daun sirih hijau (Piper betle Linn) terhadap pertumbuhan bakteri Streptococcus viridans.
- Sebagai sumber referensi bagi praktisi yang tertarik dalam
penelitian mikrobiologi.
- Sebagai data dan informasi untuk melakukan penelitian lanjut
tentang pengaruh ekstrak etanol daun sirih hijau (Piper betle Linn) terhadap pertumbuhan bakteri Streptococcus viridans.
d. Bagi Sosial
- Menambah pengetahuan masyarakat mengenai senyawa
alam yang efektif dalam menghambat pertumbuhan bakteri.
- Sebagai rujukan untuk pemanfaatan ekstrak daun sirih dalam
upaya peningkatan kesehatan masyarakat yang mudah dan
4
BAB II
TINJAUAN PUSTAKA
2.1.Landasan Teori
2.1.1. Tanaman Sirih Hijau (Piper betle Linn) 2.1.1.1. Morfologi dan Klasifikasi
Sirih hijau merupakan tumbuhan merambat dan bisa tumbuh memanjang
sampai 5-15 m dengan bunga berbentuk bulir, berdiri sendiri di ujung cabang
berhadapan dengan daun. Bulir jantan memiliki panjang gagang 1,5-3 cm dengan
benangsari yang sangat pendek, bulir betina memiliki panjang gagang 2,5-6 cm
dengan kepala putik 3-5 buah. Buah buni sirih hijau berbentuk bulat dengan ujung
gundul. Bulir masak memiliki tebal 1-1,5 cm, berambut kelabu dengan biji
membentuk lingkaran.16 Berikut adalah deskripsi daun sirih hijau :
Warna : kuning kehijauan sampai hijau gelap dengan permukaan atas
yang mengkilap.1
Aroma : khas dan berbau sedap.1
Rasa : daun sirih hijau memiliki aroma yang khas dengan rasa yang
beragam, mulai dari manis sampai tajam atau pedas dikarenakan
memiliki kandungan minyak esensial.1
Bentuk dan ukuran : daun sirih hijau memiliki bentuk seperti jantung
dengan ukuran yang beragam dengan panjang 7-15 cm dan lebar 5-14
cm, tulang daun bagian bawah gundul atau berambut sangat pendek.1,16
Berdasarkan ilmu taksonomi, berikut adalah klasifikasi dari tanaman sirih
hijau : 17
Kingdom : Plantae
Division : Magnoliophyta
Class : Magnoliopsida
Ordo : Piperales
Family : Piperaceae
Genus : Piper
Species : Piper betle Linn
Untuk keanekaragamannya, di Indonesia dikenal beberapa macam sirih.
Daun sirih dengan warna hijau tua memiliki rasa pedas tersebar di Jawa Tengah
dan Timur. Daun sirih dengan warna kuning tersebar luas di Sumatera dan Jawa
Barat. Sirih kaki merpati dengan daun berwarna kuning dan tulang daun berwarna
merah. Serta, sirih hitam yang ditanam khusus untuk obat.16
Tanaman sirih hijau tumbuh di daerah dengan kelembaban yang relatif
tinggi, tanaman ini tumbuh baik di daerah yang memiliki pengairan yang baik
dengan curah hujan 2250-4750 mm/tahun, tanah yang kaya akan materi organik
dengan pH 7-7,5 dan ketinggian sampai 900 m diatas permukaan laut.1
Gambar 2.2. Distribusi geografis sirih hijau
Tanaman sirih hijau merupakan tanaman asli kawasan Indo-Cina
(Malaysia, Vietnam, Laos, Indonesia, Thailand, Myanmar, Singapore, India) dan
tersebar luas sampai Madagaskar dan Afrika timur.1
2.1.1.2. Kandungan Kimiawi dan Manfaat Daun Sirih Hijau
Setiap daun sirih hijau memiliki kandungan air (85-90%), protein
(3-3,5%), karbohidrat (0,5-6,1%), serat (2-3%), minyak esensial (0.08-0.2%), Tannin
(0.1-1.3%), dan Alkaloid. Daun sirih hijau juga mengandung beberapa vitamin
seperti Vitamin C (0.005-0.01%), asam nikotinik (0.63-0.89mg/100gms), vitamin
A (1.9-2.9mg/100gms), thiamin (10-70μg/100gms), riboflavin
(1.9-30μg/100gms). Dan juga mineral (2.3-3.3%) yang terdiri atas kalsium (0.2-0.5%),
besi (0.005-0.007), iodin (3.4μg/100gms), fosfor (0.05-0.6%), potassium
(1,1-4,6%).1
Bau aromatik yang khas pada daun sirih hijau disebabkan oleh kandungan
minyak atsiri yang terdiri atas fenol dan badan terpen yang dimilikinya, kualitas
daun sirih hijau bergantung pada kandungan fenol, semakin besar kandungan
fenol yang dimiliki, semakin baik kualitas daun tersebut.1,6
Pada setiap daun sirih hijau mengandung 4.2% minyak atsiri yang
komponen utamanya terdiri dari bethel fenol dan beberapa derivatnya
diantaranya euganol allypyrocatechine (26.8-42.5%), cineol (2.4-4.8%), methyl euganol (4.2-15.8%), caryophyllen (3-9.8%), hidroksi kavikol, kavikol (7.2-16.7%), kavibetol (2.7-6.2%), estragol, ilypyrokatekol (0-9.6%), karvakrol (2.2-5.6%), alkaloid, flavonoid, triterpenoid atau steroid, saponin, terpen, fenilpropan, terpinen, diastase 0.8-1.8% dan tannin 1-1.3%.18
Fenol pada minyak atsiri sirih hijau memiliki fungsi bakterisidal melalui
mekanisme kebocoran komponen intraselular termasuk pelepasan K+ yang
merupakan tanda pertama kerusakan membran, euganol sebagai bakterisida
melalui peningkatan permeabilitas membran mikroba, dan kavikol memiliki daya
bakterisida lima kali lebih kuat dibandingkan senyawa fenol lainnya. 6,7,8
Sirih hijau memiliki efek analgesik, antibakteri, amebisid, fungisid,
menghilangkan bau mulut, mengobati keputihan, mastosis, displasia, konstipasi,
asma dan penyakit lainnya. 5,6,9
2.1.2.Streptococcus viridans
2.1.2.1. Morfologi dan Klasifikasi
Streptococcus viridans merupakan bakteri Gram positif dari suku Streptococcaceae, berbentuk kokus dan tersusun seperti rantai, mempunyai ukuran
0,5-11 µm, bersifat anaerob fakultatif, tumbuh baik pada pH 7,4-7,6 dan suhu
optimal 370 C selama 18-24 jam. Secara umum, pertumbuhan streptococcus pada
media tergolong lambat, kecuali jika diperkaya dengan cairan darah atau cairan
jaringan. Sifat pertumbuhan pada Agar Darah, Streptococcus viridans membentuk warna hijau dan hemolisis sebagian di sekeliling koloni.13
Ordo : Eubacteriales
Famili : Lactobacillaceae
Tribus : Streptococcaceae
Genus : Streptococcus
Spesies : Streptococcus viridans
Gambar 2.4. Hasil Pewarnaan Gram Streptococcus viridans.
Sumber : Richard Facklam. 1975.
Seperti bakteri Gram positif lainnya, selubung Streptococcus viridans
relatif sederhana, tersusun atas dua sampai tiga lapisan, membran sitoplasma,
lapisan peptidoglikan yang tipis, tanpa membran luar dan ruangan periplasma
seperti pada bakteri Gram negatif.13
Gambar 2.5. Perbedaan dinding bakteri Gram positif dan Gram negatif.
Sumber : Brooks et al. 2007.
Berikut adalah karakteristik Streptococcus viridans yang penting dalam bidang medis :13,19
Substansi kelompok spesifik : tidak ada.
Hemolisis : alfa.
Kriteria laboratorium penting : sensitif optochin, koloni larut dalam
empedu, reaksi quellung positif.
Penyakit yang sering dan penting : karies gigi, endokarditis, abses,
scarlet fever, radang tenggorokan dan febris puerpuralis
2.1.2.1. Patogenesis Streptococcus viridans
Streptococcus viridans merupakan flora normal pada saluran pernapasan atas dan berperan penting dalam menjaga kesehatan membran mukosa yang
terdapat disana.13 Bakteri ini dapat mencapai aliran darah melalui trauma dan
merupakan penyebab 50-70% bakterial endokarditis pada katup jantung yang
abnormal.13,14 Penelitian lain juga menunjukkan bahwa 30% pasien yang
melakukan operasi rongga mulut, pencabutan gigi, atau pemeriksaan gigi rutin
yang menimbulkan perdarahan minor mengalami bakteremia transien
setelahnya.14
Sekitar 30-60% mikroorganisme intraoral merupakan Streptococcus,
terutama Streptococcus alfa-hemolitikus dan Streptococcus non-hemolitikus. Refoua (2005) menyatakan bahwa Streptococcus viridans merupakan faktor penting penyebab abses lokal yang bisa merusak rahang, gigi, dan struktur vital
lainnya seperti mediastinum, perikardium, dan otot leher.14
2.1.3.Metode Pengujian Antibakteri
Uji antibakteri bertujuan untuk mengukur respon pertumbuhan populasi
mikroba terhadap suatu agen antibakteri yang telah ditentukan.15 Dua sistem uji
standar untuk menentukan level resistensi in-vitro zat antibakteri adalah difusi dan
dilusi :20
A. Metode dilusi
Pada metode ini ditentukan konsentrasi hambat minimum (KHM)
dan konsentrasi bunuh minimum (KBM) suatu zat antibakteri terhadap
bakteri yang diujikan. Prinsip dari metode dilusi adalah bahan antibakteri
yang sudah diencerkan ke dalam beberapa konsentrasi disatukan dengan
metode dilusi ini, yaitu metode dilusi cair (broth dilution) dan metode dilusi padat (solid dilution).15, 20
Selanjutnya ditentukan KHM, yaitu konsentrasi zat terkecil yang
masih menghambat pertumbuhan kuman, dan ditentukan KBM,
konsentrasi zat terkecil yang dapat membunuh 99,9% bakteri dalam
inokulum. Nilai KHM suatu zat antibakteri berkorelasi secara logaritmik
(log2) dengan diameter zona hambat metode difusi.20 Namun, dikarenakan
rumit dan memakan waktu yang lama, metode ini jarang digunakan untuk
uji laboratorium rutin.13
B. Metode difusi
Metode yang sering digunakan untuk uji resistensi zat antibakteri
adalah metode difusi. Pada metode ini zat antibakteri diberikan pada media
pembenihan yang telah diinokulasi oleh bakteri, setelah diinkubasi,
dihitung diameter zona terang disekitar zat antibakteri yang
diinterpretasikan sebagai kekuatan hambat suatu zat terhadap pertumbuhan
suatu bakteri.13 Metode ini bisa dilakukan dengan beberapa cara, yaitu :
Metode disc diffusion
Metode disc diffusion (tes Kirby & Bauer) digunakan untuk menentukan aktivitas agen antibakteri. Media agar yang telah
ditanami mikroorganisme kemudian diletakkan diatasnya piringan
yang telah diberikan suatu zat antibakteri.15
Menurut standar umum obat asal tanaman Depkes RI (1998),
suatu bakteri dinyatakan peka terhadap antibakteri asal tanaman
apabila memiliki ukuran zona hambat 12-24 mm.21 Sedangkan
menurut Greenwood (1995) efektifitas suatu zat antibakteri bisa
Tabel 2.1. klasifikasi respon hambatan pertumbuhan bakteri
Diameter zona terang Respon hambatan pertumbuhan
>20 mm Kuat
Metode E-test digunakan untuk menghitung kadar hambat minimum KHM suatu zat antibakteri. Strip plastik yang
mengandung agen antibakteri dengan konsentrasi tertinggi sampai
terendah diletakan pada media agar yang telah ditanami
mikroorganisme. Hambatan pertumbuhan mikroorganisme bisa
diamati dengan adanya area jernih di sekitar strip.15
Ditch-plate technique
Ditch-plate technique atau metode parit dilakukan dengan cara membuat parit melalui potongan membujur pada media agar. Parit
ini kemudian diisi oleh agen antibakteri, dan mikroba uji
(maksimum 6 macam) kemudian digoreskan ke arah parit yang
telah diisi agen antibakteri.15
Cup-plate technique
Cup-plate technique (metode lubang/sumur) memiliki prinsip yang serupa dengan metode disc diffusion, pada media agar yang telah ditanami mikroorganisme dibuat sumur atau lubang yang
kemudian akan diberi agen antibakteri didalamnya.15
Gradient-plate technique
Konsentrasi agen antibakteri pada metode ini bervariasi mulai dari
nol hingga maksimal. Pertama media agar dicairkan dan zat
antibakteri ditambahkan, campuran ini lalu dimasukkan ke dalam
cawan petri dan diletakkan dalam posisi miring, selanjutnya nutrisi
dituang diatasnya. Plate dalam cawan petri ini kemudian
berdifusi secara maksimal dan permukaan media mengering.
Selanjutnya mikroba uji (maksimal 6 macam) digoreskan pada
plate mulai dari konsentrasi tinggi ke rendah. Hasil pada metode
ini diinterpretasikan sebagai panjang total pertumbuhan
mikroorganisme maksimal yang mungkin dibandingkan dengan
panjang pertumbuhan aktual hasil goresan.15
Terdapat beberapa faktor yang perlu diperhatikan terkait uji antibakteri
karena bisa menyebabkan perubahan hasil yang signifikan :
pH lingkungan
beberapa zat lebih aktif bekerja di lingkungan yang asam, sedangkan zat
lainnya lebih aktif bekerja di lingkungan yang basa.13
Media pertumbuhan
beberapa zat bisa mempengaruhi pertumbuhan suatu mikroba atau
mempengaruhi efektifitas bahan antibakteri, media pertumbuhan harus
mampu mendukung pertumbuhan bakteri dan tidak menghambat efektifitas
antibakteri.11, 13
Stabilitas zat antibakteri
beberapa zat antibakteri menurun efektifitas nya pada suhu inkubator,
beberapa zat menurun dengan lambat, dan zat lainnya mampu bertahan
lama.13
Inokulum
Secara umum, semakin besar ukuran inokulum semakin rendah kepekaan
atau sensitifitas kuman sehingga zona hambatan menjadi lebih kecil.13 untuk
uji antibakteri jumlah bakteri yang dianjurkan yaitu 105-108 CFU/mL.23
Inkubasi
Waktu yang diperlukan untuk uji antibakteri umumnya 16-24 jam. Semakin
lama masa inkubasi semakin besar kemungkinan timbulnya mutan.
Sedangkan suhu optimal pertumbuhan mikroba yaitu sama seperti suhu
2.1.4.Mekanisme Kerja Antibakteri 24
Berdasarkan aktivitasnya antibakteri dapat dibagi atas 2 kelompok, yaitu
aktivitas bakteriostatik (menghambat pertumbuhan bakteri, namun tidak
membunuhnya) dan bakterisidal (bersifat membunuh bakteri dalam spektrum
yang luas). Sedangkan berdasarkan mekanisme kerjanya, obat antibakteri dapat
dibagi ke dalam 5 kelompok, yaitu :
A. Menghambat metabolisme sel mikroba
Tidak seperti mamalia yang bisa mendapatkan asam folat dari luar,
mikroba harus mensintesis asam folat dari para asam amino benzoat
(PABA) untuk kelangsungan hidupnya. Sulfonamid yang memiliki
kemiripan struktur molekul dengan PABA akan berkompetisi untuk
diikutsertakan dalam pembentukan asam folat sehingga terbentuk analog
asam folat yang nonfungsional, asam p-aminosalisilat (PAS) yang
merupakan analog PABA bekerja dengan menghambat sintesis asam folat,
contoh lain dari obat yang menghambat metabolism sel mikroba adalah
trimetropin. Dengan mekanisme kerja ini akan diperoleh efek
bakteriostatik pada mikroba.
B. Menghambat sintesis dinding sel mikroba
Dinding sel bakteri tersusun atas polipeptidoglikan yang merupakan
kompleks primer glikopeptida. Sikloserin menghambat reaksi sintesis
dinding bakteri paling dini, dan selanjutnya diikuti berturut-turut oleh
basitrasin, vankomisin. Penisilin dan sefalosporin menghambat reaksi
terakhir dari sintesis dinding sel bakteri (transpeptidasi). Perbedaan
tekanan osmotik antara sel bakteri dengan lingkungan di luar sel
menyebabkan kerusakan dinding sel bakteri sehingga bakteri akan lisis.
Mekanisme kerja ini merupakan dasar efek bakterisidal pada bakteri yang
peka.
C. Mengganggu keutuhan membran sel mikroba
Contoh obat dalam golongan adalah polimiksin, polien, antibakteri
kemoterapeutik dan antiseptic surface active agents. Polimiksin yang merupakan senyawa ammonium-kuartener merusak membran sel bakteri
bakteri Gram negatif lebih peka terhadap polimiksin disebabkan
kandungan fosfor yang lebih tinggi dibandingkan bakteri Gram positif.
Antiseptik yang mengubah tegangan permukaan (surface-active agents) merusak permeabilitas selektif dari membran sel mikroba yang berakibat
keluarnya berbagai komponen penting dari asam sel mikroba seperti
protein, asam nukleat nukleotida dan lain-lain. Oleh karena itu obat
golongan ini memiliki efek bakterisidal terhadap bakteri.
D. Menghambat sintesis protein sel mikroba
Bakteri perlu mensintesis berbagai protein untuk kehidupanya, sintesis
protein ini berlangsung di ribosom dengan bantuan mRNA dan tRNA,
pada bakteri ribosom terdiri atas dua sub-unit, 30S dan 50S, pada sintesis
protein kedua sub-unit ini akan bergabung pada pangkal rantai rantai
mRNA menjadi ribosom 70S. Streptomisin berikatan dengan ribosom 30S
dan menyebabkan tRNA salah membaca mRNA pada sintesis protein,
sehingga akan terbentuk protein yang abnormal dan nonfungsional.
Tetrasiklin berikatan dengan ribosom 30S dan mencegah masuknya koplek
tRNA-asam amino pada lokasinya. Eritromisin akan berinteraksi dengan
ribosom 50S dan menghambat translokasi kompleks tRNA-peptida dari
lokasi asam amino ke lokasi peptide, sehingga rantai polipeptida tidak
dapat diperpanjang. Kloramfenikol berikatan dengan ribosom 50S dan
menghambat kerja enzim peptidil transferasi dalam pengikatan asam
amino baru pada rantai polipeptida.
E. Menghambat sintesis asam nukleat sel mikroba
Contoh obat golongan ini adalah rifampisin dan kuinolon. Rifampisin
merupakan derivate rifamisin yang berfungsi menghambat sintesis RNA
dan DNA bakteri dengan cara berikatan dengan enzim polimerase-RNA.
Sedangkan obat golongan kuinolon menghambat enzim DNA girase pada
kuman yang fungsinya menata kromosom yang sangat panjang menjadi
2.2.Kerangka teori
2.3.Kerangka konsep
Variabel bebas : Ekstrak daun sirih hijau (Piper betle L.) dengan berbagai konsentrasi.
Variabel terikat : Pertumbuhan bakteri Streptococcus viridans di media Agar Darah, diukur dengan berbagai diameter zona hambatan (zona terang)
yang terbentuk dalam milimeter (mm).
Ekstrak daun sirih hijau
Minyak atsiri
Fenol Euganol Kavikol
Merusak permeabilitas membran bakteri
Pertumbuhan bakteri terhambat
Ekstrak daun sirih hijau dengan berbagai
konsentrasi
Biakan Bakteri
S. viridans
Pertumbuhan Bakteri Normal
Pertumbuhan Bakteri Terhambat Inokulum, suhu
inkubasi, waktu inkubasi, pH, media
2.4.Definisi Operasional
Tabel 2.2. Definisi operasional.
BAB III
METODOLOGI PENELITIAN
3.1 Desain Penelitian
Penelitian ini merupakan penelitian ekperimental dengan teknik disc diffusion untuk melihat efek ekstrak daun sirih hijau (Piper betle L.) terhadap pertumbuhan bakteri Streptococcus viridans.
3.2 Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Januari - September 2013 di
Laboratorium Mikrobiologi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif
Hidayatullah Jakarta. Proses determinasi tanaman dilakukan oleh Lembaga Ilmu
Pengetahuan Indonesia (LIPI) Bogor, sedangkan proses ekstraksi daun sirih hijau
(Piper betle L.) dilakukan oleh Balai Penelitian Tanaman Rempah dan Obat
(
BALITRO) Bogor.3.3 Bahan yang Diuji
Ekstrak daun sirih hijau (Piper betle L.) yang telah dideterminasi oleh LIPI Bogor dan diekstraksi oleh BALITRO Bogor.
3.4 Sampel Bakteri
Bakteri Streptococcus viridans diisolasi pada media Agar Darah, dan diinkubasi pada suhu 37°C selama 24 jam.
3.5 Identifikasi Variabel 3.5.1 Variabel Bebas
Ekstrak daun sirih hijau (Piper betle Linn) dengan berbagai konsentrasi.
3.5.2 Variabel Terikat
Pertumbuhan bakteri Streptococcus viridans di media Agar Darah, diukur dengan berbagai diameter zona hambatan (zona terang) dengan ukuran
dalam milimeter (mm).
3.6 Alat dan Bahan Penelitian 3.6.1 Alat Penelitian
Alat yang digunakan dalam penelitian ini yaitu : tabung reaksi, mikro
pipet, vortex, bunsen, korek api, ose, spatula besi, cawan petri, penggaris,
rak tabung, timbangan, autoclave, baki, swab kapas, pengukur waktu, inkubator, penggaris, cakram uji kosong, label, alat tulis, kamera, laminar air flow, tisu, pinset, alkohol.
3.6.2 Bahan Penelitian
Bahan yang digunakan dalam penelitian ini yaitu : media Agar Darah,
larutan Mc Farland 0,5%, ekstrak daun sirih hijau, pelarut etanol 96%,
thioglikolat, biakan Streptococcus viridans, cakram amoksilin, cakram uji kosong. Thioglikolat da Strepto o us viridans
di orte hi gga ho oge
Kekeruha i okulu dista darisasi de ga e ggu aka laruta sta darisasi
ko se trasi , M Farla d
Pe uata ko se trasi ekstrak sirih hijau, %, %, % % da %
telah dita a i Strepto o us viridans
I ku asi sela a - ja
3.8 Cara Kerja Penelitian
3.8.1 Tahap Persiapan
3.8.1.1 Sterilisasi Alat dan Bahan
Seluruh alat yang akan digunakan disterilisasi di dalam
autoclave selama 15 menit pada suhu sebesar 121°C dengan mengatur tekanan sebesar 1,5 atm setelah sebelumnya dicuci
bersih, dikeringkan dan dibungkus dengan kertas.
3.8.1.2 Persiapan dan Determinasi Daun Sirih Hijau
Daun sirih hijau diperoleh dari tanaman milik warga di
daerah Mandalawangi, Pandeglang yang homogen sebanyak
1000 gram. Kemudian dilakukan determinasi di Lembaga
Ilmu Pengetahuan Indonesia Bogor yang bertujuan untuk
memastikan kebenaran dari tanaman yang digunakan.
Determinasi tanaman sirih hijau dilakukan dengan cara
mencocokkan ciri-ciri morfologi yang ada pada tanaman sirih
terhadap kepustakaan dan dibuktikan di bidang Botani Pusat
Penelitian Biologi LIPI Bogor.
3.8.1.3 Pembuatan Ekstrak Daun Sirih Hijau
Pembuatan ekstrak dilakukan dengan metode maserasi.
Sebanyak 1000 gram daun sirih hijau dicuci bersih terlebih
dahulu, kemudian dikeringkan, diremas dan dihaluskan
sampai menjadi serbuk. Serbuk lalu direndam dalam etanol
96% selama 3x24 jam, melalui penyaringan filtrat sirih hijau
ini didapatkan. Kemudian semua filtrat digabung, dan
diuapkan atau dipekatkan dengan rotary evaporator pada suhu 40-50°C hingga diperoleh ekstrak kental sebanyak 116,3
gram.
3.8.1.4. Pembuatan Stok Variabel Konsentrasi
Variabel yang digunakan pada penelitian ini sejumlah 7
variabel, kontrol negatif berupa etanol, variasi konsentrasi
ekstrak sirih hijau 100%, 75%, 50%, 30%, 20% dengan
menggunakan cakram amoksilin yang merupakan antibiotik
spektrum luas sehingga bisa menghambat pertumbuhan
bakteri Gram positif maupun negatif.
3.8.1.5. Kultur Bakteri Streptococcus viridans
Pembuatan stok bakteri ini dilakukan untuk memperbanyak
dan meremajakan bakteri, dengan cara menginokulasikan 1
ose biakan murni bakteri Streptococcus viridans ke dalam Agar Darah, kemudian diinkubasi pada suhu 37°C selama 24
jam di dalam inkubator.
3.8.2. Tahap Pengujian
3.8.2.1. Uji Efektivitas Ekstrak Daun Sirih Hijau Terhadap
Streptococcus viridans
Bakteri diencerkan dengan mencampurkan 1 ose suspensi
bakteri Streptococcus viridans ke dalam tabung reaksi yang telah berisi Thioglikolat. Kemudian dihomogenkan dengan
menggunakan vortex dan kekeruhannya distandarisasi dengan
konsentrasi 0.5 Mc Farland agar jumlah bakteri memenuhi
syarat untuk uji kepekaan yaitu: 105–108/ml. Kemudian
larutan bakteri dioleskan pada media pertumbuhan Agar
Darah. Cakram uji kosong yang telah direndam di dalam
masing-masing stok konsentrasi ekstrak daun sirih hijau tadi
diletakkan di atas permukaan agar secara higienis di dalam
laminar air flow. Lalu media diinkubasi ke dalam inkubator. Inkubasi dilakukan pada suhu 37°C selama 24 jam, keesokan
harinya diukur diameter zona terang (clear zone) dengan menggunakan penggaris.
3.9. Analisis Data
Data hasil penelitian efek ekstrak daun sirih pada Streptococcus viridans
dianalisis dengan menggunakan program SPSS 16.0 untuk melihat apakah ada
perbedaan efektifitas yang bermakna dari masing-masing cakram uji yang
mengandung kontrol negatif, berbagai konsentrasi ekstrak daun sirih hijau dan
Data pada penelitian ini berupa variabel kategorik-numerik lebih dari 2
kelompok tidak berpasangan sehingga menggunakan uji one way ANOVA jika distribusi normal. Jika distribusi data tidak normal maka menggunakan uji
nonparametrik yakni Uji Kruskall-Wallis. Selanjutnya dilakukan uji post hoc
BAB IV
HASIL DAN PEMBAHASAN
4.1.Hasil
4.1.1. Ekstraksi Daun Sirih Hijau (Piper betle Linn)
Daun sirih hijau didapatkan di kawasan Mandalawangi, Pandeglang.
Setelah daun dikeringkan, dilakukan determinasi tanaman yang membuktikan
bahwa daun merupakan Piper betle Linn yang merupakan family piperaceae. Selanjutnya 1000 gram daun sirih hijau kering diekstrak dengan menggunakan
pelarut etanol 96%.
Gambar 4.1. Hasil ekstraksi daun sirih hijau (Piper betle L.).
Gambar 4.2. Ekstrak daun sirih hijau (Piper betle L.) pada berbagai konsentrasi.
4.1.2. Efek Ekstrak Daun Sirih Hijau Terhadap Streptococcus viridans
Gambar 4.3. Efek ekstrak daun sirih hijau terhadap pertumbuhan Streptococcus viridans.
Hasil pengukuran zona hambat pada uji efektifitas ekstrak daun sirih hijau
(Piper betle L.) terhadap Streptococcus viridans didapatkan hasil sebagai berikut : Pada konsentrasi ekstrak daun sirih hijau 20% didapatkan rata-rata zona hambat
11,67 mm dengan standar deviasi 0,58. Pada konsentrasi ekstrak daun sirih hijau
30% didapatkan rata-rata zona hambat 14 mm dengan standar deviasi 0. Pada
konsentrasi ekstrak daun sirih hijau 50% didapatkan rata-rata zona hambat 17,67
mm dengan standar deviasi 0,58. Pada konsentrasi ekstrak daun sirih hijau 75%
didapatkan rata-rata zona hambat 19 mm dengan standar deviasi 1. Pada
konsentrasi ekstrak daun sirih hijau 100% didapatkan rata-rata zona hambat
21,33 mm dengan standar deviasi 0,58. Sedangkan pada kontrol positif dengan
Ko trol -
Ko trol +
Ko se trasi %
Ko se trasi %
Ko se trasi % Ko se trasi %
menggunakan amoksilin didapatkan rata-rata zona hambat 25,33 mm dengan
standar deviasi 0,58.
Grafik 4.1. Hambatan pertumbuhan Streptococcus viridans.
Berdasarkan hasil penelitian diatas, dapat disimpulkan bahwa ekstrak
daun sirih hijau 20%, 30% memiliki respon hambatan pertumbuhan yang lemah
terhadap Streptococcus viridans, ekstrak daun sirih hijau 50% dan 75% memiliki respon hambatan pertumbuhan sedang terhadap Streptococcus viridans.
Sedangkan ekstrak daun sirih hijau 100% memiliki respon hambatan pertumbuhan
kuat terhadap Streptococcus viridans. dapat disimpulkan pula bahwa pertambahan konsentrasi ekstrak daun sirih hijau berbanding lurus dengan bertambah kuatnya
zona hambat pertumbuhan bakteri.
4.1.3. Uji Kebermaknaan Konsentrasi Ekstrak Daun Sirih Hijau
Variabel dalam penelitian ini adalah variabel kategorik-numerik tidak
berpasangan dan memiliki lebih dari dua data, sehingga uji parametrik yang
digunakan adalah uji one way ANOVA jika distribusi dan varian data normal, namun jika salah satu dari dua syarat tadi tidak terpenuhi maka akan dilakukan uji
parametrik Kruskal-wallis.
Berdasarkan uji normalitas Shapiro-Wilk didapatkan distribusi data yang normal, dan berdasarkan uji homogenitas didapatkan varian data yang sama dari
penelitian ini, sehingga bisa dilakukan uji one way ANOVA dengan hasil P = 0,000 yang menunjukkan terdapat perbedaan zona hambat yang bermakna
pada setiap konsentrasi, yang selanjutnya dilakukan uji Post hoc untuk mengetahui perbedaan konsentrasi mana yang bermakna.
Tabel 4.1. Hasil Analisis Multikomparasi dengan uji post hoc
konsentrasi Etanol 20% 30% 50% 75% 100% Amoksilin
Pada uji post hoc, perbedaan antar konsentrasi dinyatakan bermakna apabila didapatkan nilai P<0,05 pada antar konsentrasi dengan interval
kepercayaan 95%. Penelitian ini menghasilkan P<0,05 pada perbandingan semua
konsentrasi, sehingga bisa disimpulkan bahwa terdapat perbedaan yang bermakna
antar setiap konsentrasi.
4.2.Pembahasan
Berdasarkan penelitian yang telah dilakukan, ekstrak daun sirih hijau
mampu menghambat pertumbuhan Streptococcus viridans, didapatkan respon hambatan lemah pada konsentrasi 20%, 30%. Didapatkan respon hambatan
sedang pada konsentrasi 50% dan 75%. Dan didapatkan respon hambatan kuat
pada konsentrasi 100%.
Tanaman sirih hijau memiliki banyak manfaat, salah satunya adalah
sebagai antibakteri.9 Menurut Linchu (2012) ekstrak daun sirih hijau dengan
pelarut kloroform memiliki respon hambatan kuat terhadap pertumbuhan
bahwa ekstrak daun sirih hijau dengan pelarut etanol 70% pada konsentrasi 20%
mempengaruhi pertumbuhan Streptococcus viridans dengan KHM diatas 15%.11 pada penelitian yang penulis lakukan digunakan ekstrak etanol 96% dengan
diameter zona hambat yang didapat lebih besar dibandingkan ekstrak etanol 70%
pada konsentrasi yang sama.
Efek ekstrak daun sirih hijau terhadap pertumbuhan bakteri dikarenakan
kandungan minyak atsiri yang tersusun atas fenol dan derivatnya seperti euganol
dan kavikol.6 Pada konsentrasi 0,1-1% fenol bersifat bakteriostatik, sedangkan
pada konsentrasi 1-2% fenol bersifat bakteriosidal.26 Fenol memicu inaktivasi
enzim seluler sehingga terjadi perubahan permeabilitas membran, influks berlebih
substansi ekstra seluler akan memicu kebocoran komponen intraselular termasuk
pelepasan K+ yang merupakan tanda pertama kerusakan membran, melalui proses
koagulasi fenol bisa merusak organ intrasellular bakteri, selain itu fenol juga akan
merusak proton motive force yang memiliki fungsi sebagai penghasil energi bagi mikroba.27,28 Euganol sebagai bakterisida melalui peningkatan permeabilitas
membran mikroba dan kavikol memiliki daya bakterisida lima kali lebih kuat
dibandingkan senyawa fenol lainnya.7,8
Gambar 4.4. mekanisme antibakteri minyak atsiri
Sumber : Sara Burt. 2004.
Secara umum senyawa fenol dan derivatnya memiliki aktivitas antibakteri
disebabkan perbedaan yang signifikan pada lapisan luar bakteri, lapisan hidrofilik
yang kaya akan polisakarida pada membran luar bakteri Gram negatif memiliki
fungsi pelindung terhadap penetrasi berbagai molekul antibiotik, sedangkan
ruangan periplasma yang tidak dimiliki bakteri Gram positif mengandung
beberapa enzim yang bisa merusak zat ekstraseluler.13,27
Kontrol negatif pada penelitian ini tidak menimbulkan daya hambat
terhadap pertumbuhan Streptococcus viridans menunjukkan bahwa pelarut etanol tidak mempengaruhi efek antibakteri ekstrak daun sirih hijau, sedangkan kontrol
positif berupa amoksilin menunjukkan respon hambatan kuat terhadap
pertumbuhan Streptococcus viridans, amoksilin merupakan obat antibakteri golongan beta-laktam dengan spectrum luas, sehingga dapat digunakan untuk
menghambat pertumbuhan bakteri Gram positif dan Gram negatif melalui
penghambatan sintesis peptidoglikan sehingga dinding bakteri tidak terbentuk
dengan baik.29
Selain berfungsi sebagai antibakteri terhadap Streptococcus viridans, daun sirih hijau juga memiliki aktifitas antibakteri terhadap beberapa bakteri lainnya.
Seila (2012) menyatakan bahwa ekstrak etanol daun sirih hijau dapat menghambat
pertumbuhan Staphylococcus aureus dengan efektifitas kuat,19 menurut Anang (2007) ekstrak dimetil sulfoksida daun sirih hijau memiliki pengaruh terhadap
pertumbuhan Escherichia coli,24 penelitian yang dilakukan oleh Mahfuzul (2011) membuktikan bahwa ekstrak etanol daun sirih hijau memiliki aktifitas antibakteri
terhadap Vibrio cholerae dan Shigella dysenteriae.6
Uraian diatas membuktikan bahwa daun sirih hijau dapat digunakan
sebagai alternatif zat antibakteri, terutama dalam menghambat pertumbuhan
Streptococcus viridans dengan kategori hambatan lemah sampai kuat. Hambatan Penelitian
Bakteri Streptococcus viridans yang tidak bisa bertahan hidup dalam waktu yang cukup lama.
Penggunaan Agar Darah yang merupakan media pertumbuhan yang baik
bagi berbagai bakteri, sehingga memperbesar kemungkinan kontaminasi.
28
BAB V
SIMPULAN DAN SARAN
5.1.Simpulan
Berdasarkan hasil penelitian dan analisis data statistik didapatkan
kesimpulan berikut :
1. Pada pengukuran zona hambat didapatkan hasil sebagai berikut : Pada
konsentrasi ekstrak daun sirih hijau 20% didapatkan rata-rata zona hambat
11,67 mm. Pada konsentrasi ekstrak daun sirih hijau 30% didapatkan
rata-rata zona hambat 14 mm. Pada konsentrasi ekstrak daun sirih hijau 50%
didapatkan rata-rata zona hambat 17,67 mm. Pada konsentrasi ekstrak
daun sirih hijau 75% didapatkan rata-rata zona hambat 19 mm. Pada
konsentrasi ekstrak daun sirih hijau 100% didapatkan rata-rata zona
hambat 21,33 mm.
2. Ekstrak daun sirih hijau 20% dan 30% memiliki respon hambatan
pertumbuhan lemah terhadap Streptococcus viridans, ekstrak daun sirih hijau 50% dan 75% memiliki respon hambatan pertumbuhan sedang
terhadap Streptococcus viridans, ekstrak daun sirih hijau 100% memiliki respon hambatan pertumbuhan kuat terhadap Streptococcus viridans.
5.2.Saran
Setelah dilakukannya penelitian ini, maka disarankan untuk penelitian
selanjutnya :
1. Dapat melakukan uji aktivitas antibakteri ekstrak daun sirih hijau
terhadap Streptococcus viridans secara in-vivo.
2. Dapat melakukan uji aktivitas antibakteri ekstrak daun sirih hijau
terhadap Streptococcus viridans dengan menggunakan metode lain. 3. Dapat melakukan uji aktivitas antibakteri ekstrak daun sirih hijau
DAFTAR PUSTAKA
1. Pradhan, D. et al. Golden Heart of the Nature: Piper betle L. Journal of Pharmacognosy and Phytochemistry. Vol.1 No. 6 : 2013. hal. 147-167.
2. Bissa, Syarad. Songara, Dimple. Bohra A. Tradition in oral hygiene : Chewing of betel (Piper betle L.) leaves. Current science, Vol. 92, No. 1. 2007. hal. 26-28.
3. Kumar, Nikhil. Misra, Pragya. Dube, Anuradha. Piper betle Linn. a maligned Pan-Asiatic plant with an array of pharmacological activities and prospects for drug discovery. Current Science. Vol. 99, No. 7. 2010. hal. 922-932. 4. Hoque, Mahfuzul. Ratilla, Shemona. et al. Antibacterial Activity of Ethanol
Extract of Betel Leaf (Piper betle L.) Against Some Food Borne Pathogens. Bangladesh J Microbiol. Volume 28, Number 2 : 2011. hal. 58-63.
5. Damayanti R, Mulyono. Khasiat dan Manfaat Daun Sirih : Obat Mujarab dari Masa ke Masa. Jakarta : Agro Media Pustaka. 2005.
6. Dalimarth, Setiawan. Atlas Tumbuhan Obat Indoneia, jilid 4. Jakarta : puspa swara. 2006.
7. KP, Devi. SA, Nisa. R, Sakhtivel. Eugenol (an essential oil of clove) acts as an antibacterial agent against Salmonella typhi by disrupting the cellular membran. Journal of ethnopharmacology. 2010.
http://www.ncbi.nlm.nih.gov/pubmed/20435121. diakses pada 30/08/2013
pukul : 6.56 WIB.
8. McDonell, Gerald. Antiseptics and Disinfectants: Activity, Action and Resistance. Clinical microbiology review. Vol. 12 No. 1. 1999.
9. A. Duke, James. Handbook of medicinal herbs, second edition. London : CRC press. 2002. hal. 73.
10. Kuruvilla, Lincu. Studies on dental caries bacterial flora and its control by phyto derivatives. Dept. of Botany , S.B. College. 2012.
11.Pratiwi, Lidya. Perbandingan uji aktivitas dan mekanisme penghambatan antara minyak atsiri daun sirih (piper betle, linn.) dengan ekstrak etanol daun sirih terhadap beberapa bakteri gram positif. Skripsi. Jurusan Farmasi FKIK UIN Jakarta, Tangerang. 2010.
13.Brooks GF, Butel JS, Carroll KC, Morse SA. Jawetz, Melnick, & Adelberg's
Medical Microbiology. 24th Ed. USA : Mc Graw Hill. 2007. hal. 327-33. 14.Refoua, Y. A Study of Streptococcus viridans in The Maxillofacial Region.
2005.
15.Pratiwi, S. T. Mikrobiologi Farmasi. Jakarta: Penerbit Airlangga. 2008. hal. 188-191.
16.Departemen Kesehatan Republic Indonesia. Materia Medika Indonesia Jilid 4. Jakarta : Departemen Kesehatan Republic Indonesia. 1980. hal. 92-98.
17.Arambewela, S.LR. et al. Investigations on Piper betle grown in Sri Lanka.
Sri lanka : 2011
http://www.phcogrev.com/article.asp?issn=09737847;year=2011;volume=5;is sue=10;spage=159;epage=163;aulast=Arambewela. Diakses pada 2/9/2013 pukul 08:19 WIB.
18.Inayatullah, Seila. Efek Ekstrak Daun Sirih Hijau (Piper betle L.) Terhadap Pertumbuhan Bakteri Staphylococcus aureus. Skripsi. Pendidikan Dokter FKIK UIN, Jakarta. 2012.
19.Sjahrurachman, Agus dkk. Buku Ajar Mikrobiologi Kedokteran Edisi Revisi. Jakarta : Bina aksara. 1993.
20.Kayser. Color atlas of medical microbiology. Thieme. 2005.
21.Hermawan, A., Hana, W., dan Wiwiek, T. Pengaruh Ekstrak Daun Sirih (Piper betle L.) Terhadap Pertumbuhan Staphylococcus aureus dan Escherichia coli dengan Metode Difusi Disk. Skripsi : Universitas Airlangga. 2007.
22.Greenwood. Antibiotic susceptibility (sensitivity) test, antimicrobial and chemotherapy. USA: Mc Graw Hill Company. 1995.
23.Arthur. LB. Procedur for testing in agar media Dalam: Antibiotic in Laboratory Medicine. Williams and Wilkins, Baltimore. 1980. hal. 1-22. 24.Gan Gunawan, Sulistia. Farmakologi dan terapi edisi 5. Jakarta : Departemen
farmakologi dan terapeutik fakultas kedokteran universitas Indonesia. 2007.
25.Dahlan, M. Sopiyudin. Statistik untuk kedokteran dan kesehatan edisi 4. Jakarta : salemba medika. 2009.
27.Cetin-Karaca, Hayriye. Evaluation Of Natural Antimicrobial Phenolic Compounds Against Foodborne Pathogens. Tesis. University of Kentucky, USA. 2011.
28.Burt, sara. Essential oils: their antibacterial properties and potential applications in foods—a review. Elsevier : International Journal of Food Microbiology 94. 2004. hal. 223-253.
29.Brunton, L. Laurance. Lazo, John S. Parker, Keith L. Goodman & Gilman’s
Lampiran 3 (Diameter zona hambat pada uji antibakteri ekstrak sirih hijau)
A B C Rata-rata Standar
Deviasi
Kontrol (-) 0 0 0
Konsentrasi 20% . .
Konsentrasi 30%
Konsentrasi 50% . .
Konsentrasi 75%
Konsentrasi 100% . .
Lampiran 4
(Hasil uji data statistik)
1. Hasil uji normalitas
Tests of Normality
Kolmogorov-Smirnova Shapiro-Wilk
Statistic Df Sig. Statistic df Sig.
Tranz_zon .146 18 .200* .943 18 .329
a. Lilliefors Significance Correction
*. This is a lower bound of the true significance.
2. Hasil uji varian
Test of Homogeneity of Variances
Tranz_zon
Levene Statistic df1 df2 Sig.
2.442 5 12 .095
3. Hasil uji One way ANOVA
ANOVA
Tranz_zon
Sum of Squares df Mean Square F Sig.
Between Groups .225 5 .045 187.626 .000
Within Groups .003 12 .000
4. Hasil uji Post hoc
Multiple Comparisons
Tranz_zon
LSD
(I) Konsentrasi (J) Konsentrasi
Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval
Lower Bound Upper Bound
Kontrol (+) ekstrak 20% .33703* .01264 .000 .3095 .3646
ekstrak 30% .25749* .01264 .000 .2300 .2850
ekstrak 50% .15662* .01264 .000 .1291 .1842
ekstrak 75% .12527* .01264 .000 .0977 .1528
ekstrak 100% .07466* .01264 .000 .0471 .1022
Lampiran 5 (Alat dan Bahan)
Alat penelitian Inkubator Vortex
Lampiran 6 (Riwayat Hidup Penulis)
DAFTAR RIWAYAT HIDUP
Nama : Angga Maulana Ibrahim
Tempat, Tanggal Lahir : Lebak, 19 oktober 1992
Alamat : Pari RT 01/01, Mandalawangi, Pandeglang, Banten
Email : [email protected]
No.Telpon : 085215341033
Riwayat Pendidikan
1998-2000 : SDN Gunung Kencana 1
2000-2004 : SDN Mandalawangi 1
2004-2007 : SMP Daar el Falaah
2007-2010 : SMAN CMBBS
2010-sekarang : Program Studi Pendidikan Dokter, FKIK Universitas