TUGAS AKHIR
Diajukan Guna Memenuhi Persyaratan Mencapai Derajat Strata-1 Fakultas Teknik Program Studi Teknik Mesin
Universitas Muhammadiyah Yogyakarta
Disusun oleh:
Wahono Bambang Subrimobdi 20120130023
PROGRAM STUDI S.1 TEKNIK MESIN FAKULTAS TEKNIK UNIVERSITAS MUHAMMADIYAH YOGYAKARTA
TUGAS AKHIR
Diajukan Guna Memenuhi Persyaratan Mencapai Derajat Strata-1 Fakultas Teknik Program Studi Teknik Mesin
Universitas Muhammadiyah Yogyakarta
Disusun oleh:
Wahono Bambang Subrimobdi 20120130023
PROGRAM STUDI S.1 TEKNIK MESIN FAKULTAS TEKNIK UNIVERSITAS MUHAMMADIYAH YOGYAKARTA
PERNYATAAN
Saya menyatakan dengan sesungguhnya bahwa skripsi ini adalah asli hasil karya saya dan tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di Perguruan Tinggi dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah ditulis atau dipublikasikan oleh orang lain, kecuali yang secara tertulis disebutkan sumbernya dalam naskah dan dalam
daftar pustaka.
Yogyakarta,
Motto
“Dasar
dari kesuksesan besar terletak pada tekad
dan kemauan yang besar serta diiringi sikap
tidak mudah putus
asa”. (
Wahono)
“
Kita boleh berusaha dan berencana, namun
biarkan Allah yang menentukannya
”.
(Wahono)
“Teruslah mencoba dan belajarlah dari kesalahan,
dengan mengetahui kesalahan tersebut maka kita
tidak akan mengulanginya kesalahan untuk yang
kedua kalinya
”. (
Wahono)
“Ketergesaan
dalam setiap usaha membawa
PERSEMBAHAN
Bismillahirohmanirohim, dengan menyebut nama Allah SWT yang Maha Pengasih, Maha Penyayang, serta Maha Pemberi Nikmat, penulis mempersembahkan skripsi ini untuk :
1. Kedua orang tua yang telah memberikan kasih sayang, do’a, motivasi, dan dukungan.
2. Kedua dosen pembimbing tugas akhir, bapak Wahyudi, S.T., M.T, dan bapak Novi Caroko, S.T., M.Eng, yang telah memberi saran dan masukan selama pelaksanaan tugas akhir.
KATA PENGANTAR
Assalamualaikum warohmatullahi wabarokatuh,
Puji syukur kehadirat Allah SWT yang tiada hentinya memberikan rahmat, nikmat, dan hidayah-Nya kepada penulis sehingga pelaksanaan laporan tugas akhir ini dapat terselesaikan dengan baik. Solawat serta salam semoga selalu tercurahkan kepada Nabi Muhammad SAW yang telah menuntun kita dari jaman jahiliyah ke jaman terang benderang seperti yang saat ini yang kita rasakan.
Penelitian ini bertujuan untuk mengetahui jumlah yeast dan waktu optimal dalam fermentasi nira siwalan menjadi bioetanol, sehingga didapatkan hasil yang maksimal. Parameter yang dilakukan adalah pengukuran kadar gula, keasaman, volume etanol, dan kadar etanol. Dari penelitian yang dilakukan, didapatkan hasil bahwa yeast optimal sebanyak 0,5 gram dan waktu optimal adalah 48 jam.
Laporan tugas akhir ini tidak akan terselesaikan dengan baik tanpa adanya
bantuan dari berbagai pihak. Penulis mengucapkan terimakasih kepada :
1. Kedua orang tua yang telah memberi dukungan, pengertian, semangat, dan
doa.
2. Bapak Novi Caroko, S.T., M.Eng., selaku Kepala Program Studi Teknik Mesin Universitas Muhammadiyah Yogyakarta.
3. Bapak Wahyudi, S.T., M.T., selaku dosen pembimbing I yang telah bersedia memberikan bimbingan dan saran yang sangat bermanfaat.
4. Bapak Novi Caroko, S.T., M.Eng., selaku dosen pembimbing II yang telah bersedia memberikan bimbingan dan saran yang sangat bermanfaat.
5. Bapak Ir. Sudarja, M.T., selaku dosen penguji yang telah bersedia memberikan kritik dan saran dalam perbaikan laporan tugas akhir.
6. Mulyadi dan Sugini yang telah memberi dukungan, semangat, dan doa.
8. M. Diyaudin, Wiby Santoso, Roy Limey, Syaiful Husein selaku teman kontrakan yang telah banyak membantu penyelesaian tugas akhir.
9. Khairul Anam, Dimas Niko, Ariq Diky Pratama, Pandu Birawanto, Ahmad Zainal, Pungky Wijanarko, Basroni Mahfud, Galuh Yudha, dan seluruh teman
– teman kelas teknik mesin angkatan 2012 yang telah banyak memberi bantuan dan masukan dalam penyelesaian tugas akhir.
10.Arif Hadi Satria, Irfan Winindya Putra, Cendy, Arifin dan seluruh teman – teman yang telah banyak memberi semangat dan doa dalam penyelesaian
tugas akhir.
Kritik dan saran dari pembaca sangat diharapkan oleh penulis demi perbaikan laporan ini, semoga laporan tugas akhir ini dapat bermanfaat bagi penyusun dan teman-teman mahasiswa yang lain.
Wassalamualaikum Warohmatullahi Wabarokatuh.
Yogyakarta, 2016
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
HALAMAN PERNYATAAN ... iii
HALAMAN MOTTO ... iv
HALAMAN PERSEMBAHAN ... v
KATA PENGANTAR ... vii
DAFTAR ISI ... viii
DAFTAR GAMBAR ... xi
DAFTAR TABEL ... xiii
DAFTAR LAMPIRAN ... xiv
INTISARI ... xv
ABSTRACK ... xvi
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Rumusan Masalah ... 3
1.3. Batasan Masalah... 3
1.4. Tujuan Penelitian ... 4
1.5. Manfaat Penelitian ... 4
1.6. Sistematika Penulisan ... 4
BAB II LANDASAN TEORI ... 7
2.1. Tinjauan Pustaka ... 7
2.2.1. Pengertian Bioetanol ... 8
2.2.2. Prospek Nira di Indonesia ... 11
2.2.3. Pengertian Fermentasi ... 15
2.2.4. Pengertian Distilasi ... 21
2.2.4.1. Jenis-Jenis Distilasi ... 22
2.2.4.2. Proses Distilasi Bioetanol ... 24
BAB III METODE PENELITIAN... 26
3.1. Diagram Alir Penelitian ... 26
3.2. Perencanaan Penelitian... 27
3.3. Alat Penelitian ... 28
3.4. Bahan Penelitian... 38
3.5. Waktu danTempat Penelitian ... 43
3.6. Tahap Pembuatan Bioetanol ... 44
3.6.1. Fermentasi ... 44
3.6.2. Distilasi ... 46
3.7. Cara Pengujian Volume dan Kadar Etanol ... 47
BAB IV Hasil dan Pembahasan ... 49
4.1. Hasil Pengujian Metode Variasi Jumlah Yeast ... 49
4.1.1. Pengujian Kadar Gula ... 51
4.1.2. Pengujian Derajat Keasaman ... 54
4.1.3. Pengujian Volume Etanol Distilasi ... 57
4.1.4. Pengujian Kadar Etanol Distilasi ... 59
4.2. Hasil Pengujian Metode Variasi Waktu ... 61
4.2.1. Pengujian Kadar Gula ... 61
4.2.3. Pengujian Volume Etanol Distilasi ... 66
4.2.4. Pengujian Kadar Etanol Distilasi ... 68
BAB V PENUTUP ... 71
5.1. Kesimpulan ... 71
5.2. Saran ... 71
DAFTAR PUSTAKA
DAFTAR GAMBAR
Gambar 2.1. Alat Distilasi Sederhana ... 23
Gambar 3.1. Diagram Alir Penelitian ... 26
Gambar 3.2. Brix Refractometer ... 28
Gambar 3.3. pH Meter Digital ... 28
Gambar 3.4. Termometer ... 30
Gambar 3.5. Timbangan Digital ... 30
Gambar 3.6. Refraktometer Alkohol ... 31
Gambar 3.7. Fermentor ... 32
Gambar 3.8. Alat Distilasi ... 32
Gambar 3.9. Pengaduk ... 33
Gambar 3.10. Aluminum Foil ... 33
Gambar 3.11. Gelas Ukur... 34
Gambar 3.12. Erlenmeyer ... 35
Gambar 3.13. Jerigen ... 35
Gambar 3.14. Autoclave ... 36
Gambar 3.15. Pipet ... 37
Gambar 3.16. Alat Pencatat ... 37
Gambar 3.17. Stopwatch ... 38
Gambar 3.18. Nira Siwalan ... 39
Gambar 3.19. HCL ... 40
Gambar 3.20. NaOH ... 40
Gambar 3.21. Yeast Saccharomyces Cerevisiae ... 41
Gambar 3.22. Urea ... 42
Gambar 3.23. NPK ... 42
Gambar 3.25. Diagram Alir Proses Fermentasi ... 46
Gambar 3.26. Diagram Alir Proses Distilasi ... 47
Gambar 4.1. Broth Fermentasi Nira Siwalan dengan Variasi Yeast ... 50
Gambar 4.2. Pengukuran Kadar Gula ... 52
Gambar 4.3. Grafik Kadar Gula ... 53
Gambar 4.4. Pengukuran Derajat Keasaman ... 54
Gambar 4.5. Grafik Derajat Keasaman ... 56
Gambar 4.6. Pengukuran Volume Etanol Distilasi ... 57
Gambar 4.7. Grafik Volume Etanol Distilasi ... 58
Gambar 4.8. Pengukuran Kadar Etanol... 59
Gambar 4.9. Grafik Kadar Etanol Hasil Distilasi ... 60
Gambar 4.10. Pengukuran Kadar Gula ... 62
Gambar 4.11. Grafik Kadar Gula ... 63
Gambar 4.12. Pengukuran Derajat Keasaman ... 64
Gambar 4.13. Grafik Derajat Keasaman ... 65
Gambar 4.14. Pengukuran Volume Etanol Distilasi ... 67
Gambar 4.14. Grafik Volume Etanol Distilasi ... 68
Gambar 4.15. Pengukuran Kadar Etanol... 69
DAFTAR TABEL
Tabel 2.1. Sifat Fisika-Kimia Etanol ... 9
Tabel 2.2. Klasifikasi Tanaman Siwalan ... 13
Tabel 2.3. Kandungan Nira Siwalan ... 13
Tabel 2.4. Klasifikasi Saccharomyces ... 18
Tabel 4.1. Data Rata – Rata Pengukuran Kadar Gula ... 53
Tabel 4.2. Data Rata – Rata Pengukuran Derajat Keasaman... 55
Tabel 4.3. Data Rata – Rata Pengukuran Volume Etanol ... 58
Tabel 4.4. Data Rata – Rata Pengukuran Kadar Etanol ... 60
Tabel 4.5. Data Rata – Rata Pengukuran Kadar Gula ... 63
Tabel 4.6. Data Rata – Rata Pengukuran Derajat Keasaman... 65
Tabel 4.7. Data Rata – Rata Pengukuran Volume Etanol ... 67
DAFTAR LAMPIRAN
Lampiran 1 Data Pengukuran Gula Fermentasi Variasi Jumlah Yeast
Lampiran 2 Data Pengukuran Keasaman, Volume, dan Kadar Etanol Fermentasi Variasi Jumlah Yeast
Lampiran 3 Data Pengukuran Gula Fermentasi Variasi Waktu
Lampiran 4 Data Pengukuran Keasaman, Volume, dan Kadar Etanol Fermentasi Variasi Waktu
Wahono Bambang Subrimobdi 20120130023
INTISARI
Meningkatnya jumlah penduduk dunia akan membuat kebutuhan energi negara - negara di dunia meningkat termasuk Indonesia. Ketersediaan minyak bumi Indonesia semakin menipis sehingga untuk memenuhi kebutuhan minyak dalam negeri, Indonesia harus impor minyak dari negara lain. Karena menipisnya cadangan energi di Indonesia, diperlukan energi baru dan terbarukan yang mampu memenuhi kebutuhan energi dalam negeri. Salah satu energi baru tersebut yaitu bioetanol. Bioetanol merupakan penyebutan alkohol atau etanol yang bersumber dari bahan hayati, salah satunya adalah nira siwalan. Nira yang semula hanya dimanfaatkan sebagai minuman dan gula. Jika digunakan sebagai bahan bioetanol, maka nilai jualnya akan meningkat. Tujuan dari penelitian ini adalah untuk mengetahui jumlah yeast dan waktu fermentasi optimal dalam menghasilkan volume dan kadar etanol tertinggi.
Metode yang digunakan adalah fermentasi dengan menggunakan saccharomyces cerevisiae sebagai yeast penghasil etanol dan akan diukur penurunan gula, derajat keasaman, volume etanol, dan kadar etanol sebagai parameter penelitian. Variabel yang digunakan adalah variasi jumlah yeast (0,5; 1; 1,5; dan 2 gram) dan variasi waktu fermentasi (24, 48, 72, dan 96 jam). Pengukuran gula reduksi dilakukan dengan brix refractometer, pengukuran derajat keasaman dilakukan dengan pH meter, pengukuran volume etanol distilasi dilakukan dengan gelas ukur, dan pengukuran kadar etanol dilakukan dengan refraktometer alkohol.
Hasil penelitian menunjukkan bahwa jumlah yeast optimal untuk menghasilkan volume dan kadar etanol tertinggi pada jumlah yeast 0,5 gram sebanyak 7,63 ml dan kadar etanol 52, 7 %. Waktu fermentasi optimal untuk menghasilkan volume dan kadar etanol tertinggi adalah pada waktu fermentasi 48 jam sebanyak 6,33 ml dan kadar etanol 51,33 %.
Wahono Bambang Subrimobdi 20120130023
ABSTRACT
The increasing world’s population will make the energy needs consumption in the world increase, including Indonesia. The availability of petroleum in Indonesia so that to fulfill the petroleum need in this country, Indonesia should import oil from other countries. Because Indonesian’s depleation of energy reserves, it is needed for new and renewable energy that is able to meet domestic energy needs. One of new energy is bioethanol. Bioethanol is addressing of alcohol or etanol derived from biological materials; one of which material it is nira siwalan . Sap was originally only used as drink and sugar. If it is used as bioethanol production will increase the sale value. The purpose of this research was to determine the amount of yeast and optimal fermentation time in generating the highest volume and etanol content.
The method used is fermentation using yeast saccharomyces cerevsiae as yeast a producer of ethanol and it was measured the decrease sugar, acidity, etanol volume, and etanol content as parameter study. The variables used were variations of yeast amount (0,5;1,0;1,5;2,0 grams) and variation of fermentation time (24,48,72, and 96 hours). Sugar reduction measure ment was done by use brix refractometer, degrees of acidity was measured using a pH meter, distillation volume of etanol was measured using the measuring cup, and ethanol was measured using a alcohol refractometer.
The results is that the optimal amount of yeast to produce the highest volume and concentration of ethanol in yeast of 0,5 gram as much as 7,63 ml and ethanol content of 52,7%. Optimal fermentation time to produce the highest volume and concentration of ethanol in the fermentation time of 48 hours as much as 6,33 ml and ethanol content of 51,33%.
1.1. Latar Belakang
Saat ini pertumbuhan penduduk dunia semakin meningkat. Dunia yang kita tempati terdiri atas 195 negara dengan jumlah penduduk sebanyak 7.256.490.011 jiwa (CIA World Factbook, 2015). Sementara Indonesia sendiri berada di peringkat empat jumlah penduduk terbesar yaitu sebanyak 255.993.674 jiwa atau sekitar 3,5 persen dari jumlah penduduk dunia. Meningkatnya jumlah penduduk dunia membuat kebutuhan energi negara-negara di dunia meningkat. Meningkatnya kebutuhan energi negara-negara dunia ini justru berbanding terbalik dengan cadangan energi dunia (energi fosil) yang semakin menipis termasuk Indonesia. Cadangan minyak Indonesia sudah mulai berkurang dan untuk memenuhi kebutuhan minyak harus impor minyak dari luar negeri. Menurut Pusat Informasi Energi dan Daya Mineral (2004), Indonesia mulai iportir minyak pada tahun 2004. Konsumsi BBM dalam negeri sudah lama meningkat dari tahun ke tahun. Menurut Megawati (2015), kebutuhan premium terus meningkat dari tahun 2008 sebesar 19.600 dan pada tahun 2009 meningkat menjadi 21.000 kL atau kenaikannya sebesar 7 persen setahun. Jika kenaikannya 7
persen setahun, maka setiap 10 tahun akan meningkat dua kali. Karena menipisnya cadangan minyak indonesia diperlukan adanya energi baru dan
terbarukan yang mampu memenuhi kebutuhan energi dalam negeri. Salah satu energi baru tersebut yaitu bioetanol yang merupakan kategori dari bioamasa.
Bioetanol bersumber dari bahan hayati yang pada awalnya dibuat dari gula dan pati yang diperoleh dari tebu, nira aren, jagung, singkong, dan lain-lain. Gula dari berbagai bahan baku ini dapat langsung difermentasi oleh khamir untuk menjadi etanol (Megawati, 2015). Bioetanol hasil fermentasi memiliki kadar alkohol rendah, untuk mendapatkan etanol dengan kadar alkohol lebih tinggi dapat dilakukan proses berikutnya yaitu distilasi, dehidrasi dan adsorbsi. Bioetanol merupakan bahan kimia ramah lingkungan yang dapat digunakan dalam banyak hal. Bioetanol dapat digunakan sebagai bahan bakar kendaraan, namun
dengan kemurnian etanol yang tinggi. Menurut Nurdyastuti (2016), bioetanol yang dimanfaatkan sebagai campuran bahan bakar kendaraan harus betul-betul kering agar tidak korosi sehingga bioetanol harus mempunyai kemurnian diatas 99,5 persen. Selain digunakan sebagai bahan bakar kendaraan, bioetanol juga dapat digunakan sebagai bahan baku kegiatan farmasi, bahan baku industri, kosmetik, parfum, bahan dasar turunan alkohol, minuman, dan lain-lain.
Nira merupakan bahan baku pembuatan bioetanol yang memiliki potensi besar. Nira dapat diambil dari berbagai jenis pohon pinang – pinangan seperti lontar (siwalan), aren, kelapa, nipah dan lain sebagainya. Alasan pembuatan bioetanol dari nira lontar karena pohon lontar di Indonesia seperti daerah dataran Jawa Tengah bagian timur ( Pati dan Rembang) dan Jawa Timur masih sangat melimpah namun belum termanfaatkan dengan baik. Nira siwalan kebanyakan masyarakat hanya dimanfaatkan sebagai minuman dan gula,. Untuk menaikkan nilai ekonomi nira siwalan dapat dijadikann sebagai bahan produksi bioetanol. Pohon siwalan atau lontar (Borassus flabellifer) adalah sejenis palma (pinang – pinangan) yang tumbuh di Asia Tenggara dan Asia Selatan. Di Indonesia, pohon siwalan selain tumbuh di Jawa Tengah dan Jawa Timur juga tumbuh di Madura, Bali, Nusa Tenggara Barat, Nusa tenggara Timur, dan Sulawesi. Nira didapat dengan cara disadap dari tongkol bunga untuk mendapatkan air nira (legen) yang dapat langsung diminum, difermentasi menjadi tuak, atau proses fermentasi
Dalam proses fermentasi bioetnol, waktu fermentasi sangat berpengaruh dalam menghasilkan etanol. Yeast membutuhkan waktu untuk mengubah gula menjadi etanol. Menurut Putra dan Amran (2009), waktu yang dibutuhkan yeast
untuk mengubah gula menjadi etanol berbeda – beda , tergantung kadar gula dan
yeast yang diberikan. Dengan demikian waktu terbaik yang dibutuhkan untuk fermentasi setiap jenis bahan berbeda – beda. Banyaknya jumlah yeast yang diberikan akan mempebanyak jumlah mikroba. Mikroba berperan untuk mengubah gula menjadi etanol. Semakin banyak Yeast yang diberikan maka kemungkinan waktu fermentasi lebih cepat. Oleh sebab itu perlu dilakukan penelitian mengenai jumlah yeast dan waktu fermentasi, sehingga didapatkan etanol yang optimal.
1.2. Rumusan Masalah
Berdasarkan uraian latar belakang di atas, didapatkan rumusan masalah yang
akan dicari penyelesaian masalahnya baik pembahasan menurut analisa maupun teori –teori yang menjadi acuan. Adapun rumusan masalah adalah apa pengaruh variasi jumlah yeast dan variasi waktu fermentasi terhadap penurunan gula, derajat keasaman (pH), volume dan kadar etanol yang dihasilkan.
1.3. Batasan Masalah
Dalam pembuatan dan penelitian bioetanol ini difokuskan pada kajian dan
analisa sebagai berikut:
a. Bahan penelitian produksi bioetanol adalah bioetanol generasi pertama menggunakan nira siwalan 250 ml.
b. Fermentasi dilakukan dengan penambahan nutrisi (urea 0,1 g/250 ml dan NPK 0,125 g/ 250 ml).
c. Tidak mengamati tentang pertumbuhan mikroba selama fermentasi
e. Pembuatan bioetanol dilakukan hingga proses distilasi menggunakan alat distilasi sederhana.
f. Tidak menganalisis tentang asam – asam organik yang dihasilkan selama fermentasi.
g. Pengujian yang dilakukan adalah pengujian kadar gula, derajat keasaman (pH), volume etanol hasil distilasi, dan kadar etanol.
1.4. Tujuan Penelitian
Tujuan dari penelitian ini adalah sebagai berikut :
a. Mengetahui jumlah yeast paling optimal antara 0,5 g; 1 g; 1,5 g; dan 2 g dengan bahan baku nira siwalan 250 ml sehingga menghasilkan volume dan kadar etanol tertinggi.
b. Mengetahui waktu fermentasi paling optimal antara 24 jam, 48 jam, 72 jam, dan 96 jam dengan bahan baku nira siwalan 250 ml sehingga menghasilkan
volume dan kadar etanol tertinggi.
1.5. Manfaat Penelitian
Manfaat dari penelitian ini adalah sebagai berikut :
a. Didapatkannya metode paling efektif dalam proses fermentasi nira siwalan menjadi etanol.
b. Memberikan pengalaman mahasiswa dalam pembuatan bioetanol nira siwalan
c. Memperkaya khasanah ilmu pengetahuan dalam pengembangan bioetanol di Indonesia.
1.6. Sistematika Penyusunan
BAB I PENDAHULUAN
Pendahuluan menguraikan tentang pokok-pokok dalam penulisan tugas akhir yang meliputi latar belakang, rumusan masalah, batasan masalah,
tujuan penelitian, manfaat, dan sistematika penyusunan.
BAB II LANDASAN TEORI
Landasan teori menguraikan tentang studi literatur dan dasar teori. Studi literatur bersumber dari acuan pustaka maupun analisis sendiri, dan disertai pertimbangan yang mendasar. Dasar teori diawali dengan teori sebelumnya yang menjelaskan tentang bioetanol, bahan baku, dan proses selama pembuatan bioetanol.
BAB III METODE PENELITIAN
Metode penelitian berisi tentang waktu dan tempat penelitian, diagram alir penelitian, persiapan peralatan dan bahan, serta pembahasan tentang proses pembuatan bioetanol dari awal sampai akhir.
BAB IV HASIL PENELITIAN DAN PEMBAHASAN
Hasil penelitian dan pembahasan menguraikan tentang hasil penelitian
yang telah dilakukan dan menganalisis bioetanol yang dihasilkan.
BAB V PENUTUP
DAFTAR PUSTAKA
Daftar pustaka membahas mengenai penunjukan alamat ataupun identitas studi literatur yang digunakan dalam mendukung selama penyusunan dan penelitian tugas akhir.
LAMPIRAN
2.1. Studi Literatur
Nira diperoleh dengan menyadap tandan bunga jantan yang mulai mekar dan menghamburkan serbuk sari yang berwarna kuning. Tandan ini mula-mula dimemarkan dengan memukul-mukulnya selama beberapa hari, hingga keluar cairan dari dalamnya. Tandan kemudian dipotong dan di ujungnya digantungkan tahang bambu untuk menampung cairan yang menetes (Rasyid, 2012).
Untuk mendapatkan bioethanol yang sesuai standar, disarankan untuk melakukan prosedur penyimpanan bahan baku dengan baik, jangan biarkan nira siwalan terbuka bebas sehingga terkontaminasi mikroba lain (Putra dan Amran, 2009).
Waktu fermentasi optimum nira nipah pada keasaman (pH) 4,5 adalah pada waktu fermentasi 36 jam, keasaman 5,0 pada waktu fermentasi 36 jam dan keasaman 5,5 pada waktu fermentasi 24 dan 48 jam, dengan menghasilkan konsentrasi bioetanol tertinggi masing-masing keasaman (pH) yaitu 14%, 12% dan 7% (v/v). Awalnya semakin lama waktu fermentasi, konsentrasi bioetanol yang dihasilkan juga semakin tinggi, akan tetapi setelah kondisi optimum tercapai, konsentrasi bioetanol yang diperoleh cenderung mengalami penurunan. Adanya
penurunan konsentrasi bioetanol disebabkan karena bioetanol yang dihasilkan terkonversi menjadi asam-asam organik seperti asam asetat, asam cuka dan ester (Chairul dan Silvia, 2013).
Fermentasi pada keasaman (pH) 4,5 menghasilkan konsentrasi bioetanol yang tertinggi. Hal ini terjadi karena pada keasaman 4,5 adaptasi yeast lebih rendah dan aktivitas fermentasinya juga meningkat, serta berpengaruh pada pembentukan produk samping, dimana pada keasaman tinggi konsentrasi gliserol meningkat. Sedangkan pada keasaman dibawah 4,5 aktifitas enzim akan terhambat sehingga kemampuan mikroba untuk mengurai gula menjadi bioetanol semakin rendah (Chairul dan Sivia, 2013).
Menurut Putra dan Amran (2009), saccharomycess cereviseae dapat tumbuh baik pada range 3 - 6, namun apabila pH lebih kecil dari 3 maka proses fermentasi akan berkurang kecepatannya derajat keasaman (pH) yang paling optimum pada 4,3 - 4,7. Pada pH yang lebih tinggi, adaptasi yeast lebih rendah dan aktivitas fermentasinya juga meningkat, tetapi ternyata pengaruh juga pada pembentukan produk samping sebagai contoh pada keasaman tinggi, konsentrasi gliserin meningkat juga.
Kondisi yang baik selama fermentasi adalah kondisi yang tertutup atau lebih cendrung anaerob dengan dibatasi oleh udara yang tersedia sedikit ± 10% volume yaitu dari sisa rongga ruang fermentasi dalam tangki. Sehingga dalam proses fermentasi oksigen hanya dibutuhkan sedikit (Hadi dkk, 2013).
2.2. Dasar Teori
2.2.1. Pengertian Bioetanol
Bioetanol adalah senyawa alkohol dengan gugus hidroksil (OH), dua atom
karbon (C), dengan rumus kimia C2H5OH yang dibuat dengan cara fermentasi gula menggunakan khamir. Rumus kimia pada saat fermentasi adalah sebagai berikut.
C
Senyawa tersebut juga dapat diperoleh dengan cara sintetik berbahan etilena (CH2=CH2), yang lebih sering disebut etanol saja. Tahap pertama, etilena direaksikan dengan asam sulfat (H2SO4) dalam sebuah reaktor berbentuk kolom untuk menghasilkan senyawa monosulfat. Rumus kimia secara sintetik adalah sebagai berikut.
CH2 = CH2 + H2SO4→ CH3CH2OSO3H ……….(2.2) Tahap kedua, senyawa monosulfat dihidrolisis sehingga gugusnya terpisah dan masing-masing bereaksi dengan molekul H+ dan OH- . Senyawa yang
dihasilkan dari tahap ke-2 ialah etanol dan sulfat, sehingga perlu dimurnikan. Proses dari reaksi kimia adalah sebagai berikut.
CH3CH2OSO3H + H2O → CH3CH2OH + H2SO4 ……….……(2.3) Pemurnian etanol dari asam sulfat dilakukan dari kolom stripper sebagai tahap ke-3 yang kemudian diikuti dengan daur ulang asam sulfat. Sementara itu, etanol dengan bahan baku gula disebut bioetanol karena gula berasal dari sumber-sumber hayati (Megawati, 2015). Selain mengetahui cara pembuatannya, beberapa sifat – sifat fisika dan kimia yang juga harus diketahui untuk merancang pabrik bioetanol. Table 2.1 memuat sifat – sifat fisik dan kimia ethanol.
Tabel 2.1 Sifat Fisika-Kimia Etanol
Properties Nilai
Rumus molekul C2H5OH
Bobot molekul (g/mol) 46,7
Etanol (sering disebut etil-alkohol atau alkohol), adalah alkohol yang paling sering digunakan dalam kehidupan sehari-hari. Karena sifatnya yang tidak beracun, bahan ini banyak dipakai sebagai pelarut dalam dunia farmasi, industri makanan, minuman dan juga sebagai bahan bakar. Etanol tidak berwarna dan tidak berasa tapi memiliki bau yang khas. Bahan ini dapat memabukkan jika diminum.
Bioetanol dapat diperoleh dari semua jenis tanaman atau bahan hayati yang mengandung gula atau pati. Bioetanol awalnya dibuat dari gula dan pati
yang diperoleh dari tebu, jagung, singkong, dan lain – lain. Gula dari berbagai tanaman ini dapat langsung difermentasi oleh khamir menjadi etanol. Etanol berbahan gula ini selain disebut fermentation ethanol juga disebut bioetanol generasi pertama, yang berarti, etanol dari sumber hayati yang ditemukan orang pertama kali (Megawati, 2015). Seiring kebutuhan energi yang meningkat hadirlah bioetanol generasi kedua, ketiga, dan keempat. Bioetanol tiap generasinya memiliki kelebihan dan kekurangan masing-masing. Jadi semua orang berlomba-lomba melakukan penelitian untuk mengetahui prospek pembuatan biotanol yang lebih menguntungkan dan efisien.
Untuk bioetanol generasi kedua, ketiga, dan keempat ini lebih sulit dan lebih panjang pengolahannya untuk menjadi etanol. Bioetanol jenis kedua merupakan bioetanol yang bahan bakunya menggunakan tanaman yang berlignoselulosa yaitu, mengandung selulosa, hemiselulosa, dan lignin. Bioetanol dari selulosa yang sering juga disebut cellulosic ethanol dalam rangkaian proses pembuatannya juga ada tahap fermentasi, tetapi harus melalui proses pretreatment
terlebih dahulu dikarenakan tidak dapat secara langsung dilakukan proses difermentasi. Sampai sekarang belum ditemukan mikroorganisme yang dapat melakukan fermentasi secara langsung polimer gula berbentuk selulosa tersebut
menjadi etanol yang lebih ekonomis dan efisien.
etanol generasi berikutnya, yang berasal dari mikroalga dan tanaman gulma (enceng gondok dan ganggang). Etanol ini masih dalam tahap penelitian dan belum diproduksi, jadi kehadiran etanol generasi ketiga dan keempat akan menunggu temuan – temuan yang dapat diaplikasikan sampai pada skala industri.
2.2.2. Prospek Nira Di Indonesia
Nira merupakan hasil penyadapan dari suatu tanaman berjenis palma. Nira dapat diperoleh dari pohon aren, lontar (siwalan), kelapa, nipah dan lain-lain. Pohon aren (Arenga pinnata Merr) merupakan tanaman penghasil nira yang bernilai ekonomis tinggi. Pohon aren akan mencapai tingkat kematangannya pada umur 6-12 tahun, kondisi penyadapan terbaik pada umur 8-19 tahun saat keluarnya mayang. Kualitas nira yang baik adalah kandungan sukrosanya tinggi yaitu sekitar 9-16% dengan tingkat rendemen gula sekitar 15-20%. Nira diperoleh dari tandan bunga jantan yang terletak diujung batang, tandan yang terletak pada ruas batang yang rendah menghasilkan nira dalam jumlah yang seikit sedangkan
tandan bunga betina menghasilkan nira yang kadar serat tinggi. Dalam waktu 24 jam setiap tandannya dapat menghasilkan 10-30 liter nira yang dapat menghasilkan 1-3 kg gula aren. Sedangkan hasil samping seperti ijuk, lidi, daun dan produk olahan (cuka, alkohol) dapat dikembangkan sesuai dengan potensi tanaman dan dikaitkan dengan permintaan. Potensi tanaman nira aren di Indonesia cukup besar, hal ini didukung oleh letak geografis yang mempengaruhi iklim di Indonesia memiliki curah hujan yang relatife tinggi. Aren tumbuh pada daerah-daerah dengan curah hujan relatife tinggi dan merata sepanjang tahun seperti di Aceh, Sumatra Utara, Sumatra Barat, Bengkulu, jawa Barat, Jawa Tengah, Nusa Tenggara Barat, Kalimantan Selatan, Sulawesi Utara, Sulawesi Selatan, Sulawesi Tenggara, Gorontalo, Maluku Utara, Maluku, dan Papua. Sentra tanaman aren meliputi 14 provinsi dengan perkiraan total areal seluas 60.482 ha (PPPP, 2009).
merupakan pohon yang umumnya tumbuh secara liar. Aren (Arenga pinnata Merr) merupakan salah satu keluarga palma yang serbaguna, dapat tumbuh pada ketinggian 0-1500 meter di atas permukaan laut. Tanaman aren juga menghasilkan biomas di atas tanah yang sangat besar satu hingga 2 ton/pohon, sehingga dapat berperan penting dalam CO2sequestration.
Budidaya tanaman aren yang baik, jumlah tanaman aren setiap hektarnya rata-rata mampu sampai156 pohon. Jika yang berproduksi 50% dari populasi tanaman, maka produksi nira sebesar 210.600 liter/ha/tahun. Dengan asumsi,
apabila produksi aren per pohon disadap pagi dan sore hari. Setiap tahun disadap 3-5 tangkai bunga selama 9 bulan menghasilkan nira rata-rata 2.700 liter/ha/tahun. Rata-rata setiap 10 liter nira dapat menghasilkan 3,5 liter etanol. Dengan luar areal aren 60.482 ha maka, apabila yang berproduksi baik diasumsikan 30.000 ha maka potensi etanol aren yang dihasilkan adalah 2.211.300 kilo liter/tahun (PPPP, 2009).
Tabel 2.2 Klasifikasi Tanaman Siwalan
Sumber : Setiawan, 2011
Nira siwalan memiliki banyak manfaat. Selain dapat dijadikan minuman, sirup, dan gula semut nira siwalan juga dapat dijadikan bioetanol karena
mengandung gula yang tinggi. Kandungan senyawa yang terdapat pada nira siwalan ditunjukka pada tabel 2.3.
Tabel 2.3 Kandungan Nira Siwalan
Komponen Jumlah
Total gula (g/100 cc) 10,93
Gula reduksi (g/100 cc) 0,96
Protein (g/100 cc) 0,35
Nitrogen (g/100 cc) 0,056
pH (g/100 cc) 6,7-6,9
Specific gravity 1,07
Mineral sebagai abu (g/100 cc) 0,54
Kalsium (g/100 cc) Sedikit
Fosfor (g/100 cc) 0,14
Besi (g/100 cc) 0,4
Vitamin C (mg/100 cc) 13,25
Vitamin B1 (IU) 3,9
Vitamin B komplek Diabaikan
Sumber : Setiawan, 2011
Kingdom Plantae
Divisio Magnoliophyta Kelas Liliopsida
Ordo Arecales
Famili Arecaceae
Genus Borassus
Selain pohon aren dan pohon lontar, pohon kelapa juga dapat menghasilkan nira. Di sektor perkebunan, nira kelapa adalah sumber bioetanol yang prospektif. Tanaman kelapa sebagai tanaman penghasil bahan bakar nabati,
potensinya lebih baik dibandingkan jenis tanaman perkebunan lainnya terutama
penggunaan minyak murninya sebagai pengganti minyak tanah dengan
memanfaatkan kompor bertekanan yang sesuai. Menurut Prastowo (2007), bagian
lainnya yaitu nira dapat dijadikan bahan pembuatan bioetanol. Walaupun kadar energinya berbeda, tetapi bagian tanaman tersebut berpotensi sebagai sumber
energi alternatif.
Hampir semua bagian dari tanaman kelapa dapat dimanfaatkan untuk
bermacam-macam kegunaan antara lain sebagai makanan, minuman, perabotan,
hiasan dan bahan bakar. Indonesia adalah negara produsen kelapa terbesar di
dunia. Menurut Prastowo (2007), area pertanaman kelapa di Indonesia saat ini
sekitar 3,8 juta ha. Dari luas area kelapa di Indonesia tersebut, terlihat bahwa sebenarnya kelapa adalah komoditas yang sangat potensial untuk dikembangkan
lebih lanjut, salah satunya nira kelapa yang memiliki potensi yang besar selain
digunakan untuk produk pangan seperti gula merah, gula semut, dan lain-lain, tapi
juga dapat dikembangkan sebagai salah satu penganekaragaman produk non
pangan yaitu penggunaannya sebagai bahan bakar nabati. Potensi produksi nira
kelapa adalah 360.000 hingga 720.000 liter/tahun/ha. Karena nira kelapa memiliki
sifat sangat cepat terfementasi sehingga kurang menguntungkan untuk diolah
menjadi gula merah. Kondisi ini menambah besarnya kesempatan pemanfaatan
nira kelapa untuk keperluan lain yaitu sebagai sumber BBN (Bahan Bakar
Nabati).
Potensi ekosistem hutan mangrove Indonesia yang memiliki pulau dan pantai dengan wilayah pesisir terluas di dunia. Tanaman mangrove jenis nipah
angin, gelombang dan tsunami, intrusi air asin, sumber oksigen, penyerap CO2 dan nursery ground sekaligus memiliki nilai sebagai sumber bahan baku energy hijau bioetanol. Tanaman nipah (Nypa fruticans Wurmb) selama ini tumbuh liar di sekitar hutan mangrove di pesisir pantai maupun sungai. Tanaman Nipah tumbuh subur di hutan daerah pasang surut (hutan mangrove) dan daerah rawa-rawa atau muara-muara sungai yang berair payau. Di Indonesia, luas daerah tanaman nipah adalah 10% atau 700.000 ha dari luas daerah pasang surut sebesar 7 juta ha (Hadi, dkk, 2013). Penyebaran tanaman nipah meliputi wilayah kepulauan Sumatera,
Kalimantan, Jawa, Sulawesi, Maluku dan Papua. Hasil hutan non kayu dari mangrove nipah berupa nira yaitu cairan manis hasil sadapan tandan dapat difermentasi menjadi bioetanol sebagai sumber energi hijau. Menurut Hadi, dkk (2013), Potensi produksi bioetanol dari hutan mangrove nipah seluas 1 a yang disesuaikan dengan karakteristik hasil penelitian menunjukkan produksi tertinggi sebesar 13.179,43 liter/Ha/tahun dan terendah adalah sebesar 2.744,17 liter/Ha/tahun sehingga produksi rata-rata adalah 7.962,80 liter/Ha/tahun.
Nira merupakan cairan manis yang terdapat di dalam bunga tanaman aren, lontar, kelapa, dan nipah yang pucuknya belum membuka dan diperoleh dengan cara penyadapan. Pada umumnya masyarakat memanfaatkan nira aren dan nira kelapa untuk pembuatan gula merah dan gula semut, selain itu dapat digunakan sebagai minuman segar baik dari niranya langsung maupun nira yang dibuat sirup. Adapun nira yang biasa dideras dari berbagai jenis palma (Arenga pinnata, Borassus flabellifer, Cocos nucifera and Nypa fruticans) kandungan total sugarnya berkisar 10-20%. Apabila pohon penghasil nira dibudidayakan dengan baik, akan sangat potensial dimanfaatkan untuk pembuatan etanol (Putra dan Amran, 2009).
2.2.3. Fermentasi
mempunyai pengertian aplikasi metabolisme mikroba untuk mengubah bahan baku menjadi produk yang bernilai tinggi, seperti asam-asam organik, protein sel tunggal, antibiotika, dan biopolymer. Fermentasi merupakan proses yang relatif murah pada hakekatnya telah lama digunakan oleh nenek moyang kita secara tradisional dengan produk-produknya yang sudah biasa dikonsumsi menusia sampai sekarang seperti tape, tempe, oncom, dan lain-lain. Fermentasi dapat diartikan sebagai perubahan gradual oleh enzim beberapa bakteri, khamir dan jamur. Contoh perubahan kimia dari fermentasi meliputi pengasaman susu,
dekomposisi pati dan gula menjadi alkohol dan karbondioksida, serta oksidasi senyawa nitrogen organik.
Gula adalah bahan yang umum dalam fermentasi. Beberapa contoh hasil fermentasi adalah etanol, asam laktat, dan hidrogen. Akan tetapi beberapa komponen lain dapat juga dihasilkan dari fermentasi seperti asam butirat dan aseton. Fermentasi untuk menghasilkan bioetanol oleh ragi merupakan perubahan gula-gula heksosa sederhana menjadi bioetanol dan CO2 secara anaerob, udara tidak diperlukan selama proses fermentasi. Menurut Hadi, dkk (2013), pada proses fermentasi terjadi pemecahan senyawa induk dimana 1 molekul glukosa akan menghasilkan 2 molekul bioetanol, 2 molekul CO2 dan pembebasan energi.). Rumus reaksi sebagai berikut.
Yeast
C6H12O6 2C2H5OH + 2CO2 ……….…….(2.4)
Glukosa Bioetanol Karbon dioksida
Ragi dikenal sebagai bahan yang umum digunakan dalam fermentasi untuk menghasilkan etanol dalam bir, anggur dan minuman beralkohol lainnya.
Fermentasi etanol merupakan proses pembuatan etanol dengan memanfaatkan aktivitas yeast. Proses fermentasi adalah anaerob, yaitu mengubah glukosa menjadi etanol, tetapi dalam pembuatan starter dibutuhkan suasana aerob
a. Pemecahan glukosa dalam suasana aerob C
6H12O6 + 6O2 → 6CO2 + H2O ……….…….(2.6)
b. Pemecahan glukosa secara anaerob C
6H12O6 → 2C2H5OH + 2CO2……….…..(2.7)
Proses pemecahan glukosa dengan bantuan yeast termasuk salah satu proses enzimatik karena yeast ini menghasilkan enzime dan secara sederhana dapat dirumuskan sebagai berikut :
C
6H12O6 → 2C2H5OH + 2CO2 + 2ATP + 57kCal………..…(2.8)
Bila biakan yang digunakan terlalu muda atau waktu inkubasi terlalu singkat, ada kemungkinan biakan tersebut masih dalam fase adaptasi, sehingga pertumbuhan belum optimal, tetapi apabila waktu inkubasi terlalu lama kemungkinan biakan telah mencapai fase stasioner, oleh karena itu biakan yang paling baik berada pada fase log yaitu fase pertumbuhan yang paling optimal (Putra dan Amran, 2009).
Saccharomyces merupakan genus khamir atau ragi atau yeast yang memiliki kemampuan mengubah glukosa menjadi etanol dan CO2.
Saccharomyces merupakan mikroorganisme bersel satu, tidak berklorofil, dan termasuk kelompok eumycetes. Tumbuh baik pada suhu 30 oC dan keasaman 4,8. Beberapa kelebihan saccharomyces dalam proses fermentasi yaitu mikroorganisme ini cepat berkembang biak, tahan terhadap kadar alkohol tinggi, tahan terhadap suhu tinggi, mempunyai sifat stabil dan cepat beradaptasi. Pertumbuhan saccharomyces dipengaruhi oleh adanya penambahan nutrisi yaitu unsur C sebagai sumber karbon, unsur N yang diperoleh dari penambahan urea
dan saccharomyces uvarum (Setiawan, 2011). Klasifikasi saccharomyces ditunjukkan pada tabel 2.4.
Tabel 2.4 Klasifikasi Saccharomycess
Sumber : Setiawan, 2011
Saccharomyces cerevisiae merupakan mikroba yang bersifat fakultatif, ini berarti mikroba tersebut memiliki dua mekanisme dalam mendapatkan energinya. Jika ada udara, tenaga di peroleh dari respirasi aerob dan jika tidak ada udara tenaga di peroleh dari respirasi anaerob. Tenaga yang diperoleh dari respirasi aerob digunakan untuk pertumbuhan dan perkembangan sel sehingga praktis tidak ada kenaikan jumlah alkohol. Saccharomyses cerevisiae merupakan yeast yang mengandung dua enzim. Pertama enzim inverte yang bertindak sebagai katalisator dan mengubah sukrosa menjadi glukosa dan fruktosa atau gula sederhana. Kemudian enzim yang kedua adalah enzim zymase yang bertindak mengubah glukosa atau gula sederhana menjadi etanol dan CO2.
Ditinjau dari segi efisiensi penggunaan tenaga, ternyata kondisi aerob memberikan suasana lebih menguntungkan dalam usaha memperbanyak jumlah
yeast dibandingkan kondisi anaerob namun pada kondisi anaerob lebih banyak menghasilkan etanol dari pada kondisi aerob. Dalam fermentasi alkohol, mikroba yang dipakai adalah saccharomyces cerevisiae karena mempunyai daya fermentasi yang tinggi. Saccharomyces cerevisiae mempunyai daya fermentasi yang tinggi terhadap glukosa, fruktosa, galaktosa, maltosa dan mempunyai daya tahan dalam lingkungan di kadar alkohol yang relatif tinggi serta tahan terhadap mikroba lain.
Kingdom Plantae
Divisio Magnoliophyta
Kelas Liliopsida
Ordo Arecales
Syarat-syarat yeast yang dapat dipakai dalam proses fermentasi adalah:
1. Mempunyai kemampuan tumbuh dan berkembang biak dengan cepat dalam substrat yang sesuai
2. Dapat menghasilkan enzim dengan cepat untuk mengubah glukosa menjadi alkohol
3. Mempunyai daya fermentasi yang tinggi terhadap glukosa, fruktosa, galaktosa, dan maltose
4. Mempunyai daya tahan dalam lingkungan di kadar alkohol yang relatif tinggi
5. Tahan terhadap mikroba lain
Faktor-Faktor yang Mempengaruhi Fermentasi
1. Kadar gula
Bahan dengan konsentrasi gula tinggi mempunyai efek negatif pada yeast, baik pada pertumbuhan maupun aktivitas fermentasinya. Kadar glukosa yang baik berkisar 10 - 18%. Apabila terlalu pekat, aktivitas enzim akan terhambat sehingga waktu fermentasi menjadi lambat disamping itu terdapat sisa gula yang tidak dapat terpakai dan jika terlalu encer maka hasilnya berkadar alkohol rendah (Putra dan Amran, 2009). Kadar gula pada setiap nira dipengaruhi oleh jenis tanaman. Selain jenis tanaman mempengaruhi kadar gula pada air nira, cuaca, dan perawatan pohon juga akan mempengaruhi kualitas dan kandungan kadar gula.
2. Nutrisi
Nutrisi diperlukan sebagai tambahan makanan bagi pertumbuhan yeast. Nutrisi yang diperlukan misalnya : garam ammonium (NH
3. Temperatur
Suhu fermentasi secara langsung dapat mempengaruhi pertumbuhan mikroba. Untuk pertumbuhan, mikroba cocok pada suhu kamar sekitar 25 – 27 oC. Hal ini jika suhu tidak diperhatikan secara tidak langsung akan mempengaruhi etanol yang dihasilkan karena adanya penguapan. Seperti proses biologis (enzimatik) yang lain, kecepatan fermentasi akan bertambah sesuai dengan suhu
yang optimum umumnya 27 – 32 oC. Pada 27 oC etanol hilang menguap 0,83%,
pada 32 oC sebesar 1,66%. Saccharomycess cereviseae mempunyai temperatur
maksimal sekitar 40 - 50 oC dengan temperatur minimum 0 oC. Pada interval
15-30 oC fermentasi mengikuti pola bahwa semakin tinggi suhu, fermentasi makin
cepat berlangsung (Putra dan Amran,2009).
4. Nilai Derajat Keasaman (pH)
Saccharomycess cereviseae dapat tumbuh baik pada keasaman (pH) 3 - 6, namun apabila keasaman lebih kecil dari 3 maka proses fermentasi akan berkurang kecepatannya. Derajat keasaman (pH) paling optimum pada keasaman 4,3 - 4,7. Pada keasaman yang lebih tinggi, adaptasi yeast lebih rendah dan aktivitas fermentasinya juga meningkat, tetapi ternyata pengaruh juga pada pembentukan produk samping sebagai contoh, pada pH tinggi, konsentrasi gliserin meningkat juga (Putra dan Amran,2009). Sementara menurut penelitian Chairul dan Silvia (2013), kondisi optimum dari fermentasi nira nipah pada skala 50 liter adalah pada keasaman 4,5 dan waktu fermentasi 36 jam.
5. Aerasi
fermentasi. Kondisi yang baik selama fermentasi adalah kondisi yang tertutup atau lebih cendrung anaerob dengan dibatasi oleh udara yang tersedia sedikit ± 10% volume yaitu dari sisa rongga ruang tangki fermentor (Hadi dkk, 2013).
6. Waktu
Waktu fermentasi pada tiap bahan berbeda-beda tergantung kadar gula, suhu, dan faktor-faktor lain. Menurut Hadi, dkk (2013) rata-rata waktu fermentasi adalah antara 75,3 - 78 jam atau sekitar 3 hari. Tiap masing masing fermentasi membutuhkan waktu yang berbeda-beda. Hal ini dipengaruhi oleh banyak hal,
salah satunya adalah kadar gula bahan itu sendiri. Selain kadar gula nutrisi yang diberikan juga berpengaruh, karena banyaknya nutrisi berpengaruh pada kineerja mikroba dalam mengurai gula menjadi bioetanol. dan tahap ke-4 proses dehidrasi mencapai kadar kadar etanol 100 %.
2.2.4. Pengertian Distilasi
Distilasi atau penyulingan adalah suatu metode pemisahan bahan kimia berdasarkan perbedaan kecepatan atau kemudahan menguap (volatilitas) suatu bahan. Dalam penyulingan, campuran zat dididihkan sehingga menguap, dan uap
ini kemudian didinginkan kembali dalam bentuk cairan. Zat yang memiliki titik didih lebih rendah akan menguap lebih dulu. Metode ini termasuk sebagai unit operasi kimia jenis perpindahan massa. Penerapan proses ini didasarkan
pada teori bahwa pada suatu larutan, masing-masing komponen akan menguap pada titik didihnya. Dalam arti yang lebih sederhana distilasi adalah metode pemisahan zat cair berdasarkan perbedaan titik didihnya.
Bentuk modern distilasi pertama kali ditemukan oleh ahli-ahli kimia Islam pada masa kekhalifahan Abbasiah, terutama oleh Al-Razi pada pemisahan alkohol menjadi senyawa yang relatif murni melalui alat alembik, bahkan desain ini menjadi semacam inspirasi yang memungkinkan rancangan distilasi skala mikro, The Hickman Stillhead dapat terwujud. Tulisan oleh Jabir Ibnu Hayyan (721-815) yang lebih dikenal dengan Ibnu Jabir menyebutkan tentang uap anggur yang dapat terbakar. Dia juga telah menemukan banyak peralatan dan proses kimia yang bahkan masih banyak dipakai sampai saat kini.
Kemudian teknik penyulingan diuraikan dengan jelas oleh Al-Kindi (801-873).
Salah satu penerapan terpenting dari metode distilasi adalah pemisahan minyak mentah menjadi bagian-bagian untuk penggunaan khusus seperti untuk transportasi, pembangkit listrik, pemanas, dan lain-lain. Udara didistilasi menjadi komponen-komponen seperti oksigen untuk penggunaan medis dan helium untuk pengisi balon. Distilasi telah digunakan sejak lama untuk pemekatan alkohol dengan penerapan panas terhadap larutan hasil fermentasi untuk menghasilkan minuman suling.
2.2.4.1. Jenis - Jenis Distilasi
Ada beberapa macam jenis alat distilasi yaitu distilasi sederhana, distilasi fraksionasi, distilasi uap, dan distilasi vakum. Jenis – jenis alat distilasi dijelaskan
sebagai berikut :
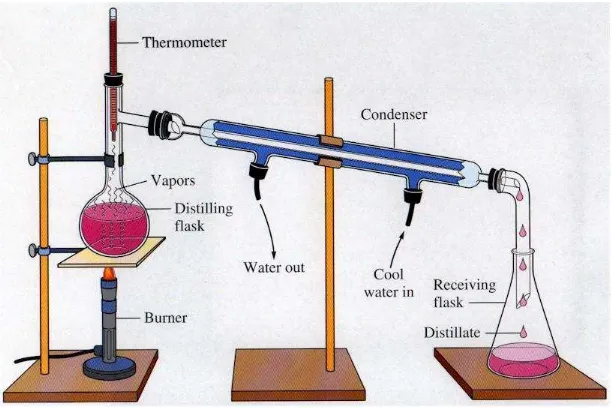
1. Distilasi Sederhana
campuran air dan alkohol. Rangkaian distilasi sederhana ditunjukkan pada gambar 2.1.
Gambar 2.1 Alat Distilasi Sederhana
2. Distilasi Fraksionisasi
Fungsi distilasi fraksionasi adalah memisahkan komponen-komponen cair, dua atau lebih, dari suatu larutan berdasarkan perbedaan titik didihnya. Distilasi ini juga dapat digunakan untuk campuran dengan perbedaan titik didih kurang dari 20 °C dan bekerja pada tekanan atmosfer atau dengan tekanan rendah. Aplikasi dari distilasi jenis ini digunakan pada industri minyak mentah, untuk memisahkan komponen-komponen dalam minyak mentah. Perbedaan distilasi fraksionasi dan distilasi sederhana adalah adanya kolom fraksionasi. Di kolom ini terjadi
pemanasan secara bertahap dengan suhu yang berbeda-beda pada setiap platnya. Pemanasan yang berbeda-beda ini bertujuan untuk pemurnian distilat yang lebih dari plat-plat di bawahnya. Semakin ke atas, semakin tidak volatil cairannya.
3. Distilasi Uap
senyawa-senyawa ini dengan suhu mendekati 100 °C dalam tekanan atmosfer dengan menggunakan uap atau air mendidih. Sifat yang fundamental dari distilasi uap adalah dapat mendistilasi campuran senyawa di bawah titik didih dari masing-masing senyawa campurannya. Selain itu distilasi uap dapat digunakan untuk campuran yang tidak larut dalam air di semua temperatur, tapi dapat didistilasi dengan air. Aplikasi dari distilasi uap adalah untuk mengekstrak beberapa produk alam seperti minyak eucalyptus dari eucalyptus, minyak sitrus dari lemon atau jeruk, dan untuk ekstraksi minyak parfum dari tumbuhan.
Campuran dipanaskan melalui uap air yang dialirkan ke dalam campuran dan mungkin ditambah juga dengan pemanasan. Uap dari campuran akan naik ke atas menuju ke kondensor dan akhirnya masuk ke labu distilat.
4. Distilasi Vakum
Distilasi vakum biasanya digunakan jika senyawa yang ingin didistilasi tidak stabil, dengan pengertian dapat terdekomposisi sebelum atau mendekati titik didihnya atau campuran yang memiliki titik didih di atas 150 °C. Metode distilasi ini tidak dapat digunakan pada pelarut dengan titik didih yang rendah jika kondensornya menggunakan air dingin, karena komponen yang menguap tidak dapat dikondensasi oleh air. Untuk mengurangi tekanan digunakan pompa vakum atau aspirator. Aspirator berfungsi sebagai penurun tekanan pada sistem distilasi.
2.2.4.2. Proses Distilasi Bioetanol
Pada penelitian ini proses distilasi bioetanol menggunakan alat distilasi sederhana. Etanol atau etil alkohol merupakan senyawa kimia yang memiliki titik didih pada suhu 70 - 78 oC. Untuk memisahkan atau memurnikan etanol yang bercampur dengan air (etanol proses fermentasi), maka dipanaskan pada suhu
dikarenakan pada suhu tersebut bioetanol sudah menguap namun air tidak ikut menguap. Uap distilasi dialirkan menuju kondensor untuk pendinginan, sehingga uap bioetanol akan menjadi cair. Uap cair tersebut kemudian ditampung pada sebuah wadah destilat. Pada distilasi tahap pertama. Biasanya kadar bioetanol masih dibawah 95% sehingga untuk mendapatkan kadar bioetanol lebih tinggi perlu dilakukan proses berikutnya.
Berdasarkan hasil penelitian Marjoni (2014), pada suhu 71 oC dengan waktu destilasi selama 4 dan 5 jam mempunyai pengaruh nyata terhadap kadar
3.1. Diagram Alir Penelitian
Diagram alir merupakan penggambaran secara singkat dari suatu proses. Diagram alir dibuat untuk memudahkan dalam memahami suatu proses. Untuk memperjelas tahapan-tahapan pembuatan bioetanol yang akan di lakukan di buat diagram alir proses pembuatan bioetanol yang ditunjukkan pada gambar 3.1.
TIDAK
YA Studi Literatur
Persiapan Alat dan Bahan
Mengukur dan Menimbang Bahan Sesuai Ukuran
Mulai
A
Apakah Sampel Telah Sesuai Metode
Gambar 3.1 Diagram Alir Penelitian
3.2. Perencanaan Penelitian
Fermentasi dilakukan pada suhu kamar yaitu antara 25 – 27 o
C . Jumlah metode yang digunakan dalam penelitian pembuatan bioetanol ini adalah dua
metode fermentasi dimana untuk setiap metodenya terdiri dari empat sampel. Jadi pada penelitian pembuatan bioetanol ini terdiri atas delapan sampel. Metode
pertama adalah variasi terhadap jumlah yeast yang diberikan (0,5 ; 1 ; 1,5 ; dan 2) gram dengan volume fermentasi 250 ml dan keasaman awal diatur 4,5. Pemberian nutrisi urea sebanyak 0,1 g/250 ml dan NPK 0,125 g/250 ml untuk semua sapel. Metode kedua adalah variasi terhadap waktu fermentasi ( 24, 48, 72, dan 96 ) jam
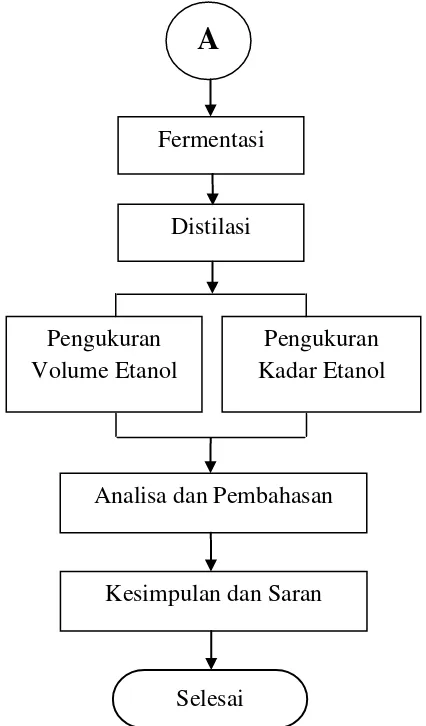
Pengukuran Kadar Etanol Pengukuran
Volume Etanol
A
Fermentasi
Distilasi
Analisa dan Pembahasan
Kesimpulan dan Saran
dengan volume fermentasi 250 ml dan keasaman awal diatur 4,5 dengan banyaknya ragi yang diberikan berdasarkan hasil terbaik untuk metode pertama . Setelah dilakukan fermentasi maka langkah selanjutnya dilakukan pemurnian
dengan cara distilasi pada suhu 78 oC . Distilasi ini bertujuan untuk mendapatkan volume dan kadar etanol yang lebih tinggi. Langkah terakhir adalah dilakukannya pengujian volume dan kadar etanol hasil distilasi.
3.3. Alat Penelitian
Dalam penelitian pembuatan bioetanol ini perlu adanya alat untuk mendukung proses penelitian yang dilakukan. Adapun peralatan tersebut adalah sebagai berikut :
1. Brix Refractometer
Brix refractometer adalah alat yang digunakan untuk mengukur kadar gula pada nira siwalan. Brix Refractometer dengan merk ATC memiliki beberapa kelebihan. Kelebihan alat ini adalah alatnya yang berukuran sedang dan portable, sehingga dapat dibawa dan digunakan disemua tempat. Selain itu sampel yang dibutuhkan juga sedikit kurang lebih 1 ml. Namun kelemahan alat ini tidak dapat mengukur kadar gula lebih dari 30 persen. Brix Refractometer ditunjukkan pada gambar 3.2.
2. Alat pH Meter Digital
Alat pH meter merupakan alat yang digunakan untuk mengukur kadar keasaman (pH) pada nira siwalan. Kadar keasaman sangat mempengaruhi dalam proses fermentasi, untuk itu keasaman harus diukur dengan pasti. Alat pH meter digital dengan merk ATC memiliki kelebihan yaitu nilai terukur dapat ditunjukkan dengan angka, sehingga lebih mudah dalam pembacaan pengukuran. Selain itu alat ini yang simpel, sehingga mudah dibawa dan digunakan di semua
tempat. Alat pH meter digital merk ATC ditunjukkan pada gambar 3.3.
Gambar 3.3 pH Meter Digital
3. Termometer
Gambar 3.4 Termometer
4. Timbangan Digital
Neraca merupakan alat yang digunakan untuk mengukur massa yeast dan nutrisi (Urea dan NPK) yang harus diberikan pada proses fermentasi. Timbangan digital merk Mettler Tolledo memiliki beberapa kelebihan. Kelebihan alat ini nilai terukur ditunjukkan dengan anggka digital, sehingga mudah dalam pembacaan. Timbangan digital dapat ditunjukkan pada gambar 3.5.
5. Refraktometer Alkohol
Refraktometer alkohol merupakan alat yang digunakan untuk mengukur kadar alkohol yang telah dilakukan distilasi. Refraktometer alkohol dengan merk ATC ini memiliki beberapa kelebihan. Kelebihan alat ini antara lain, alatnya yang berukuran sedang dan portable sehingga dapat dibawa dan digunakan disemua tempat. Selain itu sampel yang dibutuhkan juga sedikit kurang lebih 1 ml. Namun kelemahan alat ini tidak dapat mengukur kadar alkohol sebelum dilakukan
distilasi. Berikut gambar dari alkohol meter ditunjukkan pada gambar 3.6.
Gambar 3.6 Refraktometer Alkohol
6. Fermentor
Fermentor adalah alat yang digunakan untuk proses fermentasi. Fermentor menggunakan gelas minuman merk saparella dengan volume 300 ml. Dipilihnya
botol ini sebagai fermentor karena botol terbuat dari kaca dan penutup dari seng, sehingga mampu terhadap tekanan CO2. Dengan demikian alat ini tidak akan
Gamabar 3.7 Fermentor
7. Satu Unit Alat Distilasi
Alat distilasi adalah alat yang digunakan untuk proses pemurnian alkohol hasil fermentasi. Alat ini dirancang sebagai alat distilasi sederhana untuk satu tingkat atau tahap distilasi. Berikut alat distilasi ditunjukkan pada gambar 3.8.
8. Alat Pengaduk
Alat pengaduk merupakan alat yang digunakan untuk mengaduk cairan nira selama pembuatan starter. Tujuan dari pengadukan ini adalah agar yeast dapat tercampur rata dengan nira siwalan, sehingga pertumbuhan mikroba dapat maksimal. Berikut alat pengaduk ditunjukkan pada gambar 3.9.
Gambar 3.9 Pengaduk
9. Aluminum Foil
Dalam penelitian ini, alumunium foil dapat digunakan sebagai pembungkus atau penutup botol fermentor saat proses fermentasi ataupun sebagai pembungkus hal lainnya. Aluminum foil didapat dari toko kue Intisari Yogyakarta. Aluminum foil ditunjukkan pada gambar 3.10.
10. Gelas Ukur
Gelas ukur merupakan alat yang digunakan untuk mengukur volume nira, volum starter ataupun volume etanol yang telah dihasilkan melalui proses distilasi. Gelas ukur yang digunakan adalah gelas ukur kapasitas 25 ml merek Herma dan gelar ukur kapasitas 50 ml merek Pirex. Gelas ukur merk Herma ataupun Pirex didapat dari peminjaman dari Laboratorium Agrobioteknologi UMY. Gelas ukur dapat ditunjukkan pada gambar 3.11.
Gambar 3.11 Gelas Ukur
11. Erlenmeyer
Labu enlemeyer merupakan alat yang digunakan sebagai tempat pembuatan starter. Labu erlenmeyer yang digunakan adalah labu erlenmeyer
kapasitas 250 ml merek Herma. Labu erlenmeyer merk Herma didapat dari membeli di toko Alfa Kimia. Berikut adalah gambar dari labu erlenmeyer
Gambar 3.12 Erlenmeyer
12. Jerigen
Jerigen digunakan sebagai tempat nira siwalan pada saat pengambilan pada petani nira. Jerigen yang digunakan adalah jerigen kapasitas 10 liter. Jerigen ditunjukkan pada gambar 3.13.
13. Autoclave
Autoclave adalah alat yang digunakan untuk sterilisasi nira siwalan, sehingga mikroba liar yang terdapat pada nira dapat mati. Sterilisasi diatur suhu pemanasan 121 oC pada tekanan 1 atm selama 15 menit. Dengan matinya mikroba liar maka kinerja yeast akan lebih maksimal untuk memproduksi etanol. Autoclave
ditunjukkan pada gambar 3.14.
Gambar 3.14 Autoclave
14. Pipet
Gambar 3.15 Pipet
15. Alat Tulis
Alat tulis merupakan alat yang digunakan untuk melakukan pencatatan ataupun keperluan lainnya. Alat tulis yang digunakan diantaranya sepidol, bolpoin, ataupun alat sejenisnya. Berikut gambar dari alat pencatat ditunjukkan pada gambar 3.16.
Gambar 3.16 Alat Pencatat
16. Stopwatch
Gambar 3.17 Stopwatch
17. Kamera atau Alat Dokumentasi
Kamera digunakan untuk mengambil gambar atau dokumentasi selama proses penelitian. Pengambilan gambar dilakukan menggunakan kamera
handphone dikarenakan memiliki lensa yang kecil sehingga dapat memudahkan dalam pengambilan gambar pada lensa refraktometer yang relative kecil.
3.4. Bahan Penelitian
Adapun bahan yang diperlukan dan dipersiapkan dalam penelitian ini adalah :
1. Nira Siwalan
Nira siwalan digunakan sebagai substrat bahan pokok pembuatan bioetanol. Kandungan gula yang terdapat pada nira ini nantinya dilakukan
Kabupaten Pati dan Kabupaten Rembang. Nira siwalan ditunjukkan pada gambar 3.18.
Gambar 3.18 Nira Siwalan
2. HCL
Gambar 3.19 HCL
3. Natrium Hidroksida (NaOH)
Natrium Hidroksida berfungsi sebagai pengontrolan kadar pH, namun pengontrolan yang dimakud yaitu menambah atau memperbesar kadar pH karena NaOH bersifat basa. NaOH ditambahkan sedikit demi sedikit sampai kadar keasaman yang diinginkan telah terpenuhi. NaOH didapat dari toko Alfa Kimia - Yogyakarta. Untuk lebih jelasnya NaOH ditunjukkan pada gambar 3.20.
4. Yeast atau Ragi Fermentasi
Yeast atau ragi adalah jenis mikroba yang berperan mengubah gula menjadi etanol pada saat fermentasi. Dalam fermentasi ini menggunakan saccharomyces cerevisiae dikarenakan mikroba jenis ini (saccharomyces cerevisiae) mempunyai daya fermentasi yang tinggi terhadap glukosa, fruktosa, galaktose, maltose dan mempunyai daya tahan dalam lingkungan di kadar alkohol yang relatif tinggi serta tahan terhadap mikroba lain. Yeast saccharomyces
cerevisiae ditunjukkan pada gambar 3.21.
Gambar 3.21 YeastSaccharomyces Cerevisiae
5. Urea
Gambar 3.22 Urea
6. NPK
NPK atau bahan sejenis merupakan bahan pendukung yang bertindak sebagai nutrisi atau makanan bagi mikroba yang terdapat pada saccharomyces cerevisiae. NPK yang diberikan sebanyak 0,125 gram untuk sampel fermentasi sebanyak 250 ml. NPK ditunjukkan pada gambar 3.23.
7. Aquades
Aquades berfungsi sebagai pelarut yeast atau nutrient yang nantinya akan diberikan pada nira. Dipilihnya aquades sebagai bahan pelarut karena aquades adalah air murni bebas mineral dan keasaman air adalah 7. Sehingga aquades cocok digunakan sebagai bahan pelarut yeast ataupun urea dan NPK yang digunakan sebagai nutrisi mikroba. Aquades ditunjukkan pada gambar 3.24.
Gambar 3.24 Aquades
8. Air Mineral
Air mineral berfungsi sebagai pendinginan uap etanol yang melewati kondenser, sehingga nantinya uap yang mengalir melalui kondenser dapat berubah menjadi cair yang nantinya menjadi produk bioetanol.
3.5. Waktu dan Tempat Pelaksanaan Penelitian
3.6. Tahapan Pembuatan Bioetanol
Tahapan-tahapan dalam proses penelitian pembuatan bioetanol dilakukan sebagai berikut :
3.6.1. Proses Fermentasi
Fermentasi adalah proses pertama dalam pembuatan bioetanol. Dalam proses fermentasi, gula pada bahan (nira siwalan) diubah menjadi etanol dan produk samping. Langkah-langkah proses fermentasi adalah sebagai sebagai berikut:
1. Persiapan Alat dan Bahan
Langkah pertama adalah mempersiapkan alat dan bahan yang digunakan untuk penelitian. Setelah persiapan alat dan bahan telah selesai maka dilakukan pengecekan alat dan dilakukan kalibrasi jika alat ada ketidakakuratan.
2. Pengukuran dan Penimbangan Bahan
Langkah skedua adalah pengukuran dan penimbangan bahan yang digunakan. Pengukuran yang dilakukan adalah penimbangan urea, NPK, dan
3. Melarutkan Nutrisi dan Yeast
Nutrisi seperti urea dan NPK harus dilarutkan terlebih dahulu menggunakan akuades sebelum dituangkan dalam nira fermipan. Tujuan dari proses pelarutan agar nutrisi dapat tercampur merata dengan nira sehingga kinerja mikroba bekerja dengan maksimal. Untuk melarutan yeast cairan yang digunakan adalah nira siwalan. Tujuan dari pelarutan yeast agar terjadi pemecahan sel mikroba yang terdapat dalam yeast.
4. Penuangan Nutrisi pada Sampel Fermentasi
Setelah nutrisi larut keseluruhan, maka larutan nutrisi (urea dan NPK) dituangkan dalam sampel fermipan 250 ml yang akan dilakukan fermentasi. Sampel sudah siap dilakukan langkah selanjutnya.
5. Autoclave
Autoclave bertujuan agar mikroba yang ada dapat mati. Autoclave
dilakukan pada suhu 121 oC. Waktu autoclave selama 15 menit. Setelah 15 menit bahan dikeluarkan lalu didinginkan.
6. Penuangan Yeast yang Telah Larutan
Yeast dituangkan pada sampel fermipan setelah autoclave bertujuan agar mikroba yang terdapat pada yeast tidak mati akibat dari autoclave. Oleh sebab itulah mengapa penuangan yeast setelah dilakukan sterilisasi melalui cara
Gambar 3.25 Diagram Alir Proses Fermentasi
3.6.2. Proses Distilasi
Distilasi dilakukan dengan tujuan memisahkan etanol dengan broth
fermentasi sehingga mendapatkan kadar etanol yang lebih tinggi. Langkah
pertaman broth setelah dilakukan fermentasi dimasukkan pada distilat, kemudian dipanaskan dan dilakukan pengaturan suhu. Distilasi dilakukan dengan menggunakan rangkaian distilasi sederhana dan suhu dijaga pada suhu 78 oC agar etanol dapat menguap. Pada suhu tersebut etanol sudah dapat menguap namun air
Studi Literatur Mulai
Persiapan Alat dan Bahan
Pengukuran dan Penimbangan Bahan
Melarutkan Nutrisi dan Yeast
Pemberian Nutrisi
Pemberian Yeast yang Telah Dilarutkan
Fermentasi
(Pengukuran Kadar Gula dan Keasaman Setiap 12 jam)
Selesai
belum menguap, sehingga antara etanol dan air dapat terpisah. Penjagaan suhu dengan cara manual yaitu menekan tombol ON– OFF pada kompor listrik. Ketika suhu sudah mencapai 78 oC maka tombol OFF ditekan dan ketika suhu turun menjadi 76 oC maka kompor dihidupkan dengan cara menekan tombol ON. Meskipun pada teorinya air tidak ikut menguap, namun realitanya sebagian kecil kandungan air masih terbawa dan tercampur pada uap etanol. Etanol yang telah menguap tersebut kemudian dialirkan menuju kondensor untuk didinginkan, sehingga uap akan kembali dalam wujud cair. Untuk memperjelas
tahapan-tahapan proses distilasi yang akan di lakukan di buat diagram alir proses distilasi yang di tunjukkan pada gambar 3.26.
Gambar 3.26 Tahap Distilasi
3.7. Cara Pengukuran Volume dan Kadar Etanol
Setelah proses distilasi dilakukan, maka etanol yang dihasilkan dilakukan pengukuran volume dan kadar etanol. Pengukuran volume etanol dilakukan dengan cara menuangkan hasil distilasi kedalam gelas ukur kapasitas 50 ml untuk
Proses Distilasi
Selesai
Penuangan Broth Hasil Fermentasi pada Labu Distilat
Mulai
Studi Literatur
setiap sampelnya. Penunjukan ukuran volume etanol terbaca pada angka yang terdapat pada gelas ukur, dengan demikian volume etanol dapat diketahui.
Setelah dilakukan penelitian mengenai eksperimental pembuatan bioetanol menggunakan nira siwalan dengan volume fermentasi 250 ml maka diperoleh data-data pengujian yang kemudian dijabarkan melalui beberapa sub-sub pembahasan dari masing-masing jenis pengujian. Data-data pengujian tersebut meliputi data selama fermentasi dan data setelah dilakukan proses distilasi broth fermentasi nira siwalan dengan volume 250 ml. Pengujian yang dilakukan adalah pengujian pengamatan gula dan derajat keasaman (pH) selama fermentasi serta pengujian volume dan kadar etanol yang diperoleh setelah dilakukannya distilasi. Metode fermentasi yang digunakan ada dua metode yaitu variasi jumlah yeast dan variasi waktu.
4.1. Hasil Pengujian Metode Fermentasi Variasi Jumlah Yeast
Pada fermentasi nira siwalan volume 250 ml dengan variasi jumlah
Gambar 4.1 Broth Fermentasi Nira Siwalan dengan Variasi Yeast
Keterangan :
Sampel Jumlah yeast 0,5 gram dengan Fermentasi 72 Jam Sampel Jumlah yeast 1,0 gram dengan Fermentasi 72 Jam Sampel Jumlah yeast 1,5 gram dengan Fermentasi 72 Jam Sampel Jumlah yeast 2,0 gram dengan Fermentasi 72 Jam
Fermentasi sudah mulai bekerja dapat diketahui secara visual dengan adanya gelembung-gelembung gas CO2 yang naik dari dasar botol fermentor. Lama waktu frementasi terhitung, awalnya gelembung gas CO2 memiliki frekuensi yang lambat namun setelah setengah jam kemudian frekuensi gelembung gas CO2 yang keluar semakin banyak sampai waktu proses fermentasi telah selesai. Waktu fermentasi telah selesai, secara visual ditandai dengan tidak adanya gelembung – gelembung gas yang muncul dari dasar fermentor. Hal ini mengindikasikan
semakin lama waktu fermentasi, maka semakin banyak pula produksi gelembung gas CO2. Jika produksi gas CO2 semakin banyak, maka akan diindikasikan
semakin banyak pula produksi bioetanol yang dihasilkan.
Namun semakin lama waktu fermentasi yang dimaksud adalah waktu fermentasi hingga titik optimum. Berdasarkan penelitian yang dilakukan, gelembung gas terakhir berhenti yaitu pada jam ke-48 untuk sampel 0,5 gram