PENGARUH EFISIENSI ARUS (CURRENT EFFICIENCY)
TERHADAP FREKWENSI TERJADINYA ANODE EFFECT
DALAM LARUTAN KRIOLIT (Na3AlF6)
PADA PROSES EEKTROLISA
DI PT INALUM
KARYA ILMIAH
MUHAMMAD ARIF
0 7 2 4 0 9 0 4 0
PROGRAM DIPLOMA-3 KIMIA INDUSTRI DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENGARUH EFISIENSI ARUS (CURRENT EFFICIENCY)
TERHADAP FREKWENSI TERJADINYA ANODE EFFECT
DALAM LARUTAN KRIOLIT (Na
3AlF
6)
PADA PROSES EEKTROLISA
DI PT INALUM
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Ahli Madya
MUHAMMAD ARIF
072409040
PROGRAM DIPLOMA-III KIMIA INDUSTRI DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul
: PENGARUH EFISIENSI ARUS
(CURRENT EFFICIENCY)
TERHADAP FREKWENSI
TERJADINYA ANODE EFFECT
DALAM LARUTAN KRIOLIT
(Na3AlF6) PADA PROSES
EEKTROLISA DI PT INALUM
Nama
: MUHAMMAD ARIF
Nomor Induk Mahasiswa
: 072409040
Program Studi
: KIMIA INDUSTRI D-3
Departemen
: KIMIA
Fakultas
: MATEMATIKA DAN ILMU
PENGETAHUAN ALAM (FMIPA)
UNIVERSITAS SUMATERA
UTARA
Disetujui di
Medan, Juni 2010
Diketahui / Disetujui
Departemen Kimia FMIPA USU
Pembimbing
Ketua,
PERNYATAAN
PENGARUH EFISIENSI ARUS (CURRENT EFFICIENCY)
TERHADAP FREKWENSI TERJADINYA ANODE EFFECT
DALAM LARUTAN KRIOLIT (Na
3AlF
6)
PADA PROSES EEKTROLISA
DI PT INALUM
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri,
kecuali beberapa kutipan dan ringkasan yang masing-masing
disebutkan sumbernya.
Medan, Juni 2010
KATA PENGANTAR
Bismillahirrahmanirrahim
Puji dan syukur penulis haturkan kepada Allah SWT, atas segala
limpahan Rahmad dan Karunia-Nya sehingga penulis dapat
menyelesaikan Karya Ilmiah ini yang berjudul PENGARUH
EFISIENSI ARUS (CURRENT EFFICIENCY) TERHADAP
FREKWENSI TERJADINYA ANODE EFFECT DALAM
LARUTAN KRIOLIT (Na3AlF6) PADA PROSES EEKTROLISA
DI PT INALUM
Karya ilmiah ini disusun berdasarkan pengamatan yang dilakukan
penulis selama + 40 hari yaitu mulai tanggal 21 Desember 2009
sampai 29 Januari 2010 yang ditempatkan pada seksi OPERASI
TUNGKU REDUKSI ALUMINIUM di PT. Indonesia Asahan
Aluminium (PT. INALUM).
Adapun tujuan dari penulisan karya ilmiah ini adalah untuk memenuhi
persyaratan dalam menyelesaikan pendidikan Program Diploma III
Kimia Industri.
Dengan segala kerendahan hati, penulis mengucapkan terima kasih
kepada :
1.
Ayahanda Kasiman Sutan Saidi dan ibunda Ernawati, beserta
keluarga kandung saya Bang Afrizal, Bang Yusrizal, Kak
Afrida, Bang Iskandar, Bang Jonny Syahputra, Bang Robby
Syahputra, Kak Sri Wahyuni, dan adik-adikku Rahmad Dani,
Sari Astuti, dan Mitra Kaswadi. Yang memberikan semangat
serta perhatian baik materi maupun moril yang cukup besar
selama masa perkuliahan saya.
2.
Kakak Ipar saya yaitu kak Inur, kak Desi, kak Yul
3.
Ibu Dra. Yugia Muis, M.Si, sebagai Dosen Pembimbing yang
telah sabar memberikan petunjuk serta bimbingan kepada
penulis.
4.
Bapak Jasmi Baringin, Bapak Ahmad Sabran sebagai
pembimbing lapangan di PT. Inalum, yang telah membantu
saya selama PKL di PT. Inalum.
5.
Bapak Prof. Dr. Eddy Marlianto, MSc sebagai Dekan FMIPA
USU.
7.
Teman-teman satu PKL penulis yang satu jurusan yaitu Agus,
Syahri, Emir, Jefri, Hendra, Gugun, Lia, Putri, Parni, Lisik,
Leni yang sama-sama membantu saya dalam penyelesaian tugas
akhir.
8.
Teman-teman dekat saya Emir, Jaka, Agus, Syahri, Jefri, Erwin.
9.
Seluruh teman-teman saya satu angkatan 2007 di Kimia Industri
yang telah membantu saya dalam menyelesaikan karya ilmiah.
10.
Kakak dan abang senior angkatan 2006 yang telah banyak
memberikan masukan, arahan, dan pengalaman selama
perkuliahan di FMIPA USU.
11.
Adik-adik junior saya ermita trisna, supiya ningsih, maya,
hanik, fitri, nina, dan lainnya.
12.
Teman saya Novita Sari yang selalu mensupport dan membantu
saya dalam hal pengetikan karya ilmiah ini.
Hanya doa yang dapat penulis sampaikan kepada Allah SWT.
Mudah-mudahan kebaikan yang diterima penulis dari semua pihak yang telah
membantu, kiranya Allah SWT membalas kebaikan tersebut. Penulis
dengan segala kemampuan berusaha menyelesaikan karya ilmiah ini
dengan sebaik-baiknya. Apabila ada kekurangan kritik dan saran
penulis terima dengan senang hati.
Akhirnya penulis mengucapkan terima kasih dan harapan semoga
tulisan ini bermanfaat bagi yang membaca.
Medan, Agustus
2010
Penulis
ABSTRAK
Determination of Current Efficiency to Occur Anode Effect Frecuency in Cryolite Insolubility (Na3AlF6) at Electrolysis Process n PT NALUM
ABSTRACT
DAFTAR ISI
Halaman
PERSETUJUAN ii
PERNYATAAN
PENGHARGAAN
ABSTRAK
ABSTRACT
DAFTAR ISI
DAFTAR TABEL
DAFTAR GAMBAR
BAB I PENDAHULUAN
1.1Latar Belakang
1.2Permasalahan
1.3Tujuan
1.4Manfaat
BAB II TINJAUAN PUSTAKA
2.1 Aluminium
2.1.1 Sejarah Aluminium
2.1.2 Sifat-sifat Aluminium
2.2 Alumina (Al2O3)
2.2.1 Daya larut alumina (Al2O3) Pada cairan Kriolit
2.2.2 Kecepatan Melarut Alumina (Al2O3) Pada Cairan Kriolit
2.2.3 Proses Pengolahan Alumina
2.4 Elektrolit [Kriolit/bath(Na3AlF6)]
2.5 Elektrolisa
2.5.1 Proses Hall-Heroult
2.5.2 Produksi Aluminium
2.6 Anode Effect
2.6.1 Gejala-gejala dan Penyebab Terjadinya Anode Effect
2.6.3 Penanggulangan Anode Effect
2.6.4 Mekanisme Terjadinya Anode Effect
2.7 Alumina Feeding
2.7.1 Pemasukan Alumina
2.7.2 Pemasukan Alumina Ke dalam Bath (Na3AlF6)
BAB III METODOLOGI PERCOBAAN
3.1 Alat-alat yang digunakan
3.2 Bahan – bahan
3.3 Prosedur Kerja
3.3.1 Prosedur Anode Effect (AE)
3.3.2 Prosedur Alumina Feeding
BAB IV HASIL DAN PEMBAHASAN
4.1 Data Percobaan
4.2 Perhitungan
4.3 Pembahasan
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan
5.2 Saran
DAFTAR PUSTAKA
DAFTAR TABEL
Halaman
Tabel 2.1 Perbedaan sifat Alumina Sandy dan Floury
Tabel 2.2 Spesifikasi Alumina
Tabel 2.3 Komponen Bath Pada Dapur Peleburan di PT INALUM
Tabel 4.1 Data Hasil Pengamatan Efisiensi Arus (CE)
DAFTAR GAMBAR
Halaman
Gambar 2.1 Jumlah Bahan Baku dan Energi Pada Proses Elektrolisa
ABSTRAK
Determination of Current Efficiency to Occur Anode Effect Frecuency in Cryolite Insolubility (Na3AlF6) at Electrolysis Process n PT NALUM
ABSTRACT
BAB I
PENDAHULUAN 1.1 Latar Belakang
Dalam memproduksi aluminium batangan (Ingot), PT INALUM menggunakan
proses elektrolisa Hall-Heroult dengan memakai tungku jenis PAF (Prebaked
Anode Furnace). Proses elektrolisa di tungku ini menggunakan arus listrik sebesar
185 kA – 190 kA, dengan temperatur operasi normal sebesar 945 oC – 965 oC
serta beda potensial (voltase) tiap pot sekitar 4,3 – 4,5 Volt. Daya yang digunakan
untuk setiap pot kira-kira 500 watt. Dalam setiap tungku reduksi tersebut terdapat
18 anoda karbon yang berfungsi sebagai anoda, sedangkan katoda yang terbuat
dari karbon ada 16 buah. Dengan adanya larutan elektrolit (Na3AlF6) akan terjadi
elektrolisa alumina menjadi aluminium.
Suatu kinerja tinggi sering diartikan sebagai hasil prestasi dari penerapan
efisiensi arus, frekwensi anode effect yang rendah dan batas pemakaian alumina
(Al2O3) sebagai bahan baku utama yang digunakan di dalam tungku reduksi
peleburan aluminium. Namun selalu saja dilakukan perubahan-perubahan serta
perbaikan-perbaikan untuk memajukan dan mengembangkan teknologi tungku
reduksi yang digunakan untuk meningkatkan skala produksi dan mutu produksi.
Untuk mencapai kinerja yang tinggi dalam industri peleburan aluminium
biasanya disesuaikan dengan kondisi dari pot operasi. Kandungan alumina dalam
elektrolit yang tidak memenuhi syarat-syarat dan standar yang telah ditetapkan
untuk proses elektrolisa dapat menimbulkan kerugian terhadap keberlangsungan
operasi elektrolisa diantaranya terbentuknya lumpur (sludge) dan terjadinya
Tinggi atau rendahnya konsentrasi alumina di dalam pot disebabkan oleh
pemasukan alumina kedalam pot yang tidak stabil, sehingga kelarutan alumina
tidak sempurna dan akan mengendap menjadi lumpur (sludge). Jika lumpur
alumina banyak terdapat dalam pot, selain menggangu operasi juga menyebabkan
sering terjadi efek anoda (Anoda Effect). Pada prosedurnya dengan adanya anode
effect memberikan manfaat untuk kontrol alumina dan pembersihan dari
pembakaran debu karbon.
Di semua industri peleburan aluminium harus mampu mengurangi emisi
PFC (Perfluorocarbon ) berupa gas tetrafluorometana (CF4) dan hexafluoroetana
(C2F6) selama terjadinya Anode effect, tanpa adanya produksi yang hilang. Jadi
ada sedikit keraguan bagi industri peleburan aluminium di dunia pada masa
mendatang dalam pencapaian frekwensi Anoda Effect manjadi nol.
Untuk dapat memperoleh hasil operasi elektrolisa alumina (Al2O3) yang
baik maka frekwensi terjadinya anode effect pada proses elektrolisa alumina
(Al2O3) harus ditekan dalam harga yang memenuhi standar yang telah ditentukan
yaitu 2 % - 3 %. Dalam upaya untuk memperoleh frekwensi anode effect yang
memenuhi standar, maka elektrolit yang digunakan harus memenuhi persyaratan
tertentu. Oleh karena itu harus diakukan penelitian mengenai komponen yang
terdapat didalam larutan elektrolit (Na3AlF6), dimana salah satu diantaranya
adalah kandungan alumina (Al2O3). Sehingga yang menjadi pokok permasalahan
adalah membahas pengaruh efisiensi arus (current efficiency) terhadap frekwensi
terjadinya anode effect dalam larutan kriolit (Na3AlF6) terhadap keberhasilan
Sehubungan dengan adanya ulasan masalah diatas maka penulis tertarik untuk
membahasnya dimana hsil pembahasan tersebut dipaparkan dalam bentuk Tugas
Akhir dengan judul : ” PENGARUH EFISIENSI ARUS (CURRENT
EFFICIENCY) TERHADAP FREKWENSI TERJADINYA ANODE
EFFECT DALAM LARUTAN KRIOLIT (Na3AlF6) PADA PROSES
ELEKTROLISA DI PT INALUM”
1.2 Permasalahan
Menentukan banyaknya alumina yang ditambahkan kedalam larutan kriolit
(Na3AlF6) dengan efisiensi arus yang berbeda ketika peristiwa anode effect di
pabrik peleburan aluminium.
1.3 Tujuan
Untuk menentukan banyak alumina (Al2O3) yang diperlukan setiap harinya
dengan efisiensi arus yang berbeda untuk proses elektrolisa dan terhadap
frekwensi terjadinya anode effect di PT INALUM.
1.4 Manfaat
a. Dapat mengetahui faktor-faktor penyebab terjadinya anode effect pada
proses elektrolisa.
b. Dapat mengetahui cara penanggulangan dan pencegahan terjadinya anode
effect.
c. Dapat mengetahui strategi feeding alumina (Al2O3) yang didasarkan pada
BAB II
TINJAUAN PUSTAKA
2.1 Aluminium
Aluminium pertama kali ditemukan oleh Sir Humphrey Davy pada tahun
1809 sebagai suatu unsur dan pertama kali direduksi sebagai logam oleh H. C.
Oersted pada tahun 1825. Secara Industri tahun 1886, Paul Heroul di Prancis dan
C. M. Hall di Amerika Serikat secara terpisah telah memperoleh logam aluminium
dari alumina dengan cara elektrolisa dari garam yang terfusi. Penggunaan
aluminium sebagai logam setiap tahunnya adalah pada urutan yang kedua setelah
baja dan besi, yang tertinggi diantara logam non ferro. Aluminium merupakan
logam ringan mempunyai ketahanan korosi yang baik dan hantaran listrik yang
baik dan sifat-sifat baik lainnya sebagai sifat logam. Sebagai tambahan terhadap
kekuatan mekaniknya yang sangat meningkat dengan penambahan Cu, Mg, Si,
Mn, Zn, Ni dan sebagainya, secara satu persatu atau bersama-sama, memberikan
juga sifat-sifat yang baik lainnya seperti ketahanan korosi, ketahanan aus,
koefisien pemuaian rendah dan sebagainya. Material ini sangat banyak
penggunaannya bukan saja untuk peralatan rumah tangga tapi juga dipakai untuk
keperluan material pesawat terbang, mobil, kapal laut, konstruksi dan sebagainya.
2.1.1 Sejarah aluminium
Aluminium adalah logam yang terbanyak di dunia. Logam 8 % dari bagian pada
kerak bumi. Boleh dikatakan setiap negara mempunyai persediaan bahan yang
mengandung aluminium, tetapi proses untuk mendapatkan aluminium logam dari
kebanyakan bahan itu masih belum ekonomis. Logam aluminium pertama kali
Pada tahun 1854, Henri Sainte-Claire Deville membuat aluminium dari
natrium-aluminium klorida dengan jalan memanaskan dengan logam natrium.
Proses ini beroperasi selama 35 tahun dan logamnya dijual dengan harga $ 220
per kilogram. Pada tahun 1886 Charles Hall mulai memproduksi aluminium
dengan skala besar seperti sekarang, yaitu melalui elektrolisis alumina didalam
kriolit (Na3AlF6) lebur. Pada tahun itu pula, Paul Heroult mendapat hak paten dar
Prancis untuk proses serupa dengan proses Hall. Hingga pada tahun 1893,
produksi aluminium menurut cara Hall ini sudah sedemikian meningkat, sehingga
harganya sudah jatuh menjadi $ 4,40 per kilogram. Industri ini berkembang
dengan baik, berdasarkan suatu pasaran yang sehat dan berkembang atas dasar
penelitian mengenai sifat-sifat aluminium dan cara-cara pemakaian yang
ekonomis bagi bahan itu. (Austin, G.T., 1990)
2.1.2 Sifat-sifat Aluminium
Dalam tiga dasawarsa terakhir ini aluminium telah menjadi salah satu logam
industri yang paling luas penggunaannya di dunia. Aluminium banyak digunakan
didalam semua sektor utama industri seperti angkutan, konstruksi, listrik, peti
kemas dan kemasan, alat rumah tangga serta peralatan mekanis.
Penggunaan aluminium yang luas disebabkan aluminium memiliki
sifat-sifat yang lebih baik dari logam lainnya seperti :
a. Ringan : memiliki bobot sekitar 1/3 dari bobot besi dan baja, atau
tembaga dan karenanya banyak digunakan dalam industri transportasi
b. Kuat : terutama bila dipadu dengan logam lain. Digunakan untuk
pembuatan produk yang memerlukan kekuatan tinggi seperti : pesawat
terbang, kapal laut, bejana tekan, kendaraan dan lain-lain.
c. Mudah dibentuk dengan semua proses pengerjaan logam. Mudah dirakit
karena dapat disambung dengan logam/material lainnya melalui
pengelasan, brazing, solder, adhesive bonding, sambungan mekanis, atau
dengan teknik penyambungan lainnya.
d. Tahan korosi : sifatnya durabel sehingga baik dipakai untuk lingkungan
yang dipengaruhi oleh unsur seperti air, udara, suhu dan
unsur-unsur kimia lainnya, baik di ruang angkasa atau bahkan sampai ke dasar
laut.
e. Konduktor listrik : setiap satu kilogram aluminium dapat
menghantarkan arus listrik dua kali lebih besar jika dibandingkan dengan
tembaga. Karena aluminium relatif tidak mahal dan ringan, maka
aluminium sangat baik untuk kabel-kabel listrik overhead maupun bawah
tanah.
f. Konduktor panas : sifat ini sangat baik untuk penggunaan pada
mesin-mesin/alat-alat pemindah panas sehingga dapat memberikan penghematan
energi.
g. Memantulkan sinar dan panas : Dapat dibuat sedemikian rupa sehingga
h. Non magnetik : dan karenanya sangat baik untuk penggunaan pada
peralatan listrik/elektronik, pemancar radio/TV. dan lain-lain, dimana
diperlukan faktor magnetisasi negatif.
i. Tak beracun : dan karenanya sangat baik untuk penggunaan pada
industri makanan, minuman, dan obat-obatan, yaitu untuik peti kemas dan
pembungkus.
j. Memiliki ketangguhan yang baik : dalam keadaan dingin dan tidak
seperti logam lainnya yang menjadi getas bila didinginkan. Sifat ini
sangat baik untuk penggunaan pada pemrosesan maupun transportasi
LNG dimana suhu gas cair LNG ini dapat mencapai dibawah -150 oC.
k. Menarik : dan karena itu aluminium sering digunakan tanpa diberi proses
pengerjaan akhir. Tampak permukaan aluminium sangat menarik dan
karena itu cocok untuk perabot rumah (hiasan), bahan bangunan dan
mobil. Disamping itu aluminium dapat diberi surface treatment, dapat
dikilapkan, disikat atau dicat dengan berbagai warna, dan juga diberi
proses anodisasi. Proses ini menghasilkan lapisan yang juga dapat
melindungi logam dari goresan dan jenis abrasi lainnya.
l. Mampu diproses ulang-guna yaitu dengan mengolahnya kembali
melalui proses peleburan dan selanjutnya dibentuk menjadi produk seperti
yang diinginkan Proses ulang-guna ini dapat menghemat energi, modal
dan bahan baku yang berharga. (Daryus, A., 2008)
Bahan baku utama untuk pengolahan aluminium adalah alumina. Alumina (Al2O3)
diperoleh dari pengolahan biji bauksit dengan proses bayer. Proses bayer terdiri
dari tiga tahap reaksi yaitu :
a. Proses Ekstraksi
Al2O3.xH2O + 2 NaOH 2NaAlO2 + (x+1) H2O
b. Proses Dekomposisi
2NaAlO2 + 4 H2O 2NaOH + Al2O3.3H2O
c. Proses Kalsinasi
Al2O3.3H2O + Kalor Al2O3 + H2O
Pada proses kalsinasi akan dihasilkan 2 jenis alumina, yaitu :
Alumina Sandy, yaitu alumina yang diperoleh dengan kalsinasi jika operasi
berlangsung pada temperature rendah.
Alumina Fluory, yaitu alumina yang diperoleh dengan proses kalsinasi jika
operasi berlangsung pada temperatur tinggi.
Alumina sandy diproduksi pada temperature pembakaran yang lebih
rendah dari pada alumina floury. Alumina sandy biasanya digunakan untuk
tungku tipe PAF (Prebaked Anode Furnace) karena sifat dari alumina tersebut
yang bebas mengalir tanpa dipengaruhi oleh gaya luar. Sedangkan alumina floury
sebagian besar digunakan untuk tungku tipe SAF (Soederberg Anode Furnace).
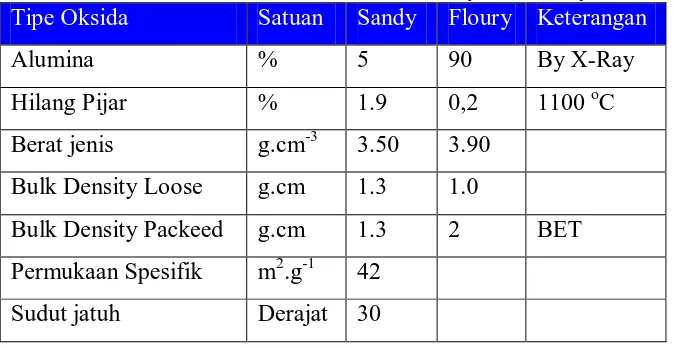
Tabel 2.1 Perbedaan sifat Alumina Sandy dan Floury
Tipe Oksida Satuan Sandy Floury Keterangan
Alumina % 5 90 By X-Ray
Hilang Pijar % 1.9 0,2 1100 oC
Berat jenis g.cm-3 3.50 3.90
Bulk Density Loose g.cm 1.3 1.0
Bulk Density Packeed g.cm 1.3 2 BET
2.2.1 Daya larut alumina (Al2O3) Pada cairan Kriolit
Didalam lelehan kriolit murni pada 975 oC, kira-kira 11% alumina (Al2O3) yang
dapat larut. Daya larut alumina (Al2O3) pada kriolit dipengaruhi oleh temperature
tambahan. Jika temperature diturunkan + 25o C, maka daya larut alumina (Al2O3)
akan turun + 7,5 % akibat adanya bahan tambahan.
2.2.2 Kecepatan Melarut Alumina (Al2O3) Pada Cairan Kriolit
Kecepatan alumina (Al2O3) didalam cairan kriolit dipengaruhi oleh temperatur
pemanasan alumina (Al2O3) dan beberapa bahan tambahan yang ditambahkan
kedalam lelehan kriolit. Alumina (Al2O3) yang dikalsinasi antara 800 oC - 900 oC
mempunyai kecepatan melarut yang besar di dalam cairan kriolit.
Hal ini sudah ditetapkan, bahwa partikel alumina (Al2O3) cepat melarut
pada cairan kriolit pada 4 sampai 8 detik dan butiran-butiran kasar melarut lebih
perlahan dibandingkan yang halus. Di lain pihak, alumina floury melarut lebih
perlahan dari pada alumina sandy. Perbedaan ini adalah akibat alumina sandy
mempunyai permukaan lebih besar bila dibandingkan alumina floury.
Pada pot peleburan (tungku reduksi), alumina (Al2O3) dimasukkan
kedalam pot dengan memecahkan kerak diatas bath/kriolit terlebih dahulu.
Jelaslah alumina (Al2O3) tidak larut seluruhnya di dalam bath/kriolit secara
tiba-tiba setelah penambahan, dan beberapa material langsung tenggelam ke dasar
pot/tungku membentuk sludge (lumpur) dibawah lapisan mtal. Terjadinya sludge
(lumpur) dalam jumlah yang banyak didalam pot/tungku akan merugikan setiap
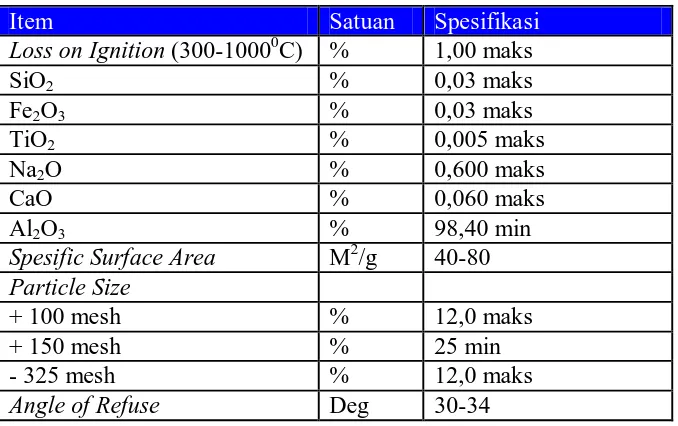
Tabel 2.2 Spesifikasi Alumina
Item Satuan Spesifikasi
Loss on Ignition (300-10000C) % 1,00 maks
SiO2 % 0,03 maks
Fe2O3 % 0,03 maks
TiO2 % 0,005 maks
Na2O % 0,600 maks
CaO % 0,060 maks
Al2O3 % 98,40 min
Spesific Surface Area M2/g 40-80 Particle Size
+ 100 mesh % 12,0 maks
+ 150 mesh % 25 min
- 325 mesh % 12,0 maks
Angle of Refuse Deg 30-34
Alumina (Al2O3) yang digunakan, diimport atau didatangkan dari
perusahaan-perusahaan penghasil alumina (Al2O3) yaitu dari Australia (Newco, Glencore,
Alcoa, Pechiney, dan Worsley), dan juga dari India (Nalco).(Anonymous, 1998)
2.2.3 Proses Pengolahan Alumina
Bauksit merupakan sumber utama aluminium dengan kadar alumina sekitar
40 – 60 % dan sisanya berupa silicon, titania, oksida, besi dan pengotor lainnya.
Alumina (Al2O3) adalah bahan baku utama untuk memproduksi aluminium,
alumina mempunyai morfologi sebagai bentuk bubuk putih. Alumina diperoleh
dari bauksit, melalui proses bayer, alumina yang dihasilkan dari proses bayer ini
mempunyai kemurnian yang tinggi dengan konsumsi energi yang relative rendah.
Proses perolehan alumina dari bauksit dapat dilakukan dengan proses bayer.
Proses bayer ini saat ini merupakan proses yang paling banyak digunakan. Proses
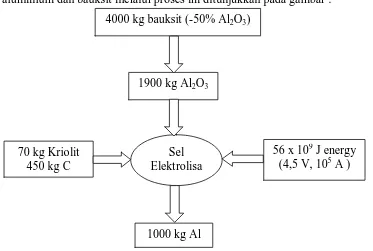
4000 kg bauksit (-50% Al2O3)
1900 kg Al2O3
70 kg Kriolit 450 kg C
56 x 109 J energy (4,5 V, 105 A ) Sel
Elektrolisa
Al2O3.xH2O + 2 NaOH 2NaAlO2 + (x+1) H2O
Selanjutnya dilakukan pengendapan alumina terhidrat menurut reaksi :
2NaAlO2 + 4 H2O + Kalor Al2O3 + 3 H2O
Dengan temperatur kalsinasi sekitar 1250 oC (Burkin,A.R., 1987)
Pada proses bayer, dimana bauksit dipekatkan untuk menghasilkan
aluminium hidroksida [Al(OH)3]. Saat larutan pekat ini dikalsinasi pada suhu
lebih dari 1000 oC, maka Al2O3 akan terbentuk. Al2O3 meleleh pada suhu diatas
2000 oC. Temperatur ini terlalu tinggi untuk digunakan sebagai medium pelelehan
untuk pembentukan elektrolisis dari aluminium bebas. Proses elektrolisis secara
komersial digunakan untuk menghasilkan aluminium yang dikenal dengan proses
Hall, dinamakan dengan nama penemunya Charles M. Hall, Al2O3 yang telah
dipurifikasi/dibersihkan dilarutkan dalam lelehan kriolit (Na3AlF6) yang memiliki
titik leleh 1012 oC dan berguna sebagai konduktor aliran listrik yang konduktif.
Batang karbon digunakan sebagai anoda dan digunakan dalam proses elektrolisis.
Reaksi dari anoda dapat ditunjukkan dengan persamaan :
Anoda : C(s) + 2 O2- CO2 + 4e
Katoda : Al3+ + 3e Al
Jumlah bahan baku dan energy yang dibutuhkan untuk menghasilkan 1000 kg
(Brown,Theodore L., 2000)
2.4 Elektrolit [Kriolit/bath(Na3AlF6)]
Dalam proses peleburan aluminium secara elektrolisa, media penghantar arus
listrik yang digunakan yaitu elektrolit. Bahan baku utama dari elektrolit yang
digunakan untuk peleburan aluminium adalah kriolit (Na3AlF6) disamping
bahan-bahan tambahan-bahan lainnya.
Bath adalah leburan dari kriolit (Na3AlF6) yang terionisasi menjadi ion sodium
(ion positif) dan ion heksafluoroaluminat (ion (-)) :
(Na3AlF6) 3 Na+ + AlF6
3-Ion-ion heksafluoroaluminat akan terurai lagi menjadi :
AlF63- AlF52- + F
-2 e + AlF63- AlF54- + F
-Leburan kriolit sangat baik sebagai pelarut alumina (Al2O3) karena ion-ion AlF6
3-reaktif terhadap alumina (Al2O3).
Pada konsentrasi alumina (Al2O3) yang rendah, reaksi yang terjadi yaitu :
Al2O3 + 4 AlF63- 3 Al2OF62- + 6 F
-Pada konsentrasi alumina (Al2O3) yang tinggi, reaksi yang terjadi yaitu :
2 Al2O3 + 2 AlF63- 3 Al2O2F4
2-Ion-ion yang ada di dalam bath yaitu :
Na+, F- ,AlF4-, AlF52-, AlF63-, Al2OF62-, Al2O2F42-
Ion dengan muatan positif (+) akan tertarik ke katoda dan yang bermuatan negatif
(-) akan tertarik ke anoda. Ion Na+ membawa 95 % - 99 % arus listrik, sisanya ion
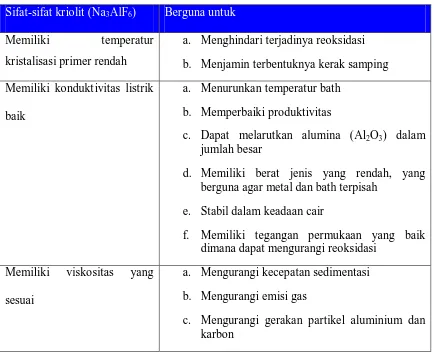
Tabel 2.3 Sifat-sifat kriolit dan kegunaannya
Sifat-sifat kriolit (Na3AlF6) Berguna untuk
Memiliki temperatur
kristalisasi primer rendah
a. Menghindari terjadinya reoksidasi
b. Menjamin terbentuknya kerak samping
Memiliki kondukt ivitas listrik
baik
a. Menurunkan temperatur bath
b. Memperbaiki produktivitas
c. Dapat melarutkan alumina (Al2O3) dalam
jumlah besar
d. Memiliki berat jenis yang rendah, yang
berguna agar metal dan bath terpisah
e. Stabil dalam keadaan cair
f. Memiliki tegangan permukaan yang baik
dimana dapat mengurangi reoksidasi
Memiliki viskositas yang
sesuai
a. Mengurangi kecepatan sedimentasi
b. Mengurangi emisi gas
c. Mengurangi gerakan partikel aluminium dan
karbon
Tabel 2.3 Komponen Bath Pada Dapur Peleburan di PT INALUM
Komponen Kandungan (%)
Aluminium Fluorida (AlF3) 5 – 8
Kalsium Fluorida (CaF2) 3 – 4
Alumina (Al2O3) 1 – 8
Kriolit (Na3AlF6) 79 – 90
Sumber : Operasi Tungku Reduksi PT INALUM (2003)
(Anonymous, 2003)
Bahan elektrolit ditambahkan melalui sel disekitar anode, pada waktu
bahan-bahan ini berangsur-angsur melebur, anode itu dinaikkan sehingga selnya
dari kriolit (Na3AlF6) dan sisanya AlF3, serta CaF2 6% sampai 10 % dan Al2O3 2
% sampai 6 %. Sebagian kriolit diimpor ke Amerika Serikat dari Greenland, tetapi
sebagian besar dibuat secara sintetis. AlF3 juga dibuat secara sintetis dari hidrogen
fluoride (HF) dan aluminium hidroksida (Al(OH)3.
Pengendalian komposisi elektrolit merupakan hal yang sangat penting
dalam proses produksi aluminium. Oleh karena titik leleh kriolit murni adalah
1009 oC, elektrolit itu mengandung kalsium flourida (CaF2) dan sisa AlF3, yang
bersama alumina yang terlarut dapat menurunkan titik leleh cukup rendah
sehingga sel itu dapat beroperasi pada suhu sekitar 940oC – 980oC. Kelebihan
AlF3 juga dapat menigkatkan efisiensi. Perbandingan berat NaF/AlF3 didalam
kriolit adalah 1,50 ; kelebihan AlF3 didalam kriolit (Na3AlF6) diatur sedemikian
rupa, sehingga menghasilkan rasio NaF/AlF3 sekitar 1,10 sampai 1,40. Dalam
beberapa minggu pertama setelah sel yang baru diberi pelapis itu beroperasi,
elektrolit itu diserap dengan cepat kedalam pelapis dan isolasi.
Komponen utama penyusun elektrolit adalah kriolit (Na3AlF6) yang
berfungsi sebagai pelarut dan alumina yang berfungsi sebagai zat terlarut, serta
beberapa zat aditif lainnya. Kriolit (Na3AlF6) digunakan dalam proses elektrolisa
aluminium, karena sifat-sifatnya yang unik dan mampu melarutkan berbagai jenis
oksida dengan baik, sifat-sifat kriolit diantaranya :
a. Kemampuan melarutkan alumina dengan baik
b. Tegangan komposisi lebih tinggi
c. Konduktivitas elektrolitnya cukup tinggi.
d. Titik leburnya relatif rendah
g. Masa jenisnya cukup rendah, bila dalam keadaan sama-sama cair
h. Tekanan uapnya relatif rendah.
Pada tekanan atmosfer aluminium fluoride (AlF3) tidak dapat dijumpai
dalam bentuk cair. Cairan kriolit-alumina juga mengandung kalsium fluorida
(CaF2) atau natrium flourida (NaF) membentuk komposisi kriolit 3NaF-AlF3.
Kriolit sebagai elektrolit dalam reduksi aluminium juga harus memenuhi
syarat-syarat elektrolit yang dibutuhkan sebagai berikut :
a. Temperatur kristalisasi primer rendah
b. Konduktivitas listrik yang baik
c. Dapat melarutkan alumina dalam jumlah besar
d. Mempunyai berat jenis kecil
e. Stabil dalam keadaan cair
Oleh karena itu untuk memperbaiki sifat-sifat dari elektrolit yang ada maka
biasanya dilakukan penambahan atau pencampuran dengan beberapa zat aditif,
seperti : Flourida atau klorida dari logam alkali, AlF3 dan CaF2 dan juga biasa
digunakan MgF2, LiF, dan NaCl. (Grjotheim, 1986)
2.5 Elektrolisa
Hampir semua logam aluminium primer dihasilkan dengan proses elektrolisa
Hall-Heroult. Bahan baku yang digunakan terdiri dari alumina, karbon, kriolit,
CaF2, HF, AlF3 dan tenaga listrik. Terdapat dua jenis tungku reduksi yang
dipergunakan dalam industry peleburan aluminium yaitu Prebaked Anode
Furnace (PAF) dan Soderberg Anode furnace (SAF). Perbedaan kedua tipe
tungku tersebut terletak pada cara pemanggangan anodanya, dalam sistem PAF
anoda dipanggang terlebih dahulu (prebaked) sebelum dipergunakan. Sedangkan
dimasukkan langsung ke dalam tungku reduksi. Pabrik peleburan aluminium di
Kuala Tanjung menggunakan sistem PAF yang telah dikembangkan oleh
Sumitomo Aluminium Smelting Co., Ltd.
Reaksi kimia yang terpenting yang terjadi di tungku reduksi, adalah reaksi
elektrolisa untuk menghasilkan logam aluminium. Dengan mengalirkan listrik
arus searah, terjadi elektrolisa alumina menjadi ion-ion positif dan ion-ion negatif
Al2O3 2 Al3+ + 3 O2-. Ion aluminium tertarik ke katoda dan dinetralisisr
sehingga terbentuk aluminium. Demikian juga ion zat asam mendekati anoda
kemudian dinetralisir. Selain daripada itu terjadi juga reaksi reduksi, dimana
karbon yang berasal dari anoda berfungsi sebagai reduktor mengikat asam :
2 Al2O3 + 3 C 4 Al + 3 CO2
Aluminium cair yang terkumpul di bagian bawah tungku selanjutnya dihisap dan
dibawa ke pabrik penuangan
Pada proses Hall-Heroult, logam aluminium diperoleh melalui dari
alumina dengan menggunakan cairan kriolit (Na3AlF6), (titik lebur 1000 oC) yang
digunakan sebagai pelarut. Sejumlah besar aluminiun oksida/alumina (Al2O3)
dilarutkan dalam kriolit, dimana larutan kriolit dapat menurunkan titik lebur
alumina. Campuran kriolit dan aluminium oksida di elektrolisa dalam sel dan sel
lapisan karbon yang berfungsi sebagai katoda tersimpan di dalam cairan
aluminium. Pada operasi sel, cairan aluminium berada pada bagian bawah sel.
Dari waktu ke waktu aluminium cair akan disedot dan selanjutnya akan dibawa ke
bagian casting untuk dicetak. Pada operasi sel ini diperlukan tegangan sebesar 4,0
sampai 5,5 Volt, dan arus yang digunakan dari 50,000 sampai 150,000 kA.
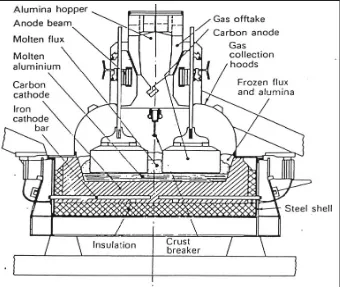
2.5.1 Proses Hall-Heroult
Alumina yang dihasilkan dari proses pemurnian masih mengandung oksigen
sehingga harus dilakukan proses selanjutnya yaitu peleburan. Peleburan alumina
dilakukan dengan proses reduksi elektrolitik. Proses peleburan ini memakai
metode Hall-Heroult.
Alumina dilarutkan dalam larutan kimia yang disebut kriolit pada sebuah
tungku yang disebut pot. Pot ini mempunyai dinding yang dibuat dari karbon.
Bagian luar pot terbuat dari baja. Aliran listrik diberikan melalui anoda dan
katoda. Proses reduksi memerlukan karbon yang diambil dari anoda. Pada proses
ini dibutuhkan arus listrik searah sebesar 50 - 150 kiloampere.
Arus listrik akan mengelektrolisa alumina menjadi aluminium dan oksigen
bereaksi membentuk senyawa CO2. Aluminium cair dari hasil elektrolisa akan
turun ke dasar pot dan selanjutnya dialirkan dengan prinsip siphon ke krusibel
yang kemudian diangkut menuju tungku-tungku pengatur (holding furnace).
Kebutuhan listrik yang dihabiskan untuk menghasilkan 1 kg aluminium berkisar
sekitar 12 - 15 kWh. Satu kg aluminium dihasilkan dari 2 kg alumina dan ½ kg
karbon. Reaksi permunian alumina menjadi aluminium adalah sebagai berikut :
970 oC
2 Al2O3 + 3 C 4 Al + 3 CO2
Na3AlF6
Gambar 2.2 Proses peleburan Al2O3 menjadi aluminium dengan cara elektrrolisa.
2.5.2 Produksi Aluminium
Aluminium adalah logam yang sangat reaktif yang membentuk ikatan kimia
berenergi tinggi dengan oksigen. Dibandingkan dengan logam lain, proses
ekstraksi aluminium dari batuannya memerlukan energi yang tinggi untuk
mereduksi Al2O3. Proses reduksi ini tidak semudah mereduksi besi dengan
menggunakan batubara, karena aluminium merupakan reduktor yang lebih kuat
dari karbon. Proses produksi aluminium dimulai dari pengambilan bahan tambang
yang mengandung aluminium (bauksit, corrondum, gibbsite, boehmite, diasphore,
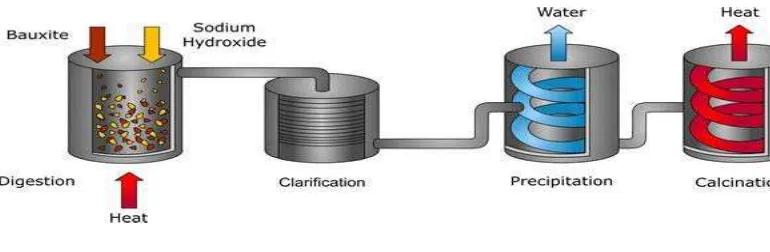
Gambar 2.3 : Proses Bayer
Proses Bayer menghasilkan alumina (Al2O3) dengan membasuh bahan tambang
yang mengandung aluminium dengan larutan natrium hidroksida pada temperatur
175oC sehingga menghasilkan aluminium hidroksida, Al(OH)3. Aluminium
hidroksida lalu dipanaskan pada suhu sedikit diatas 1000oC sehingga terbentuk
alumina dan H2O yang menjad uap air. Setelah alumina dihasilkan, alumina
dibawa ke proses Hall-Heroult. Proses Hall-Heroult dimulai dengan melarutkan
alumina dengan lelehan Na3AlF6 atau yang biasa disebut kriolit. Larutan lalu
dielektrolisis dan akan mengakibatkan aluminium cair menempel pada anoda,
sementara oksigen dari alumina akan teroksidasi bersama anoda yang terbuat dari
karbon, membentuk karbon dioksida. Aluminium cair memiliki massa jenis yang
lebih ringan dari pada larutan alumina, sehingga pemisahan dapat dilakukan
dengan mudah. Elektrolisis aluminium dalam proses Hall-Heroult menghabiskan
energi yang cukup banyak. Rata-rata konsumsi energi listrik dunia dalam
mengelektrolisis alumina adalah 15 kWh per kilogram aluminium yang
dihasilkan. Energi listrik menghabiskan sekitar 20-40 % biaya produksi
aluminium di seluruh dunia. (www.scribd.com)
2.6 Anode effect
Anode effect sering terjadi pada proses elektrolisa dari garam logam. Anode effect
Tanda fisiknya adalah timbulnya gelembung gas CO2 pada bagian bawah anoda,
yang menandakan menurunnya kemampuan elektrolit (Na3AlF6) untuk
membasahi anoda. Akhirnya gelembung-gelembung gas CO2 tersebut akan
bergabung untuk membentuk suatu lapisan tunggal yang akan menutupi sebagian
besar permukaan anoda. Dengan sumber arus listrik yang tetap, beda potensial
listrik akan naik lebih dari 30 volt. Hal ini disebabkan oleh gelembung gas CO2
yang besar dan akan menaikkan rapat arus lokal pada anoda. Satu-satunya cara
agar arus dapat melalui lapisan gas CO2 pada permukaan anoda adalah dengan
cara lompatan listrik (electric arching).
Beda tegangan listrik akan naik perlahan seiring dengan kurangnya
alumina (Al2O3) sampai suatu harga konsentrasi kritis tertentu yang berkisar
antara 1 % - 2 % berat, tergantung dari rapat arus, suhu, konveksi larutan elektrolit
(Na3AlF6), komposisi larutan elektrolit (Na3AlF6) , dan bentuk dari anoda. Anoda
effect dapat juga terjadi saat konsentrasi alumina (Al2O3) yang lebih tinggi dengan
menaikkan rapat arus.
Akibat dari anoda effect pada proses elektrolisis aluminium pada sel
Hall-Heroult yaitu adalah perubahan dari komposisi gas-gas anoda terutama CO2
menjadi CO yang disertai dengan terbentuknya gas carbontetrafluoro (CF4)
sebanyak 3 – 25 % dan sedikit gas hexafluoroetana (C2F6). Gas-gas ini akan
menutupi permukaan aktif anoda sebagai lapisan film di permukaan. Lapisan ini
juga mempengaruhi sifat pembasahan dari lapisan antar muka dan juga bertindak
sebagai penghambat listrik.
efiensi arus akan meningkat saat terjadinya anode effect, namun seiring dengan
naiknya suhu sebagai akibat dari naiknya beda tegangan listrik pada sel, maka
efiensi arus akan menurun.
2.6.1 Gejala-gejala dan penyebab terjadinya anode effect
a. Tingginya beda potensial / voltase pada anoda
b. Terjadinya pergerakan / gejolak molten dan bath yang kuat
c. Buruknya kemampuan bath (Na3AlF6) yang membasahi anoda.
Anode effect (AE) disebabkan karena kekosongan alumina (Al2O3) yang ada di
dalam bath (Na3AlF6). Hal ini diawali dengan ditandai dengan adanya kenaikan
tegangan / voltase yang lambat ataupun secara drastis/cepat hingga 20-50 volt.
Namun penyebab terjadinya anode effect secara mekanisme merupakan suatu
persoalan yang akan tetap dibahas, diantaranya adalah :
a. Kekosongan alumina (Al2O3) dalam bath (Na3AlF6) yang akan mengarah
kepada pembebasan ion fluoride.
b. Pembasahan pada permukaan anoda oleh bath (Na3AlF6) akan menjadi
semakin memburuk, yang kemungkinan dikarenakan oleh adanya
pembentukan ikatan C-F.
c. Beberapa jenis film gas yang terbentuk akan memiliki tahanan elektrik
yang tinggi.
d. Arus listrik sebagian akan dibawa secara terbatas pada satu tempat saja
(permukaan anoda akan terkikis).
Gas tetrafluorometana (CF4) dan gas hexafluoroetana (C2F6) akan terbentuk :
Na3AlF6 + C Al + ½ C2F6 + 3 NaF
Adapun komposisi gas selama terjadinya Anode effect (AE), yaitu :
CF4 = 5 – 20 % (+ < 1 % C2F6)
CO2 = 10 – 20 %
CO = 60 – 70 %
AE terjadi saat arus kritis < arus tungku
% Al2O3 pada saat AE : 0,5 – 2,5 wt %
Kandungan Al2O3 yang rendah (< 1 %) : anoda bersih dari
gelembung-gelembung gas dan operasi berjalan sebagaimana yang diharapkan. Kandungan
Al2O3 yang tinggi terbentuknya debu karbon, gejolak metal dan tungku menjadi
dingin sehingga tidak dapat beroperasi sebagaimana yang direncanakan.
2.6.2 Keuntungan dan kerugian anode effect
Keuntungan dari adanya peristiwa anode effect yaitu :
a. Proses elektrolisa di dalam tungku berjalan
b. Operasi tungku terkontrol (yakni dalam hal pemasukan alumina (Al2O3)
c. Permukaan blok anoda bersih dari gelembung gas dan debu karbon.
Kerugian dari adanya peristiwa Anode effect yaitu :
a. Pemanasan lanjut (Overheating), pemborosan energy
b. Meleburnya kerak dinding samping
c. Kehilangan efisiensi arus
d. Terjadi emisi gas CF4 dan C2F6
2.6.3 Penanggulangan Anode effect
Adapun metode kerja yang dapat dilakukan dalam penanggulangan Anode effect, yaitu :
c. Putus setrum anoda-katoda
Prosedur Manual :
a. Pipa baja diarahkan kebawah permukaan anoda (tempat terselubungnya
gas dan debu karbon)
b. Mengalirkan udara tekan pada klem yang menjepit batang anoda.
Prosedur Otomatis
a. Udara tiup di dalam pipa mengalir menuju anoda
b. Menaik-turunkan anoda
c. Pemutusan arus dengan pemasangan PHS (Pasak Hubung Singkat)
Untuk saat ini pengatasan Anode effect yang dilakukan oleh banyak pekerja yang
ada pada peleburan peleburan aluminium masih terbatas.
2.6.4 Mekanisme Anode effect (AE)
Sebagai hasil elektrolisa, kandungan alumina (Al2O3) pada bath akan turun 0,5 %
- 1 % dan pada saat alumina 0,5 % maka pada permukaan anoda akan terbentuk
flourin yang memungkinkan terbentuknya lapisan karbon carbontetrafluorida
(CF4) sehingga akan mengakibatkan terhambatnya penyaluran arus listrik. Secara
terus menerus maka akan terbentuk lapisan gas pada anoda. Bila kandungan
alumina (Al2O3) pada bath menurun, maka elektrolit dakn berhenti membasahi
anoda dan gas bebas akan berkumpul dipermukaan anoda, yang mengakibatkan
tahanan arus listrik juga akan bertambah.
Anode effect (AE) akan menyebabkan tegangan permukaan pada anoda
atau pada lapisan elektrolit pada kerapatan arus listrik kritis dimana tergantung
pada kapasitas pembasahan dari pada cairan garamnya. Kenaikan anode effect
sulit untuk bergerak keluar. Kejadian ini sering muncul dalam hal temperatur bath
rendah, sebab adanya penghentian atau pengurangan tenaga listrik.
Kemampuan yang diberikan oleh campuran garam untuk menimbulkan anode
effect (AE) dapat disebut sebagai kerapatan arus kritis. Kerapatan arus yang
maksimum dicapai sebelum reaksi anoda menjadi normal yang digantikan oleh
anode effect (AE). Kerapatan arus kritis dipengaruhi oleh komposisi bath
(Na3AlF6), temperatur bath dan bahan baku anoda, namun sebahagian besar faktor
yang mempengaruhi anode effect (AE) adalah kandungan alumina (Al2O3)
didalam bath itu sendiri sedikit, oleh sebab itu sangat perlu dipertimbangan dalam
pengoperasian pot yang optimum.
Kedalaman anoda adalah panjang anoda yang terendam didalam bath, hal
ini juga berhubungan dengan terjadinya anode effect (AE). Bila panjang tersebut
besar maka terjadinya anode effct (AE) akan kecil, dimana hal ini dapat
diilustrasikan sebagai variasi karapatan arus listrik. (Anonymous, 1998).
2.7 Alumina feeding (pemasukan alumina)
2.7.1 Alumina Feeding
Alumina feeding sebagian besar biasanya terdapat dalam prosedur sel
Hall-Heroult. Jadi, ini dilakukan dengan pengisian dan bentuk yang sangat berbeda dari
operasi yang strategis. Grjotheim telah menjelaskan beberapa karakteristik dan
konsekuensi termal untuk tipe aluminium yang berbeda, gambarannya sangat
berbeda untuk karakteristik break and feed, kebutuhan panas dan kecenderungan
endapannya (sludge), awalnya menunjukkan keuntungan dari teknik feeding
a. Dalam pembentukan lumpur/endapan (sludge) dapat diperkecil.
b. Konsentrasi alumina (Al2O3) didalam bath dapat dijaga tetap konstan.
c. Bilangan dari anode effect (AE) dapat menurun secara drastis.
Aplikasi dari proses pengontrolan alumina (Al2O3) adalah bentuk dari asumsi
bahwa kehabisan dari alumina (Al2O3) dengan waktu tertentu. Strategi
pengontrolan digunakan untuk menjaga konsentrasi alumina (Al2O3) di dalam
bath dibagian sempit dengan konsentrasi (+ 0,5 % massa) dalam alumina (Al2O3)
yang rendah pada sisi sel yang minimum.
Aliran / kecepatan feeding cocok dengan pertambahan berat unit per
waktu, tetapi karena pembuangan yang lain mempunyai berat yang sama, dan itu
tentu mempunyai waktu interval yang berlainan. Pada waktu periode tertentu
alumina (Al2O3) yang masuk ke dalam interval waktu yang singkat kepada aliran
normal dari pemakaian alumina (Al2O3) dalam sel dan pada periode alumina
(Al2O3) yang lain pemasukan alumina (Al2O3) pada interval yang lama
(underfeeding).
2.7.2 Pemasukan Alumina (Al2O3) ke larutan kriolit
Secara pokok, pemasukan alumina (Al2O3) ke sel terdiri dari memecahkan pada
pembuka pada lapisan kulit/kerak atas yang beku dan kemudian untuk dilarutkan
kedalam bath dan untuk memperbaiki thermally-insulating lapisan kulit. Dengan
tempat modern pemasukan ke dalam lobang mungkin tetap terbuka di antara
setiap tambahan alumina (Al2O3). Dulunya, pemecahan kerak dilakukan secara
manual, yang merupakan sebuah pekerjaan yang kasar pada waktu itu, khususnya
saat kerak itu keras dan kuat. Pada saat pemasukan alumina (Al2O3) dilakukan
BAB III
METODE PERCOBAAN
3.1 Alat-alat yang digunakan
1. Pada tungku reduksi/peleburan tipr Prebaked Anode Furnace (PAF),
terdiri dari :
- Kerangka baja
- Penutup bagian samping
- Gas duct
- Alumina hopper
- Dump gate
- Pemecah kerak
- Jack
- Clamp
- Anode bus bar
- Cathode bus bas
- Blok anoda
- Blok katoda
2. Pada ruangan sistem control semi desentralisas, terdiri dari :
- Level 0 (RIOU / Remote Input Output Unit)
- Level 1 (RT VAX / Remote Terminal VAX)
- level 2 (MICRO VAX)
3. Anode Changing Crane (ACC)
3.2 Bahan-bahan
- Alumina (Al2O3)
- Bath (Na3AlF6)
- Power Supply
3.3Prosedur Kerja
3.3.1 Prosedur Anode effect (AE)
a. AE terjadi saat konsentrasi alumina (Al2O3) didalam bath < 1 % yang
ditandai dengan pertambahan voltase yang drastis sehingga terbentuk
gas CO2 dan debu karbon dari bawah blok anoda.
b. Didalam kondisi AE normal dapat dilakukan secara otomatis oleh
komputer. Bila voltase tungku < 6 volt maka AE dianggap sudah
berakhir.
c. Disamping dilakukan dengan komputerisasi, pekerjaan manual di
lapangan tetap dilakukan, yaitu :
- Tombol panel swtich pada RIOU diputar posisinya ke ”manual”,
lalu tombol AE reset ditekan.
- Kemudian posisi anoda dinaik-turunkan dengan menggunakan
ACC dengan cara mengalirkan udara tekan pada klem yang
menjepit batang anoda.
- Setelah itu panel switch diputar kembali ke posisi ”auto” bila
voltase pot sudah turun < 6 volt.
3.3.2 Prosedur Alumina Feeding
a. Alumina (Al2O3) yang diperlukan sebagai bahan baku utama dapat
dilakukan dengan bantuan ACC (Anode Changing Crane) pada saat
maupun dari alumina hopper yang kemudian sudah diatur selang
waktu pemasukan alumina ke pot/tungku melalui dump gate dengan
memecahkan kerak oleh teet blade yang semuanya diatur oleh sistem
control sentral komputer RT VAX dan MICRO VAX.
b. Dari ACC itu sendiri telah diset/diatur untuk setiap melakukan
breaking crust maka akan disemburkan/dimasukkan alumina (Al2O3)
sebanyak 260 kg, sedangkan pengaturan dari sentral komputer RT
VAX dan MICRO VAX terhadap dump gate yang berkapasitas 20 kg
alumina (Al2O3) akan beroperasi dalam selang waktu yang telah
ditentukan.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Data
Data hasil pengamatan operasi tungku reduksi pada pabrik peleburan
[image:43.595.124.500.251.590.2]aluminium PT INALUM, Kuala Tanjung, Batubara.
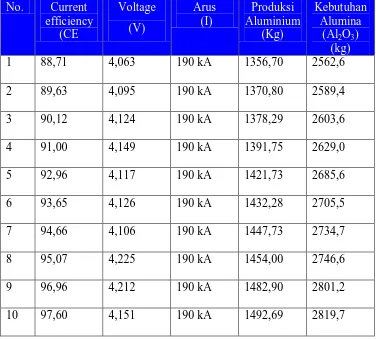
Tabel 4.1 Data Hasil Pengamatan Efisiensi Arus (CE)
No. Current
efficiency (CE
Voltage
(V)
Arus (I)
Produksi Aluminium
(Kg)
Kebutuhan Alumina
(Al2O3)
(kg)
1 88,71 4,063 190 kA 1356,70 2562,6
2 89,63 4,095 190 kA 1370,80 2589,4
3 90,12 4,124 190 kA 1378,29 2603,6
4 91,00 4,149 190 kA 1391,75 2629,0
5 92,96 4,117 190 kA 1421,73 2685,6
6 93,65 4,126 190 kA 1432,28 2705,5
7 94,66 4,106 190 kA 1447,73 2734,7
8 95,07 4,225 190 kA 1454,00 2746,6
9 96,96 4,212 190 kA 1482,90 2801,2
10 97,60 4,151 190 kA 1492,69 2819,7
Harga-harga parameter tetap :
a. Arus (I) = 190 kA
b. Volume Dump Gate (VG) = 20 kg
c. Spray alumina (Al2O3) pada saat Anode Changing (AC) = 260 kg
d. Tetapan faraday = 0,3354
Very Fast Feed Rate = 10 menit
Fast Feed Rate = 14 menit
Normal Feed Rate = 18 menit
f. Masa berlakunya feeding strategi yang diatur oleh komputer untuk :
Very Fast Feed Rate = 60 menit
Fast Feed Rate = 480 menit
Normal Feed Rate = 660 menit
g. Anode effect (AE) datang saat konsentrasi alumina (Al2O3) dalam bath (Na3AlF6) = < 1%
h. Quantity Bath (Qs) = 4000 kg
i. Konsentrasi alumina (Al2O3) dalam bath dijaga antara 2 % - 3 %
4.2 Perhitungan
Reaksi Umum Elektrolisis
a Al2O3 + b C c Al + d CO2
2 Al2O3 + 3 C 4 Al + 2 CO2
a. Produksi Aluminium (Al) per hari :
P = 0,3354 x I x % CE x 24 jam
b. Kebutuhan alumina (Al2O3) per hari (UCD)
UCD =
(
BeratMolekulAl O)
( )
PAl Ar c a 3 2 1
c. Kebutuhan alumina (Al2O3) per menit (UCDt)
) 24 60
( menitx jam UCD UCDt=
d. Alumina Feeding Rate =
t
UCD
Gate Dump Volume
e. Pada saat Anode effect, konsentrasi alumina (Al2O3) dinaikkan ke 2% dan
maka akan terbentuk lumpur (Sludge). Oleh karena itu dibutuhkan alumina
(Al2O3) 2 % - 1 % = 1%, yang berartu 1 % dari Quantity Bath (Qs) = 4000 kg.
Maka akan dapat ditentukan % Al2O3 selama VFFR, FFR, dan NFR.
%Al2O3 selama VFFR 2 % +
(
)
− t UCD x VFFR VG x VFFR VFFR 1 0 1
%Al2O3 selama FFR = %Al2O3 VFFR +
(
)
− t UCD x FFR VG x FFR FFR 1 0 1
Untuk FFR, dimana dilakukan pada saat Anode Changing (AC), maka :
Al2O3 dalam bath = Jumlah Al2O3 selama FFR + Jumlah Al2O3 saat AC pada FFR
%Al2O3 selama NFR = %Al2O3 NFR +
(
)
− t UCD x NFR VG x NFR NFR 1 0 1
f. Anode effect datang pada saat % Al2O3 = 1 % = 0,01 x Qs = 0,01 x 4000 kg = 40
kg yang terjadi pada menit ke ”A” setelah FFR (480 menit = jam ke 8),maka
dapat ditentukan frekwensi Anode effect per hari (f AE).
% Al2O3 pada saat AE= %Al2O3 FFR +
(
)
− t UCD x A VG x NFR A 0 Atau − − = t o UCD NFR VG AE O Al FFR O Al
A % 2 3 % 2 3
Maka : A FFR durasi jam waktu hari per AE f + = 24
Contoh Perhitungan :
Pada % CE = 88,71 % dan arus (I) = 190 kA
UCD =
( )(
102 1356,7)
27 1 4 2 = 2562,65 kg
menit kg menit jam x menit
UCDt 1,779 /
) 1440 ( 8 , 2562 ) 24 60 ( 8 , 2562 = = =
Alumina Feeding Rate =
menit kg kg / 779 , 1 20
= 11,24 menit
Artinya, alumina harus dimasukkan setiap 11,24 menit
%Al2O3 VFFR = 2 % +
(
)
− menit kg x menit kg x menit menit / 779 , 1 60 20 10 60
= 80 kg + [120 kg – 106,74 kg]
= 100%
4000 26 , 93 x kg kg
= 2,33 %
%Al2O3 FFR = 2,33 % +
(
)
− menit kg x menit kg x menit menit / 779 , 1 480 20 14 480
= 93,26 kg + [685,7 kg – 853,92 kg]
= 74,96 kg + 260 kg
= 100%
kg 4000
kg 334,96
x = 8,374 %
%Al2O3 NFR = 8,374 %+
(
)
− menit kg x menit kg x menit menit / 779 , 1 660 20 18 660
= 334,96 kg + [733,3 kg – 1174,14 kg]
= 100%
kg 4000
kg 105,88
x = 2,65 %
% Al2O3 pada saat AE= 8,374 %+
(
)
−
x kg Ax kg menit
− − = menit kg menit kg A / 779 , 1 18 20 % 1 % 374 , 8 =
(
kg menit)
kg kg / 667 , 0 40 96 , 334 − A =(
kg menit)
kg / 667 , 0 92 , 188= 442,21 menit = 7,37 jam
Anode effect datang setelah (480 menit = setelah jam ke 8), artinya Anode effect
datang pada jam ke 9 + 7,37 jam = 16,37 jam (yang dinyatakan untuk jam
terjadinya anode effect). Jadi :
f Anode effect per hari = kali hari jam jam / 46 , 1 37 , 16 24 =
Untuk % Current Effisiensi, 89,63 % sampai 97,60 % dilakukan dengan cara
[image:47.595.115.508.413.717.2]perhitungan dan perlakuan yang sama.
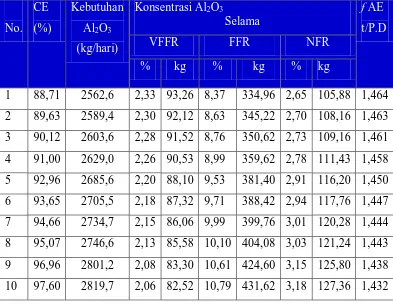
Tabel 4.2. Data Hasil Perhitungan Konsentrasi Al2O3 Terhadap Frekwensi AE
No. CE
(%)
Kebutuhan
Al2O3
(kg/hari)
Konsentrasi Al2O3
Selama
f AE
t/P.D
VFFR FFR NFR
% kg % kg % kg
1 88,71 2562,6 2,33 93,26 8,37 334,96 2,65 105,88 1,464
2 89,63 2589,4 2,30 92,12 8,63 345,22 2,70 108,16 1,463
3 90,12 2603,6 2,28 91,52 8,76 350,62 2,73 109,16 1,461
4 91,00 2629,0 2,26 90,53 8,99 359,62 2,78 111,43 1,458
5 92,96 2685,6 2,20 88,10 9,53 381,40 2,91 116,20 1,450
6 93,65 2705,5 2,18 87,32 9,71 388,42 2,94 117,76 1,447
7 94,66 2734,7 2,15 86,06 9,99 399,76 3,01 120,28 1,444
8 95,07 2746,6 2,13 85,58 10,10 404,08 3,03 121,24 1,443
9 96,96 2801,2 2,08 83,30 10,61 424,60 3,15 125,80 1,438
4.3 Pembahasan
Pada operasi tungku peleburan aluminium sangat diperlukan sekali penguasaan
strategi demand feeding alumina yang tujuannya untuk memperkecil frekwensi
terjadinya anode effect disamping itu pula bertujuan untuk mencegah terjadinya
lumpur alumina (sludge) pada dasar tungku seminimal mungkin agar didapat
produksi aluminium yang maksimum, dan perlu juga ketersediaan power supply
untuk meningkatkan efisiensi arus (Current Efficiency) pada tungku operasi
peleburan aluminium.
Jumlah alumina (Al2O3) yang dibutuhkan per harinya untuk elektrolisa
adalah 2562,2 kg/pot.hari dengan konsentrasi alumina (Al2O3) yang optimum di
dalam larutan bath (Na3AlF6) antara 2 % sampai 3 % serta frekwensi anode effect
antara 1,4 – 1,5 kali/pot.hari dan efisiensi arus antara 88,71 % sampai 97,60 %
pada operasi tungku reduksi di pabrik peleburan aluminium PT INALUM.
Konsentrasi alumina (Al2O3) dalam larutan bath (Na3AlF6) dijaga 2 %
sampai 3 % untuk menghindari terjadinya anode effect yang berlebihan. Jika
konsentrasi alumina (Al2O3) < 1 % maka akan terjadi anode effect (AE), dan jika
konsentrasi alumina (Al2O3) > 4 %, maka akan terbentuk lumpur alumina (sludge)
yang akan menghambat proses elektrolisa.
Dari data dapat dilihat bahwa kondisi yang memungkinkan untuk
memperkecil frekwensi anode effect adalah pada % CE (Current Efficiensi) =
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Efisiensi arus yang digunakan pada operasi tungku reduksi di pabrik
peleburan aluminium PT INALUM antara 88,71 % sampai 97,60 %.
b. Jumlah alumina (Al2O3) yang diperlukan setiap harinya untuk elektrolisa
dalam satu tungku reduksi adalah + 2562,2 kg/hari dengan konsentrasi
alumina (Al2O3) yang optimum di dalam larutan bath (Na3AlF6) antara 2
% sampai 3 % serta frekwensi anode effect (AE) antara 1,4 – 1,5
kali/pot.hari.
c. Hubungan antara konsentrasi alumina (Al2O3) dengan % CE adalah
berbanding lurus, namun berbanding terbalik dengan frekwensi anode
effect.
5.2 Saran
Sebaiknya untuk memperoleh produksi aluminium yang optimum maka dalam
pemasukan / penambahan alumina (Al2O3) untuk proses elektrolisa harus diatur
range-nya agar mencegah terjadinya peristiwa anode effect yang berlebihan dan
mencegah terbentuknya lumpur alumina (Al2O3) atau sludge. Dalam hal ini
memerlukan sedikit perhatian dalam system titik pemasukan / pengumpan (system
DAFTAR PUSTAKA
Anonymous, 1998.Prinsip-Prinsip Elektrolisa Aluminium,PT INALUM
Anonymous, 2007.Modul Pelatihan Operasi Tungku Reduksi,Edisi II,
PT INALUM
Austin,G.T.,1990.Industri Proses Kimia.Jilid 1.Edisi Kelima.Jakarta:Penerbit
Erlangga.
Burkin.A.R.1987.Production Of Aluminium and Alumina.New York:
John Willey &Sons.
Brown, Theodore,L., 2000,Chemistry : The Central Science, 8th edition,
Prentice Hall, New Jersey.
Daryus, A., 2008.Proses Produksi.Jakarta:Universitas Darma Persada
Kelvin.G.V.,1994.The Chemical World Concept And Aplications,
8th edition,Harcourt Brace & Company,Orlondo