SELEKSI
IN
VITRO UNTUK KETAHANAN TERHADAP
PENYAKIT LAYU FUSARIUM PADA TANAMAN
ABAKA
(Musa
textilis
Nee)
Oleh
FlTRl DAMAYANTI
PROGRAM PASCASARJANA
INSTITUT PERTANIAN BOGOR
"Seiia&6aiJ+&
iahh orang yang
&denen
pa yang umur tibn umuryang panjang
mantusia ahrlbh orang y a q di6eri T i n
umurpanjang tetapi umurparyaq ztu dia
gunakan unt@ehut (gabtan tibn ~
~
n
saja
"
(H
-
R A h d
~
n
cihn
limidzi)
UOrizngyang
sangat ~ i p a d i
b r i
&nut
ialbti mere&yang 6&sempatun
menuntut $mu
di
dunia lhlu tid2kmau menuntut $mu. a n
orang yang
meqqajarI&an ilinu
(&pad2
orang-mang) lblu orang y a q &jar
memperolih
nun fmt h r i ilinunya sedbngkan diriya sendiiri
(X
16nu
Bsyakir)
Wrya ini kupersem6ahkan unt&Mamh dan Papah tercintu
Setiap
d m . t
nadi
dun nufmya d a h h
do
'a, &sihnya d a b 6 tiarapan,
Peluh dun lbng<ahnya adalith juaq untukanu&ana~nyu
? k r u n t u k a d i i - d i yang ~ c i n t u
Ti&
h n
Tin&ABSTRAK
FITRI DAMAYANTI. Seleksi in vitn, untuk ketahanan terhadap penyakit layu Fusarium pada tanaman abaka (Musa textiles Nee). Dibimbing oleh SUHARSONO dan IKA MARISKA.
13ermasalahan yang dihadapi dalam usaha pertanaman abaka adalah serangan penyakit layu Fusarium yang disebabkan deh jamur
Fusarium
oxysporum. Varietas yang tahan penyakii tersebut sampai saat ini belum ada. Perbaikan tanaman tenrlama sifat ketahanan terhadap penyakit dapat dilakukan melalui peningkatar? keragaman somaklonal yang diikuti dengan seleksi in vitro.llntuk mendapatkan metode seleksi dalam rangka memperoleh tanaman abaka yang tahan terhadap penyakit layu Fusarium dilakukan seleksi in vitm dengan menggunakan komponen seleksi asam fusarat dengan konsentrasi: 0,15,30,45,60 dan 75 mgA. Konsentrasi 45 mgn asam fusarat merupakan konsentrasi yang letal untuk tanaman abaka yang tidak tahan terhadap Fusarium, sehingga dosis ini digunakan untuk menyeleksi tunas dari kalus yang telah diradiasi.
F'eningkatan keragaman somaklonal tanaman abaka dilakukan dengan menlggunakan mutagen fisik yaitu radiasi sinar gamma dengan dosis radiasi 0, 0.5, 1, 1.5, 2, dan 3 Krad yang dilakukan pada kalus embriogenik. Semakin tinggi dosis radia~si maka semakin rendah kemampuan kalus untuk beregenerasi. Pada dosis radia~si 3 Krad kalus tidak dapat beregenerasi dan mengalami kematian.
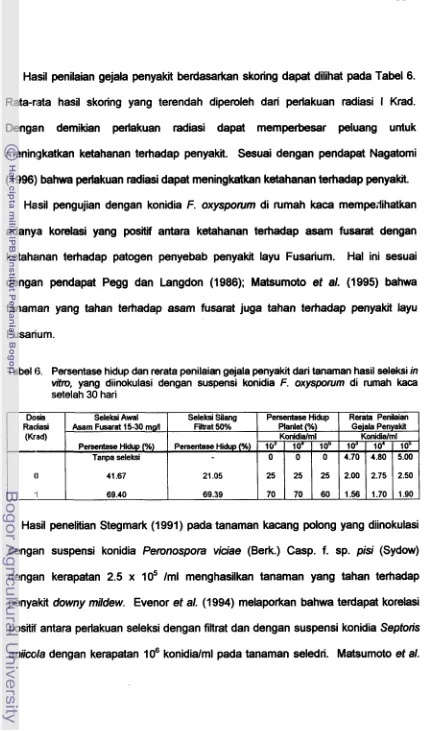
diperoleh pada kisaran dosis 1-1.5 Krad.
Sieleksi in vifm dilakukan melalui dua tahap berurutan, dimana pada seleksi tahap II konsentrasi asam fusarat dinaikkan satu tingkat dari seleksr I. Seleksi I
pade tunas yang dihasilkan dari kalus yang telah diradiasi 0.5, 1, 1.5, dan 2 Krad dalarn media yang mengandung 45 mgll asam fusarat menunjukkan semakin tinggi dosisi radiasi semakin rendah daya hidup tunas. Pada seleksi II, tunas dari kalus hasil radiasi 0.5 dan 1 Krsd dapat hidup pada media seleksi yang mengandung 63
ppm asam fusarat. Dalam media seleksi yang mengandung 50% filtrat F.
oxysporum, tunas yang tahan asam fusarat tahan juga terhadap filtrat.
SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa tesis yang berjudul:
SELEKSI
IN
WTRO
UNTUK KETAHANAN TERHADAP
PENYAKIT LAYU FUSARIUM PADA TANAMAN ABAKA
(Musa textilis
Nee)
adalah benar mempakan hasil karya saya sendiri dan belum pemah dipublikasikan. Sernua sumber data dan informasi yang digunakan telah dinyatakan secara jelas darl dapat diperiksa kebenarannya.
Bogor, Juli 2002
Firi
d,
mayantiSELEKSI
IN VITRO
UNTUK KETAHANAN TERHADAP
PENYAKIT LAYU FUSARIUM PADA TANAMAN
ABAKA
(Musa textilis
Nee)
FlTRl DAMAYANTI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Biologi
PROGRAM PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Seleksi in Wtm untuk Ketahanan Terhadap Penyakit Layu Fusarium pada Tanaman Abaka (Musa textilis, Nee)
I\lama : Fitri Damayanti
NRP : 99707
Program Studi : Biologi
Menyetujui,
1. Komisi Pembimbing
Dr. Ir. Suharsono DEA
-
Ketua
2. Ketua Program Studi Biologi
L
--
DFI. Ir. Deddv Duwadi Solihin, DEA
-
Dr. Ir. Ika Mariska APU Anggota
Mengetahui,
Penulis dilahirkan di kota minyak Balikpapan Kalimantan Timur pada tanggal 20
September 1974, sebagai anak pertama dengan dua orang adik laki-laki dari
seorang ibu teranta Maliir dengan ayah Djamaluddin Basja.
Penulis menyelesaikan sekolah dasar di Sekolah Dasar Negeri 004 Balikpapan.
Kennudian karena mengikuti orang tua, penulis pindah ke kota hujan Bogor, maka
penulis menyelesaikan sekolah lanjutan tingkat pertama di SLTPN I Bogor dan
sek~olah menengah atas di SMU I Bogor. Pada tahun 1999 penulis memperoleh gels~r Sarjana Sains dari JUNM~ Biologi Fakultas Matematika dan llmu
Penlgetahuan Alam Universitas Sriwijaya, Palembang. Pada tahun yang sama
penulis memperoleh beasiswa dari Proyek DUE untuk program Magister dan penulis
dite~ima sebagai mahasiswa
&
pada Program Studi Biologi, Sub Program Botani diPragram Pascasajana IPB. Pada saat ini, penulis merupakan salah satu staf
penlgajar di Fakultas Matematika dan llmu Pengetahuan Alam, Universitas
PRAKATA
Bisinj/ahimhmanirrohiim
Alhamdullilah atas berkah, rahmat dan hidayah Allah SWT akhimya penulis dapat menyelesaikan tesis dengan judul 'Seleksi in Vitm untuk Ketahanan Terhadap Per~yakit Layu Fusarium pada Tanaman Abaka (Musa textilis, Nee). Tesis ini
merupakan salah satu syarat untuk memperoleh gelar Magister Sains pada Program
Pascasarjana IPB.
Pada kesempatan ini penulis menyampaikan penghargaan dan ucapan terima
kasih kepada:
1. IDr. Ir. Suharsono, DEA selaku Ketua Komisi Pembimbing dan Dr. Ir. Ika Mariska,
APU sebagai Anggota Komisi Pembimbing atas bimbingan, saran, kritikan dan
lnasukan selama penyusunan proposal, pelaksanaan penelitian dan penulisan
lesis.
2. Ilirektur Program Pascasarjana IPB beserta para Asisten Direktur dan staf yang
telah menerima penulis menjadi warga PPs-IPB.
3. Ketua Program Studi Biologi dan staf pengajar PPs-IPB yang telah membirnbing
clan menularkan sebagian ilmunya.
4. Kepala Balai Penelitian Bideknologi Tanaman Pangan yang telah mengijinkan
penulis untuk melakukan penelian di Balai Penelitian Bioteknologi Tanaman
F'angan, Bogor.
5. Staf Kelti Reproduksi dan Pertumbuhan: Pak Ali Husni, Mba' Sri Utami, Mba' Ika
5. :Staf Kelti Reproduksi dan Pertumbuhan Balitbio: Pak Ali Husni, Mba' Sri Utami,
Mba' lka Roostika, Mba' Ragapadmi, Mba' Mia Kosmiatin, Mba' Suci Rahayu, I'ak Yadi, Pak Deden, Ibu Atun, Ibu Novi, Ibu Sri Hutami, Mba' Mama, Mas Joko
'ramami, Pak Mujiman, Pak Murtado, Mas Sukmawan, Pak Saefudin, Pak
Sanusi, Pak Tatang, dan Pak Darrnawan yang telah banyak membantu, memberi
saran, diskusi dan dorongan.
6. E3apak Sutoro yang telah banyak meluangkan waktu, diskusi dan saran-saran
=lama perkuliahan dan penelitian.
7. Dr. Mesak Tombe, APU dan Bang Zulhisnaen di Kelti Hama dan Penyakii Balai
F'eneliiian Tanaman Rempah dan Obat, Bogor yang telah banyak membantu dalam penyedian filtrat dan konidia F. oxyspomm, memberi saran dan diskusi.
8. Filekan-rekan mahasiswa di PPs-IPB khususnya di Sub Program Biologi
angkatan 99: Rohayati, Ibu Yennita, Jusmaldi, Yanti, Asri, Pak Teguh, Hety, Mba' Yusnaini, dan T i n atas diskusi dan kebersamaannya selama menempuh
plendidikan S2.
Semoga Allah SWT membalas kebaikan semua pihak dengan yang lebih baik. Penulis berharap semoga tesis ini dapai berguna bagi pihak-pihak yang
berkecimpung dalam bidang pemuliaan tanaman.
Bogor, Juli 2002
DAFTAR IS1
Halaman
DAF'TAR TABEL
...
xiiDAFZTAR GAMBAR
...
xiiiPEFJDAHULUAN
...
I-atar Belakang
.
. 1'Tujuan Peneli~an
...
5 I-iipotesis...
5TINJAUAN PUSTAKA
...
. 'ranaman Abaka...
I'enyakii Layu Fusarium
Metaboli yang Terdapat dalam Ekstrak F
.
oxysponm...
...
Asam Fusarat...
Gejala akibat asam fusarat...
Keragaman Somaklonal. .
...
Seleksi m Wtm...
f'enggunaan Radiasi Pada Sistem BiologiBAHIAN DAN METODE
...
WaMu dan Tempat
.
. 19...
E3ahan Peneli~an
...
.
.
.
19F'elaksanaan Penelitian
...
19 Penentuan konsentrasi asam fusarat untuk seleksi in vitro...
21 Pengaruh radiasi sinar gamma terhadap daya regenerasi darikalus
...
21 Seleksi in vitm pada tunas hasil dari kalus yang diradiasi untuk...
ketahanan terhadap asam fusarat 22
Pengujian tanaman hasil seleksi in vitm dengan suspensi konidia
F
. oxysponrm di rumah kaca...
23HASlL DAN PEMBAHASAN
...
F'enentuan Konsentrasi Asam Fusarat untuk Seleksi in Vitm 25 F'engaruh Radiasi Sinar Gamma Terhadap Daya Regenerasi dari
Kalus
...
27 Sieleksi in Vitm pada Tunas Hasil dari Kalus yang Diradiasi untukKetahanan Terhadap Asam Fusarat
...
Seleksi tahap I 30
...
Seleksi tahap II 32
F3engujian Tanaman Hasil Seleksi in Vifm dengan Suspensi Konidia F .
...
cxysporum di Rumah Kaca 37
...
KESIMPULAN DAN SARAN 41
...
DAFTAR TABEL
Halaman
1 Pengaruh asam fusarat terhadap jumlah dan tinggi tunas abaka pada
umur delapan minggu setelah tanam
...
262 Pengaruh radiisi sinar gamma pada kalus embriogenik terhadap jumlah dan tinggi tunas yang dihasilkan pada umur delapan minggu
setelah tanam
...
293 .iumlah dan tinggi tunas yang dihasilkan pada media seleksi I yang
rnengandung 45 mgA asam fusarat delapan minggu setelah tanam..
...
324 .lumlah dan tinggi tunas yang dihasilkan pada media seleksi II yang
rnengandung 60 mgA asam fusarat delapan minggu setelah tanam
...
345 Jumlah dan tinggi tunas yang dihasilkan dari seleksi silang 50% filtrat
...
1:. oxysporum delapan minggu setelah tanam 36
6 F'ersentase hidup dan rerata penilaian gejala penyakit dari tanaman t~asil seleksi in vitm, yang diinokulasi dengan suspensi konidia F.
...
Halaman
...
Bagan alir tahapan penelitian 20
Kalus embriogenik tanaman abaka
...
22Tanaman hasil seleksi in V&D yang siap untuk pengujian di rumah
kaca
...
23Daya- hidup tunas abaka pada media seleksi asarn fusarat delapan
minggu setelah tanam
...
26Daya tahan kalus embriogenik setelah radiasi pada media regenerasi
umur delapan minggu
...
27Penampakan tunas dari kalus yang d i r a d i i pada berbagai dosis radiasi. a=O Krad, b=0.5 Krad, c=1 Krad, dz1.5 Krad, e=2 Krad, dan
f=3 Krad
...
30Daya tahan tunas yang didapat dari kalus yang diradisi pada berbagai dosis dalam media seleksi I yang mengandung 45 mgA asam fusarat dan media pemulihan delapan minggu setelah
tanam..
...
31Daya tahan tunas yang didapat dari kalus yang diradisi pada berbagai dosis dalam media seleksi II yang mengandung 60 mgn
asam fusarat dan media pemulihan delapan minggu setelah tanam..
..
33Daya tahan tunas yang dihasilkan dari kalus yang diradisi dengan berbagai dosis pada media seleksi yang mengandung 50% filtrat F.
oxysporum delapan minggu setelah tanam
...
35Penampakan tunas yang dihasilkan oleh kalus yang diradisi dengan rberbagai dosis pada media seleksi yang mengandung 50% liltrat F.
loxysponrm. a=O Krad, b=0.5 Krad, dan c=l Krad
...
36IPenampakan tanaman yang tahan hasil pengujian dengan suspensi konidia F. oxysponrm 30 hari setelah inokulasi di rumah kaca hasil seleksi in v h dengan 15-30 mgA asam fusarat. a=kontrol tanpa
PENDAHULUAN
Latar Belakang
Abaka (Musa textilis Nee) yang dikenal secara intemasional dengan nama
"Manila Hemp* adalah komodii pertanian yang berasal dari Filipina (Wardlaw 1972;
DAAPDP 1988). Abaka merupakan salah satu jenis pisang penghasil serat yang
banyak digunakan sebagai bahan pernbuatan taliitemali dan bahan baku kertas
khutsus (PCARRD 1988).
!Serat abaka dimanfaatkan untuk tali kapal laut karena kuat, tahan terhadap air
asin dan kelembaban tinggi (PCARRD 1988). Pulp abaka baik digunakan untuk
bahan baku kertas berkualitas tinggi misalnya kertas saring, kertas dasar stensil,
kerbs berharga (check, kertas dokurnen di bank), kertas uang (dollar Amerika),
tissue, kantung teh celup, bahan tekstil, kain jok, dan popok bayi (PCARRD 1977;
Wardiyati 1999).
F'ermintaan dunia terhadap bahan baku abaka dari tahun 1994 ke 1995
mennngkat 6,6%. Kebutuhan pasar dunia terhadap seiat abaka semakin tinggi dan
tidak dapat dipenuhi oleh negara-negara produsen yaitu Filipina dan Equador yang
selarna ini me~pakan pemasok utama. ProduMivitas yang telah dicapai oleh kedua
negara tersebut adalah masing-masing sebesar 80.000 ton dan 20.000 ton per
tahun. Sedangkan kebutuhan serat abaka dunia mencapai 600.000 ton.
Pern~intaan akan serat abaka terutarna datang dari Jepang, Amerika, Brazil,
Jerman, Prancis, dan lnggris (Wardiyati 1999). Keadaan ini memberikan peluang
dan iklim tropis yang sesuai bagi karakteristik komoditi pisang-pisangan, sehingga
abaka merupakan tanaman yang potensial untuk dikembangkan saat ini. Banyak
kalangan swasta yang akan mengembangkan secara luas dan pada tahun-tahun
men~datang kebutuhan bibii diproyeksikan lebih dari 6 juta.
I'ermasalahan utama yang dihadapi dalam pengembangan tanaman abaka
adalah serangan penyakii layu Fusarium yang disebaokan oleh jamur Fusarium
oxpporum Schlencht f. sp. cubense
(E.
F. Smith) Wr (PCARRD 1977). Pertanamanabaka yang akan dikembangkan secara besar-besaran dapat mencapai ratusan ribu
hektar. Varietas yang ada tidak tahan penyakit layu Fusarium sehingga
dikhinrvatirkan dapat menimbulkan masalah penyebaran penyaki yang sangat cepat.
Salah satu usaha untuk mengatasi permasalahan tersebut adalah antara lain
penggunaan varietas yang tahan penyakii disamping mempunyai sifat produktivitas
dan mutu yang tinggi. Perakitan varietas yang tahan penyakii memerlukan
keralgaman genetik yang tinggi. Di lain pihak, keragaman genetik tanaman abaka
relatif rendah tenrtama s ' M yang berhubungan dengan ketahanan terhadap
penyakit. Hal ini terjadi karena tanaman abaka diperbanyak secara vegetatif.
F'erbaikan tanaman secara in vitm dilakukan antara lain melalui keiagaman somiaklonal. Ketidakstabilan genetik pada keragaman somaklonal dapat diperoleh
melalui fase pertumbuhan yang dediferensiasi. Telah banyak dilaporkan bahwa
sejurnlah mutan dapat dihasilkan dari kalus dan sel bebas seperti tanaman yang
tahan terhadap penyakit, toleran terhadap garam, kekeringan dan herbisida (Duncan
dan Widholm 1990). Ahloowalia (1982) dan Van den Bulk (1991) menyatakan
pelu~ang baru untuk pengembangan seleksi in vifro yang berguna dalam menunjang
program pemuliaan tanaman.
13erubahan keragaman genetik tidak hanya terjadi secara spontan dalam sel
tetapi juga diinduksi dengan pemberian mutagen fisik maupun kimia. Menurut
Larkin dan Scowcroff (1 981), keragaman somaklonal dapat dihasilkan dari mutasi
genetik, perubahan epigenetik, atau kombinasi kedua proses tersebut. Salah satu
caral untuk meningkatkan keragaman genetik tanaman yang diperbanyak secara
vegetatif adalah dengan menggunakan mutagen fisik yaitu radiasi sinar gamma.
Radiasi sinar gamma dapat digunakan untuk menghasilkan mutan sehingga dapat
meningkatkan keragaman genetik. Nagatomi (1996) melaporkan bahwa di Jepang
telah dihasilkan beberapa varietas yang memiliki sifat ketahanan terhadap penyakii
melalui keragaman somaklonal yang ditimbulkan oleh mutagen fisik.
Keragaman genetik yang relatif rendah, terutama untuk sifat ketahanan terhadap
penyakit, pada tanaman abaka menyebabkan perbaikan genetik secara
konvensional sulit dilakukan sehingga seleksi in vitm merupakan altematif yang
sangat menarik untuk dilakukan. Seleksi ketahanan terhadap penyakii melalui
keralgaman somaklonal lebih efisien bila menggunakan sel atau jaringan. Metode ini
telah terbukli dapat menghasilkan varietas baru yang tahan terhadap penyakit.
Tanaman yang tahan terhadap suatu penyakit yang diwariskan ke generasi
berikutnya telah didapatkan dari seleksi in vitm seperti pada tanaman seledri
(Pagliuso
ef
a/. 1988; Pagliuso dan Rappaport 1990; Evenor et a/. 1994), tembakau(Toyoda et a/. 1989), gandum (Fadel dan Wenzel 1993; Ahmed et a/. 1996) dan
Micke et a/. (1987)' Nagatomi (1996)' dan Matsumoto et a/. (2000a, 2000b);
menyatakan bahwa perlakuan radiasi yang dikombinasi dengan seleksi in vitm
memperbesar peluang ontuk mendapatkan varietas yang tahan terhadap penyakit.
Has~il peneliian Epp (1986) dan Smith et a/. (1996)' menunjukkan bahwa perlakuan
radiasi sinar gamma dan seleksi in vitm dapat menghasilkan pisang caven-h yang
tahan terhadap penyakii layu Fusarium. Imelda et a/. (1997) melaporkan bahwa
radiasi sinar gamma pada dosis 200 rad dapat menghasilkan beberapa klon pisang
raja sereh yang toleran terhadap Banana Bunchy Top Virus (BBTV). Sedangkan
penelian Mathius dan Hans (1999) pada tanaman pisang nangka yang diradiasi
sinar gamma pada dosis 100 rad dan seleksi in vitro dengan 71.6 mgA asam fusarat
menghasilkan beberapa galur yang toleran terhadap asam fusarat.
Seleksi ketahanan tanaman terhadap penyakit layu Fusarium secara in vitm
dilakukan terhadap sel, kalus atau jaringan yang dikulturkan pada media yang
menlgandung toksin murni asam fusarat atau filtrat yang diisolasi dari patogen yang
menyerang tanaman abaka yang mempunyai virulensi tinggi. Menurut Arai dan
Takeuchi (1993)' toksin mumi asam fusarat dan filtrat Fusarium dapat digunakan
sebagai komponen seleksi karena adanya korelasi antara ketahanan terhadap
toksin dengan ketahanan terhadap penyakit. Melalui metode ini beberapa tanaman yang tahan terhadap penyaki layu Fusarium telah berhasil didapatkan seperti pada
camistion (Buiatti et a/. 1985; Arai dan Takeuchi 1993), gandum (Fade1 dan Wenzel
1993; Ahmed et a/. 1996)' dan pisang (Morpurgo et a/. 1994; Matsumoto et a/. 1995;
Tujuan Penelitian
I>eneliiian ini dilakukan untuk mendapatkan metode seleksi in vitm yang tepat
dan mendapatkan nomor-nomor harapan
baru
tanaman abaka yang tahan penyakitlayu Fusariurn.
Hipc~tesis
Iiipotesis yang melandasi penelitian ini adalah terdapat metode seleksi in vitm
yang dapat digunakan untuk mendapatkan tanaman yang tahan terhadap
F
usarium.Radiasi sinar gamma dapat menghasilkan tanaman abaka yang tahan terhadap
penyakit layu Fusarium. Terdapat korelasi yang positif antara ketahanan massa sel
yang tahan terhadap toksin murni asam fusarat dengan ketahanan terhadap
TINJAUAN PUSTAKA
Tanaman Abaka
,4baka (Musa textilis Nee) adalah tanaman sejenis pisang yang termasuk dalam
genus Musa, suku Musaceae, bangsa Zingiberales dan tergolong tanaman
morlokotil (Wardlaw 1972). Tanaman ini merupakan tanaman asli Filipina,
khu:susnya dari Pulau Bicol, Visayas, dan Mindanao yang telah dikenal dan
dikembangkan sejak tahun 1519. Tanaman abaka terdapat juga di daerah di luar
Filip~~na, misalnya di Sabah Serawak, di Kepulauan Sangihe Talaud Sulawesi Utara,
dan di India. Bukti adanya plasma nutfah tanaman abaka di Pulau Sangihe yaitu
tanaman ini sudah lama digunakan sebagai bahan tenunan yang disebut 'kofo',
hanya tidak pernah dikembangkan secara komersial.
ili Indonesia, tanaman abaka sudah di tanam secara komersial sejak tahun 1905
yaitb~ di perkebunan Jawa dan Sumatera, pada tahun 191 1 telah dapat diekspor 200
ton serat abaka. Pada tahun 1916, di daerah Besuki Jawa Timur terdapat
pertanaman abaka seluas 200 ha, namun pada waktu itu komoditi ini kurang
menguntungkan. Di Sumatra Timur dan Lampung juga pemah diusahakan
pertanaman abaka. Di daerah Banyuwangi terdapat perkebunan sisa jaman
Belanda dari tahun 1928 yang sampai sekarang masih mempunyai tanaman seluas
300 iha. Pada tahun yang sama juga dibuka perkebunan abaka di Sumatra Selatan,
Kalimantan, dan Sulawesi.
P,baka mempunyai batang dan daun yang lebih ramping dari pisang biasa.
menutupi. Tingginya dapat mencapai 3.5-7.5 m dalam waMu 30 bulan, dengan
diameter batang antara 12-30 cm. Setiap upih daun disusun oleh tiga lapisan, yaitu
lapisIan teduar mengandung serat yang kuat, kasar dengan panjang 1.5-3 m yang
disetbut Wuxy" dimana serat "Manila Hempn dihasilkan; lapisan tengah, mengandung
sejum!eh kecil serat putih yang lebih lunak dari pada lapisan terluar dengan daya
rentang serat yang rendah; dan lapisan dalam yang tidak mengandung serat
(DAAPDP 1988).
F'ada tepi daun terdapat garis hitam yang merupakan pembeda antara pisang
bias3 dan abaka. Abaka mempunyai daun yang lebih sempit dan meruncing pada
bagiisn pucuk. Bunga abaka mirip dengan pisang pada umumnya, tetapi buahnya
lebih kecil dan tidak dapat dikonsumsi. Tandan dan rangkaian buah abaka lebih
pendek, berwama hijau, panjangnya sekitar 5-8 cm dengan penampang sekitar 2.5
cm (PCARRD 1977; Wardiyati 1999).
Jenis abaka yang tumbuh di Filipina sekiiar 100 varietas (PCARRD 1988).
Menl~rut Haroen (1999), terdapat tiga varietas tanaman abaka yang dibudidayakan
di lntlonesia yaitu: varietas Bongolanon, Manguindanao dan Tangongon. Tanaman
abaka tumbuh baik di daerah dengan ketinggian di bawah 500 m di atas permukaan
laut, suhu 20' dan 25' C, rata-rata curah hujan 2000-3500 mm per tahun (DAAPDP
1988) dan kelembaban 78-88% (PCARRD 1977).
Penyakit Layu Fusarium
Penyaki layu Fusarium disebabkan oleh jamur F. oxyspomm f. sp cubense yang
dalam struktur klamidospora yang bersifat saprofi pada sisa-sisa tanaman yang
kernudian merupakan sumber inokulum yang dapat menyerang tanaman lain.
Pemyakit ini dapat menular karena perakaran tanaman sehat berhubungan dengan
spora yang dilepaskan oleh tanaman saki yang ada disekitamya, dapat juga melalui
bibit dan tanah yang terinfeksi (Bilgrami dan Dube 1976; Agrios 1988).
Gejala awal tanaman yang terinfeksi adalah berupa bercak kekuningan atau
garis-garis pada bagian bawah daun pertama atau kedua. Wama kekuningan akan
berkembang disepanjang tepi daun dan menyebar ke arah tulang daun yang
kemudian menjadi coklat dan mengering. Apabila te rjadi serangan
berat
tangkaif
dautl patah disekeliling batang semu, kadang-kadang lapisan luar batang semu juga
merr~belah dimulai dari permukaan tanah (Wardlaw 1972; PCARRD 1977; Ploetz et
a/. 1 !394).
C3ejala yang paling khas dari penyakii ini adalah gejala dalam yaitu bila pangkal
batamg dibelah membujur akan terlihat garis-garis coklat atau h i m menuju ke
semua arah, dari bonggol ke pangkal dan tangkal daun melalui jaringan pembuluh.
Gejala infeksi lanjut akan terlihat pada bonggol. Bonggol menjadi berwama merah
gelap atau merah kecoklatan. Tunas yang tumbuh pada bagian bonggol yang
terserang akan berwama kuning atau merah (PCARRD 1977). Parenkhim pada
awal~iya tidak terserang, tetapi setelah gejala sekunder timbul pembusukan. Berkas
pembuluh akar tanaman saki umumnya berwama hitam dan membusuk (Wardlaw
1972; DAAPDP 1988).
Tandan buah yang terserang oleh F. oxyspomm akan terlihat beiwama kuning
serta batang semu pecah akan terlihat setelah 2-6 bulan tanaman terinfeksi. Daun
yansl menguning pada tanaman sehat dapat dibedakan dengan tanaman yang
terinfeksi sekitar dua minggu sebelum gejala penyakit layu Fusarium yang lebih
nyata muncul (Wardlaw 1972).
F'enyakii layu Fusarium disebabkan adanya pertumbuhan miselium di antara
jaringan inang. Patogen mampu menghasilkan enzim, toksin dan polisakarida
dalaln jaringan inang. Toksin menyebabkan kerusakan pada permeabilitas
merrlbran s d tanaman yang dapat mengakibatkan kematian sel.
F'atogen yang ada di tanah akan masuk ke dalam akar melalui lenti sel akar.
Patogen berkembang sangat cepat disepanjang akar dan menghasilkan miselium.
Kemudian miselium masuk ke dalam pembuluh xilem melalui noktah dan
menghasilkan mikrokonidium. Spora ini dapat terbawa oleh aliran zat cair ke atas,
tementi dan tersangkut pada dinding sel jaringan pembuluh xilem dan berkecambah
membentuk miselium. Polisakarida dan enzim yang dihasilkan patogen ini dapat
menyebabkan kerusakan pada sel-sel jaringan xilem dan menyebabkan
penyumbatan pembuluh. Selain itu adanya sekresi berupa massa koloidal serta
mengkerutnya sel-sel pembuluh menyebabkan aliran zat cair menjadi terhambat
sehir~gga tejadi proses penurunan laju aliran air dalam pembuluh dan akhimya
menimbulkan kelayuan (Agrios 1988).
Metabolit yang Terdapat dalam Ekstrak F. oxyspomm
Mletabol'i yang disintesis oleh F. oxyspomm antara lain zat pengatur tumbuh dari
oxyspomm adalah asam indol-3-asetat (IAA). Menurut Agrios (1988), meningkatnya
kandungan IAA menyebabkan peningkatan plastisitas dinding set sehingga pektin,
selulosa dan protein penyusun dinding sel lebih mudah dilewati dan tejadi
perombakan oleh enzim-enzim yang disekresi patogen. Selain itu kandungan IAA
yang tinggi menyebabkan peningkatan laju respirasi pada jaringan yang terinfeksi
dan mempengaruhi permeabiliis sel sehingga terjadi peningkatan transpirasi.
Gaumann (1957) dan Davis (1969) menyatakan bahwa asam fusarat adalah
penyebab penyakit layu. Menurut Page (1959) dan Vesonder dan Hessettine
(19811), asam fusarat dapat mempengaruhi fungsi organel, protein atau enzim
tertentu dari sel tanaman seperti mitokondria sehingga mempengaruhi respirasi,
menghambat enzim kristalin katalase, dan mengganggu membran sel yang dapat
mengakibatkan kebocoran set.
FZusarium menghasilkan enzim pektolitik yaitu pektinmetilesterase, depolimerase
atau poligalakturonase, pektin transeliminase (Gothoskar 1955; Trione 1960;
Heitefuss et a/. 1960), dan enzim selulase (Waggoner dan Dimond 1955; MacHardy
dan Beckman 1981). Enzim-enzim pektolitik memecah bahan pektin dalam dinding
set pembuluh kayu dan masuk ke dalam dinding parenkhim xilem.
Pektinmetilesterase memegang peranan penting penyebab penyumbatan pada
pembuluh dan pencoklatan (Winstead dan Walker 1954). Enzim tersebut dapat
mewlotong metil pada rantai pektin dan menghasilkan asam pektat. Depolimerase
mem~ecah rantai asam pektat menjadi poligalakturonida. Fragmen-fragmen asam
pektat masuk ke dalam pembuluh kayu dan membentuk massa koloidal yang dapat
dilepaskan dan mengalami polimerisasi menjadi melamin yang berwama coklat oleh
sisterri fen01 oksidase tumbuhan inang. Wama wklat tersebut merupakan ciri khas pada penyaki layu Fusarium (Gothoskar et a/. 1955; Waggoner dan Dimond 1955;
MacHardy dan Beckman 1981 ; Agrios 1988).
Asam Fusarat
Aaam fusarat pertama kali diisolasi oleh Yabuta, Kambe dan Hayashi pada tahun
1 934, merupakan produk metabolit yang dihasilkan oleh jamur Fusarium
hetert~spo~m, Nee. Jamur ini bersifat sapmfit atau non spesifik inang pada rumput,
ape1 clan tanaman lain. Tahun 1952 Gaumann, Naef-Roth dan Kobel menemukan
asam fusarat sebagai toksin penyebab layu pada F. lycope~sici, F. vasenfectum Alk
dan G;ibberella fujikuroi (Saw) Wr (Gaumann, 1 957).
S w r a kimia, asam fusarat disebut asam piridine karboksilat (5 butil asam
pikolir~at) dengan forrnulasi CloHI3O2N dan mempunyai berat molekul 179. Asam
fusarat mumi mempunyai titik lebur 98°-1000C, tetapi bila mengandung asam
dehidlFofusarat mempunyai tiik lebur di atas 1 Og°C.
'Pads jamur tertentu yang menghasilkan asam fusarat seperti G. fujikuroi, filtrat
menyebabkan klorosis pada daun muda tunas tomat yang tidak ditemukan pada
perwbaan layu dengan asam fusarat mumi. Ekstraksi dan pemumian dari filtrat
dapat menghasilkan asam dehidrofusarat mumi (5 butil asam enikpikolinat) dengan
forrnulasi CloHI1O2N, berat molekul 177, dan mempunyai tiik lebur 1 18-1 20'~.
Asam dehidrofusarat dapat berubah menjadi asam fusarat melalui proses
Asam fusarat dapat diperoleh dari filtrat pada pH 4 dan diekstrak dengan etil
asetat. Ekstrak etil asetat dievaporasi dan residu yang diperoleh dilarutkan dalam
sedikit air kemudin dibuat alkalin dengan menggunakan bikarbonat pada pH 8-8.5.
Pemurniaan dilakukan dengan cara diekstrak dengan eter kemudian dikristalkan
(Gaurrlann, 1957).
Gejala~ akibat asam fusarat
Jika tanaman tomat ditanam pada media yang mengandung M asam
fusarat, gejala pertama kali te Qadi pada batang kemudian pada daun. Pada batang,
pembuluh vaskular mengalami kerusakan, mengkerut berwama abu-abu hijau
terang dan secara gradual menyebar ke petiol. Pengkerutan pada batang dan petiol
adalatl umum tejadi akibat asam fusarat, kemudian petiol mulai membengkok.
Pada konsentrasi yang lebih tinggi, seluruh jaringan pada batang melemah sehingga
batang menjadi kurus. Gejala terlihat empat jam setelah kontak dengan toksin dan
setelalh dua hari perkembangan gejala menjadi sempuma.
Pa~aa daun dari tunas tomat, munculnya gejala lebih lambat dari batang. Daun
yang 1.erserang terdapat bercak-bercak yang tidak beraturan yang berukuran kecil,
berwarna abu-abu hijau dan transparan, kemudian nekrosis berkembang sepanjang
jaringan daun. Setelah 24 jam dari saat inokulasi, daun menjadi keriting dan layu.
Keragaman Somaklonal
Keragaman somaklonal adalah keragaman genetik dari tanaman yang dihasilkan
regenerasi tidak langsung, kultur sel tunggal atau kultur protoplas (Earle dan Gracen
1985; Kwang dan KO 1986; Van den Bulk 1991). Ahloowalia (1986) menyatakan
bahwia keragaman somaklonal yang terjadi dapat berupa defisiensi klorofil,
ketahanan terhadap penyaki atau kadang-kadang muncul keragaman yang
sebelumnya tidak pernah ada di alam. Keragaman dapat juga terjadi pada sifat
tinggi tanaman, ketebalan batang, luas dan bentuk daun, vigor tanaman,
pembungaan, dan fertilitas.
Manurut D'Amarato (1 986) dan George dan Sherrington (1 984), keragaman
somalklonal tejadi karena perubahan genetik yang meliputi perubahan gen atau
kromosom yang terjadi pada saat induksi kalus atau selama pertumbuhan sel dan
jaringan in vitm. Earle dan Gracen (1985) menyatakan bahwa perubahan genetik
dapat menimbulkan perubahan penampilan, baik untuk perubahan sifat yang
menguntungkan ataupun merugikan.
Mutasi secara umum dibedakan dalam dua kelompok, yaitu mutasi alami dan
mutasi buatan. Mutasi alami terjadi secara spontan dan berkaitan dengan faktor-
faktor lingitungan. Mutasi alami terjadi secara lambat, tetapi berlangsung secara
terus-menerus sehingga memerlukan waktu yang lama untuk mengakumulasikan
mutali dalam populasi alami. Menurut Micke et a/. (1987) mutasi secara alami
merupakan sumber keragaman tanaman yang sangat berguna terhadap populasi,
dan berperan dalam menimbulkan keragaman genetik yang berguna untuk
pemuliaan tanaman yang diperbanyak secara vegetatii.
Mutasi buatan adalah mutasi yang diinduksi yang dipakai sebagai salah satu
fisik ~nenggunakan radiasi atau dengan cam kimia menggunakan senyawa yang
bersilat mutagen.
Radiasi yang umum digunakan yaitu sinar-X atau gamma, sedangkan cara kimia
yaitu menggunakan colchicin dan etilmetan sulfonat (EMS). Penggunaan radiasi
sinar gamma telah dilakukan untuk meningkatkan keragaman tanaman pisang
cavertdish pada kisaran dosis 2.5 Krad (Krikorian dan Cronauer 1986). Pada
tanannan pisang ambon kuning yang berasai dari tunas yang diradiasi sinar gamma
pada dosis 1 dan 1.5 Krad terjadi peningkatan keragaman somaklonal (Sutarto et a/.
1998:l. Widyastuti (2000) menggunaan radiasi sinar gamma pada dosis 2.5-1 0 Krad
untuk mendapatkan keragaman yang tinggi pada tanaman pisang cavendish.
Seleksi in Vitro
Parbaikan tanaman secara in vitm dapat dilakukan melalui keragaman
somakionai. Epp (1986); Van den Bulk (1991); Brazoiot et
al.
(1994); Nagatomi(1996) menyatakan bahwa penggunaan mutagen kimia atau radiasi yang
dikonlbinasi dengan seleksi in vitro dapat menghasilkan keragaman genetik dan
mempercepat terjadinya mutasi yang berpotensi untuk perbaikan sifat genetik
tananian.
Seleksi in vitm ditujukan untuk memilih mutan secara efektif dan efisien yang
mempunyai sifat sesuai dengan yang diinginkan. Seleksi in v i m pada stadium sel,
kalus dan jaringan dapat menghasiikan varietas baru yang tahan terhadap penyakit,
toleran terhadap salinitas, kekeringan dan herbisida (Duncan dan Widholm 1990;
Toyoda et a/. (1989) berhasil mendapatkan tanaman tembakau yang tahan
terhadap tobacco mosaic vims melalui seleksi in vitm pada kalus tembakau.
Hutatmat (1991) telah berhasil memperoleh galur-galur mutan padi varietas sentani
yang toleran terhadap aluminium melalui radiasi sinar gamma pada dosis 1 dan 2
Krad yang diikuti dengan seleksi in vitm. Penelitian ECFiki (1997) menghasilkan
bahwa perlakuan radiasi sinar gamma pada dosis 4 dan 5 Krad yang diikuti dengan
seleksi in vitm terhadap garam menghasilkan tanaman kentang yang toleran
terhadap garam. Nagatomi (1996) berhasil mendapatkan tanaman pir (Pynrs
semtina Rhed) 'Gold Nijisseiki" yang tahan penyaki black spot melalui radiasi sinar
gamma yang diikuti dengan seleksi in vifro. Ochatt et a/. (1999) melaporkan bahwa
seleksi in vitm dapat menghasilkan kalus kentang yang toleran terhadap garam.
Yoshioka et al. (1999) menyatakan bahwa penggunaan radiasi sinar gamma pada
dosis 250 rad yang diikuti dengan seleksi menggunakan toksin spesifik inang
Altemaria altemata (AK-toksin) menghasilkan tanaman persik yang tahan penyakii
black spot.
Seleksi in v i h untuk meningkatkan ketahanan terhadap penyakii dilakukan
dengan menggunakan
filtrat
dari patogen yang menyerang tanaman dan toksinmumi (Earle 1983). Penggunaan toksin dan filtrat dari patogen sebagai komponen -*
selekrsi telah banyak dilakukan untuk mendapatkan sifat ketahanan terhadap
penyakit. Toyoda et a/. (1984a, 1984b) menggunakan filtrat F. oxyspomm f. sp.
lycop"~!~si dan toksin mumi asam fusarat untuk mendapatkan sifat ketahanan
terhatlap penyakit layu Fusarium pada kalus tomat. Hammerschlag (1988)
Xanft~omonas campestris pv. pmni
lo6
kolonilml pada tanaman persik. Arai danTakel~ci (1993), menggunakan filtrat yang diisolasi dari patogen dan asam fusarat
untuk mendapatkan sifat ketahanan terhadap penyaki layu Fusarium pada kalus
carnation. Pada tanaman gandum, Ahmed et a1 (1 996) menggunakan filtrat sebagai
komponen seleksi.
Penggunaan Radiasi Pada Sistem Biologi
Radiasi adalah pemberian sinar, biasanya radioaktif, pada suatu objek dengan
konsentrasi tertentu selama periode waMu tertentu (Ismachin 1988). Sinar radioaktif
yang biasa dipakai untuk menimbulkan mutasi adalah sinar4 dan sinar gamma.
Salah~ satu sifat dari radioaktii tersebut adalah kemampuannya untuk menghasilkan
radiasi pengion yaitu radiasi dengan energi tinggi yang dapat bereaksi dengan objek
yang dikenai radiasi dengan cara pengionan. Molekul objek akan mengalami
ionisasi dan tereksitasi. lonisasi tejadi bila elektron terlepas dari orbiinya,
sedarigkan eksitasi adalah keadaan dimana satu elektron ditingkatkan
kedutlukannya dari tempat semula menggunakan energi yang lebih tinggi. Elektron
yang terlepss akibat ionisasi akan ditangkap oleh molekul lain yang kemudian dapat
membentuk radikal bebas yang sangat reaktii. Pembentukan radikal bebas tersebut
akan mempengaruhi air yang merupakan komponen terbesar di dalam sel atau
dalarri sistem biologi.
Radikal bebas yang bereaksi dengan molekul-molekul di dalam sistem biologi
mengganggu homeostatis sel. Keadaan tersebut dapat mengakibatkan molekul-
molekul di dalam sel tidak dapat beke ja seperti semula (Ismachin 1988).
Pemberian radiasi untuk menimbulkan mutasi harus mempengaruhi DNA sel
objek., karena DNA merupakan komponen utama dari gen. Mutasi tersebut
selanjutnya akan membentuk keragaman genetik baru (Djojosoebagio 1988).
Perul~ahan genetik di dalam sel somatik dapat diwariskan dan dapat menyebabkan
tejadinya perubahan fenotipe. Perubahan tersebut dapat terjadi pada tingkat sel
atau sekelompok sel sehingga individu dapat mengalami khimera (Micke et a/.
1987).
Di dalam jaringan yang diradiasi dengan mutagen radioaktii akan terjadi ionisasi
molekul air, kemudian mengoksidasi gula dalam DNA sehingga rangkaian
nukleotidanya rusak atau susunan nukleotidanya berubah. Perubahan susunan
nukleotida dapat menyebabkan terganggunya replikasi, transkripsi dan translasi
(Crowder 1990). Menurut Djojosoebagio (1988) radiasi dapat menyebabkan
te jadinya perubahan dalam komposisi basa, dapat menyebabkan putusnya rantai
DNA. Pengaruh radiasi terhadap basa nukleotida menyebabkan terjadinya rnutasi
gen seperti subsitusi, penambahan atau hilangnya basa dalam molekul DNA.
Radiasi dapat juga menginduksi perubahan krornosom. Perubahan kromosom
yang tejadi dapat berupa perubahan struktur atau jumlah kromosom sehingga
menyebabkan perubahan dalam susunan dan jumlah bahan genetik (Crowder 1990;
Djojosoebagio 1988). Perubahan struktur kromosom meliputi delesi, inversi,
duplik.asi atau translokasi (Crowder 1990; Griffihs et a/. 1993). Perubahan jumlah
(1988), poliploidi yang disebabkan oleh radiasi sebagian besar karena pengaruh
sekuinder akibat aberasi kromosom yang menyebabkan tidak dapat terjadinya
BAHAN DAN METODE
Waktu dan Tempat
Penelitian dilaksanakan mulai bulan November 2000 sampai April 2002
bertempat di Laboratorium Kultur Jaringan Balai Penelitian Bioteknologi Tanaman
Pangan, Bogor. Perlakuan radiasi sinar gamma dilakukan di Pusat Aplikasi lsotop
dan Ftadiasi (PAIR), Badan Tenaga Atom Nasional (BATAN), Pasar Jumat, Jakarta.
Bahan Penelitian
Bahan tanaman yang digunakan dalam penelitian ini adalah tanaman abaka
(Musa textilis Nee) varietas Tangongon. Komponen seleksi yang digunakan adalah
toksirl murni asam fusarat. Filtrat F. oxyspomm yang digunakan untuk seleksi in
vitro berasal dari kultur F. oxyspomm selama empat hari, dalam satu lier media
PDB (Potato Dextose Broth) yang diekstraksi menjadi 600 ml filtrat (Tombe M 20
Agustus 2001, komunikasi pribadi). Pengujiin ketahanan tanaman di rumah kaca
menggunakan suspensi konidia F. oxyspomm yang diperoleh dari Laboratorium
Hama dan Penyakit Balai Peneliian Tanaman Rempah dan Obat, Bogor.
Pelaksanaan Penelitian
Penelitian ini terdiri dari empat tahapan yaitu (1) Penentuan konsentrasi asam
fusarifi untuk seleksi in vitro, (2) Pengaruh radiasi sinar gamma terhadap daya
regen~erasi dari kalus, (3) Seleksi in vitm pada tunas hasil dari kalus yang diradiasi
vitro ~clengan suspensi konidia F. oxyspomm di rumah kaca. Tahapan penelitian
disajikan pada Gambar 1.
P'enentuan konsentrasi asam lusarat untuk seleksi in vitm
I
Konsentrasi terpilihI
embriogenik
Tunas
n
Pemulihan tahap 1
1
Pemulihan tahap II
I
Seleksi dengan media yang mengandung 50% filtrat F. oxyspomm
Pengujian dengan suspensi konidia F. oxyspomm di rumah kaca
Peneman konsentrasi asam fusarat untuk seleksi in v h
Tahap ini dilakukan untuk menentukan konsentrasi yang menyebabkan kematian
tunas Konsentrasi yang diperoleh digunakan untuk menyeleksi tunas yang
dihasilkan oleh kalus yang telah diradiasi. Eksplan yang digunakan adalah tunas
berurr~ur dehpan minggu. Tunas ditanam di media dasar Murashige dan Skwg
(1962) ditambah dengan zat pengatur tumbuh yaitu 5 mgll BAP (Benzil Amino Purin)
+
0.4 mgn thidiazuron+
100 mgA asam askorbat serta asam fusarat pada berbagaikonsentrasi: 0, 15, 30, 45, 60, dan 75 mgll. Penelitian disusun berdasarkan
rancangan acak lengkap dengan tiga ulangan. Pengamatan dilakukan pada umur
delapn minggu setelah tanam yang meliputi persentase hidup eksplan, L D ~ , L D , ,
jumlah dan tinggi tunas.
Pengaruh radiasi sinar gamma terhadap daya regenerasi dari kalus
Alat yang digunakan untuk radiasi adalah Irradiator Gammacell 220 (sumber Co
60) dctngan dosis radiasi 0, 0.5, 1, 1.5, 2, dan 3 Krad. Eksplan yang diradiasi adalah
kalus embriogenik tanaman abaka yang berukuran 5 mm (Gambar 2). Setelah
radiasi kalus ditanam di dalam media regenerasi yaitu media MS yang diperkaya
dengan 5 mgn BAP
+
0.4 mgll thidiazuron+
100 mgll asam askorbat selamadelapan minggu. Penelitian disusun berdasarkan ran'cangan acak lengkap.
Penelitian ini menggunakan 10 kalus tiap perlakuan dan dilakukan empat ulangan.
Parameter yang diamati adalah persentase hidup kalus, jumlah dan tinggi
I
Gambar 2. Kalus embriogenik tanaman abaka
S s l e b i in v i h pada tunas hasil dari kalus yang d i r a d i i i untuk ketahanan terhadap asam fusarat
Seleksi ketahanan tanaman terhadap Fusarium dilakukan dalam dua tahap yang
berurutan. Seleksi tahap I dilakukan pada tunas yang dihasilkan oleh kalus yang
telah diradiasi dalam media seleksi yang mengandung asam fusarat dengan
konsentrasi berdasarkan hasil yang dipemleh dari penelitian sebelumnya. lnkubasi
pada media seleksi dilakukan selama delapan minggu. Tunas yang tahan
disubkultur pada media bebas toksin asam fusarat selama delapan minggu untuk
proses pemulihan I dan multiplikasi yaitu media MS
+
5 mgll BAP+
0.4 mgtlthidiazumn + 100 mgll asam askorbat. Selanjutnya dilakukan seleksi tahap II pada
media yang mengandung asam fusarat dengan konsentrasi yang dinaikkan satu
tingkat dari seleksi tahap I. Setelah delapan minggu tunas yang tahan dilakukan
pemulihan II dan multiplikasi. Tunas yang tetap hidup kemudian diseleksi dengan
media yang mengandung filtrat F. oxyspomm dengan konsentrasi 50% selama
perlakuan dilakukan tiga kali ulangan. Parameter yang diamati adalah persentase
hidup tunas, jumlah dan tinggi tunas.
Pengujimn tanaman hasil seleksi in v h dengan suspensi konklia
F.
oxysporum dl rumah kacaUntuk mengetahui hubungan ketahanan tanaman terhadap asam fusarat yang
diperoleh dari sebksi in vitro dan ketahanan tanaman terhadap Fusarium maka
dilakukan pengujian dengan menggunakan suspensi konidia F. oxysporum di rumah
kaca. Tunas yeng diperoleh dari perlakuan seleksi in vitro diakarkan pada media
perakaran yaitu media MS yang diperkaya dengan 0.5 mgA NAA selama enam minggu (Gambar 3).
[image:106.579.76.388.372.712.2]1
Gambar 3. Tangman hasil seleksi in v i h yang siap untuk pengujian di rumah kaca
Tanaman diuji dengan suspensi konidia F. oxysponm dengan metode dipping
(Peg13 dan Langdon 1986) yaitu dengan mencelupkannya dalam suspensi konidia F. oxyspomm dengan kerapatan konidia 1 03, 1
o4
dan 10' Iml air steril selama 30 menit, selarlljutnya ditanam pada tanah steril dan diinkubasi di rumah kaca. Penilaianterhadap gejala penyakii yang timbul dilakukan pada 30 hari setelah inokulasi.
Penilaian dilaku kan berdasarkan Epp (1 986) dengan skala 1-5 dimana 1 =tidak ada
yang menguning; 2=sediki menguning pada daun terbawah; 3-fejadi penguningan
yang meluas dengan kelayuan yang nyata; 4=terjadi penguningan pada daun yang
belurn dan baru membuka; 5=tanam mati. Parameter yang diamati yaitu persentase
Penentuan Konsentasi Asam Fusarat untuk Seleksi in V i i
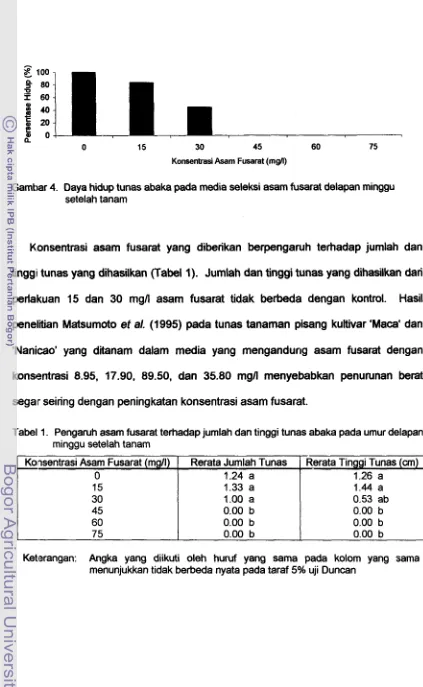
$;emakin tinggi asam fusarat yang diberikan ke dalam media tumbuh semakin
rendah persentase hidup tunas yang ditanam di media tersebut (Gambar 4). LOQ
dipe~~oleh pada konsentrasi 30 mgn asam fusarat. Setelah delapan minggu, semua
tunas mati pada dosis 45 mgtl asam fusarat (LOfoo), sehingga untuk memilih
tanaman yang tahan terhadap Fusarium, seleksi dilakukan di dalam media yang
mengandung 45 mgA asam fusarat. Penelitian Toyoda et a/. (1984b) pada kalus
tanaman tomat yang diseleksi pada media yang mengandung asam fusarat dengan
konsentrasi 0.5, 1, 5, 10, 50, 100, 500, dan 1000 mgll menghasilkan LDlw pada
konsentrasi 10 mg/l asam fusarat, sedangkan LD50 diperoleh pada konsentrasi 5
mgn.
Tunas yang mati pada awalnya menunjukkan gejala busuk pada pangkal batang
kemudian menjalar ke bagian atas dan berwarna coklat kehitaman. Gejala tersebut
menyerupai gejala penyaki l a y Fusarium yang menyerang pertanaman di
laparigan. Asam fusarat dapat menghambat pertumbuhan sel. Menurut Van den
Bulk (1991) penghambatan pertumbuhan sel disebabkan karena asam fusarat
menghambat respirasi pada mitokondria, menurunkan ATP pada membran plasma
u
0 15 30 45 60 75
Konsentrasi Asam Fusarat (rng~l)
Gamtmr 4. Daya hidup tunas abaka pada media seleksi asam fusarat delapan minggu setelah tanam
Konsentrasi asam fusarat yang diberikan berpengaruh terhadap jumlah dan
tingg~i tunas yang dihasilkan (Tabel 1). Jumlah dan tinggi tunas yang dihasilkan dari
perlakuan 15 dan 30 rngA asam fusarat tidak berbeda dengan kontrol. Hasil
penelitian Matsumoto et a/. (1995) pada tunas tanaman pisang kultivar 'Maca' dan
'Nanicao' yang ditanam dalam media yang rnengandung asam fusarat dengan
konsentrasi 8.95, 17.90, 89.50, dan 35.80 mgn menyebabkan penurunan berat
segar seiring dengan peningkatan konsentrasi asam fusarat.
Ketlerangan: Angka yang diikuti oleh huruf yang sama pada kolom yang sama menunjukkan tidak berbeda nyata pada taraf 5% uji Duncan
Tabel 1. Pengaruh asam fusarat terhadap jumlah dan tinggi tunas abaka pada umur delapan minggu setelah tanam
Ko~nsentrasi Asam Fusarat (mgll)
i
015 30 45 60 75
Rerata Jumlah Tunas
1.24 a
1.33 a
1.00 a
0.00 b
0.00 b
0.00 b
Rerata Tinggi Tunas (cm)
1.26 a
1.44 a
0.53 ab
0.00 b
0.00 b
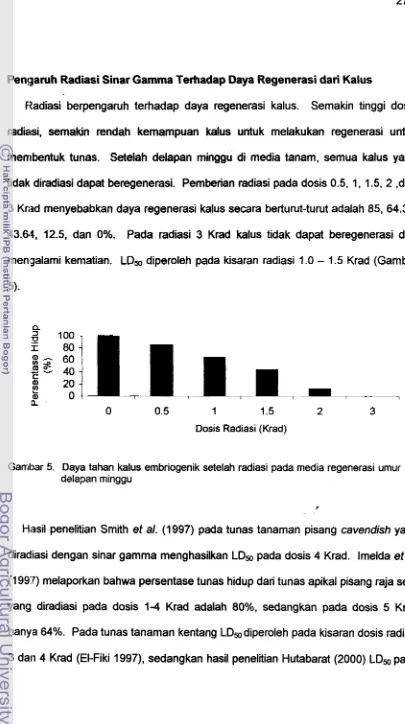
[image:109.574.71.494.72.759.2]Pengaruh Radiasi Sinar Gamma Terhadap Daya Regenerasi dari Kalus
Ftadiasi berpengaruh terhadap daya regenerasi kalus. Semakin tinggi dosis
radiasi, semakin rendah kemampuan kalus untuk melakukan regenerasi untuk
menlbentuk tunas. Setelah delapan minggu di media tanam, semua kalus yang
tidak diradiasi dapat beregenerasi. Pemberian radiasi pada dosis 0.5, 1, 1.5, 2 ,dan
3 Kriad rnenyeba b k ~ n daya regenerasi kalus secara berturut-turut adalah 85, 64.36,
43.64, 12.5, dan 0%. Pada radiasi 3 Krad kalus tidak dapat beregenerasi dan
menlgalami kematian. LDS diperoleh pada kisaran radiasi 1.0
-
1.5 Krad (Gambar5)-
u.
0 0.5 1 1.5 2 3
[image:110.572.75.480.43.767.2]Dosis Radiasi (Krad)
Gambar 5. Daya tahan kalus embriogenik setelah radiasi pada media regenerasi umur
delapan minggu
i.
Hesil peneliian Smith et a/. (1997) pada tunas tanaman pisang cavendish yang
diradiasi dengan sinar gamma menghasilkan LDm pada dosis 4 Krad. Imelda et a/.
(199'7) melaporkan bahwa persentase tunas hidup dari tunas apikal pisang raja sere
yang diradiasi pada dosis 1-4 Krad adalah 80%, sedangkan pada dosis 5 Krad hanya 64%. Pada tunas tanaman kentang LDm diperoleh pada kisaran dosis radiasi
benilr manggis diperoleh pada kisaran dosis 2 dan 4 Krad. Menurut Nagatomi
(1998), dosis terbaik untuk menghasilkan mutan terletak di bawah LDS0, walaupun
padai dosis tersebut menyebabkan lebih banyak kenrsakan pada stadia awal.
F'enampakan wama tunas yang terbentuk dari perlakuan radiasi bervariasi
antala putih kehijauan dan putih kekuningan, sedangkan pada kontrol tunas yang
dihaaiilkan berwama hijau (Gam~ar 6). Tunas yang diperoleh dari kalus yang
mentlapat perlakuan radiasi dig unakan untuk seleksi in vitro ketahanan terhadap
penyaki layu Fusarium dengan menggunakan toksin murni asam fusarat.
Perlakuan radiasi yang diberikan pada kalus sebelumnya berpengaruh terhadap
jumlah dan tinggi tunas yang dihasilkan (Tabel 2). Semakin tinggi dosis radiasi yang
diberikan semakin rendah kemampuan kalus untuk beregenerasi membentuk tunas
adventi. Hal ini sejalan dengan hasil penelitian Novak et a/. (1990) pada tunas
pucuk pisang dari klon SH 3142, Grand Nain, Highgate, SH 3436, AVP 67, Saba
dan Pelipita yang diradiasi dengan sinar gamma 1.5, 3, 4.5, dan 6 Krad
memperlihatkan jumlah tunas dan berat segar semakin menurun seiring dengan
penin~gkatan dosis radiasi yang diberikan. Demikian juga pada ka!us padi indica
menghasilkan penurunan laju pertumbuhan dan jumlah tunas yang dihasilkan
denglan semakin tingginya dosis radiasi yang diberikan, dimana pada dosis 0.5-1.0
Krad menghasilkan keragaman genetik yang tinggi (Gao dan Liang 1992).
Sebaliknya pada batang tanaman kentang kultivar Atlantik yang diradiasi sinar
gamnna pada beberapa taraf yaitu 0.1,1,2,3 dan 4 Krad temyata pada dosis 4 Krad
meng~hasilkan jumlah tunas lebih banyak dengan planlet yang lebih tinggi, berbatang
Tabell 2. Pengaruh radiasi sinar gamma pada kalus embriogenik terhadap jumlah dan tinggi tunas yang dihasilkan pada umur delapan minggu setelah tanam
7
Dosis Radiasi (Krad) ( Rerata Jumlah Tunas tiap
I
Rerata Tinggi Tunas (cm) tiap1
Keterangan: Angka yang diikuti oleh huruf yang sama pada kolom yang sama
menunjukkan tidak berbeda nyata pada taraf 5% uji Duncan
-
0.0
12erlakuan radisi 3 Krad menyebabkan tidak satupun kalus yang menghasilkan
tunas. Proses regenerasi yang terhambat karena radiasi dapat menyebabkan Kalus yang Beregenerasi
3.61 a
rusaknya DNA sehingga proses sintesis protein atau enzim terganggu. Gangguan Kalus yaG Beregenerasi
2.32 a
pada sintesis protein menyebabkan gangguan metabolisme sehingga proses
morfogenesis pada kalus embriogenik terganggu yang menyebabkan proses
regerierasinya terganggu.
F'erlakuan radiasi pada jaringan dapat menyebabkan perubahan pada jumlah
dan struktur kromosom (Djojosoebagio 1988; Larkin dan Scrowcroft 1981).
Pemlberian radiasi yang diharapkan adalah yang mempunyai pengaruh fisiologi
rendah namun berpengaruh terhadap perubahan-perubahan sifat tanaman ke arah
Gambar 6. Penampakan tunas dari kalus yang diradiasi pada berbagai dosis radiasi a=O Krad, b=0.5 Krad, c=l Krad, d=1.5 Krad, e=2 Krad, dan f=3 Krad
Seleksi in VHm Pada Tunas Hasil dari Kalus yang Diradiasi untuk Ketahanan Terhadap Asam Fusarat
Seleksi tahap I
Seleksi in vim tahap I pada tunas hasil dari kalus yang diradiasi 0.5, 1, 1.5 dan L
Krad dalam medii yang mengandung komponen seleksi 45 mgn asam fusarat
menunjukkan bahwa semakin tinggi dosis radiasisemakin rendah daya hidup tunas,
yaitu bertunrt-turut sebesar 46.67, 38.89, 16.67, dan 0% (Gambar 7). Pada
perlakuan radiasi 2 Krad tidak ada tunas yang tahan dalam media seleksi, yang
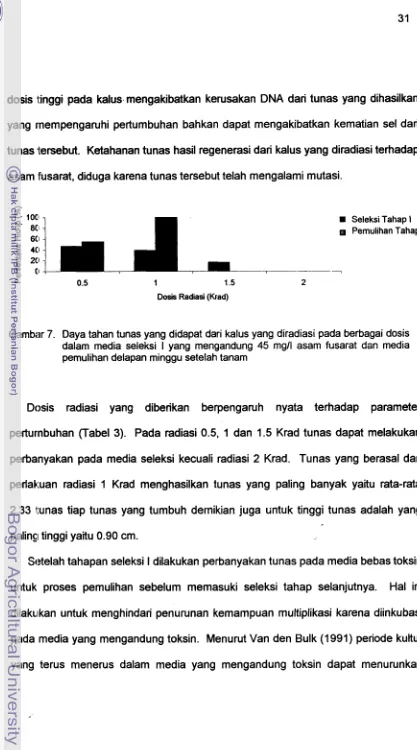
[image:113.564.69.499.67.767.2]dosis l:inggi pada kalus mengakibatkan kerusakan DNA dari tunas yang dihasilkan
yang rnempengaruhi pertumbuhan bahkan dapat mengakibatkan kematian sel dari
tunas 'tersebut. Ketahanan tunas hasil regenerasi dari kalus yang diradiasi terhadap
asam fusarat, diduga karena tunas tersebut telah mengalami mutasi.
Seleksi Tahap l
Pemulihan Tahap I
d 0.5 1 1.5
[image:114.570.67.484.21.771.2]Dosis Radiasi (Krad)
Gambar 7. Daya tahan tunas yang didapat dari kalus yang diradiasi pada berbagai dosis dalam media seleksi I yang mengandung 45 mgll asam fusarat dan media pemulihan delapan minggu setelah tanam
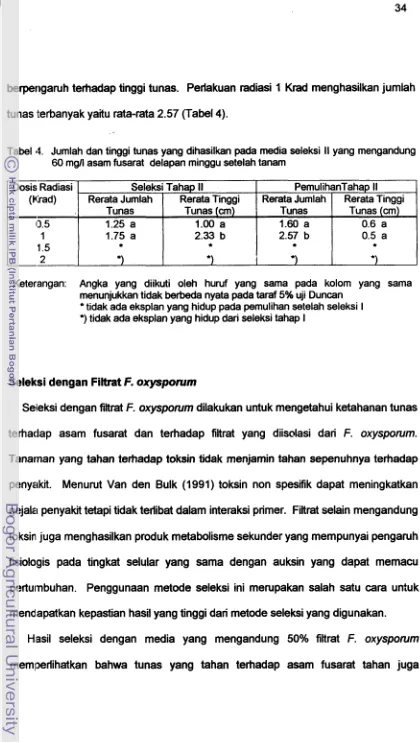
Dosis radiasi yang diberikan berpengaruh nyata terhadap parameter
perturnbuhan (Tabel 3). Pada radiasi 0.5, 1 dan 1.5 Krad tunas dapat melakukan
perbanyakan pada media seleksi kecuali radiasi 2 Krad. Tunas yang berasal dari
perlak~uan radiasi 1 Krad menghasilkan tunas yang paling banyak yaitu rata-rata
2.33 tunas tiap tunas yang tumbuh demikian juga tintuk tinggi tunas adalah yang
paling1 tinggi yaitu 0.90 cm.
Setelah tahapan seleksi I dilakukan perbanyakan tunas pada media bebas toksin
untuk proses pemulihan sebelum memasuki seleksi tahap selanjutnya. Hal ini
dilakilkan untuk menghindari penurunan kemampuan multiplikasi karena diinkubasi
pada media yang mengandung toksin. Menurut Van den Bulk (1991) periode kuttur
keman~puan set untuk beregenerasi. Brazolot et al. (1994) melaporkan bahwa
subkultur yang berulang pada media bebas toksin dapat meningkatkan ketahanan
tanamian alfafa terhadap toksin.
Tabel 2;. Jumlah dan tinggi tunas yang dihasilkan pada media seleksi I yang mengandung 45 mgll asam fusarat delapan minggu setelah tanam
Keterangan: Angka yang diikuti oleh huruf yang sama pada kolom yang sama menunjukkan tidak berbeda nyata pada taraf 5% uji Duncan
*) tidak ada eksplan yang hidup dari seleksi tahap I Dosis Radiasi
(Krad)
F
0.51 1.5
2
Tunas yang dihasilkan dari radiasi 1 Krad dapat tumbuh semua pada media
pemulihan, sedangkan yang dihasilkan dari radiasi 0.5 Krad hanya 50% yang
tumbuh (Gambar 7). Tunas yang dihasilkan dari kalus yang diradiasi 1.5 Krad tidak
Seleksi Tahap I
dapat diperbanyak pada media pemulihan sehingga tidak dapat diseleksi pada tahap
11.
Rerata Jumlah Tunas
1.44 ab
2.33 a 1 .OO bc 0.00 c.
Pemulihan Tahap I
Pejrlakuan radiasi 0.5 dan 1 Krad pada kalus tidak berbeda pengaruhnya
Rerata Tinggi Tunas (crn)
0.81 a 0.90 a 0.05 ab 0.00 b
Rerata Jumlah Tunas
3.67 a 3.94 a 0.00 b
terhaclap jumlah tunas yang dihasilkan. Namun demikian perlakuan radiasi 1 Krad
Rerata Tinggi Tunas (cm)
2.08 a 2.24 a 0.00 a
*
menglrlasilkan jumlah tunas yaitu rata-rata 3.94 tunas dan tinggi tunas rata-rata 2.24
cm yang cenderung lebih tinggi dari perlakuan lainnya (Tabel 3).
Seleksi tahap II
Tunas yang tahan hasil seleksi tahap I setelah melalui proses pemulihan diseleksi
[image:115.572.72.492.33.774.2]menjiidi 60 mgn. Seleksi bertahap dilakukan untuk mendapatkan tanaman yang
tahan secara konsisten.
Pa~da seleksi tahap II tunas hasil radiasi 0.5 dan 1 Krad dapat hidup pada media
seleksi dengan persentase hidup sebesar 18.89 dan 20.37 % (Gambar 8).
Pengaruh radiasi 0.5 dan 1 Krad tidak berbeda terhadap jumlah tunas yang
dihasilkan pada media seleksi yang mengandung 60 mgll asam fusarat, namun
berpe!ngaruh terhadap tinggi tunas yang dihasilkan (Tabel 4). Jumlah dan tinggi
tunas tertinggi dihasilkan dari perlakuan radiasi 1 Krad yaitu sebesar 1.75 dan 2.33
cm.
Seleksi Tahap II
Pemulihan Tahap II
0.5 1
Dosis Radiasi (Krad)
Gamtlar 8. Daya tahan tunas yang didapat dari kalus yang diradiasi pada berbagai dosis di dalam media seleksi II yang mengandung 60 mgll asam fusarat dan media pemulihan delapan minggu setelah tanam
Setelah tahapan seleksi II dilakukan proses pemulihan pada media bebas toksin
sebellum memasuki seleksi tahap selanjutnya. Tunas yang dihasilkan dari radiasi
0.5 Krad dapat tumbuh 50%, sedangkan yang dihasilkan dari radiasi 1 Krad hanya
45.45% yang tumbuh (Gambar 8).
Pada media pemulihan setelah seleksi II, perlakuan radiasi berpengaruh
berperrgaruh tethadap tinggi tunas. Perlakuan radiasi 1 Krad menghasilkan jumlah
tunas 'terbanyak yaitu rata-rata 2.57 (Tabel 4).
Tabel 4. Jumlah dan tinggi tunas yang dihasilkan pada media seleksi II yang mengandung 60 mg/i asam fusarat delapan minggu setelah tanam
Keterangan: Angka yang diikuti oleh huruf yang sama pada kolom yang sama rnenunjukkan tidak berbeda nyata pada taraf 5% uji Duncan
tidak ada eksplan yang hidup pada pemulihan setelah seleksi I *) tidak ada eksplan yang hidup dari seleksi tahap I
Seleksi dengan Filtrat F. oxysporum
Seileksi dengan filtrat F. oxyspomm dilakukan untuk mengetahui ketahanan tunas
terhadap asam fusarat dan terhadap filtrat yang diisolasi dari F. oxyspomm.
Tanarnan yang tahan terhadap toksin tidak menjamin tahan sepenuhnya terhadap
penyakii. Menurut Van den Bulk (1991) toksin non spesifik dapat meningkatkan
gejala penyakit tetapi tidak terlibat dalam interaksi primer. Filtrat selain mengandung
toksin juga menghasilkan produk metabolisme sekunder yang mempunyai pengaruh
fisiologis pada tingkat selular yang sama dengan auksin yang dapat memacu
pertu~nbuhan. Penggunaan metode seleksi ini merupakan salah satu cara untuk
mendapatkan kepatiian hasil yang tinggi dari metode seleksi yang digunakan.
Hasil seleksi dengan media yang mengandung 50% filtrat F. oxyspomm
memlwrlihatkan bahwa tunas yang tahan terhadap asam fusarat tahan juga
r;;;iasi
1 1.5
Seleksi Tahap II
Rerata Jumlah Tunas
1.60 a 2.57 b
PemulihanTahap I1
2
Rerata Tinggi Tunas (cm)
0.6 a 0.5 a Rerata Jumlah
Tunas 1.25 a 1.75 a
Rerata Tinggi Tunas (cm)
1.00 a 2.33 b
*
*)
[image:117.570.69.489.31.774.2]terhadap filtrat F. oxyspomm. Perlakuan radiasi 0.5 Krad pada kalus menghasilkan
tunas yang semuanya dapat hidup di media seleksi dengan 50% filtrat F. oxyspomm
selama delapan minggu, sedangkan perlakuan radiasi 1 Krad hanya menghasilkan
80% tunas yang bertahan hidup pada kondisi yang sama. Pada tunas yang
dihasiHkan dari kalus yang tidak diradiasi hanya 13.33% tunas yang dapat hidup
pada media yang mengandung 50% filtrat F. oxyspomm (Gambar 9).
0.5
Dosis Radiasi (Krad)
Gztmbar 9. Daya tahan tunas yang dihasilkan oleh kalus yang diradiasi dengan berbagai dosis pada media seleksi yang mengandung 50% filtrat F. oxysporum delapan minggu setelah tanam
Perlakuan radiasi pada kalus dapat meningkatkan persentase daya tahan tunas
dalarr~ media seleksi yang mengandung 50% filtrat dibandingkan kontrol. Hal ini
didugla telah te jadi mutasi pada s