nikmat jasmani dan rohani kepada penulis, sehingga sampai saat ini penulis dapat menjalankan berbagai aktifitas termasuk pelaksanaan tugas akhir mulai dari pencarian data hingga pada penyusunan laporan. Selawat serta salam selalu tercurah pada manusia sempurna, kekasih Allah sekaligus pemimpin tauladan umat dunia, Nabi besar Muhammad SAW, yang selalu menjadi inspirasi dan contoh dalam melaksanakan aktifitas hablumminannas dan hablumminAllah.
Alhamdulillah atas dukungan dari semua pihak akhirnya penulis dapat menyelesaikan skripsi ini dengan tepat waktu yang berjudul ”Ekstraksi dan Penentuan Kadar Senyawa β-1,3;1,6-D-Glukan dari Jamur Shiitake
(Lentinula edodes) “. Penulis mengucapkan terima kasih yang sedalam-dalamnya kepada seluruh pihak yang telah membantu serta memudahkan penulis dalam menyelesaikan skripsi ini, antara lain
1. Dr. Syopiansyah Jaya Putra, M. Sis sebagai Dekan Fakultas Sains dan Teknologi UIN Syarif Hidayatullah Jakarta.
2. Sri Yadial Chalid, M. Si sebagai Ketua Program Studi Kimia Fakultas Sains dan Teknologi UIN Syarif Hidayatullah Jakarta.
5. Sandra Hermanto, M. Si, sebagai dosen pembimbing II yang telah memberikan saran-saran, kemudahan, motivasi, meluangkan waktu, serta mengarahkan penulis sehingga penulisan skripsi ini dapat berjalan dengan baik.
6. Sri Yadial Chalid, M. Si dan Siti Nurbayti, M. Si, sebagai dosen penguji yang memberikan banyak saran dalam perbaikan skripsi.
7. Seluruh dosen kimia yang telah banyak memberikan ilmunya.
8. Teman-temanku kimia angkatan 2005, HIMKA (Himpunan Mahasiswa Kimia) dan teman-temanku di GCMS (Green Chemistry Movement Study) yang banyak memberikan warna dalam perjalanan penulis selama menempuh pendidikan di kimia UIN Syarif Hidayatullah Jakarta.
Penulis sadar skripsi ini masih jauh dari sempurna, untuk itu saran dan kritik yang membangun diharapkan dari para pembaca. Akhir kata, penulis berharap semoga skripsi ini dapat berguna bagi penulis khususnya dan bagi pembaca pada umumnya.
Jakarta, Juni 2010
KATA PENGANTAR ………... vi
DAFTAR ISI ………...………..… viii
DAFTAR GAMBAR ………... xi
DAFTAR TABEL ………... xii
DAFTAR LAMPIRAN ……….... xiii
ABSTRAK ………. xiv
ABSTRACT ……….………... xv
BAB I PENDAHULUAN ………...… 1
1.1Latar Belakang ………..………... 1
1.2Rumusan Masalah ………..……..… 2
1.3Tujuan Penelitan ……….……... 3
1.4Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ………... 4
2.1 Bahan Pangan Fungsional ……… 4
2.2 Jamur Shiitake ………. 6
2.2.1 Morfologi Jamur Shiitake …………..………... 7
2.2.2 Klasifikasi Jamur Shiitake ……….... 8
2.2.3 Kandungan Nutrisi Jamur Shiitake ………... 9
2.2.4 Khasiat Jamur Shiitake ………... 10
2.7 Spektrofotometer UV-Vis ………... 19
2.8 Spektrofotometer IR ………... 23
BAB III METODE PENELITIAN ……...………...…….…… 29
3.1 Tempat dan Waktu Penelitian ………... 29
3.2 Alat dan Bahan ……….. 29
3.2.1 Alat ………. 29
3.2.2 Bahan ……….. 30
3.3 Prosedur Penelitian ……… 31
3.3.1 Pengambilan Sampel ………... 31
3.3.2 Preparasi Reagen ……...………... 31
3.3.3 Ekstraksi Jamur Shiitake dengan metode Yap & Ng ...………….... 31
3.3.4 Identifikasi Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering Jamur Shiitake dengan FTIR …...…...….… 32
3.3.5 Analisis Kadar Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering Jamur Shiitake dengan Metode Megazyme …..……. 33
3.3.6 Analisis Kadar Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering Jamur Shiitake dengan Metode Congo Red ... 34
BAB IV HASIL DAN PEMBAHASAN ………... 36
4.1 Hasil Ekstraksi Jamur Shiitake ………..…………... 37
4.2 Hasil Identifikasi Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering Jamur Shiitake dengan FTIR ..…...…...…. 38
Gambar 1. Jamur Shiitake …..……… 6 Gambar 2. Struktur Senyawa β-1,3;1,6-D-glukan (Lentinan) .………. 12 Gambar 3. Mekanisme Penghambatan Sel Kanker oleh
Senyawa β-1,3-Glukan …... 14 Gambar 4. Struktur Senyawa Congo Red ... 18 Gambar 5. Skema Alat Spektrofotometer UV-Vis Single Beam ………….…… 21 Gambar 6. Skema Alat Spektrofotometer UV-Vis Double Beam ……….... 21 Gambar 7. Spektrum IR Ekstrak Kering Jamur Shiitake dan
Table 1. Kandungan Nutrisi Jamur Shiitake ……….... 9
Tabel 2. Senyawa Aktif di Dalam Jamur Shiitake ………... 11
Tabel 3. Perbandingan Metode Ekstraksi Yp & Ng dan Chihara ……….... 15
Lampiran 1. Desain penelitian ………. 49 Lampiran 2. Data Hasil Ekstraksi ………..………..… 50 Lampiran 3. Gambar-gambar Tahapan Ekstraksi Hingga Freez Drying ………. 51 Lampiran 4. Data Hasil Pengukuran Kadar Senyawa β-1,3;1,6-D-glukan
dengan Metode Megazyme ... 52 Lampiran 5. Reaksi Selama Analisis Kadar Senyawa β-1,3;1,6-D-glukan
dengan Metode Megazyme ... 56 Lampiran 6. Data Hasil Pengukuran Kadar Senyawa β-1,3;1,6-D-glukan
Semakin meningkatnya kesadaran masyarakat terhadap pentingnya hidup sehat, membuat tuntutan terhadap bahan pangan bergeser. Kini masyarakat tidak hanya menginginkan bahan pangan yang mempunyai komposisi gizi baik, serta penampakan dan cita rasanya yang menarik, tetapi juga memiliki fungsi fisiologis seperti menurunkan tekanan darah, kadar kolesterol, serta aktivitas antikanker dan lainnya. Fenomena ini melahirkan konsep pangan fungsional. Salah satu bahan pangan yang memiliki potensi sebagai bahan pangan fungsional adalah jamur shiitake. Jamur shiitake memiliki fungsi fisiologis salah satunya sebagai antikanker. Aktivitas antikanker jamur shiitake ini disebabkan kandungan senyawa β-1,3;1,6-D-glukan, Untuk mendapatkan senyawa β-1,3;1,6-D-glukan, maka dilakukan proses ekstraksi untuk mengisolasi senyawa tersebut. Metode ekstraksi Yap & Ng (2001) dipilih karena proses ekstraksinya yang cepat, murah dan menggunakan pelarut yang aman (aquades) untuk bahan pangan. Identifikasi senyawa β-1,3;1,6-D-glukan dalam ekstrak jamur shiitake, maka dilakukan analisis FTIR. Selanjutnya dilakukan pengukuran kadar senyawa β -1,3;1,6-D-glukan dengan metode megazyme. Selain menggunakan metode megazyme, pada penelitian ini dikembangkan metode alternatif dengan biaya lebih efisien dan waktu pengerjaan yang lebih efektif yaitu menggunakan pewarna congo red,
sebagai pengganti metode megazyme. Hasil ekstraksi metode Yap & Ng diperoleh kadar ekstrak kering jamur shiitake sebesar 4,4987 gr dengen rendemen hasil sebesar 0,4999%. Hasil analisis FTIR menunjukkan keberadaan senyawa senyawa
β-1,3;1,6-D-glukan dalam ekstrak jamur shiitake, yang teridentifikasi khususnya pada bilangan gelombang 890 nm yang menunjukkan ikatan β-1,3 yang spesifik untuk senyawa β-1,3;1,6-D-glukan. Hasil analisis metode megazyme diperoleh kadar rata-rata (triplo) senyawa β-1,3;1,6-D-glukan sebesar 30,8882%, sedangkan untuk hasil analisis metode congo red belum menunjukkan hasil yang spesifik untuk kadar senyawa β-1,3;1,6-D-glukan.
Increasing of publics consciousness of the importance healthy living, making demands on food shift. Now people do not just want food that has a good nutrient composition, appearance and flavor is interesting, but also has physiological functions such as lowering blood pressure, cholesterol levels, anticancer and other activities. This phenomenon gave birth the concept of functional foods. One of the foodstuffs that have potential as functional food is shiitake mushroom. Shiitake mushroom have a physiological function as an anticancer. Its anticancer activity is due to β-1,3;1,6-D-glukan compound. Lentinan compound is a polysaccharide with a β-1,3 and 1,6-D-glucan bond. To get β-1,3;1,6-D-glukan of shiitake mushroom, then do the extraction process to isolate the β-1,3;1,6-D-glukan compound. Yap & Ng extraction method was chosen because the extraction proces is quick, cheap and safe used for solvents (distilled water) of food. To identification β-1,3;1,6-D-glukan compound in shiitake’s extract, then do the FTIR analysis. Further measured concentration of β -1,3;1,6-D-glukan compound by the megazyme method. In this research developed alternative methods with more efficient cost and effective time by using the Congo red dye, as chance of megazyme method . The Yap & Ng extraction method result obtained dry shiitake’s extract at 4.4987 gr (0,4999%). FTIR analysis result show the existence of β-1,3;1,6-D-glukan compound in the extract glucan, which identified particularly at wave numbers 890 nm is the β-1,3 bond wich specific for the β-1,3;1,6-D-glukan compound. The analysis megazyme method result obtained average (triplo) β-1,3;1,6-D-glukan compound at 30.8882%, while for analysis Congo red method result has not shown specific result for concentration of β-1,3;1,6-D-glukan compound.
BAB I PENDAHULUAN
1.1 Latar Belakang
Seiring dengan makin meningkatnya kesadaran masyarakat akan pentingnya hidup sehat, tuntutan konsumen terhadap bahan pangan juga bergeser. Bahan pangan yang kini banyak diminati konsumen bukan saja yang mempunyai komposisi gizi yang baik serta penampakan dan cita rasanya menarik, tetapi juga harus memiliki fungsi fisiologis tertentu bagi tubuh, seperti dapat menurunkan tekanan darah, kadar kolesterol, kadar gula darah, meningkatkan penyerapan kalsium, serta aktivitas antikanker. Fenomena tersebut melahirkan konsep pangan fungsional (litbang pertanian, Bogor).
Salah satu bahan pangan yang berpotensi sebagai bahan pangan fungsional adalah jamur shiitake. Jamur shiitake dikenal sejak 199 M di China dan telah dibudidayakan secara luas. Jamur shiitake mengandung senyawa β -1,3;1,6-D-glukan, yang dalam jamur shiitake dikenal sebagai senyawa lentinan, yaitu polisakarida yang larut di dalam air dan diakui memiliki aktivitas sebagai antikanker (Hendry, 2005). Kemampuan senyawa β-1,3;1,6-D-glukan dari jamur shiitake sebagai antikanker dibuktikan pada hasil penelitian di lingkungan Cancer Center Institute di Tokyo, Jepang, dan beberapa lembaga sejenis di benua Eropa
Melihat pentingnya senyawa β-1,3;1,6-D-glukan tersebut dalam aktivitas antikanker, maka pada penelitian ini dilakukan proses ekstraksi untuk mengisolasi senyawa β-1,3;1,6-D-glukan dalam jamur shiitake. Metode ekstraksi yang dipilih adalah metode Yap & Ng (2001) karena menggunakan pelarut aquades. Sehingga diperoleh hasil ekstraksi yang aman untuk dikonsumsi (Widyastuti, 2009). Identifikasi senyawa β-1,3;1,6-D-glukan dalam ekstrak jamur shiitake dilakukan analisis FTIR.
Penentuan kadar senyawa β-1,3;1,6-D-glukan pada ekstrak jamur shiitake digunakan metode megazyme, metode ini dapat mengukur secara spesifik kadar senyawa β-1,3;1,6-D-glukan, namun kelemahan metode ini adalah dibutuhkan biaya yang cukup mahal dan waktu analisis yang kurang efektif, selain bahan ujinya sulit didapat dan memiliki batas waktu penggunaan. Untuk itu dalam penelitian ini digunakan pula metode congo red, sebagai alternatif pengukuran kadar senyawa β-1,3;1,6-D-glukan dengan biaya lebih efisien dan waktu pengerjaannya lebih efektif dibandingkan metode megazyme.
Apabila metode congo red dapat secara spesifik mengukur kadar senyawa
β-1,3;1,6-D-glukan, maka diharapkan metode ini nantinya dapat diaplikasikan
untuk industri jamur skala kecil dalam mengukur kadar β-1,3;1,6-D-glukan dari jamur yang mereka miliki.
Rumusan Masalah
2. Apakah senyawa β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake
dapat teridentifikasi dengan analisis FTIR?
3. Bagaimana spesifitas hasil pengukuran kadar senyawa senyawa β -1,3;1,6-D-glukan pada ekstrak kering jamur shiitake dengan metode congo red?
Tujuan Penelitian
1. Mendapatkan nilai berat kering ekstrak jamur shiitake hasil ekstraksi metode Yap & Ng
2. Mengidentifikasi senyawa β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake dengan analisis FTIR.
3. Mengetahui spesifitas metode congo red dalam mengukur kadar senyawa
β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake.
Manfaat Penelitian
1. Memberikan informasi bahwa untuk mengisolasi senyawa β -1,3;1,6-D-glukan pada jamur shiitake, maka dapat dilakukan metode ekstraksi Yap & Ng (2001) dengan hasil ekstrak yang aman dikonsumsi, selain prosesnya yang cepat dan murah.
2. Memberikan informasi bahwa metode congo red dapat digunakan sebagai
alternatif yang lebih murah dan efisien dalam menentukan kadar senyawa
BAB II
TINJAUAN PUSTAKA
2.1 Bahan Pangan Fungsional
Istilah pangan fungsional dipilih dari sederet istilah yang pernah dipopulerkan sebelumnya seperti “pharmafoods”, “designer foods”, “nutraceutical food”, “health foods”, “therapeutic foods” dan banyak lagi.
Secara mudah dapat dikatakan bahwa pangan fungsional adalah bahan pangan yang berpengaruh positif terhadap kesehatan seseorang, selain kandungan gizi dan cita-rasa yang dimilikinya. Jadi dalam hal ini keberadaan faktor ´plus´ bagi kesehatan yang diperoleh karena adanya komponen aktif pada bahan pangan tersebut adalah merupakan ´keharusan´ (Wijaya, 2002).
1. Harus berupa suatu produk pangan (bukan kapsul, tablet atau bubuk) yang berasal dari bahan atau ingredient alami.
2. Layak dikonsumsi sebagai bagian dari diet atau menu setiap hari 3. Mempunyai fungsi tertentu pada saat dicerna.
4. Memberikan peran khusus dalam proses metabolisme tubuh seperti meningkatkan imunitas tubuh, mencegah penyakit tertentu, membantu pemulihan tubuh setelah menderita sakit, menjaga kondisi fisik dan mental serta memperlambat proses penuaan.
Pangan fungsional dibedakan dari suplemen makanan atau obat berdasarkan penampakan dan pengaruhnya terhadap kesehatan. Bila fungsi obat terhadap penyakit bersifat penyembuhan, maka pangan fungsional lebih bersifat pencegahan terhadap penyakit (litbang pertanian, Bogor). Sedangkan menurut Mary K. Schmild dalam salah satu paparannya menyampaikan ada tiga hal utama yang membedakan pangan dengan obat, yaitu:
1. Obat bersifat treatment (perlakuan penyembuhan), sedang pangan fungsional lebih bersifat mengurangi resiko.
2. Pada obat, efek harus dapat dirasakan segera, sedang pada pangan fungsional lebih pada keuntungan di masa mendatang.
2.2 Jamur Shiitake
[image:16.595.110.507.234.597.2]Jamur Shiitake, Lentinula edodes, atau Hioko, adalah jamur pangan asal Asia Timur yang terkenal di seluruh dunia. Namanya diambil dari bahasa Jepang. Shiitake secara harafiah berarti jamur dari pohon shii (Castanopsis cuspidate). Batang pohon shii yang sudah lapuk merupakan tempat tumbuh jamur ini (Widyastuti, 2009).
Gambar 1. Jamur Shiitake
Lentinula edodes atau Lentinus edodes adalah jamur kayu yang di Jepang
dikenal sebagai shiitake. Di China dikenal dengan nama shiang-gu, sedangkan di pasar internasional dikenal sebagai chinese black mushroom atau black forest mushroom (Widyastuti, 2009). Di Indonesia, jamur shiitake dikenal dengan nama
jamur kayu cokelat. Selain itu, jamur ini juga disebut jamur payung karena tudungnya memang berbentuk seperti payung. Di Jawa Barat, khususnya di daerah Pengalengan, shiitake terkenal dengan sebutan jamur jengkol karena bentuk dan aromanya bagaikan jengkol (Sarwintyas dkk, 2001).
alami belum menggunakan bibit buatan, tetapi masih mengandalkan spora yang berterbangan di udara atau dari miselium yang menempel di pepohonan ataupun di tanah. Selain secara alami, shiitake juga dapat dibudidayakan secara tradisional dengan balok kayu. Budidaya ini merupakan usaha agribisnis yang penting di negeri Cina, Jepang dan Korea Selatan. Ada tiga jenis bibit jamur yang dapat digunakan, yaitu jamur yang dapat membentuk tubuh buah pada suhu di atas 20oC, antara 10-15oC, dan pada suhu 10oC (Sarwintyas dkk, 2001).
2.2.1 Morfologi Jamur Shiitake
Morfologi dari jamur shiitake dapat dikenali dengan tudungnya yang berbentuk payung, berwarna coklat muda sampai tua, kadang-kadang berbintik putih yang sering disebut ‘renda’, bahkan ada juga yang retak-retak (bukan pecah), lebar tudung bervariasi antara 2,5-9 cm dan terdapat selaput kutikula. Bagian bawah tudung terdapat lamella (insang) yang berisi spora. Tangkai tudung berwarna seperti tudungnya dan sedikit agak keras, panjang tangkai tudung 3-9 cm dan diameternya 0,5-1,5 cm (Sarwintyas dkk, 2001).
Pertumbuhan badan buah dibagi menjadi empat tingkatan atau stadium, yaitu:
1. Stadium pinhead, berupa tonjolan, merupakan bentuk awal dari calon
jamur.
4. Stadium masak, yakni jamur utuh yang tudungnya sudah mengembang
penuh tetapi lamella-nya belum membuka. Jamur seperti ini yang dipanen. Dalam keadaan normal, dari bentuk pinhead sampai masak memerlukan waktu 2-3 hari.
Jamur shiitake adalah tumbuhan yang berinti spora, tidak mempunyai klorofil dan berupa sel-sel yang menandung selulosa atau chitin. Tubuh jamur dapat berupa sel-sel yang lepas tetapi dapat juga berupa sel-sel yang bergandengan atau berupa benang. Benang ini merupakan tabung atau buluh yang bersekat atau tidak bersekat. Satu helai benang disebut hifa dan kumpulan hifa bercabang disebut miselium hifa, miselium merupakan jaringan tanaman jamur. Hifa yang bersekat-sekat memiliki aliran protoplasma dari sel yang satu ke sel
yang lain melalui pori-pori yang terdapat di sekat. Inti sel dapat berpindah tempat melalui pori-pori tersebut. Dinding sel atau dinding hifa yang mengandung selulosa atau chitin merupakan polisakarida yang mengandung nitrogen (Widyastuti, 2009).
2.2.2 Klasifikasi Jamur Shiitake
Menurut sistematikanya, jamur shiitake termasuk jamur dengan klasifikasi sebagai berikut:
Kingdom : Mycota
Divisio : Amastigomycota Sub division : Basidiomycota
Ordo : Agaricales
Famili : Marasmiaceae
Genus : Lentinula
Spesies : Lentinula edodes
Spesies ini dulu dikenal sebagai Lentinus edodes. Ahli botani Inggris bernama Miles Joseph Berkeley menamai spesies ini sebagai Agaricus edodes di tahun 1878 (Widyastuti, 2009).
Kerabat dekat dari genus Lentinus adalah Lentinellus, misalnya Lentinellus cochleats yang warna dan ukurannya mirip. Perbedaan yang mencolok terdapat
pada tangkai, yang mana bagian yang mengarah ke ujung membesar karena bersatu dengan lamella (gill) (Widyastuti, 2009).
2.2.3 Kandungan Nutrisi Jamur Shiitake
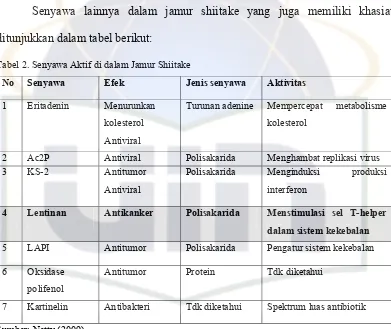
[image:19.595.112.512.347.751.2]Kandungan asam glutamat dalam shiitake cukup tinggi, asam amino tersebut berhubungan dengan cita rasa yang timbul dari jamur ini sebagai penyedap makanan. Selain mempunyai kandungan asam glutamat yang tinggi, shiitake juga mengandung beberapa nutrisi berikut:
Tabel 1. Kandungan Nutrisi Jamur Shiitake
Gizi Dalam 100 gram Berat Kering (%)
Protein Kasar 13,4-17,5
Lemak Kasar 4,9-8,9
Total Karbohidrat (+N) 67,5-78
Karbohidrat (tanpa N) 59,5-70,7
Abu 3,7-7 Kalori 387-392
5 Ribonukleat 165,5 mg
Asam Amino Leucine, isoleucine, valine, tryptophan, lysine, threonine, phenylalanine, methionine dan
histidine
Vitamin B1, B2, D
(Widyastuti, 2009).
2.2.4 Khasiat Jamur Shiitake
Ekstrak jamur shiitake memiliki kemampuan menghambat pertumbuhan kanker sampai 72-92 %. Penemuan paling baru mengungkapkan bahwa ekstrak shiitake berpengaruh juga terhadap penurunan kolesterol dan gula darah, sehingga sangat diharapkan dapat digunakan untuk pengobatan penyakit jantung dan kencing manis. Kandungan protein dan polisakarida pada jamur ini juga berkhasiat sebagai antivirus. Pengaruh buruk akibat rokok dan alkohol yang dapat menyerang jantung dapat dinetralkan dengan mengonsumsi jamur shiitake. Statistik kesehatan wanita di Jepang menunjukkan bahwa persentase wanita penderita kanker uterus atau indung telur di Jepang sangat rendah jika dibandingkan dengan wanita Inggris dan Amerika, karena wanita Jepang sering mengkonsumsi jamur ini (Sarwintyas dkk, 2001).
Jamur shiitake juga mengandung senyawa β-1,3;1,6-D-glukan yang memang sejak lama diakui memiliki kemampuan sebagai antikanker. Senyawa
dan sel natural killer serta sel darah putih lain, mengontrol kanker dan infeksi, mempertinggi efektifitas kekebalan tubuh, mempercepat penyembuhan setelah operasi kanker payudara dan saluran pencernaan, serta penyembuhan kanker leher rahim dan kanker perut (Sarwintyas dkk, 2001). Kandungan senyawa β -1,3;1,6-D-glukan tertinggi didapatkan di bagian batang dekat tudung dan bagian tudungnya. Bagian batang pada umumnya merupakan makanan kaya serat yang sangat bermanfaat untuk mencegah terjadinya kanker usus (Suriawiria, 2005).
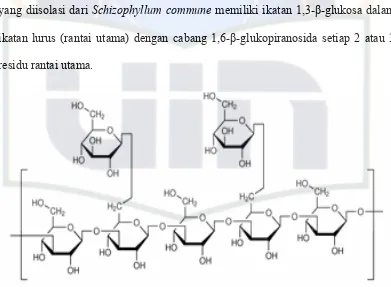
[image:21.595.117.508.303.632.2]Senyawa lainnya dalam jamur shiitake yang juga memiliki khasiat ditunjukkan dalam tabel berikut:
Tabel 2. Senyawa Aktif di dalam Jamur Shiitake
No Senyawa Efek Jenis senyawa Aktivitas
1 Eritadenin Menurunkan
kolesterol
Antiviral
Turunan adenine Mempercepat metabolisme
kolesterol
2 Ac2P Antiviral Polisakarida Menghambat replikasi virus
3 KS-2 Antitumor
Antiviral
Polisakarida Menginduksi produksi
interferon
4 Lentinan Antikanker Polisakarida Menstimulasi sel T-helper dalam sistem kekebalan
5 LAPI Antitumor Polisakarida Pengatur sistem kekebalan
6 Oksidase
polifenol
Antitumor Protein Tdk diketahui
7 Kartinelin Antibakteri Tdk diketahui Spektrum luas antibiotik
Sumber: Netty (2009)
2.3 Senyawa β-1,3;1,6-D-glukan
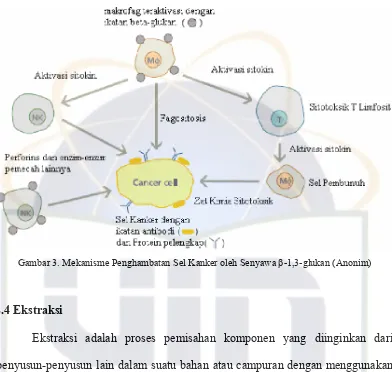
dan dikenal dengan nama senyawa 1,3-β glukan, senyawa ini terdapat pada beberapa jamur seperti shiitake (Lentinula edodes), tiram (Pleurotus ostreatus) dan Schizophyllum commune. Jika senyawa ini diekstraksi dari jamur shiitake maka dikenal dengan nama senyawa lentinan, yang diambil dari bahasa latin jamur shiitake ”Lentinula edodes”. Struktur Senyawa β-1,3;1,6-D-glukan dari jamur shiitake terdiri dari lima residu 1,3-β-glukosa dalam ikatan rantai lurus (rantai utama) dan dua cabang 1,6-β-glukopiranosida rantai samping yang menghasilkan struktur triple helix kanan (Aryantha, 2005). Perbedaan senyawa
β-1,3;1,6-D-glukan (lentinan) yang diisolasi dari jamur shiitake dengan jamur
[image:22.595.115.506.386.673.2]lainnya adalah bentuk strukturnya. Misalnya, untuk senyawa β-1,3;1,6-D-glukan yang diisolasi dari Schizophyllum commune memiliki ikatan 1,3-β-glukosa dalam ikatan lurus (rantai utama) dengan cabang 1,6-β-glukopiranosida setiap 2 atau 3 residu rantai utama.
Konformasi senyawa polisakarida antikanker meliputi bentuk single helix, triple helix dan random coiled. Senyawa β-1,3;1,6-D-glukan dengan konformasi triple helix memiliki berat molekul sekitar 400-800 x 103 kDa (Ooi & Liu, 2000).
Senyawa β-Glukan yang mengandung terutama ikatan 1,6 memiliki aktivitas antikanker lebih rendah. Senyawa glukan dengan berat molekul yang lebih tinggi tampak lebih efektif dibandingkan dengan yang berbobot molekul lebih rendah. Ada berbagai variasi senyawa polisakarida anti tumor dengan struktur kimia berbeda, seperti hetero-β-glukan, heteroglukan, β-glukan-protein,
α-manno-β-glukan, α-glukan, α-glukan-protein dan kompleks
heteroglukan-protein (Ooi & Liu, 2000).
Dr. Chihara yang banyak meneliti dalam masalah antikanker dari jamur shiitake beranggapan bahwa penelitian kanker harus difokuskan terhadap mekanisme peningkatan sistim intrinsik tubuh untuk melawan atau menangkal kanker bukan ke obat pembunuh sel kankernya. Senyawa senyawa β -1,3;1,6-D-glukan adalah salah satu bahan aktif dari jamur shiitake yang berperan dalam meningkatkan sistim pertahanan tubuh terhadap serangan kanker melalui sistim yang kompleks termasuk produksi sitokin dari immunocyte yang telah
direkomendasikan sebagai salah satu obat antikanker di Jepang (Okamoto et al, 2004).
tumor dan menstimulasi sel-sel T-helper. Senyawa lentinan juga berperan sebagai inducer interferon yang dapat mengontrol pertumbuhan dan replikasi sel kanker
[image:24.595.117.509.189.561.2](Aryantha, 2005).
Gambar 3. Mekanisme Penghambatan Sel Kanker oleh Senyawa β-1,3-glukan (Anonim)
2.4Ekstraksi
Ekstraksi adalah proses pemisahan komponen yang diinginkan dari penyusun-penyusun lain dalam suatu bahan atau campuran dengan menggunakan pelarut. Jenis ekstraksi terdiri dari ekstraksi cair-cair dan padat-cair. Ekstraksi padat-cair dapat dilakukan dengan dua cara yaitu aqueus phase dan organic phase. Cara aqueus phase dilakukan dengan menggunakan pelarut air, sedangkan
dalam organic phase digunakan pelarut organik (Pudjaatmaka dan Qodratillah, 2002).
-1,3;1,6-D-glukan dari jamur shiitake dengan pelarut aquades menggunakan metode ekstraksi Yap & Ng.
Menurut Widyastuti (2009), Yap & Ng (2001) telah menetapkan prosedur yang lebih efisien untuk melakukan ekstraksi senyawa β-1,3;1,6-D-glukan jamur shiitake. Uji kemurnian menggunakan kolom analisis karbohidrat, didapat kemurnian β-1,3;1,6-D-glukan 87,5 %. Dari segi komersial, metode ini lebih hemat waktu, lebih efisien dan relatif lebih rendah biaya dibanding metode asli Chihara, et al (1970).
Prinsip metode ekstraksi Yap & Ng (2001) yaitu dengan proses perebusan jamur shiitake menggunakan pelarut aquades pada suhu 100oC. Selanjutnya Hasil ekstraksi diinkubasi pada suhu ruang dan kemudian ditambahkan alkohol 95% dingin (4oC) untuk proses pengendapan ekstrak jamur shiitake. Presipitan (ekstrak cair jamur shiitake) yang diperoleh dimurnikan dengan merebusnya kembali pada suhu 100oC, kemudian didiamkan pada suhu ruang dan diendapkan kembali dengan alkohol 95 % dingin (4oC). Selanjutnya presipitan yang diperoleh dikeringkan dengan menggunakan metode freeze drying.
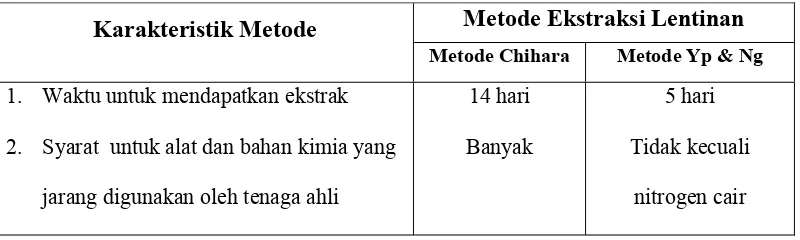
[image:25.595.115.515.626.746.2]Berikut tabel yang menunjukkan perbandingan antara metode ekstraksi Yap & Ng (2001) dan metode asli Chihara et, al (1970).
Table 3. Perbandingan Metode Ekstraksi Yap & Ng dan Chihara.
Metode Ekstraksi Lentinan Karakteristik Metode
Metode Chihara Metode Yp & Ng 1. Waktu untuk mendapatkan ekstrak
2. Syarat untuk alat dan bahan kimia yang
jarang digunakan oleh tenaga ahli
14 hari
Banyak
5 hari
Tidak kecuali
3. Biaya preparasi
4. Total hasil dari 100gr jamur segar
5. Persen Lentinan dari ekstrak yang
dihasilkan (%)
6. Kemurnian
Tinggi
4 mg
96,03
99,23
Rendah
325 mg
87,50
87,65
Sumber: Widyastuti, 2009
2.5 Megazyme
Megazyme merupakan salah satu metode analisis yang spesifik untuk
mengukur kadar senyawa β-1,3;1,6-D-glukan dari yeast dan jamur, namun metode ini memiliki kelemahan dari segi biaya pengujian yang cukup mahal, waktu pengujian yang kurang efisien dan sulitnya mendapatkan bahan uji. Pengukuran kadar senyawa β-1,3;1,6-D-glukan dilakukan secara tidak langsung yaitu dengan mengukur terlebih dahulu kadar total glukan dan α-glukan dalam ekstrak glukan, kemudian kadar senyawa β-1,3;1,6-D-glukan didapat dengan menghitung selisih antara kadar total glukan dan α-glukan.
Prinsip analisis senyawa β-1,3;1,6-D-glukan secara umum dengan megazyme adalah dengan menghidrolisis ekstrak glukan dengan HCl (37 %) yang dilanjutkan dengan pemanasan pada suhu 100oC selama 2 jam menjadi D-glucose. Untuk menyempurnakan proses hidrolisis, ditambahkan exo-1,3-β-glucanase dan β -glucosidase yang berfungsi menghidrolisis Laminarisaccharides (dihasilkan dari
quinoneimine yang dihasilkan, diukur dengan spektrofotometer UV-Vis sebagai
nilai yang menunjukkan kadar senyawa β-1,3;1,6-D-glukan ((McCleary, 2009). Metode megazyme teramasuk kedalam metode enzimatis karena dalam analisisnya digunakan beberapa enzim yang berperan dalam proses hidrolisis, enzim yang digunakan diantaranya (McCleary, 2009):
1. (exo-1,3-β-glucanase + β-glucosidase), enzim ini berperan dalam
menghidrolisis Laminarisaccharides + H2O menjadi D-glucose,
Laminarisaccharides merupakan hasil hidrolisis pertama pada
pengukuran total glukan menggunakan HCl 37 %.
2. Glucose oxidase, enzim ini berperan dalam mengoksidasi D-glucose + H2O + O2 menjadi D-gluconate + H2O2.
3. Amyloglucosidase, enzim ini berperan dalam menghidrolisis ikatan α -glukan menghasilkan D-glucose pada analisis kadar α-glukan.
4. Peroxidase, enzim ini berperan dalam mempercepat reaksi antara
H2O2 yang dihasilkan dengan p-hydroxybenzoic acid +
4-aminoantipyrine menghasilkan quinoneimine (warna merah). Quinoneimine yang dihasilkan diukur menggunakan spektrofotometer
UV-Vis.
2.6 Congo Red
Congo red adalah suatu garam natrium dari
berat molekul 696,66 g/mol. Congo red larut dalam air, dan kelarutan congo red paling baik dalam pelarut organik (wikipedia.com).
Gambar 4. Struktur Senyawa Congo Red (Anonim)
Pada penelitian ini pereaksi warna congo red coba dikembangkan sebagai salah satu metode analisis alternatif yang digunakan untuk menentukan adanya senyawa β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake. Uji kuantitatif kadar senyawa β-1,3;1,6-D-glukan dengan pereaksi congo-red diharapkan menjadi prosedur pengujian yang memiliki kelebihan dari segi keefektifan waktu dan biaya yang lebih efisien dibandingkan metode megazyme.
Pertimbangan dalam melakukan analisis kadar lentinan menggunakan pereaksi warna congo red didasarkan pada penelitian yang dilakukan oleh Ronald M. Teather dan Peter J. Wood (1981) bahwa terjadi interaksi signifikan antara congo-red dengan ikatan β-1,3-D-glukan: “Percobaan terbaru dimana congo red memperlihatkan interaksi dengan polisakarida yang mengandung unit ikatan β -(1,4)-D-glukopiranosil dan interaksi signifikan dengan β-(1,3)-D-glukan dan kemungkinan beberapa hemiselulosa galaktoglukomannan (17-19).
pengukuran yang signifikan, dengan hasil pengukuran yang mendekati hasil pengukuran metode megazyme.
2.7 Spektrofotometer UV-Vis
Pengukuran absorbansi atau transmitansi dalam spektrofotometer ultraviolet dan sinar tampak digunakan untuk analisis kuantitatif spesies kimia. Pengukuran UV-Vis dilakukan pada panjang gelombang 200 nm - 800 nm. Absorbansi spesies ini berlangsung dalam dua tahapan, yaitu:
1. Tahap pertama M + hv = M*, merupakan eksitasi spesies akibat absorbsi foton (hv) dengan waktu hidup terbatas (10-8-10-9 detik).
2. Tahap kedua adalah relaksasi dengan berubahnya M* menjadi spesies baru dengan reaksi fotokimia.
Absorpsi dalam daerah ultraviolet dan daerah tampak menyebabkan eksitasi elektron ikatan. Puncak absorpsi (λ maks) dapat dihubungkan dengan jenis
ikatan-ikatan yang ada dalam spesies. Spektroskopi absorpsi berguna untuk mengkarakterisasikan gugus fungsi dalam suatu molekul dan untuk analisis kuantitatif (Khopkar, 2003).
memberikan keterangan untuk penetuan struktur. Di atas 200 nm merupakan daerah eksitasi elektron dari orbital molekul π dan n, terutama sistem π terkonjugasi mudah pengukurannya dan spektrumnya memberikan banyak keterangan. Karena alasan praktis maka spektrometri ultraviolet-tampak biasa dilakukan di atas 200 nm. Untuk keperluan penentuan sruktur, spektrofotometri ultraviolet-tampak penggunaanya tidak seluas spektrometri inframerah, spektrometri massa dan spektrometri resonansi magnit proton. Kegunaan spektrometri ultraviolet-tampak ini terletak pada kemampuannya mengukur jumlah ikatan rangkap atau konjugasi aromatik di dalam suatu molekul. Elektron sunyi pada oksigen, nitrogen dan sulfur dapat juga termasuk dalam perluasan konjugasi dari sistem rangkap.
Dua hukum empiris telah merumuskan tentang intensitas serapan. Hukum Lambert menyatakan bahwa fraksi penyerapan sinar tidak bergantung dari intensitas sumber cahaya. Hukum Beer mengatakan bahwa penyerapan sebanding dengan jumlah molekul yang menyerap. Dari hukum Lambert-Beer dapat diketahui bahwa hubungan antara transmitansi, tebal cuplikan dan konsentrasi. Hubungan ini dinyatakan sebagai berikut:
Log Io/I = kcb = A
Dimana:
b = tebal sel (cm) dan
A = serapan
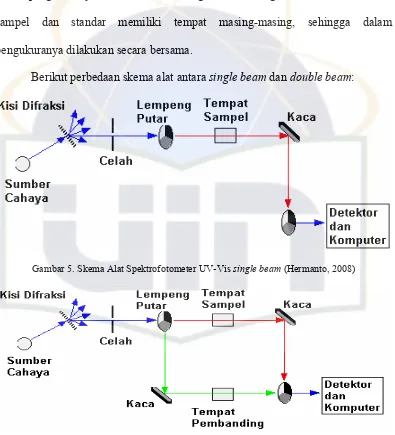
Alat spektrofotometer UV-Vis ada dua macam yaitu single beam dan double beam, perbedaan antara keduanya adalah pada tempat sampel dan standar.
Untuk single beam, tempat sampel dan standar digunakan bergantian, sehingga dalam pengukuranya harus dilakukan bergantian. Sedangkan untuk double beam sampel dan standar memiliki tempat masing-masing, sehingga dalam pengukuranya dilakukan secara bersama.
[image:31.595.118.513.264.699.2]Berikut perbedaan skema alat antara single beam dan double beam:
Gambar 5. Skema Alat Spektrofotometer UV-Vis single beam (Hermanto, 2008)
Walaupun Spektrofotometer single beam dan double beam memiliki perbedaan dalam susunan alatnya, namun keduanya terdiri dari bagian-bagian yang sama. Bagian-bagian dari alat spektrofotometer UV-Vis terdiri dari (Khopkar, 2003):
1. Sumber cahaya: sumber yang biasa digunakan dalam spektrofotometer UV-Vis adalah lampu hidrogen atau lampu deuterium. Kebaikan lampu wolfram adalah energi radiasi yang dibebaskan tidak bervariasi pada berbagai panjang gelombang. Untuk memperoleh tegangan yang stabil dapat digunakan transformator. Jika potensial tidak stabil kita akan mendapatkan energi yang bervariasi. Untuk mengkompensasi hal ini maka dilakukan pengukuran transmitan larutan sampel selalu disertai larutan pembanding
2. Monokromator: digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya dapat berupa prisma atau grating. Untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian ini dapat digunakan celah. Jika celah posisinya tetap maka prisma atau gratingnya yang dirotasikan untuk mendapatkan yang diinginkan. Ada dua tipe prisma yaitu susunan cornu dan susunan littrow. Secara umum tipe cornu menggunakan sudut 60°, sedangkan tipe littrow menggunakan prisma dimana pada sisinya tegak lurus dengan arah sinar yang berlapis alumunium serta mempunyai sudut optik 30°. 3. Sel absorpsi: pada pengukuran di daerah tampak, kuvet kaca atau kuvet kaca
lebih besar dapat digunakan. Sel yang biasa digunakan berbentuk persegi, tetapi bentuk silinder juga dapat digunakan. Kita harus menggunakan kuvet yang bertutup untuk pelarut organik. Sel yang baik adalah kuarsa dan gelas hasil leburan, serta seragam keseluruhannya.
4. Detektor: peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang.
2.8Spektrofotometer IR
hanya terbatas pada perubahan energi setingkat molekul. Untuk tingkat molekul, perbedaan dalam keadaan vibrasi dan rotasi digunakan untuk mengabsorpsi sinar infra merah. Jadi untuk dapat mengabsorpsi, molekul harus memiliki perubahan momen dipole sebagai akibat dari vibrasi. Berarti radiasi medan listrik yang berubah-ubah akan berinteraksi dengan molekul dan akan menyebabkan perubahan amplitudo salah satu gerakan molekul (Khopkar, 2003).
Posisi relatif atom dalam molekul tidak pasti, tetapi berubah-ubah terus-menerus karena vibrasi. Untuk molekul dwi-atom dan tri-atom, vibrasi dapat dianggap dan dihubungkan dengan energi absorpsi tetapi untuk molekul poliatom, vibrasi tidak dapat dengan mudah diperkirakan, karena banyaknya pusat vibrasi yang berinteraksi. Umumnya vibrasi diklasifikasikan sebagai vibrasi ulur dan vibrasi tekuk. Vibrasi ulur menyangkut konstanta vibrasi antara dua atom sepanjang sumbu ikatan, sedangkan vibrasi tekuk karena berubahnya sudut antara dua ikatan dan ada empat tipe, yaitu scrissoring, rocking, wagging, dan twisting. Keempat vibrasi tersebut hanya mungkin bagi molekul yang mempunyai lebih dari dua atom (Khopkar, 2003).
Berikut bentuk-bentuk vibrasi: 1. bending
3. wagging (kibasan) : atom-atomnya bergerak bolak balik keluar bidang atau
molekul
4. rocking (goyangan) : atom-atomnya bergerak bolak-balik dalam bidang
5. scissoring (guntingan) : dimana atom-atom yang terikat pada atom pusat bergerak mendekat dan menjauh satu sama lain sehingga sudutnya berubah-ubah
6. twisting (plintiran) : atom-atom yang terikat pada molekul yang diam
Berikut ini adalah beberapa gugus fungsi dengan daerah serapannya:
Tabel 4. Beberapa Gugus Fungsi dengan Daerah Serapanya
Gugus Jenis Senyawa Daerah Serapan (cm-1)
C-H C-H C-H C-H C=H C≡H C=C C-H C-O C=O O-H O-H O-H N-H C-N C≡N -NO2 Alkana Alkena Aromatik Alkuna Alkena Alkuna Aromatik Alkana
Alkohol, eter, asam karboksilat, ester Aldehid, keton, asam karboksilat, ester Alkohol, fenol (monomer)
Alkohol, fenol (ikatan H) Asam karboksilat Amina Amina Nitril Nitro 2850-2960, 1350-1470 3020-3080, 675-1000 3000-3100, 675-870 3300 1640-1680 2100-2260 1500-1600 2850-2960, 1350-1470 1080-1300 1690-1760 3610-3640 200-3500 (lebar) 500-3000 (lebar) 3300-3500 1180-1360 2210-2260 1515-1560, 1345-1385
Sumber: Takeuchi (2009)
Spektrofotometer infra merah biasanya merupakan spektrofotometer ganda dan terdiri dari 5 bagian utama yaitu sumber radiasi, daerah cuplikan, kisi difraksi (monokromator), dan detektor.
batang cekung dari sirkonium dan yitrium oksida yang dipanasi sekitar 1500oC dengan arus listrik. Sumber ini memancarkan radiasi antara 0,4-20 m dan kurang stabil jika dibandingkan dengan globar, tetapi globar memerlukan pendinginan air.
2. Monokromator, monokromator terdiri dari sistim celah masuk dan celah keluar, alat pendispersi yang berupa kisi difraksi atau prisma, dan beberapa cermin untuk memantulkan dan memfokuskan berkas sinar. Bahan yang lazim digunakan prisma adalah natrium klorida, kalium bromida, sesium bromida dan litium fluorida. Prisma natrium klorida paling banyak digunakan untuk monokromator infra merah, karena dispersinya tinggi untuk daerah antara 5,0-16 m, tetapi dispersinya kurang baik untuk daerah antara 1,0-5,0 m. Kalium bromida dan sesium bromida merupakan bahan prisma yang baik untuk infra merah jauh. Litium fluorida merupakan bahan yang baik untuk infra merah dekat. Bahan-bahan tersebut diatas bersifat higroskopis, sehingga dapat dirusak oleh uap air.
orde saja. Hal yang sama juga dapat diperoleh dengan membuat sudut jalur kisi sedemikian rupa sehingga sinar yang didispersikan terpusat hanya pada satu orde saja.
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di tiga tempat yaitu Laboratorium Bahan Alam, Kimia LIPI-PUSPIPTEK, Serpong, Tanggerang; Laboratorium Mikologi, Teknologi Bioindustri, gedung 1 LAPTIAB, BPPT-PUSPIPTEK, Serpong, Tanggerang dan Laboratorium Pangan, Pusat Laboratorium Terpadu UIN Syarif Hidayatullah, Jakarta. Penelitian ini dilakukan mulai bulan Oktober 2009 hingga Januari 2010.
3.2 Alat dan Bahan 3.2.1 Alat
Peralatan yang digunakan pada penelitian ini terdiri dari peralatan untuk ekstraksi, yaitu: blender, beackerglass, hot plate, magnetic stirrer, sentrifius (sigma 201m) dan batang pengaduk. Peralatan untuk pengeringan sampel hasil ekstraksi, yaitu: cawan petri dan alat freeze-dryer (telstar iyoalfa 15). Peralatan untuk uji megazyme dan congo red, yaitu: tabung uji dengan tutup, tabung reaksi, waterbath (Kottermann Labortechnik), mikro pipet, magnetic strirrer, vortex, sentrifius (HIMAC CR 21G), rak tabung reaksi, hot plate, termometer raksa.
lentinan), Spektrometer UV-Vis double beam Hitachi tipe V-2001 (untuk analisis kadar senyawa lentinan).
3.2.2 Bahan
Bahan-bahan yang dipakai pada penelitian ini terdiri dari bahan sampel dan bahan untuk analisis. Bahan sampel adalah jamur shiitake yang diperoleh dari swalayan jln. Ampera Raya No.38 Cilandak Timur, Jakarta-Selatan dan β -1,3;1,6-D-glukan Standar (from barley, SIGMA, (C6H10O5)n, powder, glukosa >95 %)
diperoleh dari Kimia LIPI Pasar Jumat, Lebak Bulus, Jakarta-Selatan.
Bahan untuk analisis terdiri dari: bahan ekstraksi adalah aquades dan alkohol 96%. Bahan analisis FTIR adalah serbuk KBr. Bahan untuk analisis kadar senyawa β-1,3;1,6-D-glukan dengan metode congo red terdiri dari NaOH 1 M dan pereaksi congo red. Bahan analisis kadar senyawa β-1,3;1,6-glukan dengan metode Megazyme yaitu Megazyme kits (dari Irlandia) dipesan oleh laboratorium Mikologi, laboratorium Teknologi Bioindustri, BPPT-PUSPIPTEK, serpong, tanggerang, terdiri dari Kit: botol 1 (suspensi exo-1,3-β-Glucanase (100 U/mL) + β-Glucosidase (20 U/mL), 2.0 mL); botol 2 (larutan Amyloglucosidase (1630
U/mL) + invertase (500 U/mL) dalam 50 % v/v gliserol, 20 mL); botol 3 (pereaksi buffer glukosa (pekat; 50 mL)); botol 4 (Glucose oxidase >12,000 U/L, Peroxidase >650 U/L, 4-Aminoantipyrine 0.4 mM); botol 5 (larutan standar
D-Glucose (5 mL, 1.00 mg/mL) in 0.2 % w/v asam benzoid); botol 6 (control yeast β-glucan, 56 %), dan Reagen: buffer sodium asetat (1,2 M; pH-3,8), buffer
3.3 Prosedur Penelitian 3.3.1 Pengambilan Sampel
Jamur shiitake diperoleh dari swalayan jln. Ampera Raya No.38 Cilandak Timur, Jakarta-Selatan pada tanggal 12 Oktober 2009. Jamur shiitake yang digunakan merupakan jamur shiitake segar.
3.3.2 Preparasi Reagen
Reagen 1: ditambahkan 8 mL buffer natrium asetat (200 mM, pH-5,0) ke dalam botol 1, kemudian disimpan dalam tabung polypropylene pada suhu -20oC (reagen stabil > 2 tahun pada suhu -20oC). Reagen 2: diencerkan isi botol 3 (pereaksi buffer glukosa (pekat; 50 mL)) menjadi 1 L dengan air yang didistilasi atau diionisasi (stabil >2 tahun pada suhu 4oC). Reagen 3: dilarutkan isi botol 4 (Glucose oxidase >12,000 U/L, Peroxidase >650 U/L, 4-Aminoantipyrine 0.4 mM) kedalam isi botol 3 yang telah diencerkan (stabil 2-3 bulan pada suhu 4oC dalam botol gelap, atau >12 bulan pada suhu -20oC).
3.3.3 Ekstraksi Jamur Shiitake dengan Metode Yap & Ng
1:1 dan disimpan dalam freezer pada suhu -15oC selama 1 malam untuk mengendapkan senyawa β-1,3;1,6-D-glukan yang terlarut dalam pelarut aquades. Endapan ekstrak basah jamur shiitake (berbentuk gel) yang diperoleh dipisahkan, kemudian direbus kembali dengan aquades (100oC) hingga larut. Setelah semua endapan larut kemudian diinkubasi pada suhu ruang, hingga suhunya ±27oC dan disaring. Selanjutnya ditambahkan kembali etanol 95 % (4oC) dengan volume 1:1 dan disimpan dalam freezer pada suhu -15oC selama satu malam untuk mengendapkan senyawa β-1,3;1,6-D-glukan kembali. Residu (ampas) dari jamur shiitake diekstrak kembali, ekstraksi berulang dilakukan hingga didapatkan ekstrak basah jamur shiitake dengan berat minimun. Setelah diperoleh ekstrak basah jamur shiitake, kemudian dilakukan proses pengeringan dengan metode freeze drying selama 5 hari, untuk selanjutnya dihaluskan menjadi serbuk.
3.3.4 Identifikasi Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering Jamur
Shiitake dengan FTIR
3.3.5 Analisis Kadar Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering
Jamur Shiitake dengan Metode Megazyme
1. Penentuan Kadar Total Glukan
2. Penentuan Kadar α-glukan
Ditimbang 100 mg ekstrak kering jamur shiitake, kemudian ditambahkan 2 ml KOH 2 M, kemudian divortex selama 20 menit, ditambahkan 8ml buffer natrium Asetat 1,2 M pH-3,8 dan divortex, kemudian ditambahkan 0,2 ml enzim botol 2 (larutan Amyloglucosidase (1630 U/mL) + invertase (500 U/mL) dalam 50 % v/v gliserol, 20 mL) dan divortex kembali, selanjutnya diinkubasi pada 40oC selama 30 menit dan divortex pelan-pelan. Kemudian disentrifugasi selama 10 menit, diambil 0,1 ml supernatan dan ditambahkan 0,1 ml buffer sodium asetat pH-5 dan divortex, ditambahkan kembali 3 ml reagen 3 (GOPOD) dan divortex, diinkubasi pada 40oC selama 20 menit. Diukur absorbansi dengan spektrofotometer UV-Vis pada panjang gelombang 510 nm. Penentuan Kadar α -glukan dilakukan sebanyak tiga kali (triplo). Dilakukan pula Penentuan Kadar α -glukan dari yeast dengan perlakuan dan waktu yang sama.
3.3.6 Analisis Kadar Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering Jamur Shiitake dengan Metode Congo Red
500 l NaOH 0,2 M dan divortex. Selanjutnya ditambahkan 400 l pereaksi congo red dan divortex kembali untuk mencampurnya dan diinkubasi selama 20 menit
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Ekstraksi Jamur Shiitake
Hasil Ekstraksi jamur shiitake menggunakan metode Yap & Ng dengan proses ekstraksi berulang sebanyak tujuh kali, maka dari 900 g sample jamur diperoleh total ekstrak basah jamur shiitake basah sebesar 84 g. Dengan hasil berat kering sebesar 4,4987 g atau 0,4999 % (w/w) . Menurut penelitian yang dilakukan Yap & Ng (2001), bahwa dengan metode ekstraksi yang sama dari 100 g sample jamur shiitake diperoleh berat kering sebesar 325 mg (0,3250 % w/w)
Penggunaan pelarut aquades panas dalam proses ekstraksi jamur shiitake didasarkan pada sifat kelarutan senyawa β-glukan yang akan diekstraksi, menurut Widyastuti (2009): β-glukan adalah polisakarida yang larut dalam pelarut aquades panas dan NaOH. Terekstraknya senyawa β-1,3;1,6-D-glukan oleh aquades panas, dapat terjadi karena pada saat proses pemanasan membuat rantai cabang dari senyawa β-1,3;1,6-D-glukan terbuka, kondisi ini memungkinkan aquades untuk masuk kedalam struktur polisakarida β-1,3;1,6-D-glukan dan berinteraksi ikatan hidrogen dengan gugus –OH dari senyawa β-1,3;1,6-D-glukan. Sehingga senyawa
β-1,3;1,6-D-glukan dapat terekstrak kedalam pelarut aquades. Pada proses ini
terjadi gelatinisasi yang dapat terlihat dari supernatan hasil ekstraksi yang mengental.
pelarut aqudes. Dengan penambahan etanol maka interaksi hidrogen antara aquades dengan senyawa β-1,3;1,6-D-glukan tergantikan dengan interaksi antara etanol dengan aquades, sehingga menyebabkan senyawa β-1,3;1,6-D-glukan mengendap. Ketidakmampuan senyawa β-1,3;1,6-D-glukan untuk berinteraksi dengan etanol karena sifat kelarutanya yang kecil. Menurut penelitian yang dilakukan oleh Kusmawati dan Irma, telah dibuktikan bahwa semakin rendah suhu etanol yang digunakan dalam proses pengendapan, maka semakin banyak polisakarida yang dapat diendapkan. Untuk lebih mengoptimalkan proses pengendapan ekstrak glukan, maka setelah penambahan etanol dingin 95 % (4oC) dilanjutkan dengan proses penyimpanan dalam freezer (-150C) selama 1 malam, sehingga diharapkan semakin banyak ekstrak glukan yang terendapkan.
Perebusan kembali endapan ekstrak basah jamur shiitake yang telah diperoleh dilakukan untuk menghilangkan partikel pengotor ataupun senyawa lain yang masih terbawa selama proses perebusan pertama ataupun selama proses pengendapan senyawa β-1,3;1,6-D-glukan. Proses pengeringan ekstrak basah jamur shiitake menggunakan metode freeze drying dipilih agar supaya struktur ekstrak kering jamur shiitake yang diperoleh tidak rusak, karena dalam metode freeze drying tidak digunakan panas yang tinggi. Sedangkan jika proses
pengeringan menggunakan oven dapat merusak struktur ekstrak kering jamur shiitake yang diperoleh.
4.2 Hasil Identifikasi Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering
Jamur Shiitake dengan FTIR
Identifikasi senyawa β-1,3;1,6-D-glukan dalam ekstrak kering jamur shiitake dapat ditentukan dengan melihat kemiripan peak-peak yang muncul pada spektrum ekstrak kering jamur shiitake dengan spektrum β-1,3;1,6-D-glukan standar (from barley, sigma, kemurnian >95 %).
Hasil analisis IR menghasilkan data spektrum sebagai berikut:
4000.0 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 600 450.0
10.0 15 20 25 30 35 40 45 50 55 59.4 cm-1 %T
Len t in an St an dar B- Glu k an
[image:48.595.118.504.265.561.2]3840.30 3424.24 2892.74 1650.75 1375.65 1070.34 895.57 600.17 890 Standar 470.44 653.21 Ekstrak Shiitake 1431.10 1541.64 3395.21 2927.96 1651.79 1076.20
Gambar 7. Spektrum IR Ekstrak Kering Jamur Shiitake dan β-1,3;1,6-Glukan Standar (Barley)
standar, sehingga perlu dilakukan identifikasi lebih lanjut terhadap peak-peak yang muncul pada spektrum ekstrak kering jamur shiitake tersebut.
Dari beberapa peak-peak yang muncul pada spektrum ekstrak kering jamur shiitake maka dapat teridentifikasi beberapa gugus fungsi sebagai berikut: pada bilangan gelombang 3395,21 cm-1 menunjukkan gugus fungsi OH asam, pada bilangan gelombang 2927,96 cm-1 menunjukkan gugus fungsi CH aromatik, pada bilangan gelombang 1076,20 cm-1 menunjukkan gugus fungsi C-O-C stretching dan yang paling spesifik adalah keberadaan peak pada bilangan gelombang 890 cm-1 yang menunjukkan ikatan 1,3-β-glikosidik.
Keberadaan gugus-gugus fungsi tersebut sebagai identifikasi β -1,3;1,6-D-glukan dibuktikan juga dengan penelitian yang dilakukan oleh Synytsya dkk (2008) bahwa adanya senyawa β-1,3;1,6-glukan dapat dilihat dari ikatan polisakarida yang kuat terutama dalam cincin piran yang ditunjukkan pada bilangan gelombang 950-1200 cm-1, adanya C-O-C stretching dari ikatan glikosida pada bilangan gelombang 1150-1160 cm-1, ikatan β-glikosidik yang spesifik pada bilangan gelombang 894 cm-1.
dilakukan oleh Werning (2008) pada penentuan β-glukan, dimana pada bilangan gelombang tersebut menunjukkan adanya vibrasi CO-NH dari protein atau proteoglukan. Ini diperkuat pula oleh penelitian yang dilakukan oleh Synytsya dkk (2008), bahwa pada sekitar bilangan gelombang 1650 cm-1 dan 1540 cm-1 menunjukkan vibrasi amida dari protein.
Dengan demikian, dari hasil analisis FTIR dapat diidentifikasi senyawa
β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake. Namun demikian dari
hasil tersebut belum bisa memastikan kadar senyawa β-1,3;1,6-D-glukan secara kuantitatif. Sehingga, perlu dilakukan pengujian lebih lanjut.
4.3 Hasil Analisis Kadar Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering
Jamur Shiitake dengan Metode Megazyme
Selanjutnya dilakukan pengukuran kadar senyawa β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake. Hasil pengukuran (triplo) kadar senyawa β -1,3;1,6-D-glukan menggunakan metode megazyme dengan proses perhitungan melalui program komputerisasi Mega-Cal Yeast and Mushroom β-glucan Determination maka diperoleh kadar senyawa β-1,3;1,6-D-glukan sebesar 32,8279 %; 30,5821 %; 29,2545 % dengan kadar rata-rata sebesar 30,8882 %. Sedangkan untuk pengukuran (triplo) kadar β-1,3;1,6-D-glukan dari yeast diperoleh nilai sebesar 54,2977 %; 54,2433 % dan 53,2018 %.
kadar senyawa β-1,3;1,6-D-glukan menggunakan metode megazyme. Sebagai kontrol positif maka pengukuran kadar β-1,3;1,6-D-glukan dari yeast dilakukan dengan perlakuan dan waktu yang sama terhadap pengukuran kadar β -1,3;1,6-D-glukan pada ekstrak kering jamur shiitake, selain itu kadar β-1,3;1,6-D-glukan dari yeast yang diperoleh harus berkisar antara 50-56 %, sebagaimana yang ditetapkan dalam prosedur pengukuran metode megazyme. Apabila kadar β -1,3;1,6-D-glukan dari yeast yang diperoleh <50% maka prosedur pengujian kadar senyawa β-1,3;1,6-D-glukan dari sampel harus diulang.
Terjadinya penurunan kadar dari setiap pengulangan pada pengujian kadar senyawa β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake maupun kadar β -1,3;1,6-D-glukan dari yeast, kemungkinan dapat disebabkan oleh kerja enzim yang digunakan dalam pengujian kurang optimum. Berkurangnya aktivitas enzim ini kemungkinan bisa disebabkan karena terkontaminasinya enzim selama perlakuan. Namun karena penurunan kadar senyawa β-1,3;1,6-D-glukan dalam eksrak kering jamur shiitake maupun kadar senyawa β-1,3;1,6-D-glukan dari yeast tidak terlalu signifikan maka tidak terlalu jadi masalah untuk menyimpulkan
kadar yang diperoleh.
4.4 Hasil Analisis Kadar Senyawa β-1,3;1,6-D-glukan pada Ekstrak Kering
Jamur Shiitake dengan Metode Congo Red
sigma, kemurnian >95 %), maka didapat konsentrasi senyawa β-1,3;1,6-D-glukan sebesar 44.5200 ppm dengan rendemen hasil sebesar 890,0400 %.
Jika dilihat dari persen kadar senyawa β-1,3;1,6-D-glukan yang didapat maka nilai ini sangat tidak mungkin menunjukkan hasil pengukuran yang tepat. Begitu juga jika hasil tersebut dibandingkan dengan hasil pengukuran kadar senyawa β-1,3;1,6-D-glukan dengan metode megazyme, maka kedua metode ini menunjukkan hasil yang sangat jauh berbeda.
Dari hasil ini maka dapat terlihat ketidakmampuan metode congo red dalam menentukan kadar senyawa β-1,3;1,6-D-glukan secara spesifik, hal ini kemungkinan disebabkan karena pada pengukuran dengan metode congo red bukan hanya senyawa β-1,3;1,6-D-glukan yang terukur, melainkan seluruh polisakarida (ikatan β dan α-glukan). Kemungkinan ikut terukurnya polisakarida lain dikarenakan terjadinya interaksi antara pewarna congo red dengan polisakarida lain. Hal ini dapat dibuktikan dari penelitian yang dilakukan oleh Anugraha (2008) bahwa Congo red akan bereaksi dengan polisakarida, termasuk D-glukan dan selulosa yang telah disubstitusi (CMC) menjadi polisakarida kompleks yang berwarna merah.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan, dapat disimpulkan: 1. Hasil ekstraksi metode Yap & Ng diperoleh berat kering ekstrak jamur
shiitake (ekstrak glukan) sebesar 4,4987 g dengan rendemen hasil per berat sampel adalah 0,4999 %
2. Analisis dengan FTIR dapat mengidentifikasi senyawa β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake, yang ditunjukkan dengan keberadaan beberapa gugus fungsi seperti OH dari asam pada bilangan gelombang 3395,21 cm-1, gugus fungsi CH aromatik pada bilangan gelombang 2927,96 cm-1,gugus fungsi C-O-C stretching pada bilangan gelombang 1076,20 cm-1 dan ikatan 1,3-β-glikosidik pada bilangan gelombang 890 cm-1.
3. Metode congo red belum mampu secara spesifik menentukan kadar senyawa
β-1,3;1,6-D-glukan pada ekstrak kering jamur shiitake, terlihat dari hasil
pengukuran kadar senyawa β-1,3;1,6-D-glukan yang diperoleh berbeda jauh dengan hasil pengukuran metode megazyme
5.2 Saran
1. Dalam melakukan penentuan kadar β-1,3;1,6-D-glukan menggunakan metode megazyme, perlu diperhatikan proses penyimpanan (harus dalam lemari es dan
DAFTAR PUSTAKA
Anugraha, Prasidi. 2008. Deteksi Aktivitas Enzim Eksoglukanase Bakteri Selulolitik dalam Menghidrolisis Secara In-vitro. Surabaya:
Perpustakaan Universitas Erlangga.
Anonim. Beta-Glucan And The Immune System. New Zealand : Glucagel. Anonim. Struktur Congo Red. Wikipedia. Com.
Anonim. Peluang Tanaman Rempah dan Obat Sebagai Sumber Bahan Pangan. Bogor: Litbang Pertanian.
Aryantha, I Nyoman P. 2005. Pengembangan Produk Kesehatan dari Jamur Shiitake. Jakarta: BPPT.
Hendry, Reni Efita. 2005. Manfaat Jamur Sebagai Bahan Pangan & Obat. Majalah Health Today.
Hermanto, Sandra. 2008. Mengenal Lebih Jauh Teknik Analisa Kromatografi & Spektrofotometri. Jakarta: Pusat Laboratorium Terpadu UIN syahid.
Khopkar, S. M. 1990. Konsep Dasar Kimia Analitik. Jakarta: Universitas Indonesia (UI-Press).
Kusmawati, Ati dan Irma Budi P. Pengambilan Polisakarida Acemannan dari Aloe vera menggunakan Etanol Sebagai Pengendap. Seamarang:
Universitas Diponegoro.
Kusmiati, dkk. 2007. Produksi β-Glukan Dari Dua Galur Agrobacterium sp. Pada Media Mengandung Kombinasi Molase dan Urasil. Surakarta:
Jurusan Biologi FMIPA UNS.
McCleary, Barry V. 2009. Mushroom and Yeast Beta-Glucan Assay Procedure. Irlandia: Megazym. Com.
Megazym.com.
Okamoto et al. 2004. Lentinan From Shiitake Mushroom (Lentinus edodes) Suppresses Expression of Cytochromen P450 IA Subfamily in The
Mouse Liver. Biofactors. 21(1-4):407-9.
Ooi, V. E. C. dan F. Liu. 2000. Immunomodulation and Anti-Cancer Activity of Polysaccharide-Protein Complexes, Current Medicinal Chemistry, (7)
715-729.
Pudjaatmaka, A. H dan M. T Qodratillah. 2002. Kamus Kimia. Jakarta: Balai Pustaka.
Sarwintyas, dkk. 2001. Tinjauan Literatur Jamur Kegunaan Kimia dan Khasiat. Jakarta: LIPI.
Sudjadi. 1986. Metode Pemisahan. Yogyakarta: UGM Press.
Suriawiria, Unus. 2005. Teknologi Produksi Shiitake. Makalah Pra Workshop Pengembangan Produk dan Industri Jamur Pangan, BPPT Jakarta 1-2 Agustus 2005.
Synytsya, Andriy. dkk. 2008. Glucans from fruit bodies of cultivated mushrooms Pleurotus ostreatus and leurotus eryngii: Structure and potential
prebiotic activity. Czech Republic: www.elsevier.com/locate/carbpol.
Synytsya, Andriy. 2008. Mushrooms of Genus Pleurotus as a Source of Dietary Fibres and Glucans for Food Supplements. Czech Journal Food Sci.
Takeuchi, Yoshito. 2009. Metode Spektroskopik. Situs Resmi Kimia Indonesia: Chem-is-try. Org.
Theather, Ronald M dan Peter J. Wood. 1981. Use of Congo Red-Polysaccharide Interactions in Enumeration and Characterization of Cellulolytic
Bacteria from the Bovine Rument. Kanada.
Werning, Laura Maria. 2008. Heterologous Expression of a Position 2-Substituted (1,3)-β-D-Glucan in Lactococcus lactis. Journal of American Society
for Microbiology.
Widyastuti, Netty. 2009. Jamur Shiitake-Budidaya & Pengolahan Si Jamur Penakluk Kanker. Jakarta: Lily Publisher.
Lampiran 1. Desain penelitian
Jamur Shiitake
Dicuci dan Diblender
Ekstraksi (7x pengulangan)
Jamur Shiitake Halus
Ekstrak Basah Jamur Shiitake
freeze drying
Ekstrak Kering Jamur Shiitake
Penghalusan Serbuk
Analisa Kualitatif Analisa Kuantitatif
Analisa FTIR
Teknik Cakram KBr
Metode Megazym
Pj. Gel 540nm
Metode Congo Red
Lampiran 2. Data Hasil Ekstraksi
Hasil Ekstraksi Jamur Shiitake dengan Ekstraksi Berulang
Pengulangan ∑ Pelarut Aquades (L) Ekstrak Glukan (grm)
1 2,55 27
2 2,30 24
3 1,45 17
4 1,05 7
5 0,95 4
6 0,65 3
7 0,90 2
Perhitungan Rendemen Ekstrak Kering Jamur Shiitake: % rendemen = berat ekstrak kering jamur shiitake x 100%
Lampiran 3. Gambar-gambar Tahapan Ekstraksi Hingga Freeze Drying
Penghalusan
Jamur Shiitake Kasar Jamur Shiitake Halus
+ Aquades
sentrifugasi
Proses Perebusan Ekstrak dan Residu Terpisah
Proses Presipitasi I Ekstrak Basah Jamur Shiitake I
Proses Perebusan Proses Penyaringan
Proses Presipitasi II Ekstrak Basah Jamur Shiitake II
Freez Drying Pemisahan + alkohol 4oC
Disaring Pemisahan + alkohol 4oC
Pemurnian
Lampiran 4. Data Hasil Pengukuran Kadar Senyawa β-1,3;1,6-D-glukan dengan Metode Megazyme
Tabel Absorbansi Total Glukan, α-glukan dan Glukosa Hasil Analisis Spektrofotometer UV-Vis
Ulangan 1 A1 A2 A1-rata2 Blanko A2-rata2 Blanko ∆E
Ekstrak shiitake:
- total glukan
- alfa glukan
Ekstrak Yeast:
- total glukan
- alfa glukan
Glukosa Blanko 0,438 0,053 0,693 0,079 1,063 0,017 0,451 0,060 0,651 0,076 1,090 0,017 0,421 0,036 0,676 0,062 1,046 -0,434 0,043 0,634 0,059 1,073 - 0,4275 0,0395 0,6550 0,0605 1,0595 - Ulangan 2 Ekstrak shiitake:
- total glukan
- alfa glukan
Ekstrak Yeast:
- total glukan
- alfa glukan
Glukosa Blanko 0,433 0,083 0,675 0,078 1,088 0,016 0,439 0,061 0,676 0,080 1,079 0,016 0,417 0,067 0,659 0,062 1,072 -0,423 0,045 0,660 0,064 1,063 - 0,4200 0,0560 0,6595 0,0630 1,0675 Ulangan 3 Ekstrak shiitake:
- total glukan
- alfa glukan
Ekstrak Yeast:
- total glukan
- alfa glukan
Tabel Hasil Pengukuran Kadar Total Glukan, α-glukan dan β-glukan
% Total Glukan % α-glukan % β-glukan Ulangan ke-1
Ekstrak Shiitake 36,1336 3,3058 32,8279
Ekstrak Yeast 54,8172 0,5195 54,2977
Ulangan ke-2
Ekstrak Shiitake 35,2337 4,6515 30,5821
Ekstrak Yeast 54,7802 0,5369 54,2433
Ulangan ke-3
Ekstrak Shiitake 33,3994 4,1449 29,2545
Ekstrak Yeast 53,7179 0,5161 53,2018
• Cara Perhitungan Kadar Senyawa β-1,3;1,6-D-glukan dengan Persamaan
Total Glukan (% w/w) = ∆E x F x 100 x 1 x 100 x 162 (+ oligomer dll) 0.1 1000 W 180
= ∆E x F/W x 90
α-glukan (% w/w) = ∆E x F x 1000 x 1 x 100 x 162 (+ oligomer dll) (or 103) 1000 W 180
= ∆E x F/W x 90 (volume akhir 100 ml) = ∆E x F/W x 9.27 (volume akhir 10.3 ml)
β-glukan = Total glukan - α-glukan
(+ oligomer dll) (+ oligomer dll)
Dimana:
∆E = absorban sampel – absorban blanko
F = faktor untuk mengkonversi absorban ke g dari D-glukosa 100/0,1= faktor koreksi volume; untuk total glukan (yeast)
103 = faktor koreksi volume; untuk α-glucan (10,3 ml yang dianalisa) atau 1000 = faktor koreksi volume; untuk α-glucan (100 ml yang dianalisa)
1/1000 = konversi dari g ke miligram
162/180 = faktor untuk mengkonversi dari D-glukosa bebas, yang diukur, untuk anhidroglukosa
Contoh Perhitungan Pada Ulangan Pertama Shiitake :
Total glukan (%w/w) = 0,4275 x (94,3841/100,5) x 90
= 36,1336
α-glukan (%w/w) = 0,0395 x (94,3841/101,5) x 90
= 3,3058
% β-glukan = 36,1336 – 3,3058 = 32,8279
Yeast :
Total glukan (%w/w) = 0,6550 x (94,3841/101,5) x 90
= 54,8172
α-glukan (%w/w) = 0.0605 x (94,3841/101,9) x 9,27
= 0,5195
• Cara Perhitungan Kadar Senyawa β-1,3;1,6-D-glukan dengan Program Komputerisasi
Contoh Perhitungan Pada Ulangan Pertama
Dengan melihat hasil perhitungan kadar senyawa β-1,3;1,6-D-glukan dari jamur shiitake pada ulangan pertama, ternyata hasil perhitungan dengan cara manual dan komputerisasi diperoleh kadar yang sama. Namun untuk memperoleh hasil perhitungan yang cepat, maka pada penelitian ini penentuan kadar senyawa
Lampiran 5. Reaksi Selama Analisis Kadar Senyawa β-1,3;1,6-D-glukan dengan Metode Megazyme
Reaksi selama Analisis α-glukan Tahap 1
α-glukan(s) + KOH α-glukan(l)
Tahap 2
α-glukan(l) + H2O amyloglucosidase
Tahap 3
+ O2 + glucose oxidase
+ Tahap 4
+ +
Peroxidase
[image:66.595.112.510.207.684.2]
+ 4
Reaksi selama analisis total glukan Tahap 1
1,3:1,6-β-glukan(s) + 1,3- β-glukan + α-glukan(s) + H2O HCl,30 C, 45 menit
Glukan(l) + H2O
1,3 M HCl, 100 C, 2jam
exo-1,3- β-glucanase + β -glucosidase
laminarisaccharides + H2O
Tahap 2
+ O2 + glucose oxidase
+
Tahap 3
+ +
peroxidase
[image:67.595.115.514.166.712.2]+ 4
Lampiran 6. Data Hasil Pengukuran Kadar Senyawa β-1,3;1,6-D-glukan dengan Metode Congo Red
Nilai Absorban Ekstrak Kering Jamur Shiitake
Sampel Absorban 1 Absorban 2 Rata2 Absorban
Ekstrak kering jamur shiitake
Ekstrak kering (pengenceran 2x)
Blanko
0,572
0,287
0
0,565
0,283
0
0,569
0,285
0
Nilai Absorbansi dari Beragam Konsentrasi β-1,3;1,6-glukan Standar (Barley) [β-glucan] ppm Abs 1
0 0,000 5.000 0,070 15.000 0,158 35.000 0,228 50.000 0,302
Kurva Standar Barley
kurva diatas memiliki persamaan regresi linier Y = 5.10-6 X + 0,0624 dengan R2 = 0,972
Nilai absorbansi dari ekstrak kering jamur shiitake, dimasukkan kedalam persamaan regresi linier dari kurva standar barley sebagai nilai Y
0,285 = 5.10-6 X + 0,0624 0,285 – 0,0624 = 5.10-6 X X = 0,2226 : 5.10-6
X = 0,04452.106 = 44.520 ppm
Karena ekstrak kering jamur shiitake yang diukur merupakan hasil pengenceran 2x, maka konsentrasi sebenarnya dari kandungan senyawa β-1,3;1,6-D-glukan yang diukur adalah 44.520 x 2 = 89.040 ppm.
Untuk menghitung konsentrasi senyawa β-1,3;1,6-D-glukan dalam % maka konsentrasi yang didapat dalam ppm (mg/L) terlebih dahulu dikonversi ke (gr/ml), maka konsentrasinya menjadi 0,089040 gr/ml.
Selanjutnya dihitung dengan rumus:
konsentrasi senyawa β-1,3;1,6-D-glukan x 100% Konsentrasi ekstrak kering jamur shiitae
Konsentrasi ekstrak kering jamur shiitake didapat dengan membagi berat ekstrak glukan yang dianalisis dengan volume pelarut yang digunakan yaitu 0,02 gr : 2ml = 0,01 gr/ml
Maka persen (%) senyawa β-1,3;1,6-D-glukan yang didapat: