PERAKITAN TANAMAN CABAI HAPLOID MELALUI
INDUKSI GINOGENESIS DENGAN MENGGUNAKAN
SERBUK SARI YANG DIRADIASI SINAR GAMMA
OLEH
:MUHAMMAD ALWI
PROGRAM PASCASARJANA
INSTITUT PERTANIAN BOGOR
Terima kasih pula penulis sampaikan kepada seluruh warga kost WSMA
AL-MUQARRABIIN No.71 Ciheuleut Pakuan atas kerjasama dan saling
pengertian serta kekornpakannya selama ini. Khususnya kepada adik Dedi
Lesmana, S.Si dan Ibunda Hj. Fatimah, penulis ucapkan banyak terima kasih atas
segala bantuannya selama penulis berada di Bogor.
Akhirnya penulis menyadari bahwa dalam penyajian hasil penelitian ini
mungkin banyak ditemukan kekurangan-kekurangan, oleh karena itu saran dan
kritikan yang bersifat konstruktif senantiasa penulis harapkan.
Bogor, Juni 2002
SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa tesis yang berjudul:
Perakitan Tanaman Cabai Haploid Melalui Induksi Ginogenesis dengan Menggunakan Serbuk Sari yang Diradiasi dengan Sinar Gamma
adalah benar merupakan hasil karya saya sendiri dan belum pernah dipublikasikan untuk kepentingan lain. Semua sumber data dan informasi yang digunakan telah
dinyatakan secara jelas dan dapat diperiksa kebenarannya.
ABSTRAK
MUHAMMAD ALWI. Perakitan tanaman cabai haploid melalui induksi gino- genesis dengan menggunakan serbuk sari yang diradiasi sinar gamma. Dibimbing
oleh SUHARSONO sebagai ketua d m AGUS PURWITO sebagai anggota.
Penelitian ini bertujuan untuk merakit tanaman cabai haploid melalui
induksi ginogenesis dengan menggunakan serbuk sari yang telah diradiasi sinar
gamma untuk penyerbukan. Selain itu, penelitian ini juga bertujuan untuk
mengetahui pengaruh radiasi terhadap daya kecambah serbuk sari, dan juga
pengaruh radiasi yang diberikan pada serbuk sari yang digunakan untuk
penyerbukan terhadap pembentukan buah.
Untuk mendapatkan tanaman haploid, buah yang terbentuk dari
penyerbukan dengan serbuk sari yang telah diradiasi sinar gamma dijadikan
sebagai eksplan yang dikulturkan pada media MS padat yang mengandung zat
pengatur tumbuh BAP, IAA dan GA3, yang diinkubasikan dalam keadaan terang.
Tunas yang terbentuk, ditanam di media MS-0 padat untuk pemanjangan batang
dan pengakaran tanaman. Pengamatan sitologi dilakukan pada ujung akar untuk
mengevaluasi tingkat ploidi tanaman.
Hasil penelitian menunjukkan bahwa daya kecambah serbuk sari cabai
merah besar varietas LV-2323 lebih tinggi daripada varietas lainnya. Dosis radiasi
sinar gamma mulai dari 10 Gy berpengaruh terhadap daya kecarnbah serbuk sari
cabai besar. Radiasi 10 Gy tidak berpengaruh terhadap persentase buah yang
RIWAYAT
HIDUP
Penulis dilahirkan di Lamunre, Palopo, Sulawesi Selatan pada tanggal
05 Juli 1969 sebagai anak ketiga dari 3 bersaudara dari pasangan Bapak Millang
Dg. Pawero (almarhum) dan Ibunda Atirah.
Penulis menyelesaikan pendidikan dasar di SD Negeri Kampung
Tangnga Belopa pada tahun 1982, pendidikan lanjutan pertama di SMP Negeri
Belopa pada tahun 1985, dan pendidikan lanjutan atas di SMA Negeri 37 1 Belopa
pada tahun 1988. Pada tahun yang sama, penulis melanjutkan pendidikan di
Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
Hasanuddin (UNHAS) Makassar hingga tahun 1995.
Setelah menyelesaikan pendidikan sq-ana, maka pada tahun 1998
penulis bekerja sebagai staf pengajar di Program Studi Biologi, Jumsan MIPA,
Fakultas Keguruan dan Ilmu Pendidikan Universitas Tadulako (UNTAD) Palu
sampai sekarang. Pada tahun yang sama, penulis mendapat beasiswa dari Proyek
DUE-Dikti untuk melanjutkan studi S-2 pada Program Studi Biologi, Sub
2
PERAKITAN TANAMAN CABAI HAPLOID MELALUI
INDUKSI GINOGENESIS DENGAN MENGGUNAKAN
SERBUK SARI YANG DIRADIASI SINAR GAMMA
MUHAMMAD ALWI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar
Magister Sains pada
Program Studi Biologi
PROGRAM
PASCASARJANA
Judul Tesis : Perakitan Tanaman Cabai Haploid Melalui Induksi Ginogenesis dengan Menggunakan Serbuk Sari yang Diradiasi dengan Sinar Gamma
Nama Mahasiswa :
Muhammad Alwi
NRP : 98273
Program Studi : Biologi 1 Botani
Menyetujui,
1. Komisi Pembimbing
(Dr. Ir. Suharsono, DEA)
Ketua
(Dr. Ir. Agus Purwito, MSc.)
Anggota
Mengetahui,
2. Ketua Program Studi Biologi
Dr. Ir. Dedy Duryadi Solihin
DAFTAR IS1
Halaman
.
. .
ABSTRAK...
ill...
RIVJAYAT HIDUP...
... ... ...
v i i ~PRAKATA
...
ix. .
DAFTAR IS1...
xi1DAFTAR TABEL
. . .. . . ... .
.
. .. . . . .. .. .. . .
.
.
.. .
...
..
. .. .. . . .. .. . . . .. . .. . .. . .
.
.. . ... ... . .. . . .. ... . .
....
xivDAFTAR GAMBAR
...
xvDAFTAR LAMPIRAN
. . .. . . .. . .. .. . . ... . . .. . . .. . . .. ...
.
..
. .
.
.
. . .
..
,.
.
.
. .
... . .. . .
...
...
...
.
.
.. . . . .. ..
..
.
.xviPENDAHULUAN
... .. .
..
..
. ... .. .. .
.
. . .
. . .
.
. .
. . .
.
. . . . . .
. .
.
.
.
1 Latar Belakang...
1Tujuan Penelitian
...
3TINJAUAN PUSTAKA
...
4Botani
...
4 Biologi Reproduksi Tanaman...
6 Mikrosporofil (Androesium). . . .
. . . .
.
. . .
.
. . .
. .
. .
.
. . .
6Megasporofil (Ginoesiurn)
...
7Penyerbukan dan Pembuahan
...
9Usaha-Usaha Mendapatkan Tanaman Haploid
...
10Keberhasilan Kultur Ginogenesis In Vitro
...
12BAHAN DAN METODE
...
20 Bahan Tanaman...
20 Radiasi dengan Sinar Gamma...
20 Pengujian Daya Kecambah Serbuk Sari...
20...
Proses Penyerbukan dan Pembuahan 21
Kultur Buah/Biji Muda
...
22...
Analisis Sitologi Tanaman 23
Analisis Data
...
24HASIL DAN PEMBAHASAN
...
26 Pengaruh Radiasi Terhadap Daya Kecarnbah Serbuk Sari...
26...
Pengaruh Radiasi Pada Serbuk.Sari Terhadap Pembentukan Buah 28...
Penyelamatan Embrio Muda 31
Analisis Sitologi Tanaman yang Dihasilkan dari Buah Muda
...
35KESIMPULAN DAN SARAN
...
39...
Kesimpulan 39
Saran ... 40
...
DAFTAR PUSTAKA 41
DAFTAR
TABEL
1 Daya kecambah serbuk sari beberapa cabai besar yang diradiasi sinar gamma
dan tanpa radiasi
...
272 Pengaruh serbuk sari yang diradiasi dan tanpa radiasi terhadap pembentukan
buah dari beberapa varietas cabai besar
...
29 3 Pengaruh radiasi pada serbuk sari yang digunakanuntuk
penyerbukan ter-hadap pembentukan tamman melalui kultur buahhiji mu&
...
32 4 Pengiuuh media tumbuh terhadapjumlah
eksplan yang menghasilkan tanaman.
335 Pengaruh radiasi sinar gamma yang diberikan pada serbuk sari yang
digunakan
untuk
pyerbukan terhadap rataan jumlah daun clan akar dari tanaman yang...
DAFTAR GAMBAR
Halaman
...
1 Tahap pertumbuhan dan perkembangan megaspora pa& tanaman 8 2 Proses pembuahan dan embriogenesis pada tanaman dikotil...
10 3 a.
Bmga cabai besar untuk sumber serbuk sari...
22b
.
Bunga cabai besar yang akan diemaskulasi...
22 4 Perkecambahan serbuk sari cabai besar...
265 Buah cabai merah
besar
dan
cabai kerithg hasit penyerbukan dengan...
serbuk sari yang diradiasi dan tanpa radiasi 30 6 Hasil kultur induksi pertumbuhan embrio muda cabai
besar
varietasLV-2323 dan LV-23 19
...
34DAFTAR
LAMPIRAN
Halaman
1 Komposisi medium Murashige dan Skoog (MS. 1962)
...
462 Hasil perhitungan persentase daya kecambah serbuk sari beberapa varietas
...
cabai besar yang tidak diradiasi clan diradiasi sinar gamma 47
3
.
Hasil perhitungan persentase keberhasilan pembentukan buah beberapavarietas cabai besar yang telah diserbuki serbuk sari tanpa radiasi dan
diradiasi sinar gamma
...
484 a
.
Hasil analisis sidik ragam perkecambahan serbuk sari cabai besar...
49PRAKATA
Syukur Alharndulillah penulis panjatkan ke Khadirat Allah Rabbul
Alamin, karena atas rakhmat dan hidayah-Nya, sehingga penulis dapat me-
rarnpungkan dan menyelesaikan Tesis ini dengan judul: "Perakitan Tanaman
Cabai Haploid Melalui Induksi Ginogenesis dengan Menggunakan Serbuk Sari
yang Diradiasi dengan Sinar Gamma" sebagaimana mestinya.
Pada kesempatan ini penulis ingin menyampailcan penghargaan yang
setinggi-tingginya dan ucapan terima kasih yang sebesar-besarnya kepada Bapak
DR. IR. Suharsono, DEA selaku ketua kornisi pembimbing, dan DR. IR, Agus
Purwito, MSc. sebagai anggota komisi pembirnbing, atas segala upaya dan waktu
yang telah disediakan dengan penuh keikhlasan dan kesabaran dalam memberikan
bimbingan, nasehat dan dorongan, mulai dari tahap awal sampai dengan selesai-
nya penulisan tesis ini. Ucapan terima kasih pula disampaikan kepada Bapak
Ir. Ence Darmo Jaya Supena, M.Si. atas saran dan bimbingan serta banhan
informasi yang sangat bermanfaat dalam pelaksanaan penelitian ini.
Terima kasih juga disampaikan kepada Rektor IPB, Direktur Program
Pascasarjana (PPs) IPB, Ketua Program Studi Biologi PPs-IPB, Rektor
Universitas Tadulako Palu, serta Dekan Fakultas Keguruan dan Ilmu Pendidikan
Untad Palu, atas kesempatan yang diberikan kepada penulis untuk mengikuti
pendidikan pascasarjana di
IPB
Bogor. Kepada Tim Proyek Development ofBioteknologi IPB, penulis mengucapkan terima kasih atas bantuannya dalam
menyediakan biaya pendidikan dan fasilitas penelitian. Dan penelitian ini didanai
oleh Pusat Penelitian Bioteknologi IPB dalam rangka kejasama BIORM
(Biotechnology Research Indonesia The Netherlands).
Secara khusus, penulis sampaikan terima kasih yang tulus ikhlas kepada
istri tercinta Eny Yuniati, S.Si, atas segala bentuk pengorbanan, kesetiaan,
kesabaran, pengertian, dorongan moril dan doa sejak menikah hingga sekarang.
Kepada keempat orang tua penulis: Ibunda Atirah dan Ayahanda Milang
Dg. Pawero (almarhum), serta Ibunda Hj. R. Daryati Djayaningrat dan Ayahanda
Drs. H. T. Miryadi Mertadinata yang tanpa mengenal lelah memanjatkan doa
demi keberhasilan penulis, diucapkan terima kasih dan rasa hormat yang setulus-
tulusnya. Kepada Kakak-Kakakku serta segenap keluarga atas segala bantuannya
baik materi maupun moril, dan khususnya kepada Kakanda Ir. Syamsuddin
Millang, MS. dan Ahmad Pallu sekeluarga yang telah memberikan arahan,
motivasi dan bantuan dana untuk menyelesaikan tugas akhir ini. Semoga Allah
S WT. memberikan balasan yang setimpal, amiien.
Kepada rekan-rekan sekerja di Laboratorium Biologi Molekuler dan
Seluler Tanaman PP-BT IPB: Dra. Muswita, Yanti Puspita Sari, S.Si, Asri Pirade
Pasirang, S.Si, Muzuni,S.Si, M.Si, Ir. Ixora Sartika Mercuriani, Teguh Julianto,
S.Pd, Dra. Lilis Sugiarti, Lili Darlian, S.Si, Ir. Nurhasanah W.S., laboran Bapak
Adi Supardi, Abd. Mulya, dan rekan-rekan sejawat lainnya yang tidak dapat
penulis sebutkan satu per satu penulis mengucapkan salam kompak selalu dan
PENDAHULUAN
Latar Belakang
Cabai besar (Capsicum annuum L.) adalah salah satu jenis sayuran yang
telah membudaya di kalangan petani Indonesia. Tanaman ini menjadi salah satu
komoditas alternatif pada masa-masa mendatang, karena mempunyai nilai
ekonomi yang cukup tinggi. Oleh karena itu, perlu penanganan dan pengelolaan
yang benar dan efektif.
Daerah-daerah yang merupakan sentra penanaman cabai besar
(Capsicum annuum L.) yang tersebar di seluruh Nusantara, tidak mampu me-
menuhi permintaan untuk skala nasional yang bertambah dari tahun ke tahun
(Prajnanta 1999). Hal ini disebabkan karena rendahnya produksi cabai secara
nasional. Luas pertanaman cabai di Indonesia pada tahun 1999 adalah 183.347
ha
dengan rata-rata produksi 1,63 tonha. Rata-rata produktivitas cabai dunia yakni
9,5 tonha (Deptan 2000). Penyebab utama rendahnya produksi cabai di Indonesia
adalah keterbatasan teknologi budidaya yang dimiliki oleh para petani. Kemudian
penyebab yang lain adalah penggunaan benih lokal yang diturunkan terus
menerus. Serangan hama dan penyakit juga menyebabkan rendahnya produksi
cabai di Indonesia.
Salah satu usaha untuk meningkatkan produksi cabai adalah dengan
menggunakan benih unggul. Benih hibrida merupakan benih unggul cabai. Untuk
meqdapatkan benih hibrida diperlukan tanarnan homosigot atau galur murni yang
konvensional untuk mendapatkan tanaman yang homozigot memerlukan banyak
biaya, tenaga dan waktu, sehingga cara ini kurang efisien.
Pembentukan galur homosigot melalui penggandaan jumlah kromosom
pada tanaman haploid adalah suatu metode alternatif. Dengan demikian perakitan
tanaman haploid merupakan salah satu tahapan awal yang digunakan untuk
perakitan benih hibrida. Salah satu cara untuk merakit tanaman haploid adalah
dengan induksi ginogenesis dengan memanfaatkan teknik in vitro (Supena &
Suharsono 1997; Suharsono & Supena 1998).
Menurut Mukhambekzhanov (1997), keberhasilan dalam induksi gino-
genesis melalui kultur in vitro untuk menghasilkan tanaman haploid sangat di-
tentukan oleh beberapa faktor ysiitu: stadium perkembangan ginogenesium,
genotipe tanaman, komposisi media, serta metode dan kondisi kultur. Selain itu
faktor suhu, cahaya, oksigen dan kondisi perturnbuhan tanaman induk, juga
menentukan keberhasilan dalam kultur ginogenesium atau embrio muda
(Pierik 1987).
Penelitian ini merupakan tahapan awal dalam rangka usaha untuk men-
dapatkan tanaman haploid cabai melalui induksi ginogenesis. Ginogenesis dapat
diinduksi dengan menggunakan serbuk sari yang telah diradiasi sinar gamma
untuk penyerbukan.
Induksi ginogenesis dengan serbuk sari yang diradiasi sinar gamma yang
diikuti dengan penyelamatan embrio untuk mendapatkan tanaman haploid sudah
diterapkan pada beberapa tanaman, misalnya pada Triticum aestivum (Bajaj
Petunia (Raquin 1984 dalam Suharsono 1993), tanaman tembakau (Suharsono
1993), Cucumis sativus ( A M & Caglar 1999). Sedangkan tanaman semangka
hanya terbentuk buah yang berbiji kecil (Sugiyama & Morishita 1998). Demikian
pula pada pir Jepang menghasilkan jumlah buah dan biji lebih rendah dari kontrol
(Kotobuki et al. 1998). Selain itu Mukhambetzhanov (1997) melaporkan pula
bahwa tanarnan Beta vulgaris berhasil dikultur menjadi tanarnan haploid melalui
kultur ovarium yang tidak dibuahi. Usaha untuk mendapatkan tanaman cabai
(Capsicum annuum L.) haploid dengan metode ini telah dilakukan, namun belum
mendapatkan tanaman haploid O;ahmi 1996; Suharsono & Supena 1998).
Tujuan Penelitian
Tujuan utarna penelitian ini adalah untuk merakit tanaman cabai haploid
melalui induksi ginogenesis dengan menggunakan serbuk sari yang telah diradiasi
dengan sinar gamma
untuk
penyerbukan. Selain itu, penelitian ini juga bertujuanuntuk mengetahui pengaruh radiasi terhadap daya kecambah serbuk sari, dan juga
pengaruh radiasi yang diberikan pada serbuk sari yang digunakan
untuk
TINJAUAN PUSTAKA
Botani
Tanaman cabai besar (Capsicum annuum L.) menurut sejarah berasal
dari Peru. Pada abad ke-15 baru menyebar ke benua Eropa dan Arnerika. Bangsa
Eropa inilah yang menyebarkan ke daerah-daerah tropis seperti Indonesia
(Rukmana 1996). Tanaman ini mempunyai manfaat yang bermacam-macam,
misalnya digunakan sebagai rempah dan bahan pengobatan. Cabai mengandung
vitamin A dan C yang cukup tinggi.
Cabai besar (Capsicum annuum L) termasuk tanaman semusim yang
berbentuk perdu, mempunyai akar yang menyebar. Penyebaran akamya dangkal
sehingga cabang dan rambut akar banyak terdapat di permukaan tanah, dan
semakin ke dalam akar-aka. tersebut semakin berkurang. Akar horizontal cepat
berkembang di dalam tanah dan menyebar dengan kedalaman 10
-
15 cm(Messiaen 1992). Tanaman ini mempunyai batang tegak, tingginya 50
-
90 cmdari permukaan tanah. Daun berbentuk lonjong dan bagian ujungnya meruncing.
Panjang daun antara 4 - 10 cm, dan lebarnya antara 1,5
-
4 cm.Cabai besar berbunga tunggal, yang keluar dari ketiak-ketiak dam.
Posisi bunga menggantung, dan memiliki 5 - 6 daun mahkota bunga. Panjang
bunga biasanya 1 - 1,s cm, lebar 0,5 cm dan panjang tangkai bunga 1 - 2 cm.
Tangkai putik berwarna putih, panjangnya sekitar 0,5 cm. Sedangkan kepala
panjang sekitar 0,5 cm. Kepala sarinya yang belum matang berwarna biru atau
ungu (Rukmana 1996).
Struktur buah cabai besar terdiri atas kulit, daging buah clan sebuah
plasenta tempat melekatnya biji. Bentuk buahnya memanjang antara 1
-
30 cmdan setelah tua berwarna merah kecoklatan sarnpai merah tua. Biji buah berwarna
kuning kecoklatan (Prajnanta 1999).
Di Indonesia tanaman cabai telah dikenal secara luas di kalangan para
petani. Sentra produsen cabai sekarang ini tidak hanya di pulau Jawa, tetapi juga
di luar pulau Jawa. Berdasarkan data Departemen Pertanian bahwa luas areal
panen cabai pada tahun 1999 di Indonesia mencapai 183.347 hektar dengan
produksi sebesar 298.856 ton. Produktivitas rata-ratanya sebesar 1,63 tonlha
(Deptan 2000). Produksi ini sangat rendah jika dibandingkan dengan rata-rata
produksi dunia 9,5 tonha.
Berdasarkan data Informasi Hortilcultura dan Aneka Tanaman, Deptan
(2000) produsen terbesar cabai adalah daerah Jawa Timur, Jawa Barat, Jawa
Tengah, Sumatera Utara, Nusa Tenggara Barat dan Sulawesi Selatan. Tanarnan
cabai ini mempunyai nilai ekonomi yang tinggi, sehingga berpeluang besar
menjadi salah satu komoditas ekspor yang unggul. Berdasarkan data ekspor
komoditi hortikultura, cabai merah telah berhasil diekspor ke negara Singapura,
Taiwan, Emirat Arab dan Arab Saudi.
Jenis-jenis cabai yang sudah dibudidayakan secara komersial dan
berkembang di Indonesia ada 2 spesies, yaitu cabai besar (Capsicum annuum L.)
cabai merah (varietas longurn), cabai keriting, dan cabai paprika (varietas
grossum). Perbedaan varietas cabai merah besar dengan cabai merah keriting
terletak pada morfologi buahnya. Cabai merah besar ukuran buahnya besar,
panjang, ujungnya runcing, dan rasanya sedikit pedas serta agak manis. Buah pada
saat muda berwarna hijau, dan setelah tua menjadi merah. Sedangkan cabai merah
keriting ukuran buahnya panjang, runcing, kecil dan rasanya lebih pedas dari
cabai merah besar. Disamping itu kulit buah agak tipis serta diameter buahnya
lebih kecil dibanding cabai merah besar (Messiaen 1992; Rukmana 1996).
Biologi Reproduksi Tanaman
Pengetahuan tentang cara perkembangbiakan tanaman sangat penting
bagi pemuliaan tanaman, karena dapat menentukan metode seleksi yang diper-
gunakan untuk memperoleh varietas unggul yang diharapkan. Cara perkembang-
biakan tanaman secara seksual menggunakan 2 bagian organ reproduktif, yaitu
mikrosporofil (androesium) dan megasporofil (ginoesium) (Kaufinan 1989;
Sedgley & Griffin 1989).
Mikrosporofil (Androesium)
Menurut Crepet (1983); Sedgley & Griffin (1989) androesium adalah
keseluruhan benang sari (stamen) yang terdiri atas kepala sari (anter) dan tangkai
sari (filamen). Kepala sari yang matang mempunyai 2 kantung (lokus). Di dalam
Proses ringkas terbentuknya inti sperma berawal dari sebuah sel induk
serbuk sari (mikrospora) dalam kepala sari (anter) yang mengalami dua kali
meiosis. Meiosis pertama menghasilkan sepasang sel haploid. Meiosis kedua
menghasilkan 4 mikrospora haploid. Tiap mikrospora tersebut mengalami karyo-
kinesis, sehingga memiliki 2 inti haploid. Inti tersebut adalah inti generatif dan
inti saluran serbuk sari. Setelah terbentuk serbuk sari, inti generatif membelah
membentuk 2 inti sperma (Kaufinanl989; Sedgley & Griffi 1989). Sebutir
serbuk sari yang telah matang mengandung 3 inti haploid, yaitu sebuah inti salur-
an serbuk sari (inti vegetatif) dan dua buah inti sperma (inti generatif) (Satifah &
Darjanto 1990; Suradinata 1998).
Megasporofil (Ginoesium)
r
Menurut Suradinata (1998) karpel yang secara keseluruhan disebut alat
kelamin betina (ginoesium) adalah megasporofil yang melipat memanjang, yang
menutup satu atau lebih bakal biji.
Megasporogenesis adalah proses pembentukan megaspora di dalam
ovarium (Satifah & Darjanto, 1990). Proses awal terbentuknya inti sel telur adalah
dimulai dari sebuah sel megaspora dalam ovulurn. Kemudian sel megaspora
mengalami proses meiosis dua kali, sehingga menghasilkan 4 megaspora haploid.
Tiga diantaranya mengalami degenerasi dan mati, sedangkan yang satu meng-
alami pembelahan secara mitosis 3 kali berturut-turut tanpa diikuti pembelahan
plasma. Hasilnya sebuah sel besar yang mengandung 8 inti haploid yang disebut
menempatkan diri di dekat
mikrofil,
tetapi dua diantaranya mengalami degenerasi (sinergid). Inti yang ketigaini
berkembang menjadisel
telur yang nantinyaakan
dibuahi oleh inti sperma. Tiga buah
inti
lainnya bergerakke
arah
yang berlawanan lalu mengalami degenerasi pula (antipoda). Kemudian2
inti yang tersisa bersatu di tengah kantung ernbriodm
membentuk sebuah inti diploid yang nantinya akm dibuahi f nti s p m a membentuk endosperma (Kaufman 1 989; Satifah & Darjanto1 990; Suradinata I 998). Untuk lebih jelasnya tahapan pertumbuhan dm perkem-
bangan megaspom &pat dilihat pada Gambar 1.
Kandung E d l l o
Garnbar 1. Tahap perhmbuhan dm perkembangan megaspom pada tanaman
Penyerbukan dan Pembuahan
Serbuk sari yang telah matang akan melekat di kepala putik oleh ber-
bagai vektor. Kepala putik yang reseptif akan mengeluarkan lendir. Lendir ini
mengandung larutan gula dan zat-zat lain yang dibutuhkan untuk perkecambahan
serbuk sari. Serbuk sari yang telah melekat di kepala putik akan menyerap lendir
tadi, lalu akan menggembung dan berkecambah. Kemudian membentuk tabung
serbuk sari yang memanjang dan masuk ke dalam tangkai putik. Tabung serbuk
sari melekat pada ovulum dan masuk ke dalarn kantung embrio lewat mikrofil
(Satifah & Darjanto 1990; Suradinata 1998).
Di dalam tabung serbuk sari terdapat tiga inti haploid, yaitu inti saluran
serbuk sari terdapat di depan sedang kedua inti spenna mengikuti dibelakangnya.
Kedua inti spenna masuk ke kantung embrio. Salah satu inti spenna bersatu
dengan inti sel telur dan membentuk zigot diploid, yang kemudian &an ber-
kembang menjadi embrio. Inti spenna lainnya bersatu dengan inti diploid yang
merupakan hasil penyatuan dari dua inti kutublinti polar yang menghasilkan inti
triploid (3n). Setelah mengalami pembelahan berkali-kali, inti triploid ini akan
membentuk jaringan besar yang berisi zat makanan untuk pertumbuhan embrio,
yang biasa disebut endosperma atau putih lembaga (Crepet 1983; Kaufinan 1989;
Satifah & Darjanto 1990). Pembuahan akan berjalan normal, bila serbuk sari dan
inti sel telur dalam keadaan sehat dan subur (fertil). Oleh karena itu serbuk sari
harus mempunyai daya turnbuh yang tinggi, sedang kepala putik hams merupakan
medium yang baik untuk perkecambahan dan pertumbuhan serbuk sari. Untuk
Garnbar 2. Proses pembuahan dm embriogenesis pada tamman
dik~til
(dari Kaufman, 1989).
Usaha-Usaha Mendolpatkan Twnaman Haploid
Tanaman haploid adalah tanaman yang mempunyai jumlah kromosum yang sama dengan jumlah kromosom pada garnetnya (Wanimena 1992).
Tanaman
haploid dapat terjadi, namun fiekuensinya sangat kecil sekali. Pierik (1987)
menyebutkan cara-cara mendapatkan tanaman haploid baik secara in vivo maupun
secara in vitro.
Secara in vivo, tanaman haploid diperoleh dengan cara-cara: (1) Gino-
genesis yaitu perkembangan sel telur yang tidak dibuahi sebagai hasil persilangan
antar jenis. (2) Androgenesis, perkembangan sel telur yang mengalami eliminasi,
intinya diganti oleh inti gamet jantan. (3) Eliminasi genom, perkembangan zigot
yang mengalami eliminasi salah satu genomnya sebagai hasil persilangan antar
jenis atau antar marga. (4) Semigami, inti sel telur dan inti sel generatif serbuk
sari berkembang dan menghasilkan khimera haploid. (5) Perlakuan kimiawi
untuk
mengeliminasi kromosom. (6) Pemberian kejutan dengan suhu tinggi atau rendah,
dan (7) Radiasi dengan sinar X atau sinar
UV.
Tanaman haploid yang dihasilkan dengan cara in vitro dapat diperoleh
melalui: (1) Kultur kepala sari, yaitu kepala sari yang telah diisolasi dari tanaman
induk ditumbuhkan dalam medium buatan secara aseptik. (2) Kultur serbuk sari,
yaitu serbuk sari dalam tingkat perkembangan tertentu diisolasi dari kepala sari,
kemudian ditumbuhkan dalam medium sintetis. (3) Kultur perbungaan, seluruh
perbungaan ditumbuhkan dalam medium buatan secara aseptik. (4) Kultur embrio
yaitu penyelamatan embrio dari hasil persilangan antar jenis atau antar marga.
Embrio ditumbuhkan secara aseptik dalam medium buatan. (5) Fertilisasi semu
ailtar marga yang kemudian ditanam dalam kultur buatan secara aseptik.
(6) Penumbuhan ovul yang tidak dibuahi dalam kultur buatan secara aseptik, dan
Menurut Foroughi & Wenzel(1994), tanaman haploid diperoleh melalui
dua cara: spontan dan secara induksi. Cara induksi diterapkan pada proses andro-
genesis dan partenogenesis. Pada androgenesis tanaman haploid dapat diperoleh
melalui kultur anter, kultur floret, dan kultur mikrospora. Sedangkan pada
partenogenesis tanaman haploid dapat dihasilkan melalui pseudogami, meng-
gunakan gen-gen khusus, persilangan dengan tingkat ploidi yang berbeda, kultur
ovul, dan penyelamatan embrio setelah kromosomnya tereliminasi.
Tanaman haploid yang berasal dari gametofit betina berupa kantung
embrio dan sel telur disebut partenogenesis. Untuk menghasilkan tanaman
haploid, maka metode ini menerapkan pemisahan sel telur yang belum dibuahi,
lalu diregenerasikan secara in vitro (Foroughi & Wenzel, 1994).
Proses partenogenesis sama dengan proses ginogenesis, yaitu per-
kembangan dari bunga betina dengan diinduksi serbuk sari yang belum masak,
atau serbuk sari yang diradiasi, dan juga dari serbuk sari kerabat jauh (Pierik
1987; Yang & Zhao 1990; Foroughi & Wenzel 1994). Proses ini telah dilakukan
oleh Cuny et al. (1993) pada tanaman Cucumis melo L) yang dikombinasikan
dengan cara in vitro.
Keberhasilan Ginogenesis
In
Vitro
Keberhasilan dalam induksi ginogenesis in vitro untuk menghasilkan
tanaman haploid sangat ditentukan oleh beberapa faktor. Menurut Yang & Zhou
(1990); Mukhambekzhanov (1997) faktor tersebut terutama adalah umur gino-
kultur. Sedangkan menurut Pierik (1987), selain faktor-faktor tersebut keber-
hasilan induksi genogenesis in vitro ditentukan pula oleh suhu, cahaya, oksigen,
dan kondisi pertumbuhan tanaman induk.
Medium kultur untuk induksi ginogenesis adalah medium yang lengkap
dan spesifik dibanding dengan kultur organ yang lain. Kultur embrio muda mem-
butuhkan medium lebih lengkap dan spesifik daripada embrio dewasa (Yang & ,
Zhou 1990). Biasanya zat pengatur tumbuh BAP dan
IAA
ditambahkan ke dalammedium untuk merangsang proses diferensiasi atau dediferensiasi. Jenis dan
konsentrasinya akan mempengaruhi arah pertumbuhan eksplan.
Auksin adalah zat pengatur turnbuh yang berperan dalam pembesaran sel
dan diferensiasi akar @odds & Robert 1995). Auksin berpengaruh pula terhadap
pembentukan kalus, senyawa etilen, buah partenokarpi, dominasi apikal dan
respirasi (Wattimena 1988). Salah satu jenis auksin yang digunakan untuk meng-
induksi eksplan menjadi tanaman adalah indoleacetic acid (IAA). Pada
konsentrasi optimum 0.1 mgll IAA dapat merangsang pembentukan tanaman pada
kultur anter Nicotiana tabacum (Nitsch & Nitsch 1969).
Pada kultur in vitro sitokinin berpengaruh terhadap pembelahan sel
(Wattimena 1988). Benzylamino purine (BAP) merupakan sitokinin yang banyak
digunakan dalam kultur in vitro. Seperti yang dilaporkan oleh Sukamto (1998),
penambahan BAP pada medium MS dapat meningkatkan fi-ekuensi terbentuknya
embrio somatik belimbing. BAP adalah zat pengatur turnbuh yang berfbngsi
untuk merangsang terbentuknya tunas-tunas. Kombinasi BAP dan
IAA
padapengakaran dan pemanjangan tunas (Christopher & Rajam 1996). Sedangkan bila
menggunakan kombinasi BAP dan IAA yang hampir seimbang, maka yang ter-
induksi adalah kalus. Seperti hasil penelitian Kesaulya (1996), penggunaan BAP
1,35 mg/l dan IAA 1,05 mg/l hanya mampu menginduksi pembentukan kalus dari
jaringan somatik serbuk sari kentang kultivar ASX 5.
Pernberian Gibberellic acid (GA3) pada tanarnan menyebabkan per-
tambahan panjang batang, menambah luas dam, dan menambah besar bunga serta
daun (Wattimena 1988). GA3 pada konsentrasi 1 mg/l medium tidak mening-
katkan pembentukan embrio, tetapi memacu pembentukan tunas pada kultur anter
Nicotiana spp. (Nitsch & Nitsch 1969). Pada konsentrasi 1 mgfl medium, GA3
menyebabkan pemanjangan hipokotil dan menghasilkan tanaman yang kurus serta
klorosis.
Sukrosa merupakan sumber karbon yang paling baik dan biasa dipakai
dalam kultur embrio, tetapi glukosa dan fruktosa terkadang juga dapat dipakai
(Yang & Zhou 1990; Dodds & Roberts 1995). Selain sebagai sumber karbon,
sukrosa berfiingsi pula sebagai pengatur tekanan osmotik yang sangat penting
bagi embrio muda. Embrio dewasa biasanya tumbuh baik dalam kadar gula 2-3%,
sedangkan embrio muda pada kadar 8
-
12% (Pierik 1987). Peningkatankonsentrasi gula dalam media kultur ternyata menghambat pembesaran sel
somatik dan pembentukan kalus, namun dapat merangsang pembelahan sel dari
serbuk sari. Frekuensi pembentukan embrioid tertinggi didapatkan pada perlakuan
dengan kandungan gula sebanyak 10% dan terendah pada kadar 2% pada media
(1 98 1) dalam Gandawidjaja (1 997), menyatakan bahwa pembentukan tanaman
dihaploid pada kultur anter Ulmus americana makin meningkat dengan adanya
interaksi antara kandungan gula dengan zat pengatur tumbuh dalam media kultur.
Untuk mencapai keberhasilan pada kultur ginogenesis, khususnya kultur
embrio atau biji muda maka vitamin, ekstrak malt, air kelapa dan kasein hidrolisat
sering pula ditambahkan pada medium kultur. Ekstrak tersebut mengandung
beberapa asam amino yang merupakan sumber nitrogen yang sangat dibutuhkan
dalam pertumbuhan dan perkembangan embrio selanjutnya (Yang & Zhou 1990;
Dodds & Roberts 1995).
Selain itu stadium perkembangan ginoesium (ovarium dan ovul) sangat
penting untuk keberhasilan induksi tanaman haploid. Pada penelitian Castillio dan
Cistue (1993), bahwa penginduksian ovarium Hordeum vulgare untuk mem-
bentuk tanaman haploid terjadi pada kantung embrio stadium trinucleate,
sedangkan pada tanaman barley kantung embrionya berada pada stadium
uninuclear (berinti satu).
Metode dan kondisi kultur sangat mempengaruhi keberhasilan induksi
ginogenesis dalam membentuk tanaman haploid. Seperti yang dikatakan
Mukharnbetzhanov (1997), pengisolasian ovarium dan ovul biasanya ditumbuh-
kan pada kondisi suhu 22 - 26 "C, namun kadang-kadang juga dapat diturnbuhkan
pada suhu rendah yaitu 20 - 21 OC. Beberapa hasil penelitian telah dilaporkan
bahwa umur tanaman untuk sumber eksplan, dan kondisi kultur sangat
berpengaruh terhadap respons morfogenetik didalam memacu pertumbuhan kultur
Menurut Mukhambetzhanov (1 997) bahwa untuk menginduksi tanaman
menjadi haploid sangat bergantung pada genotipe tanaman. Dilaporkan bahwa
frekuensi untuk mendapatkan tanaman haploid terhadap perbedaan genotipe
tanaman hanya 0,2 sampai dengan 1 ,I%.
Interaksi antara umur biji muda dengan media dan kombinasi zat peng-
atur tumbuh dapat mempercepat proses perkecambahan biji muda cabai. Seperti
yang dilaporkan Supena dan Suharsono (1997) media MS dengan kombinasi ZPT
0,l mgll
BA
+
0,5 mgll GA3 dan 0,l mg/l BA+
0,s mg/l IAA+
0,s mg/l GA3mempercepat perkecambahan serta menginduksi perakaran pada biji muda cabai.
Mukhambetzhanov (1 997) melaporkan pula bahwa ada beberapa tanarn-
an yang telah berhasil diinduksi menjadi tanaman haploid melalui kultw ovarium
yang tidak dibuahi yaitu Nicotiana tabacum, Triticum aestivum dan Beta vulgaris
Efek Radiasi Sinar Gamma
Menurut Djojosoebagio (1988) bahwa sinar gamma termasuk dalam
kelompok radiasi elektromagnetik. Terjadinya kerusakan-kerusakan akibat radiasi
bergantung kepada besarnya energi yang diserap oleh organisme. Satuan dosis
radiasi dinyatakan sebagai banyaknya energi yang diserap oleh satu kesatuan
benda disebut rad (radiation absorbes dose). Satu rad saka dengan penyerapan
dosis radiasi sebanyak 100 erg oleh bahan yang diradiasi (Bosemark et at. 1994;
van Harten 1998).
Salah satu efek yang ditimbulkan oleh radiasi pada organisme adalah
struktur
DNA
(Bosemark et al. 1994). Mutasi gen terjadi karena perubahan padastruktur primer dari
DNA.
Mutasi gen dapat terjadi karena substitusi, tambahanataupun hilangnya satu atau lebih basa-basa di dalam sebuah molekul
DNA
(Bosemark et 01. 1994; van Harten 1998). Substitusi dapat timbul karena
pasangan yang keliru pada susunan basa pada saat terjadinya proses replikasi.
Kekeliruan di dalam pasangan dapat ditimbulkan karena terjadinya ionisasi pada
basa-basa dan karena pergeseran secara tautomeris di dalam posisi atom-atomnya.
Sedangkan penambahan atau kehilangan satu atau beberapa nukleotida akan
menyebabkan mutasi ubah kerangka. Mutasi kromosom dapat disebabkan karena
kerusakan benang gelendong atau tefhambatnya pembentukan bakal dinding sel,
sehingga pembagian sel tidak dapat terbentuk setelah proses mitosis tejadi
(Bosemark et al. 1994).
DNA
sangat sensitif terhadap radiasi, sehingga radiasi sinar gammadapat menyebabkan perubahan
DNA
makhluk hidup (van Harten 1998).DNA
memiliki peranan yang sangat penting di dalam sel, maka perubahan molekul ini
akan menimbulkan efek atau gangguan dalam aktivitas sel. Serbuk sari cabai yang
telah diradiasi yang digunakan untuk penyerbukan menyebabkan terbentuknya
buah dan biji cabai yang berukuran kecil dibanding dengan hasil penyerbukan
dengan serbuk sari yang tidak diradiasi (Fahrni 1996).
Berbagai penelitian tentang pengaruh radiasi sinar gamma terhadap per-
tumbuhan dan perkembangan tanaman telah dilikukan. Raquin (1984) dalam
Suharsono (1993) menggunakan serbuk sari Petunia yang telah diradiasi untuk
Suharsono (1993) yang meradiasi serbuk sari tanaman Nicotiana tabacum untuk
menghasilkan tanaman haploid dengan menggunakan dosis 600, 1000, 2000 Gy.
Daya kecambah serbuk sari tembakau yang telah diradiasi 2000 Gy masih men-
capai 65%, dan tidak berbeda nyata dengan yang tidak diradiasi.
Abak & Caglar (1999), telah meradiasi serbuk sari ketimum (Cucumis
sativus L.) untuk mendapatkan tanarnan haploid. Penggunaan dosis 300 Gy pada
serbuk sari yang digunakan untuk penyerbukan, hanya menghasilkan 25
-
35%tanaman haploid. Demikian pula Faris et al. (1999) yang meradiasi serbuk sari
ketimun untuk pembentukan embrio haploid. Pada Cucumis melo, Cuny et al.
(1993) mendapatkan buah dan biji yang dihasilkan dari penyerbukan dengan
menggunakan serbuk sari yang diradiasi dengan dosis 0,15 dan 1,6 kGy tidak
berbeda nyata dengan yang dihasilkan dengan serbuk sari normal. Namun pada
dosis 2,s kGy hanya menginduksi embrio sekitar 3,4%. Dari pembentukan embrio
ini dapat menghasilkan 70% tanarnan haploid.
Radiasi sinar gamma sering dipakai pula dalam usaha pernuliaan
tanaman (Wattimena 1992; Zottini et al. 1997). Pada tanaman semangka, dosis
800 Gy yang diberikan pada serbuk sari yang digunakan
untuk
penyerbukan dapatmenyebabkan buah yang terbentuk berbiji kecil dan jumlahnya sedikit dibanding
dengan yang yang tidak diradiasi (Sugiyama & Morishita 1998). Demikian pula
pada pir Jepang kultivar Hosui buah yang terbentuk dari hasil penyerbukan
dengan serbuk sari yang telah diradiasi 20 Gy menghasilkan buah dan biji lebih
sedikit dibanding dengan yang tidak diradiasi (Kotobuki et al. 1998). Organ
BAHAN
DAN
METODE
Bahan Tanaman
Bahan tanaman yang digunakan adalah tanaman cabai besar varietas
LV-2319, LV-2323, CK-C dan CK-L. Tanaman ini ditanam di pot dan diletakkan
di rumah kaca Pusat Penelitian Bioteknologi IPB Bogor sampai membentuk
bunga dan buah. Bunga yang digunakan sebagai sumber serbuk sari untuk uji
perkecambahan dan penyerbukan berasal dari tanaman yang berumw 45 hari
setelah tanarn (hst).
Radiasi dengan Sinar Gamma
Radiasi sinar gamma berasal dari atom 1 3 7 ~ s yang dilakukan dengan alat
radiasi IBL 437-C. Radiasi dilakukan di Pusat Studi Ilmu Hayati IPB Bogor.
Debit radiasi pada saat penelitian adalah 2,72 Gylmenit (Maret
-
April 2001).Bunga yang &an diradiasi (Garnbar 3a.) dimasukkan ke dalam cawan petri,
kemudian cawan petri dimasukkan ke dalam tabung radiasi. Dosis radiasi yang
diberikan adalah 10 dan 25 Gy.
Pengujian Daya Kecambah Serbuk Sari
Pengujian daya kecambah serbuk sari dilakukan dengan menwnbuhkan
serbuk sari di dalam medium tumbuh yang mengandung sukrosa 50 g/l ditambah
(Suharsono 1993) di dalam botol kultur. Daya hidup serta banyaknya serbuk sari
yang berkecambah diketahui dengan pewarnaan IKI. Larutan IKI mengandungr
0,6 g iodine
+
0,7 g KI yang dilarutkan dalam 50 ml akuades steril. Pewarnaan inidiberikan setelah perhitungan jumlah serbuk sari.
Percobaan ini menggunakan rancangan acak kelompok (RAK) sub
sampling dengan dua faktor yaitu dosis radiasi dan varietas cabai. Dalam
penelitian ini 3 dosis radiasi digunakan yaitu 0 (tanpa radiasi), 10 dan 25 Gy, dan
4 varietas cabai yaitu LV-2319, LV-2323, CK-C, dan CK-L. Satu satuan perwba-
an terdiri dari 3 botol kultur yang masing-masing berisi 10 anter. Setiap perlakuan
dilakukan 3 kali, sehingga secara keseluruhan terdapat 108 botol pengamatan.
Jumlah rata-rata serbuk sari yang diamati tiap botol kultur adalah 90,21 butir.
Pengamatan dan perhitungannya menggunakan hemasitometer dan rnikroskop.
Peubah yang diamati adalah banyaknya serbuk sari yang berkecambah.
Proses Penyerbukan dan Pembuahan
Bunga diemaskulasi dengan membuang semua benang sari dan mahkota
bunganya, kemudian ditutup dengan kertas transparan. Bunga yang diemaskulasi
adalah bunga yang diperkirakan akan mekar satu hari kemudian (Gambar 3b).
Penyerbukan dilakukan dengan melekatkan serbuk sari yang telah diradiasi pada
kepala putik pada varietas yang sama, lalu ditutup kembali untuk menghindari
kontaminasi dari serbuk sari lain.
Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap
3 dosis radiasi
yang
digmakm
yolitu 0 (tanpa rdasi), 10 dm 25Gy,
d m
4 varietas cabai yaitu LV-23 1 9,LV-2323,
CK-C,dm
CK-L. Satu satuan percob- terdiri dari 15 pmyerbukan yang terdapat pada satu pohon.Percobam
dhkukan dewan tigakali
uIangan, sehingga terdapat 36 pohon. Peubahyang
a i dadalah
p-tase banyahya busth yang terbentuk. [image:104.563.8.549.23.607.2]a
b
Gambar
3. ,a. Bunga cabai besaruntuk
sumberd u k
sarib.
Bunga ymgakan
diemaskuhi.
Kaltur
Buah/Biji Muda
Buah dipetik pada umur 3 , 5 , 7 , 9 dan 1 1 hari setelah penyerbukan (hsp).
Buah
tersebut d i b e r s h dengan akuades, lalu direndamdalam
larutan klowks15% selama 5 menit,
dan dibilas
3 kali dengan akuades steril. Pengerjaan inidilakukan di
dalam
laminar air flow untuk rnenmdari konaminasi.Buah
dibelah secrura membujur menjadi dua, lalu d i m pada media turnbuh se-
(Lampiran 1) yang diperkaya dengan kasein hidrolisat (100 mg/l), dan asam
askorbat (20 mg/l). Untuk mencegah terjadinya kontaminasi oleh bakteri yang
terkandung dalam biji, maka ditambahkan kanamycin dalam media kultur dengan
konsentrasi 20 mg/l.
Perlakuan kombinasi zat pengatur tumbuh BAP, IAA dan GA3 yang
diberikan (dalam mg/l) ke dalam media adalah:
a. BAP 0,l + IAA 0,4
+
GA3 0,5b. BAP 0,2 +
IAA
0,3+
GA3 0,sC. BAP 0,3 +
IAA
0,2+
GA3 0,sd. BAP 0,4
+
IAA
0,l+
GA3 0,5.Kultur selanjutnya diinkubasi pada ruang kultur yang bersuhu sekitar 25 OC
dengan penyinaran 16 jam tiap hari pada intensitas cahaya antara 1000 sampai
2000 lux.
Pengamatan yang dilakukan adalah persentase eksplan yang ber-
kecarnbah, dan waktu yang dibutuhkan untuk berkecambah serta menilai per-
tumbuhan dan perkembangan tanaman yang dihasilkan.
Analisis Sitologi Tanaman
Untuk mengidentifikasi tingkat ploidi pada tanaman yang terbentuk,
ujung akar tanaman dari botol kultur dipotong 3-5 mrn. Ujung akar direndam
dalam larutan 8-Hydroxyquinolin 0,002 M selama 90 menit dalam lemari
pendingin @4 OC) sebagai pra-perlakuan. Setelah itu ujung
akar
dibilas denganKemudian dilakukan maserasi yaitu dimasukkan dalam campuran larutan HCl 1N
dengan asam asetat 45% dengan perbandingan (3:l) selama 2 menit pada suhu
60 OC. Ujung akar segera dibilas dengan akuades steril, lalu diwarnai dengan
menggunakan aceto orcein 2%. Ujung akar kemudian diletakkan diatas gelas
preparat, lalu ditutup dengan gelas penutup. Gelas penutup ditekan dengan ujung
jari agar rapat, lalu diketuk dengan ujung pensil yang berkaret (Darnaedi 1991).
Pengamatan dilakukan di bawah mikroskop untuk mengamati kromosom.
Analisis Data
Hasil pengamatan dalam penelitian daya kecambah serbuk sari dianalisis
dengan mengikuti model linear berikut:
Yijk =
p
+ y i+
a j+
pk+
(ap)jk+
EijkYijk = hasil pengamatan
P = nilai tengah umum
Yi = pengaruh kelompok
a j = faktor dosis radiasi (0, 10,25 Gy)
pk = faktor varietas (LV-23 19, LV-2323, CK-C, CK-L)
(ap)jk = pengaruh interaksi antara dua faktor
Sedangkan pengaruh serbuk sari yang telah diradiasi terhadap pembentukan buah
cabai dianalisis dengan mengikuti model linear RAL faktorial sebagai berikut:
Yijk =
p
+
a i+
pj+
(ap)ij+
EijkYijk = hasil pengamatan
p
= nilai tengah urnuma i = faktor dosis radiasi (0, 10,25 Gy)
pj = faktor varietas (LV-23 19, LV-2323, CK-C, CK-L)
(ap)ij = pengaruh interaksi antara dua faktor
Eijk = galat ke-ijk
Analisis ragam (analysis of variance) menggunakan perangkat lunak
komputer Minitab for Windows Release 11.12. Perbedaan nilai tengah dianalisis
HASIL DAN
PEMBAHASAN
Pengaruh
Radiasi Terhadap
Daya Kecrmmbah Serbuk Sari
Viabilitas serbuk sari dapat ditentukan berdasarkan daya kecambahnya. Berkecambahnya suatu serbuk sari ditandai dengan terbentuknya tabung serbuk sari. Selain daya kecambah, viabilitas serbuk sari juga dapat ditentulran melalui pewanman dengan IKI (Yodium Kalim Yodida). Serbuk sari yang bemama gelap kebhaa mmunjukkan serbuk sari yang
viabel,
sBdangkm yang berwamaterang merupakau serbuk sari yang
tidak viabel.
Serbuk sari yang berwarna gelapkebiruan berukmn relrttif
besard m
bentulrnyabulat,
sedangkan
yang bewarna temg berukuran kecil dan keriput. Sebagian besar serbuksari
yang b e r w kgelap kebiruan berkecambah dalam waktu 3
jam
di
dalam medium perkecambah-an,
sedangkan yang berwarna terang tidak ada yang berkecanibah (Gambar 4).Garnbar 4.
Perkecambahan
sexbuk saricabai
besarA = Serbuk sari yang
tidak viabel (tidak
berkecambah)Tabel 1. Daya kecambah serbuk sari yang diradiasi dan tanpa radiasi dari
beberapa varietas cabai besar
Keterangan: Muruf yang sarna pada baris atau kolom yang sama b e d tidak berbeda.
Tanda (- dan +) yang sama pada baris atau kolom yang sama b d tidak berbeda.
Dosis radiasi (GY)
0
10
2 5 Rata-rata
Daya kecambah serbuk sari cabai besar disajikan pada Tabel 1 dan
Lampiran 2. Dosis radiasi mulai 10 Gy berpengaruh terhadap daya kecambah
serbuk sari (Tabel 1 dan Lampiran 4a). Hasil ini bertentangan dengan Suharsono
(1993) yang menggunakan dosis 600 sampai dengan 2000 Gy pada tanarnan
tembakau. Daya kecambah serbuk sari yang tidak diradiasi adalah 48,11%,
sedangkan yang diradiasi 10 Gy dan 25 Gy bertunrt-turut adalah 39,64% dan
37,29%.
Bagian terbesar dari serbuk sari adalah inti. Di dalam inti mengandung
material genetik yang berupa DNA. Radiasi
pads
intensitas tertentu dapatmenyebabkan kerusakan DNA yang akan berpengaruh terhadap ekspresi gen.
Perkecambahan serbuk sari memerlukan ekspresi gen, sehingga radiasi pada
intensitas tertentu dapat mempengaruhi perkecambahannya.
Daya kecambah serbuk sari (%)
Rata-rata
48,ll
-
39,64
+
37,29
+
LV-23 19
39,28 b
37,76 b
35,26 b
37,43
+
CK-C
45,60 b
39,53 b
35,78 b
40,30
+-
LV-232358,86 a
42,53 b
38,57 b
46,65
-
CK-L
48,72 ab
38,78 b
39,55 b
[image:109.553.80.492.110.488.2]Walaupun telah terjadi perubahan struktur DNA kromosom pada serbuk
sari yang diradiasi, tetapi kerusakan atau perubahan ini belum mampu meng-
hentikan perkecambahan serbuk sari. Hal ini kemungkinan karena serbuk sari
yang matang telah mempunyai semua kebutuhan untuk perkecambahan pada saat
diradiasi. Hasil penelitian Zottini et al. (1997) menunjukkan bahwa pemberian
radiasi dengan dosis 200, 600 dan 1000 Gy tidak berpengaruh terhadap viabilitas
serbuk sari Cannabis saliva L.
Daya kecambah serbuk sari antar varietas berbeda. Varietas LV-2323
menghasilkan serbuk sari dengan daya kecambah paling tinggi (Tabel 1 dan
Lampiran 4a). Hal ini kemungkinan karena keadaan fisik serbuk sari varietas
LV-2323 lebih baik dibandingkan dengan varietas lainnya.
Pengaruh Radiasi Pada Serbuk Sari Terhadap Pembentukan Buah
Dosis radiasi yang diberikan pada serbuk sari varietas cabai merah besar
(LV-2319 dan LV-2323) maupun pada cabai keriting (CK-C clan CK-L) ber-
pengaruh terhadap keberhasilan pembentukan buah @it set). Serbuk sari yang
tidak diradiasi (normal) yang digunakan untuk penyerbukan memberikan ke-
berhasilan pembentukan buah yang berkisar 93
-
100%. Pemberian radiasi 10 Gytidak berpengaruh nyata terhadap persentase jumlah buah yang terbentuk,
walaupun jumlah buah yang terbentuk mencapai 91,83%. Radiasi 25 Gy pada
serbuk sari menyebabkan p e n m a n secara nyata terhadap persentase jwnlah
buah yang terbentuk menjadi 89,90% (Tabel 2 dan Lampiran 4b). Hal ini sesuai
berpengaruh terhadap persentase pembentukan buah cabai. Sedangkan pada dosis
25 Gy nyata menurunkan persentase pembentukan buah cabai. Pada tembakau,
perlakuan radiasi sampai dengan 2000 Gy tidak berpengaruh terhadap buah yang
terbentuk (Suharsono 1993). Demikian juga pada Cucumis sativus L., bahwa
pemberian dosis radiasi 300 hingga 600 Gy pada serbuk sari tidak memberi
pengaruh nyata terhadap pembentukan buah dibandingkan tanpa perlakuan radiasi
(Abak & Caglar 1999).
Pembentukan buah dari penyerbukan serbuk sari yang tidak diradiasi
dari 4 varietas cabai adalah sama. Varietas LV-2323 mempunyai kemampuan
membentuk buah yang paling tinggi, baik pada tanaman yang serbuk sarinya
diradiasi maupun yang tidak diradiaii (Tabel 2).
Tabel 2. Pengaruh serbuk sari yang diradiasi dan tanpa radiasi terhadap pem- bentukan buah pada beberapa varietas cabai besar
Keterangan: Huruf yang sama pada baris atau kolom yang sama berarti tidak berbeda.
Tanda (- dan +) yang sama pada baris atau kolom yang sama berarti tidak berbeda. Dosis radiasi (GY) 0 10 25 Rata-rata
Keberhasilan pembentukan buah cabai, selain disebabkan oleh pengaruh
dosis radiasi yang diberikan, juga oleh faktor fisiologis tanaman. Tanaman yang
Pembentukan buah (%)
LV-23 19
93,OO ab
86,OO bc
86,33 bc
88,44
-+
LV-2323
100,OO a
100,OO a
96,67 ab
98,90
+
CK-C
96,67 ab
98,33 a
96,59 ab
97,20
+
CK-L
96,67 ab
83,OO bc
80,OO c
86,56
-
Rata-rata
96,60
-
91,83
-+
Buah yang terbentuk dari penyerbukan oleh serbuk sari yang diradiasi
berbeda dengan penyerbukan oleh serbuk sari yang tidak diradiasi (kontrol). Pada
umur 3 hari setelah penyerbukan (hsp) W a n buah yang terbentuk tidak berbeda
antara kontrol dengan yang diradiasi, yaitu panjangnya berkisar 2-5
mm.
Namunmulai hari ke-5 setelah penyerbukan, nampak jelas pengaruh radiasi pada serbuk
sari terhadap ukuran buah yang terbentuk, khususnya panjang buah (Gambar 5).
Penyelamatan Embrio Muda
Penyelamatan embrio muda dilakukan hanya pada cabai merah besar.
Tanaman dihasilkan dari embrio yang berumur 9 hari setelah penyerbukan (hsp).
Tidak satupun tanaman dihasilkan dari embrio yang benunur kurang dari 9 hari
setelah penyerbukan (Tabel 3). Hasil ini menunjukkan bahwa embrio yang
benunur kurang dari 9 hsp adalah terlalu muda dan belum siap untuk per-
tumbuhan dan perkembangan selanjutnya.
Pada umur 9 hari setelah penyerbukan, hanya
16,67%
eksplan yangmenghasilkan tanaman. Untuk setiap eksplan yang menghasilkan tanamap, hanya
terdapat satu tanaman. Rendahnya jumlah eksplan yang menghasilkan tanaman
dan jumlah tanaman tiap eksplan dapat disebabkan oleh halangan fisik daging
buah yang menghambat sentuhan, fisik antara embrio muda dan media tumbuh.
Sentuhan langsung antara embrio pada media tumbuh sangat berperan dalam
keberhasilan embrio untuk tumbuh menjadi tanaman. Pada cabai, penanaman
yang sangat kecil dan mudah rusak. Pada penelitian ini, pembelahan buah cabai
untuk dijadikan sebagai eksplan dan cara peletakannya di media turnbuh dengan
posisi tertelungkup dimaksudkan untuk membuat persentuhan antara biji muda
dengan media tumbuh.
Perlakuan radiasi pada serbuk sari yang digunakan untuk penyerbukan
menyebabkan terhambatnya perturnbuhan embrio. Pada dosis 10 Gy, tanaman
dapat dihasilkan dari buah yang berumur 11 hari setelah penyerbukan. Jumlah
eksplan yang menghasilkan tanaman hanya 5,56% pada varietas LV-2319 dan
13,89% pada varietas LV-2323. Tidak ada tanaman yang dihasilkan dari buah
yang terbentuk dari penyerbukan dengan serbuk sari yang telah diradiasi dengan
25 Gy (Tabel 3).
Tabel 3. Pengaruh radiasi pada serbuk sari yang digunakan
untuk
penyerbukanterhadap pembentukan tanaman melalui kultur buah muda
Keterangan:
*) Satu buah = 2 eksplan.
Angka yang terdapat dalam kurung adalah persentase dari total eksplan yang ditanam pada setiap perlakuan.
Umur Panen bush (hsp) 3 5 7 9 11 Jumlah eksplan yang dikultur tiap perlakuan
3 6
3 6
36
3 6
36
Jumlah eksplan yang menghasilkan tanaman
. LV-23 19
O G~ lOGy 25Gy
0 (0,OO) 0 (0,OO) 0 (0,OO)
0 (0,OO) 0 (0,OO) 0 (0,OO)
0 (0,OO) 0 (0,OO) 0 (0,OO)
6 (16,67) 0 (0,OO) 0 (0,OO)
6 (16,67) 2 (536) 0 (0,OO)
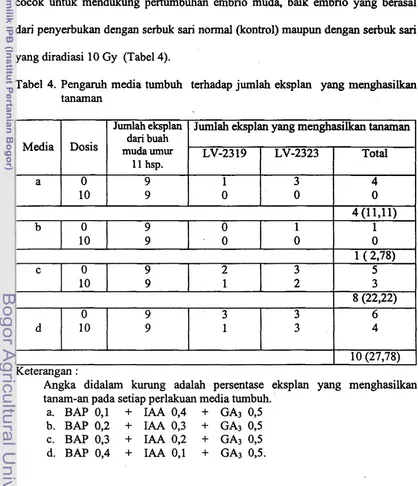
Keempat macam media tumbuh dapat digunakan untuk menumbuhkan
embrio muda cabai. Media a (BAP 0,l
+
IAA 0,4+
GA3 0,s) dan b (BAP 0,2+
IAA 0,3
+
GA3 0,5) tidak mendukung pertumbuhan embrio muda dari buah hasilpenyerbukan dengan menggunakan serbuk sari yang diradiasi. Hal ini dapat
ditunjukkan karena tidak satupun tanaman dihasilkan dari media ini. Media c
(BAP 0,3
+
IAA 0,2+ GA3
0,5) dan d (BAP 0,4+
IAA 0,1+
GA3 0,s) sangatcocok untuk mendukung pertumbuhan embrio muda, baik embrio yang berasal
dari penyerbukan dengan serbuk sari normal (kontrol) maupun dengan serbuk sari
yang diradiasi 10 Gy (Tabel 4).
Tabel 4. Pengaruh media tumbuh terhadap jumlah eksplan yang menghasilkan tanaman
Keterangan :
Angka didalam kurung adalah persentase eksplan yang menghasilkan tanam-an pada setiap perlakuan media tumbuh.
a. BAP 0,l
+
IAA 0,4+
GA3 0,5b. BAP 0,2
+
IAA 0,3+
GA3 0,5c. BAP 0,3
+
IAA 0,2+
GA3 0,5d. BAP 0,4
+
IAA 0,l+
GA3 0,s.Media a Dosis 0 10 Jumlah eksplan dari buah
,
&
,
,
11 hsp. 9 9
4 (11,ll) 1 0 1 ( 2978)
5 3 8 (22,22) 6 4 10 (27,78) b
Jumlah eksplan yang menghasilkan tanaman
[image:114.555.76.494.267.753.2]Analisis Sitologi Tanaman yang Dihasilkan dari Buah Muda
Radiasi pada serbuk sari cabai dapat menyebabkan kerusakan DNA
krornosom, sehingga embrio yang dihasilkan dari proses pembuahan oleh serbuk
sari yang diradiasi hanya mengandung kromosom dari sel telur. Pada saat zigot,
kronlosom dari serbuk sari yang telah diradiasi dapat bergabung dengan
kromosom dari sel telur. Namun selama perkembangan zigot menjadi embrio
kromosom yang rusak dari serbuk sari dapat hilang selama proses mitosis.
Senlakin besar dosis radiasi yang diberikan pada serbuk sari, maka semakin rusak
kromosom serbuk sari tersebut. Rusaknya kromosom dari serbuk sari menyebab-
kan biji yang terbentuk tidak mengandung endosperma. Serbuk sari yang dirusak
kromosomnya dengan radiasi telah banyak digunakan untuk menginduksi ter-
jadinya partenokarpi atau proses ginogenesis seperti pada tanaman petunia
(Raquin 1984 dalanz Suharsono 1993), tembakau (Suharsono 1993) dan semangka
(Sugiyama & Morishita 1998). Selain itu, Muzial & Przywara (1999) melaporkan
dengan pemberian dosis 500 Gy pada serbuk sari tembakau yang digunakan untuk
penyerbukan dapat menurunkan jumlah sel endosperma pada biji yang terbentuk.
Tanaman mulai muncul (berkecambah) pada minggu ke-5 setelah di-
kultur (msk) pada buah hasil penyerbukan dengan serbuk sari normal maupun
yang diradiasi. Pertumbuhan tanaman dari biji hasil penyerbukan serbuk sari yang
diradiasi lebih lambat daripada tanaman normal. Ukuran tanaman dari biji hasil
penyerbukan oleh serbuk sari yang diradiasi lebih kecil daripada tanaman normal.
Hal ini menunjukkan bahwa radiasi pada serbuk sari yang digunakan untuk
600 Gy dapat menjamin terbentuknya tanaman haploid (Suharsono 1993). Pada
selllangka dosis 800 Gy menyebabkan buah yang terbentuk berbiji kecil dan
jumlah serta ukurannya berbeda dengan koritrol (Sugiyama & Morishita 1998).
Na~ilun pada pir Jepang kultivar Hosui hanya diradiasi 20 Gy dapat menghasilkan
jumlah buah dan biji yang rendah dibanding~an yang tidak diradiasi. Demikian
pula kultivar Gold Nijisseki menghasilkan jumlah buah yang sedikit pada
peiliberian dosis 20 Gy bila dibanding dengan kontrolnya.
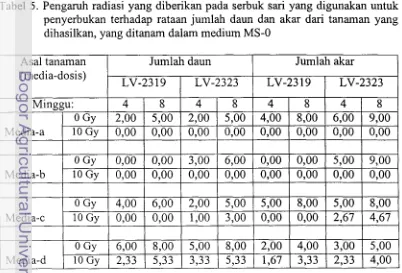
Pertumbuhan dan ukuran yang dicerminkan oleh jumlah daun dan akar
pada tanaman yang dihasilkan dari buah hasil penyerbukan dengan serbuk sari
yang diradiasi lebih kecil daripada yang dihasilkan dari penyerbukan dengan
serbuk sari normal (Tabel 5 dan Gambar 8) yang berkorelasi dengan hasil analisis
ploidi. Tanaman haploid tumbuh lambat dan mempunyai ukuran yang lebih kecil
daripada tanaman normal (diploid).
Tabel 5. Pengaruh radiasi yang diberikan pada serbuk sari yang digunakan untuk
[image:116.511.56.458.461.734.2]Embrio cabai merah besar hasil dari penyerbukan dengan serbuk sari
yang normal dapat tumbuh menjadi tanaman mulai umur 9 hari setelah
penyerbukan (hsp), sedangkan embrio yang dihasilkan dari penyerbukan dengan
serbuk sari yang diradiasi 10 Gy dapat tumbuh menjadi tanaman pada umur 11
hsp. Tunas mulai muncul pada umur 5 minggu setelah tanam. Media yang cocok
untuk menumbuhkan embrio muda hasil penyerbukan dengan serbuk sari yang
diradiasi 10 Gy adalah media MS yang mengandung BAP 0,3 mgll, IAA 0,2 mgll,
GA3 0,5 mgll (c), dan BAP 0,4 mgll, IAA 0,l mgll, GA3 0,5 mgll (d). Persentase
keberhasilan pembentukan tanaman haploid pada varietas LV-23 19 adalah 5,56%
KESIMPULAN DAN SARAN
Kesimpulan
Radiasi sinar gamma pada dosis 10 dan 25 Gy berpengaruh terhadap
daya kecambah serbuk sari cabai merah besar (LV-2319, LV-2323) dan cabai
keriting (CK-C, CK-L).
Serbuk sari yang diradiasi sinar gamma pada dosis 10 Gy tidak ber-
pengaruh terhadap pembentukan buah pada cabai merah besar (CB) dan cabai
keriting (CK). Namun pada dosis 25 Gy terjadi pengaruh terhadap pembentukan
buah cabai merah besar (CB) maupun cabai keriting (CK).
Embrio cabai merah besar ~ (LV-23 19, LV-2323) dapat tumbuh menjadi
tanaman s