PENYAKIT DIABETES MELITUS TIPE 2
ELIS LISTIANDINI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis dengan judul Model Matematika Dinamika Glukosa, Insulin, Massa Sel-β, dan Reseptor Insulin Pada Penyakit Diabetes Melitus Tipe 2 adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, September 2011
ELIS LISTIANDINI. A Mathematical Model of the Dynamics of Glucose, Insulin, β-cells Mass, and Insulin Receptors in Diabetes Mellitus Disease Type 2. Supervised by PAIAN SIANTURI and ALI KUSNANTO.
The diabetes mellitus is a disease in glucose-insulin regulatory system, which is referred to as hyperglikemia. Most cases are categorized as type 2 of the diabetes mellitus (T2DM), which are characterized by high blood glucose levels. The T2DM is associated with a deficit in the mass of β-cells. If the blood glucose consentration level is high, then the β-cells release insulin into the pancreas. The aim of this research is to study the glucose-insulin dynamics. A βIG model was proposed to describe the glucose-insulin dynamics. This model provide a pathway for diabetes development through the introduction of a 3rd dynamical variable, the β-cell mass. The addition of insulin receptor is an important factor in this quantitative improvement in order to make the model more realistic. Incorporation of the insulin receptor into the existing mathematical model gives a four dimensional system of nonlinear ordinary differential equations, which is introduced as the modified model. Both of the models have two stable equilibria representing physiological steady state and pathological steady state. Furthermore the third steady state is found to be a saddle point. Nevertheless the average mass of β-cell in the modified model is quantitatively more reasonable and therefore better then βIG models.
ELIS LISTIANDINI. Model Matematika Dinamika Glukosa, Insulin, Massa sel-β, dan Reseptor Insulin pada Penyakit Diabetes Melitus Tipe 2. Dibimbing oleh PAIAN SIANTURI dan ALI KUSNANTO.
Diabetes melitus tipe 2 (DMT2) merupakan penyakit gangguan kesehatan akibat kadar glukosa yang tinggi terus menerus sehingga mengakibatkan penurunan fungsi sel-β penghasil insulin. Hampir sebagian besar kasus diabetes adalah DMT2, yang disebabkan karena pola hidup tidak sehat. DMT2 awalnya ditandai dengan penurunan sensitivitas insulin (kepekaan terhadap insulin) dan peningkatan resistansi insulin (perlawanan terhadap insulin), dan jika kondisi ini secara signifikan meningkat terus maka akan terjadi hiperglikemia akut yang mengakibatkan komplikasi dan kematian. DMT2 merupakan penyakit global yang banyak diidap penduduk dunia, dan Indonesia berada pada peringkat ke-4 setelah Cina, India, dan Amerika.
Fenomena yang terjadi memerlukan adanya suatu penelitian dan pemikiran dari pihak kesehatan maupun bidang ilmu lainnya. Matematika, khususnya pemodelan matematika dapat membantu memahami dan mengidentifikasi hubungan DMT2 dengan berbagai variabel maupun parameter. Pentingnya penelitian DMT2 telah banyak dilakukan para ilmuwan.
Dalam tesis ini dibahas model βIG Topp (Topp et al. 2000) yang menambahkan dinamika massa sel-β pada dinamika glukosa-insulin. Pada model βIG dilakukan analisis kestabilan dan simulasi numerik dengan pemrograman berbasis fungsional menggunakan software Mathematica 7. Pengembangan model selanjutnya adalah yang disebut model modifikasi (Ryan et al, 2001) yang menambahkan variabel dinamika reseptor insulin pada model sebelumnya.
Analisis kestabilan dari model βIG menghasilkan tiga titik tetap, yaitu: titik tetap stabil yang merupakan titik tetap penyakit, titik tetap sadel , dan titik tetap stabil yang merupakan titik tetap bebas penyakit. Untuk analisis kestabilan dari model modifikasi juga dihasilkan tiga titik tetap yaitu titik tetap, yaitu: titik tetap stabil yang merupakan titik tetap penyakit, titik tetap sadel , dan titik tetap stabil yang merupakan titik tetap bebas penyakit. Dari titik tetap yang diperoleh pada kedua model tersebut diperoleh hasil bahwa massa sel-β individu normal pada model βIG memiliki rentang yang telalu jauh dibandingkan massa sel-β pada model modifikasi, sehingga model modifikasi dianggap lebih realistis untuk menggambarkan fenomena nyata.
Beberapa perubahan parameter model menghasikan perubahan dinamika massa sel-β yang menunjukkan bahwa pada model βIG, dinamika massa sel-β tidak pernah mencapai nol, sedangkan pada model modifikasi, dinamika massa sel-β dapat mencapai nol. Secara biologis model modifikasi lebih representatif menunjukkan dinamika diabetes, karena dengan membuktikan bahwa massa sel-β mencapai nol berarti terjadi kerusakan fungsi sel-β sehingga insulin tidak dihasilkan.
informasi untuk pencegahan maupun pengobatan penyakit diabetes melitus tipe 2.
© Hak Cipta milik Institut Pertanian Bogor, tahun 2011 Hak Cipta dilindungi Undang-undang
1 Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian,
penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar Institut
Pertanian Bogor.
2 Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
MODEL MATEMATIKA DINAMIKA GLUKOSA, INSULIN,
MASSA SEL-β, DAN RESEPTOR INSULIN PADA
PENYAKIT DIABETES MELITUS TIPE 2
ELIS LISTIANDINI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Matematika Terapan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Reseptor Insulin pada Penyakit Diabetes Melitus Tipe 2 Nama : Elis Listiandini
NRP : G551070511 Program Studi : MatematikaTerapan
Disetujui Komisi Pembimbing
Dr. Paian Sianturi Drs. Ali Kusnanto, M.Si.
Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Matematika Terapan
Dr. Ir. Endar H. Nugrahani, M.S Dr. Ir. Dahrul Syah, M.Sc. Agr
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Penyusunan karya ilmiah ini juga tidak terlepas dari dukungan dan bantuan berbagai pihak. Penulis mengucapkan terimakasih yang sebesar-besarnya kepada:
1. Dr. Paian Sianturi selaku dosen pembimbing I dan Drs. Ali Kusnanto, M.Si. selaku pembimbing II. Terimakasih atas waktu, ilmu yang diberikan dan kesabarannya dalam memberikan bimbingan dan motivasi kepada penulis. 2. Dr. Ir. Endar H. Nugrahani, MS. selaku dosen penguji yang telah memberikan
saran dan kritiknya.
3. Seluruh dosen Departemen Matematika yang telah memberikan ilmu, bimbingan, dan motivasi selama penulis menuntut ilmu.
4. Seluruh staf pegawai yang telah membantu kelancaran administrasi.
5. Kementerian Agama Republik Indonesia, yang telah memberikan biaya kepada penulis selama menempuh pendidikan program magister di Institut Pertanian Bogor.
6. H. Tojo Wasman dan Hj. Iis Aisyah, yang telah memotivasi dan membantu kelanjutan studi hingga selesai.
7. Keluarga di Lampung, suami, dan anak-anakku yang telah memberikan semangat, doa, kesabaran, dan kasih sayangnya selama ini.
8. Teman-teman Mahasiswa S-2 Matematika Terapan IPB angkatan 2007 dan 2009 yang telah memberi inspirasi.
9. Rekan-rekan kerja di MTs Negeri 33 Jakarta yang telah banyak mendukung secara moral.
10.Semua pihak yang telah membantu penulis, yang tidak bisa penulis sebutkan satu persatu.
Akhirnya penulis menyadari bahwa Tulisan ini masih jauh dari sempurna. Oleh karena itu sumbangsih kritik dan saran demi kemajuan tulisan selanjutnya sangat penulis harapkan.
Semoga karya ilmiah ini bermanfaat.
Bogor, September 2011
Penulis dilahirkan di Banjarmasin pada tanggal 29 Januari 1968 dari ayah Tojo Wasman dan ibu Iis Aisyah. Penulis merupakan putri pertama dari empat bersaudara.
Tahun 1986 penulis lulus dari SMA Negeri 60 Jakarta dan pada tahun 1997 masuk Universitas Lampung. Penulis memilih Jurusan Pendidikan Matematika pada Fakultas Keguruan dan Ilmu Pendidikan Program Sarjana dan selesai pada tahun 1992.
DAFTAR ISI
Halaman
DAFTAR TABEL ... xix
DAFTAR GAMBAR ... xxi
DAFTAR LAMPIRAN ... xxiii
I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan Penelitian ... 3
II TINJAUAN PUSTAKA ... 5
2.1 Sistem Persamaan Diferensial ... 5
2.2 Titik Tetap ... 6
2.3 Nilai Eigen dan Vektor Eigen ... 6
2.4 Analisis Kestabilan Titik Tetap ... 7
III MODEL MATEMATIKA ... 9
3.1 Sistem Pengaturan Glukosa-Insulin ... 9
3.2 Model βIG ... 12
3.3 Model Modifikasi ... 14
IV ANALISIS KESTABILAN DAN SIMULASI SOLUSI ... 17
4.1 Analisis Kestabilan Model βIG ... 17
4.2 Simulasi Model βIG ... 22
4.3 Analisis Kestabilan Model Modifikasi ... 24
4.4 Simulasi Model Modifikasi... 28
V KESIMPULAN DAN SARAN ... ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 39
Halaman
1 Nilai-nilai parameter model βIG ... 19
2 Kestabilan pada titik tetap model βIG ... 20
3 Nilai-nilai parameter model modifikasi ... 26
Halaman 1 Skema diagram sistem pengaturan glukosa-insulin ... 10 2 Hubungan antara insulin, reseptor insulin, dan alat pengangkut
glukosa atau glucose transporter-4 (GLUT 4) ... 11 3 Hubungan antara , , dan dalam waktu 3 hari dengan nilai
parameter pada Tabel 1 ... 20 4 Hubungan antara , , dan untuk 3 hari dengan nilai
parameter pada Tabel 1 ... 21 5 Plot perubahan dinamika massa sel-β untuk nilai = 0.5, 0.72, 0.9, pada
saat = 43.2 ... 22 6 Plot perubahan dinamika massa sel-β untuk nilai = 0.1, 0.72, 0.9, pada
saat = 50 ... 23 7 Hubungan antara , , , dan untuk 3 hari dengan nilai parameter
pada Tabel 2 ... 27 8 Hubungan antara , , , dan dengan nilai = 0.079 dan = 0.00057 28 9 Hubungan antara , , , dan dengan nilai c = 0.2 dan = 50 ... 29 10 Hubungan antara , , , dan dengan . dan = 45 ... 30 11 Plot perubahan dinamika massa sel-β untuk nilai = 0.2, 0.85, 0.9, pada
saat = 43,2 ... 31 12 Plot perubahan dinamika massa sel-β untuk nilai = 0.1, 0.85, 0.9, pada
saat = 50 ... 31 13 Plot perubahan dinamika reseptor insulin untuk nilai = 0.1, 0.85, 1, dan
Halaman 1 Penentuan titik tetap model βIG ... 40 2 Penentuan nilai eigen pada titik tetap ... 43 3 Perintah Mathematica untuk menentukan titik tetap dan nilai eigen pada
model βIG ... 45 4 Penentuan titik tetap model modifikasi ... 46 5 Penentuan nilai eigen pada titik tetap ... 51
IPENDAHULUAN
1.1 Latar BelakangDiabetes melitus adalah suatu penyakit gangguan kesehatan dimana kadar gula darah seseorang menjadi tinggi karena gula dalam darah tidak dapat digunakan oleh tubuh. Diabetes mekitus dikenal juga dengan sebutan penyakit gula darah atau kencing manis. Diabetes terjadi jika tubuh tidak menghasilkan insulin yang cukup untuk mempertahankan kadar gula darah yang normal atau jika sel tidak memberikan respon yang tepat terhadap insulin. Terdapat dua tipe diabetes melitus yaitu: diabetes melitus tipe 1(DMT1) dimana tubuh kekurangan hormon insulin karena serangan autoimun pada sel-β, dan diabetes mellitus tipe 2 (DMT2) dimana hormon insulin dalam tubuh tidak dapat berfungsi dengan semestinya.
Sebagian besar kasus adalah DMT2 yang disebabkan faktor obesitas, dan pola hidup tidak sehat.Individu yang terkena DMT2 cenderung memiliki sensitivitas insulin yang rendah dan tingkat resistansi insulin yang tinggi.Resistansi insulin sangat berhubungan dengan kemampuan tubuh yang rendah terhadap tingkat pengaturan reseptor insulin.Reseptor insulin merupakan protein pada permukaan sel yang mengikat insulin. Pada DMT2 massa sel-β terlalu bekerja keras karena kadar gula yang tinggi sehingga terjadi kelelahan yang menyebabkan penurunan produktivitas massa sel-βdan sekresi insulin berkurang. Kekurangan insulin dapat menyebabkan berkurangnya tingkat penyerapan glukosa oleh tubuh.
Penelitian tentang penyakit diabetes telah banyak dilakukan, salah satunya adalah Topp et al. (2000) yang memodelkan dinamika glukosa-insulin.Model ini menggabungkan model Bergmanet al. (1979) dengan laju perubahan massa sel-β, dan memberikan jalur untuk terbentuknya diabetes.Model Topp atau disebut juga model βIG ini telah banyak dikembangkan oleh ilmuwan lain.
Dari beberapa perkembangan model, model Ryan et al. (2001) atau disebut juga model modifikasi yang mengkoreksi model βIG dengan cara menambahkan variabel dinamika reseptor insulin.Dalam tulisan iniakan ditunjukkan lebih jelas bagaimana reseptor insulin menjalani fungsinya pada penderita dengan resistansi insulin yaitu penderita dengan kemampuan pengaturan reseptor insulin yang rendah.
Jalur yang berbeda untuk membangun diabetes dimana dengan melibatkan peningkatan pada resistansi insulin yang disebabkan sekresi insulin, yang bebas dari massa sel-β telah memperkuat penelitian sebelumnya. Revisi yg dilakukan menunjukkan pendekatan bahwa solusi sistem menunjukkan massasel-β dapat mencapai nol, yaitupendekatan untuk penyakit diabetes (Mason 2006).
Perkembangan selanjutnya pendekatan secaraFarmakoKinetik-FarmakoDinamik Mekanistik (PK-PD) yang menggabungkan model konsentrasi glukosa saat puasa, konsentrasi insulin saat puasa, sensitivitas insulin dan massa sel-β, yang menjelaskan pasien pada berbagai tahap penyakit, dari non-diabetes sampai resistansi insulin jangka panjang pada pasien DMT2, dan menggabungkan dampak pengobatan terhadap keempat variabel dilakukan olehRibbing et al. (2008).
1.2 Tujuan Penelitian
Tujuan utama dari penulisan karya ilmiah ini adalah: 1 Mengkaji kestabilan model βIG dan model modifikasi.
2 Membandingkan dinamika model βIGdengan model modifikasi.
IITINJAUAN PUSTAKA
2.1 Sistem Persamaan Diferensial (SPD)Definisi 1 SPD Linear
Jika suatu Sistem Persamaan Diferensial (SPD) dinyatakan sebagai berikut:
, , (2.1)
dengan adalah matriks koefisien berukuran x dan vektor konstan , maka sistem tersebut dinamakan SPD linear orde 1 dengan kondisi awal
. Sistem (2.1) disebut homogen jika dan non homogen, jika .
(Tu 1994)
Definisi 2 Sistem Persamaan Diferensial Tak Linear Misalkan diberikan SPD sebagai berikut:
, (2.2) dengan
dan ,
, , , ,
, , , , diasumsikan fungsi tak linier
pada , , , .Sistem (2.2) disebut SPD tak linear.
(Braun 1983)
Definisi 3 Sistem Persamaan Diferensial Mandiri
Misalkan suatu SPD dinyatakan sebagai berikut:
, , (2.3)
dengan merupakan fungsi kontinu bernilai real dari dan mempunyai turunan parsial kontinu. Sistem (2.3) disebut sistem persamaan diferensial mandiri
(autonomous) karena tidak memuat t secara eksplisit di dalamnya.
2.2 Titik Tetap Definisi 4Titik Tetap
Misalkan diberikan sistem persamaan diferensial mandiri (2.3). Titik disebut titik tetap atau titik kritis atau titik kesetimbangan jika .
(Tu 1994)
Definisi 5Titik Tetap Stabil
Misalkan adalah titik tetap sebuah persamaan diferensial dan adalah solusi dengan kondisi awal , dimana .Titik dikatakan titik tetap stabil, jika untuk setiap , terdapat , sedemikian sehingga| | ,
maka | | untuk .
(Verhulst 1990)
2.3 Nilai Eigen dan Vektor Eigen
Jika A adalah matriks , maka sebuah vektor taknol di dalam disebut vektor eigen dariA, jika A adalah sebuah kelipatan skalar dari ; jelasnya:
A (2.4) Untuk skalar sembarang . Skalar disebut nilai eigendari A, dan disebut sebagai vektor eigen dari A terkait dengan .
Untuk memperoleh nilai eigen dari sebuah matriks , persamaan (2.4) dapat ditulis kembali sebagai
(2.5) Dengan matriks identitas. Persamaan (2.5) mempunyai solusi tak nol jika dan hanya jika
det | | (2.6) Persamaan (2.6) disebut persamaan karakteristik dari matriks , skalar-skalar yang memenuhi persamaan ini adalah nilai-nilai eigen A.
2.4 Analisis Kestabilan Titik Tetap
Diberikan sistem persamaan diferensial sembarang
,
Analisis kestabilan titik tetap dilakukan melalui matriks Jacobi darimatriks . Penentuan kestabilan titik tetap diperoleh dengan melihat nilai-nilai eigennya, yaitu dengan , ,3, … , yang diperoleh dari det . Secara umum, kestabilan titik tetap mempunyai tiga perilaku sebagai berikut:
1. Stabil, jika
a. Setiap nilai eigen real bernilai negatif ( untuk semua ,
b. Setiap bagian real dari nilai eigen kompleks bernilai lebih kecil atau sama dengan nol untuk semua .
2. Tak stabil, jika
a. Setiap nilai eigen real bernilai positif untuk semua ,
b. Setiap bagian real dari nilai eigen kompleks bernilai lebih besar atau sama dengan nol untuk semua .
c. Sadel, jika perkalian dari kedua nilai eigen real sembarang adalah negatif , untuk semua dan sembarang. Titik tetap sadel ini bersifat tak stabil.
(Tu 1994)
IIIMODEL MATEMATIKA
3.1 Sistem Pengaturan Glukosa-Insulin
Pada proses metabolisme, zat-zat hasil pencernaan akan diserap pembuluh darah kapiler di usus (vili), dan diangkut ke hati ke vena porta. Di dalam hati beberapa zat akanberubah ke bentuk lain dan beberapa lainnya akan diedarkan ke seluruh tubuh, seperti glikogendiubah menjadi glukosa. Glukosa mempunyai peranan penting sebagai energi bagi sel-sel otot organ tubuh.
Glukosa tidak dapat langsung masuk kedalam sel, karena itu dibutuhkan insulin untuk menyerap glukosa.Insulin dikeluarkkan oleh pankreas yang jumlahnya diatur pada tingkat gula darah.Jika tingkat gula darah tinggi maka sel-β pada pankreas mengeluarkan insulin yang menyebabkan diambilnya glukosa dari darah. Kemudian insulin berikatan dengan reseptor insulin pada permukaan sel, sehingga terjadi peningkatan afinitas yang tinggi molekul transporter glukosa GLUT 4, yang diangkut ke permukaan sel, kemudian memediasi penyerapan glukosa ke dalam sel. Proses ini menyebabkan kembali normal.
Kadar gula penderita diabetes saat puasa adalah lebih dari 126 mg/dl dan saat tidak puasa lebih dari 200 mg/dl.Pada orang normal kadar gulanya berkisar 70-110 mg/dl. Sedangkan kisaran yang konsisten dibawah 70 mg/dl dianggap gula darah rendah. Tingkat glukosa darah tidak boleh melebihi 300 mg/dl, karena jika hal ini berkelanjutan dapat menyebabkan kerusakan pada pembuluh darah dan organ yang mengarah ke komplikasi diabetes.Untuk menghindari komplikasi serius jangka panjang harus dilakukan pengobatan yang bertujuan untuk mempertahankan kadar glukosa pada tingkat normal sedekat mungkin.
Gambar 1Skema diagram sistem pengaturan glukosa-insulin(Ryan et al. 2001).
Pada Gambar 1 menunjukkan bahwajika saat tingkat glukosa rendah maka sel-α pankreas menghasilkan glukogen yang merupakan hormon yang bekerja pada hati untuk mengubah glikogen menjadi glukosa, dan kemudian membebaskannya ke darah.Jika pada sisi lain tingkat glukosa tinggi maka sel-β pankreas menghasilkan hormon insulin yang membantu penyerapan glukosa kedalam sel-sel tubuh, sehingga tingkat glukosa kembali berada pada tingkat normal.
Kemampuan glukosa tergantung pada respon dari sel sel-βpankreas dan sensitivitas insulin. Sensitivitas insulin adalah kondisi yang menggambarkan kebutuhan relatif seseorang terhadap insulin untuk memproses glukosa.Keduanya berkontribusi terhadap toleransi glukosa.Jika toleransi glukosa rendah pada individumakakondisi ini berhubungan dengan berkurangnya respon sel-β ataupun menurunnya sensitivitas insulin.Sedangkan orang dengan resistansi insulin membutuhkan banyak insulin untuk proses penyerapan glukosa, dan ini menyebabkan masalah kesehatan. Resistansi insulin merupakan kodisi fisiologis dimana hormon insulin menjadi kurang efektif dalam menurunkan kadar glukosa. Resistansi insulin sangat berhubungan dengan kemampuan tubuh yang rendah terhadap pengaturan reseptor insulin, sehingga glukosa tidak dapat diserap dengan baik oleh sel-sel otot dan menyebabkan kelebihan glukosa (gula darah
Glukosa Rendah
Glukosa Tinggi
Pankreas
Insulin dilepas oleh sel-β dari pankreas
Glukogen dilepas oleh sel-α dari pankreas
Hati melepas glukosa Masuk ke darah
Sel-sel mengambil glukosa dari darah
tinggi).Dengan demikian resistansi Insulin dianggap sebagai penyebab yang mendasaripotensi pengembangan DMT2.
Gambar 2Hubungan antara insulin, reseptor insulin dan alat pengangkut glukosa atau Glucose Transporter- 4 (GLUT 4).
Gambar2di atas menjelaskan bahwa insulin mengikat pada reseptor insulin, yang merupakan protein pada membran sel (1),kemudian mulai aktivasi banyak protein (2).Sebagai respon terhadap insulin menyebabkan terbentuknya pengangkut glukosa atau glukosa transporter-4 (GLUT 4), yang kemudian berpindah kepermukaan sel dan mengalami penyesuaian sehingga memfasilitasi jalan masuk glukosa ke sel-sel otot (3), sintesis glikogen (4), glikolisis yang mengubah glukosa menjadi asam piruvat (5), sintesis asam lemak (6).
Setelah terjadi pengikatan insulin oleh reseptor insulin, kemudian terjadi peristiwa internalisasi yaitu terjadinya pemisahan hormon dari reseptor.Pada saat hormon kompleks diinternalisasi (tidak lagi pada permukaan sel) dan tidak dapat menyebabkan respon seluler terhadap insulin sampai reseptor insulin didaur ulang dan bergerak kembali ke membran sel.Pada saat insulin dimediasi oleh internalisasi,akan mengurangi konsentrasi reseptor insulin pada permukaan sel. Hal ini merupakan faktor potensial pada pemeriksaan resistansi insulin.
Glukosa
Insulin
Reseptor
Insulin
GLUT
‐
4
Asam
Lemak
Penjelasan di atas menunjukkan peranan penting reseptor insulin pada subyek resistansi insulin yang mengarah menuju penyakit DMT2.Olehkarena itu dalam model ini difokuskan penulisan pada analisis dinamika glukosa, insulin, massasel-β, dan dinamika reseptor insulin.
3.2 Model βIG
Keberadaan model matematika memberikan kontribusi untuk mempelajari penyakit secara kualitatif dan kuantitatif.Model βIG atau disebut juga model
Toppet al. (2000) memperkenalkan massa sel-β ke dalam sistem dinamik
glukosa-insulin. Massa sel-β muncul untuk membangun jalur terbentuknya diabetes. Pada model βIG, dipertimbangkan dinamika hubungan tiga variabel, yaitu: 1 konsentrasi glukosa darah pada waktu (mg/dl),
2 konsentrasi insulin darah pada waktu ( U/ml), 3 Massa sel- penghasil insulin pada waktu (mg).
Pemodelan yang terdiri dari tiga variabel (glukosa, insulin, dan massa sel-β
dinyatakan dalam bentuk persamaan:
(3.1)
(3.2)
)β (3.3) Dengan penjelasan notasi:
laju produksi glukosa oleh hati (mg/dl perhari),
lajupelepasanglukosa dari darah,bebas dari insulin (perhari), lajupelepasan glukosa, karena insulin (ml/ U perhari),
tingkatsel-β maksimum pada sekresi insulin ( U/ml.mg perhari), penentuan titik belok dari fungsi sigmoidal(mg²/dl²),
laju pelepasan insulin dari darah, untuk sel otot, hati dan ginjal (perhari), tingkat kematian sel- (perhari),
Pada persamaan (3.1) dapatdijelaskan bahwa laju produksi glukosa oleh hati ( sampai ke aliran darah terjadi pada saat konsentrasi glukosa , yaitu darah tidak melepaskan glukosa.Kemudian diikuti oleh laju pelepasan glukosadari darahyang tergantung pada kemampuan tubuh dan bebas dari insulin
.Laju pelepasan glukosa dari darah juga ada yang tergatung pada insulin . Jika dan meningkat maka mengakibatkan konsentrasi glukosa akan menurun, diberikan oleh penjumlahan .
Dari persamaan (3.2) diperoleh informasi bahwa konsentrasi insulin meningkat karena dipengaruhi oleh tingkat sel-β maksimal pada sekresi insulin (s . Hubungan antara konsentrasi glukosa dengan tingkat sel-β maksimal pada sekresi insulin mengikuti fungsi sigmoidal . Setelah itu diikuti oleh laju pelepasan insulin dari darah ( ). Pada saat f meningkat maka konsentrasi insulin akan menurun.
Dinamika massa sel-β yang ditunjukkan pada persamaan (3.3) dapat ditulis dalam bentuk logistik sebagai berikut:
/
Kenaikan massa sel-β terjadi karena pengaruh toleransi glukosa ( ), dan batas maksimal toleransi glukosa ( / ).Jika / maka
/ mendekati 0, ini
berarti produksimassa sel-β meningkat karena dipengaruhi oleh tingkat kenaikan konsentrasi glukosa pada batas toleransi. Karena massa sel-β mengalami peningkatan sehingga tingkat kematian massa sel-β( ) mengalami penurunan. Sedangkan Jika / , maka
/ bernilai negatif sehingga
produksi massa sel-β menurundan kematian massa sel-β meningkat.
yang dipengaruhi adanya insulin yang disekresi oleh sel-β, tetapi hanya menjelaskan pelepasan glukosa dari darah yang dipengaruhi oleh insulin. Oleh karena itu, akan dibahas lebih lanjut pengembangan model yang dapat menjelaskan adanya laju penyerapan glukosa oleh sel tubuh, yaitu model modifikasi Ryan.
3.3 Model Modifikasi
Model modifikasi merupakan pengembangan dari model βIG, yang menambahkan pengaruh reseptor insulin untuk menunjukkan penyerapan glukosa oleh sel tubuh. Padadinamika konsentrasi glukosa ( ), konsentrasi insulin ( ), dan massa sel-β ( ), Ryan et al. (2001) memperkenalkan fraksi reseptor insulin yang tersedia pada permukaan sel-sel otot .Reseptor insulin berfungsi untuk memediasi aktivitas insulin pada penyerapan glukosa danmetabolisme.Reseptor insulin ini aktif jika mengikat ke hormon insulin, sedangkan jika tidak ada insulin dalam darah maka reseptor insulin tidak akan diaktifkan. Model tersebut adalah
(3.4)
(3.5)
(3.6) (3.7) Dengan penjelasan notasi:
tingkat pengulangan reseptor insulin (per hari),
tingkatpengaturan reseptor pada permukaan sel otot karena rangsangan insulin(ml/ U perhari),
tingkatpengaturan reseptor pada permukaan sel otot, bebas dariinsulin (perhari).
glukosa dari aliran darah,yang tergantung pada kemampuan tubuh ( , menggambarkan efektifitas glukosa).Tingkat penyerapan glukosa juga dipengaruhi oleh laju pelepasan glukosa karena insulin ( , yang disebut sensitivitas insulin), Konsentrasi insulin ( ), dan fraksi reseptor insulin yang tersedia pada permukaan sel-sel otot ( ).Nilai-nilai yang lebih tinggi dari
, , , dan menyebabkan laju penyerapan meningkat sehingga konsentrasi
glukosa menurun.
Dari persamaan (3.5) dapat diperoleh informasi bahwa konsentrasi insulin ( ) akan meningkat karena pengaruh tingkat sel- tunggal pada sekresi insulin
. Sel-β akan mencapai kapasitas maksimal pada sekresi insulin ketika , yaitu pada saat hilangnya reseptor insulin darisel-sel otot.Hubungan yang terjadi antara konsentrasi glukosadan tingkat sel-β tunggal dalam mensekresi insulin adalah hubungan sigmoidal yang ditandai fungsi . Namun, peningkatan konsentrasi insulin diikuti oleh laju pelepasan insulin dari darah ( ).Peningkatan juga diikuti oleh penyerapan insulin pada reseptor sel otot ( ).
Penjelasan dari persamaan (3.6), bahwa dinamika massa sel-β tidak bergantung langsung pada fraksi reseptor insulin yang tersedia. Oleh karena itu kita tetap menggunakan persamaan yang diturunkan oleh Topp et al.Peningkatan massa sel-β dipengaruhi oleh batas toleransi glukosa ( , dan ). Tetapi massa sel-β akan menurun jika berada diluar batas toleransi.
IV ANALISIS KESTABILAN DAN SIMULASI SOLUSI
4.1 Analisis Kestabilan Model βIGTitik tetap pada sistem persamaan diferensialdari persamaan (3.1)-(3.3)akan diperoleh dengan menetapkan , , dan , sehingga diperoleh tiga
titik tetap
yaitu: ( ,0,0), , , ,
, , , dengan
h ,
h ,
(penurunan rumus ini dapat dilihat pada Lampiran 1).
Setelah diperoleh titik tetap , , dan , selanjutnya dilakukan analisis kestabilan di sekitar titik tetap dengan prosedur sebagai berikut:
1 Menentukan Matriks Jacobi dari sistem persamaan. 2 Menentukan Matriks Jacobi pada titik tetap.
3 Menentukan nilai eigen ( , dengan menyelesaikan persaamaan karakteristik det . Jika semua real negatif maka titik tetap tersebut stabil.jika semua real positif maka titik tetap tersebut tidak stabil. Tetapi jika minimal satu nilai eigenreal positif maka titik tetap tersebut sadel bersifat tak stabil.
Untuk menentukan Matriks Jacobi terlebih dahulu dilakukan pelinearan persamaan (3.1) - (3.3). Misalkan persamaan (3.1)- (3.2) ditulis sebagai berikut:
Untuk melihat kestabilan titik tetap setelah dilakukan pelinearan, kemudian ditentukan matriks Jacobi pada titik tetap ( , 0, 0 ), sebagai berikut:
Dengan menyelesaikan persamaankarakteristik det , dengan adalah Matriks Jacobi untuk titik tetap , adalahnilai eigen, dan adalah Matriks Identitas, sehingga diperolehnilai-nilai eigen sebagai berikut:
, ,
(penurunan nilai ini dapat dilihat pada Lampiran 2).
Kestabilan akan diperoleh jika semua nilai eigen bernilai negatif. Karena parameter diasumsikan tidak negatif, maka nilaieigen dan bernilai negatif. Agar nilai eigen bernilai negatif maka haruslah
Yang akan mengakibatkan titik tetap bersifat stabil.
Untuk melihat kestabilan pada titik tetap setelah dilakukan pelinearan, ditentukanMatriks Jacobi pada titik tetap , , , yaitu:
Untuk memperoleh kestabilan sistem di titik tetap , , setelah dilakukan pelinearan, sehingga diperoleh Matriks Jacobi:
Nilaieigen akan diperoleh dengan menyelesaikan persamaan karakteristik det . Karena nilai eigen dari titik tetap tidak mudah diperoleh secara analitik maka analisis dilakukan dengan bantuan softwareMathematica 7.(lihat Lampiran 3)
Nilai titik tetap , , dan dapat diperoleh dengan mensubtitusikan parameter normal dari Tabel 1 hasil penelitian Topp et al. (2000).
Tabel1 Nilai-nilai Parameter Model
Parameter Nilai Satuan
864 perhari
1.44 Perhari 0.72 perhari
43.2 perhari
20000
432 Perhari
0.06 Perhari
0.00084 perhari 0.0000024 perhari
[image:34.595.89.493.29.767.2]Dengan menggunakan software Mathematica 7 dan nilai parameter pada Tabel 1 diperoleh tiga titik tetap , , yaitu: , , , , . , 3 ,
Titik tetap disebut titik tetap patologis atau titik tetap penyakit yang memuat dan , dengan kadar glukosa tinggi = 600 mg/dl. Titik tetap
merupakan titik tetap menuju penyakit dengan kadar glukosa cukup tinggi yaitu = 250 mg/dl. Sedangkan titik tetap merupakan titik tetap fisiologis atau titik tetap bebas penyakit yang memuat dan , dengan kadar glukosa normal = 100 mg/dl.
Kestabilan pada titik tetap dan diperoleh dengan menentukan nilai
[image:35.595.76.484.29.778.2]eigen, sebagaimana ditunjukkan pada Tabel 2.
Tabel 2 Kestabilan Pada Titik Tetap Model TITIK
TETAP
NILAI EIGEN
HASIL
-432 -1.44 -0.42 Stabil
-431.01 -4.48 0.04 Sadel
-421.97 -18.66 -0.01 Stabil
Untuk memperjelas analisis yang telah dilakukan, kita dapat mengamati interaksimassa sel-β terhadap dinamika glukosa-insulin.Pada Gambar 3ditunjukkan hubungan konsentrasi glukosa , konsentrasi insulin , dan Massa sel-β terhadap waktu .
Keterangan:
: Konsentrasi glukosa ( :Konsentrasi Insulin (
: Massa sel-β (β)
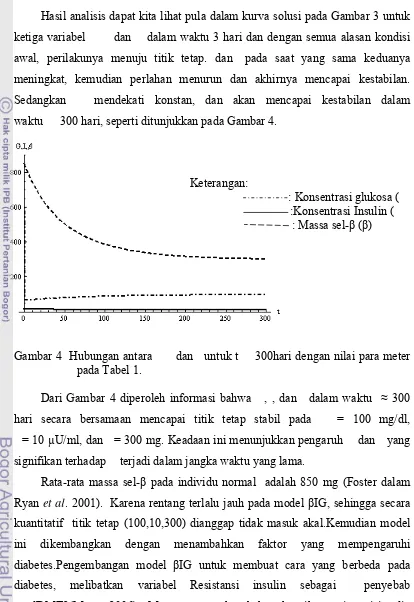
Hasil analisis dapat kita lihat pula dalam kurva solusi pada Gambar 3 untuk ketiga variabel dan dalam waktu 3 hari dan dengan semua alasan kondisi awal, perilakunya menuju titik tetap. dan pada saat yang sama keduanya meningkat, kemudian perlahan menurun dan akhirnya mencapai kestabilan. Sedangkan mendekati konstan, dan akan mencapai kestabilan dalam waktu 300 hari, seperti ditunjukkan pada Gambar 4.
Keterangan:
: Konsentrasi glukosa ( :Konsentrasi Insulin (
[image:36.595.100.514.86.688.2]: Massa sel-β (β)
Gambar 4 Hubungan antara dan untuk t 300hari dengan nilai para meter pada Tabel 1.
Dari Gambar 4 diperoleh informasi bahwa , , dan dalam waktu ≈ 300
hari secara bersamaan mencapai titik tetap stabil pada = 100 mg/dl, = 10 µU/ml, dan = 300 mg. Keadaan ini menunjukkan pengaruh dan yang
signifikan terhadap terjadi dalam jangka waktu yang lama.
Tulisan ini selanjutnya akan lebihdifokuskanpada kajian penambahan variabel reseptor insulin sebagai faktor penting pengembangan kuantitatif yang mempunyai peranan untuk memberikan informasi mengenai penyakit diabetes, khususnya DMT2.Seseorang dengan resistansi insulin memiliki tingkat pengaturan reseptor insulin yang rendah.Karena penyerapan glukosa dan insulin ke sel-sel tubuh sangat berhubungan dengan tingkat pengaturan reseptor insulin pada permukaan sel, sehingga dinamika reseptor ini penting dalam pengembangan kuantitatif.
4.2 Simulasi Model βIG
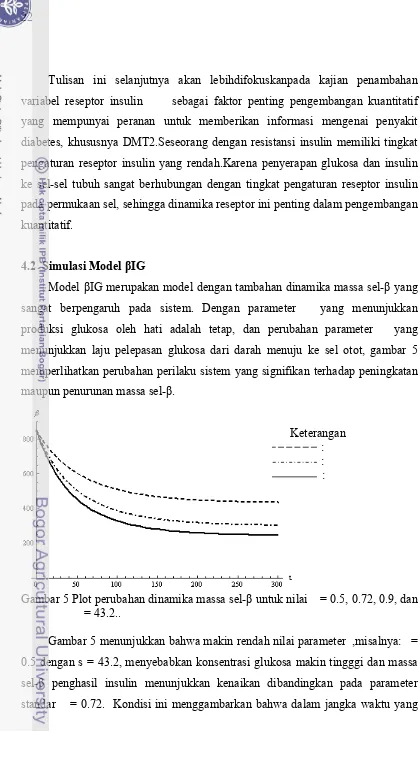
Model βIG merupakan model dengan tambahan dinamika massa sel-β yang sangat berpengaruh pada sistem. Dengan parameter yang menunjukkan produksi glukosa oleh hati adalah tetap, dan perubahan parameter yang menunjukkan laju pelepasan glukosa dari darah menuju ke sel otot, gambar 5 memperlihatkan perubahan perilaku sistem yang signifikan terhadap peningkatan maupun penurunan massa sel-β.
[image:37.595.64.484.26.790.2]Keterangan : : :
Gambar 5 Plot perubahan dinamika massa sel-β untuk nilai = 0.5, 0.72, 0.9, dan = 43.2..
panjang dan signifikan kadar glukosa terus menerus tinggi dan massa sel-β meningkat terus, sehingga dapat menyebabkan hiperglikemia (gula darah tinggi).
Jika nilai parameter makin tinggi, misalnya: = 0.9 dengan = 43.2,maka konsentrasi glukosa menurun dan massa sel-β menunjukkan penurunan dibandingkan pada parameter standar = 0.72. Kondisi ini menggambarkan bahwa dalam jangka waktu lama dan secara signifikan terjadi penurunan kadar glukosa dan massa sel-β sehingga dapat meyebabkan hipoglikemia (gula darah rendah).
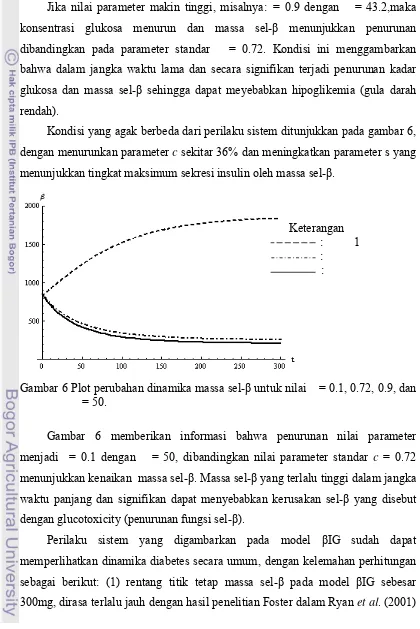
Kondisi yang agak berbeda dari perilaku sistem ditunjukkan pada gambar 6, dengan menurunkan parameter c sekitar 36% dan meningkatkan parameter s yang menunjukkan tingkat maksimum sekresi insulin oleh massa sel-β.
Keterangan : 1 :
[image:38.595.94.514.134.763.2]:
Gambar 6 Plot perubahan dinamika massa sel-β untuk nilai = 0.1, 0.72, 0.9, dan = 50.
Gambar 6 memberikan informasi bahwa penurunan nilai parameter menjadi = 0.1 dengan = 50, dibandingkan nilai parameter standar c = 0.72 menunjukkan kenaikan massa sel-β. Massa sel-β yang terlalu tinggi dalam jangka waktu panjang dan signifikan dapat menyebabkan kerusakan sel-β yang disebut dengan glucotoxicity (penurunan fungsi sel-β).
yaitu sebesar 850 mg, (2)dari Gambar 5 dan 6 telah ditunjukkan bahwa massa sel-β tidak akan pernah mencapai , keadaan ini diperkuat oleh hasil penelitian Mason (2000), dimana secara biologis bahwa massa sel-β akan mencapai nilai nol pada saat sel-β tidak lagi mensekresi insulin.Karena itu model ini dimodifikasi oleh Ryan et al. (2001) untuk pendekatan yang diharapkan lebih realistis dan representatif.
4.3 Analisis Kestabilan Model Modifikasi
Titik tetap dari persamaan (3.4) – (3.7) akan diperoleh dengan menetapkan , , , dan , sehingga diperoleh tiga titik tetap yaitu:
( , , , ), , , , ), dengan
,
Dan , , E , ), dengan
, (penurunan dapat dilihat pada Lampiran 4)
Setelah diperoleh titik tetap , , dan , selanjutnya dilakukan analisis kestabilan di sekitar titik tetap dengan menentukan Matriks Jacobi terlebih dahulu untuk pelinearan, kemudian menentukan nilai eigen untuk melihat perilaku sistem pada titik tetap.
Setelah dilakukan pelinearan, kemudian dianalisis kestabilan sistem di titik tetap dengan menentukan matriks Jacobi pada titik tetap sebagai berikut:
Nilai eigen akan diperoleh dengan menyelesaikan persamaan karakteristik det , sehingga akan diperoleh nilai eigen untuk matriks yaitu:
, , ,
(penurunan nilai ini dapat dilihat pada Lampiran 5).
Kestabilan akan diperoleh jika semua nilai eigen bernilai negatif. Karena parameter diasumsikan tidak negatif, maka nilaieigen , , dan
bernilai negatif. Agar nilai eigen bernilai negatif maka haruslah
Yang akan mengakibatkan titik tetap bersifat stabil.
Untuk memperoleh kestabilan sistem di titik tetap terlebih dahulu dilakukan pelinearan, sehingga diperoleh matriks Jacobi pada titik tetap yaitu:
A Q
Q
Q
Nilai eigen akan diperoleh dengan menyelesaikan persamaan karakteristik det . Karena nilai eigen dari titik tetap tidak mudah diperoleh secara analitik maka analisis dilakukan dengan bantuan software Mathematica 7.
Untuk memperoleh kestabilan sistem di titik tetap terlebih dahulu dilakukan pelinearan, sehingga diperoleh Matriks Jacobi:
s
Nilaieigen akan diperoleh dengan menyelesaikan persamaan karakteristik det .Karena nilai eigen dari titik tetap tidak mudah diperoleh secara analitik maka analisis dilakukan dengan bantuan software Mathematica 7.
Nilai titik tetap , , dan dapat diperoleh dengan mensubtitusikan parameter normal dari Tabel 3 hasil revisi Ryan et al. (2001)
Tabel3Nilai-nilai Parametermodelm modifikasi
Parameter Nilai Satuan
864 perhari
1.44 Perhari 0.85 perhari 43.2 perhari 20000
216 Perhari
0.03 Perhari 0.00057 perhari 0,0000025 perhari
2.64 Perhari
0.02 perhari
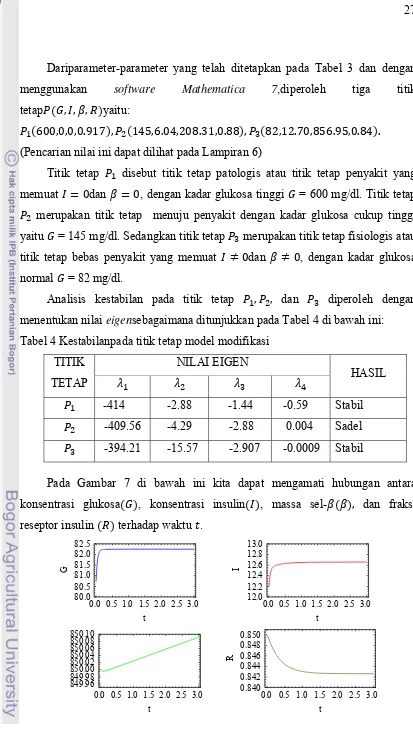
Dariparameter-parameter yang telah ditetapkan pada Tabel 3 dan dengan menggunakan software Mathematica 7,diperoleh tiga titik tetap , , , yaitu:
, , , . , , . , .3 , . , , . , . , . .
(Pencarian nilai ini dapat dilihat pada Lampiran 6)
Titik tetap disebut titik tetap patologis atau titik tetap penyakit yang memuat dan , dengan kadar glukosa tinggi = 600 mg/dl. Titik tetap
merupakan titik tetap menuju penyakit dengan kadar glukosa cukup tinggi yaitu = 145 mg/dl. Sedangkan titik tetap merupakan titik tetap fisiologis atau titik tetap bebas penyakit yang memuat dan , dengan kadar glukosa normal = 82 mg/dl.
[image:42.595.94.507.33.773.2]Analisis kestabilan pada titik tetap , , dan diperoleh dengan menentukan nilai eigensebagaimana ditunjukkan pada Tabel 4 di bawah ini:
Tabel 4 Kestabilanpada titik tetap model modifikasi TITIK
TETAP
NILAI EIGEN
HASIL
-414 -2.88 -1.44 -0.59 Stabil -409.56 -4.29 -2.88 0.004 Sadel -394.21 -15.57 -2.907 -0.0009 Stabil
Pada Gambar 7 di bawah ini kita dapat mengamati hubungan antara konsentrasi glukosa , konsentrasi insulin , massa sel- , dan fraksi reseptor insulin terhadap waktu .
0.0 0.5 1.0 1.5 2.0 2.5 3.0 80.0 80.5 81.0 81.5 82.0 82.5 t G
0.0 0.5 1.0 1.5 2.0 2.5 3.0 12.0 12.2 12.4 12.6 12.8 13.0 t I
0.0 0.5 1.0 1.5 2.0 2.5 3.0 849.96 849.98 850.00 850.02 850.04 850.06 850.08 850.10 t
Gambar 7Hubungan antara , , , dan untuk 3 hari dengan nilaiparameterparameter pada Tabel 2.
Dari gambar 7diperoleh informasi bahwa dalam waktu 3hari untuk setiap kondisi awal, saat konsentrasi glukosa dan konsentrasi insulin meningkat, kemudian stabil pada titik tetap = 82 mg/dl dan = 12.70 µU/ml. Sedangkan massa sel-β meningkat konstan dan stabil pada titik tetap = 856.95 mg dalam waktu 600 hari. Sebaliknya fraksi reseptor insulin menurun dan mencapai kestabilan pada titik tetap = 0.84. Telah ditemukan bahwa rata-rata massa sel-β pada individu normal ditutup pada nilai 850 mg, sehingga model modifikasi dianggap lebih realistis dibandingkan model βIG.
Secara biologis kondisi ini sesuai, bahwa pada saat terjadi pelepasan glukosa dan insulin dari hati, ginjal, dan aliran darah, akanterjadi peningkatan kosentrasi glukosa-insulin, dan massa sel-β secara konstan. Pada saat yang samakondisi fraksi reseptor insulin menurun, karena belum ada pengikatan insulin pada reseptor insulin.
4.4 Simulasi Model Modifikasi
Berikut ini akan dijelaskan bagaimana pengaruh perubahan beberapa nilai parameter pada sistem. Perubahan ini dapat dilihat pada gambar 8, 9 dan 10, yang menunjukkan pengaruh signifikan nilai parameter , , dan terhadap sistem.
Gambar 8: Hubungan antara , , , dan dengan nilai = 0.079 dan = 0.0009.
50 100 150 200t 80
100 120 140 G
50 100 150 200 t 8 10 12 14 16 I
50 100 150 200t 300 400 500 600 700 800
Dari Gambar 8 diperoleh informasi bahwa perubahan dari = 0.03 ditingkatkan menjadi . , dan perubahan dari = 0.00057 ditingkatkan menjadi . menandakan terjadinya peningkatan glukosaterus menerus, dan peningkatan fraksi reseptor insulin tidak menyebabkan menurunnya konsentrasi glukosa. Karena konsentrasi glukosa terus meningkat, ini berarti massa sel-β bekerja keras menghasilkan insulin sehingga fungsi sel-β makin menurun mencapai = 0. Penurunan fungsi sel-βdiikuti penurunan sekresi insulin.Keadaan ini menggambarkan penyakit diabetes parah dengan tingkat kematian tinggi.
Perubahan c berpengaruh pada sensitivitas insulin. Kenaikan 36% akan menyebabkan titik tetap fisiologis menjadi (82, 9.13, 628.95, 0.86). Dibandingkan dengan parameter normal , kenaikan mengakibatkan konsentrasi insulin menurundari = 12.70 µU/ml menjadi = 9.13. Pada keadaan inikonsentrasi glukosa tetap normal = 82 mg/dl, dan fraksi reseptor insulin meningkat dari = 0.84 menjadi = 0.86. Penurunan dan peningkatan menunjukkan, bahwapenggunaan insulin lebih efesien dengan tingkat pengaturan reseptor insulin yang lebih baik. Kondisi ini biasanya dipengaruhi oleh aktivitas olahraga sejalan
[image:44.595.102.465.457.671.2]dengan pertambahan usia.
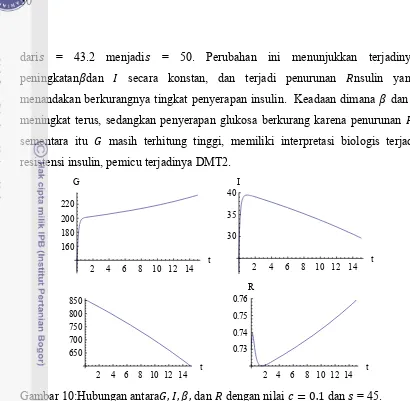
Gambar 9 Hubungan antara , , , dan dengan nilai = 0.2 dan = 50.
Pada Gambar 9 diperlihatkan perubahan parameter (laju pelepasan glukosa dari darah dan diserap oleh sel-sel otot) diturunkan sebesar 60% yaitu dari = 0.85 menjadi = 0.2, dan (tingkat maksimal sekresi insulin) ditingkatkan
2 4 6 8 10 12 14 t 126
127 128 129 G
2 4 6 8 10 12 14 t 24 26 28 30 32 34 36 I
2 4 6 8 10 12 14 t 855
860 865 870 875
2 4 6 8 10 12 14 t 0.731
dari = 43.2 menjadi = 50. Perubahan ini menunjukkan terjadinya peningkatan dan secara konstan, dan terjadi penurunan nsulin yang menandakan berkurangnya tingkat penyerapan insulin. Keadaan dimana dan meningkat terus, sedangkan penyerapan glukosa berkurang karena penurunan , sementara itu masih terhitung tinggi, memiliki interpretasi biologis terjadi resistensi insulin, pemicu terjadinya DMT2.
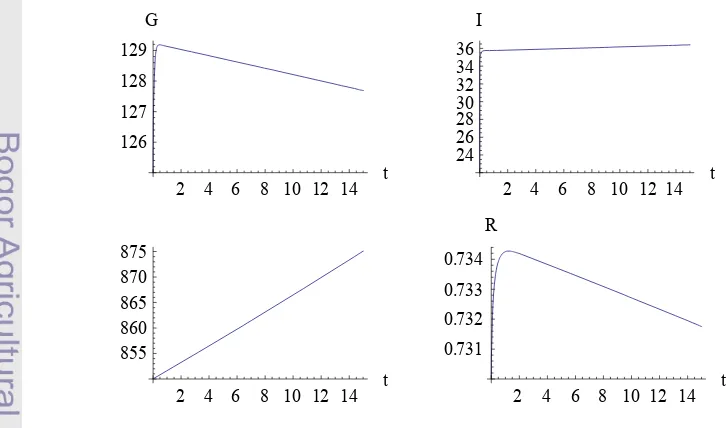
Gambar 10:Hubungan antara , , , dan dengan nilai . dan = 45.
Pada Gambar 10 diperoleh informasi bahwa penurunan parameter yang berhubungan dengan sensitivitas insulin (kebutuhan relatif seseorang terhadap insulin) ke tingkat yang lebih rendah lagi yaitu: , ,menunjukkan tinggi, penurunan dan ke tingkat yg parah dan mencapai = 0. Keadaan ini dapat dikatakan bahwa sistem menuju ke jalur diabetes yang disebutTopp et al. (2000)sebagai “dinamika hiperglikemia”.
Secara biologis diterima pula bahwa diabetes terjadi ketika massa sel-β tidak dapat lagi mengimbangi untuk tingkat resistansi insulin yang ada. Karena itu kita dapat melihat perilaku resistansi insulin pada nilai-nilai yang berbeda dari .
Gambar 8, 9, dan 10 telah menunjukkan bahwa dengan perubahan parameter , , dan terjadi perubahan yang signifikan terhadap perilaku sistem yang menggambarkan hubungan , , , dan . Kondisi yang telah digambarkan di atas sesuai secara biologi dan dirasa lebih realistis dan representatif dengan adanya penambahan dinamika reseptor insulin.
2 4 6 8 10 12 14 t 160
180 200 220 G
2 4 6 8 10 12 14 t 30
35 40 I
2 4 6 8 10 12 14 t 650
700 750 800 850
2 4 6 8 10 12 14 t 0.73
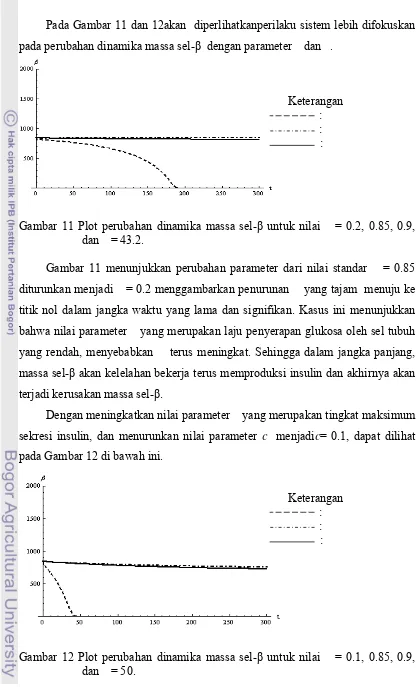
Pada Gambar 11 dan 12akan diperlihatkanperilaku sistem lebih difokuskan pada perubahan dinamika massa sel-β dengan parameter dan .
[image:46.595.95.511.73.760.2]Keterangan : : :
Gambar 11 Plot perubahan dinamika massa sel-β untuk nilai = 0.2, 0.85, 0.9, dan = 43.2.
Gambar 11 menunjukkan perubahan parameter dari nilai standar = 0.85 diturunkan menjadi = 0.2 menggambarkan penurunan yang tajam menuju ke titik nol dalam jangka waktu yang lama dan signifikan. Kasus ini menunjukkan bahwa nilai parameter yang merupakan laju penyerapan glukosa oleh sel tubuh yang rendah, menyebabkan terus meningkat. Sehingga dalam jangka panjang, massa sel-β akan kelelahan bekerja terus memproduksi insulin dan akhirnya akan terjadi kerusakan massa sel-β.
Dengan meningkatkan nilai parameter yang merupakan tingkat maksimum sekresi insulin, dan menurunkan nilai parameter c menjadic= 0.1, dapat dilihat pada Gambar 12 di bawah ini.
Keterangan : : :
Gambar 12 memberikan informasi, walaupun nilai parameter s ditingkatkan dari 43.2 menjadi 50 ternyata kondisi tidak menjadi lebih baik dan lebih parah karena disertai penurunan β yang diakibatkan oleh penurunan nilai parameterc = 0.1 dalam jangka waktu tidak begitu lama.
Berikut ini akan diperlihatkan perubahan dinamika reseptor insulin untuk nilai parameter dinaikkan atau diturunkan terhadap nilai standar, seperti ditunjukkan pada Gambar 13.
Keterangan : : :
Gambar 13 Plot perubahan dinamika Reseptor insulin untuk nilai = 0.1, 0.85, 1, dan = 43.2.
Pada gambar 13 ditunjukkan pengaruh perubahan parameter c terhadap dinamika reseptor insulin. Semakin tinggi tingkat penyerapan glukosa, misalnya: c = 1 dan = 43.2, berarti penyerapan insulin terjadi peningkatan, dan konsentrasi fraksi insulin stabil mendekati normal. Tetapi jika semakin rendah tingkat penyerapan glukosa, misalkan c = 0.1, berarti terjadi penurunan tingkat penyerapan insulin sehingga terjadi pula penurunan konsentrasi fraksi reseptor insulin.
dan . . Kemudian perubahan dalam mempengaruhi sistem, dengan titik tetapnya , 3. , . , dan . . Perubahan dan secara bersamaan mengakibatkan titik tetap menjadi , . ,
.3, dan . .Ternyata pengaruh dari perubahan parameter-parameter ini secara serentak lebih bagus dari pada mengkombinasikan pengaruh dari perubahan setiap individu.
Berikut ini akan kita bahas perilaku sistem untuk semua kondisi awal dan nilai parameter normal dengan aplikasi pada individu diabetes atau non diabetes. Gambaran ini dapat mengarahkan kita pada pencegahan dan penanganan penyakit secara umum.Gambar 9 menunjukkan keadaan seseorang dalam berbagai kondisi dan prediksi yang akan terjadi selanjutnya jika dilakukan pencegahan, pengobatan, ataupun tanpa pengobatan.
[image:48.595.102.471.425.726.2]Tujuan utama dari pengobatan diabetes adalah untuk mempertahankan kadar gula darah dalam kisaran yang normal. Namun, kadar gula darah yang benar-benar normal sulit untuk dipertahankan. Meskipun demikian, semakin mendekati kisaran yang normal, maka kemungkinan terjadinya komplikasi sementara maupun jangka panjang menjadi semakin berkurang. Untuk itu diperlukan pemantauan kadar gula darah secara teratur.
Gambar 14 Perilaku sistem terhadap titik tetap, untuk setiap kondisi awal.
0 1 2 3 4 5
100 200 300 400 500 600 700
Perilaku G t
0 100 200 300 400 500
2 4 6 8 10 12 14
Perilaku I t
0 100 200 300 400 500
200 400 600 800 1000
Perilaku t
0 1 2 3 4 5
0.75 0.80 0.85 0.90 0.95 1.00
Pada gambar 14 ditunjukkan kurva solusi yang menggambarkan perilaku konsentrasi glukosa , konsentrasi insulin , massa sel-β , dan hubungannya dengan fraksi reseptor insulin . Jika kondisi awal
maka konsentari glikosa meningkat menuju solusi kesetimbangan dan stabil pada titik tetap . Jika maka konsentrasi glukosa menurun menuju titik kesetimbangan dan stabil pada titik tetap . Pada saat yang sama . dan konsentrasi insulin menurun menuju solusi kesetimbangan dan stabil pada titik tetap . . Pada saat yang sama . dan massa sel-β menurun menuju salusi kesetimbangan dan stabil pada titik tetap . . Sedangkan . dan fraksi reseptor insulin meningkat menuju solusi kesetimbangan dan stabil pada titik tetap . . Sementara itu 84 < < 0.88 dan fraksi reseptor insulin menurun menuju solusi kesetimbangan dan stabil pada titik tetap 0.84.Keadaan ini menggambarkan kadar gula darah normalyang stabil pada titik tetap , . , . , dan
. . Jika konsentrasi glukosa konsisten berada dibawah 82 maka individu tersebut memiliki kadar gula rendah (hipoglikemia) sehingga harus dilakukan pengobatan untuk menormalkan kadar gula darah.
Jika kondisi awal maka konsentrasi glukosa meningkat menuju solusi kesetimbangan dan stabil pada titik tetap . Sementara itu
. . dan konsentrasi insulin meningkat menuju solusi kesetimbangan dan stabil pada titik tetap . .Pada saat yang sama
.3 . ,dimana massa sel-β meningkat menuju solusi kesetimbangan dan stabil pada titik tetap . . Sedangkan .
Jika kondisi awal maka konsentrasi glukosa akan menurun menuju solusi kesetimbangan dan cenderung stabil pada titik tetap . Pada saat yang sama dimana . dan konsentrasi insulin menurun
menuju solusi kesetimbangan dan cenderung stabil pada titik tetap .Sementara itu .3 dan massa sel-β menurun menuju solusi
kesetimbangan dan stabil pada titik tetap . Pada saat yang sama
V KESIMPULAN
5.1 KesimpulanHasil kajian pada model dinamika glukosa-insulin,dengan melakukan penambahan variabel massa sel-β dan variabel fraksi reseptor insulin, dan perubahan nilai parameter, diperoleh beberapa kesimpulan:
1. Kajian model βIG dari hasil analisis memiliki titik tetap stabil yang rentangnya terlalu jauh dari rata-rata normal massa sel-β pada individu yang sehat,jadi model βIG belum representatif. Sedangkan kajian model modifikasi memiliki titik tetap stabil yang hasilnyalebih mendekati rata-rata normal massa sel-β pada individu yang sehat, sehingga model modifikasi lebih representatif.
2. Penambahan variabel dinamika reseptor insulin dalam sistem pengaturan glukosa memberikan pengaruh pada dinamika massa sel-β. Massa sel-β dapat mencapai nol yang menunjukkan kerusakan massa sel-β.
3. Model βIG tidak mempunyai anggapan adanya pengaruh dinamika reseptor insulin, sedangkan model modifikasi memberikan penjelasan alami dan sesuai secara biologi (teoritis) melalui analisis dapat digambarkan secara kualitatif perilaku dinamika reseptor insulin, dan memberikan perbaikan hitungan secara kuantitatif.
4. Perubahan nilai parameter yang berhubungan degan laju penyerapan glukosa, tingkat sekresi insulin, akan mempengaruhi dinamika massa sel-β
dan dinamika Reseptor insulin.
5. Analisis model modifikasi dapat digunakan untuk menjelaskan tentang penyakit seperti hipoglikemia (kadar glukosa rendah), kondisi normal (non diabetes), Resistansi insulin, hiperglikemia (kadar glukosa tinggi), hiperglikemia kronis (diabetes parah).
5.2. Saran
Pengembangan penelitian dapat dilakukan lebih lanjut dengan menggabungkan dinamika sensitivitas insulin ataupun resistansi insulin yang berhubungan dengan kemampuan tubuh seseorang dalam menghasilkan ataupun menyerap insulin.
DAFTAR PUSTAKA
Anton H. 2000.Elementary Linear Algebra.Eight edition. Lehigh Press, Inc. USA.
Bergman RN, Ider YZ, Bowden CR, Cobellic. 1979. Quantitative Estimation of Insulin Sensitivity. Am J Physiol. Jun;236(6): E67-77.
Braun M. 1983.Differential Equations and Their Applications.New York: Springer-Verlag.
Edelstein-Keshet L. 1988.Mathematical Models in Biology.New York: Random House.
Mason CC. 2006. Improved Modeling of the Glucose-Insulin Dynamical System Leading to a Diabetic State. Arizona State University National Institutes of Diabetes and Digestive and Kidney Diseases.
PDPERSI. 2008. Perubahan Gaya Hidup dan Pola Makan Picu Diabetes.Pusat
Data dan Informasi PERSI. Jakarta.
Ribbing J, Hamren B, Svenson MK, Karlsson MO. 2008.Modelling the Dynamics of Glucose-Insulin Sensitivity and Beta-Cells in Subjects with Insulin Resistance and Patients with Type 2 Diabetes.Manuscript.June: Page 19. Ryan DH, Danielle JL, Daniel BR, Thomas BV, Stephen AW. 2001. A Model
of β-Cell Mass, Insulin, Glucose, and Receptor Dynamics with Applications to Diabetes.Cornell Univ Dept of Biometrics Technical Report BU-1579-M.
August:1-24.
Topp B, Promislow K, Devries G, Miura RM, Fine good DT. 2000. Amodel of Beta-Cells Mass, Insulin, and Glucose, Kinetics: Pathways to Diabetes.J Theor Biol. 206:605-619.
Tu PNV. 1994.Dynamical Systems An Introduction with Applications in
Economics and Biology. Springer-Verlag, New York.
Lampiran 1 Penentuan titik tetap model βIG Titik tetap akan diperoleh dengan menetapkan
i
ii
iii
• Dari persamaan (iii) diperoleh nilai dan sebagai berikut:
atau atau
atau = atau =
• Dari persamaan (ii) diperoleh nilai sebagai berikut:
• Dari persamaan (i) diperoleh nilai sebagai berikut:
• Subtitusikan untuk mendapatkan nilai
, karena maka
Subtitusikan untuk mendapatkan nilai
, karena maka
Sehingga diperoleh titik tetap , , , ,
isalkan , sehingga
Subtitusikan = untuk mendapatkan
nilai
Sehingga diperoleh titik tetap
, , , , 3
• Subtitusikan = untuk mendapatkan nilai
↔
Subtitusikan = untuk mendapatkan nilai
Sehingga diperoleh titik tetap
, , , , 3
Lampiran 2 Penentuan nilai eigen pada titik tetap
Misalkan persamaan (3.1), (3.2), dan (3.3) dituliskan sebagai berikut:
Dengan melakukan pelinieran didapat matriks Jacobi sebagai berikut:
• Pelinieran titik tetap , , aka diperoleh matriks Jacobi sebagai berikut:
Kemudian dicari nilai eigen dengan menggunakan persamaan karakteristik det sehingga diperoleh
Jadi nilai eigennya adalah sebagai berikut
Lampiran 3 Perintah Mathematica untuk menentukan titik tetap dan nilai eigen model βIG
Lampiran 4 Penentuan titik tetap model modifikasi
Titik tetap akan diperoleh dengan menetapkan
a
b
c
d
• Dari persamaan (c) akan diperoleh nilai dan sebagai berikut:
atau
atau
atau = atau =
• Dari persamaan (b) diperoleh nilai sebagai berikut:
↔
• Dari persamaan (a) diperoleh nilai sebagai berikut:
• Dari persamaan (d) diperoleh nilai sebagai berikut:
• Subtitusikan untuk mendapatkan nilai
, karena maka
, karena maka
Subtitusikan untuk mendapatkan nilai
, karena maka
Sehingga diperoleh titik tetap , , , , , ,
• Subtitusikan = untuk mendapatkan nilai
isalkan p , sehingga , dan
Subtitusikan untuk mendapatkan nilai R
Sehingga diperoleh
Subtitusikan untuk mendapatkan nilai
↔
Sehingga diperoleh
Subtitusikan , , untuk mendapatkan
nilai
Sehingga nilai
dan diperoleh titik tetap sebagai berikut: , , ,
, , ,
• Subtitusikan = untuk mendapatkan nilai
isalkan , sehingga , dan
Subtitusikan untuk mendapatkan nilai R
Sehingga diperoleh
Subtitusikan untuk mendapatkan nilai
↔
Sehingga diperoleh
Subtitusikan , , untuk mendapatkan
nilai
Sehingga diperoleh titik tetap sebagai berikut: , , ,
, , ,
Lampiran 5 Penentuan nilai eigen pada titik tetap
Misalkan persamaan (3.4), (3.5), (3.6), dan (3.7) dituliskan sebagai berikut:
B
C
Dengan melakukan pelinieran didapat matriks Jacobi sebagai berikut:
• Pelinieran titik tetap , , , akan diperoleh matriks Jacobi sebagai berikut:
:
Jadi nilai eigennya sebagai berikut:
Lampiran 6 Perintah Mathematica untuk menentukan titik tetap dan nilai eigen model modifikasi
Lampiran 7 Perintah Mathematica untuk gambar a. Gambar 3
[image:69.595.97.479.80.799.2]h. Gambar 10
ELIS LISTIANDINI. A Mathematical Model of the Dynamics of Glucose, Insulin, β-cells Mass, and Insulin Receptors in Diabetes Mellitus Disease Type 2. Supervised by PAIAN SIANTURI and ALI KUSNANTO.
The diabetes mellitus is a disease in glucose-insulin regulatory system, which is referred to as hyperglikemia. Most cases are categorized as type 2 of the diabetes mellitus (T2DM), which are characterized by high blood glucose levels. The T2DM is associated with a deficit in the mass of β-cells. If the blood glucose consentration level is high, then the β-cells release insulin into the pancreas. The aim of this research is to study the glucose-insulin dynamics. A βIG model was proposed to describe the glucose-insulin dynamics. This model provide a pathway for diabetes development through the introduction of a 3rd dynamical variable, the β-cell mass. The addition of insulin receptor is an important factor in this quantitative improvement in order to make the model more realistic. Incorporation of the insulin receptor into the existing mathematical model gives a four dimensional system of nonlinear ordinary differential equations, which is introduced as the modified model. Both of the models have two stable equilibria representing physiological steady state and pathological steady state. Furthermore the third steady state is found to be a saddle point. Nevertheless the average mass of β-cell in the modified model is quantitatively more reasonable and therefore better then βIG models.
IPENDAHULUAN
1.1 Latar BelakangDiabetes melitus adalah suatu penyakit gangguan kesehatan dimana kadar gula darah seseorang menjadi tinggi karena gula dalam darah tidak dapat digunakan oleh tubuh. Diabetes mekitus dikenal juga dengan sebutan penyakit gula darah atau kencing manis. Diabetes terjadi jika tubuh tidak menghasilkan insulin yang cukup untuk mempertahankan kadar gula darah yang normal atau jika sel tidak memberikan respon yang tepat terhadap insulin. Terdapat dua tipe diabetes melitus yaitu: diabetes melitus tipe 1(DMT1) dimana tubuh kekurangan hormon insulin karena serangan autoimun pada sel-β, dan diabetes mellitus tipe 2 (DMT2) dimana hormon insulin dalam tubuh tidak dapat berfungsi dengan semestinya.
Sebagian besar kasus adalah DMT2 yang disebabkan faktor obesitas, dan pola hidup tidak sehat.Individu yang terkena DMT2 cenderung memiliki sensitivitas insulin yang rendah dan tingkat resistansi insulin yang tinggi.Resistansi insulin sangat berhubungan dengan kemampuan tubuh yang rendah terhadap tingkat pengaturan reseptor insulin.Reseptor insulin merupakan protein pada permukaan sel yang mengikat insulin. Pada DMT2 massa sel-β terlalu bekerja keras karena kadar gula yang tinggi sehingga terjadi kelelahan yang menyebabkan penurunan produktivitas massa sel-βdan sekresi insulin berkurang. Kekurangan insulin dapat menyebabkan berkurangnya tingkat penyerapan glukosa oleh tubuh.
Penelitian tentang penyakit diabetes telah banyak dilakukan, salah satunya adalah Topp et al. (2000) yang memodelkan dinamika glukosa-insulin.Model ini menggabungkan model Bergmanet al. (1979) dengan laju perubahan massa sel-β, dan memberikan jalur untuk terbentuknya diabetes.Model Topp atau disebut juga model βIG ini telah banyak dikembangkan oleh ilmuwan lain.
Dari beberapa perkembangan model, model Ryan et al. (2001) atau disebut juga model modifikasi yang mengkoreksi model βIG dengan cara menambahkan variabel dinamika reseptor insulin.Dalam tulisan iniakan ditunjukkan lebih jelas bagaimana reseptor insulin menjalani fungsinya pada penderita dengan resistansi insulin yaitu penderita dengan kemampuan pengaturan reseptor insulin yang rendah.
Jalur yang berbeda untuk membangun diabetes dimana dengan melibatkan peningkatan pada resistansi insulin yang disebabkan sekresi insulin, yang bebas dari massa sel-β telah memperkuat penelitian sebelumnya. Revisi yg dilakukan menunjukkan pendekatan bahwa solusi sistem menunjukkan massasel-β dapat mencapai nol, yaitupendekatan untuk penyakit diabetes (Mason 2006).
Perkembangan selanjutnya pendekatan secaraFarmakoKinetik-FarmakoDinamik Mekanistik (PK-PD) yang menggabungkan model konsentrasi glukosa saat puasa, konsentrasi insulin saat puasa, sensitivitas insulin dan massa sel-β, yang menjelaskan pasien pada berbagai tahap penyakit, dari non-diabetes sampai resistansi insulin jangka panjang pada pasien DMT2, dan menggabungkan dampak pengobatan terhadap keempat variabel dilakukan olehRibbing et al. (2008).
1.2 Tujuan Penelitian
Tujuan utama dari penulisan karya ilmiah ini adalah: 1 Mengkaji kestabilan model βIG dan model modifikasi.
2 Membandingkan dinamika model βIGdengan model modifikasi.
IITINJAUAN PUSTAKA
2.1 Sistem Persamaan Diferensial (SPD)Definisi 1 SPD Linear
Jika suatu Sistem Persamaan Diferensial (SPD) dinyatakan sebagai berikut:
, , (2.1)
dengan adalah matriks koefisien berukuran x dan vektor konstan , maka sistem tersebut dinamakan SPD linear orde 1 dengan kondisi awal
. Sistem (2.1) disebut homogen jika dan non homogen, jika .
(Tu 1994)
Definisi 2 Sistem Persamaan Diferensial Tak Linear Misalkan diberikan SPD sebagai berikut:
, (2.2) dengan
dan ,
, , , ,
, , , , diasumsikan fungsi tak linier
pada , , , .Sistem (2.2) disebut SPD tak linear.
(Braun 1983)
Definisi 3 Sistem Persamaan Diferensial Mandiri
Misalkan suatu SPD dinyatakan sebagai berikut:
, , (2.3)
dengan merupakan fungsi kontinu bernilai real dari dan mempunyai turunan parsial kontinu. Sistem (2.3) disebut sistem persamaan diferensial mandiri
(autonomous) karena tidak memuat t secara eksplisit di dalamnya.
2.2 Titik Tetap Definisi 4Titik Tetap
Misalkan diberikan sistem persamaan diferensial mandiri (2.3). Titik disebut titik tetap atau titik kritis atau titik kesetimbangan jika .
(Tu 1994)
Definisi 5Titik Tetap Stabil
Misalkan adalah titik tetap sebuah persamaan diferensial dan adalah solusi dengan kondisi awal , dimana .Titik dikatakan titik tetap stabil, jika untuk setiap , terdapat , sedemikian sehingga| | ,
maka | | untuk .
(Verhulst 1990)
2.3 Nilai Eigen dan Vektor Eigen
Jika A adalah matriks , maka sebuah vektor taknol di dalam disebut vektor eigen dariA, jika A adalah sebuah kelipatan skalar dari ; jelasnya:
A (2.4) Untuk skalar sembarang . Skalar disebut nilai eigendari A, dan disebut sebagai vektor eigen dari A terkait dengan .
Untuk memperoleh nilai eigen dari sebuah matriks , persamaan (2.4) dapat ditulis kembali sebagai
(2.5) Dengan matriks identitas. Persamaan (2.5) mempunyai solusi tak nol jika dan hanya jika
det | | (2.6) Persamaan (2.6) disebut persamaan karakteristik dari matriks , skalar-skalar yang memenuhi persamaan ini adalah nilai-nilai eigen A.
2.4 Analisis Kestabilan Titik Tetap
Diberikan sistem persamaan diferensial sembarang
,
Analisis kestabilan titik tetap dilakukan melalui matriks Jacobi darimatriks . Penentuan kestabilan titik tetap diperoleh dengan melihat nilai-nilai eigennya, yaitu dengan , ,3, … , yang diperoleh dari det . Secara umum, kestabilan titik tetap mempunyai tiga perilaku sebagai berikut:
1. Stabil, jika
a. Setiap nilai eigen real bernilai negatif ( untuk semua ,
b. Setiap bagian real dari nilai eigen kompleks bernilai lebih kecil atau sama dengan nol untuk semua .
2. Tak stabil, jika
a. Setiap nilai eigen real bernilai positif untuk semua ,
b. Setiap bagian real dari nilai eigen kompleks bernilai lebih besar atau sama dengan nol untuk semua .
c. Sadel, jika perkalian dari kedua nilai eigen real sembarang adalah negatif , untuk semua dan sembarang. Titik tetap sadel ini bersifat tak stabil.
(Tu 1994)