KERAGAMAN CENDAWAN Botryodiplodia theobromae
DARI BERBAGAI TANAMAN INANG
BERDASARKAN MORFOLOGI DAN POLA RAPD
FITRI KEMALA SANDRA
A34063054
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
ABSTRAK
FITRI KEMALA SANDRA. Keragaman Cendawan Botryodiplodia theobromae
dari Berbagai Tanaman Inang Berdasarkan Morfologi dan Pola RAPD. Dibimbing oleh KIKIN HAMZAH MUTAQIN dan SURYO WIYONO.
Cendawan Botryodiplodia theobromae Pat. menjadi penyebab penyakit pada berbagai tanaman serta memiliki kisaran inang yang luas yang dapat menurunkan kualitas maupun kuantitas produksi tanaman.
Variabilitas gejala penyakit dan kisaran inang yang dimiliki oleh cendawan ini menunjukkan bahwa mungkin terdapat keragaman dalam karakter morfologi maupun molekulernya. Pendekatan terhadap karakter morfologi cendawan B. theobromae dilakukan berdasarkan pengamatan bentuk, ukuran, dan warna dari struktur hifa, konidia, dan piknidia. Hasil pengamatan cendawan B. theobromae secara morfologi dapat dikonfirmasi menggunakan metode molekuler dengan teknik Random Amplified Polymorphic DNA (RAPD) untuk menganalisis keragaman genetiknya.
Penelitian bertujuan untuk membandingkan keragaman morfologi dan pola DNA molekuler berdasarkan teknik RAPD dari isolat B. theobromae yang diperoleh dari berbagai tanaman inang.
Sebanyak lima isolat B. theobromae yang diperoleh dari Klinik Tanaman, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor yang berasal dari tanaman dari berbagai daerah, yaitu Jeruk dari Jember, Jawa Timur; Karet dari Pematang Siantar, Sumatra Utara; Pisang dari Bogor, Jawa Barat; Manggis dari Bukit Tinggi, Sumatra Barat; dan Kakao diperoleh dari Taman Nasional (TN) Lorelindu, Sulawesi Tengah berdasarkan pengamatan morfologi mempunyai penampilan koloni dan morfologi cendawan yang bervariasi baik dari segi bentuk maupun ukuran; hifa, miselium, konidia, dan piknidia. Piknidia yang ditumbuhkan pada media Potato Dextrose Agar (PDA) terbentuk pada isolat asal jeruk dan isolat asal karet sedangkan pada media Water Agar (WA) yang diberi bahan induksi berupa potongan jerami terbentuk pada semua isolat kecuali isolat asal manggis. Piknida isolat asal manggis hanya dapat terbentuk pada media WA yang diberi bahan induksi berupa kulit manggis. Hal ini menunjukkan bahwa dalam pembentukan piknidia diperlukan nutrisi tertentu agar dapat memaksimumkan pembentukannya.
KERAGAMAN CENDAWAN Botryodiplodia theobromae
DARI BERBAGAI TANAMAN INANG
BERDASARKAN MORFOLOGI DAN POLA RAPD
FITRI KEMALA SANDRA
A34063054
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Pertanian
pada Fakultas Pertanian, Institut Pertanian Bogor
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
Judul Skripsi : Keragaman Cendawan Botryodiplodia theobromae dari Berbagai Tanaman Inang Berdasarkan Morfologi dan Pola RAPD
Nama Mahasiswa : Fitri Kemala Sandra
NRP : A34063054
Menyetujui,
Pembimbing I Pembimbing II
Dr. Ir. Kikin H. Mutaqin, MSi Dr. Ir. Suryo Wiyono MSc.Agr NIP. 19680602 199303 1003 NIP. 19690212 199203 1003
Mengetahui,
Ketua Departemen Proteksi Tanaman
RIWAYAT HIDUP
Penulis dilahirkan di Bandung, Jawa Barat pada tanggal 10 Januari 1988 sebagai anak ke-8 dari delapan bersaudara dari pasangan Bapak Kosih Sandra Djuhara dan Ibu Dewi Setiawaty.
Pendidikan yang ditempuh mulai dari Sekolah Dasar Negeri Kayu Ambon 1 Kecamatan Lembang Kabupaten Bandung pada tahun 1994-2000, dilanjutkan di Sekolah Menengah Pertama Negeri 12 Bandung pada tahun 2000-2001 kemudian berpindah sekolah ke Sekolah Menengah Pertama Negeri 1 Baleendah Kabupaten Bandung pada tahun 2001-2002. Pada tahun 2003 penulis melanjutkan pendidikan di Sekolah Menengah Atas Negeri 11 Bandung dan lulus pada tahun 2006. Pada tahun 2006 penulis diterima di Institut Pertanian Bogor melalui jalur Seleksi
Penerimaan Mahasiswa Baru (SPMB). Pada tahun 2007 penulis diterima di Departemen Proteksi Tanaman, Fakultas Pertanian.
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT atas limpahan nikmat dan karunia-Nya penulis dapat menyelesaikan skripsi yang berjudul “Keragaman Cendawan Botryodiplodia theobromae dari Berbagai Tanaman Inang Berdasarkan Morfologi dan Pola RAPD”. Skripsi ini disusun untuk memenuhi salah satu syarat untuk memperoleh gelar sarjana pada Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor.
Penulis menyampaikan terimakasih sebesar-besarnya kepada Dr. Ir. Kikin H. Mutaqin, MSi., Dr. Ir Suryo Wiyono MSc.Agr. sebagai Dosen Pembimbing Tugas Akhir, Dr. Ir. Idham Sakti Harahap, MSi. sebagai Dosen Penguji Tamu, dan Dr. Ir. Nina Maryana, MSi. sebagai Dosen Pembimbing Akademik.
Penulis mengucapkan terima kasih kepada Pak Dadang (Laboran
Laboratorium Mikologi) dan Bu Ita (Staf Klinik Tanaman Departemen Proteksi Tanaman) atas semua bantuannya. Terimakasih kepada Aisah, Eka, Yeyen, Weni, Dedek, Arni, Eva, Alvian, Rodiah, Oci atas doa dan dukungannya, dan mahasiswa Departemen Proteksi Tanaman angkatan 43 atas semua dukungan dan bantuannya. Penulis menyampaikan terima kasih yang sebesar-besarnya kepada ayahanda yang telah berpulang ke rahmatullah, ibunda tercinta, Teh Rina, Teh Novi, Aulya Rachman, Aulya Rachim, dan Teh Lia juga seluruh keluarga besar di kampung halaman atas do’a dan dorongan yang telah diberikan.
Bogor, Maret 2011
DAFTAR ISI
Nilai Ekonomi Cendawan Botryodiplodia theobromae ... 3
Gejala Penyakit Blendok pada Berbagai Tanaman ... 3
Gejala pada tanaman jeruk ... 3
Karakterisasi Morfologi Cendawan B. theobromae ... 11
Penyiapan isolat cendawan ... 11
Peremajaan dan Isolasi ... 11
Pengamatan morfologi ... 12
Analisis data ... 12
Deteksi Molekuler Menggunakan Teknik RAPD-PCR ... 12
Ekstraksi DNA cendawan ... 12
RAPD-PCR ... 13
Elektrophoresis Hasil RAPD-PCR ... 13
HASIL DAN PEMBAHASAN ... 15
Karakter Morfologi B. theobromae ... 15
Karakter Molekuler B. theobromae... 22
KESIMPULAN DAN SARAN ... 26
Kesimpulan ... 26
Saran ... 26
DAFTAR PUSTAKA ... 27
ix DAFTAR GAMBAR
Halaman
1. Piknidia dan konidia cendawan B. theobromae ... 7 2. Peralatan elektroforesis. A. Gel tray, B. Cara mencetak gel agarose. C.
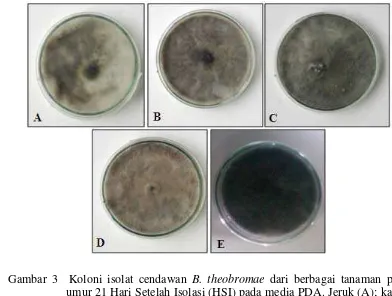
Peralatan lengkap untuk elektroforesis. ... 14 3. Koloni isolate cendawan B. theobromae ... 15 4. Grafik pertumbuhan koloni cendawan B. theobromae pada
media PDA. ... 16 5. Morfologi hifa dan klamidospora pada manggis ... 17 6. Piknidia B. theobromae yang terbentuk pada media WA + jerami padi dan
WA + kulit manggis ... 18 7. Piknidia yang pecah mengeluarkan konidia (pewarnaan dengan laktofenol)
pada isolat B. theobromae ... 18 8. Konidia muda isolat cendawan B. theobromae ... 22 9. Konidia matang isolat cendawan B. theobromae ... 22
10. Profil DNA lima isolat cendawan yang diamplifikasi dengan RAPD-PCR menggunakan primer OPB 01 ... 24 11. Profil DNA lima isolat cendawan yang diamplifikasi dengan RAPD-PCR
DAFTAR TABEL
Halaman
1. Pembentukan Piknidia cendawan B. theobromae pada berbagai media . 19 2. Ukuran panjang, lebar, dan tebal dinding konidia muda cendawan B.
theobromae pada lima tanaman inang ... 20 3. Ukuran panjang dan lebar konidia matang cendawan B. theobromae pada
tiga tanaman inang ... 21 4. Ukuran fragmen DNA cendawan B. theobromae menggunakan
primer OPB 01 ... 24 5. Ukuran fragmen DNA cendawan B. theobromae menggunakan
PENDAHULUAN
Latar Belakang
Penyakit yang disebabkan oleh Botryodiplodia theobromae (Patouillard) Griffon dan Maublanc ditemukan pada lebih dari 280 genus tanaman inang yang berbeda di daerah tropis dan subtropis di dunia (Nunes etal. 2008). Kisaran inang cendawan B. theobromae sangat luas, sehingga sumber infeksi selalu ada. Ekundayo (1978) menyebutkan bahwa B. theobromae dapat menyerang tanaman pisang, kakao, karet, kelapa, dan kelapa sawit.
Cendawan B. theobromae dilaporkan telah menyebabkan berbagai penyakit diantaranya mati ujung, busuk akar, busuk buah, bercak daun, dan sapu setan (Punithalingam 1980). Pada jeruk, B. theobromae menyebabkan kematian cabang, pada kakao dapat menyebabkan mati pucuk, busuk buah, dan kanker batang, pada karet menyebabkan mati pucuk, pada pisang dan manggis cendawan
B. theobromae dapat menyebabkan busuk buah. Cendawan B. theobromae
dianggap sebagai masalah serius bagi pertanian karena hal ini terkait dengan penyebab beberapa penyakit pada buah-buahan tropis (Nunes et al. 2008).
menggunakan suatu primer acak yang tidak didasarkan pada organisme tertentu dengan desain berupa primer tunggal yang pendek. Analisis keragaman genetik dilakukan terhadap cendawan B. theobromae untuk mengetahui apakah B. theobromae dari berbagai tanaman itu memiliki kesamaan atau perbedaan genetik.
Informasi tentang perbedaan morfologi dan genetik cendawan B. theobromae belum tersedia banyak di Indonesia. Oleh karena itu dilakukan penelitian tentang keragaman cendawan B. theobromae dari berbagai tanaman inang secara morfologi dan melalui analisis RAPD.
Tujuan Penelitian
Penelitian bertujuan untuk membandingkan keragaman morfologi dan pola DNA molekuler berdasarkan RAPD isolat-isolat B. theobromae dari berbagai tanaman inang.
Manfaat Penelitian
Penelitian ini diharapkan mampu memberikan informasi tentang karakter morfologi dan molekuler B. theobromae dari berbagai tanaman inang.
Hipotesis
Hipotesis yang disusun dalam penelitian ini adalah
1. Isolat Botryodiplodia theobromae dari berbagai tanaman tidak dapat dibedakan secara morfologi.
TINJAUAN PUSTAKA
Nilai Ekonomi Cendawan Botryodiplodia theobromae
B. theobromae dilaporkan telah menyebabkan berbagai penyakit diantaranya mati ujung, busuk akar, busuk buah, bercak daun, dan sapu setan (Punithalingam 1980). Pada jeruk, B. theobromae menyebabkan kematian cabang, pada kakao dapat menyebabkan mati pucuk, busuk buah, dan kanker batang, pada karet menyebabkan mati pucuk, pada pisang dan manggis cendawan B. theobromae dapat menyebabkan busuk buah.
Di pulau Jawa, cendawan B. theobromae mempunyai arti penting terutama di daerah dataran rendah. Jenis jeruk keprok (Citrus nobilis) dan jeruk besar (Citrus grandis) sering sangat menderita karena serangannya. Di Kabupaten Magetan sekitar 500 ha pertanaman jeruk besaryaitu 85% dari jumlah pohon telah
terserang oleh cendawan ini dengan tingkat serangan ringan sampai sedang (22 - 37%) (Wiratno dan Nurbanah 1997). Serangan juga terjadi di Kamerun pada tahun 1985 pada kakao dan menjadi faktor pembatas produksi kakao (Mbenoun et al. 2008). Pohon karet di Vietnam tahun 1921 terdeteksi terserang cendawan ini dan menjadi wabah pertama pada tahun 1998 di daerah penanaman karet tradisional di Vietnam (Pha et al. 2010). B. theobromae telah diketahui menyerang pada pisang sejak 1931 dan mampu menyebabkan pembusukan cepat buah pisang di gudang (Goos et al. 1961). Di Brasil, cendawan ini dianggap sebagai masalah utama bagi pertanian karena hal ini terkait dengan beberapa penyakit buah-buahan tropis (Nunes et al. 2008).
Gejala Penyakit Blendok pada Berbagai Tanaman Gejala pada tanaman jeruk (penyakit kulit diplodia)
ke dalam kulit kayu, merusak kambium, kemudian cabang digelang dan mati. Serangan patogen dengan gejala seperti ini disebut diplodia basah. Pada diplodia kering lebih berbahaya, karena gejala permulaan sulit diketahui. Infeksi baru diketahui jika daun telah menguning sehingga cabang yang sakit tidak dapat tertolong. Kulit mengering, dan jika dipotong, kulit dan kayu di bawahnya berwarna hitam kehijauan. Kulit yang sakit membentuk celah-celah kecil, dari dalamnya keluar massa spora yang semula berwarna putih, tetapi akhirnya berwarna hitam (Semangun 2007). B. theobromae tumbuh secara saprofit di kayu mati untuk meningkatkan potensi inokulum sebelum dapat menyebabkan kerusakan yang signifikan pada jaringan sehat (Davis et al. 1987).
Gejala pada tanaman kakao (penyakit botryodiplodia)
Cendawan B. theobromae berperan sebagai parasit lemah pada cabang dan ranting. Cendawan ini hanya dapat menginfeksi jaringan-jaringan yang lemah, atau menjadi patogen sekunder, atau menginfeksi melalui luka-luka karena serangga. Botryodiplodia dapat menyebabkan mati pucuk, busuk buah, dan kanker
batang (Semangun 2000).
Gejala pada tanaman karet
Gejala awal ditandai dengan terbentuknya pustul secara sporadis dan kemudian mereka menyatu menjadi lesio luas pada batang karet. Infeksi berat menyebabkan perdarahan pada lateks, retak, kulit membusuk dan gumosis. Pada tanaman yang masih muda, infeksi awal pada tunas muda berupa lesio kecil berwarna cokelat gelap, menyebar cepat, kemudian kulit membusuk, bagian daun yang terinfeksi menjadi kuning karena kurangnya pasokan gizi dan air. Infeksi yang parah menyebabkan kematian pada ranting mulai dari ujung (mati pucuk) (Pha et al. 2010).
Gejala pada tanaman pisang (busuk buah)
5
apabila buah mulai matang spora akan berkecambah dan mengadakan infeksi. Gejala mulai timbul pada tangkai buah kemudian meluas ke seluruh bagian buah. Gejala yang timbul yaitu buah menjadi lunak dan berair, serta mengeluarkan bau (aroma) yang khas. B. theobromae menyebabkan busuk ujung buah (tip rot),
busuk telapak, dan busuk pangkal. Penyakit ini merusak buah pisang yang matang dalam pengangkutan atau simpanan (Semangun 2007).
Gejala pada tanaman manggis
Penyakit busuk buah manggis menunjukkan gejala awal berupa kerak atau burik pada buah muda. Burik berwarna cokelat, pecah-pecah, dan mengeluarkan getah berwarna kuning. Burik biasanya berawal dari ujung buah, lalu menjalar kearah sepal atau sebaliknya (AgroMedia 2009). Kulit tampak kehitaman dan mengkilat kemudian menjadi burik karena cendawan membentuk banyak piknidium yang menghasilkan konidium (Semangun 2007).
Pengendalian Penyakit B. theobromae
Bentuk kegiatan pengendalian penyakit B. theobromae dapat dilakukan
Taksonomi & Morfologi Cendawan B. theobromae Taksonomi Cendawan B. theobromae
Menurut Semangun (2007) penyakit kulit diplodia disebabkan oleh cendawan Botryodiplodia theobromae Pat., yang dulu banyak dikenal dengan nama Diplodia natalensis P. Evans. Klasifikasi B. theobromae adalah (Alexopoulos 1960) :
Kingdom : Fungi
Phylum : Deuteromycota Kelas : Deuteromycetes Ordo : Sphaeropsidales Famili : Sphaeropsidaceae Genus : Botryodiplodia
Spesies : Botryodiplodia theobromae
Morfologi Cendawan B. theobromae
Botryodiplodia theobromae (Pat.) merupakan sinonim dari Lasiodiplodia theobromae (Pat.) Griff. & Maubl. yang memiliki perkembangbiakan secara
aseksual dari genus Botryosphaeria rhodina (Berk. & MA Curtis) ARX (Mohali 2005). Lasiodiplodia theobromae adalah bentuk anamorf dari Botryosphaeria rhodina (Berkeley & Curtis) von ARX dan sebagai cendawan yang memiliki kelas deuteromycetes (Nunes 2008).
Punithalingam (1976) menyebutkan bahwa karakter morfologi cendawan
B. theobromae ditandai dengan pertumbuhan miselia dari isolat B. theobromae
seperti benang rambut halus atau kapas, miselium udara berlimpah. Koloni mula-mula berwarna sepia berubah menjadi abu-abu kemudian menjadi hitam. Piknidia sederhana, bergerombol, sering agregat, stromatik, ostiolate, lebar sampai dengan 5 mm. Konidia awalnya uniseluler, hialin, granulosa, subovoid sampai ellipsoid-ooblong, berdinding tebal, memotong seperti sekat; konidia matang uniseptate, coklat seperti warna kayu manis, berukuran 20-30 µm x 10-15 µm.
7
µm x 15 µm, eksosporanya mempunyai jalur-jalur (Semangun 2007). Berbeda dengan pada jeruk, pembentukan piknidium cendawan B. theobromae pada kakao memerlukan cahaya. Piknidium berukuran 135 - 230 µm x 95 - 155 µm. konidium (piknidiospora) mula-mula berwarna coklat muda dan tidak bersekat, tetapi menjelang dilepaskan coklat tua dengan satu sekat melintang, dengan dinding spora sekunder. Konidium berukuran 24 - 30 µm x 11.5 - 13.5 µm, keluar melalui lubang ostiol seperti masa lengket berwarna putih sampai coklat muda. (Semangun 2000). Botryodiplodia theobromae pada pisang memiliki konidia berbentuk elips, mula-mula hialin dan uniseluler kemudian menjadi coklat dan bersekat tunggal. Konidia berukuran 20-30 µm x 10-18 µm (Goos et al. 1961).
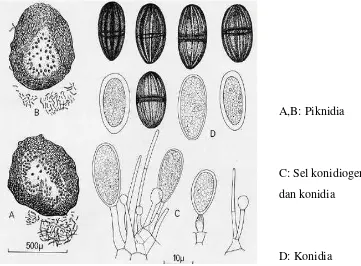
Gambar 1 Piknidia dan konidia cendawan B. theobromae (Punithalingam 1976).
Pavlic etal. (2004) dalam penelitiannya menemukan ciri umum pada isolat
B. theobromae yang berasal dari Amerika Serikat, Amerika Selatan, Afrika Selatan dan Asia memiliki konidia berukuran 18–30 x 10–15 µm.
Polymerase Chain Reaction (PCR)
Reaksi berantai polymerase (Polymerase Chain Reaction, PCR) adalah metode enzimatis untuk melipatgandakan secara eksponensial suatu sekuen
A,B: Piknidia
C: Sel konidiogen dan konidia
nukleotida tertentu secara in vitro. Metode PCR sangat sensitif. Sensitivitas tersebut membuatnya dapat digunakan untuk melipatgandakan satu molekul DNA. Dengan metode PCR, dapat diperoleh pelipatgandaan suatu fragmen DNA sebesar 200.000 kali setelah dilakukan 20 siklus reaksi selama 220 menit. Hal ini menunjukkan bahwa pelipatgandaan suatu fragmen DNA dapat dilakukan secara cepat. Kelebihan lain metode PCR adalah bahwa reaksi ini dapat dilakukan dengan menggunakan template DNA dalam jumlah sangat sedikit (Yuwono 2006).
Prosedur reaksi PCR terdiri dari tiga tahap yaitu denaturasi, annealing (penempelan primer) dan ekstensi (sintesis DNA). Reaksi PCR ditentukan oleh kondisi suhu, denaturasi template, primer, annealing (penempelan primer) dan ekstensi (sintesis DNA). Pada langkah pertama, denaturasi template DNA untai ganda pada suhu 90-95 °C. Kemudian suhu diturunkan hingga sekitar 55 °C, primer menempel ke ujung 5 pada template yang telah terpisah menjadi untai tunggal. Untuk langkah ekstensi, suhu dinaikkan menjadi 72 °C dan primer-target berfungsi sebagai titik awal untuk sintesis DNA baru. Waktu untuk setiap langkah
biasanya 1-2 menit. Tiga langkah berurutan ini disebut sebagai satu siklus PCR. Pada siklus kedua, untai DNA yang baru disintesis dipisahkan dari untai asal oleh denaturasi dan masing-masing untai berfungsi lagi sebagai template dalam penempelan dan ekstensi. Secara teoritis, siklus PCR memungkinkan amplifikasi 2n kali lipat DNA target. Biasanya PCR dilakukan sebanyak 30-40 siklus. Namun banyaknya siklus tergantung pada konsentrasi DNA target didalam campuran reaksi (Edel 1998).
Random Amplified Polymorphic DNA Polymerase Chain Reaction (RAPD-PCR)
Random Amplified Polymorphic DNA (RAPD) merupakan salah satu teknik molekuler berupa penggunaan penanda tertentu untuk mempelajari keanekaragaman genetika. Dasar analisis RAPD adalah menggunakan mesin PCR yang mampu mengamplifikasi sekuen DNA secara in vitro. Teknik ini melibatkan penempelan primer tertentu yang dirancang sesuai dengan kebutuhan. Tiap primer
9
fragmen DNA yang diseleksi dengan menggunakan satu primer arbitrasi, terutama karena amplifikasi DNA secara in vitro dapat dilakukan dengan baik dan cepat dengan adanya PCR. Penggunaan penanda RAPD relatif sederhana dan mudah dalam hal penyiapannya. Teknik RAPD memberikan hasil yang lebih cepat dibandingkan dengan teknik molekuler lainnya. Teknik ini juga mampu menghasilkan jumlah karakter yang relatif tidak terbatas, sehingga sangat membantu untuk keperluan analisis keanekaragaman organisme yang tidak diketahui latar belakang genomnya. Teknik RAPD sering digunakan untuk membedakan organisme tingkat tinggi (eucaryote). Namun demikian beberapa peneliti menggunakan teknik ini untuk membedakan organisme tingkat rendah (procaryote) atau melihat perbedaan organisme tingkat rendah melalui piranti organel sel seperti mitokondria (Suryanto 2003).
Menurut WSSP (2009) RAPD PCR memiliki keterbatasan diantaranya hampir semua penanda RAPD adalah dominan karena tidak mampu membedakan apakah suatu segmen DNA dari lokus yang heterozigot (1 salinan) atau homozigot (2 salinan). PCR adalah reaksi enzimatik, sehingga kualitas dan konsentrasi DNA
template, konsentrasi komponen PCR, dan kondisi siklus PCR dapat sangat mempengaruhi hasil dari amplifikasi DNA. Ketidaksesuaian antara primer dan DNA template dapat berpengaruh terhadap total produk PCR serta penurunan dalam jumlah produk sehingga mengakibatkan hasil RAPD sulit diinterpretasikan.
Penggunaan RAPD-PCR dalam Analisis DNA Cendawan
Teknik RAPD-PCR memanfaatkan primer acak oligonukleotida pendek (dekamer) untuk mengamplifikasi DNA genom organisme. Prinsip teknik RAPD didasarkan pada kemampuan primer menempel pada DNA template. Primer yang didesain berupa primer tunggal pendek agar dapat menempel secara acak pada DNA genom organisme. Dengan demikian akan terdapat banyak pola fragmen DNA. Perbedaan ini dapat dilihat dengan adanya pola pita pada gel agarosa setelah diwarnai dengan pewarnaan DNA seperti seperti etidium bromide (Sambrook et al. 1989).
BAHAN DAN METODE
Tempat dan Waktu
Penelitian dilakukan di Laboratorium Mikologi Tumbuhan dan
Laboratorium Bakteriologi Tumbuhan Departemen Proteksi Tanaman, Fakultas
Pertanian, Institut Pertanian Bogor. Penelitian ini berlangsung mulai bulan
Februari 2010 sampai November 2010.
Karakterisasi Morfologi Cendawan B. theobromae
Penyiapan isolat cendawan
Isolat cendawan B. theobromae diperoleh dari Klinik Tanaman yang
berasal dari tanaman di berbagai daerah antara lain Jeruk dari Jember, Jawa
Timur; Karet dari Pematang Siantar, Sumatera Utara; Pisang dari Bogor, Jawa
Barat; Manggis dari Bukit Tinggi, Sumatera Barat (koleksi Dr. Ir. Suryo Wiyono
MSc.Agr); dan Kakao diperoleh dari Taman Nasional (TN) Lorelindu, Sulawesi
Tengah (koleksi Efi Toding Tondok SP.MSc.Agr).
Peremajaan dan Isolasi
Inokulum B. theobromae ditanam dalam media Potato Dextrose Agar
(PDA) dan Water Agar (WA) yang diberi potongan jerami padi, pelepah pisang
yang kering, kulit manggis steril dengan ukuran ± 0,5 cm kemudian diinkubasi
dalam suhu ruang selama kurang lebih tujuh hari. Konfirmasi cendawan dilakukan
terhadap isolat yang telah diremajakan dengan menggunakan kunci identifikasi
Barnett dan Hunter (1999).
Penyiapan preparat
Cendawan B. theobromae yang tumbuh dibuat preparat menggunakan
gelas objek, gelas tutup, dan laktofenol. Selanjutnya diamati dibawah mikroskop
cahaya dan dipotret dengan menggunakan kamera digital.
Pengamatan Morfologi
Pengamatan koloni cendawan yang tumbuh dilakukan setiap hari selama
tujuh hari sejak 1 Hari Setelah Isolasi (HSI) terhadap bentuk, warna, dan diameter
koloni pada media PDA. Pengamatan dibawah mikroskop cahaya dilakukan
terhadap struktur cendawan berupa hifa, piknidia, dan konidia sampai dengan 34
HSI.
Analisis data
Data tentang ukuran konidia dan rasio panjang/lebar diolah dengan analisis
ragam menggunakan program SAS ver. 9.1 dan dilanjutkan dengan uji
perbandingan nilai tengah Duncan's Multiple Range Test (DMRT) untuk peubah
pengamatan ukuran konidia dan rasio panjang/lebar.
Deteksi Molekuler Menggunakan Teknik RAPD-PCR
Deteksi molekuler DNA cendawan dengan teknik RAPD-PCR meliputi
tiga tahap kegiatan, yaitu ekstraksi DNA cendawan, RAPD-PCR, dan
elektroforesis hasil RAPD-PCR.
Ekstraksi DNA Cendawan
Ekstraksi DNA dilakukan untuk menyiapkan DNA template dalam PCR.
Ektraksi DNA cendawan dilakukan dengan menggunakan metode ekstraksi yang
digunakan Moller et al. (1992). Miselium cendawan B. theobromae dan
Rhizoctonia sp. (kontrol) yang telah ditumbuhkan di media PDA digunakan
sebanyak 0,1 gram. Miselium ditumbuk dalam mortar yang sebelumnya
didinginkan dalam freezer dan ditambahkan 600 µl TES (100 mm Tris, pH 8, 10
mM EDTA, 2% SDS) kemudian diinkubasi selama 30 menit pada suhu 60 oC
dengan melakukan pencampuran secara perlahan setiap 10 menit sekali.
Konsentrasi garam diatur sampai 1,4 M dengan menambahkan 5 M NaCl (=140
µl) kemudian ditambahkan CTAB 10% sebanyak 65 µl 1/10 vol dan
diinkubasikan selama 10 menit pada suhu 65 oC. Secara perlahan ditambahkan 1
vol SEVAG (Isoamyl alcohol, Chloroform dengan perbandingan 1:24) sebanyak
700 µl lalu diinkubasi selama 30 menit, pada suhu 0 oC, kemudian disentrifuse
13
dalam tabung 1,5 µl, kemudian ditambahkan sebanyak 225 µl NH4Ac dengan
konsentrasi 5 M, selanjutnya dicampurkan secara perlahan. Tabung dimasukkan
ke dalam kulkas selama 30 menit, kemudian disentrifus selama 10 menit, 4 oC,
12000 rpm. Supernatan dipindahkan ke tabung baru kemudian ditambahkan
isopropanol 0,55 volume (= 510 µl) untuk mengendapkan DNA, lalu dimasukkan
ke dalam freezer selama 15 menit selanjutnya suspensi disentrifuse selama 5
menit, 4 oC, 12000 rpm. Supernatan yang telah disentrifuse dibuang untuk
diperoleh peletnya. Pelet dicuci dua kali dengan etanol dingin 70%, kemudian
diperoleh pelet kering dan dilarutkan dalam sekitar 50 µl Buffer TE. Pelet
disimpan untuk selanjutnya digunakan dalam proses RAPD-PCR.
RAPD-PCR
PCR disiapkan terpisah untuk masing-masing primer (OPB01 dan OPB07)
dalam total volume 25 μl/reaksi. Air sebanyak 16,2 µl dicampurkan dengan buffer PCR 10 + Mg2+ sebanyak 2,5 µl, MgCl 2+ dengan konsentrasi 25 µm sebanyak 0,5
µl, dNTPs 2 mM sebanyak 2,5 µl, primer 10 µM/µl, dan Taq DNA 5U/µl
sebanyak 0,5 µl. Template DNA yang telah dilarutkan dalam buffer TE diambil
sebanyak 2 µl kemudian dimasukan ke dalam tabung ependorf 200 µl yang telah
berisi campuran komponen bahan RAPD-PCR. Kemudian proses PCR dilakukan
dengan program RAPD. Program untuk menjalankan mesin PCR untuk 45 siklus
diatur masing-masing suhu denaturasi 94 oC selama 2 menit 30 detik; suhu
annealing 40 oC selama 1 menit; suhu ekstensi 72 oC selama 1 menit dan suhu
ekstensi akhir 72 oC selama 7 menit.
Elektrophoresis Hasil RAPD-PCR
Elektroforesis DNA digunakan untuk membaca hasil amplifikasi RAPD
dari mesin PCR. Produk hasil PCR dianalisis dengan gel agarose 1.5%. Gel
agarose disiapkan dengan melarutkan agarose sebanyak 0,75 gr, 50 ml larutan
buffer TAE (242 g tris-base; 57,1 g asam asetat glacial; 100 ml EDTA 0,5 M pH
8; dilarutkan dalam akuades hingga 1000 ml), dan 10 µl EtBr, kemudian
dipanaskan untuk dihomogenkan dengan temperatur medium selama 4 menit
telah dipasangkan sisir pencentak sumuran, kemudian dibiarkan hingga berubah
menjadi gel yang padat. Baki yang telah berisi gel agarosa dimasukkan ke dalam
bak elektroforesis yang telah diisi dengan larutan bufer TAE (gel dipastikan
terendam seluruhnya dalam TAE). Loading dye 4 µl dicampurkan dengan tiap
sample cendawan hasil PCR sebanyak 10 µl diatas kertas parafilm menggunakan
mikropipet kemudian di campurkan dan ditempatkan dalam sumuran pada agarose
yang telah diletakkan di mesin elektrophoresis. Selanjutnya dilakukan proses
running elektrophoresis selama 60 menit pada tegangan listrik 75 V. Hasil
elektroforesis divisualisasikan dengan transluminator ultraviolet. Pita DNA yang
terbentuk pada hasil elektrophoresis tersebut diamati dan difoto dengan
menggunakan kamera digital.
Gambar 2 Peralatan elektroforesis. A. Gel tray, B. Cara mencetak gel agarose. C. Peralatan lengkap untuk running elektroforesis (Fatchiyah 2006 ).
HASIL DAN PEMBAHASAN
Karakter Morfologi B.theobromae
Hasil pengamatan karakter morfologi pada penelitian ini menunjukkan bahwa pertumbuhan maksimum miselium B. theobromae dari berbagai tanaman inang pada media PDA dalam cawan petri berdiameter 9 cm secara umum pada 3 - 5 HSI. Pada awalnya, miselium isolat asal jeruk, kakao, karet, pisang berwarna putih sampai dengan 3 HSI kemudian berubah warna menjadi abu-abu muda sampai dengan umur 4 - 5 HSI dan setelah 10 HSI bertambah gelap sesuai dengan pertambahan umur isolat. Isolat cendawan asal manggis awalnya berwarna putih sampai dengan 3 HSI kemudian berubah warna menjadi dominan gelap sampai dengan umur 4 - 5 HSI dan bertambah gelap sesuai dengan pertambahan umur isolat.
Punithalingam (1976) dalam penelitiannya menyebutkan karakter morfologi cendawan B. theobromae ditandai dengan pertumbuhan miselium dari isolat B. theobromae seperti benang rambut halus atau kapas, miselium udara berlimpah. koloni mula-mula berwarna sepia berubah menjadi abu-abu kemudian menjadi hitam. Pertumbuhan koloni secara teratur membentuk lingkar sampai koloni memenuhi cawan petri. Koloni yang telah memenuhi cawan petri pada umur isolat 21 HSI tidak hanya memperlihatkan perbedaan warna namun juga telah membentuk piknidia. Warna dan penampilan koloni isolat B. theobromae
yang diamati sangat bervariasi. Koloni jeruk berwarna abu-abu muda, kakao berwarna abu-abu, karet berwarna abu-abu gelap, pisang berwarna coklat, dan manggis berwarna dominan hitam (Gambar 2).
Hasil pengamatan yang ditunjukkan Gambar 3 memperlihatkan bahwa pertumbuhan koloni B. theobromae isolat asal jeruk, kakao, karet, pisang, dan manggis pada media PDA memenuhi cawan setelah mencapai 4 HSI. Pada isolat asal jeruk, karet, dan pisang pertumbuhan koloni lebih cepat dibandingkan isolat asal kakao dan manggis. Rata-rata pertumbuhan koloni diantara kelima isolat B. theobromae memperlihatkan perbedaan kecepatan tumbuh.
17
Secara mikroskopis, bentuk hifa B. theobromae bersekat pada isolat asal jeruk, kakao, karet, dan pisang sedangkan pada isolat asal manggis hifa muda membengkak seperti ‘sate’. Hifa awalnya hialin kemudian berubah warna menjadi coklat. Khlamidospora terbentuk pada isolat asal manggis secara interkaler (Gambar 4).
Gambar 5 Morfologi hifa dan klamidospora pada manggis. Hifa membengkak seperti sate (A); pembentukan klamidospora secara interkaler (B), dengan perbesaran 40x.
Piknidia B. theobromae isolat asal jeruk, kakao, karet, pisang, dan manggis terbentuk secara berkelompok pada media WA yang diberi bahan induksi berupa potongan jerami padi dan kulit manggis (Gambar 5). Ciri ini yang membedakan piknidia B. theobromae dengan piknidia yang dihasilkan oleh Diplodia sp. Menurut Barnett dan Hunter (1999) piknidia B. theobromae terbentuk secara bergerombol dan berwarna hitam sedangkan piknidia Diplodia sp. tunggal atau tidak berkelompok.
Gambar 6 Piknidia B. theobromae yang terbentuk pada media WA + jerami padi (A, B, C, D) dan WA + kulit manggis (E). Jeruk (A); kakao (B); karet (C); pisang (D); manggis (E) dengan perbesaran 100x.
Gambar 7 Piknidia yang pecah mengeluarkan konidia (pewarnaan dengan laktofenol) pada isolat B. theobromae.
Piknidia B. theobromae yang ditumbuhkan pada media PDA dapat terbentuk pada isolat asal jeruk dan isolat asal karet sedangkan pada media WA yang diberi bahan induksi berupa potongan jerami terbentuk pada semua isolat kecuali isolat asal manggis. Piknida isolat asal manggis hanya dapat terbentuk pada media WA yang diberi bahan induksi berupa kulit manggis (Tabel 1). Hal ini menunjukkan bahwa dalam pembentukan piknidia diperlukan nutrisi tertentu agar dapat memaksimumkan pembentukannya. Menurut Winarsih (2007) jerami padi mengandung serat sampai 67%. Kandungan serat yang tinggi ini yang memicu pertumbuhan dan merangsang sporulasi cendawan. Salah satu enzim yang penting
19
dihasilkan cendawan adalah enzim selulase. B.theobromae adalah salah satu cendawan yang menghasilkan enzim selulase. Menurut Shivas dan Beasley (2005) media agar-agar yang kaya sumber gulanya merupakan kondisi yang tidak baik untuk terjadinya sporulasi pada kebanyakan cendawan patogen tanaman. Sporulasi biasanya ditingkatkan dengan penambahan material daun inang yang telah disterilkan, misalnya jerami gandum, daun jagung, daun bunga anyelir, atau media yang ‘kurus’ seperti WA.
Tabel 1 Pembentukan piknidia cendawan B. theobromae asal beberapa tanaman pada berbagai media sampai dengan 34 HSI
Media pembentukan piknidia
Piknidia B. theobromae asal
Jeruk Kakao Karet Pisang Manggis
PDA + - + - - - Piknidia tidak terbentuk
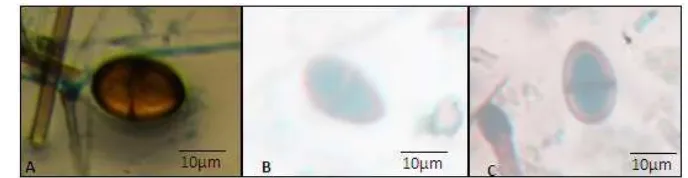
Konidia B. theobromae secara umum berbentuk jorong atau ovoid, hialin, tidak bersekat, dan memiliki dinding ganda saat muda dan saat matang berwarna coklat, bersekat, dan memiliki dinding tunggal. Pada konidia isolat asal jeruk, kakao, karet yang masih muda konidia hialin, tidak bersekat, dan memiliki dinding ganda namun setelah matang menjadi berwarna coklat, bersekat tebal seperti membentuk dua buah sel, dan memiliki dinding tunggal yang tebal. Barnett dan Hunter (1999) mendeskripsikan cendawan B.theobromae memiliki kekhasan yang ditandai dengan piknidia berwarna gelap dan terbentuk secara
berkelompok dalam stroma, konidia berwarna gelap dan memiliki dua buah sel saat matang, berbentuk jorong atau ovoid.
konidia berukuran 24 - 30 µm x 11,5 – 13,5 µm (Semangun 2000). B. theobromae
pada pisang memiliki konidia berukuran 20-30 µm x 10-18 µm (Goos 1961). Ukuran konidia bervariasi yaitu panjangnya 10,00 µm – 28,64 µm, lebarnya 6,36 µm – 15,91 µm, dan tebal dindingnya 0,80 µm – 2,50 µm. Pavlic et al. (2004) menemukan ciri umum pada isolat B.theobromae yang berasal dari Amerika Serikat, Amerika Selatan, Afrika Selatan dan Asia memiliki konidia berukuran 18–30 µm x 10–15 µm.
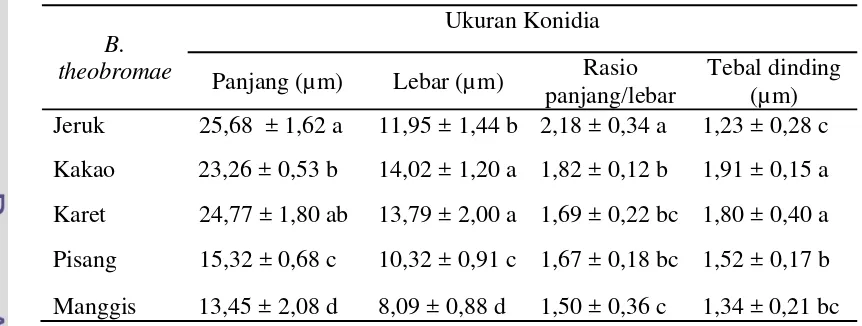
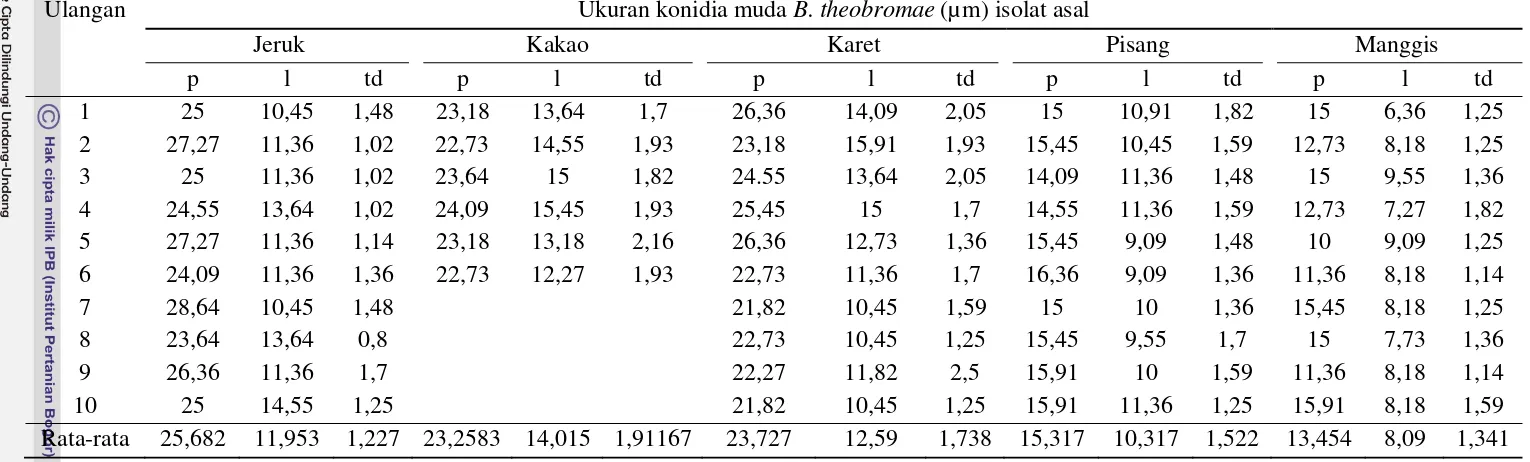
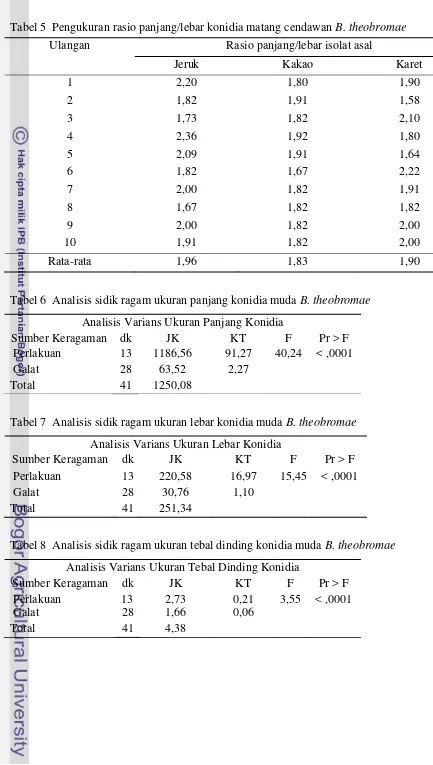
Hasil uji lanjut Duncan's Multiple Range Test (DMRT) pada tabel 2 menunjukkan bahwa ukuran panjang, lebar, dan tebal dinding konidia muda berbeda sangat nyata pada isolat asal jeruk, kakao, karet, pisang, dan manggis. Perbedaan yang ditunjukkan oleh konidia muda memperlihatkan keragaman ukuran konidia cendawan B. theobromae yang diperoleh dari inang berbeda. Pada konidia muda asal isolat jeruk memiliki rasio panjang/lebar tertinggi yaitu 2,18 dan konidia muda asal isolat manggis memiliki nilai rasio panjang/lebar terendah yaitu 1,50. Hal ini menunjukkan bentuk konidia yang semakin elips memiliki nilai rasio panjang/lebar yang tinggi dan cenderung bulat untuk nilai rasio
panjang/lebar yang rendah.
Tabel 2 Ukuran panjang, lebar, dan tebal dinding konidia muda cendawan B. theobromae pada lima tanaman inang
B.
Keterangan: Angka selajur yang diikuti oleh huruf yang sama tidak berbeda nyata (uji selang ganda Duncan, α = 0,01).
21
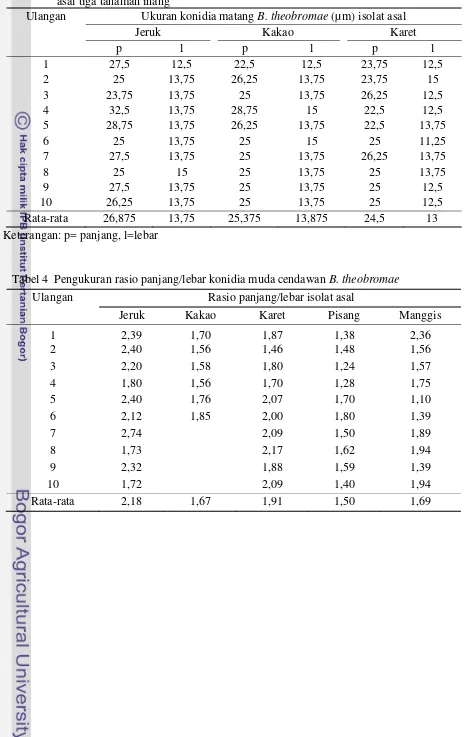
memperlihatkan keragaman ukuran konidia cendawan B. theobromae yang diperoleh dari inang berbeda. Pada konidia matang asal isolat jeruk memiliki rasio panjang/lebar 1,96, konidia asal isolat kakao 1,90, dan konidia asal isolat karet 1,83. Hasil pengukuran rasio panjang/lebar menunjukkan bahwa ukuran konidia kelima cendawan > 1 (bentuk jorong). Punithalingam (1976) dalam penelitiannya menyebutkan konidia B. theobromae memiliki bentuk subovoid-elipsoid oblong.
Tabel 3 Ukuran panjang dan lebar konidia matang cendawan B. theobromae pada tiga tanaman inang
Keterangan: Angka selajur yang diikuti oleh huruf yang sama tidak berbeda nyata (uji selang ganda Duncan, α = 0.05).
Konidia secara umum berbentuk jorong atau ovoid, hialin, tidak bersekat, dan memiliki dinding ganda saat muda dan saat matang berwarna coklat, bersekat, dan memiliki dinding tunggal. Pada konidia jeruk, kakao, karet yang masih muda konidia hialin, tidak bersekat, dan memiliki dinding ganda (Gambar 7) namun setelah matang menjadi berwarna coklat, bersekat tebal seperti membentuk dua buah sel, dan memiliki dinding tunggal yang tebal (Gambar 8). Barnett dan Hunter (1999) mendeskripsikan cendawan B.theobromae memiliki kekhasan yang ditandai dengan piknidia berwarna gelap dan terbentuk secara berkelompok dalam stroma. Konidia hialin dan tidak bersekat saat muda. Konidia berwarna gelap dan memiliki dua buah sel saat matang. Konidia berbentuk jorong atau ovoid.
B. theobromae Ukuran konidia
Gambar 8 Konidia muda isolat cendawan B. theobromae dari berbagai tanaman inang. Jeruk (A); karet (B); kakao (C); manggis (D); pisang (E) dengan perbesaran 100x.
Gambar 9 Konidia matang isolat cendawan B. theobromae dari berbagai tanaman inang.Jeruk (A); karet (B); kakao (C) dengan perbesaran 100x.
Karakter Molekuler B. theobromae
Penanda molekuler DNA telah digunakan untuk mengenali dan mengkarakterisasi populasi cendawan. Teknik RAPD sering digunakan untuk membedakan organisme tingkat tinggi atau kelompok eukaryote (Suryanto 2003).
B. theobromae termasuk ke dalam kelompok eukaryote sehingga teknik ini dapat digunakan untuk menganalisis DNA cendawan tersebut.
Teknik RAPD melibatkan penempelan primer tertentu yang dirancang sesuai dengan kebutuhan. Tiap primer dapat berbeda untuk menelaah keanekaragaman genetik kelompok yang berbeda (Suryanto 2003). Analisis molekuler dilakukan dengan teknik RAPD-PCR dengan menggunakan dua primer
yaitu OPB 01 dan OPB 07.
23
DNA cendawan B. theobromae dari berbagai tanaman pada lokasi yang berbeda. Keberhasilan amplifikasi DNA genom dalam teknik RAPD ditentukan salah satunya oleh kesesuaian primer dan efisiensi serta optimasi proses PCR (Suryanto 2003).
Kualitas pita yang tajam dipengaruhi oleh konsentrasi semua komponen dalam reaksi campuran (Edel 1998). Menurut Takamatsu (1998) komponen reaksi Mg 2+, DNA polimerase, primer, template DNA, dan suhu yang digunakan mempengaruhi konsistensi produk amplifikasi DNA.
Shah et al. (2010) melaporkan bahwa pendekatan RAPD mampu mendeteksi keanekaragaman genetik B. theobromae. Dalam penelitian Henuk (2010) melalui pendekatan PCR, cendawan B. theobromae telah berhasil diidentifikasi dengan menghasilkan produk PCR yang sesuai dengan yang dilaporkan Begoude et al. (2009).
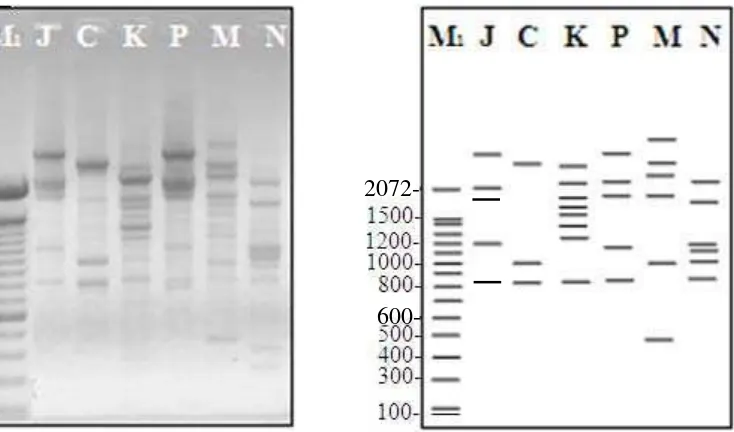
Profil DNA antara kelima isolat cendawan yang ditunjukkan Tabel 4 memperlihatkan bahwa jumlah dan ukuran pita DNA yang dihasilkan berbeda-beda kecuali antara isolat asal karet dan manggis menunjukkan pola yang serupa.
Gambar 10 Profil DNA lima isolat cendawan B. theobromae yang diamplifikasi dengan RAPD-PCR menggunakan primer OPB 01. M1 molecular
marker (DNA leader); isolat jeruk (J); isolat kakao (C); isolat karet (K); isolat pisang (P); isolat manggis (M); pembanding R. solani asal nanas (N).
Tabel 4 Ukuran fragmen DNA cendawan B. theobromae asal berbagai tanaman inang menggunakan primer OPB 01
Isolat Ukuran pita DNA (bp)
B. theobromae 1 2 3 4 5 6 7
Jeruk 500 700 900 1200 > 2072 Kakao 500 600 1500 2072 > 2072
Karet 500 600 900 1200 1300 1500 2072
Pisang 500 700 900 1200 1500 2072
Manggis 700 1200 2072
Kontrol 700 1300
600-25
Gambar 11 Profil DNA lima isolat cendawan B. theobromae yang diamplifikasi dengan RAPD PCR menggunakan primer OPB 07. M1 molecular
marker (DNA leader); isolat jeruk (J); isolat kakao (C); isolat karet (K); isolat pisang (P); isolat manggis (M), pembanding R. solani asal nanas (N).
Tabel 5 Ukuran fragmen DNA cendawan B. theobromae asal berbagai tanaman inang menggunakan primer OPB 07
Isolat
Ukuran pita DNA (bp)
B. theobromae 1 2 3 4 5 6 7 8
Jeruk 1200 2072 > 2072 Kakao 800 1000 > 2072
Karet 800 1200 1300 1500 1600 1700 2072 > 2072
Pisang 800 1000 1100 1700 2072 >2072
Manggis 500 1000 1700 >2072
Kontrol 800 1000 1100 1200 1600 2072
600-KESIMPULAN DAN SARAN
Kesimpulan
Isolat cendawan B. theobromae yang berasal dari tanaman jeruk, kakao, karet,
pisang, dan manggis memiliki morfologi yang bervariasi baik dari segi bentuk dan
penampilan koloni, kecepatan tumbuh koloni, pembentukan piknidia, dan ukuran
konidia. Pengukuran rasio panjang/lebar memperlihatkan variasi bentuk konidia
kelima cendawan yaitu subovoid-elipsoid oblong dengan ukuran konidia > 1 (bentuk
jorong). Hasil RAPD-PCR menggunakan primer OPB 01 menunjukkan bahwa
diantara kelima isolat cendawan dapat dibedakan kecuali antara isolat karet dan
manggis yang menghasilkan pola identik sedangkan melalui primer OPB 07 kelima
isolat cendawan dapat dibedakan kecuali antara isolat jeruk dan pisang. Morfologi
cendawan B. theobromae dan RAPD- PCR berhasil memperlihatkan keragaman isolat B.
theobromaeyang diperoleh dari tanaman inang berbeda.
Saran
Perlu adanya penelitian lebih lanjut terkait dengan patogenisitas dari
cendawan B. theobromae dari berbagai tanaman inang untuk mengetahui hubungan
DAFTAR PUSTAKA
AgroMedia. 2009. Budidaya Tanaman Buah Unggul Indonesia. Jakarta: PT Agromedia Pustaka.
Alexopoulos CJ. 1960. Introductory Mycology. Ed ke-5. New York: John Wiley and Sons, Inc.
Barnett HL, Hunter BB. 1999. Illustrated Genera of Imperfect Fungi. Ed ke-2. Minnesota: APS Press.
Begoude BAD, Bernard S, Michael JW, Jolanda R. 2009. Botryosphaeriaceae associated with Terminalia cattapa in Cameroon, South Africa and Madagascar. Mycol Progress 9: 101-123.
Davis RM, Farrald CJ, Davila D. 1987. Botryodiplodia trunk lesions in Texas citrus plant disease. Plant Disease 71 (9): 848-849.
Edel V. 1998. Polymerase Chain Reaction in Mycology. France: Dijon Cedex.
Ekundayo JA. 1978. Botryodiplodia theobromae Pat. Diseases, Pest, and Weeds in Tropical Crops. New York: Wiley-Interscience
Fatchiyah. 2006. Gel Elektroforesis. Malang: Universitas Brawijaya.
Goos RD, Cox EA, Stotz G. 1961. Botryodiplodia theobromae and its association with musa species [abstrak]. Mycologia 53 (3): 262-277. http:// www.jstor.org/stable/3756274 [21 Oktober 2010].
Henuk JBD. 2010. Identifikasi dan uji patogenisitas penyebab busuk pangkal batang pada jeruk (Citrus spp.) dari beberapa sentra produksi jeruk di Indonesia [tesis]. Bogor: Fakultas Pertanian, Institut Pertanian Bogor.
Mbenoun M, Momo Zeutsa EH, Samuels G, Amougou FN, Nyasse S. 2008. Dieback due to Lasiodiplodia theobromae, a new constraint to cocoa production in Cameroon. Plant Pathology 57: 381. hhtp://ddr.nal.usda.gov/bitstream/10113/13435/1/IND44032848.pdf [18 Agustus 2010].
Moller EM, Bahnweg G, Sandermann H, Geiger HH. 1992. A simple and efficient protocol for isolation of high molecular weight DNA from filamentous fungi, fruit Bodies, and infected plant tissues. Nucleic Acids Research 20 (22): 6115-6116.
Nunes FM, Oliveira MCF, Arriaga AMC, Lemos TLG, Neto MA. 2008. A New eremophilane-type sesquiterpene from the phytopatogen fungus
478-482 [jurnal on-line]. http://www.scielo.br/pdf/jbchs/v19n3/ a15v19n3.pdf [27 Agusutus 2010].
Pavlic D, Slippers B, Coutinho TA, Gryenhout M, Wingfield MJ. 2004.
Lasiodiplodia gonubiensis sp. nov., a new Botryosphaeria anamorph from native Syzygium cordatum in South Africa. Stud Mycol 50: 313–322.
Pha TA, Dung PT, Hieu ND, Nghia NA. 2010. Disease caused by
Botryodiplodia theobromae Pat. on rubber tree in Vietnam. Rubber Risearch Institute of Vietnam. http://www.rriv.org.vn/uploads/ userfiles/28-BCMalaysia-Pha.ppt- [8 Desember 2010].
Punithalingam E. 1976. CMI Descriptions of Pathogenic Fungi and Bacteria No. 519. Kew, Surrey, England: Commonwealth Mycological Institute.
Punithalingam E. 1980. Plant diseases attributed to Botryodiplodia theobromae
Pat. Letters in Applied Microbiology 1: 17–20.
Sambrook J, Fritsch EF, Maniatis T. 1989. Molecular Cloning. A Laboaratory Manual. Edke-2. New York: Cold Spring Harbor Laboratory Press.
Semangun H. 2000. Penyakit-Penyakit Tanaman Perkebunan di Indonesia. Yogyakarta: Gajah Mada University Press.
Semangun H. 2007. Penyakit-Penyakit Tanaman Hortikultura di Indonesia. Ed ke-2. Yogyakarta: Gajah Mada University Press.
Shah MD, Verma KS, Singh K, Kaur R. 2010. Morphological, pathological and molecular variability in Botryodiplodia theobromae (Botryosphaeriaceae) isolates associated with die-back and bark cancer of pear trees in Punjab, India. Genetics and Molecular Research 9 (2): 1217-1228.
Shivas R, Beasley D. 2005. Pengelolaan Koleksi Patogen Tanaman. Kramadibrata K, Soetjipto NW, Machmud M, penerjemah. Queensland: Department of Primary Industries and Fisheries. Terjemahan dari: Plant Pathology Herbarium.
Suryanto D. 2003. Melihat keanekaragaman organisme melalui beberapa teknik genetika molekuler. Medan: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara.
Takamatsu S. 1998. PCR Applications in Fungal Phylogeny. Japan: Mie University.
29
Wiratno AT, Nurbanah S. 1997. Pengendalian Penyakit Blendok pada Tanaman Jeruk Besar. Wonocolo: IPPTP. http://www.pustaka-deptan.go.id/agritek/jwtm0106.pdf [ 18 Agustus 2010].
[WSSP] Waksman Student Scholar Program. 2009. PCR primer design guidelines. Piscataway: Rutgers University Waksman Institute. http://www.premierbiosoft.com/tech_notes/PCR_Primer_Design.html
161209 [28 Nopember 2010].
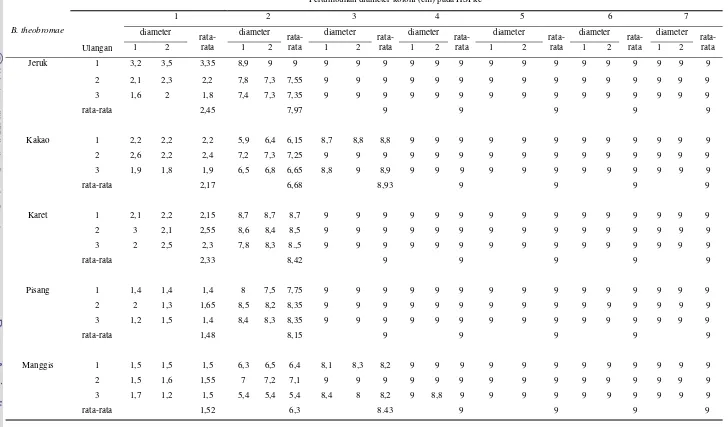
Tabel 1 Pertumbuhan diameter koloni cendawan B. theobromae
B. theobromae
Pertumbuhan diameter koloni (cm) pada HSI ke-
Tabel 2 Ukuran panjang, lebar, dan tebal dinding konidia muda cendawan B. theobromae asal lima tanaman inang
Keterangan: p= panjang, l=lebar, td= tebal dinding
Ulangan Ukuran konidia muda B. theobromae (µm) isolat asal
Jeruk Kakao Karet Pisang Manggis
p l td p l td p l td p l td p l td
1 25 10,45 1,48 23,18 13,64 1,7 26,36 14,09 2,05 15 10,91 1,82 15 6,36 1,25 2 27,27 11,36 1,02 22,73 14,55 1,93 23,18 15,91 1,93 15,45 10,45 1,59 12,73 8,18 1,25
3 25 11,36 1,02 23,64 15 1,82 24.55 13,64 2,05 14,09 11,36 1,48 15 9,55 1,36
4 24,55 13,64 1,02 24,09 15,45 1,93 25,45 15 1,7 14,55 11,36 1,59 12,73 7,27 1,82 5 27,27 11,36 1,14 23,18 13,18 2,16 26,36 12,73 1,36 15,45 9,09 1,48 10 9,09 1,25 6 24,09 11,36 1,36 22,73 12,27 1,93 22,73 11,36 1,7 16,36 9,09 1,36 11,36 8,18 1,14
7 28,64 10,45 1,48 21,82 10,45 1,59 15 10 1,36 15,45 8,18 1,25
8 23,64 13,64 0,8 22,73 10,45 1,25 15,45 9,55 1,7 15 7,73 1,36
9 26,36 11,36 1,7 22,27 11,82 2,5 15,91 10 1,59 11,36 8,18 1,14
10 25 14,55 1,25 21,82 10,45 1,25 15,91 11,36 1,25 15,91 8,18 1,59
Tabel 3 Ukuran panjang, lebar, dan tebal dinding konidia matang cendawan B. theobromae
asal tiga tanaman inang
Ulangan Ukuran konidia matang B. theobromae (µm) isolat asal
Jeruk Kakao Karet
Rata-rata 26,875 13,75 25,375 13,875 24,5 13 Keterangan: p= panjang, l=lebar
Tabel 4 Pengukuran rasio panjang/lebar konidia muda cendawan B. theobromae
Ulangan Rasio panjang/lebar isolat asal
Jeruk Kakao Karet Pisang Manggis
Tabel 5 Pengukuran rasio panjang/lebar konidia matang cendawan B. theobromae
Ulangan Rasio panjang/lebar isolat asal
Jeruk Kakao Karet
Tabel 6 Analisis sidik ragam ukuran panjang konidia muda B. theobromae
Analisis Varians Ukuran Panjang Konidia
Sumber Keragaman dk JK KT F Pr > F Perlakuan 13 1186,56 91,27 40,24 < ,0001
Galat 28 63,52 2,27
Total 41 1250,08
Tabel 7 Analisis sidik ragam ukuran lebar konidia muda B. theobromae
Analisis Varians Ukuran Lebar Konidia
Sumber Keragaman dk JK KT F Pr > F Perlakuan 13 220,58 16,97 15,45 < ,0001
Galat 28 30,76 1,10
Total 41 251,34
Tabel 8 Analisis sidik ragam ukuran tebal dinding konidia muda B. theobromae
Analisis Varians Ukuran Tebal Dinding Konidia
Sumber Keragaman dk JK KT F Pr > F
Perlakuan 13 2,73 0,21 3,55 < ,0001
Galat 28 1,66 0,06
Tabel 9 Analisis sidik ragam rasio panjang/lebar konidia muda B. theobromae
Analisis Varians Rasio panjang/lebar Konidia
Sumber Keragaman dk JK KT F Pr > F
Perlakuan 13 3,16 0,24 3,05 0,0065
Galat 28 2,23 0,08
Total 41 5,39
Tabel 10 Analisis sidik ragam ukuran panjang konidia matang B. theobromae
Analisis Varians Ukuran Panjang Konidia
Sumber Keragaman dk JK KT F Pr > F Perlakuan 11 54,06 4,91 1,26 0,3193
Galat 18 70,10 3,89
Total 29 124,17
Tabel 11 Analisis sidik ragam ukuran lebar konidia matang B. theobromae
Analisis Varians Ukuran Lebar Konidia
Sumber Keragaman dk JK KT F Pr > F Perlakuan 11 10,99 1,00 1,61 0,1774
Galat 18 11,15 0,62
Total 29 22,14
Tabel 12 Analisis sidik ragam rasio panjang/lebar konidia matang B. theobromae
Analisis Varians Rasio panjang/lebar Konidia
KERAGAMAN CENDAWAN Botryodiplodia theobromae
DARI BERBAGAI TANAMAN INANG
BERDASARKAN MORFOLOGI DAN POLA RAPD
FITRI KEMALA SANDRA
A34063054
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
ABSTRAK
FITRI KEMALA SANDRA. Keragaman Cendawan Botryodiplodia theobromae
dari Berbagai Tanaman Inang Berdasarkan Morfologi dan Pola RAPD. Dibimbing oleh KIKIN HAMZAH MUTAQIN dan SURYO WIYONO.
Cendawan Botryodiplodia theobromae Pat. menjadi penyebab penyakit pada berbagai tanaman serta memiliki kisaran inang yang luas yang dapat menurunkan kualitas maupun kuantitas produksi tanaman.
Variabilitas gejala penyakit dan kisaran inang yang dimiliki oleh cendawan ini menunjukkan bahwa mungkin terdapat keragaman dalam karakter morfologi maupun molekulernya. Pendekatan terhadap karakter morfologi cendawan B. theobromae dilakukan berdasarkan pengamatan bentuk, ukuran, dan warna dari struktur hifa, konidia, dan piknidia. Hasil pengamatan cendawan B. theobromae secara morfologi dapat dikonfirmasi menggunakan metode molekuler dengan teknik Random Amplified Polymorphic DNA (RAPD) untuk menganalisis keragaman genetiknya.
Penelitian bertujuan untuk membandingkan keragaman morfologi dan pola DNA molekuler berdasarkan teknik RAPD dari isolat B. theobromae yang diperoleh dari berbagai tanaman inang.
Sebanyak lima isolat B. theobromae yang diperoleh dari Klinik Tanaman, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor yang berasal dari tanaman dari berbagai daerah, yaitu Jeruk dari Jember, Jawa Timur; Karet dari Pematang Siantar, Sumatra Utara; Pisang dari Bogor, Jawa Barat; Manggis dari Bukit Tinggi, Sumatra Barat; dan Kakao diperoleh dari Taman Nasional (TN) Lorelindu, Sulawesi Tengah berdasarkan pengamatan morfologi mempunyai penampilan koloni dan morfologi cendawan yang bervariasi baik dari segi bentuk maupun ukuran; hifa, miselium, konidia, dan piknidia. Piknidia yang ditumbuhkan pada media Potato Dextrose Agar (PDA) terbentuk pada isolat asal jeruk dan isolat asal karet sedangkan pada media Water Agar (WA) yang diberi bahan induksi berupa potongan jerami terbentuk pada semua isolat kecuali isolat asal manggis. Piknida isolat asal manggis hanya dapat terbentuk pada media WA yang diberi bahan induksi berupa kulit manggis. Hal ini menunjukkan bahwa dalam pembentukan piknidia diperlukan nutrisi tertentu agar dapat memaksimumkan pembentukannya.
PENDAHULUAN
Latar Belakang
Penyakit yang disebabkan oleh Botryodiplodia theobromae (Patouillard) Griffon dan Maublanc ditemukan pada lebih dari 280 genus tanaman inang yang berbeda di daerah tropis dan subtropis di dunia (Nunes etal. 2008). Kisaran inang cendawan B. theobromae sangat luas, sehingga sumber infeksi selalu ada. Ekundayo (1978) menyebutkan bahwa B. theobromae dapat menyerang tanaman pisang, kakao, karet, kelapa, dan kelapa sawit.
Cendawan B. theobromae dilaporkan telah menyebabkan berbagai penyakit diantaranya mati ujung, busuk akar, busuk buah, bercak daun, dan sapu setan (Punithalingam 1980). Pada jeruk, B. theobromae menyebabkan kematian cabang, pada kakao dapat menyebabkan mati pucuk, busuk buah, dan kanker batang, pada karet menyebabkan mati pucuk, pada pisang dan manggis cendawan
B. theobromae dapat menyebabkan busuk buah. Cendawan B. theobromae
dianggap sebagai masalah serius bagi pertanian karena hal ini terkait dengan penyebab beberapa penyakit pada buah-buahan tropis (Nunes et al. 2008).
2 menggunakan suatu primer acak yang tidak didasarkan pada organisme tertentu dengan desain berupa primer tunggal yang pendek. Analisis keragaman genetik dilakukan terhadap cendawan B. theobromae untuk mengetahui apakah B. theobromae dari berbagai tanaman itu memiliki kesamaan atau perbedaan genetik.
Informasi tentang perbedaan morfologi dan genetik cendawan B. theobromae belum tersedia banyak di Indonesia. Oleh karena itu dilakukan penelitian tentang keragaman cendawan B. theobromae dari berbagai tanaman inang secara morfologi dan melalui analisis RAPD.
Tujuan Penelitian
Penelitian bertujuan untuk membandingkan keragaman morfologi dan pola DNA molekuler berdasarkan RAPD isolat-isolat B. theobromae dari berbagai tanaman inang.
Manfaat Penelitian
Penelitian ini diharapkan mampu memberikan informasi tentang karakter morfologi dan molekuler B. theobromae dari berbagai tanaman inang.
Hipotesis
Hipotesis yang disusun dalam penelitian ini adalah
1. Isolat Botryodiplodia theobromae dari berbagai tanaman tidak dapat dibedakan secara morfologi.
TINJAUAN PUSTAKA
Nilai Ekonomi Cendawan Botryodiplodia theobromae
B. theobromae dilaporkan telah menyebabkan berbagai penyakit diantaranya mati ujung, busuk akar, busuk buah, bercak daun, dan sapu setan (Punithalingam 1980). Pada jeruk, B. theobromae menyebabkan kematian cabang, pada kakao dapat menyebabkan mati pucuk, busuk buah, dan kanker batang, pada karet menyebabkan mati pucuk, pada pisang dan manggis cendawan B. theobromae dapat menyebabkan busuk buah.
Di pulau Jawa, cendawan B. theobromae mempunyai arti penting terutama di daerah dataran rendah. Jenis jeruk keprok (Citrus nobilis) dan jeruk besar (Citrus grandis) sering sangat menderita karena serangannya. Di Kabupaten Magetan sekitar 500 ha pertanaman jeruk besaryaitu 85% dari jumlah pohon telah
terserang oleh cendawan ini dengan tingkat serangan ringan sampai sedang (22 - 37%) (Wiratno dan Nurbanah 1997). Serangan juga terjadi di Kamerun pada tahun 1985 pada kakao dan menjadi faktor pembatas produksi kakao (Mbenoun et al. 2008). Pohon karet di Vietnam tahun 1921 terdeteksi terserang cendawan ini dan menjadi wabah pertama pada tahun 1998 di daerah penanaman karet tradisional di Vietnam (Pha et al. 2010). B. theobromae telah diketahui menyerang pada pisang sejak 1931 dan mampu menyebabkan pembusukan cepat buah pisang di gudang (Goos et al. 1961). Di Brasil, cendawan ini dianggap sebagai masalah utama bagi pertanian karena hal ini terkait dengan beberapa penyakit buah-buahan tropis (Nunes et al. 2008).
Gejala Penyakit Blendok pada Berbagai Tanaman Gejala pada tanaman jeruk (penyakit kulit diplodia)
4
ke dalam kulit kayu, merusak kambium, kemudian cabang digelang dan mati. Serangan patogen dengan gejala seperti ini disebut diplodia basah. Pada diplodia kering lebih berbahaya, karena gejala permulaan sulit diketahui. Infeksi baru diketahui jika daun telah menguning sehingga cabang yang sakit tidak dapat tertolong. Kulit mengering, dan jika dipotong, kulit dan kayu di bawahnya berwarna hitam kehijauan. Kulit yang sakit membentuk celah-celah kecil, dari dalamnya keluar massa spora yang semula berwarna putih, tetapi akhirnya berwarna hitam (Semangun 2007). B. theobromae tumbuh secara saprofit di kayu mati untuk meningkatkan potensi inokulum sebelum dapat menyebabkan kerusakan yang signifikan pada jaringan sehat (Davis et al. 1987).
Gejala pada tanaman kakao (penyakit botryodiplodia)
Cendawan B. theobromae berperan sebagai parasit lemah pada cabang dan ranting. Cendawan ini hanya dapat menginfeksi jaringan-jaringan yang lemah, atau menjadi patogen sekunder, atau menginfeksi melalui luka-luka karena serangga. Botryodiplodia dapat menyebabkan mati pucuk, busuk buah, dan kanker
batang (Semangun 2000).
Gejala pada tanaman karet
Gejala awal ditandai dengan terbentuknya pustul secara sporadis dan kemudian mereka menyatu menjadi lesio luas pada batang karet. Infeksi berat menyebabkan perdarahan pada lateks, retak, kulit membusuk dan gumosis. Pada tanaman yang masih muda, infeksi awal pada tunas muda berupa lesio kecil berwarna cokelat gelap, menyebar cepat, kemudian kulit membusuk, bagian daun yang terinfeksi menjadi kuning karena kurangnya pasokan gizi dan air. Infeksi yang parah menyebabkan kematian pada ranting mulai dari ujung (mati pucuk) (Pha et al. 2010).
Gejala pada tanaman pisang (busuk buah)
apabila buah mulai matang spora akan berkecambah dan mengadakan infeksi. Gejala mulai timbul pada tangkai buah kemudian meluas ke seluruh bagian buah. Gejala yang timbul yaitu buah menjadi lunak dan berair, serta mengeluarkan bau (aroma) yang khas. B. theobromae menyebabkan busuk ujung buah (tip rot),
busuk telapak, dan busuk pangkal. Penyakit ini merusak buah pisang yang matang dalam pengangkutan atau simpanan (Semangun 2007).
Gejala pada tanaman manggis
Penyakit busuk buah manggis menunjukkan gejala awal berupa kerak atau burik pada buah muda. Burik berwarna cokelat, pecah-pecah, dan mengeluarkan getah berwarna kuning. Burik biasanya berawal dari ujung buah, lalu menjalar kearah sepal atau sebaliknya (AgroMedia 2009). Kulit tampak kehitaman dan mengkilat kemudian menjadi burik karena cendawan membentuk banyak piknidium yang menghasilkan konidium (Semangun 2007).
Pengendalian Penyakit B. theobromae
Bentuk kegiatan pengendalian penyakit B. theobromae dapat dilakukan
6
Taksonomi & Morfologi Cendawan B. theobromae Taksonomi Cendawan B. theobromae
Menurut Semangun (2007) penyakit kulit diplodia disebabkan oleh cendawan Botryodiplodia theobromae Pat., yang dulu banyak dikenal dengan nama Diplodia natalensis P. Evans. Klasifikasi B. theobromae adalah (Alexopoulos 1960) :
Kingdom : Fungi
Phylum : Deuteromycota Kelas : Deuteromycetes Ordo : Sphaeropsidales Famili : Sphaeropsidaceae Genus : Botryodiplodia
Spesies : Botryodiplodia theobromae
Morfologi Cendawan B. theobromae
Botryodiplodia theobromae (Pat.) merupakan sinonim dari Lasiodiplodia theobromae (Pat.) Griff. & Maubl. yang memiliki perkembangbiakan secara
aseksual dari genus Botryosphaeria rhodina (Berk. & MA Curtis) ARX (Mohali 2005). Lasiodiplodia theobromae adalah bentuk anamorf dari Botryosphaeria rhodina (Berkeley & Curtis) von ARX dan sebagai cendawan yang memiliki kelas deuteromycetes (Nunes 2008).
Punithalingam (1976) menyebutkan bahwa karakter morfologi cendawan
B. theobromae ditandai dengan pertumbuhan miselia dari isolat B. theobromae
seperti benang rambut halus atau kapas, miselium udara berlimpah. Koloni mula-mula berwarna sepia berubah menjadi abu-abu kemudian menjadi hitam. Piknidia sederhana, bergerombol, sering agregat, stromatik, ostiolate, lebar sampai dengan 5 mm. Konidia awalnya uniseluler, hialin, granulosa, subovoid sampai ellipsoid-ooblong, berdinding tebal, memotong seperti sekat; konidia matang uniseptate, coklat seperti warna kayu manis, berukuran 20-30 µm x 10-15 µm.
µm x 15 µm, eksosporanya mempunyai jalur-jalur (Semangun 2007). Berbeda dengan pada jeruk, pembentukan piknidium cendawan B. theobromae pada kakao memerlukan cahaya. Piknidium berukuran 135 - 230 µm x 95 - 155 µm. konidium (piknidiospora) mula-mula berwarna coklat muda dan tidak bersekat, tetapi menjelang dilepaskan coklat tua dengan satu sekat melintang, dengan dinding spora sekunder. Konidium berukuran 24 - 30 µm x 11.5 - 13.5 µm, keluar melalui lubang ostiol seperti masa lengket berwarna putih sampai coklat muda. (Semangun 2000). Botryodiplodia theobromae pada pisang memiliki konidia berbentuk elips, mula-mula hialin dan uniseluler kemudian menjadi coklat dan bersekat tunggal. Konidia berukuran 20-30 µm x 10-18 µm (Goos et al. 1961).
Gambar 1 Piknidia dan konidia cendawan B. theobromae (Punithalingam 1976).
Pavlic etal. (2004) dalam penelitiannya menemukan ciri umum pada isolat
B. theobromae yang berasal dari Amerika Serikat, Amerika Selatan, Afrika Selatan dan Asia memiliki konidia berukuran 18–30 x 10–15 µm.
Polymerase Chain Reaction (PCR)
Reaksi berantai polymerase (Polymerase Chain Reaction, PCR) adalah metode enzimatis untuk melipatgandakan secara eksponensial suatu sekuen
A,B: Piknidia
C: Sel konidiogen dan konidia
8
nukleotida tertentu secara in vitro. Metode PCR sangat sensitif. Sensitivitas tersebut membuatnya dapat digunakan untuk melipatgandakan satu molekul DNA. Dengan metode PCR, dapat diperoleh pelipatgandaan suatu fragmen DNA sebesar 200.000 kali setelah dilakukan 20 siklus reaksi selama 220 menit. Hal ini menunjukkan bahwa pelipatgandaan suatu fragmen DNA dapat dilakukan secara cepat. Kelebihan lain metode PCR adalah bahwa reaksi ini dapat dilakukan dengan menggunakan template DNA dalam jumlah sangat sedikit (Yuwono 2006).
Prosedur reaksi PCR terdiri dari tiga tahap yaitu denaturasi, annealing (penempelan primer) dan ekstensi (sintesis DNA). Reaksi PCR ditentukan oleh kondisi suhu, denaturasi template, primer, annealing (penempelan primer) dan ekstensi (sintesis DNA). Pada langkah pertama, denaturasi template DNA untai ganda pada suhu 90-95 °C. Kemudian suhu diturunkan hingga sekitar 55 °C, primer menempel ke ujung 5 pada template yang telah terpisah menjadi untai tunggal. Untuk langkah ekstensi, suhu dinaikkan menjadi 72 °C dan primer-target berfungsi sebagai titik awal untuk sintesis DNA baru. Waktu untuk setiap langkah
biasanya 1-2 menit. Tiga langkah berurutan ini disebut sebagai satu siklus PCR. Pada siklus kedua, untai DNA yang baru disintesis dipisahkan dari untai asal oleh denaturasi dan masing-masing untai berfungsi lagi sebagai template dalam penempelan dan ekstensi. Secara teoritis, siklus PCR memungkinkan amplifikasi 2n kali lipat DNA target. Biasanya PCR dilakukan sebanyak 30-40 siklus. Namun banyaknya siklus tergantung pada konsentrasi DNA target didalam campuran reaksi (Edel 1998).
Random Amplified Polymorphic DNA Polymerase Chain Reaction (RAPD-PCR)
Random Amplified Polymorphic DNA (RAPD) merupakan salah satu teknik molekuler berupa penggunaan penanda tertentu untuk mempelajari keanekaragaman genetika. Dasar analisis RAPD adalah menggunakan mesin PCR yang mampu mengamplifikasi sekuen DNA secara in vitro. Teknik ini melibatkan penempelan primer tertentu yang dirancang sesuai dengan kebutuhan. Tiap primer
fragmen DNA yang diseleksi dengan menggunakan satu primer arbitrasi, terutama karena amplifikasi DNA secara in vitro dapat dilakukan dengan baik dan cepat dengan adanya PCR. Penggunaan penanda RAPD relatif sederhana dan mudah dalam hal penyiapannya. Teknik RAPD memberikan hasil yang lebih cepat dibandingkan dengan teknik molekuler lainnya. Teknik ini juga mampu menghasilkan jumlah karakter yang relatif tidak terbatas, sehingga sangat membantu untuk keperluan analisis keanekaragaman organisme yang tidak diketahui latar belakang genomnya. Teknik RAPD sering digunakan untuk membedakan organisme tingkat tinggi (eucaryote). Namun demikian beberapa peneliti menggunakan teknik ini untuk membedakan organisme tingkat rendah (procaryote) atau melihat perbedaan organisme tingkat rendah melalui piranti organel sel seperti mitokondria (Suryanto 2003).
Menurut WSSP (2009) RAPD PCR memiliki keterbatasan diantaranya hampir semua penanda RAPD adalah dominan karena tidak mampu membedakan apakah suatu segmen DNA dari lokus yang heterozigot (1 salinan) atau homozigot (2 salinan). PCR adalah reaksi enzimatik, sehingga kualitas dan konsentrasi DNA
template, konsentrasi komponen PCR, dan kondisi siklus PCR dapat sangat mempengaruhi hasil dari amplifikasi DNA. Ketidaksesuaian antara primer dan DNA template dapat berpengaruh terhadap total produk PCR serta penurunan dalam jumlah produk sehingga mengakibatkan hasil RAPD sulit diinterpretasikan.
Penggunaan RAPD-PCR dalam Analisis DNA Cendawan
Teknik RAPD-PCR memanfaatkan primer acak oligonukleotida pendek (dekamer) untuk mengamplifikasi DNA genom organisme. Prinsip teknik RAPD didasarkan pada kemampuan primer menempel pada DNA template. Primer yang didesain berupa primer tunggal pendek agar dapat menempel secara acak pada DNA genom organisme. Dengan demikian akan terdapat banyak pola fragmen DNA. Perbedaan ini dapat dilihat dengan adanya pola pita pada gel agarosa setelah diwarnai dengan pewarnaan DNA seperti seperti etidium bromide (Sambrook et al. 1989).
10
BAHAN DAN METODE
Tempat dan Waktu
Penelitian dilakukan di Laboratorium Mikologi Tumbuhan dan
Laboratorium Bakteriologi Tumbuhan Departemen Proteksi Tanaman, Fakultas
Pertanian, Institut Pertanian Bogor. Penelitian ini berlangsung mulai bulan
Februari 2010 sampai November 2010.
Karakterisasi Morfologi Cendawan B. theobromae
Penyiapan isolat cendawan
Isolat cendawan B. theobromae diperoleh dari Klinik Tanaman yang
berasal dari tanaman di berbagai daerah antara lain Jeruk dari Jember, Jawa
Timur; Karet dari Pematang Siantar, Sumatera Utara; Pisang dari Bogor, Jawa
Barat; Manggis dari Bukit Tinggi, Sumatera Barat (koleksi Dr. Ir. Suryo Wiyono
MSc.Agr); dan Kakao diperoleh dari Taman Nasional (TN) Lorelindu, Sulawesi
Tengah (koleksi Efi Toding Tondok SP.MSc.Agr).
Peremajaan dan Isolasi
Inokulum B. theobromae ditanam dalam media Potato Dextrose Agar
(PDA) dan Water Agar (WA) yang diberi potongan jerami padi, pelepah pisang
yang kering, kulit manggis steril dengan ukuran ± 0,5 cm kemudian diinkubasi
dalam suhu ruang selama kurang lebih tujuh hari. Konfirmasi cendawan dilakukan
terhadap isolat yang telah diremajakan dengan menggunakan kunci identifikasi
Barnett dan Hunter (1999).
Penyiapan preparat
Cendawan B. theobromae yang tumbuh dibuat preparat menggunakan
gelas objek, gelas tutup, dan laktofenol. Selanjutnya diamati dibawah mikroskop
cahaya dan dipotret dengan menggunakan kamera digital.