ABSTRAK
PURIFICATION AND CHARACTERIZATION OF CGT-ase (CYCLODEXTRIN GLUCANOTRANSFERASE) FROM AMYLOLYTIC BACTERIAL ISOLATES LOCAL LTi-21-3
Oleh
Miftahul Jannah
Pemurnian dan karakterisasi enzim CGT-ase dari bakteri amilolitik isolat LTi-21-3 telah dilakukan. Penelitian ini bertujuan untuk menyelidiki tahapan pemurnian enzim ase menggunakan metode ultrafiltrasi dan mendapatkan enzim CGT-ase murni-sebagian (partial purified) beserta karakteristiknya. Penelitian ini
diawali dengan studi pendahuluan produksi enzim CGT-ase untuk menyelidiki nutrisi dan waktu optimum produksi enzim CGT-ase. Penentuan pertumbuhan sel, uji aktivitas ekstrak kasar enzim CGT-ase, dan uji kadar protein enzim CGT-ase dilakukan menggunakan spektofotometer UV-VIS, secara berurutan
masing-masing pada panjang gelombang 600 nm, 550 nm dan 600 nm. Pemurnian enzim ase dilakukan menggunakan metode ultrafiltrasi. Karakterisasi enzim CGT-ase hasil pemurnian dilakukan pada pengamatan pengaruh pH dan suhu terhadap aktivitas enzim, penentuan konstanta kinetik (KM) dan Vmaks) serta penentuan
spesifitas substrat dari beberapa jenis pati. Hasil penelitian menunjukkan bahwa produksi enzim CGTase dari isolat LTi-21-3 optimum dengan medium Horikoshi’s II yang berkomposisi menggunakan sumber nitrogen yeast extract
-pepton dengan waktu inkubasi selama 36 jam. Pemurnian menggunakan metode ultrafiltrasi mampu meningkatkan kemurnian enzim CGTase isolat LTi-21-3 sebesar 1.6 kali lipat dengan perolehan sebesar 29 % dibandingkan dengan ekstrak kasarnya. Karakteristik enzim CGT-ase hasil pemurnian tersebut, memiliki aktivitas optimum pada pH 5.5 dan 7.5, suhu 60°C, dengan KM = 9 mg/mL dan
Vmaks = 500U/mL, serta memiliki substrat spesifitas tertinggi pada soluble starch
dibandingkan substrat jenis lainnya.
DAFTAR ISI
Halaman LEMBAR PENGESAHAN
DAFTAR ISI ... i
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan Penelitian ... 2
Manfaat Penelitian ... 3
TINJAUAN PUSTAKA ... 4
Bakteri ... 4
Nutrien untuk Pertumbuhan Bakteri ... 4
Fase Pertumbuhan Bakteri ... 6
Amilum ... 7
Enzim ... 9
Faktor-Faktor yang Mempengaruhi Aktivitas Enzim ... 11
Mekanisme Reaksi Enzim ... 14
Enzim CGT-ase ... 15
Stabilitas Enzim ... 17
Siklodekstrin ... 17
Isolasi dan Produksi ... 19
Pengujian Aktivitas Enzim CGT-ase ... 19
Penentuan Kadar Protein ... 19
Pemurnian Enzim ... 21
Fraksinasi Ammonium Sulfat ... 21
Ultrafiltrasi ... 21
METODOLOGI PENELITIAN ... 23
Waktu dan Tempat Penelitian ... 23
Prosedur Penelitian ... 24
Tahap Persiapan ... 24
Pembuatan Pereaksi ... 24
Penentuan Pertumbuhan Sel ... 25
Produksi Enzim CGT-ase ... 26
Penentuan Aktivitas Enzim CGT-ase ... 26
Penentuan Kadar Protein Enzim CGT-ase ... 26
Uji Kestabilan Enzim ... 27
Pemurnian Enzim CGT-ase ... 27
Karakterisasi Enzim CGT-ase ... 27
Diagram Alir Prosedur Penelitian... 29
HASIL DAN PEMBAHASAN ... 30
Studi Pendahuluan Produksi Enzim CGT-ase dari Isolat LTi-21-3 ... 30
Aktivitas Amilolitik Isolat Lti-21-3 ... 30
Variasi Nutrien Sumber Nitrogen ... 31
Penentuan Waktu Kultur Inkubasi Kultur Optimum untuk Produksi Enzim CGT-ase ... 33
Kestabilan Ekstrak Kasar Enzim CGT-ase dari Isolat LTi-21-3 ... 35
Pemurnian Enzim CGT-ase ... 36
Karakterisasi Enzim CGT-ase ... 39
Pengaruh Temperatur terhadap Aktivitas Enzim CGT-ase ... 39
Pengaruh pH terhadap Aktivitas Enzim CGT-ase... 40
Konstanta Kinetik CGT-ase ... 41
Penentuan Substrat Spesifitas CGT-ase ... 42
SIMPULAN DAN SARAN ... 44
Simpulan ... 44
Saran ... 45 DAFTAR PUSTAKA
I. PENDAHULUAN
A. Latar Belakang
Bakteri amilolitik merupakan mikroorganisme yang mampu memecah pati menjadi senyawa yang lebih sederhana dengan bantuan enzim yang
dihasilkan. Selain menghasilkan enzim amilase yang memecah pati menghasilkan monosakarida (glukosa), bakteri amilolitik juga
berkemungkinan menghasilkan enzim ekstraseluler yaitu enzim Siklodekstrin Glukanotransferase (CGT-ase) yang memecah pati menjadi oligosakarida. Siklodekstrin merupakan oligosakarida berbentuk siklik yang pada umumnya diproduksi dari pati oleh enzim CGT-ase (Lee et al., 1992).
Siklodekstrin dapat digunakan dalam berbagai industri, seperti pada industri kimia, farmasi, pangan dan kosmetika. Hal ini karena struktur siklodekstrin berbentuk seperti silinder dengan permukaan luarnya bersifat hidrofilik sedangkan bagian dalam rongganya bersifat non polar sehingga mempunyai sifat enkapsulasi, termasuk peningkatan kelarutan dan perlindungan
komponen kimia yang labil dari pengaruh oksidasi (Laga, 2001).
CGT-ase pada medium Horikoshi’s II dengan sumber karbon 1% (b/v) pati singkong, sumber nitrogen 0,5% (b/v) NH4Cl, dan sumber ion 0,02% (b/v)
MgSO4. Untuk menyelidiki enzim tersebut lebih lanjut, maka pemurnian dan
karakterisasi enzim CGT-ase dari isolat LTi-21-3 tersebut perlu dilakukan.
Pemurnian enzim bertujuan untuk memisahkan enzim spesifik dari enzim atau banyak komponen lain yang tidak diinginkan. Molekul-molekul kecil dapat disingkirkan lewat dialisis atau filtrasi gel, ultrafiltrasi dan lainnya. Pemurnian enzim merupakan hal yang penting, khususnya untuk proses karakterisasi. Enzim yang lebih murni menghasilkan produk yang lebih banyak karena enzim bekerja maksimal, hal ini ditandai dengan meningkatnya aktivitas enzim hasil pemurnian.
Pada penelitian ini telah dilakukan tahapan pemurnian enzim CGT-ase dari isolat LTi-21-3 dan karakterisasi enzim CGT-ase hasil pemurnian.
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah :
1. Mempelajari tahapan pemurnian enzim CGT-ase dari isolat LTi-21-3 menggunakan metode ultrafiltrasi.
2. Memperoleh enzim CGT-ase murni-sebagian (partial purified) dan
C. Manfaat Penelitian
Manfaat yang dapat diperoleh dari penelitian ini adalah
1. Memberikan informasi tentang produksi dan pemurnian enzim CGT-ase dari isolat LTi-21-3.
2. Memberikan informasi karakteristik enzim CGT-ase dari isolat LTi-21-3 yang selanjutnya dapat dilakukan kloning gen.
II. TINJAUAN PUSTAKA
A. Bakteri
Bakteri, berasal dari kata Latin bacterium, adalah kelompok raksasa dari
organisme hidup. Ukuran bakteri sangatlah kecil (mikroskopik) dan kebanyakan uniselular, dengan struktur sel yang relatif sederhana tanpa
nucleus (inti sel), cytoskeleton, dan organel lain seperti mitokondria dan
kloroplas. Bakteri digolongkan menjadi dua, yaitu bakteri yang
menguntungkan dan bakteri yang merugikan. Bakteri tersebar di tanah, air, dan sebagai simbiosis dari organisme lain. Bakteri rata-rata mengandung 40-70% protein, 13-34% asam nukleat, 10-30% lipid (angka-angka ini
menunjukkan persen berat kering) (Lehninger, 1997).
1. Nutrien untuk Pertumbuhan Bakteri
Organisme hidup memerlukan nutrisi untuk pertumbuhannya. Kebutuhan nutrien meliputi unsur makro esensial dan unsur mikro esensial. Unsur makro digunakan oleh mikroba dalam metabolisme sel, sedangkan unsur mikro digunakan untuk mengaktifkan enzim (Suhartono, 1989). Substansi kimia organik dan inorganik diperoleh dari lingkungan dalam berbagai macam bentuk. Nutrien diambil dari lingkungan kemudian
nutrisi diolah menghasilkan energi yang digunakan dalam proses seluler (Lim, 1998).
Jasad renik heterotrof membutuhkan nutrien untuk kehidupan dan
pertumbuhannya, yakni sebagai: (1) sumber karbon, (2) sumber nitrogen, (3) sumber energi, (4) dan faktor pertumbuhan, yakni mineral dan vitamin. Nutrien tersebut dibutuhkan untuk membentuk energi dan menyusun komponen-komponen sel. Setiap jasad renik bervariasi dalam kebutuhannya akan zat-zat nutrisi tersebut.
Ada tujuh komponen utama yang dibutuhkan semua makhluk hidup, yaitu karbon, oksigen, nitrogen, hidrogen, fosfor, sulfur dan kalium. Untuk kebutuhan akan sumber karbon dipenuhi oleh adanya gula, pati, serta karbohidrat lainnya. Ada dua macam mikronutrien yakni mikronutrien organik dan mikronutrien anorganik. Zat-zat yang bertindak sebagai mikronutrien organik pada beberapa asam amino (triptofan) dan pada beberapa komponen-komponen DNA dan RNA (purin dan pirimidin). Beberapa unsur logam yang termasuk dalam mikronutrien anorganik adalah Co, Mo, Cu, Zn. Unsur logam ini sangat diperlukan untuk kehidupan sel meskipun jumlahnya sangat sedikit (Irianto, 2006).
umum nutrien dalam media pembenihan harus mengandung seluruh elemen yang penting untuk sintesis biologik organisme baru (Jawetz, β001).”
2. Fase Pertumbuhan Bakteri
Suatu mikroorganisme mempunyai siklus pertumbuhan tertentu tergantung produk yang akan dihasilkan. Fase pertumbuhan bakteri dapat dibagi menjadi 4 fase, yaitu fase lag, fase logaritma (eksponensial), fase stasioner dan fase kematian. Fase lag merupakan fase penyesuaian bakteri dengan lingkungan yang baru. Lama fase lag pada bakteri sangat bervariasi, tergantung pada komposisi media, pH, suhu, aerasi, jumlah sel pada inokulum awal dan sifat fisiologis mikroorganisme pada media
sebelumnya. Ketika sel telah menyesuaikan diri dengan lingkungan yang baru maka sel mulai membelah hingga mencapai populasi yang maksimum. Fase ini disebut fase logaritma atau fase eksponensial.
Fase eksponensial ditandai dengan terjadinya periode pertumbuhan yang cepat. Variasi derajat pertumbuhan bakteri pada fase eksponensial ini sangat dipengaruhi oleh sifat genetik yang diturunkannya. Selain itu, derajat pertumbuhan juga dipengaruhi oleh kadar nutrien dalam media, suhu inkubasi, kondisi pH dan aerasi. Ketika derajat pertumbuhan bakteri telah menghasilkan populasi yang maksimum, maka akan terjadi
keseimbangan antara jumlah sel yang mati dan jumlah sel yang hidup.
Fase stasioner terjadi pada saat laju pertumbuhan bakteri sama dengan laju kematiannya, sehingga jumlah bakteri keseluruhan akan tetap.
pengurangan derajat pembelahan sel. Hal ini disebabkan oleh kadar nutrisi yang berkurang dan terjadi akumulasi produk toksik sehingga mengganggu pembelahan sel. Fase stasioner ini dilanjutkan dengan fase kematian yang ditandai dengan peningkatan laju kematian yang melampaui laju
pertumbuhan, sehingga secara keseluruhan terjadi penurunan populasi bakteri (Volk dan Wheeler, 1993).
B. Amilum
Amilum atau dalam bahasa sehari-hari disebut pati terdapat pada umbi, daun, batang dan biji-bijian (Poedjiadi, 1994). Pati (C6H10O5)n adalah homopolimer
glukosa dengan ikatan α-glikosidik yang merupakan rantai gula yang panjang. Sifat berbagai macam pati tidak sama, tergantung dari panjang rantai C dan cabang rantai molekul. Pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan fraksi tidak larut disebut amilopektin (Winarno, 1986).
Berbagai macam pati ditemukan di alam karena dapat disintesis oleh berbagai macam tumbuhan. Setiap macam pati memiliki bentuk partikel atau granula yang berbeda, dan secara mikroskopis dipakai untuk membedakan berbagai pati alamiah. Pati terbagi menjadi dua golongan yaitu pertama adalah amilosa (15-20%) yang merupakan rantai panjang tidak bercabang yang terdiri dari molekul-molekul α-D-glukopiranosa yang bersambungan dengan ikatan α-1,4. Amilosa terdiri atas 250-300 unit D-glukosa yang terikat dengan ikatan α -1,4-glikosidik, jadi molekulnya merupakan rantai terbuka. Kedua adalah
molekul α-D-glukopiranosa yang bersambungan dengan ikatan α1,4 dan α1,6. Adanya ikatan α-1,6-glikosidik ini menyebabkan terjadinya cabang, sehingga molekul amilopektin berbentuk rantai terbuka dan bercabang (Poedjiadi, 1994). Struktur amilosa dan amilopektin dapat dilihat pada Gambar 1.
(B) Amilopektin
Gambar 1. Struktur kimia dari (A) Amilosa dan (B) Amilopektin
Amilum dapat dihidrolisis sempurna dengan menggunakan asam sehingga menghasilkan glukosa. Hidrolisis juga dapat dilakukan dengan bantuan enzim amilase. Pada reaksi hidrolisis parsial, amilum terpecah menjadi molekul-molekul yang lebih kecil yang dikenal dengan nama dekstrin. Jadi dekstrin
adalah hasil antara pada proses hidrolisis amilum sebelum terbentuk maltosa (Poedjiadi, 1994). Untuk mengetahui adanya pati maka dilakukan pengujian dengan menggunakan larutan iodium (I2 dalam KI). Bila terdapat amilosa,
polimer-polimer glukosa yang lebih besar dari 20 maka akan menghasilkan warna biru. Bila polimer-polimer glukosa kurang dari 20 maka akan
menghasilkan warna merah. Dekstrin dengan polimer enam, tujuh, dan delapan akan memberikan warna coklat. Polimer yang lebih kecil dari lima tidak memberikan warna dengan iodium (Winarno, 1986).
Dalam kehidupan manusia amilum berperan sebagai sumber makanan
penghasil energi utama dari golongan karbohidrat, di samping itu amilum juga dapat berperan sebagai bahan aditif pada proses pengolahan makanan,
misalnya sebagai penstabil dalam proses pembuatan puding. Amilum juga berperan dalam pembuatan sirup dan pemanis buatan seperti sakarin. Dalam bidang non makanan, amilum digunakan untuk bahan baku dalam proses pembuatan kertas, pakaian dari katun, industri cat, maupun untuk produksi hydrogen (Liu, 2005).
C. Enzim
Menurut Page (1997), sebagai katalis enzim adalah satu-satunya dibanding dengan katalis-katalis anorganik atau organik sederhana. Sifat-sifat katalitik dari enzim termasuk hal-hal berikut:
1. Enzim meningkatkan laju reaksi pada kondisi biasa (fisiologik) dari tekanan, suhu, dan pH. Hal ini merupakan keadaan yang jarang dengan katalis-katalis lain.
2. Enzim berfungsi dengan selektivitas dan spesifisitas bertingkat luar biasa tinggi terhadap reaktan yang dikerjakan dan jenis reaksi yang
dikatalisasikan.
3. Enzim memberikan peningkatan laju reaksi yang luar biasa dibanding dengan katalis biasa.
Klasifikasi enzim secara internasional berdasarkan atas reaksi yang dikatalisis antara lain:
1. Oksidoreduktase, mengkatalisis berbagai macam reaksi oksidasi reduksi serta sering menggunakan koenzim seperti NAD, NADP, FAD, atau lipoleat sebagai akseptor hidrogen.
2. Transferase, mengkatalisis berbagai jenis transfer kelompok seperti aminotransferase, karnitin asil transferase, dan transkarboksilase.
3. Hidrolase, mengkatalisis pembelahan ikatan antara karbon dan beberapa atom lain dengan adanya penambahan air.
4. Liase, mengkatalisis pemecahan ikatan karbon-karbon, karbon sulfur dan karbon nitrogen tertentu.
5. Isomerase, mengkatalisis isomer optik dan geometrik dan oksidasi reduksi intramolekuler tertentu.
6. Ligase, mengkatalisis pembentukan ikatan antara karbon dan oksigen
(Lehninger, 1997).
Semua enzim adalah protein, dan aktivitas katalitiknya bergantung kepada integritas strukturnya sebagai protein. Enzim seperti protein lain, mempunyai berat molekul berkisar dari kira-kira 12.000 sampai 1 juta. Oleh karena itu, enzim berukuran amat besar dibandingkan dengan substrat atau gugus
terhubung dengan sisi aktif atau didekatnya. Molekul-molekul enzim ini disebut kofaktor atau koenzim (Ngili, 2009).
Beberapa enzim memerlukan kofaktor atau koenzim untuk aktivitas katalitiknya, dan enzim lain mungkin membutuhkan koenzim maupun satu atau lebih ion logam untuk aktivitas katalitiknya. Bagian haloenzim (koenzim dan ion) bersifat stabil sewaktu pemanasan, sedangkan bagian apoenzim (protein) terdenaturasi oleh pemanasan (Poedjiadi dan Supriyanti, 1994).
1. Faktor-Faktor yang Mempengaruhi Aktivitas Enzim
a. Suhu
Pengaruh suhu sangat menentukan aktivitas enzim pada waktu mengkatalisa suatu reaksi. Seluruh enzim memerlukan jumlah panas tertentu untuk dapat aktif. Sejalan dengan meningkatnya suhu, makin meningkat pula aktivitas enzim. Secara umum, setiap peningkatan 10oC di atas suhu minimum, aktivitas enzim akan meningkat sebanyak
dua kali lipat. Aktivitas enzim meningkat pada kecepatan ini hingga mencapai kondisi optimum. Peningkatan suhu yang melebihi suhu optimumnya menyebabkan lemahnya ikatan di dalam enzim secara struktural (Pratiwi, 2008). Pada suhu maksimum enzim akan
b. Konsentrasi Substrat
Aktivitas enzim dipengaruhi oleh konsentrasi substrat. Pada
konsentrasi substrat rendah, enzim tidak mencapai konversi maksimum akibat sulitnya enzim menemukan substrat yang akan direaksikan. Seiring dengan meningkatnya konsentrasi substrat, kecepatan reaksi juga akan meningkat akibat makin cepatnya substrat terikat pada enzim. Peningkatan konsentrasi substrat pada titik jenuh tidak lagi dapat
meningkatkan kecepatan laju reaksi (Pratiwi, 2008). Facilitation of proximaty, atau kemudahan berdekatan yang disebut sebagai efek
keakraban, yang berarti bahwa laju reaksi antara dua molekul ditingkatkan bila dalam larutan encer keduanya dijaga dalam jarak dekat dalam sisi aktif enzim, sehingga menaikkan konsentrasi efektif reaktan (Ngili, 2009).
c. pH
pH lingkungan juga berpengaruh terhadap kecepatan aktivitas enzim dalam mengkatalisis suatu reaksi. Hal ini disebabkan konsentrasi ion hidrogen mempengaruhi struktur tiga dimensi enzim dan aktivitasnya. Setiap enzim memiliki pH optimum di mana pada pH tersebut struktur tiga dimensinya paling kondusif untuk mengikat substrat. Bila
d. Inhibitor
Selain suhu, pH dan konsentrasi substrat, aktivitas enzim juga
dipengaruhi oleh ada tidaknya inhibitor. Jika terdapat pengurangan laju reaksi oleh suatu senyawa, senyawa tersebut dinamakan inhibitor. Inhibitor dapat bersaing dengan substrat dalam berikatan dengan enzim, sehingga menghalangi substrat terikat pada tapak aktif enzim (Poedjiadi dan Supriyanti, 1994). Peningkatan laju reaksi yang disebabkan oleh aktivator adalah kebalikan dari efek inhibitor.
2. Mekanisme Reaksi Enzim
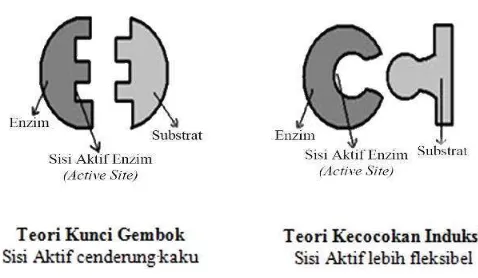
Enzim bekerja dengan dua cara, yaitu menurut Teori Kunci-Gembok (Lock and Key Theory) dan Teori Kecocokan Induksi (Induced Fit Theory).
Mekanisme kerja enzim dapat dilihat pada Gambar 2.
Gambar 2. Mekanisme kerja reaksi enzim
Teori Kunci-Gembok (Lock and Key Theory) dikemukakan oleh Emil
ruang antara substrat dengan sisi aktif (active site) dari enzim. Dengan
begitu sisi aktif enzim cenderung kaku. Substrat berperan sebagai kunci (key) dan sisi aktif (lock) berperan sebagai gembok. Substrat masuk ke
dalam sisi aktif sehingga terjadi kompleks enzim-substrat. Hubungan antara enzim dan substrat membentuk ikatan yang lemah. Pada saat ikatan kompleks enzim-substrat terputus, produk hasil reaksi akan dilepas dan enzim akan kembali pada konfigurasi semula.
Teori Kecocokan Induksi (Induced Fit Theory) dikemukakan oleh Daniel
Koshland yang menyatakan bahwa ini sisi aktif tidak bersifat kaku tetapi lebih fleksibel. Sisi aktif secara terus menerus berubah bentuknya sesuai dengan interaksi antara enzim dan substrat. Ketika substrat memasuki sisi aktif enzim, bentuk sisi aktif akan termodifikasi menyesuaikan bentuk substrat sehingga terbentuk kompleks enzim substrat. Sisi aktif akan terus berubah bentuknya sampai substrat terikat secara sepenuhnya, yang mana bentuk akhir dan muatan enzim ditentukan. Ketika substrat terikat pada enzim, sisi aktif enzim mengalami beberapa perubahan sehingga ikatan yang terbentuk antara enzim dan substrat menjadi menjadi lebih kuat Interaksi antara enzim dan substrat disebut Induced fit (Shahib, 2005).
D. Enzim CGT-ase
Enzim CGT-ase yaitu enzim ekstraseluler yang dapat mengubah pati menjadi siklodekstrin (Tonkova, 1998). CGT-ase diklasifikasikan menjadi tiga tipe berdasarkan jenis-jenis siklodekstrin yang dihasilkan dari ikatan α
Bacillusmacerans yang menghasilkan α-siklodekstrin, tipe Bacillus megaterium yang menghasilkan -siklodekstrin, dan tipe Bacillus sp.
menghasilkan -siklodekstrin (Mori et al.,1994).
Enzim CGT-ase merupakan keluarga dari enzim α-amilase (Leemhuis et al.,
2003). CGT-ase memiliki berat molekul yang bervariasi dari 60-110 kDa dan terdiri dari 700 asam amino. Sebagian memerlukan kalsium sebagai agen pelindung terhadap denaturasi panas (Bovetto et al., 1992) dan CGT-ase
alkalofilik optimum pada pH 9-10 (Tao, 1991). Suhu maksimal untuk bakteri yang menghasilkan enzim CGT-ase antara 40ºC sampai 80ºC. Sebagian besar CGT-ase diinhibisi kuat oleh Zn2+, Cu2+ dan Fe2+ (Tonkova, 1998).
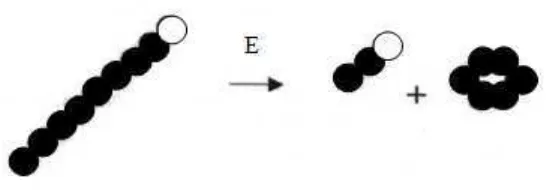
Reaksi katalisis oleh enzim CGT-ase dapat terjadi secara intramolekul
(siklisasi) dan antarmolekul (kopling, disproporsionasi), serta reaksi hidrolisis (Penninga, 1996). Reaksi siklisasi yaitu transfer residu gula akhir ke residu gula yang lain pada rantai oligosakarida yang sama untuk membentuk suatu senyawa siklik. Ini merupakan reaksi intramolekul dimana pati dihubungkan dengan ikatan α-1,4-glukan yang dikonversi ke dalam siklodekstrin. Reaksi ini bersifat reversible dan cincin dapat dibuka oleh CGT-ase untuk reaksi
enzim CGT-ase (Salva et al., 1997). Reaksi siklisasi enzim CGT-ase dapat
dilihat pada Gambar 3.
Gambar 3. Reaksi siklisasi enzim CGT-ase (Van der Veen et al., 2000)
E. Stabilitas Enzim
Stabilitas enzim adalah kestabilan aktivitas selama penyimpanan dan penggunaan enzim, kestabilan terhadap berbagai senyawa yang bersifat merusak enzim seperti pelarut tertentu (asam atau basa) dan oleh pengaruh suhu dan pH yang ekstrim atau kondisi non fisiologis lainnya (Wiseman, 1985).
F. Siklodekstrin
Siklodekstrin adalah merupakan oligosakarida yang tersusun atas 6, 7 atau 8 unit glukosa anhidrat melalui ikatan (1-4) dengan membentuk struktur melingkar seperti kue donat. Berdasarkan jumlah unit glukosa penyusun, siklodekstrin dipilah menjadi tiga, yaitu alfa (6 unit), beta (7 unit) dan gamma (8 unit). Cincin luar struktur siklodekstrin bersifat polar (hidrofilik)
sedangkan bagian dalam rongga bersifat lebih nonpolar (hidrofobik) (Szetjli, 1982). Produk siklik dapat terbentuk secara kompleks inklusi dengan
banyak digunakan dalam berbagai industri seperti pangan, kosmetika, farmasi, agrokimia serta untuk penanganan polusi (Bender, 1977; Kaneto and
Fumithasi, 1996; Szetjli, 1982).
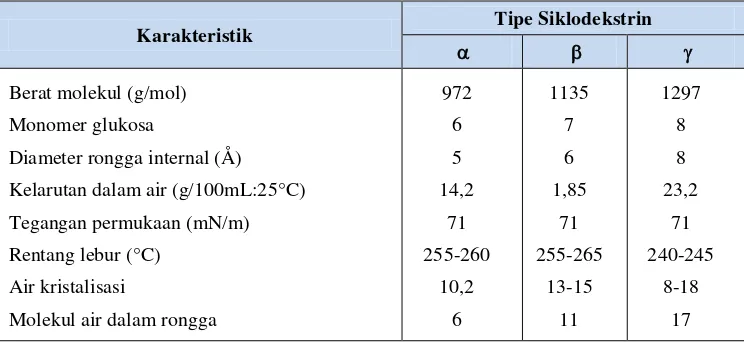
Adapun struktur α- siklodekstrin, - siklodekstrin dan - siklodekstrin dapat dilihat pada Gambar 4 serta sifat-sifat siklodekstrin dapat dilihat pada Tabel 1.
Gambar 4. Struktur α-, - dan -siklodekstrin (Van der Veen et al., 2000)
Tabel 1. Sifat-sifat siklodekstrin (Van der Veen et al., 2000)
Karakteristik Tipe Siklodekstrin
Berat molekul (g/mol) Monomer glukosa
Diameter rongga internal (Å) Kelarutan dalam air (g/100mL:25°C) Tegangan permukaan (mN/m) Rentang lebur (°C)
Air kristalisasi
Molekul air dalam rongga
972 6 5 14,2 71 255-260 10,2 6 1135 7 6 1,85 71 255-265 13-15 11 1297 8 8 23,2 71 240-245 8-18 17
G. Isolasi dan Produksi Enzim
Enzim dapat diperoleh secara ekstraseluler dan intraseluler. Enzim ekstraseluler merupakan enzim yang bekerja di luar sel, sedangkan enzim intraseluler merupakan enzim yang bekerja di dalam sel. Ekstraksi enzim ekstraseluler lebih mudah dibandingkan ekstraksi dari intraseluler, karena tidak memerlukan pemecahan sel, dan enzim yang dikeluarkan dari sel mudah dipisahkan dari pengotor lain serta tidak banyak bercampur dengan bahan-bahan sel lain (Pelczar and Chan, 1986).
Produksi enzim dilakukan dengan sentrifugasi dengan memisahkan enzim ekstraseluler dari sisa-sisa sel. Sentrifugasi dilakukan pada suhu rendah (dibawah suhu kamar) untuk menjaga kehilangan aktivitas enzim (Suhartono, 1989) selain itu mempercepat pengendapan debris sel. Sentrifugasi akan menghasilkan filtrat yang jernih yang merupakan ekstrak kasar enzim dan endapan yang terikat kuat pada dasar tabung, yang kemudian dipisahkan.
H. Pengujian Aktivitas Enzim CGT-ase
Pada uji aktivitas, larutan pati berperan sebagai substrat untuk enzim CGT-ase. Enzim ini akan mengurai pati menjadi siklodekstrin. Proses penguraian pati menjadi siklodekstrin, berlangsung saat inkubasi pada suhu 55°C selama 10 menit. Penghentian reaksi antara pati dengan enzim dilakukan dengan penambahan Na2CO3. Selanjutnya, ditambahkan larutan fenolftalein untuk
daerah visible (campuran reaksi berwarna merah muda keunguan) dengan
spektrofotometer UV-Vis. Nilai serapan yang terukur pada spektrofotometer UV-Vis dapat digunakan untuk menghitung besarnya aktivitas unit, satu unit
enzim yang didefinisikan sebagai jumlah enzim yang dapat membentuk satu µmol -siklodekstrin per menit di bawah kondisi kultur (Alves-Prado et al.,
2008).
I. Penentuan Kadar Protein
Penentuan kadar protein dengan metode Lowry didasarkan pada pengukuran serapan cahaya oleh ikatan kompleks yang berwarna ungu. Ini terjadi karena protein bereaksi dengan tembaga dalam lingkungan alkali yang mudah larut, dimana kompleks Cu2+ dengan ikatan peptida akan tereduksi menjadi Cu+.
Lalu, Cu+ akan mereduksi folin-ciocalteu yang mengikat protein sekitar pH 10. Sehingga kompleks fosfomolibdat-fosfotungstat menghasilkan
heteropolymolybdenum dari warna kuning menjadi biru. Ini disebabkan
karena oksidasi gugus aromatik terkatalis Cu, sehingga menghasilkan kompleks berwarna biru dalam derajat yang berbeda tergantung pada komposisi triftofan dan tirosinnya. Karena itu, protein yang berbeda akan memberikan tingkat warna yang berbeda (Alexander and Griffith, 1993).
J. Pemurnian Enzim
Pemurnian enzim bertujuan untuk memisahkan enzim yang dikehendaki dari enzim lain yang tidak diinginkan. Pemurnian enzim umumnya dilakukan dalam beberapa tahapan yaitu: fraksinasi dengan garam atau pelarut organik, sentrifugasi, dialisis, dan pemisahan dengan kromatografi kolom (Scopes, 1987). Adapun tahapan pemurnian enzim sebagai berikut:
1. Fraksinasi Ammonium Sulfat
Penambahan garam seperti natrium klorida, natrium sulfat atau ammonium sulfat menimbulkan pengendapan protein , yang disebut peristiwa salting out. Penambahan garam ke dalam larutan enzim akan mempengaruhi
kelarutan enzim. Pada konsenrasi garam rendah, kelarutan enzim dalam air bertambah, disebut dengan peristiwa “salting in”, sedangkan pada
konsentrasi tinggi kelarutan enzim akan menurun sehingga enzim akan mengendap, disebut dengan peristiwa “salting out” . Setelah dilakukan pengendapan dengan garam ammonium sulfat dilakukan proses
sentrifugasi dingin untuk memisahkan endapan garam ammonium sulfat dengan filtratnya yang kemudian endapannya di ambil dengan cara dilarutkan dengan buffer asetat (Scopes, 1982).
2. Ultrafiltrasi
Ultrafiltrasi adalah teknik pemisahan dengan menggunakan membran untuk menghilangkan zat terlarut dengan bobot molekul (BM) tinggi, aneka koloid, mikroba sampai padatan tersuspensi dari air lautan.
Ultrafiltrasi memisahkan molekul terlarut berdasarkan ukuran dengan melewatkan larutan tersebut pada filter. Ultrafiltrasi merupakan membran permeabel kasar, tipis, dan selektif yang mampu menahan makromolekul seperti koloid, mikroorganisme, dan pirogen. Molekul yang lebih kecil seperti pelarut dan kontaminan terionisasi dapat melewati membran ultrafiltrasi sebagai filtrat. Keuntungan ultrafiltrasi secara efektif mampu menghilangkan sebagian besar partikel, pirogen, mikroorganisme, dan koloid dengan ukuran tertentu. Proses membran ultrafiltrasi merupakan upaya pemisahan dengan membran yang menggunakan gaya dorong beda tekanan yang sangat dipengaruhi oleh ukuran dan distribusi pori membran (Malleviale, 1996). Ultrafiltrasi adalah proses pemurnian menggunakan Millipore Ultrafiltrasi System (Bedford, Massachusetts, USA) dan PLTK selulosa membran, 30 kDa (Millipore, USA). Ultrafiltrasi menghasilkan enzim yang lebih pekat dengan aktivitas spesifik yang lebih tinggi,
aktivitas enzim CGT-ase dari isolat Alkaliphile Bacillus Pseudalcaliphilus 20RF meningkat dua kali lipat (Torkova, 2011).
III.METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini telah dilakukan pada bulan Juni-November 2013 di
Laboratorium Biokimia dan Laboratorium Biomassa Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
B. Alat dan Bahan
Alat-alat yang digunakan pada penelitian ini adalah autoclave (model S-90N),
laminar air flow (CURMA model 9005-FL), timbangan digital, inkubator, shaker incubator, sentrifuga, lemari pendingin, kompor, tabung sentrifuga, mikropipet, waterbath, oven, spektofotometer UV-Vis, amicon ultra-15, inkubator,kasa, rak tabung, jarum ose dan alat-alat gelas lain seperti tabung reaksi, cawan petri, erlenmeyer, beaker gelas, gelas ukur, labu ukur, pipet tetes, batang pengaduk, serta pemanas bunsen.
Bahan-bahan yang digunakan pada penelitian ini yaitu pati singkong, pepton,
yeast extract, K2HPO4, MgSO4.7H2O, fenolftalein (PP), methyl orange, agar,
Na2CO3, pH indikator, Na(K)-tartarat, CuSO4.5H2O, reagen folin ciocelteau,
aquadest, soluble starch, pati ubi jalar, pati jagung, buffer sitrat 0,1M, buffer
C, pereaksi D, spiritus dan alkohol. Sampel yang digunakan adalah bakteri isolat lokal LTi-21-3 yang telah diperoleh dari peneliti sebelumnya.
C. Prosedur Penelitian
1. Tahapan Persiapan
a. Pembuatan Medium
Medium Pertumbuhan dibuat dengan komposisi medium Horikoshi’s
II termodifikasi (Park et al, 1989). Medium Horikoshi’s II terdiri dari
Larutan I (pati singkong 1%, pepton 0,5%, ekstrak ragi 0,5%, K2HPO4
0,1%, MgSO4.7H2O 0,02%, fenolftalein 0,03%, metil jingga 0,01%,
dan agar 1,5%), Larutan II (Na2CO3 1%), dan Larutan III (Akuades). Medium starter dan kultur menggunakan medium Horikoshi’s II tanpa
fenolftalein, metil jingga, dan agar.
b. Peremajaan Bakteri Isolat LTi-21-3
Peremajaan Bakteri Isolat LTi-21-3 dilakukan dengan
menginokulasikan bakteri LTi-21-3 pada medium padat Horikoshi’s II agar miring.
2. Pembuatan Pereaksi
a. Larutan Buffer Asetat 0,1 M (pH 5,5)
b. Pereaksi Enzim CGT-ase (Kaneko et al., 1987; Alves- Prado et al., 2008)
Pereaksi ini digunakan untuk menguji aktivitas ekstrak kasar enzim CGT-ase. Pereaksi enzim CGT-ase yaitu larutan pati soluble 1%
(b/v). Larutan pati soluble disiapkan dengan melarutkan 1 g pati soluble ke dalam 100 mL 0,1M buffer asetat pH 5,5 kemudian
dipanaskan hingga larut.
c. Pereaksi Lowry (Lowry et al., 1951)
Pereaksi Lowry terdiri atas 4 macam, yang meliputi Pereaksi A, B, C, dan D. Masing-masing pereaksi tersebut disiapkan sebagai berikut : Pereaksi A : 2 g Na2CO3 dilarutkan dalam 100 mL NaOH 0,1N; Pereaksi B : 5 mL larutan CuSO4.5H2O 1% (b/v) ditambahkan 5 mL
larutan Na(K)-tartarat 1% (b/v); Pereaksi C : 2 mL pereaksi B ditambah 100 mL pereaksi A; dan Pereaksi D : reagen
Folin-Ciocelteau diencerkan dengan akuades 1:1. Larutan standar protein digunakan BSA (Bovine Serum Albumine) dengan konsentrasi 500-5000 ppm.
3. Penentuan Pertumbuhan Sel
4. Produksi Enzim CGT-ase
Sebanyak 2 ose Bakteri Isolat LTi-21-3 dari media agar miring
dipindahkan ke dalam media starter secara aseptis lalu dikocok dengan
shaker incubator, dengan kecepatan 140 rpm pada suhu ruang selama overnight 17 jam. Selanjutnya 2ml media starter dipindahkan ke dalam
medium kultur volume 100 mL dalam Erlenmeyer 500 mL. Kultur dikocok dengan shaker incubator dengan kecepatan 105 rpm, suhu ruang, selama waktu inkubasi yang diperlukan. Kemudian sentrifugasi kultur selama 30 menit untuk mendapatkan ekstrak kasar enzim CGT-ase.
5. Penentuan Aktivitas Enzim CGT-ase
Ekstrak kasar enzim CGT-ase yang diperolah kemudian diuji aktivitas enzim CGT-ase nya. Sebanyak 100 µL larutan enzim ditambahkan 800 µL pati soluble 1% yang disiapkan dalam buffer asetat 0,1M pH 5,5 dan
diinkubasi pada suhu 55ºC selama 10 menit. Reaksi dihentikan dengan menambahkan 4 mL Na2CO3 0,25M dan 0,1 mL larutan fenolftalein 1
mM. Absorbansi diukur menggunakan spektrofotometer UV-Vis pada λmaks 550 nm. Kontrol dibuat dengan cara menginaktifkan larutan enzim
pada suhu 100ºC selama 30 menit, dan selanjutnya diperlakukan sama dengan sampel.
6. Penentuan Kadar Protein Enzim CGT-ase
Ekstrak kasar enzim CGT-ase yang diperoleh kemudian diuji kadar
lalu ditambahkan dengan 5 mL pereaksi C. Campuran diaduk secara merata dan dibiarkan selama 10 menit pada suhu kamar. Kemudian ditambahkan dengan cepat 0,5 mL pereaksi D dan diaduk dengan sempurna. Setelah itu didiamkan selama 30 menit pada suhu kamar. Sebagai kontrol, larutan enzim diganti dengan akuades. Perlakuan kontrol sama dengan perlakuan pada sampel. Pengukuran serapan dilakukan menggunakan spektrofotometer UV-Vispada λmaks 600 nm.
7. Uji Kestabilan Enzim CGT-ase
Ekstrak Kasar Enzim CGT-ase disimpan pada suhu 4oC kemudian diukur aktivitas CGT-ase dan kadar proteinnya untuk menentukan aktifitas spesifik. Pengujian dilakukan berkala setiap 24 jam.
8. Pemurnian Enzim CGT-ase
Ekstrak kasar enzim yang diperoleh dimurnikan dengan pemekatan menggunakan Amicon Ultra-15 (Millipore) dengan kecepatan 5000rpm, temperatur 4oC selama 20 menit. Hasil pemurnian ini kemudian
digunakan untuk karakterisasi.
9. Karakterisasi Enzim (Tonkova et al., 2011).
Enzim CGT-ase isolat LTi-21-3 hasil pemurnian dikarakterisasi.
a. Pengaruh pH dan Temperatur terhadap Aktivitas CGTase
Efek pH terhadap aktivitas CGTase dilakukan dengan buffer sitrat 0.1 M pada interval pH 4.5 dan 5, dan menggunakan buffer phosfat pada interval 5.5-7.5. Efek temperatur dilakukan pada interval suhu dari 45
– 65ºC.
b. Penentuan Konstanta Kinetik CGTase
Konstanta kinetika ditentukan dengan soluble starch sebagai substrat pada konsentrasi 2.5 – 20.0 mg/mL pada pH 5,5 dan dikalkulasi menggunakan transformasi Lineweaver-Burk.
c. Penentuan Substrat Spesifitas CGTase
Berbagai jenis pati (pati singkong, pati jagung, pati ubi jalar dan
soluble starch) masing-masing 1% divariasikan pada proses reaksi
D . Diagram Alir Prosedur Penelitian
Prosedur penelitian dapat dilihat pada diagram alir berikut:
Penanaman bakteri ke dalam starter
Inokulasi dari media starter ke medium Horikoshi’s II termodifikasi
Penentuan pertumbuhan sel, uji aktivitas ekstrak kasar enzim CGT-ase dan penentuan kadar protein enzim CGTase
Produksi enzim CGT-ase
Pemurnian enzim CGT-ase dengan metode ultrafiltrasi Ekstrak kasar dengan aktivitas spesifik enzim terbaik
Peremajaan bakteri isolat LTi-21-3
Karakterisasi enzim
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil yang diperoleh dari penelitian yang telah dilakukan maka dapat ditarik simpulan sebagai berikut:
1. Isolat LTi-21-3 mampu menghasilkan enzim ekstraseluler dengan nutrisi sumber nitrogen terbaik yeast extract-pepton dengan waktu kultur 36 jam.
2. Pada kestabilan ekstrak kasar enzim CGT-ase dari isolat LTi-21-3, sisa aktivitas enzim sampai hari kedua adalah 71,27% dan enzim kehilangan aktivitas pada hari kelima.
3. Kemurnian enzim CGT-ase dari isolat LTi-21-3 dengan metode ultrafiltrasi naik 1,6 kali lipat dengan perolehan 29 %.
4. Aktivitas enzim CGT-ase dari isolat LTi-21-3 optimum pada pH 5.5 dan 7.5, temperatur 60oC dengan konstanta kinetik Vmaks = 500 U/mL dan
KM = 9 mg/mL serta subsrat spesifik tertinggi pada soluble starch
B. Saran
Dari hasil penelitian yang diperoleh disarankan hal-hal sebagai berikut: 1. Perlu dilakukan variasi pH>7,5 pada karakterisasi pengaruh pH terhadap
aktivitas enzim CGT-ase dari isolat LTi-21-3.
2. Perlu dilakukan identifikasi lebih lanjut terhadap bakteri isolat LTi-21-3 untuk mengetahui jenis dan morfologinya dan perlu diketahui komponen kimia dalam pati singkong yang digunakan sehingga dapat menghasilkan enzim CGT-ase pada isolat LTi-21-3.
3. Enzim CGT-ase dari isolat LTi-21-3 dengan produk siklodekstrinnya diharapkan dapat dimanfaatkan untuk proses pembentukan obat-obatan. Oleh karena itu, perlu dilakukan tahap pemurnian lebih lanjut yaitu kromatografi untuk mendapatkan enzim yang lebih murni.
DAFTAR PUSTAKA
Alexander, R.R. and J.M. Griffith. 1993. Basic Biochemical Methods, 2nd ed.
Wiley-Liss, Inc. New York.
Alves-Prado, H.F., A.A. Carneiro, F.C. Pavezzi, E. Gomes, M. Boscolo, C.M. Franco and R. Silva. 2008. Production of Cyclodextrins by CGT-ase from
Bacillus clausii Using Different Starches as Substrates. Appl Biochem. Biotechnol. 146: 3–13.
Bender, L. 1977. Enzyme and Microbial Systems Involved in Starch Processing.
Arch. Microbiol. 3: 272-282.
Bovetto, L.J., D.P. Backer, J.R. Villette, P.J. Sicard , and S.J.L. Bouquelet. 1992. Cyclomaltodextrin Glucanotransferase from Bacillus circulans E 192. Biotechnol and Appl Biochem. 15: 48-58.
Cao X, Jin Z, Wang X, Chen F. 2005. A Novel Cyclodextrin Glycosyl Transferase from An Alkalophilic Bacillus species: Purification and Characterization.
Food Res Int. 38:309–14.
Fujita Y, Tsubouchi H, Inagi Y, Tomita K, Ozaki A, and Nakamura K. 1990. Purification and Properties of Cyclodextrin Glycosyltransferase from Bacillus
sp. AL-6. J Ferment Bioeng. 70:150–4.
Gawande BN, Goel A, Patkar AY, and Nene SN. 1999. Purification and properties of a novel raw Starch Degrading Cyclomaltodextrin
Glucanotransferase from Bacillus firmus. Appl Microbiol Biotechnol.
51:504–9.
Hedges, A.R. 1992. Cyclodextrin : Production, Properties and Applications. In: Schenck, F.W., and Hebeda R.E. Starch Hydrolysis Products. New York:
VCH Publishers. 319-334.
Hidayat, N., M.C. Padaga dan S. Suhartini. 2006. Mikrobiologi Industri. Penerbit
ANDI. Yogyakarta.
Hirano K, Ishihara T, Ogasawara S, Maeda H, Abe K, and Nakajima T. 2006. Molecular Cloning and Characterization of a Novel CGT-ase from
Irianto, K. 2006. Mikrobiologi Menguak Dunia Mikroorganisme. Yrama Media.
Bandung.
Jawetz. 2001. Mikrobiologi Kedokteran. Salemba Medika. Jakarta.
Kaneto, U. and H. Fumitashi. 1996. Improvement of Drug Properties by Cyclodextrins. Pract. Med. Chem. 14: 793-825.
Lehninger, A.L. 1997. Biochemistry. Academic Press. New York.
Laga, A. 2001. Produksi Siklodekstrin dengan Menggunakan Substrat Tapioka Terlikuifikasi dengan Aseptor Minimal. (Disertasi). Pasca Sarjana Teknologi
Industri Pertanian FATETA-IPB. Bogor.
Lee, J.H, K.J.L. Choi, J.Y. Choi, Y.S. Lee, I.B. Kwon, and J.H. Yu. 1992. Enzymatic Production of Cyclodextrin Glucanotransferase of Klebsiella oxytoca 19-1. Enzyme Microbial. Technol. 14: 1017-1020.
Lim, D. 1998. Microbiology, 2nd Edition. McGrow-Hill Book. New York.
Liu, Q. 2005. Understanding Starch and Their Role in Foods. Taylor and
Francis Group, LLC.
Lowry, C.H., N.J. Roseburgh, Y.L. Farr and R.J. Randall. 1951. Protein
Measurement with The Folin Phenol Reagent. J. Biol. Chem. 193: 365-275.
Mallaviale, J. 1996. Water Treatment Membran Processes, AWWA, Lyonnaise des Eaux, Water Research Commission of South Africa, Mc Graw Hill, New York
Martins RF and Hatti-Kaul R. 2002. A New Cyclodextrin Glycosyltransferase from an Alkalophilic Bacillus Agaradhaerens Isolate: purification and characterization. Enzyme Microb Technol. 30:116–24.
Mori, S., S. Hirose, T. Oya and S. Kitahata. 1994. Purification and Properties Cyclodextrin Glucanotransferase from Brevibacterium sp. No. 9505. Biosci. Biotech. Biochem. 58: 1968-1972.
Ngili, Y. 2009. Biokimia: Struktur dan Fungsi Biomolekul. Graha Ilmu.
Yogyakarta.
Page, D.S. 1997. Prinsip-Prinsip Biokimia. Erlangga. Jakarta.
Palmer, T. 1985. Understanding Enzyme. Ellishorwood Publisher.
Pelczar, M. J. and E. C. S. Chan. 1986. Dasar-Dasar Mikrobiologi. UI-Press.
Penninga, D. 1996. Protein Engineering of Cyclodextrin Glycosyltransferase from Bacillus circulans strain 251. (Thesis). University of Groningen. Netherlands.
Poedjiadi, A. dan F.M. Supriyanti. 1994. Dasar-Dasar Biokimia. Universitas
Indonesia. Jakarta.
Prado, A. 2008. Production of Cyclodextrins by CGTase from clausii using Different Starches as Substratses. Humana Press Inc.12 pp.
Pratiwi S.T. 2008. Mikrobiologi Farmasi. Erlangga. Jakarta.
Purnawati, A. 2012. Pengaruh Beberapa Faktor pada Medium Kultur terhadap Produksi Enzim CGT-ase dari Bakteri Amilolitik Isolat Lokal LTi-21-3. (Skripsi). Universitas Lampung. Bandar Lampung.
Salva, T.J.G., V.B. Lima and A.P. Pagan. 1997. Screening of Alkaphilic Bacteria for Cyclodextrin Glycosyltransferase Production. Revista de Microbiologia.
28: 157-164.
Sabioni JG, Park YK. 1992. Cyclodextrin Glycosyltransferase Production by
Alkalophilic Bacillus lentus. Rev Microbiol. 23:128–32.
Sastrawiyana, H. 2011. Isolasi dan Penapisan Bakteri Amilolitik Isolat Lokal Pendegradasi Pati Singkong Penghasil Enzim CGT-ase (Siklodekstrin Glukanotransferase). (Skripsi). Universitas Lampung. Bandar Lampung. Scopes, R.K. 1982. Protein Purification. Springer Verlag. New York.
Shahib, M.N. 2005. Biologi: Molekular Medik I. UGM Press. Yogyakarta.
Sian HK, Said M, Hassan O, Kamaruddin K, Ismail AF, and Rahman RA. 2005. Purification and Characterization of Cyclodextrin Glucanotransferase from
Alkalophilic Bacillus sp. G1. Proc Biochem. 40:1101–11.
Sin KA, Nakamura A, Kobayashi K, Masaki H, Uozumi T. 1991. Cloning and Sequencing of a Cyclodextrin Glucanotransferase Gene from Bacillus Ohbensis and its expression in Escherichia coli. Appl Microbiol Biotechnol.
35:600–5.
Suhartono, M.T. 1989. Enzim dan Bioteknologi. PAU Bioteknologi IPB. Bogor.
Sundari, E.S. 2011. Peningkatan Kestabilan Enzim α-amilase dari Bacillus subtilis
ITBCCB148 dengan Modifikasi Kimia Menggunakan Sitrakonat Anhidrida. (Skripsi). Universitas Lampung. Bandar Lampung.
Szejtli, J. 1982. Cyclodexrtins in Food, Cosmetics and Toiletries. Starch/Starke.
Szejtli, J. 1988. Cyclodextrin Technology. Kluwer Academic Publishers,
Dordrecht. Netherlands.
Tao, B.Y. 1991. Cyclodextrin Glucanotransferases: Technology and Biocatalyst Design. In : Himmel, M. E. and Leatham, G. F. Enzyme in Biomass
Conversion. Washington, D.C. American Chemical Society. 372-383.
Tonkova, A. 1998. Bacterial Cyclodextrin Glucanotransferase. Enzyme Microbial. Technol. 22: 678-686.
Tonkova, A., Atanasofa, N., Kitayska, T., Bojadjieva, I., and Yankov, D. 2011. A novel cyclodextrin glucanotransferase from alkaliphilic Bacillus
pseudalcaliphilus 20RF: Purification and properties.Bulgaria: Elsevier.
Van der Veen, B.A., J.C.M. Uitdehaag, D. Penninga, G.J.W.M. van Aleebek, L.M. Smith, B.W. Dijkstra, and L. Dijkhuizen. 2000. Rational Design of Cyclodextrin Glycosyltransferase from Bacillus circulans Strain 251 to
Increase α-Cyclodextrin Production. J. Mol. Biol. 296: 1027-1038.
Volk, W.A. dan M.F. Wheeler. 1993. Mikrobiologi Dasar, Jilid 1, Edisi kelima.
Alih bahasa oleh Soenarto Adisoemarto, Ph.D. Erlangga. Jakarta. 396 hlm. Wiseman, Y. 1985. Hand Book of Enzyme Biotechnology. Ellis Harwood
Limited.
Whistler, R.L, J.N Bemiler, and E.F Paschall.1984. Starch: Chemistry and Technology (2nd edition). Academic Press. Inc. New York.
Winarno, F.G. 1986. Enzim Pangan. PT Gedia Pustaka Utama. Jakarta.
Yim DG, Sato YH, and Park YK. 1997. Production of cyclodextrin from starch by Cyclodexrin Glycosyltransferase from Bacillus firmus and Characterization
Lampiran 1
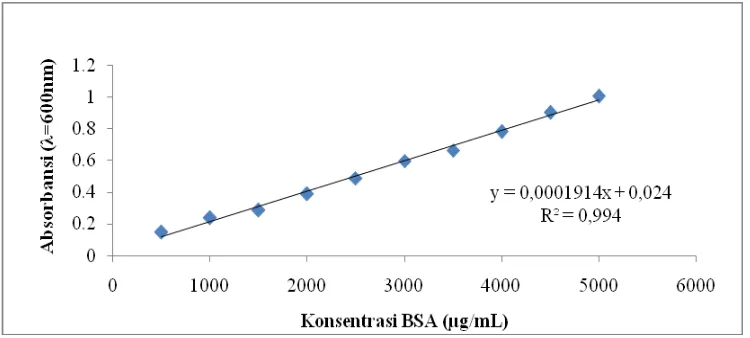
Kurva Kalibrasi Larutan Standar Bovine Serum Albumine (BSA)
[image:42.595.114.496.308.491.2]Kurva standar BSA digunakan untuk menentukan kadar protein (metode Lowry). Untuk mendapatkan gambar kurva standar BSA digunakan persamaan regresi linier Y = a + bx, dengan :
Tabel 5. Absorbansi BSA pada berbagai konsentrasi untuk menentukan kurva standar protein
Konsentrasi BSA (µg/mL) Absorbansi (λ=600 nm)
500 0,149
1000 0,238
1500 0,285
2000 0,389
2500 0,488
3000 0,598
3500 0,665
4000 0,782
4500 0,904
5000 1,005
Data yang diperoleh didapatkan nilai a = 0,024 dan b = 0,0001914 sehingga persamaan garis menjadi y = 0,0001914x + 0,024.
[image:42.595.113.488.557.726.2]Lampiran 2
Kurva Standar β-Siklodekstrin
Untuk mendapatkan nilai % OD Decrease digunakan persamaan:
% OD decrease = [(Abs.kontrol – Abs.sampel)] x 100%
[image:43.595.113.516.258.389.2]Abs.kontrol
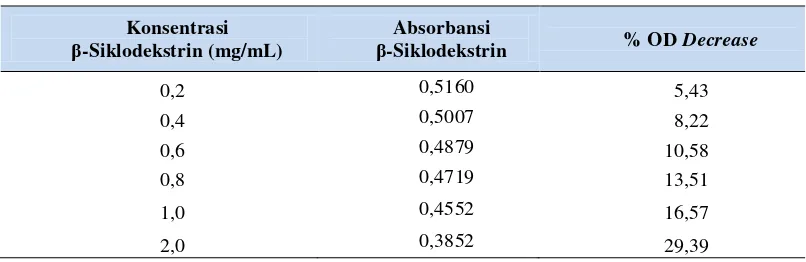
Tabel 6. %OD Decreaseβ-Siklodekstrin pada berbagai konsentrasi untuk menentukan kurva standar β-Siklodekstrin (Abs.Kontrol = 0,5456)
Konsentrasi β-Siklodekstrin (mg/mL)
Absorbansi
β-Siklodekstrin % OD Decrease
0,2 0,5160 5,43
0,4 0,5007 8,22
0,6 0,4879 10,58
0,8 0,4719 13,51
1,0 0,4552 16,57
2,0 0,3852 29,39
Data yang diperoleh didapatkan nilai a = 2,831 dan b = 13,34 sehingga persamaan garis menjadi y = 13,34x + 2,831.
[image:43.595.113.498.493.707.2]Lampiran 3
Perhitungan Aktivitas Unit
A = (%OD decrease x Yp x Df x 103) (MW x ti)
A = Aktivitas enzim untuk sampel yang tidak diketahui (U/mL atau µmol/mL)
% OD decrease = [(Abs.kontrol – Abs.sampel)] x 100%
Abs.kontrol
Yp = mg β-Siklodekstrin yang setara dengan 100% OD decrease
standar
Df = Dilutionfactor (faktor pengenceran)
ti = waktu inkubasi
Lampiran 4
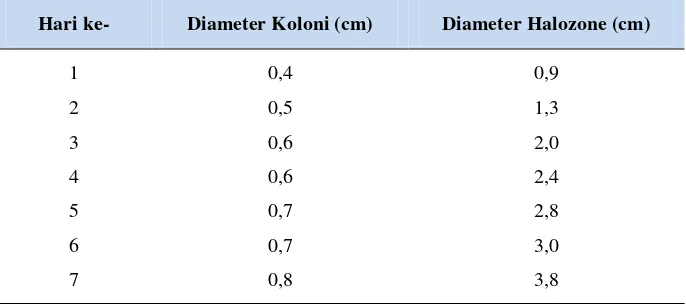
Tabel 7. Pertumbuhan koloni dan halozone isolat LTi-21-3
Hari ke- Diameter Koloni (cm) Diameter Halozone (cm)
1 0,4 0,9
2 0,5 1,3
3 0,6 2,0
4 0,6 2,4
5 0,7 2,8
6 0,7 3,0
Lampiran 5
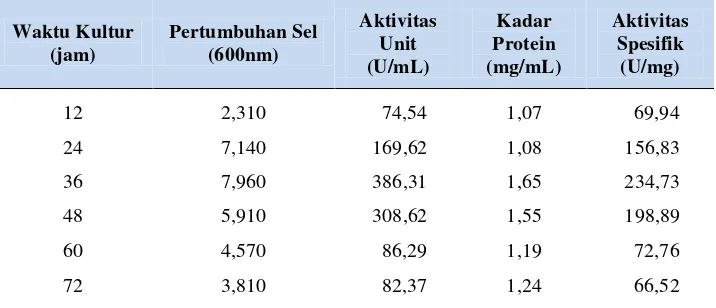
Tabel 8. Pertumbuhan isolat LTi-21-3 sumber nitrogen pepton-yeast extract
Waktu Kultur (jam) Pertumbuhan Sel (600nm) Aktivitas Unit (U/mL) Kadar Protein (mg/mL) Aktivitas Spesifik (U/mg)
12 2,310 74,54 1,07 69,94
24 7,140 169,62 1,08 156,83
36 7,960 386,31 1,65 234,73
48 5,910 308,62 1,55 198,89
60 4,570 86,29 1,19 72,76
72 3,810 82,37 1,24 66,52
Tabel 9. Pertumbuhan isolat LTi-21-3 sumber nitrogen urea-yeast extract
Waktu Kultur (jam) Pertumbuhan Sel (600nm) Aktivitas Unit (U/mL) Kadar Protein (mg/mL) Aktivitas Spesifik (U/mg)
12 1,271 67,87 0,50 136,74
24 5,530 71,91 0,87 82,42
36 6,273 128,09 1,30 98,46
48 5,723 58,08 0,72 81,15
60 4,372 31,46 0,64 49,36
[image:46.595.114.474.378.530.2]Lampiran 6
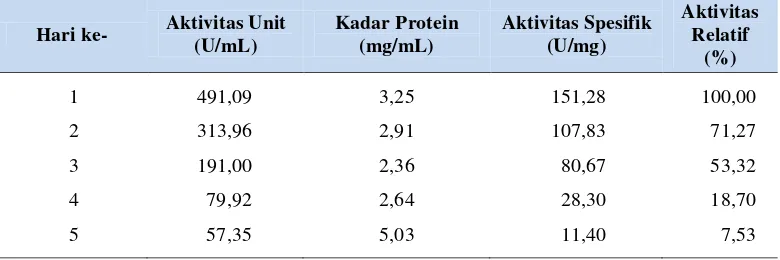
Tabel 10. Kestabilan ekstrak kasar enzim CGT-ase isolat LTi-21-3
Hari ke- Aktivitas Unit (U/mL)
Kadar Protein (mg/mL)
Aktivitas Spesifik (U/mg)
Aktivitas Relatif
(%)
1 491,09 3,25 151,28 100,00
2 313,96 2,91 107,83 71,27
3 191,00 2,36 80,67 53,32
4 79,92 2,64 28,30 18,70
Lampiran 7
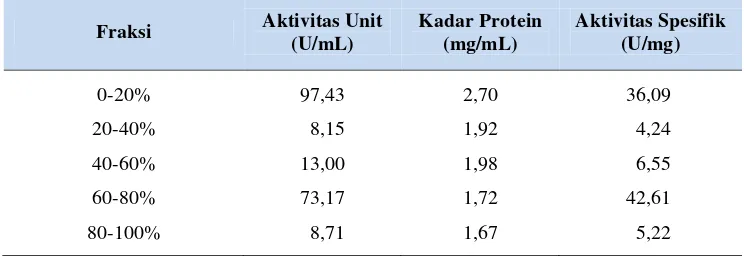
Tabel 11. Pemurnian enzim CGT-ase dari isolat LTi-21-3 dengan fraksinasi ammonium sulfat
Fraksi Aktivitas Unit
(U/mL)
Kadar Protein (mg/mL)
Aktivitas Spesifik (U/mg)
0-20% 97,43 2,70 36,09
20-40% 8,15 1,92 4,24
40-60% 13,00 1,98 6,55
60-80% 73,17 1,72 42,61
80-100% 8,71 1,67 5,22
Lampiran 8
Tabel 12. Pengaruh temperatur terhadap aktivitas enzim CGT-ase
Temperatur (OC)
Aktivitas Unit (U/mL) Kadar Protein (mg/mL) Aktivitas Spesifik (U/mg) Aktivitas Relatif (%)
45 193,39 1,55 125,14 28
50 523,15 1,55 338,51 77
55 627,95 1,55 406,32 92
60 682,67 1,55 441,73 100
65 250,61 1,55 162,16 37
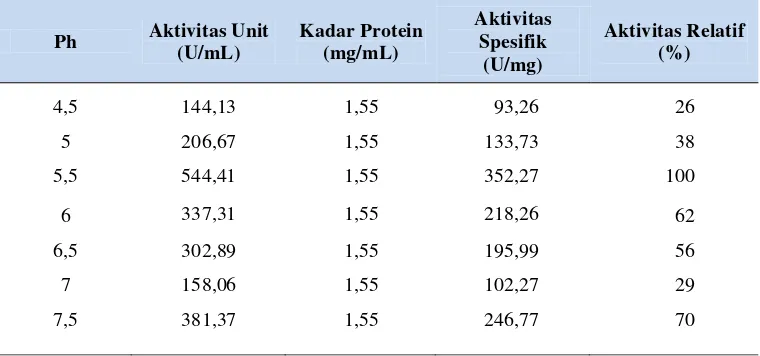
Tabel 13. Pengaruh pH terhadap aktivitas enzim CGT-ase
Ph Aktivitas Unit
(U/mL) Kadar Protein (mg/mL) Aktivitas Spesifik (U/mg) Aktivitas Relatif (%)
4,5 144,13 1,55 93,26 26
5 206,67 1,55 133,73 38
5,5 544,41 1,55 352,27 100
6 337,31 1,55 218,26 62
6,5 302,89 1,55 195,99 56
7 158,06 1,55 102,27 29
[image:49.595.113.493.383.561.2]Lampiran 9
Tabel 14. Data untuk penentuan konstanta kinetik enzim CGT-ase dari isolat LTi-21-3 berdasarkan persamaan Lineweaver-Burk
Soluble Starch (mg/mL)
Aktivitas Unit (U/mL)
1/S
(mL/mg) 1/V (ml/U)
2.5 111,29 0,40 0,008985
5 154,83 0,20 0,006459
7.5 202,10 0,13 0,004948
10 265,57 0,10 0,003766
12.5 297,77 0,08 0,003358
15 327,66 0,07 0,003052
17.5 341,65 0,06 0,002927
20 356,24 0,05 0,002807
Tabel 15. Spesisitas substrat enzim CGT-ase dari isolat LTi-21-3
Jenis Pati Aktivitas Unit (U/mL) Kadar Protein (mg/mL) Aktivitas Spesifik (U/mg) Aktivitas Relatif (%)
Pati Jagung 263,45 1,55 170,47 48
Pati Singkong 205,75 1,55 133,14 38
Pati Ubi Jalar 108,89 1,55 70,46 20
Soluble Starch 544,41 1,55 352,27 100
[image:50.595.112.487.433.559.2]