DAUN TANAMAN PADI
FADHILA ACHMAD SYACHRONI
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Penyakit Hawar Pelepah Daun Tanaman Padi. Dibimbing oleh NISA RACHMANIA MUBARIK dan YADI SURYADI.
Penyakit hawar pelepah daun (HPD) banyak ditemukan pada tanaman padi dan menurunkan hasil produksi. Penyakit HPD disebabkan oleh Rhizoctonia solani. Pengendalian penyakit HPD dapat menggunakan fungisida dan varietas resisten. Penggunaan bakteri sebagai agen pengendali yang ramah lingkungan menjadi penting dan harus dikembangkan. Penelitian ini bertujuan mengetahui efektivitas formulasi dari konsorsium bakteri sebagai pengendali penyakit HPD. Uji kompatibilitas dilakukan dengan uji antagonis menggunakan metode kultur berpasangan. Pembuatan formulasi biokontrol dengan menggunakan tiga jenis bahan pembawa yaitu talk, bentonit, dan minyak sayur. Aplikasi formulasi biokontrol dengan cara perendaman benih dengan formulasi dan penyemprotan forrmulasi secara langsung. Hasil uji kompatibilitas didapatkan dua formula terbaik yaitu A2 yang merupakan isolat bakteri Bacillus firmus E65, serta A8 merupakan konsorsium bakteri B. firmus E65, B. cereus II.14, Pseudomonas aeruginosa C32b, dan Serratia marcescens E31. Berdasarkan aplikasi formulasi terhadap penyakit HPD, formula A8 dengan bentonit merupakan formulasi yang paling efektif.
Kata kunci : padi, agen pengendali hayati, hawar pelepah daun, Rhizoctonia solani
ABSTRACT
FADHILA ACHMAD SYACHRONI. Effectiveness Formulation of Bacterial Consortia for Controlling Sheath Blight Disease on Rice Plants. Supervised by NISA RACHMANIA MUBARIK and YADI SURYADI.
Sheath blight disease caused by Rhizoctonia solani is mostly found in rice and reduce its production. Controlling this disease could be used a fungicide or resistant varieties. The use of bacteria as biocontrol agents are environmentally friendly and need to be explored. This study was aimed to determine the effectiveness of the consortium of bacteria to control sheath blight disease. The compatibility test in the antagonist test was dual culture method. Biocontrol formulation was used three carriers ie talc, bentonite, and vegetable oil. Aplication of the biocontrol formulation can done by soaking with formulation and direct spraying formulation to plant. Compatibility test results found the best formula was A2 consisted Bacillus firmus E65, and A8 formula consisted of a mixture of Bacillus firmus E65, Serratia marcescens E31, Pseudomonas aeruginosa C32b, and
Bacillus cereus II.14. Based on aplication formulation to sheath blight desease, it was found that formula A8 with bentonite is the most effective formulation.
DAUN TANAMAN PADI
FADHILA ACHMAD SYACHRONI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Biologi
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
NIM
: G34070098
Menyetujui,
Mengetahui,
Ketua Departemen Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Ir. Ence Darmo Jaya Supena, M.S.
NIP 19641002 198903 1 002
Tanggal Lulus:
Pembimbing I
Dr. Nisa Rachmania Mubarik, M.Si.
NIP 19671127 199302 2 001
Pembimbing II
ilmiah ini berhasil diselesaikan. Judul yang dipilih dalam penelitian yang dilaksanakan sejak Februari hingga Juli 2011 ini ialah Efektivitas Konsorsium Bakteri sebagai Pengendali Penyakit Hawar Pelepah Daun Tanaman Padi. Penelitian ini dilaksanakan di Laboratorium Konservasi Mikrob dan Rumah Kaca Balai Besar Bioteknologi dan Sumberdaya Genetika Pertanian (BB Biogen).
Terima kasih penulis ucapkan kepada Ibu Dr. Nisa Rachmania Mubarik, M.Si dan Bapak Ir. Yadi Suryadi, M.Sc atas bimbingan, bantuan pendanaan, dan pengarahan yang diberikan selama penelitian dan penyusunan skripsi ini. Terima kasih disampaikan pula kepada Bapak Dr. Ir. Dedy Duryadi Solihin, DEA sebagai dosen penguji dan wakil komisi pendidikan atas saran dan diskusi yang diberikan. Ungkapan terima kasih juga disampaikan kepada Papah Arin Syachroni, Mamah Sudrajati Asih, Adikku Renny Sithi Fauziah dan M. Ilham Syachroni, serta seluruh keluarga atas segala doa dan kasih sayangnya. Penulis juga mengucapkan terima kasih kepada Aidatun Fitriyah, Kosmas, Nisful, Henny, Komal, Rahmah, Fahmi, Rindi, Eko, Alma, Nia, Susan, Adian, Ari, Wagner, bapak dan ibu yang membantu penulis di laboratorium Konservasi Mikrob BB Biogen, Ibu Aminah, Pak Jajang, Pak Eep, Ibu Endang, Mas Alan, Ibu Yuli, dan teman-teman Biologi 44 atas segala doa, dukungan, dan perhatiannya.
Semoga karya ilmiah ini bermanfaat.
Bogor, September 2011
ibu Sudrajati Asih. Penulis merupakan anak pertama dari tiga bersaudara.
Tahun 2007 penulis lulus dari SMA Negeri 65 Jakarta dan pada tahun yang sama lulus seleksi masuk IPB melalui Seleksi Penerimaan Mahasiswa Baru (SPMB). Penulis memilih Program Studi Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis aktif menjadi anggota Divisi Bioworld Himpunan Mahasiswa Biologi (Himabio) pada tahun 2008-2009, penanggung jawab acara Biologi on Show (BIOS) dalam rangkaian acara Biologi Interaktif tahun 2009, Ketua Divisi Informasi dan Komunikasi (Infokom) Himabio pada tahun 2009-2010, Ketua Divisi Tata terib (Tatib) Masa Perkenalan Departemen (MPD) tahun 2010, Ketua Divisi Pertandingan acara Grand Biodiversity tahun 2010. Penulis menjadi asisten praktikum mata kuliah Biologi Dasar Tingkat Persiapan Bersama pada tahun ajaran 2010/2011, dan mata kuliah Mikrobiologi Dasar pada tahun ajaran 2010/2011.
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN Latar Belakang ... 1
Tujuan ... 1
BAHAN DAN METODE Bahan ... 1
Peremajaan Isolat Bakteri ... 1
Peremajaan Isolat Cendawan Patogen (Rhizotocnia solani)... 2
Uji Kompatibilitas Bakteri terhadap R. solani secara in vitro ... 2
Uji Antagonis Cendawan Patogen R. solani dengan Formula Terbaik ... 2
Pembuatan Bahan Pembawa Agensia Biokontrol dengan Formula Terbaik ... 3
Aplikasi Formulasi Bahan Pembawa Agensia Biokontrol terhadap R. solani secara in-vivo ... 3
HASIL Kompatibilitas Bakteri Endofitik terhadap R. solani secara in vitro ... 3
Uji Antagonis Cendawan Patogen R. solani dengan Formula Terbaik ... 4
Aplikasi Formulasi Bahan Pembawa Agensia Biokontrol terhadap R. solani secara in-vivo ... 4
PEMBAHASAN... 5
SIMPULAN DAN SARAN Simpulan ... 7
Saran ... 7
DAFTAR PUSTAKA ... 7
2 Perlakuan formulasi isolat yang digunakan pada penelitian ... 2
3 Luas pertumbuhan dan luas zona hambat R. solani hasil uji kompatibilitas isolat secara in vitro ... 4
4 Luas pertumbuhan dan luas zona hambat R. solani pada uji antagonis R. solani dengan formula A2 dan A8 ... 4
5 Hasil pengamatan jumlah anakan, panjang akar, bobot basah, dan bobot kering tanaman padi ... 5
DAFTAR GAMBAR
Halaman 1 Desain uji kompatibilitas formula terhadap cendawan patogen R. solani secara in vitro ... 22 Penghambatan pertumbuhan R.solani uji kompatibilitas oleh formula A2 (a) dan formula A8 (b) pada media Potato Dextrose Agar ... 3
3 Penghambatan pertumbuhan R.solani uji antagonis oleh formula A2 (a) dan formula A8 (b) pada media PDA ... 4
4 Grafik pengamatan TLR penyakit HPD pada tanaman padi ... 4
DAFTAR LAMPIRAN
Halaman 1 Komposisi media tumbuh bakteri dan cendawan ... 102 Hasil uji kompatibilitas formula dengan R.solani ... 11
3 Hasil aplikasi formulasi terhadap penyakit HPD ... 12
4 Hasil uji kompatibilitas formula terhadap R.solani ... 13
5 Hasil uji antagonis formula terhadap R.solani ... 13
6 Jumlah anakan tanaman padi ... 14
7 Panjang akar tanaman padi ... 14
8 Bobot basah dan bobot kering tanaman padi ... 15
9 Hasil pengamatan TLR, AUDPC, dan persentase penghambatan penyakit HPD pada tanaman padi ... 15
10 Viabilitas isolat bakteri bulan ke-0... 16
11 Viabilitas isolat bakteri pada formulasi bulan ke-1 ... 16
12 Viabilitas isolat bakteri pada formulasi bulan ke-2 ... 16
Indonesia sebagai negara agraris, dengan mata pencaharian utama penduduk Indonesia bergerak pada sektor pertanian. Produksi padi Indonesia tahun 2010 sekitar 65,98 juta ton (BPS 2010). Permasalahan utama produksi padi Indonesia antara lain penyakit yang menyerang tanaman padi, seperti penyakit blas oleh Pyricularia grisea (Utami et al.
2006), hawar daun bakteri (HDB) oleh
Xanthomonasoryzae (Dewi et al. 2007), dan penyakit hawar pelepah daun (HPD) akibat cendawan Rhizoctonia solani (Prayudi 2000).
Hawar pelapah daun dapat menyerang tanaman padi pada tahap benih, hingga dewasa sebelum waktu panen, penyakit ini menyebabkan tanaman mudah rebah (Deptan 2009). Pengendalian penyakit HPD dapat dilakukan dengan penggunaan tanaman yang resisten dan cara pemberian fungisida (Lee & Rush 1983). Pemberian fungisida pada jangka panjang dengan dosis yang berlebihan dapat memberikan dampak yang negatif. Pengendali hayati dapat digunakan karena jauh lebih aman dari pada penggunaan bahan kimia (Ardakani et al. 2009). Selain itu, pengendali hayati juga dapat memberikan manfaat ganda memacu pertumbuhan tanaman (pupuk hayati) dan mengendalikan patogen tanaman (biopestisida) (Kumar et al.
2005).
Bakteri yang dapat digunakan sebagai agen hayati pengendali penyakit akibat R. solani yang menyerang tanaman, antara lain:
Pseudomonas aeruginosa (Perveen et al.
1998), Serratia marcescens (Someya et al.
2000), dan Bacillus spp. (Asaka & Shoda 1996). Bacillus spp. dapat digunakan sebagai agen pengendali hayati yang aman dan lebih efektif dari pada penggunaan bahan kimia. Spesies B. firmus E65, S. marcescens dan P. aeruginosa yang akan digunakan dalam penelitian ini dilaporkan Putri (2010) memiliki kemampuan menekan pertumbuhan
Rhizoctonia solani penyebab hawar pelepah (sheath blight) secara in vivo maupun in vitro. Bacillus merupakan bakteri Gram positif penghasil endospora sehingga tahan
(Mubarik et al. 2010). Sedangkan
Pseudomonas dan Serratia termasuk bakteri Gram negatif yang dapat tumbuh pada kondisi nutrisi sederhana dan mudah berkolonisasi di rhizosfer (Pseudomonas) dan filosfer (Serratia) tanaman padi. Bahan pembawa formulasi yang banyak digunakan dalam pengendali hayati antara lain bentuk padat (granul), tepung, dan suspensi (Ardakani et al. 2009).
Tujuan
Penelitian ini bertujuan mengetahui efektivitas beberapa formulasi dari konsorsium bakteri sebagai pengendali penyakit HPD pada tanaman padi.
Hipotesis yang digunakan dalam penelitian ini bahwa formulasi konsorsium bakteri sebagai pengendali penyakit hawar pelepah daun pada tanaman padi lebih efektif dari pada bukan konsorsium.
BAHAN DAN METODE
Bahan
Bakteri Bacillus firmus E65,
Pseudomonas aeruginosa C32b, Seratia marcescens E31, cendawan Rhizoctonia solani, dan bibit padi IR-64 yang digunakan pada penelitian ini berasal dari koleksi Laboratorium Konservasi Mikrobiologi BB Biogen. Selain itu juga terdapat isolat bakteri koleksi Laboratorium Mikrobiologi Departemen Biologi, FMIPA, IPB dan IPB
Culture Collection yaitu Bacillus cereus II.14 (Tabel 1).
Peremajaan Isolat Bakteri
Semua isolat bakteri diperbanyak dengan memindahkan kultur pada medium nutrient agar (NA) dan diinkubasi pada suhu ruang selama 24-48 jam. Isolat tersebut diremajakan dan diperiksa kemurniannya dengan menggunakan metode kuadran. Biakan yang telah murni ditumbuhkan pada media agar-agar miring dan disimpan dalam lemari pendingin pada suhu -20oC.
Tabel 1 Daftar isolat bakteri yang digunakan pada penelitian.
Kode isolat Spesies bakteri Asal isolat Tahun koleksi
Seluruh biakan bakteri yang telah diinkubasi selama 24 jam pada media agar-agar miring NA dilakukan pengenceran serial menggunakan garam fisologis 0,85% dan dihitung jumlahnya dengan menggunakan metode angka lempeng total (ALT).
Peremajaan Isolat Cendawan Patogen (Rhizotocnia solani)
Cendawan R. solani ditumbuhkan pada media potato dextrose agar (PDA), lalu diinkubasi selama 1 minggu pada suhu ruang (Putri 2010). Peremajaan cendawan pada media PDA dilakukan setiap satu bulan sekali.
Uji Kompatibilitas Bakteri terhadap R. solani secara in vitro
Pengujian dilakukan dengan metode kultur berpasangan yaitu dengan cara bakteri dan cendawan patogen R. solani
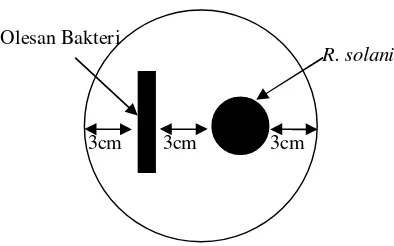
ditumbuhkan pada cawan Petri yang berisi media PDA. Masing-masing bakteri ditumbuhkan pada media kaldu nutrien (NB) dan diinkubasi selama 24 jam. Sebanyak 1 lup suspensi bakteri dioleskan pada cawan PDA sepanjang 3 cm. Potongan biakan murni
R. solani pada media PDA dipindahkan dengan menggunakan bor gabus, diletakkan berhadapan dengan olesan bakteri dan berjarak 3 cm dari olesan bakteri (Gambar 1). Perlakuan yang digunakan sebanyak sepuluh perlakuan dengan tiga ulangan setiap perlakuan, kontrol negatif menggunakan olesan air, dan kontrol kimia menggunakan fungisida streptomisin 2% yang dilarutkan pada media PDA (Tabel 2).
Gambar 1 Desain uji kompatibilitas formula terhadap cendawan patogen R. solani secara in vitro.
Diameter zona pertumbuhan cendawan patogen yang terbentuk diukur setelah diinkubasi selama 7 hari pada suhu ruang.
Pengukuran zona pertumbuhan cendawan dengan cara:
Zonaper tumbuhancendaw an = r 1 + r 2 2 r1 adalah jari-jari zona pertumbuhan miselia terpanjang, r2 adalah jari-jari pertumbuhan miselia terpendek (Suryadi 2009).
Luas zona hambat (ZH) dihitung dengan rumus : ZH = LC – LP, ZH adalah luas zona hambat, LC adalah luas cawan (cm2), dan LP adalah luas pertumbuhan cendawan patogen
R. solani (cm2) (Putri 2010). Dua perlakuan terbaik digunakan untuk pengujian lebih lanjut.
Tabel 2 Perlakuan formulasi isolat yang digunakan pada penelitian
Kode
perlakuan Isolat
A0 Kontrol air
A1 Bacillus cereus (II.14) A2 Bacillus firmus (E65)
A3 Pseudomonas aeruginosa
(C32b)
A4 Seratia marcescens (E31) A5 B. firmus (E65) + P. aeruginosa
(C32b)
A6 B. cereus (II.14) + B. firmus
(E65) + P. aeruginosa (C32b) A7 B. cereus (II.14) + P.
aeruginosa (C32b) + S. marcescens (E31)
A8 B. cereus (II.14) + P. aeruginosa (C32b) + S. marcescens (E31) + B. firmus
(E65)
A9 Kontrol kimia (Streptomisin 2%)
Uji Antagonis Cendawan Patogen R. solani
dengan Formula Terbaik
Perlakuan terbaik dari hasil uji kompatibilitas digunakan dalam uji antagonis cendawan R. solani. Bakteri tiap-tiap formula terbaik ditumbuhkan pada media kaldu nutrien dan diinkubasi selama satu hari, semua perlakuan dilakukan ulangan sebanyak tujuh kali ulangan. Sebanyak 1 ml suspensi biakan disentrifugasi dengan kecepatan 8944 g selama 5 menit. Sebanyak 100 µl supernatan (filtrat) bakteri dicampurkan dengan media PDA dan dituang ke cawan Petri. Cendawan R. solani diletakkan di atas media PDA yang berisi supernatan bakteri dan diinkubasi selama satu minggu, kemudian dihitung zona hambat cendawan 3cm 3cm 3cm
R. solani
dibandingkan dengan kontrol tanpa perlakuan.
Pembuatan Bahan Pembawa Agensia Biokontrol dengan Formula Terbaik
Dua formula terbaik diujikan pada berbagai bahan pembawa (Ardakani et al.
2009). Bahan pembawa yang digunakan antara lain formulasi talk (300 ml suspensi formula bakteri, 1 Kg talk, 10 g
carboxymethyl cellulose (CMC), 15 g CaCO3), formulasi bentonit (300 ml suspensi formula bakteri, 1 Kg bentonit, 10 g CMC, 15 g CaCO3), formulasi minyak (300 ml suspensi formula bakteri, 6 ml minyak sawit, 0,15 ml Triton X-100), dan formulasi suspensi (300 ml suspensi formula bakteri).
Aplikasi Formulasi Bahan Pembawa Agensia Biokontrol terhadap R. solani
secara in-vivo
Bibit padi yang digunakan ialah varietas IR-64. Bibit padi disemai dengan menggunakan tanah sawah pada bak plastik berukuran 15x30 cm2. Penyemaian dilakukan selama 18 hari. Bibit padi yang telah berumur 18 hari direndam pada 100 ml tiap-tiap formulasi selama satu malam, kemudian ditanam pada pot-pot kecil yang berisi tanah sawah sebanyak 3 Kg dan pupuk NPK (1:1:1). Setiap perlakuan dilakukan tiga kali ulangan. Aplikasi pada tanaman padi dilakukan dengan cara penyemprotan langsung. Sebanyak 100 ml tiap-tiap formulasi disemprotkan pada 6 rumpun padi pada pot-pot. Aplikasi pertama dilakukan pada umur 28 hari setelah tanam (hst) dan penyemprotan kedua dilakukan pada umur 42 hst.
Cendawan patogen R. solani ditumbuhkan pada media PDA. Kemudian potongan agar-agar ± 4 cm2 yang berisi cendawan patogen
R. solani disisipkan pada bagian pangkal padi. Inokulasi cendawan patogen R. solani
dilakukan pada umur 30 hst. Pengamatan penyakit HPD dilakukan setiap 7 hari setelah inokulasi sebanyak empat kali pengamatan dibandingkan dengan dua kontrol yang digunakan antara lain kontrol cendawan dan kontrol tanpa perlakuan. Kontrol cendawan adalah kontrol tanaman padi yang hanya disisipkan cendawan R. solani tanpa pemberian formulasi, sedangkan kontrol tanpa perlakuan adalah kontrol tanaman padi yang tidak disisipkan cendawan R. solani dan formulasi. Pengamatan intensitas penyakit HPD dengan mengukur tinggi lesio relatif (TLR) (Suryadi et al. 1991):
TLR = panjanglesio
tinggitanaman × 100% Nilai yang didapat dari perhitungan TLR kemudan dikonversi dengan perhitungan area under the disease progress curve (AUDPC). Perhitungan AUDPC bertujuan untuk mengetahui hubungan antara intensitas penyakit terhadap respon waktu (Shaner & Finney 1977):
= +
2 ( − )
n = jumlah pengamatan ti = waktu pengamatan Yi = intensitas penyakit HPD
Selain dilakukan pengamatan intensitas penyakit HPD pada tanaman padi juga dilakukan pengamatan agronomi terhadap formulasi yang diberikan pada tanaman padi yang meliputi jumlah anakan, panjang akar, bobot basah dan bobot kering. Data yang didapat dibandingkan dengan dua kontrol, antara lain kontrol cendawan dan kontrol tanpa perlakuan.
HASIL
Kompatibilitas Bakteri terhadap R. solani
secara in vitro
Uji kompatibilitas menunjukkan beberapa formula mampu menekan pertumbuhan R. solani dengan terbentuknya zona hambat. Pada perlakuan kontrol, R. solani dapat tumbuh memenuhi cawan Petri. Formula A8 menunjukkan zona hambat paling besar, yaitu 62,47 cm2 jika dibandingkan dengan kontrol streptomisin 2% dengan zona hambat 55,92 cm2(Gambar 2, Tabel 3).
(a) (b)
Gambar 2 Penghambatan pertumbuhan R. solani uji kompatibilitas oleh (a) formula A2 dan (b) formula A8 pada media potato dextrose agar
Luas R. solani yang tumbuh pada formula A8 tidak berbeda nyata dengan luas R. solani
yang tumbuh pada kontrol kimia streptomisin 2% (Tabel 3). Pengujian berikutnya formula A2 yang mengandung isolat tunggal B. firmus
E65 yang memiliki rata-rata luas zona hambat tertinggi setelah formula A8 digunakan sebagai pembanding.
Tabel 3 Luas pertumbuhan dan luas zona hambat R. solani hasil uji kompatibilitas isolat secara in vitro Kode formula Rata-rata luas pertumbuhan R. solani
(cm2)
Rata-rata luas zona hambat
R. solani
(cm2)
A0 63,59 a 0 a
A1 61,29 a 2,29 a
A2 21,67 bc 41,92 bc
A3 63,59 a 0 a
A4 63,59 a 0 a
A5 45,15 ab 18,43 ab A6 42,65 ab 20,93 ab
A7 63,59 a 0 a
A8 1,11 c 62,47 c
A9 7,67 c 55,92 c
Keterangan : angka pada kolom yang diikuti dengan huruf yang sama tidak berbeda nyata berdasarkan uji jarak berganda Duncan (DMRT) pada taraf 5%.
Uji Antagonis Cendawan Patogen R. solani
dengan Formula Terbaik
Uji antagonis menunjukkan formula A2 dan A8 tidak berbeda nyata dengan uji kompatibilitas. Formula A2 menunjukkan nilai rata-rata luas zona hambat R. solani
mencapai 55,73 cm2, namun R. solani
tumbuh dengan rata-rata luas pertumbuhan sebesar 7,86 cm2. Hal ini berbeda dengan
formula A8 yang menunjukkan rata-rata luas zona hambat sebesar 63,59 cm2 dan tidak ada pertumbuhan R. solani. Jika dibandingkan dengan kontrol rata-rata zona hambat sebesar 0 cm2(Gambar 3, Tabel 4).
Tabel 4 Luas pertumbuhan dan luas zona hambat R. solani pada uji antagonis R. solani dengan formula A2 dan A8
Perlakuan
Rata-rata luas pertumbuhan
R. solani (cm2)
Rata-rata luas zona hambat R.
solani (cm2)
A2 7,86 55,73
A8 0 63,59
Kontrol tanpa perlakuan
63,59 0
Aplikasi Formulasi Bahan Pembawa Agensia Biokontrol terhadap R. solani
secara in-vivo
Hasil pengamatan penyakit HPD pada tanaman padi selama empat minggu menunjukkan formula yang efektif untuk menghambat pertumbuhan penyakit HPD ialah formula A2 dengan formulasi bentonit, sedangkan formula yang kurang efektif ialah formula A8 formulasi suspensi.
(a) (b) Gambar 3 Penghambatan pertumbuhan R.
solani uji antagonis oleh (a) formula A2 dan (b) formula A8 pada media PDA.
Keterangan : TLR : tinggi lesio relatif penyakit HPD.
Gambar 4 Grafik pengamatan TLR penyakit HPD pada tanaman padi. 0 2 4 6 8 10 12 14 16 minggu ke 0 minggu ke 1 minggu ke 2 minggu ke 3 minggu ke 4 P er se n ta se T L R (%)
Tinggi Lesio Relatif (TLR)
A2 talk A2 bentonit A2 minyak A2 suspensi A8 talk A8 bentonit A8 minyak A8 suspensi
Formula A2 dengan formulasi bentonit memiliki persentase penghambatan HPD sebesar 35,57% dengan nilai AUDPC yaitu 225,49. Sedangkan formula A8 formulasi suspensi memiliki persentase penghambatan HPD 12,69% dengan nilai AUDPC 305,59 (Lampiran 9). Pada formula A2 formulasi minyak semua tanaman padi mengalami kematian, dan formula A8 formulasi minyak selain menghambat pertumbuhan penyakit HPD juga menghambat pertumbuhan tanaman padi.
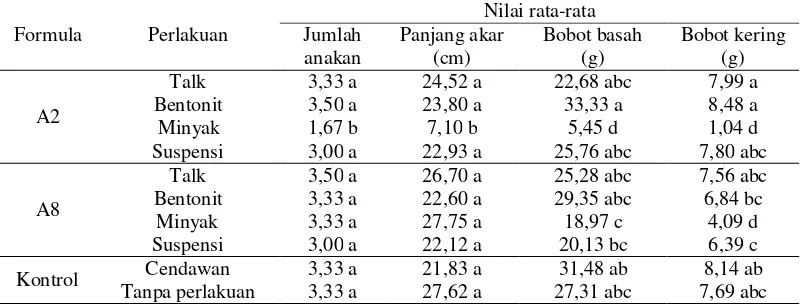
Pengamatan agronomi meliputi jumlah anakan, panjang akar, bobot basah, dan bobot kering. Hasil pengamatan agronomi didapatkan jumlah anakan dan panjang akar pada tiap-tiap perlakuan tidak berbeda nyata, dengan rata-rata jumlah anakan 1,67 sampai 3,50 anakan, sedangkan untuk panjang akar rata-rata 7,10 cm sampai 27,75 cm. Rata-rata bobot basah tertinggi untuk perlakuan ialah formula A2 perlakuan bentonit dengan rata-rata 33,33 g, bobot basah terendah ialah formula A2 perlakuan minyak sebesar 5,45 g, jika dibandingkan dengan kontrol negatif yang memiliki bobot basah 31,48 g. Untuk bobot kering terberat ialah formula A2 dengan perlakuan bentonit yaitu 8,48 g, bobot kering teringan ialah formula A2 perlakuan minyak sebesar 1,04 g, dan untuk bobot kering kontrol negatif sebesar 8,14 g (Tabel 5).
PEMBAHASAN
Hasil uji kompatibilitas menunjukkan dua formula terbaik yaitu formula A2 yang mengandung isolat B. firmus E65 dan formula A8 yang merupakan konsorsium isolat B. firmus E65, B. cereus II.14, S. marcescens E31, dan P. aeruginosa C32b.
Semua isolat yang digunakan dilaporkan dapat menekan pertumbuhan dari R. solani
(Putri 2010). Uji antagonis formula terbaik juga tidak berbeda nyata dengan uji kompatibilitas, hal ini menunjukkan bahwa formula A2 dan A8 yang digunakan efektif dalam menekan pertumbuhan R. solani secara
in vitro.
Berdasarkan uji kompatibilitas dan uji antagonis, isolat yang digunakan mampu menekan pertumbuhan R. solani karena diduga memiliki senyawa antimikrob (Putri 2010) dan menghasilkan enzim kitinase yang m en d eg r a d a si k i t i n ya n g m er u p a k a n komponen utama dinding sel cendawan (Mubarik et al. 2010). Senyawa antimikrob adalah senyawa yang dapat membunuh atau men ghambat per tumbuhan mikr ob lain (Rach man 2011). Sen ya wa an timikr ob yang dihasilkan oleh bakteri antara lain, iturin yang dihasilkan oleh Bacillus (Asaka & Shoda 1996), pyrrolnitrin oleh P. aeruginosa
(Howell & Stipanovic 1979). S. marcescens
menghasilkan enzim kitinolitik yang mampu mendegradasi kitin yang merupakan komponen dinding sel dari R. solani (Someya
et al. 2000).
Berdasarkan hasil uji in vivo nilai TLR mengalami nilai maksimal serangan cendawan R. solani pada minggu kedua, dan pada minggu ketiga intensitas serangan mengalami penurunan. Hal ini diduga karena pada minggu kedua tanaman padi dilakukan perlakuan penyemprotan dengan formulasi agen hayati sehingga intensitas serangan pada minggu ketiga mengalami penurunan yang terjadi hingga minggu keempat pengamatan TLR.
Tabel 5 Hasil pengamatan jumlah anakan, panjang akar, bobot basah, dan bobot kering tanaman padi
Formula Perlakuan
Nilai rata-rata Jumlah anakan Panjang akar (cm) Bobot basah (g) Bobot kering (g) A2
Talk 3,33 a 24,52 a 22,68 abc 7,99 a
Bentonit 3,50 a 23,80 a 33,33 a 8,48 a
Minyak 1,67 b 7,10 b 5,45 d 1,04 d
Suspensi 3,00 a 22,93 a 25,76 abc 7,80 abc
A8
Talk 3,50 a 26,70 a 25,28 abc 7,56 abc
Bentonit 3,33 a 22,60 a 29,35 abc 6,84 bc
Minyak 3,33 a 27,75 a 18,97 c 4,09 d
Suspensi 3,00 a 22,12 a 20,13 bc 6,39 c
Kontrol Cendawan 3,33 a 21,83 a 31,48 ab 8,14 ab
Tanpa perlakuan 3,33 a 27,62 a 27,31 abc 7,69 abc Keterangan : angka pada kolom yang diikuti dengan huruf yang sama tidak berbeda nyata
Mekanisme serangan cendawan R. solani
dimulai karena R. solani tertarik dengan simultan yang dikeluarkan oleh tanaman, hifa
R. solani melekat pada permukaan luar tanaman, setelah melekat R. solani
membentuk apresorium dan melakukan penetrasi terhadap dinding sel tanaman, penetrasi pada dinding sel tanaman juga dibantu dengan adanya enzim ekstraseluler yang mendegradasi beberapa komponen penyusun dinding sel tanaman antara lain selulosa, kutin, dan pektin. Setelah berhasil merusak sel tanaman dan mengambil nutrisi dari tanaman R. solani akan membentuk sklerotium, sklerotium merupakan bentuk pertahanan R. solani sehingga mampu bertahan pada kondisi yang sangat sederhana dan mampu tumbuh kembali pada kondisi nutrisi yang berlimpah dengan membentuk hifa untuk serangan berikutnya (Muis 2007).
Fomula A2 dengan bahan pembawa bentonit merupakan formulasi yang paling efektif menekan pertumbuhan R. solani pada tanaman padi. Dua penelitian sebelumnya melaporkan bahwa B. firmus E65 memiliki kemampuan yang paling baik dalam menghambat pertumbuhan R. solani (Putri 2010; Rachman 2011). Isolat B. firmus E65 merupakan isolat yang digunakan dalam formula A2. Ardakani et al. (2009) melaporkan bentuk formulasi biokontrol bentonit dengan penambahan CMC merupakan bentuk yang paling efektif. Bentonit berupa bubuk yang sangat halus, ringan, dan mudah menyerap banyak cairan karena kapasitas serap yang meningkat sehingga jumlah sel bakteri yang terikat lebih banyak dari formulasi lain (Ting et al. 2009). Formulasi bentonit memiliki keuntungan yang lain yaitu sangat efiesien dalam pembuatannya. Selain itu, formulasi bentonit mudah larut dalam air pada saat aplikasi pada tanaman. Dengan demikian formulasi ini merupakan bahan pembawa yang tepat untuk biokontrol penyakit HPD tanaman padi.
Formulasi talk merupakan formulasi yang cukup baik, namun tidak sebaik bentonit dalam menekan penyakit HPD. Sama seperti formulasi bentonit, talk merupakan bubuk yang ringan dan mudah larut dalam air, namun formulasi ini sedikit sulit pada saat pencampuran untuk formulasi sehingga masih terbentuk gumpalan-gumpalan. Formulasi minyak menunjukkan ketidakefektifan pada setiap perlakuan, diduga karena komposisi pada formulasi minyak kurang tepat dan perlu dilakukan modifikasi untuk menentukan komposisi
yang tepat. Jika dilihat dari segi ekonomi formulasi talk lebih murah dari formulasi bentonit, namun dari segi efektifitas dan kemudahan dalam pengaplikasian formulasi bentonit lebih efektif dan mudah, karena kelebihan dari formulasi bentonit tersebut.
Daya simpan formulasi pada suhu ruang, untuk bulan ke-0 yaitu pada saat isolat belum dicampurkan dengan formulasi memiliki rata-rata jumlah sel 40x108 cfu/ml (Lampiran 10). Pada bulan pertama penyimpanan jumlah sel bakteri pada formulasi rata-rata 1,9x108 cfu/ml (Lampiran 11). Sedangkan pada bulan kedua jumlah sel bakteri pada formulasi didapatkan jumlah sel sebanyak 34x108 cfu/ml (Lampiran 12). Kenaikan jumlah bakteri pada bulan kedua diduga pada bulan pertama isolat bakteri masih dalam fase lag, yang artinya bakteri masih menyesuaikan diri dengan bahan formulasi yang digunakan, sedangkan pada bulan kedua isolat bakteri berada pada fase log, yaitu fase penggandaan bakteri dengan sangat cepat, sehingga jumlah sel bakteri yang terdapat pada bulan ke dua lebih tinggi daripada bulan pertama.
Selain dapat menghambat pertumbuhan
R. solani, formula A2 dengan formulasi bentonit juga mampu memberikan pengaruh terhadap pertumbuhan tanaman padi, yaitu bobot basah dan bobot kering. Selain itu, pertumbuhan padi pada formulasi lebih tinggi dibandingkan dengan kedua kontrol, hal ini diduga karena bakteri yang digunakan dalam bentuk konsorsium memiliki berbagai kemampuan lain seperti menghasilkan aktivitas auksin sehingga mampu memacu pertumbuhan seperti bakteri P. aeruginosa
C32b, B. firmus E65, dan S. marcescens
E31(Lampiran 13). Bakteri P. aeruginosa
mampu menghasilkan IAA paling tinggi dari isolat lain yang digunakan. Spesies bakteri dari genus Bacillus dan Pseudomonas yang tergolong plant growth promoting rhizobacteria selain memacu pertumbuhan tanaman juga dapat meningkatkan ketahanan terhadap penyakit (Wahyudi et al. 2009).
Selain bakteri yang digunakan sebagai agen hayati terhadap cendawan R. solani, pada beberapa penelitian lain menggunakan cendawan endofitik untuk menekan pertumbuhan cendawan patogen R. solani. Cendawan yang digunakan antara lain
Tricoderma dengan mekanisme menghasilkan enzim-enzim yang mampu mendegradasi dinding sel cendawan R. solani
solani (Howell & Stipanovic 1995). Jika dibandingkan dengan cendawan, efektivitas penghambatan R. solani dengan menggunkan bakteri lebih efektif dari penggunaan cendawan sebagai agen hayati, diduga karena bakteri lebih cepat tumbuh dari cendawan, dan lebih efesien dalam menekan pertumbuhan cendawan R. solani
.
SIMPULAN DAN SARAN
Simpulan
Berdasarkan uji in vitro formula A2 yang mengandung isolat B. firmus E65 serta formula A8 yang mengandung konsorsium bakteri Bacillus firmus E65, Serratia marcescens E31, Pseudomonas aeruginosa
C32b, dan Bacillus cereus II.14 memiliki potensi menekan pertumbuhan R. solani. Sedangkan berdasarkan uji in vivo formula A2 dengan formulasi bentonit merupakan formulasi yang efektif dalam menghambat pertumbuhan R. solani mencapai 35,57%. dibandingkan kontrol negatif yang diinokulasikan dengan R. solani.
Saran
Perlu dilakukan penelitian lebih lanjut untuk mengkaji kembali bahan pembawa dengan penambahan bahan pengkaya untuk meningkatkan efektivitas formulasi
.
DAFTAR PUSTAKA
Ardakani SS, Heydari A, Khorasani NA, Ehteshami M. 2009. Preparation of new biofungicides using antagonistic bacteria and mineral compounds for controlling cotton seedling damping-off disease. J Plant Protect Res 49: 49-55.
Asaka O, Shoda M. 1996. Biocontrol of
Rhizoctonia solani damping-off of tomato with Bacillus subtilis RB14. Appl Environ Microbiol 62: 4081–4085.
[BPS] Badan Pusat Statistik. 2010. Produksi Padi Jagung dan Kedelai 2010. Jakarta : BPS.
[Deptan] Departemen Pertanian. 2009.
Hawar Pelepah Rhizoctonia solani kuhn.
Jakarta : Deptan.
Dewi I, Apriana A, Sisharmini A, Somantri IH. 2007. Evaluasi ketahanan tanaman padi haploid ganda calon tetua padi hibrida terhadap wereng batang coklat dan hawar daun bakteri. J Bul Agron 35: 15-21.
Gao FK, Dai CC, Liu XZ. 2010. Mechanisms of fungal endophytes in plant protection against pathogens. Afr J Microbiol Res 4: 1346-1351.
Howell CR, Stipanovic RD. 1979. Control of
Rhizoctonia solani on cotton seedlings with Pseudomonas fluorescens and with an antibiotic produced by the bacterium. J Ame Phyto Soc 69 : 480-482.
Howell CR, Stipanovic RD. 1995. Mechanisms in the biocontrol of
Rhizoctonia solani – induced cotton seedling disease by Gliocladium virens: antibiotic. J Ame Phyto Soc 85: 469-472. Kumar RS et al.. 2005. Characterization of
fungal metabolite produced by a new strain Pseudomonas aeruginosa PUPa3 that exhibits broad-spectrum antifungal activity and biofertilizing traits. J Appl Microbiol 98: 145-154.
Lee NF, Rush MC. 1983. Rice sheath blight a major rice disease. J Am Phyto Soc 67: 829-832.
Mubarik NR, Mahagiani I, Putri AA, Santoso S, Rusmana I. 2010. Chitinolytic bacteria isolated from chili rhizosphere: chitinase characterization and application as biocontrol for whitefly (Bemisia tabaci
Genn.). Am J Agric Biol Sci 5: 430-535. Muis A. 2007. Pengelolaan penyakit busuk
pelepah (Rhizoctonia solani Kuhn.) pada tanaman jagung. J Litbang Pertanian 26: 100-103.
Perveen S, Haque SE, Gaffar A. 1998. Efficacy of Pseudomonas aeruginosa and
Paecilomyces lilacinus in the control of root rot-root knot disease complex on some vegetables. Nematol Medit 26: 209-212.
Prayudi B. 2000. Toleransi padi lokal rawa pasang surut terhadap penyakit hawar pelepah daun padi (Rhizoctonia solani). J Bul Agron 28: 37-40.
Putri KE. 2010. Potensi bakteri penghambat cendawan patogen Rhizoctonia solani dan
Pyricularia grisea pada tanaman padi [skripsi]. Bogor: Insitut Pertanian Bogor. Rachman SI. 2011. Potensi Bacillus sp. galur
G3, Bacillus firmus E65, dan bakteri metanotrof sebagai penghambat pertumbuhan patogen Xanthomonas oryzae pv. oryzae dan Rhizoctonia solani
[skripsi]. Bogor: Institut Pertanian Bogor. Shaner G, Finney RE. 1997. The effect of
nitrogen fertilization on the expression of slow-mildewing resistance in knox wheat.
Suryadi Y, Triny, Kadir S, Daradjat AA. 1991. Pengendalian penyakit blast dan hawar pelepah daun padi dengan fungisida. Bul Pertan 10: 13-17.
Suryadi Y. 2009. Efektivitas Pseudomonas fluorescens terhadap penyakit layu bakteri (Ralstonia solanacearum) pada tanaman kacang tanah. J HPT Trop 9 : 174-180. Someya N, Kataoka N, Komagata T, Hirayae
K, Hibi T, Akutsu K. 2000. Biological control of cyclamen soilborne diseases by
Serratia marcescens strain B2. J Am Phyto Soc 84: 334-340.
Ting ASY, Fang MT, Tee CS. 2009. Assesment on the effect of formulative materials on the viability and efficacy of
Serratia marcescens-a biocontrol agent againts Fusarium oxysporum F. Sp.
cubense race 4. Am J Agric & Biol Sci 4: 283-288.
Utami DW, Aswidinnoor H, Moeljopawiro S, Hanarida I, Reflinur. 2006. Pewarisan ketahanan penyakit blas (Pyricularia grisea sacc.) pada persilangan padi ir64 dengan Oryza rufipogon griff. J Hayati Biosci 13: 107-112.
Lampiran 1 Komposisi media tumbuh bakteri dan cendawan
1. Nutrient Agar (NA) untuk volume 100 ml - 0,8 g nutrient broth (NB)
- 1,5 g agar - 100 ml akuades
2. Luria Broth (LB) untuk volume 100 ml - 1 g Trypton
- 1 g NaCl
- 0,5 g yeast extract
- 100 ml akuades
3. Potato Dextrose Agar (PDA) untuk volume 1 L - 300 g kentang
- 10 g Dextrose - 11 g Agar
Lampiran 2 Hasil uji kompatibilitas formula dengan R. solani
A0
A1 A2
A6
A3 A4 A5
A7
A8
A9 a
a
a
a a a
a
a a
a
b b
b b
b
b
b b
Keterangan : A0 : kontrol air A1 : B. cereus (II.14) A2 : B. firmus (E65) A3 : P. aeruginosa (C32b) A4 : S. marcescens (E31)
A5 : B. firmus (E65) + P. aeruginosa (C32b)
A6 : B. cereus (II.14) + B. firmus (E65) + P. aeruginosa (C32b) A7 : B. cereus (II.14) + P. aeruginosa (C32b) + S. marcescens
(E31)
A8 : B. cereus (II.14) + B. firmus (E65) + P. aeruginosa (C32b) + S. marcescens (E31)
A9 : kontrol kimia (Streptomisin 2%) a : R. solani
Lampiran 3 Hasil aplikasi formulasi terhadap penyakit HPD
A2 formulasi talk A2 formulasi bentonit
A2 formulasi suspensi A8 formulasi talk A8 formulasi bentonit
kontrol tanpa perlakuan
kontrol cendawan A8 formulasi suspensi
A8 formulasi minyak
Keterangan :
A2 : B. firmus (E65)
A8 : B. cereus (II.14) + B. firmus (E65) + P. aeruginosa (C32b) + S. marcescens (E31)
Kontrol cendawan : Tanaman + R. solani
Kontrol tanpa perlakuan : Tanaman tanpa perlakuan dan formulasi Tanda panah : Daerah yang diserang penyakit HPD
13
13
Lampiran 4 Hasil uji kompatibilitas formula terhadap R. solani
Formula Diameter cendawan (cm) Rata-rata Luas pertumbuhan R. solani Rata-rata Luas zona hambat R. solani Rata-rata
I II III I II III I II III
A0 9,00 9,00 9,00 9,00 63,59 63,59 63,59 63,59 0,00 0,00 0,00 0,00
A1 9,00 9,00 8,50 8,83 63,59 63,59 56,72 61,30 0,00 0,00 6,87 2,29
A2 5,00 5,50 5,25 5,25 19,63 23,75 21,64 21,67 43,96 39,84 41,95 41,92
A3 9,00 9,00 9,00 9,00 63,59 63,59 63,59 63,59 0,00 0,00 0,00 0,00
A4 9,00 9,00 9,00 9,00 63,59 63,59 63,59 63,59 0,00 0,00 0,00 0,00
S5 9,00 9,00 3,25 7,08 63,59 63,59 8,29 45,15 0,00 0,00 55,29 18,43
A6 1,00 9,00 9,00 6,33 0,79 63,59 63,59 42,65 62,80 0,00 0,00 20,93
A7 9,00 9,00 9,00 9,00 63,59 63,59 63,59 63,59 0,00 0,00 0,00 0,00
A8 1,00 1,50 1,00 1,17 0,79 1,77 0,79 1,11 62,80 61,82 62,80 62,47
A9 3,13 3,13 3,13 3,13 7,67 7,67 7,67 7,67 55,92 55,92 55,92 55,92
A0 9,00 9,00 9,00 9,00 63,59 63,59 63,59 63,59 0,00 0,00 0,00 0,00
Keterangan : angka pada kolom yang diikuti dengan huruf yang sama tidak berbeda nyata berdasarkan uji jarak berganda Duncan (DMRT) pada taraf 5%.
Lampiran 5 Hasil uji antagonis formula terhadap R. solani
Formula Luas (ulangan) (cm
2 )
Rata-rata Luas zona hambat (ulangan) (cm 2
)
Rata-rata
1 2 3 4 5 6 7 1 2 3 4 5 6 7
14
14
1 2 3
A2
Talk 3 4 3 3,33 a
Bentonit 4 4 3 3,50 a
Minyak 0 0 5 1,67 b
Suspensi 3 3 3 3,00 a
A8
Talk 3 4 4 3,50 a
Bentonit 3 3 4 3,33 a
Minyak 3 4 4 3,33 a
Suspensi 3 3 3 3,00 a
kontrol Cendawan 3 4 4 3,33 a
Tanpa perlakuan 3 4 4 3,33 a
Keterangan : angka pada kolom yang diikuti dengan huruf yang sama tidak berbeda nyata berdasarkan uji jarak berganda Duncan (DMRT) pada taraf 5%.
Lampiran 7 Panjang akar tanaman padi
Formula Formulasi Panjang akar (ulangan) (cm) Rata-rata (cm)
1 2 3
A2
Talk 19,25 32,55 21,75 24,52 a
Bentonit 23,1 24,45 23,85 23,80 a
Minyak 0 0 21,3 7,10 b
Suspensi 22,4 19 27,4 22,93 a
A8
Talk 19,95 29 31,15 26,70 a
Bentonit 20,75 17,25 29,8 22,60 a
Minyak 27,35 19,9 36 27,75 a
Suspensi 22,4 18,85 25,1 22,12 a
kontrol Cendawan 19,35 22,15 24 21,83 a
Tanpa perlakuan 29,2 21 32,65 27,62 a
15
1
5
Lampiran 8 Bobot basah dan bobot kering tanaman padi
Formula Formulasi Bobot basah tanaman padi (ulangan) (g) Rata-rata (g) Bobot kering tanaman padi (ulangan) (g) Rata-rata (g)
1 2 3 1 2 3
A2
Talk 28,65 16,52 22,88 22,68 abc 7,40 8,37 8,19 7,99 a
Bentonit 30,49 31,05 38,45 33,33 a 7,21 8,05 10,19 8,48 a
Minyak 0 0 16,34 5,45 d 0,00 0,00 3,12 1,04 d
Suspensi 14,53 26,58 36,17 25,76 abc 6,88 7,76 8,75 7,80 abc
A8
Talk 31,48 17,70 26,68 25,28 abc 7,60 8,82 6,26 7,56 abc
Bentonit 29,38 27,26 31,41 29,35 abc 6,91 6,17 7,43 6,84 bc
Minyak 11,64 23,06 22,20 18,97 c 3,71 4,36 4,20 4,09 d
Suspensi 13,61 27,55 19,22 20,13 bc 6,20 6,87 6,10 6,39 c
kontrol Cendawan 30,32 29,65 34,48 31,48 ab 7,52 8,73 8,17 8,14 ab
Tanpa perlakuan 26,22 31,36 24,35 27,31 abc 7,64 8,18 7,27 7,69 abc
Keterangan : angka pada kolom yang diikuti dengan huruf yang sama tidak berbeda nyata berdasarkan uji jarak berganda Duncan (DMRT) pada taraf 5%.
Lampiran 9 Hasil pengamatan TLR, AUDPC, dan persentase penghambatan penyakit HPD pada tanaman padi
Formulasi Perlakuan TLR 0 (%) TLR I (%) TLR II (%) TLR III (%) TLR IV (%) AUDPC Persentase penghambatan (%)
0 hs 7 hsi 14 hsi 21 hsi 28 hsi
A2
Talk 0 7,98 12,11 10,98 12,24 260,37 25,61
Bentonit 0 5,33 10,01 11,77 10,19 225,49 35,57
Minyak 0 * * * * * *
Suspensi 0 9,20 11,97 11,38 11,80 269,15 23,10
A8
Talk 0 6,35 12,09 10,35 10,60 238,63 31,82
Bentonit 0 7,88 11,87 11,71 10,63 257,43 26,45
Minyak 0 10,01 12,62 11,40 10,35 274,46 21,58
Suspensi 0 12,08 13,18 12,47 11,85 305,59 12,69
kontrol Cendawan 0 14,43 14,65 14,13 13,58 349,98 0,00
Tanpa perlakuan 0 0,00 0,00 0,00 0,00 0,00 100,00
Lampiran 10 Viabilitas isolat bakteri bulan ke-0
Isolat Jumlah sel (cfu/ml)
II.14 2,5x109
E65 2,6x109
E31 6,0x109
C32b 5,1x109
Lampiran 11 Viabilitas isolat bakteri pada formulasi bulan ke-1
Formula Formulasi Jumlah sel (cfu/ml)
A2
Talk 4,5x108
Bentonit 9,0x109
Minyak 2,0x108
Suspensi 1,5x108
A8
Talk 9,4x109
Bentonit 9,8x109
Minyak 3,2x108
Suspensi 8,6x109
Lampiran 12 Viabilitas isolat bakteri pada formulasi bulan ke-2
Formula Formulasi Jumlah sel (cfu/ml)
A2 Talk 4,4x10
9
Bentonit 2,7x109
A8 Talk 5,8x10
9
Bentonit 6,8x108
Lampiran 13 Uji IAA isolat bakteri
Ulangan Kontrol Kontrol media E65 C32b II14 E31
1 0 67,60 120,40 158,00 70,80 90,40
2 0 68,00 126,00 150,80 71,20 78,00
3 0 69,60 130,00 150,40 70,40 93,60
Penyakit Hawar Pelepah Daun Tanaman Padi. Dibimbing oleh NISA RACHMANIA MUBARIK dan YADI SURYADI.
Penyakit hawar pelepah daun (HPD) banyak ditemukan pada tanaman padi dan menurunkan hasil produksi. Penyakit HPD disebabkan oleh Rhizoctonia solani. Pengendalian penyakit HPD dapat menggunakan fungisida dan varietas resisten. Penggunaan bakteri sebagai agen pengendali yang ramah lingkungan menjadi penting dan harus dikembangkan. Penelitian ini bertujuan mengetahui efektivitas formulasi dari konsorsium bakteri sebagai pengendali penyakit HPD. Uji kompatibilitas dilakukan dengan uji antagonis menggunakan metode kultur berpasangan. Pembuatan formulasi biokontrol dengan menggunakan tiga jenis bahan pembawa yaitu talk, bentonit, dan minyak sayur. Aplikasi formulasi biokontrol dengan cara perendaman benih dengan formulasi dan penyemprotan forrmulasi secara langsung. Hasil uji kompatibilitas didapatkan dua formula terbaik yaitu A2 yang merupakan isolat bakteri Bacillus firmus E65, serta A8 merupakan konsorsium bakteri B. firmus E65, B. cereus II.14, Pseudomonas aeruginosa C32b, dan Serratia marcescens E31. Berdasarkan aplikasi formulasi terhadap penyakit HPD, formula A8 dengan bentonit merupakan formulasi yang paling efektif.
Kata kunci : padi, agen pengendali hayati, hawar pelepah daun, Rhizoctonia solani
ABSTRACT
FADHILA ACHMAD SYACHRONI. Effectiveness Formulation of Bacterial Consortia for Controlling Sheath Blight Disease on Rice Plants. Supervised by NISA RACHMANIA MUBARIK and YADI SURYADI.
Sheath blight disease caused by Rhizoctonia solani is mostly found in rice and reduce its production. Controlling this disease could be used a fungicide or resistant varieties. The use of bacteria as biocontrol agents are environmentally friendly and need to be explored. This study was aimed to determine the effectiveness of the consortium of bacteria to control sheath blight disease. The compatibility test in the antagonist test was dual culture method. Biocontrol formulation was used three carriers ie talc, bentonite, and vegetable oil. Aplication of the biocontrol formulation can done by soaking with formulation and direct spraying formulation to plant. Compatibility test results found the best formula was A2 consisted Bacillus firmus E65, and A8 formula consisted of a mixture of Bacillus firmus E65, Serratia marcescens E31, Pseudomonas aeruginosa C32b, and
Bacillus cereus II.14. Based on aplication formulation to sheath blight desease, it was found that formula A8 with bentonite is the most effective formulation.
Indonesia sebagai negara agraris, dengan mata pencaharian utama penduduk Indonesia bergerak pada sektor pertanian. Produksi padi Indonesia tahun 2010 sekitar 65,98 juta ton (BPS 2010). Permasalahan utama produksi padi Indonesia antara lain penyakit yang menyerang tanaman padi, seperti penyakit blas oleh Pyricularia grisea (Utami et al.
2006), hawar daun bakteri (HDB) oleh
Xanthomonasoryzae (Dewi et al. 2007), dan penyakit hawar pelepah daun (HPD) akibat cendawan Rhizoctonia solani (Prayudi 2000).
Hawar pelapah daun dapat menyerang tanaman padi pada tahap benih, hingga dewasa sebelum waktu panen, penyakit ini menyebabkan tanaman mudah rebah (Deptan 2009). Pengendalian penyakit HPD dapat dilakukan dengan penggunaan tanaman yang resisten dan cara pemberian fungisida (Lee & Rush 1983). Pemberian fungisida pada jangka panjang dengan dosis yang berlebihan dapat memberikan dampak yang negatif. Pengendali hayati dapat digunakan karena jauh lebih aman dari pada penggunaan bahan kimia (Ardakani et al. 2009). Selain itu, pengendali hayati juga dapat memberikan manfaat ganda memacu pertumbuhan tanaman (pupuk hayati) dan mengendalikan patogen tanaman (biopestisida) (Kumar et al.
2005).
Bakteri yang dapat digunakan sebagai agen hayati pengendali penyakit akibat R. solani yang menyerang tanaman, antara lain:
Pseudomonas aeruginosa (Perveen et al.
1998), Serratia marcescens (Someya et al.
2000), dan Bacillus spp. (Asaka & Shoda 1996). Bacillus spp. dapat digunakan sebagai agen pengendali hayati yang aman dan lebih efektif dari pada penggunaan bahan kimia. Spesies B. firmus E65, S. marcescens dan P. aeruginosa yang akan digunakan dalam penelitian ini dilaporkan Putri (2010) memiliki kemampuan menekan pertumbuhan
Rhizoctonia solani penyebab hawar pelepah (sheath blight) secara in vivo maupun in vitro. Bacillus merupakan bakteri Gram positif penghasil endospora sehingga tahan
(Mubarik et al. 2010). Sedangkan
Pseudomonas dan Serratia termasuk bakteri Gram negatif yang dapat tumbuh pada kondisi nutrisi sederhana dan mudah berkolonisasi di rhizosfer (Pseudomonas) dan filosfer (Serratia) tanaman padi. Bahan pembawa formulasi yang banyak digunakan dalam pengendali hayati antara lain bentuk padat (granul), tepung, dan suspensi (Ardakani et al. 2009).
Tujuan
Penelitian ini bertujuan mengetahui efektivitas beberapa formulasi dari konsorsium bakteri sebagai pengendali penyakit HPD pada tanaman padi.
Hipotesis yang digunakan dalam penelitian ini bahwa formulasi konsorsium bakteri sebagai pengendali penyakit hawar pelepah daun pada tanaman padi lebih efektif dari pada bukan konsorsium.
BAHAN DAN METODE
Bahan
Bakteri Bacillus firmus E65,
Pseudomonas aeruginosa C32b, Seratia marcescens E31, cendawan Rhizoctonia solani, dan bibit padi IR-64 yang digunakan pada penelitian ini berasal dari koleksi Laboratorium Konservasi Mikrobiologi BB Biogen. Selain itu juga terdapat isolat bakteri koleksi Laboratorium Mikrobiologi Departemen Biologi, FMIPA, IPB dan IPB
Culture Collection yaitu Bacillus cereus II.14 (Tabel 1).
Peremajaan Isolat Bakteri
Semua isolat bakteri diperbanyak dengan memindahkan kultur pada medium nutrient agar (NA) dan diinkubasi pada suhu ruang selama 24-48 jam. Isolat tersebut diremajakan dan diperiksa kemurniannya dengan menggunakan metode kuadran. Biakan yang telah murni ditumbuhkan pada media agar-agar miring dan disimpan dalam lemari pendingin pada suhu -20oC.
Tabel 1 Daftar isolat bakteri yang digunakan pada penelitian.
Kode isolat Spesies bakteri Asal isolat Tahun koleksi
Indonesia sebagai negara agraris, dengan mata pencaharian utama penduduk Indonesia bergerak pada sektor pertanian. Produksi padi Indonesia tahun 2010 sekitar 65,98 juta ton (BPS 2010). Permasalahan utama produksi padi Indonesia antara lain penyakit yang menyerang tanaman padi, seperti penyakit blas oleh Pyricularia grisea (Utami et al.
2006), hawar daun bakteri (HDB) oleh
Xanthomonasoryzae (Dewi et al. 2007), dan penyakit hawar pelepah daun (HPD) akibat cendawan Rhizoctonia solani (Prayudi 2000).
Hawar pelapah daun dapat menyerang tanaman padi pada tahap benih, hingga dewasa sebelum waktu panen, penyakit ini menyebabkan tanaman mudah rebah (Deptan 2009). Pengendalian penyakit HPD dapat dilakukan dengan penggunaan tanaman yang resisten dan cara pemberian fungisida (Lee & Rush 1983). Pemberian fungisida pada jangka panjang dengan dosis yang berlebihan dapat memberikan dampak yang negatif. Pengendali hayati dapat digunakan karena jauh lebih aman dari pada penggunaan bahan kimia (Ardakani et al. 2009). Selain itu, pengendali hayati juga dapat memberikan manfaat ganda memacu pertumbuhan tanaman (pupuk hayati) dan mengendalikan patogen tanaman (biopestisida) (Kumar et al.
2005).
Bakteri yang dapat digunakan sebagai agen hayati pengendali penyakit akibat R. solani yang menyerang tanaman, antara lain:
Pseudomonas aeruginosa (Perveen et al.
1998), Serratia marcescens (Someya et al.
2000), dan Bacillus spp. (Asaka & Shoda 1996). Bacillus spp. dapat digunakan sebagai agen pengendali hayati yang aman dan lebih efektif dari pada penggunaan bahan kimia. Spesies B. firmus E65, S. marcescens dan P. aeruginosa yang akan digunakan dalam penelitian ini dilaporkan Putri (2010) memiliki kemampuan menekan pertumbuhan
Rhizoctonia solani penyebab hawar pelepah (sheath blight) secara in vivo maupun in vitro. Bacillus merupakan bakteri Gram positif penghasil endospora sehingga tahan
(Mubarik et al. 2010). Sedangkan
Pseudomonas dan Serratia termasuk bakteri Gram negatif yang dapat tumbuh pada kondisi nutrisi sederhana dan mudah berkolonisasi di rhizosfer (Pseudomonas) dan filosfer (Serratia) tanaman padi. Bahan pembawa formulasi yang banyak digunakan dalam pengendali hayati antara lain bentuk padat (granul), tepung, dan suspensi (Ardakani et al. 2009).
Tujuan
Penelitian ini bertujuan mengetahui efektivitas beberapa formulasi dari konsorsium bakteri sebagai pengendali penyakit HPD pada tanaman padi.
Hipotesis yang digunakan dalam penelitian ini bahwa formulasi konsorsium bakteri sebagai pengendali penyakit hawar pelepah daun pada tanaman padi lebih efektif dari pada bukan konsorsium.
BAHAN DAN METODE
Bahan
Bakteri Bacillus firmus E65,
Pseudomonas aeruginosa C32b, Seratia marcescens E31, cendawan Rhizoctonia solani, dan bibit padi IR-64 yang digunakan pada penelitian ini berasal dari koleksi Laboratorium Konservasi Mikrobiologi BB Biogen. Selain itu juga terdapat isolat bakteri koleksi Laboratorium Mikrobiologi Departemen Biologi, FMIPA, IPB dan IPB
Culture Collection yaitu Bacillus cereus II.14 (Tabel 1).
Peremajaan Isolat Bakteri
Semua isolat bakteri diperbanyak dengan memindahkan kultur pada medium nutrient agar (NA) dan diinkubasi pada suhu ruang selama 24-48 jam. Isolat tersebut diremajakan dan diperiksa kemurniannya dengan menggunakan metode kuadran. Biakan yang telah murni ditumbuhkan pada media agar-agar miring dan disimpan dalam lemari pendingin pada suhu -20oC.
Tabel 1 Daftar isolat bakteri yang digunakan pada penelitian.
Kode isolat Spesies bakteri Asal isolat Tahun koleksi
Seluruh biakan bakteri yang telah diinkubasi selama 24 jam pada media agar-agar miring NA dilakukan pengenceran serial menggunakan garam fisologis 0,85% dan dihitung jumlahnya dengan menggunakan metode angka lempeng total (ALT).
Peremajaan Isolat Cendawan Patogen (Rhizotocnia solani)
Cendawan R. solani ditumbuhkan pada media potato dextrose agar (PDA), lalu diinkubasi selama 1 minggu pada suhu ruang (Putri 2010). Peremajaan cendawan pada media PDA dilakukan setiap satu bulan sekali.
Uji Kompatibilitas Bakteri terhadap R. solani secara in vitro
Pengujian dilakukan dengan metode kultur berpasangan yaitu dengan cara bakteri dan cendawan patogen R. solani
ditumbuhkan pada cawan Petri yang berisi media PDA. Masing-masing bakteri ditumbuhkan pada media kaldu nutrien (NB) dan diinkubasi selama 24 jam. Sebanyak 1 lup suspensi bakteri dioleskan pada cawan PDA sepanjang 3 cm. Potongan biakan murni
R. solani pada media PDA dipindahkan dengan menggunakan bor gabus, diletakkan berhadapan dengan olesan bakteri dan berjarak 3 cm dari olesan bakteri (Gambar 1). Perlakuan yang digunakan sebanyak sepuluh perlakuan dengan tiga ulangan setiap perlakuan, kontrol negatif menggunakan olesan air, dan kontrol kimia menggunakan fungisida streptomisin 2% yang dilarutkan pada media PDA (Tabel 2).
Gambar 1 Desain uji kompatibilitas formula terhadap cendawan patogen R. solani secara in vitro.
Diameter zona pertumbuhan cendawan patogen yang terbentuk diukur setelah diinkubasi selama 7 hari pada suhu ruang.
Pengukuran zona pertumbuhan cendawan dengan cara:
Zonaper tumbuhancendaw an = r 1 + r 2 2 r1 adalah jari-jari zona pertumbuhan miselia terpanjang, r2 adalah jari-jari pertumbuhan miselia terpendek (Suryadi 2009).
Luas zona hambat (ZH) dihitung dengan rumus : ZH = LC – LP, ZH adalah luas zona hambat, LC adalah luas cawan (cm2), dan LP adalah luas pertumbuhan cendawan patogen
R. solani (cm2) (Putri 2010). Dua perlakuan terbaik digunakan untuk pengujian lebih lanjut.
Tabel 2 Perlakuan formulasi isolat yang digunakan pada penelitian
Kode
perlakuan Isolat
A0 Kontrol air
A1 Bacillus cereus (II.14) A2 Bacillus firmus (E65)
A3 Pseudomonas aeruginosa
(C32b)
A4 Seratia marcescens (E31) A5 B. firmus (E65) + P. aeruginosa
(C32b)
A6 B. cereus (II.14) + B. firmus
(E65) + P. aeruginosa (C32b) A7 B. cereus (II.14) + P.
aeruginosa (C32b) + S. marcescens (E31)
A8 B. cereus (II.14) + P. aeruginosa (C32b) + S. marcescens (E31) + B. firmus
(E65)
A9 Kontrol kimia (Streptomisin 2%)
Uji Antagonis Cendawan Patogen R. solani
dengan Formula Terbaik
Perlakuan terbaik dari hasil uji kompatibilitas digunakan dalam uji antagonis cendawan R. solani. Bakteri tiap-tiap formula terbaik ditumbuhkan pada media kaldu nutrien dan diinkubasi selama satu hari, semua perlakuan dilakukan ulangan sebanyak tujuh kali ulangan. Sebanyak 1 ml suspensi biakan disentrifugasi dengan kecepatan 8944 g selama 5 menit. Sebanyak 100 µl supernatan (filtrat) bakteri dicampurkan dengan media PDA dan dituang ke cawan Petri. Cendawan R. solani diletakkan di atas media PDA yang berisi supernatan bakteri dan diinkubasi selama satu minggu, kemudian dihitung zona hambat cendawan 3cm 3cm 3cm
R. solani
dibandingkan dengan kontrol tanpa perlakuan.
Pembuatan Bahan Pembawa Agensia Biokontrol dengan Formula Terbaik
Dua formula terbaik diujikan pada berbagai bahan pembawa (Ardakani et al.
2009). Bahan pembawa yang digunakan antara lain formulasi talk (300 ml suspensi formula bakteri, 1 Kg talk, 10 g
carboxymethyl cellulose (CMC), 15 g CaCO3), formulasi bentonit (300 ml suspensi formula bakteri, 1 Kg bentonit, 10 g CMC, 15 g CaCO3), formulasi minyak (300 ml suspensi formula bakteri, 6 ml minyak sawit, 0,15 ml Triton X-100), dan formulasi suspensi (300 ml suspensi formula bakteri).
Aplikasi Formulasi Bahan Pembawa Agensia Biokontrol terhadap R. solani
secara in-vivo
Bibit padi yang digunakan ialah varietas IR-64. Bibit padi disemai dengan menggunakan tanah sawah pada bak plastik berukuran 15x30 cm2. Penyemaian dilakukan selama 18 hari. Bibit padi yang telah berumur 18 hari direndam pada 100 ml tiap-tiap formulasi selama satu malam, kemudian ditanam pada pot-pot kecil yang berisi tanah sawah sebanyak 3 Kg dan pupuk NPK (1:1:1). Setiap perlakuan dilakukan tiga kali ulangan. Aplikasi pada tanaman padi dilakukan dengan cara penyemprotan langsung. Sebanyak 100 ml tiap-tiap formulasi disemprotkan pada 6 rumpun padi pada pot-pot. Aplikasi pertama dilakukan pada umur 28 hari setelah tanam (hst) dan penyemprotan kedua dilakukan pada umur 42 hst.
Cendawan patogen R. solani ditumbuhkan pada media PDA. Kemudian potongan agar-agar ± 4 cm2 yang berisi cendawan patogen
R. solani disisipkan pada bagian pangkal padi. Inokulasi cendawan patogen R. solani
dilakukan pada umur 30 hst. Pengamatan penyakit HPD dilakukan setiap 7 hari setelah inokulasi sebanyak empat kali pengamatan dibandingkan dengan dua kontrol yang digunakan antara lain kontrol cendawan dan kontrol tanpa perlakuan. Kontrol cendawan adalah kontrol tanaman padi yang hanya disisipkan cendawan R. solani tanpa pemberian formulasi, sedangkan kontrol tanpa perlakuan adalah kontrol tanaman padi yang tidak disisipkan cendawan R. solani dan formulasi. Pengamatan intensitas penyakit HPD dengan mengukur tinggi lesio relatif (TLR) (Suryadi et al. 1991):
TLR = panjanglesio
tinggitanaman × 100% Nilai yang didapat dari perhitungan TLR kemudan dikonversi dengan perhitungan area under the disease progress curve (AUDPC). Perhitungan AUDPC bertujuan untuk mengetahui hubungan antara intensitas penyakit terhadap respon waktu (Shaner & Finney 1977):
= +
2 ( − )
n = jumlah pengamatan ti = waktu pengamatan Yi = intensitas penyakit HPD
Selain dilakukan pengamatan intensitas penyakit HPD pada tanaman padi juga dilakukan pengamatan agronomi terhadap formulasi yang diberikan pada tanaman padi yang meliputi jumlah anakan, panjang akar, bobot basah dan bobot kering. Data yang didapat dibandingkan dengan dua kontrol, antara lain kontrol cendawan dan kontrol tanpa perlakuan.
HASIL
Kompatibilitas Bakteri terhadap R. solani
secara in vitro
Uji kompatibilitas menunjukkan beberapa formula mampu menekan pertumbuhan R. solani dengan terbentuknya zona hambat. Pada perlakuan kontrol, R. solani dapat tumbuh memenuhi cawan Petri. Formula A8 menunjukkan zona hambat paling besar, yaitu 62,47 cm2 jika dibandingkan dengan kontrol streptomisin 2% dengan zona hambat 55,92 cm2(Gambar 2, Tabel 3).
(a) (b)
Gambar 2 Penghambatan pertumbuhan R. solani uji kompatibilitas oleh (a) formula A2 dan (b) formula A8 pada media potato dextrose agar
dibandingkan dengan kontrol tanpa perlakuan.
Pembuatan Bahan Pembawa Agensia Biokontrol dengan Formula Terbaik
Dua formula terbaik diujikan pada berbagai bahan pembawa (Ardakani et al.
2009). Bahan pembawa yang digunakan antara lain formulasi talk (300 ml suspensi formula bakteri, 1 Kg talk, 10 g
carboxymethyl cellulose (CMC), 15 g CaCO3), formulasi bentonit (300 ml suspensi formula bakteri, 1 Kg bentonit, 10 g CMC, 15 g CaCO3), formulasi minyak (300 ml suspensi formula bakteri, 6 ml minyak sawit, 0,15 ml Triton X-100), dan formulasi suspensi (300 ml suspensi formula bakteri).
Aplikasi Formulasi Bahan Pembawa Agensia Biokontrol terhadap R. solani
secara in-vivo
Bibit padi yang digunakan ialah varietas IR-64. Bibit padi disemai dengan menggunakan tanah sawah pada bak plastik berukuran 15x30 cm2. Penyemaian dilakukan selama 18 hari. Bibit padi yang telah berumur 18 hari direndam pada 100 ml tiap-tiap formulasi selama satu malam, kemudian ditanam pada pot-pot kecil yang berisi tanah sawah sebanyak 3 Kg dan pupuk NPK (1:1:1). Setiap perlakuan dilakukan tiga kali ulangan. Aplikasi pada tanaman padi dilakukan dengan cara penyemprotan langsung. Sebanyak 100 ml tiap-tiap formulasi disemprotkan pada 6 rumpun padi pada pot-pot. Aplikasi pertama dilakukan pada umur 28 hari setelah tanam (hst) dan penyemprotan kedua dilakukan pada umur 42 hst.
Cendawan patogen R. solani ditumbuhkan pada media PDA. Kemudian potongan agar-agar ± 4 cm2 yang berisi cendawan patogen
R. solani disisipkan pada bagian pangkal padi. Inokulasi cendawan patogen R. solani
dilakukan pada umur 30 hst. Pengamatan penyakit HPD dilakukan setiap 7 hari setelah inokulasi sebanyak empat kali pengamatan dibandingkan dengan dua kontrol yang digunakan antara lain kontrol cendawan dan kontrol tanpa perlakuan. Kontrol cendawan adalah kontrol tanaman padi yang hanya disisipkan cendawan R. solani tanpa pemberian formulasi, sedangkan kontrol tanpa perlakuan adalah kontrol tanaman padi yang tidak disisipkan cendawan R. solani dan formulasi. Pengamatan intensitas penyakit HPD dengan mengukur tinggi lesio relatif (TLR) (Suryadi et al. 1991):
TLR = panjanglesio
tinggitanaman × 100% Nilai yang didapat dari perhitungan TLR kemudan dikonversi dengan perhitungan area under the disease progress curve (AUDPC). Perhitungan AUDPC bertujuan untuk mengetahui hubungan antara intensitas penyakit terhadap respon waktu (Shaner & Finney 1977):
= +
2 ( − )
n = jumlah pengamatan ti = waktu pengamatan Yi = intensitas penyakit HPD
Selain dilakukan pengamatan intensitas penyakit HPD pada tanaman padi juga dilakukan pengamatan agronomi terhadap formulasi yang diberikan pada tanaman padi yang meliputi jumlah anakan, panjang akar, bobot basah dan bobot kering. Data yang didapat dibandingkan dengan dua kontrol, antara lain kontrol cendawan dan kontrol tanpa perlakuan.
HASIL
Kompatibilitas Bakteri terhadap R. solani
secara in vitro
Uji kompatibilitas menunjukkan beberapa formula mampu menekan pertumbuhan R. solani dengan terbentuknya zona hambat. Pada perlakuan kontrol, R. solani dapat tumbuh memenuhi cawan Petri. Formula A8 menunjukkan zona hambat paling besar, yaitu 62,47 cm2 jika dibandingkan dengan kontrol streptomisin 2% dengan zona hambat 55,92 cm2(Gambar 2, Tabel 3).
(a) (b)
Gambar 2 Penghambatan pertumbuhan R. solani uji kompatibilitas oleh (a) formula A2 dan (b) formula A8 pada media potato dextrose agar
[image:30.595.316.520.556.678.2]Luas R. solani yang tumbuh pada formula A8 tidak berbeda nyata dengan luas R. solani
yang tumbuh pada kontrol kimia streptomisin 2% (Tabel 3). Pengujian berikutnya formula A2 yang mengandung isolat tunggal B. firmus
E65 yang memiliki rata-rata luas zona hambat tertinggi setelah formula A8 digunakan sebagai pembanding.
Tabel 3 Luas pertumbuhan dan luas zona hambat R. solani hasil uji kompatibilitas isolat secara in vitro Kode formula Rata-rata luas pertumbuhan R. solani
(cm2)
Rata-rata luas zona hambat
R. solani
(cm2)
A0 63,59 a 0 a
A1 61,29 a 2,29 a
A2 21,67 bc 41,92 bc
A3 63,59 a 0 a
A4 63,59 a 0 a
A5 45,15 ab 18,43 ab A6 42,65 ab 20,93 ab
A7 63,59 a 0 a
A8 1,11 c 62,47 c
A9 7,67 c 55,92 c
Keterangan : angka pada kolom yang diikuti dengan huruf yang sama tidak berbeda nyata berdasarkan uji jarak berganda Duncan (DMRT) pada taraf 5%.
Uji Antagonis Cendawan Patogen R. solani
dengan Formula Terbaik
Uji antagonis menunjukkan formula A2 dan A8 tidak berbeda nyata dengan uji kompatibilitas. Formula A2 menunjukkan nilai rata-rata luas zona hambat R. solani
mencapai 55,73 cm2, namun R. solani
tumbuh dengan rata-rata luas pertumbuhan sebesar 7,86 cm2. Hal ini berbeda dengan
formula A8 yang menunjukkan rata-rata luas zona hambat sebesar 63,59 cm2 dan tidak ada pertumbuhan R. solani. Jika dibandingkan dengan kontrol rata-rata zona hambat sebesar 0 cm2(Gambar 3, Tabel 4).
Tabel 4 Luas pertumbuhan dan luas zona hambat R. solani pada uji antagonis R. solani dengan formula A2 dan A8
Perlakuan
Rata-rata luas pertumbuhan
R. solani (cm2)
Rata-rata luas zona hambat R.
solani (cm2)
A2 7,86 55,73
A8 0 63,59
Kontrol tanpa perlakuan
63,59 0
Aplikasi Formulasi Bahan Pembawa Agensia Biokontrol terhadap R. solani
secara in-vivo
Hasil pengamatan penyakit HPD pada tanaman padi selama empat minggu menunjukkan formula yang efektif untuk menghambat pertumbuhan penyakit HPD ialah formula A2 dengan formulasi bentonit, sedangkan formula yang kurang efektif ialah formula A8 formulasi suspensi.
(a) (b) Gambar 3 Penghambatan pertumbuhan R.
solani uji antagonis oleh (a) formula A2 dan (b) formula A8 pada media PDA.
Keterangan : TLR : tinggi lesio relatif penyakit HPD.
Gambar 4 Grafik pengamatan TLR penyakit HPD pada tanaman padi. 0 2 4 6 8 10 12 14 16 minggu ke 0 minggu ke 1 minggu ke 2 minggu ke 3 minggu ke 4 P er se n ta se T L R (%)
Tinggi Lesio Relatif (TLR)
A2 talk A2 bentonit A2 minyak A2 suspensi A8 talk A8 bentonit A8 minyak A8 suspensi
[image:3