PERANAN KADAR FERITIN DAN ASAM URAT
SERUM SEBAGAI FAKTOR PROGNOSTIK PADA
STROKE ISKEMIK AKUT
T E S I S
OLEH
FASIHAH IRFANI FITRI
NIM : 087112001
PROGRAM MAGISTER KEDOKTERAN KLINIK
SPESIALIS ILMU PENYAKIT SARAF
FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA
MEDAN
PERANAN KADAR FERITIN DAN ASAM URAT
SERUM SEBAGAI FAKTOR PROGNOSTIK PADA
STROKE ISKEMIK AKUT
T E S I S
Untuk Memperoleh Gelar Magister Kedokteran Klinis Spesialis Saraf Pada
Program Studi Magister Kedokteran Klinik Fakultas Kedokteran Universitas Sumatera Utara
Oleh
FASIHAH IRFANI FITRI
NIM : 087112001
PROGRAM MAGISTER KEDOKTERAN KLINIK– SPESIALIS ILMU PENYAKIT SARAF
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN
Judul Tesis : Peranan Kadar Feritin Dan Asam Urat Serum Sebagai Faktor Prognostik Pada Stroke Iskemik Akut
Nama Mahasiswa : FASIHAH IRFANI FITRI Nomor Induk Mahasiswa : 087112001
Program Magister : Magister Kedokteran Klinik Konsentrasi : Ilmu Penyakit Saraf
Menyetujui Komisi Pembimbing
Prof. DR. dr. Hasan Sjahrir, Sp.S (K) Ketua
Mengetahui / Mengesahkan :
Ketua Program Studi
Dr. Rusli Dhanu, Sp.S (K)
Ketua TKP PPDS I
dr. Zainuddin Amir, SpP(K)
Telah diuji pada : Senin, 7 Juni 2010
PANITIA PENGUJI TESIS
Ketua : Prof. DR. dr. Hasan Sjahrir, Sp.S (K) Anggota : 1. Prof.dr. Darulkutni Nasution,SpS(K)
2. Dr. Darlan Djali Chan,SpS 3. Dr. Yuneldi Anwar,SpS(K) 4. Dr. Rusli Dhanu,SpS(K)
5. Dr.Kiking Ritarwan,MKT,SpS 6. Dr. Aldy S Rambe,SpS
7. Dr. Puji Pinta O Sinurat,SpS 8. Dr.Khairul P Surbakti,SpS 9. Dr. Cut Aria Arina,SpS 10. Dr. Kiki M Iqbal,SpS 11. Dr. Alfansuri Kadri,SpS
12. Dr. Dina Listyaninhrum,SpS,Msi,Med 13. Dr. Aida Fithrie,SpS
PERNYATAAN
PERANAN KADAR FERITIN DAN ASAM URAT SERUM SEBAGAI FAKTOR PROGNOSTIK PADA STROKE ISKEMIK AKUT
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan disuatu perguruan tinggi, dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah dituliskan atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Medan, 7 Juni 2010
UCAPAN TERIMA KASIH
Dengan memanjatkan puji dan syukur kehadirat Allah SWT, Tuhan
Yang Maha Esa yang telah memberikan segala berkah, rahmat dan
hidayah-Nya sehingga penulis dapat menyelesaikan penulisan tesis ini.
Tesis ini dibuat untuk memenuhi persyaratan dan merupakan tugas
akhir Program Pendidikan Magister Kedokteran Klinik – Spesialis Ilmu
Penyakit Saraf di Fakultas Kedokteran Universitas Sumatera Utara/Rumah
Sakit Umum Pusat H. Adam Malik Medan.
Pada kesempatan ini perkenankanlah penulis menyatakan
penghargaan dan ucapan terima kasih yang sebesar-besarnya kepada :
1. Rektor Universitas Sumatera Utara, Dekan Fakultas Kedokteran
Universitas Sumatera Utara, dan Ketua TKP PPDS I Fakultas
Kedokteran Universitas Sumatera Utara yang telah memberikan
kepada penulis kesempatan untuk mengikuti Program Pendidikan
Magister Kedokteran Klinik Spesialis Ilmu Penyakit Saraf di Fakultas
Kedokteran Universitas Sumatera Utara.
2. Prof. DR. dr. H. Hasan Sjahrir, Sp.S (K), selaku Ketua Departemen
Neurologi Fakultas Kedokteran Universitas Sumatera Utara/RSUP
H.Adam Malik Medan, guru dan pembimbing penulis dalam
penyusunan tesis ini, yang dengan penuh kesabaran dan ketelitian
membimbing, mengoreksi, dan memberikan masukan-masukan
3. Dr. H. Rusli Dhanu, Sp.S (K), Ketua Program Studi PPDS-I Neurologi
Fakultas Kedokteran Universitas Sumatera Utara yang banyak
memberikan masukan-masukan berharga kepada penulis dalam
menyelesaikan tesis ini.
4. Dr. Puji Pinta O Sinurat dan Dr. Yuneldi Anwar,Sp.S (K), selaku
pembimbing penulis yang dengan sepenuh hati telah mendorong,
membimbing, mengoreksi dan mengarahkan penulis mulai dari
perencanaan, pembuatan dan penyelesaian tesis ini.
5. Guru-guru penulis: Prof. DR. Dr. Hasan Sjahrir,SpS(K); Prof. Dr. H.
Darulkutni Nasution, Sp.S (K); Dr. H. Hasanuddin Rambe, Sp.S (K);
Alm. Dr. Syawaluddin Nasution, Sp.S (K); Alm. Dr. Ahmad Syukri, Sp.S
(K); Dr. LBM Sitorus, Sp.S; Dr. Darlan Djali Chan, Sp.S; Dr. Aldy S
Rambe,SpS; Dr. Kiking Ritarwan, MKT, Sp.S; Dr. Irsan NHN Lubis,
Sp.S; Alm. Dr. Dadan Hamdani, Sp.S;, Sp.S; Dr. Khairul P. Surbakti,
Sp.S; Dr. Cut Aria Arina, Sp.S; Dr. S. Irwansyah, Sp.S; Dr. Kiki M.Iqbal,
Sp.S; Dr. Alfansuri Kadri, Sp.S; Dr. Dina Listyaningrum, Sp.S,
Msi,Med; Dr. Aida Fithrie, Sp.S dan guru lainnya yang tidak dapat
penulis sebutkan satu persatu, yang telah banyak memberikan
masukan selama mengikuti Program Pendidikan Magister Kedokteran
Klinik.
6. Direktur Rumah Sakit Umum Pusat H. Adam Malik Medan yang telah
sehingga penulis dapat mengikuti Program Pendidikan Magister
Kedokteran Klinik.
7. Drs. Abdul Jalil Amri Arma, M.Kes, selaku pembimbing statistik yang
telah banyak meluangkan waktu untuk membimbing dan berdiskusi
dengan penulis dalam pembuatan tesis ini.
8. Rekan-rekan sejawat peserta PPDS-I Departemen Neurologi
FK-USU/RSUP. H. Adam Malik Medan, yang banyak memberikan
masukan berharga kepada penulis melalui diskusi-diskusi kritis dalam
berbagai pertemuan formal maupun informal, serta selalu memberikan
dorongan-dorongan yang membangkitkan semangat kepada penulis
menyelesaikan Program Pendidikan Magister Kedokteran Klinik
Spesialis Ilmu Penyakit Saraf.
9. Para perawat dan pegawai di berbagai tempat dimana penulis pernah
bertugas selama menjalani Program Pendidikan Magister Kedokteran
Klinik ini, serta berbagai pihak yang tidak dapat penulis sebutkan satu
persatu, yang telah banyak membantu penulis dalam menjalani
Program Pendidikan Magister Kedokteran Klinik Spesialis Ilmu
Penyakit Saraf.
10. Semua pasien stroke iskemik yang telah bersedia berpartisipasi secara
sukarela dalam penelitian ini.
11. Kedua orang tua yang sangat penulis hormati dan sayangi Alm. Prof.
Dr. M. Dahlan Darip,SpMK dan ibunda Dra. Syahyar Hanum,DPFE
sayang, memberikan rasa aman, cinta, dukungan moril dan materi,
bimbingan dan nasehat serta doa yang tulus agar penulis tetap sabar
dan tegar dalam mengikuti pendidikan ini sampai selesai.
12. Kedua mertua saya, Prof. DR.Ir. A. Rahim Matondang,MSIE, dan Hj.
Ifin Tifah Sibarani yang banyak memberikan dorongan, semangat dan
nasehat serta doa yang tulus agar tetap sabar dan tegar dalam
mengikuti pendidikan sampai selesai
13. Abang kandung saya, dr. M. Shahreza dan kakak ipar saya Elva Citra
Sari,SE dan adik kandung saya dr. Ahmad Handayani yang banyak
memberikan semangat dan doa kepada penulis selama menjalani
Program Pendidikan Magister Kedokteran Klinik Spesialis Ilmu
Penyakit Saraf.
14. Teristimewa kepada suamiku tercinta Rahmat Hidayat Matondang,ST
atas doa dan dukungan, kesabaran dan pengertian yang mendalam,
mendampingi dengan penuh cinta dan kasih sayang dalam suka dan
duka selama penulis menjalani Program Pendidikan Magister
Kedokteran Klinik dan menyelesaikan tesis ini.
Semoga Tuhan Yang Maha Pengasih membalas semua jasa dan budi
baik mereka yang telah membantu penulis tanpa pamrih dalam
Akhirnya penulis mengharapkan semoga penelitian dan tulisan ini
dapat bermanfaat bagi kita semua.
Amin.
Penulis
DAFTAR ISI
BAB II. TINJAUAN PUSTAKA
II.1. STROKE ISKEMIK 9
II.2.2. Regulasi Absorpsi Zat Besi 18
II.2.3. Keseimbangan Zat Besi Pada Otak 18
II.2.4. Zat Besi, Radikal Bebas dan Cedera Oksidatif 19
II.2.5. Peroksidasi Lipid 23
II.3. ASAM URAT 25
II.3.1. Asam Urat Sebagai Antioksidan 26
II.3.2. Peran Asam Urat Saat Cedera Oksidatif 27
II.4. OUTCOME STROKE 30
BAB III. METODE PENELITIAN 34
III.1. TEMPAT DAN WAKTU 34
III.2. SUBJEK PENELITIAN 34
III.2.1. Populasi Sasaran 34
III.4. RANCANGAN PENELITIAN 37
III.5. PELAKSANAAN PENELITIAN 38
III.5.1. Instrumen 38
III.5.1.1. Pemeriksaan kadar ferritin serum 38 III.5.1.2. Pemeriksaan kadar asam urat serum 38
III.5.1.3. Computed Tomography Scan 38
III.5.1.4. Pengukuran Outcome 38
IV.1. HASIL PENELITIAN 41
IV.1.1. Karakteristik Subjek Penelitian 41
IV.1.2. Rerata nilai kadar asam urat dan feritin serum 43 IV.1.3. Distribusi Rerata Nilai Kadar Asam Urat
Serum Berdasarkan Variabel 43
IV.1.4. Distribusi Rerata Nilai Kadar Feritin Serum
Berdasarkan Variabel 46
IV.1.5. Distribusi Rerata Nilai NIHSS,mRS dan BI
Berdasarkan Variabel 50
IV.I.5.1. Distribusi Rerata Nilai NIHSS
Berdasarkan Variabel 50
IV.I.5.2. Distribusi Rerata Nilai mRS
Berdasarkan Variabel 52
IV.I.5.3. Distribusi Rerata Nilai BI
Berdasarkan Variabel 54
IV.1.6. Hubungan Antara Kadar Asam Urat dengan
Feritin Serum 56
IV.1.7. Peranan Kadar Asam Urat dan Feritin Serum
Terhadap Nilai NIHSS 57
IV.1.8. Peranan Kadar Asam Urat dan Feritin Serum
Terhadap Nilai mRS 60
IV.1.9. Peranan Kadar Asam Urat dan Feritin Serum
IV.2. PEMBAHASAN
IV.2.1. Karakteristik Subjek Penelitian 65
IV.2.2. Rerata Nilai Kadar Asam Urat dan
Distribusinya Berdasarkan Variabel 67 IV.2.3. Rerata Nilai Kadar Feritin Serum dan
Distribusinya Berdasarkan Variabel 68
IV.2.4. Distribusi Rerata Nilai NIHSS,mRS dan BI
Berdasarkan Variabel 69
IV.2.5 Hubungan Antara Kadar Asam Urat dengan
Feritin Serum 69
IV.2.6. Peranan Kadar Asam Urat Serum
Terhadap Outcome 70
IV.2.7. Peranan Kadar Feritin Terhadap Outcome 72
BAB V. KESIMPULAN DAN SARAN 74
V.1. KESIMPULAN 74
V.2. SARAN 75
DAFTAR PUSTAKA 76
DAFTAR SINGKATAN
ASNA : Asean Neurologic Association
BI : Barthel Index
CSF : Cerebro Spinal Fluid
DMT1 : Divalent Metal Transporter
DNA : Deoxyribonucleatid Acid
LDL : Low-Density Lipoprotein
mRS : Modified Rankin Scale
NADPH : Nicotinamide Adenin Dinucleotide Phosphate-Oxidase
NIHSS : National Institute Of Health Stroke Scale
NSE : Neuron-Specific Enolase
PJK : Penyakit Jantung Koroner
ROS : Reactive Oxygen Species
TfR : Transferrin Receptor
XDH : Xanthine Dehidrogenase
DAFTAR LAMBANG
Nilai baku normal berdasarkan nilai α (0,01) yang telah
ditentukan Æ 1,96
Nilai baku berdasarkan nilai β (0,10) yang ditentukan oleh
peneliti Æ 1,282
DAFTAR TABEL
Halaman
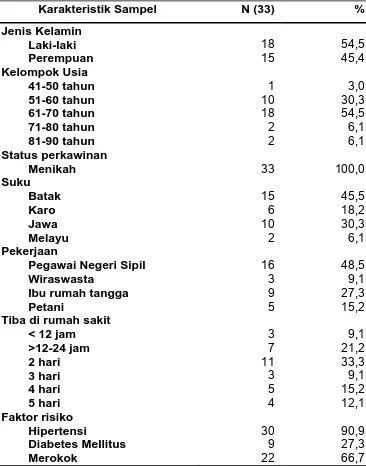
Tabel 1. Karakteristik Subjek Penelitian 42
Tabel 2. Rerata nilai kadar asam urat dan feritin serum 43
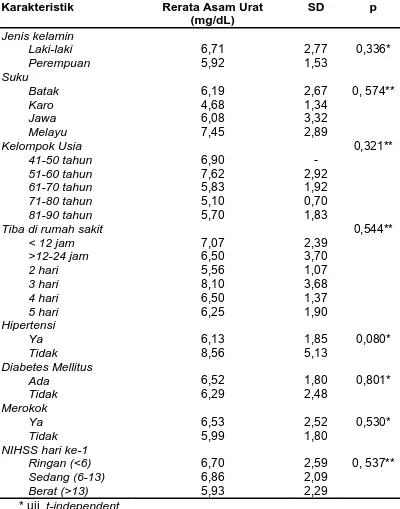
Tabel 3. Distribusi rerata nilai kadar asam urat berdasarkan variabel
45
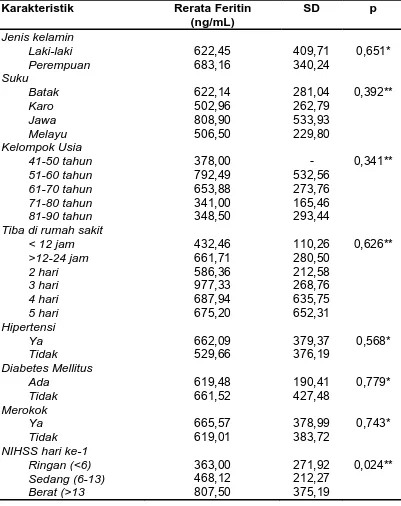
Tabel 4. Distribusi rerata nilai kadar feritin berdasarkan
variabel
48
Tabel 5. Distribusi rerata nilai NIHSS berdasarkan variabel 52
Tabel 6. Distribusi rerata nilai mRS berdasarkan variabel 54
Tabel 7. Distribusi rerata nilai BI berdasarkan variabel 56
Tabel 8. Uji regresi linear ganda untuk menentukan peranan
variabel prediktor terhadap skor NIHSS
58
Tabel 9. Uji regresi linear ganda untuk menentukan peranan
variabel prediktor terhadap skor mRS
60
Tabel 10. Uji regresi linear ganda untuk menentukan peranan
variabel prediktor terhadap skor BI
DAFTAR GAMBAR
Halaman
Gambar 1 Mekanisme seluler pada iskemik SSP akut 12
Gambar 2. Iskemik/reperfusi menyebabkan pembentukan
radikal bebas dan kerusakan jaringan
14
Gambar 3. Distribusi Zat Besi Pada Orang Dewasa 17
Gambar 4. Transpor Zat Besi Melalui Epitel Intestinal 17
Gambar 5. Keseimbangan Zat Besi Di Otak 19
Gambar 6. Produksi superoksidadan hidrogen peroksida
menyebabkan kematian sel
22
Gambar 7. Keseimbangan Asam Urat Tubuh 26
Gambar 8. Hipotesis Cedera Iskemik-Reperfusi 28
Gambar 9. Peranan Xanthine Oxidase dan Zat Besi yang
Dimobilisasi dari Feritin pada Kerusakan Jaringan pada Saat Iskemik
29
Gambar 10. Grafik Hubungan Feritin dengan NIHSS hari ke-1 49
Gambar 11. Korelasi antara asam urat dan feritin serum 57
Gambar 12 Grafik linear peran kadar asam urat terhadap skor
NIHSS
59
Gambar 13 Grafik linear peran kadar feritin terhadap skor
NIHSS
59
Gambar 14 Grafik linear peranan kadar asam urat terhadap
skor mRS
61
Gambar 15 Grafik linear peranan kadar feritin terhadap skor
mRS
62
Gambar 16 Grafik linear peranan kadar asam urat terhadap
skor BI
64
DAFTAR LAMPIRAN
HALAMAN
Lampiran 1. Lembar Penjelasan Kepada Penderita/Keluarga 83
Lampiran 2. Persetujuan Setelah Penjelasan 85
Lampiran 2. Lembar Pengumpul Data 86
Lampiran 3. National Institute of Health Stroke Scale 88
Lampiran 4. Barthel Index 90
Lampiran 5. Modified Rankin Scale 92
Lampiran 6. Surat Komite Etik Penelitian Bidang Kesehatan 93
FK-USU
Lampiran 7. Data Dasar Penelitian 94
ABSTRAK
Latar belakang dan Tujuan : Stroke iskemik masih menjadi masalah kesehatan utama dan penyebab utama mortalitas dan disabilitas. Studi eksperimental menunjukkan bukti adanya hubungan antara stroke iskemik dengan peningkatan stres oksidatif. Peningkatan zat besi, yang diukur dengan tingginya kadar feritin, telah dihubungkan dengan stres oksidatif yang lebih berat, sedangkan asam urat terbukti memiliki kapasitas antioksidan. Tujuan penelitian ini adalah untuk mengetahui peranan feritin dan asam urat sebagai factor prognostic pada stroke iskemik akut.
Metode : Studi observasional dengan rancangan potong lintang dilakukan pada penderita stroke iskemik akut di RS Adam Malik pada Agustus 2009 hingga Mei 2010. Diagnosis stroke iskemik akut ditegakkan berdasarkan
anamnesis, pemeriksaan neurologis dan CT scan kepala yang dilakukan
saat masuk. Kadar feritin dan asam urat diukur dalam 24-48 jam setelah dirawat. Outcome stroke diukur dengan menggunakan National Institute of Health Stroke Scale (NIHSS), modified Rankin Scale (mRS), Barthel Index (BI) pada hari ke-empatbelas.
Hasil : Terdapat 33 pasien dalam penelitian ini, terdiri dari 18 lelaki dan 15 perempuan. Tidak dijumpai perbedaan signifikan pada kadar feritin dan asam urat serum berdasarkan usia, jenis kelamin dan faktor risiko stroke. Terdapat korelasi positif yang signifikan antara kadar feritin dan asam urat
(r=0,345, p=0,049). Uji regresi multipel stepwise menunjukkan bahwa
kadar feritin yang lebih tinggi dan asam urat yang lebih rendah merupakan prediktor yang independen terhadap skor NIHSS dan mRS yang lebih tinggi dan skor BI yang lebih rendah,sedangkan kadar feritin yang lebih rendah dan asam urat yang tinggi merupakan prediktor yang independen terhadap skor NIHSS dan mRS yang lebih rendah dan skor BI yang lebih tinggi.
Kesimpulan : Kadar feritin dan asam urat memiliki peran sebagai faktor prognostik pada stroke iskemik akut. Kadar feritin yang tinggi dan asam
urat yang rendah merupakan faktor prognostik untuk outcome yang buruk
pada pasien stroke iskemik. Temuan ini dapat memperkuat adanya kerusakan oksidatif pada pasien stroke iskemik
ABSTRACT
Background and Purpose : Ischemic stroke remains a major healthcare problem and a leading cause of mortality and disability. Experimental studies provide evidence of an association between ischemic stroke and increased oxidative stress. Iron overload, as measured by high serum ferritin levels, has been associated with greater oxidative stress, whereas uric acid has been shown to have an antioxidant capacity. The purpose of this study was to investigate the role of serum ferritin and uric acid as prognostic factors of ischemic stroke outcome.
Methods : This was an observational cross-sectional study performed on acute ischemic stroke patients in Adam Malik General Hospital in August 2009 until May 2010. Acute ischemic stroke diagnosis was established based on history, neurological examination and cranial CT that were performed on admission. Serum ferritin and uric acid were measured within 24-48 hours from admission. Stroke outcome was` evaluated by using the National Institute of Health Stroke Scale (NIHSS), modified Rankin Scale (mRS), Barthel Index (BI) on fourteenth day.
Results : Thirty three patients, consisted of 18 men and 15 women were studied. There was no significant difference on ferritin and uric acid levels based on age, sex and stroke risk factors. There was a significant positive correlation between serum ferritin and uric acid (r=0,345,p=0,049). A stepwise multiple regression revealed that higher ferritin and lower uric acid levels independently predicted higher NIHSS and mRS scores, and lower BI score, while lower ferritin and higher uric acid levels independently predicted lower NIHSS and mRS scores and higher BI score.
Conclusions : Serum ferritin and uric acid have a role as prognostic factors for outcome in ischemic stroke patients. Higher serum ferritin and lower uric acid were prognostic factors for poor outcome in ischemic stroke patients. This finding may reinforce the relevance of oxidative damage in ischemic stroke.
ABSTRAK
Latar belakang dan Tujuan : Stroke iskemik masih menjadi masalah kesehatan utama dan penyebab utama mortalitas dan disabilitas. Studi eksperimental menunjukkan bukti adanya hubungan antara stroke iskemik dengan peningkatan stres oksidatif. Peningkatan zat besi, yang diukur dengan tingginya kadar feritin, telah dihubungkan dengan stres oksidatif yang lebih berat, sedangkan asam urat terbukti memiliki kapasitas antioksidan. Tujuan penelitian ini adalah untuk mengetahui peranan feritin dan asam urat sebagai factor prognostic pada stroke iskemik akut.
Metode : Studi observasional dengan rancangan potong lintang dilakukan pada penderita stroke iskemik akut di RS Adam Malik pada Agustus 2009 hingga Mei 2010. Diagnosis stroke iskemik akut ditegakkan berdasarkan
anamnesis, pemeriksaan neurologis dan CT scan kepala yang dilakukan
saat masuk. Kadar feritin dan asam urat diukur dalam 24-48 jam setelah dirawat. Outcome stroke diukur dengan menggunakan National Institute of Health Stroke Scale (NIHSS), modified Rankin Scale (mRS), Barthel Index (BI) pada hari ke-empatbelas.
Hasil : Terdapat 33 pasien dalam penelitian ini, terdiri dari 18 lelaki dan 15 perempuan. Tidak dijumpai perbedaan signifikan pada kadar feritin dan asam urat serum berdasarkan usia, jenis kelamin dan faktor risiko stroke. Terdapat korelasi positif yang signifikan antara kadar feritin dan asam urat
(r=0,345, p=0,049). Uji regresi multipel stepwise menunjukkan bahwa
kadar feritin yang lebih tinggi dan asam urat yang lebih rendah merupakan prediktor yang independen terhadap skor NIHSS dan mRS yang lebih tinggi dan skor BI yang lebih rendah,sedangkan kadar feritin yang lebih rendah dan asam urat yang tinggi merupakan prediktor yang independen terhadap skor NIHSS dan mRS yang lebih rendah dan skor BI yang lebih tinggi.
Kesimpulan : Kadar feritin dan asam urat memiliki peran sebagai faktor prognostik pada stroke iskemik akut. Kadar feritin yang tinggi dan asam
urat yang rendah merupakan faktor prognostik untuk outcome yang buruk
pada pasien stroke iskemik. Temuan ini dapat memperkuat adanya kerusakan oksidatif pada pasien stroke iskemik
ABSTRACT
Background and Purpose : Ischemic stroke remains a major healthcare problem and a leading cause of mortality and disability. Experimental studies provide evidence of an association between ischemic stroke and increased oxidative stress. Iron overload, as measured by high serum ferritin levels, has been associated with greater oxidative stress, whereas uric acid has been shown to have an antioxidant capacity. The purpose of this study was to investigate the role of serum ferritin and uric acid as prognostic factors of ischemic stroke outcome.
Methods : This was an observational cross-sectional study performed on acute ischemic stroke patients in Adam Malik General Hospital in August 2009 until May 2010. Acute ischemic stroke diagnosis was established based on history, neurological examination and cranial CT that were performed on admission. Serum ferritin and uric acid were measured within 24-48 hours from admission. Stroke outcome was` evaluated by using the National Institute of Health Stroke Scale (NIHSS), modified Rankin Scale (mRS), Barthel Index (BI) on fourteenth day.
Results : Thirty three patients, consisted of 18 men and 15 women were studied. There was no significant difference on ferritin and uric acid levels based on age, sex and stroke risk factors. There was a significant positive correlation between serum ferritin and uric acid (r=0,345,p=0,049). A stepwise multiple regression revealed that higher ferritin and lower uric acid levels independently predicted higher NIHSS and mRS scores, and lower BI score, while lower ferritin and higher uric acid levels independently predicted lower NIHSS and mRS scores and higher BI score.
Conclusions : Serum ferritin and uric acid have a role as prognostic factors for outcome in ischemic stroke patients. Higher serum ferritin and lower uric acid were prognostic factors for poor outcome in ischemic stroke patients. This finding may reinforce the relevance of oxidative damage in ischemic stroke.
BAB I PENDAHULUAN
I.1. Latar Belakang
Stroke masih menjadi salah satu masalah kesehatan yang utama
dan merupakan penyebab kematian yang ketiga terbanyak di
negara-negara maju, setelah penyakit kardiovaskular dan kanker. Setiap
tahunnya,lebih kurang 795.000 orang mengalami serangan stroke, baik
yang pertama, maupun serangan berulang. Diperkirakan 610.000
merupakan serangan pertama dan 185.000 adalah serangan berulang.
(Goldstein,dkk 2006; Hacke dkk,2003; Lloyd-Jones dkk,2009).
Di Indonesia penelitian berskala cukup besar dilakukan oleh survey
ASNA (Asean Neurologic Association) di 28 rumah sakit di seluruh
Indonesia. Penelitian ini dilakukan pada penderita stroke akut yang
dirawat di rumah sakit, dan dilakukan survey mengenai faktor-faktor risiko,
lama perawatan dan mortalitas serta morbiditasnya. Hasil penelitian
menunjukkan bahwa penderita laki-laki lebih banyak dari perempuan dan
profil usia di bawah 45 tahun cukup banyak yaitu 11,8%, usia 45-64 tahun
berjumlah 54,7% dan di atas usia 65 tahun 33,5%. (Misbach,2007).
Stroke juga merupakan penyebab utama gangguan fungsional,
dimana 20% penderita yang bertahan hidup masih membutuhkan
perawatan di institusi kesehatan setelah 3 bulan dan 15-30% penderitanya
kehidupan dan tidak hanya mempengaruhi penderitanya namun juga
seluruh keluarga dan pengasuh. (Goldstein dkk,2006).
Variabilitas outcome pasien stroke yang sangat besar memicu
berbagai penelitian yang berupaya mengidentifikasi faktor-faktor prediktor
outcome. Sejumlah prediktor untuk outcome fungsional yang telah diteliti
pada berbagai studi sebelumnya mencakup usia, skor NIHSS (National
Institute Of Health Stroke Scale) awal, tipe stroke, riwayat
stroke,diabetes,disabilitas sebelumnya, penyakit jantung, demensia,
status sosioekonomik, penanda keparahan stroke, demam, undernutrition,
hiperglikemia, tempat rawatan (stroke unit vs ruangan biasa), dan variabel
imejing. (Johnston dkk,2000; Appelros dkk,2003; Ng dkk, 2007; Johnston
dkk, 2002; Uchino dkk,2001; Paul dkk,2005;Greer dkk, 2008; Davis dkk,
2004; Yong dkk, 2008;Glader dkk, 2001; Rudd dkk, 2005).
Berbagai penanda biokimiawi juga telah diteliti sebagai faktor
prediktor outcome, seperti C-Reactive Protein, protein S-100B,
neuron-specific enolase (NSE), myelin basic protein, dan thrombomodulin.
(Wunderlich dkk, 1999; Napoli dkk,2001; Jauch dkk, 2006).
Beberapa penelitian terdahulu telah menunjukkan adanya
hubungan antara stroke iskemik dengan peningkatan stres oksidatif, yang
disertai dengan pembentukan radikal bebas dan menyebabkan penurunan
kadar antioksidan di otak, mencakup vitamin C, asam urat, vitamin A dan
E. Kadar antioksidan yang rendah berhubungan dengan outcome yang
lebih buruk. (Cherubini dkk, 2000). Selain kadar vitamin C dan asam urat
penanda inflamasi dan penanda stres oksidatif yang lebih tinggi.(Gariballa
dkk, 2002; Sanchez-Moreno dkk, 2004). Aktivitas antioksidan yang rendah
di plasma juga berhubungan dengan volume lesi yang lebih luas dan
gangguan neurologis pada stroke. (Leinonen dkk, 2000).
Sewaktu terjadi iskemik serebral, zat besi yang dibebaskan dari
cadangan intraseluler—seperti ferritin—mengkatalisasi reaksi yang
memproduksi radikal bebas dan berhubungan dengan outcome yang
buruk, transformasi hemoragik, dan edema otak setelah terapi trombolitik
pada pasien stroke iskemik akut. Kadar feritin yang lebih tinggi pada
baseline dijumpai pada pasien dengan outcome yang buruk setelah hari
ke-90 (median [kuartil], 165 [98,307] vs 17 [12.37] ng/mL; p<0.001) dan
pada pasien yang mengalami hematoma parenkim (p=0.006),
transformasi hemoragik simptomatik (p=0.008) dan yang mengalami
edema otak yang berat (p<0.001). (Millan dkk, 2007).
Davalos dkk (2000) melakukan penelitian terhadap 100 pasien
stroke iskemik akut dan menemukan bahwa peningkatan kadar ferritin
plasma dan CSF dalam 24 jam pertama setelah onset berhubungan
dengan perburukan neurologis. Peningkatan cadangan zat besi tubuh
menyebabkan perkembangan gejala stroke dengan mempercepat
mekanisme sitotoksik pada iskemia serebral.
Hasil yang berbeda didapatkan pada penelitian oleh Millerot dkk
(2005). Hasil penelitian menunjukkan bahwa peningkatan cadangan zat
besi tubuh tidak meningkatkan kerentanan otak terhadap iskemia, dan
Terdapat beberapa studi terdahulu mengenai serum ferritin sebagai
faktor risiko stroke iskemik, aterosklerosis dan penyakit kardiovaskular
lainnya, dengan hasil yang bervariasi. Hasil penelitian dari Van Der dkk
(2005) menunjukkan bahwa kadar serum ferritin yang lebih tinggi pada
wanita pasca menopause berhubungan dengan peningkatan risiko stroke
iskemik.
Rossi,dkk (2000) melakukan penelitian untuk menilai ketebalan
dinding intima-media karotis dan pembentukan plak fokal dengan
high-resolution B-mode ultrasound, faktor risiko konvensional, kadar serum
ferritin, dan mutasi C282Y dari gen hemokromatosis pada 1098 subjek.
Hasil penelitian menunjukkan bahwa nilai serum ferritin berhubungan
secara independen dengan plak karotis.
Wolff,dkk (2004) melakukan penelitian hubungan antara kadar
serum ferritin dengan aterosklerosis karotis pada 2443 partisipan.
Hubungan yang signifikan antara kadar serum ferritin dengan plak karotis
dijumpai pada laki-laki (OR tiap peningkatan 1-SD kadar serum ferritin,
1.33; 95% CI, 1.08 sampai 1.44) namun tidak pada wanita (OR 1.29; 95%
CI 0.98 sampai 1.75). Ditemukan interaksi antara kadar serum ferritin
dengan kolesterol LDL (Low-Density Lipoprotein) (p=0.039) pada laki-laki.
Penelitian ini menyimpulkan adanya hubungan antara kadar serum ferritin
dengan aterosklerosis yang dipotensiasi oleh kolesterol LDL.
Beberapa penelitian lainnya tidak menunjukkan adanya hubungan
antara feritin serum dengan penyakit kardiovaskular.Knuiman dkk (2003)
kejadian penyakit jantung koroner dan stroke pada tahun 1981 hingga
1998. Didapat tidak ada atau hanya sedikit bukti bahwa kadar ferritin
merupakan faktor risiko untuk penyakit kardiovaskular. Penelitian oleh
Ellervik,dkk (2005) tidak menunjukkan adanya hubungan antara
hemokromatosis herediter dengan risiko penyakit jantung iskemik. Van
Der (2006) meneliti hubungan antara non-transferrin-bound iron, kadar zat
besi serum, saturasi transferin dan feritin dengan risiko penyakit jantung
koroner (PJK) dan infark miokard. Hasilnya menunjukkan tidak ada
peningkatan risiko PJK atau infark miokard pada pasien dengan tertil
tertinggi dibandingkan dengan tertil terendah.
Pada percobaan eksperimental dijumpai peningkatan kadar asam
urat setelah stroke,yang berhubungan dengan pembentukan radikal bebas
oleh xanthine oxidase (XO) karena terjadinya iskemik lokal menyebabkan
perubahan pada metabolisme purin. (Uemura,dkk 1991). Sewaktu
iskemik serebral terjadi peningkatan kadar xanthine dan asam urat akibat
reaksi enzimatis yang membentuk asam urat (Kanemitsu dkk, 1988) dan
konversi xanthine dehydrogenase (XDH) menjadi XO. (Engerson
dkk,1987).
Namun berbagai penelitian terdahulu tentang hubungan antara
asam urat dengan stroke dan penyakit kardiovaskular lainnya memberikan
hasil yang cukup beragam dan kadang bertentangan satu sama lain.
Beberapa penelitian menunjukkan efek protektif dari asam urat, namun
Chamorro,dkk (2002) melakukan penelitian terhadap 881 pasien
stroke iskemik akut untuk mengatahui relevansi klinis dari asam urat
serum dengan outcome fungsional. Hasil penelitian menunjukkan bahwa
kadar asam urat yang tinggi berhubungan dengan outcome yang lebih
baik. Romanos,dkk (2007) melakukan studi untuk mengetahui apakah
asam urat bersifat protektif pada model iskemik tromboembolik otak pada
tikus. Hasilnya menunjukkan bahwa pemberian asam urat pada saat awal
setelah stroke tromboembolik bersifat neuroprotektif, yaitu mengurangi
volume infark, memperbaiki fungsi neurologis, melemahkan respon
inflamasi dan menambah manfaat terapi recombinant tisue-Plasminogen
Activator.
Penelitian oleh Weir,dkk (2003) menunjukkan hasil yang berbeda.
Hasil penelitian menunjukkan bahwa kadar asam urat yang lebih tinggi
memprediksi kemungkinan outcome yang lebih buruk pada stroke akut,
independen terhadap keparahan stroke dan faktor prognostik lainnya.
Asam urat juga dapat bersifat sebagai pro-oksidan, dengan
membebaskan radikal bebas sewaktu degradasinya maupun dengan
menstimulasi NADPH oxidase. (Feig dkk,2008).
Asam urat telah diteliti sebagai faktor prediktor yang kuat untuk
stroke pada pasien dengan Non-Insulin-Dependent Diabetes Mellitus.
(Lehto dkk, 1998). Hasil peneltian lainnya menunjukkan bahwa asam urat
merupakan faktor risiko untuk penyakit kardiovaskular dan stroke, juga
berhubungan dengan mortalitasnya. (Bos dkk,2006; Meisinger dkk,2008;
I.2. Perumusan Masalah
Berdasarkan latar belakang penelitian –penelitian terdahulu seperti
yang telah diuraikan di atas dirumuskanlah msalah sebagai berikut :
Bagaimanakah peranan kadar ferritin dan asam urat serum sebagai
faktor prognostik pada stroke iskemik akut ?
I.3. Tujuan Penelitian
Penelitian ini bertujuan :
I.3.1. Tujuan Umum
Untuk mengetahui peranan kadar ferritin dan asam urat serum
sebagai faktor prognostik pada stroke iskemik akut.
I.3.2. Tujuan Khusus
1. Untuk mengetahui peranan kadar ferritin dan asam urat serum
sebagai faktor prognostik pada pasien stroke iskemik akut di
RSUP H.Adam Malik Medan.
2. Untuk mengetahui hubungan antara kadar ferritin dan kadar asam
urat serum pada pasien stroke iskemik akut di RSUP H.Adam
Malik Medan.
3. Untuk mengetahui gambaran karakteristik demografik, kadar feritin
serum dan kadar asam urat serum pada penderita stroke iskemik
akut di RSUP H. Adam Malik Medan.
4. Untuk mengetahui perbedaan distribusi kadar asam urat serum
berdasarkan karakteristik demografi pada pasien stroke iskemik
5. Untuk mengetahui perbedaan distribusi kadar feritin serum
berdasarkan karakteristik demografi pada pasien stroke iskemik
akut di RSUP H.Adam Malik Medan.
6. Untuk mengetahui perbedaan distribusi nilai NIHSS, mRS, BI
berdasarkan karakteristik demografi pada pasien stroke iskemik
akut di RSUP H.Adam Malik Medan.
I.4. Hipotesis
Kadar serum ferritin dan asam urat memliki peran sebagai faktor
prognostik pada pasien stroke iskemik akut.
I.5. Manfaat Penelitian
Dengan mengetahui adanya peranan kadar serum ferritin dan
asam urat sebagai faktor prognostik pasien stroke iskemik, maka dapat
diprediksi outcome pasien yang dirawat di bangsal Neurologi RSUP. H.
BAB II
TINJAUAN PUSTAKA
II.1. STROKE ISKEMIK II.1.1. Definisi
Stroke adalah tanda-tanda klinis yang berkembang cepat akibat
gangguan fungsi otak fokal atau global, dengan gejala-gejala yang
berlangsung selama 24 jam atau lebih atau menyebabkan kematian,
tanpa adanya penyebab lain yang jelas selain vaskuler (WHO,2005).
Stroke iskemik adalah tanda klinis disfungsi atau kerusakan
jaringan otak yang disebabkan kurangnya aliran darah ke otak sehingga
mengganggu kebutuhan darah dan oksigen di jaringan otak (Sjahrir,2003).
II.1.2. Epidemiologi
Insiden stroke bervariasi di berbagai negara di Eropa, diperkirakan
terdapat 100-200 kasus stroke baru per 10.000 penduduk per tahun
(Hacke dkk,2003). Di Amerika diperkirakan terdapat lebih dari 700.000
insiden stroke per tahun, yang menyebabkan lebih dari 160.000 kematian
per tahun, dengan 4.8 juta penderita stroke yang bertahan hidup.
(Goldstein dkk, 2006). Insiden stroke pada pria lebih tinggi daripada
wanita, pada usia muda, namun tidak pada usia tua. Rasio insiden pria
dan wanita adalah 1.25 pada kelompok usia 55-64 tahun, 1.50 pada
kelompok usia 65-74 tahun, 1.07 pada kelompok usia 75-84 tahun dan
II.1.3. Faktor Risiko
Faktor risiko untuk terjadinya stroke dapat diklasifikasikan
berdasarkan kemungkinannya untuk dimodifikasi atau tidak
(nonmodifiable, modifiable, atau potentially modifiable) dan bukti yang
kuat (well documented atau less well documented) (Goldstein,2006).
1. Non modifiable risk factors :
a. Usia
b. Jenis kelamin
c. Berat badan lahir rendah
d. Ras/etnis
e. Genetik
2. Modifiable risk factors
a. Well-documented and modifiable risk factors
1. Hipertensi
2. Paparan asap rokok
3. Diabetes
4. Atrial fibrilasi dan beberapa kondisi jantung tertentu
5. Dislipidemia
6. Stenosis arteri karotis
7. Sickle cell disease
8. Terapi hormonal pasca menopause
9. Diet yang buruk
10. Inaktivitas fisik
b. Less well-documented and modifiable risk factors
1. Sindroma metabolik
2. Penyalahgunaan alkohol
3. Penggunaan kontrasepsi oral
4. Sleep-disordered breathing
5. Nyeri kepala migren
6. Hiperhomosisteinemia
7. Peningkatan lipoprotein (a)
8. Peningkatan lipoprotein-associated phospholipase
9. Hypercoagulability
10. Inflamasi
11. Infeksi
II.1.4. Patofisiologi
Iskemik otak mengakibatkan perubahan dari sel neuron otak secara
bertahap (Sjahrir,2003)
Tahap 1 : a. Penurunan aliran darah
b. Pengurangan O2
c. Kegagalan energi
d. Terminal depolarisasi dan kegagalan homeostasis ion
Tahap 2 : a. Eksitoksisitas dan kegagalan homeostasis ion
b. Spreading depression
Tahap 3 : Inflamasi
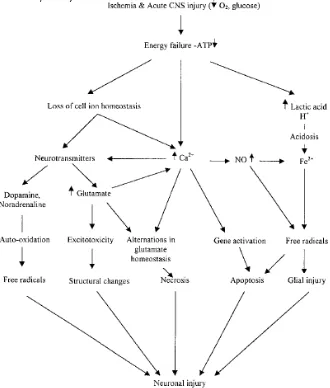
Proses patofisiologi pada cedera SSP akut sangat kompleks dan
melibatkan permeabilitas patologis dari sawar darah otak, kegagalan
energi, hilangnya homeostasis ion sel, asidosis, peningkatan kalsium
ekstraseluler, eksitotoksisitas dan toksisitas yang diperantarai oleh radikal
bebas. (Sherki dkk,2002)
Gambar 1. Mekanisme seluler pada iskemik SSP akut.
II.1.5. Stres Oksidatif pada Stroke Iskemik
Stres oksidatif didefinisikan sebagai suatu gangguan pada
keseimbangan pro-oksidan dan anti-oksidan, yang dapat menimbulkan
kerusakan pada keadaan pro-oksidan yang lebih banyak. Otak
menggunakan jumlah oksigen yang relatif banyak, sehingga rentan
terhadap stres oksidatif. Pembentukan oksidan secara alami sewaktu
transpor elektron mitokondrial, auto-oksidasi beberapa neurotransmitter
dan kejadian sewaktu hipoksia atau iskemia dapat menyebabkan
pembentukan oksidan dan menimbulkan kerusakan jaringan. (Warner
dkk,2004).
Berbagai bukti menunjukkan adanya keterlibatan radikal oksigen
dalam patogenesis lesi iskemik. Reoksigenasi pada saat reperfusi
menyediakan substrat bagi sejumlah reaksi oksidasi enzimatik.
Mitokondria memproduksi radikal anion superoksida dan hidrogen
peroksida (H2O2) dalam keadaan normal. Repefusi setelah iskemik
menyebabkan produksi reactive oxygen species (ROS) yang berlebih
pada mitokondria. ROS dapat secara langsung terlibat dengan
makromolekul seluler seperti lipid, protein dan asam nukelat pada jaringan
iskemik, yang akhirnya dapat menyebabkan kematian sel. (Sugawara
Proses reduksi oksigen menghasilkan superoksida, hidrogen
peroksida, radikal hidroksil dan air. Superoksida merupakan radikal
utama. Ia membentuk hidrogen peroksida dengan dismutasi. Radikal
hidroksil terbentuk dari hidrogen peroksida dengan adanya zat besi
ferrous atau logam transisi lainnya melalui reaksi Haber-Weiss.
Superoksida diproduksi dalam jaringan melalui sejumlah reaksi enzimatis
atau auto-oksidasi, mencakup autooksidasi molekul-molekul kecil,
hemoglobin,mioglobin, komponen mitokondria, melalui enzim oksidatif
seperti xanthine oxidase, NADH oxidase, cyclooxygenase, NADPH
oxidase, dan proses oksidasi asam lemak tidak jenuh. (Kontos,2001).
Tingkat produksi superoksida oleh autooksidasi dipengaruhi oleh
Gambar 2. Iskemik/reperfusi menyebabkan pembentukan radikal bebas dan kerusakan jaringan.
konsentrasi dari substrat yang teroksidasi dan ketersediaan oksigen.
(Kontos, 2001).
Radikal oksigen memiliki efek selular yang sangat luas. Kerjanya
yang relevan terhadap iskemik serebral mencakup peroksidasi lipid,
denaturasi protein, inaktivasi enzim, kerusakan asam nukleat dan DNA,
pelepasan ion kalsium dari cadangan intrasel,kerusakan sitoskeleton,
kemotaksis. Efek terhadap vaskular serebral adalah vasodilatasi,
perubahan reaktivitas terhadap CO2 dan vasodilator yang bergantung
endotel, peningkatan agregasi platelet, peningkatan permeabilitas endotel,
lesi destruktif fokal dari membran sel endotel. (Kontos,2001).
Iskemik serebral komplit yang diikuti reperfusi menyebabkan
terbentuknya superoksida. Konsentrasinya mencapai puncak pada fase
awal reperfusi dan menurun selama 2 jam setelahnya. Produksi
superoksida tidak terdeteksi sewaktu iskemik komplit karena tidak ada
oksigen. Produksi radikal oksigen sewaktu reperfusi setelah iskemia
disertai dengan vasodilatasi dan menghilangnya respon yang bergantung
endotel. Permeabilitas sawar darah otak menjadi meningkat dan
memungkinkan terjadinya ekstravasasi albumin dan komponen lainnya. Ini
menyebabkan edema dan peningkatan tekanan intra kranial.
(Kontos,2001).
II.2. FERRITIN
Ferritin merupakan protein yang penting dalam metabolisme zat
dipergunakan jika diperlukan sewaktu-waktu. Ferritin tersusun oleh 24
subunit yang terdiri dari 18.5 kDa, yang mengelilingi 3000-4500 atom
ferric. Normalnya, hanya sedikit ferritin yang terdapat di plasma. Jumlah
ferritin di plasma dapat diukur dan merupakan indeks cadangan zat besi
dalam tubuh. Sintesis reseptor transferin (TfR) dan feritin secara
resiprokal berkaitan dengan kandungan zat besi selular. Ketika kadar zat
besi tinggi, sel menggunakan mRNA ferritin untuk mensintesis ferritin, dan
mRNA TfR dihancurkan. Sebaliknya, jika kadar zat besi rendah, mRNA
TfR menjadi stabil dan terjadi peningkatan sintesis reseptor, dan mRNA
tampaknya disimpan dalam bentuk inaktif. (Murray,2003).
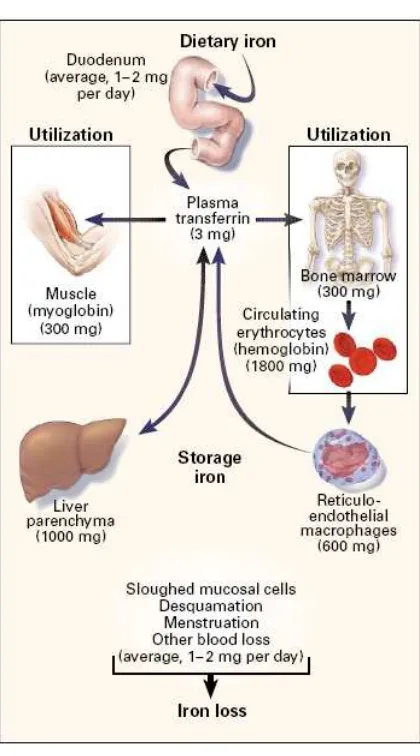
II.2.1. Distribusi Zat Besi
Distribusi zat besi di jaringan ditunjukkan pada gambar 3. Lelaki
dewasa normalnya memiliki 35 sampai 45 mg zat besi per kilogram berat
badan. Wanita premenopause memiliki cadangan zat besi yang lebih
rendah sebagai akibat kehilangan darah yang berulang pada saat
menstruasi. Lebih dari dua pertiga dari kandungan zat besi tubuh
digabung menjadi hemoglobin pada prekursor eritroid yang sedang
berkembang dan pada sel darah merah yang matang. Tiap eritrosit
mengandung jutaan atom besi; pada tingkat turnover yang normal,
konsentrasi ini menggambarkan inkorporasi 2X 1020 atom besi per hari.
Sebagian besar dari zat besi tubuh lainnya terdapat di hepatosit dan
Hepar memiliki kemampuan untuk mengambil zat besi yang bersirkulasi
yang melebihi kemampuan pengikatan transferin plasma. (Andrews,1999)
Gambar 3. Distribusi Zat Besi Pada Orang Dewasa
Gambar 4. Transpor Zat Besi Melalui
Epitel Intestinal
Dikutip dari: Andrews,N.C. 1999. Disorders of Iron Metabolism. New England Journal of Metabolism. 341;26: 1986-1994.
II.2.2. Regulasi Absorpsi Zat Besi
Walaupun jumlah zat besi yang diekstraksi dari makanan relatif
kecil, namun regulasi absorpsi zat besi sangat penting karena manusia
tidak memiliki jalur fisiologis untuk eksresi. Sel enterosit yang melapisi vili
absorptif yang dekat dengan gastroduodenal junction, bertanggungjawab
untuk seluruh absorpsi zat besi. Zat besi harus melewati dari lumen usus
melalui membran apikal dan basolateral untuk mencapai plasma. Divalent
metal transporter 1 (DMT1) merupakan protein yang mentransfer zat besi
sepanjang membran apikal ke dalam sel. Di dalam enterosit, zat besi
memiliki 2 kemungkinan : dapat disimpan sebagai ferritin atau dapat
ditransfer melalui membran basolateral untuk mencapai plasma. Zat besi
yang berada dalam bentuk ferritin, seiring dengan enterosit menjalani
siklusnya, akan dihancurkan dengan senescent sel dan meninggalkan
tubuh ,melalui traktus gastrointestinal. Proses ini mewakili mekanisme
kehilangan zat besi yang penting. (Andrews, 1999)
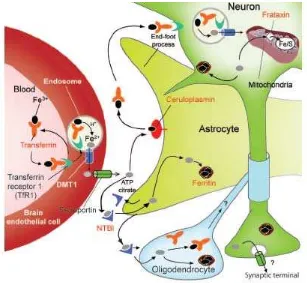
II.2.3. Keseimbangan Zat Besi Pada Otak
Transportasi zat besi pada otak bergantung pada interaksi antara
sel endotel dengan astrosit. (Gambar 5). Sel endotel otak
mengekspresikan reseptor transferin 1 (TfR1) pada membran luminalnya;
reseptor ini mengikat transferin dan menginternalisasikan kompleks ini ke
dalam endosom. Di dalam endosom, lingkungan asam memfasilitasi
pelepasan zat besi ferri dari transferin dan diikuti dengan reduksi ion ferri
dipindahkan dari endosom ke sitosol oleh divalent metal transporter-1
(DMT-1) dan kemudian dibawa keluar oleh kerja dari ferroportin. Prosesus
astrosit mengekspresikan ceruloplasmin, yang bekerja sebagai
ferroxidase yang mengoksidasi ion ferro menjadi ferri, yang kemudian
terikat ke transferin pada cairan interstisial otak. (Benarroch, 2009).
Gambar 5. Keseimbangan Zat Besi Di Otak
Dikutip dari : Benarroch E. Brain Iron Homeostasis and Neurodegenerative Disease. Neurology. 2009;72; 1436-1440.
II.2.4. Zat Besi, Radikal Bebas dan Cedera Oksidatif
Kerusakan reperfusi, yang disebabkan oleh restorasi metabolisme
aerob setelah periode iskemia, bergantung pada adanya radikal bebas.
merusak sel dengan mengoksidasi berbagai komponen selular. Bukti
menunjukkan bahwa zat besi mempercepat kerusakan yang terjadi
sewaktu iskemik dan reperfusi. Zat besi dimobilisasi sewaktu iskemik
organ, sehingga tersedia untuk pembentukan radikal bebas. (Valk
dkk,1999).
Superoksida adalah suatu radikal bebas—suatu senyawa dengan
jumlah elektron yang ganjil, berasal dari okigen molekular dengan
penambahan suatu elektron tunggal. Reaksi yang menghasilkan
superoksida secara biologis berlangsung pada berbagai keadaan,
mencakup penyakit infeksi, inflamasi dan berbagai penyakit yang
melibatkan iskemia dan reperfusi. Mitokondria yang mengalami cedera
iskemik menjadi sumber utama radikal superoksida saat terjadi
reoksigenasi pasca-iskemik. Radikal superoksida dapat berfungsi sebagai
oksidan ringan, reduktan yang kuat, atau sebagai inisiator dari reaksi
radikal bebas berantai. Banyak enzim penting yang dapat diinaktivasi
secara langsung oleh superoksida, seperti catalase, creatine
phosphokinase, glyceraldehyde-3-phosphate dehidrogenase, gluthathione
peroxidase, myofibrillar ATPase, adenylate cyclase, dan Ca2+-Mg2+
-ATPase. Walaupun begitu, kerja yang paling destruktif dari radikal
superoksida tampaknya adalah pelepasan zat besi dari ferritin. Telah
dianggap bahwa O2.- memasuki inti-ferritin melalui saluran hidrofilik, diikuti
dengan reduksi Fe3+ menjadi Fe2+. Ini menyebabkan pelepasan zat besi
Zat besi adalah logam transisi redoks-aktif, yang artinya dapat
dengan mudah berpindah antara ferrous atau (Fe2+) dan ferric (Fe3+),
menerima atau memberikan suatu elektron ke berbagai substansi biologis,
dengan demikian mengkatalisasi berbagai reaksi yang merusak dalam sel.
Pada keadaan normal, tidak pernah ada kadar zat besi ‘bebas’ (atau zat
besi yang mengalami chelation oleh senyawa dengan berat molekul
rendah). Setiap pelepasan Fe2+ dengan segera mengalami chelation oleh
senyawa seperti sitrat atau ADP, namun kompleks ini dengan mudah
berpartisipasi dalam reaksi redoks, mengkatalisasi pembentukan HO. atau
memulai peroksidasi lipid. (McCord,1998)
Makromolekul chelator zat besi seperti transferin dan feritin,
menyediakan tempat pengikatan dengan spesifisitas yang demikian rigid
sehingga Fe3+ terikat sangat kuat, namun Fe2+ tidak terikat sama sekali.
Selama perpindahan dari satu jaringan ke jaringan lain, zat besi dibawa
oleh transferrin. Ketika kompleks besi ini memasuki suatu sel melalui
reseptor transferrin, zat besi ditranspor atau disimpan dalam protein
ferritin. Suatu karakteristik penting dari kedua protein ini adalah bahwa
keduanya mengikat zat besi dalam bentuk Fe3+. Akibat keterbatasan
kinetik dan termodinamik dari ikatan ini, zat besi sangat sulit untuk
dilepaskan dari transferin dan feritin sehingga mencegah partisipasinya
yang tidak diinginkan dalam reaksi redoks. Dalam keadaan normal,
cadangan zat besi dalam tubuh tampaknya tidak menimbulkan masalah.
signifikan sebagai akibat dari berbagai kemungkinan untuk produksi
superoksida. (MCord,1998)
Seperti yang ditunjukkan pada gambar 6, bahwa bentuk
penyimpanan zat besi—ferritin—yang rentan terhadap serangan oleh
radikal superoksida (O2.- ) menyebabkan pelepasan simpanan logamnya.
Begitu zat besi dibebaskan akibat adanya superoksida dan produk Gambar 6. Produksi superoksida dan hidrogen peroksida
menyebabkan cedera dan kematian sel.
dismutasinya, hidrogen peroksida, radikal hidroksil (HO.) dapat terbentuk
oleh reaksi Haber-Weiss. (McCord,1998)
Fe2+ + H2O2 Æ Fe3+ + OH⎯ + HO˙
O2˙⎯+ Fe3+ Æ O2 + Fe2+________
O2˙⎯+ H2O2 Æ O2 + OH⎯ + HO˙
Radikal hidroksil merupakan spesies pengoksidasi yang sangat
kuat. Kemampuan potensial oksidasinya kedua setelah atom oksigen.
Radikal hidroksil dapat diproduksi oleh sistem biologis sendiri, oleh
pembentukan sederhana superoksida pada keadaan adanya zat besi
yang redoks-aktif dan hidrogen peroksida. Radikal hidroksil ini dapat
menyerang semua kelas makromolekul biologis. Ia dapat
mendepolimerase polisakarida, menyebabkan putusnya rantai DNA,
menginaktivasi enzim dan mengawali peroksidasi lipid. Karena lipid
peroksidasi adalah reaksi berantai yang diamplifikasi oleh zat besi yang
redoks aktif, kerja radikal hidroksil yang inilah yang tampaknya memiliki
konsekuensi patofisologis yang paling berat pada penyakit seperti
penyakit jantung iskemik dan stroke. (Mc Cord,1998)
II.2.5. Peroksidasi Lipid
Radikal hidroksil memiliki kemampuan untuk mengambil suatu atom
hidrogen allylic (H˙) dari suatu rantai asam lemak polyunsaturated pada
Radikal lemak yang carbon-centered yang dihasilkan (L˙) dengan
segera bereaksi dengan oksigen molekuler untuk menghasilkan suatu
radikal lipid dioxyl (LOO˙) : L˙ + O2Æ LOO˙
Radikal lipid dioxyl ini mampu untuk mengambil suatu atom hidrogen dari
rantai asam lemak polyunsaturated lainnya, membentuk radikal L˙ lainnya
yang meneruskan rantai reaksi lainnya : LOO˙ + LH Æ LOOH + L˙
Secara in vivo, diperkirakan bahwa kejadian awal (seperti
pembentukan radikal HO˙ tunggal) menimbulkan rantai sepanjang 10-15
siklus sebelum rantai ini berakhir, biasanya dengan reaksi oleh molekul
vitamin E. Efek dari reaksi berantai seperti ini adalah akumulasi dari 10
sampai 15 molekul lipid hidroperoksida (LOOH). Area lokal pada membran
sel ini sekarang dipenuhi dengan pembuatan 10 sampai 15 reaksi rantai
baru akibat zat besi yang redoks-aktif, tereduksi menjadi ferrous oleh
reaksi dengan superoksida, yang mampu mereduksi hidroksi peroksida
untuk membentuk radikal baru, radikal alkoxy (LO˙), yang dapat memulai
reaksi berantai baru :
Fe2+ + LOOHÆ Fe3+ + LO˙ + OH⎯
LO˙ + LH Æ LOH + L˙
Oleh sebab itu, adanya radikal superoksida dan zat besi redoks-aktif
secara bersamaan dapat sangat membahayakan sel dalam hal menjaga
struktur dan fungsi membran. (McCord 1998). Lipid peroksidasi dapat
permeabilitas, menghambat proses metabolik dan perubahan transpor ion.
(Adibhatla dkk, 2006)
Gambar 6 juga menunjukkan mekanisme pertahanan seluler yang
bekerja untuk mencegah urutan kejadian ini. Enzim antioksidan seperti
superoxide dismutase, catalase, dan gluthathione peroxidase bekerja
sebagai lini pertama pertahanan. Jika mekanisme pertahanan ini habis
dan kejadian ini berlanjut menjadi peroksidasi lipid, maka lini kedua
bekerja. Enzim antioksidan phospholipid hydroperoxide, gluthathione
peroxidase bekerja untuk mengeliminasi komponen membran yang
mengalami peroksidase dengan mengubah peroksida menjadi alkohol.
Aksi ini mencegah mulainya rantai reaksi baru oleh zat besi ferrous seperti
yang tadi dijelaskan. Antioksidan vitamin E dan C juga berkolaborasi untuk
mengakhiri reaksi berantai ini, menghentikan akumulasi peroksida lebih
lanjut. Jika semua mekanisme pertahanan ini terpakai atau habis,
membran sel menjadi rusak sehingga sel mati. (McCord,1998; Thomas,
1985).
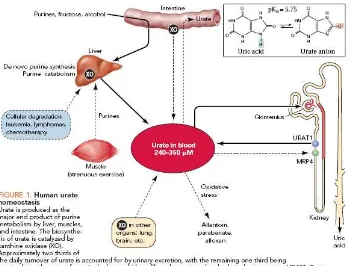
II.3. ASAM URAT
Asam urat adalah hasil akhir pemecahan nukleotida purin karena
manusia tidak memliki enzim urikase yang mengubah urat menjadi
alantoin seperti pada spesies lain. Biosintesis asam urat dikatalisasi oleh
enzim xanthin oxidase (XO) dan/atau bentuk isoformnya, xanthine
dapat dioksidasi menjadi alantoin atau produk lain, seperti parabanate dan
allloxan.
II.3.1. Asam Urat Sebagai Antioksidan
Akumulasi asam urat pada manusia dianggap memiliki manfaat.
serupa dengan vitamin C, asam urat merupakan antioksidan yang poten.
(Hediger dkk,2004). Asam urat berkontribusi sampai dengan 60% dari
aktivitas total antioksidan plasma pada orang sehat. Asam urat bekerja
sebagai antioksidan dengan berinteraksi dengan 10 sampai 15% radikal
hidroksil yang diproduksi tiap hari dan dengan memusnahkan radikal Gambar 7. Keseimbangan Asam Urat Tubuh
peroksil dan oksigen tunggal dengan efisien. Asam urat juga mampu
berikatan dengan zat besi dan bekerja secara tidak langsung dengan
menstabilkan askorbat plasma. (Sherki dkk,2002).
Asam urat menghambat oksidasi askorbat yang bergantung Fe3+
dengen membentuk ikatan yang stabil dengan Fe2+ dan Fe3+. Asam urat
juga merupakan scavenger yang sangat efektif pada lipid peroksidasi dan
bersifat protektif terhadap hemolisis oksidatif dari membran eritrosit oleh
lipid hidroksiperoksida. Dalam seluruh prosesnya sebagai antioksidan,
asam urat dioksidasi menjadi allantoin dan produk lainnya. (Daves
dkk,1986)
Kadar asam urat pada awal proses aterosklerosis berfungsi sebagai
antioksidan dan tampaknya merupakan penentu kapasitas antioksidan
plasma yang paling kuat. Namun pada proses selanjutnya, ketika kadar
asam urat serum meningkat (> 6mg/dl pada wanita dan >6.5-7 mg/dl pada
pria), asam urat menjadi bersifat pro-oksidan. (Hayden,2004)
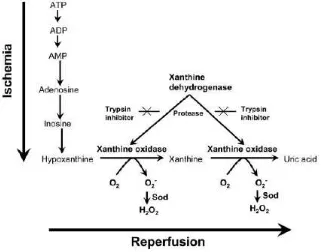
II.3.2. Peran Asam Urat Saat Cedera Oksidatif
Sewaktu terjadi iskemik,terdapar perubahan pada ion transmembran,
yang memungkinkan kadar kalsium sitosol meningkat, yang kemudian
mengaktivasi protease yang secara irreversible mengkatalisasi perubahan
XDH menjadi XO. Sewaktu reperfusi, terbentuklah superoksida dan
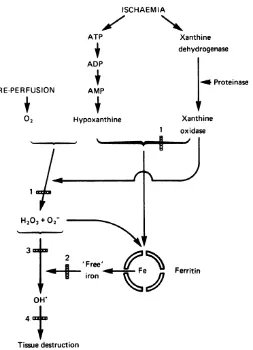
Akibat dari mobilisasi zat besi dari feritin oleh enzim XO
diperlihatkan pada gambar 9. Saat iskemik, XO akan melepaskan zat besi
dari feritin. Zat besi yang tidak terikat ini akan berakumulasi dan mampu
mengkatalisasi pembentukan radikal bebas radikal hidroksil oleh XO.
(Biemond dkk, 1986).
Gambar 8. Hipotesis Cedera Iskemik-Reperfusi
Gambar 9. Peranan Xanthine Oxidase dan Zat Besi yang Dimobilisasi dari
Feritin pada Kerusakan Jaringan pada Saat Iskemik
II.4. OUTCOME STROKE
Kehilangan fungsi yang terjadi setelah stroke sering digambarkan
sebagai impairment, disabilitas dan handicaps. World Health Organization
(WHO) membuat batasan sebagai berikut (Caplan,2000) :
1. Impairment adalah suatu kehilangan atau abnormalitas psikologis,
fisiologis atau fungsi atau struktur anatomis.
2. Disabilitas adalah setiap keterbatasan atau ketidakmampuan untuk
melakukan suatu aktivitas dengan cara atau dalam rentang yang
dianggap normal untuk orang sehat.
3. Handicap adalah gangguan yang dialami oleh individu akibat
impairment atau disabilitas tersebut, yang membatasi perannya
sebagai manusia normal.
Penelitian klinis tentang stroke secara rutin menggunakan
mortalitas sebagai outcome, namun terdapat outcome lainnya yang
penting untuk investigasi klinis dan relevan dengan pasien, mencakup
perubahan fungsi tubuh dan disabilitas. Sejumlah instrumen untuk menilai
fungsi dan disabilitas telah dikembangkan. Pada berbagai penelitian klinis,
skala Barthel Index dan Modified Rankin Scale umumnya digunakan untuk
menilai outcome karena mudah digunakan dan merupakan pengukuran
yang sensitif terhadap derajat keparahan stroke.(Weimar dkk, 2002).
Modified Rankin Scale mengukur tingkat ketergantungan, baik
mental maupun adaptasi fisik yang digabungkan dengan defisit
tidak ada gejala dan 5 berarti cacat/ketidakmampuan yang berat. (Weimar
dkk,2002).
National Institute of Health Stroke Scale (NIHSS) digunakan untuk
menilai impairment, yang terdiri dari 12 pertanyaan—tingkat kesadaran,
respon terhadap pertanyaan, respon terhadap perintah, gaze palsy,
pemeriksaan lapangan pandang, facial palsy, motorik, ataksia, sensori,
bahasa, disartria dan inatensi. Skala ini telah banyak digunakan pada
berbagai penelitian tentang terapi stroke akut dan merupakan
pemeriksaan standar dalam penelitian klinis. (Meyer dkk,2002; Schlegel
dkk,2003).
Skor ini tidak hanya membantu untuk mengukur derajat defisit
neurologis,namun juga untuk memfasilitasi komunikasi antara penyedia
layanan kesehatan, mengidentifikasi kemungkinan lokasi oklusi pembuluh
darah, menyediakan prognosis awal, dan membantu mengidentifikasi
eligibilitas pasien untuk berbagai intervensi dan potensial komplikasi.
(Adams dkk, 2007). Penilaian retrospektif untuk menilai keparahan stroke
dengan NIHSS menunjukkan bahwa skor ini reliable dan tidak bias
bahkan jika elemen pemeriksaan fisik ada yang hilang dari rekam medis
pasien. (Williams dkk, 2000).
Barthel Index telah dikembangkan sejak tahun 1965, yang kemudian
dimodifikasi oleh Granger dkk sebagai suatu teknik mengukur performa
pasien dalam 10 aktifitas hidup sehari-hari yang dikelompokkan menjadi 2
- Bagian yang berhubungan dengan perawatan diri antara lain :
makan, membersihkan diri, mandi, berpakaian, perawatan buang air
besar dan buang air kecil, penggunaan toilet
- Bagian yang berhubungan dengan mobilitas antara lain : berjalan,
berpindah dan naik tangga.
Skor BI maksimum adalah 100 yang menunjukkan bahwa fungsi
fisik pasien benar-benar tanpa bantuan, dan nilai terendah adalah 0 yang
II.5. KERANGKA KONSEPSIONAL
STROKE ISKEMIK
STRES OKSIDATIF
ASAM URAT
FERRITIN
OUTCOME
Uemura,dkk 1991 :peningkatan asam urat saat iskemik.
Weir,dkk,2003 : asam urat
Æ prediktor outcome yang buruk pada stroke akut. outcome yang baik pada stroke iskemik akut
Millan,dkk,2007 : feritin Æ outcome buruk pada stroke
Davalos,dkk,2000 : ferritin Æ perburukan neurologis pada stroke iskemik akut
Millerot,dkk,2005 : ferritin
Æ meningkat pada iskemik otak berat
Gariballa,dkk,2002: penurunan kapasitas antioksidan pada SI akut
Cherubini,dkk,2000 : anti oksidan berkurang pada stroke iskemik akut
Leinonen,dkk,2000 : aktivitas antioksidan plasma yg rendah Æ volume lesi yang luas dan gangguan neurologis
Thomas,dkk,1985 : Ferritin Æ peroksidasi lipid
Davies,dkk,1986: ikatan asam urat-zat besi Æ antioksidan Feig,dkk,2008 : asam urat
Æ radikal bebas
Warner,dkk,2004 : iskemia Æ pembentukan oksidan
BAB III
METODE PENELITIAN
III.1. TEMPAT DAN WAKTU
Penelitian dilakukan di Departemen Neurologi FK USU/RSUP
H.Adam Malik Medan dari tanggal 26 Agustus 2009 s.d 30 April 2010.
III.2. SUBJEK PENELITIAN
Subjek penelitian diambil dari populasi pasien rumah sakit.
Penentuan subjek penelitian dilakukan menurut metode sampling
konsekutif.
III.2.1. Populasi Sasaran
Semua penderita stroke iskemik akut yang ditegakkan dengan
pemeriksaan klinis dan CT Scan kepala.
III.2.2. Populasi Terjangkau
Semua penderita stroke iskemik yang dirawat di ruang rawat inap
terpadu (Rindu) A4 Departemen Neurologi FK USU / RSUP.H.Adam Malik
Medan.
III.2.3. Besar Sampel
Besar sampel dihitung menurut rumus (Madiyono, 2008)
2 n = (Zα + Zβ) s
Xa-Xo
Zα = nilai baku normal dari tabel Z yang besarnya bergantung pada
Zβ = nilai baku normal dari tabel Z yang besarnya tergantung pada
nilai β yang ditentukan (untuk β = 0,10 Æ Zβ = 1,282
S = simpangan baku populasi = 8.8
Xa-Xo = perbedaan klinis yang diinginkan = 5
n = 32.557 = 33 orang
III.2.4. Kriteria Inklusi
1. Semua pasien stroke iskemik fase akut yang dirawat di bangsal
Neurologi Rindu A4 RSUP H.Adam Malik Medan
2. Memberikan persetujuan untuk ikut serta dalam penelitian ini
III.2.5. Kriteria Eksklusi
1. Pasien stroke yang tidak dikonfirmasi dengan pemeriksaan CT
Scan kepala.
2. Pasien dengan serangan stroke berulang.
3. Pasien stroke yang mendapat terapi / suplemen zat besi
III.3. BATASAN OPERASIONAL
Stroke adalah tanda-tanda klinis yang berkembang cepat akibat gangguan fungsi otak fokal atau global, dengan gejala-gejala yang
berlangsung selama 24 jam atau lebih atau menyebabkan kematian,
Stroke iskemik adalah tanda klinis disfungsi atau kerusakan jaringan otak yang disebabkan kurangnya aliran darah ke otak sehingga
mengganggu kebutuhan oksigen di jaringan otak (Caplan,2009).
Fase akut stroke adalah jangka waktu antara 24 jam pertama serangan stroke hingga 7 hari. (Sullivan,2007)
Kadar ferritin serum : rentang nilai normal kadar ferritin serum
adalah 40-350 μg/L (ng/mL) untuk pria dan 20-250 μg/L (ng/mL) untuk
wanita. (Munker,dkk 2007)
Kadar asam urat serum : rentang nilai normal kadar asam urat serum adalah 2-7 mg/dL (Ferri,2008)
Faktor prognostik : dalam penelitian ini faktor prognostik akan
ditentukan berdasarkan outcome pasien yang diukur dengan
menggunakan skala NIHSS, BI dan MRS pada hari ke-14.
National Institute of Health Stroke Scale (NIHSS) merupakan pengkuran kuantitatif defisit neurologis berkaitan dengan stroke yang
dapat memprediksi outcome stroke jangka panjang, terdiri dari 12
pertanyaan—tingkat kesadaran, respon terhadap pertanyaan, respon
terhadap perintah, gaze palsy, pemeriksaan lapangan pandang, facial
palsy, motorik, ataksia, sensori, bahasa, disartria dan inatensi. Nilai skor
≤5 menunjukkan stroke ringan, 6-13 stroke sedang dan > 13 menunjukkan
stroke berat. (Adams dkk, 2007; Meyer dkk,2002; Schlegel dkk,2003;
William dkk,2000).
benar-benar tanpa bantuan) dan nilai terendah adalah 0 (fungsi bergantung
total). (Uyttenboogart,dkk 2005; Weimar dkk,2002 ;Sulter dkk, 1999;)
Modified Rankin Scale (mRS) merupakan skala yang menilai
outcome secara global dengan rentang nilai dari 0 (tidak ada gangguan)
hingga 5 (hanya terbaring di tempat tidur dan membutuhkan perawatan
berkelanjutan), dan 6 (fatal). Nilai mRS 0-2 dikategorikan sebagai
outcome baik dan nilai mRS 3-6 dikategorikan sebagai outcome buruk.
(Millan,dkk 2007)
Serangan Stroke Berulang adalah adanya riwayat stroke
sebelumnya pada distribusi arteri yang sama yang terjadi ≥ 29 hari
sebelumnya atau kejadian stroke pada teritori arteri berbeda dari yang
sebelumnya yang terjadi ≤ 28 hari sebelumnya. (WHO,2005)
Terapi / Suplemen Zat Besi adalah konsumsi suplemen yang mengandung zat besi. (Blanck,2005)
III.4. RANCANGAN PENELITIAN
Penelitian ini merupakan penelitian observasional tanpa perlakuan
dengan sumber data primer diperoleh dari semua penderita stroke iskemik
fase akut yang dirawat di Departemen Neurologi FK-USU / RSUP H.Adam
Malik Medan
a. Studi observasi dilakukan untuk memperoleh gambaran kadar asam
urat dan feritin serum, nilai NIHSS, mRS dan BI.
b. Studi korelasi dilakukan untuk mengetahui hubungan antara kadar
c. Studi regresi dilakukan untuk mengetahui peranan kadar asam urat
dan feritin serum terhadap skor NIHSS, mRS dan BI
III.5. PELAKSANAAN PENELITIAN III.5.1. Instrumen
III.5.1.1. Pemeriksaan kadar ferritin serum
Pemeriksaan kadar feriritin serum diukur dengan menggunakan
Cobas e 601 dengan prinsip electrochemiluminessence.
III.5.1.2. Pemeriksaan kadar asam urat serum
Pemeriksaan kadar asam urat serum diukur dengan menggunakan
Hitachi 902 Automatic Analyzer, dengan prinsip photometer.
III.5.1.3. Computed Tomography Scan (CT Scan)
CT Scan yang digunakan adalah X Ray Ct System, merk Hitachi
seri W 450.
III.5.1.4. Pengukuran Outcome
Studi ini menggunakan NIHSS, BI dan MRS sebagai skala
pengukuran outcome.
III.5.2. Pengambilan Sampel
Semua penderita stroke iskemik akut yang telah ditegakkan dengan
pemeriksaan CT scan kepala yang dirawat di ruang rawat inap neurologi
(RA4) RSUP. H. Adam Malik Medan yang memenuhi kriteria inklusi dan
tidak ada kriteria eksklusi, diambil darah vena setelah berpuasa selama
Klinik RSUP. H. Adam Malik. Penilaian NIHSS,BI dan MRS dilakukan oleh
dokter pemeriksa
III.5.3. Kerangka Operasional
Penderita Stroke
Anamnese
Pemeriksaan Neurologis
CT Scan Kepala
Kriteria Inklusi Kriteria Eksklusi
Surat Persetujuan Ikut Penelitian
Pemeriksaan NIHSS
Pemeriksan kadar feritin serum
Pemeriksaan kadar asam urat serum
Pemeriksaan BI, MRS,NIHSS (hari ke-14)
Analisa Data
III.5.4. Variabel yang Diamati
Variabel Bebas : Kadar feritin serum, kadar asam urat serum
III.5.5. Analisa Statistik
Data hasil penelitian dianalisa secara statistik dengan bantuan
program komputer Windows SPSS (Statistical Product and Science
Service) 15.
Analisa dan penyajian data dilakukan sebagai berikut
1. Analisa deskriptif digunakan untuk melihat gambaran karakteristik
demografik, kadar feritin serum dan kadar asam urat serum pada
penderita stroke iskemik akut.
2. Untuk mengetahui hubungan antara kadar ferritin dengan kadar asam
urat serum digunakan uji korelasi Pearson
3. Untuk mengetahui peranan kadar feritin dan asam urat dengan skor
NIHSS,MRS dan BI digunakan uji regresi linear ganda
4. Untuk mengetahui perbedaan kadar asam urat serum berdasarkan
jenis kelamin, ada tidaknya faktor risiko stroke,digunakan uji
t-independent, sedangkan berdasarkan skor NIHSS awal, suku dan
kelompok usia digunakan uji Anova
5. Untuk mengetahui perbedaan kadar feritin serum berdasarkan jenis
kelamin, ada tidaknya faktor risiko stroke,digunakan uji t-independent,
sedangkan berdasarkan skor NIHSS awal, suku dan kelompok usia
digunakan uji Anova
6. Untuk mengetahui perbedaan skor NIHSS,mRS dan BI berdasarkan
jenis kelamin, ada tidaknya faktor risiko stroke,digunakan uji
t-independent, sedangkan berdasarkan kelompok usia digunakan uji