63
Lampiran 1. Hasil Determinasi Tumbuhan pecut kuda (Stachytharpheta
64
65
Lampiran 3. Karakteristik Tumbuhan Pecut Kuda
66
Ekstrak etanol pecut kuda
67
Lampiran 4. Hasil Pemeriksaan Mikroskopik
Gambar: Serbuk simplisia pecut kuda
Keterangan: 1. Rambut
2. Rambut kelenjar 3. Jaringan palisade
4. Pembuluh kayu dengan penebalan jala 5. Fragmen mesofil
6. Epidermis
6 4 3
5
68
Lampiran 5. Perhitungan karakterisasi simplisia dan ekstrak pecut kuda
Perhitungan penetapan kadar air dari serbuk simplisia pecut kuda
No Berat Sampel (g) Volume Awal (ml) Volume Akhir (ml)
69
% Kadar sari larut dalam air rata-rata =
3
70
% Kadar sari larut dalam etanol rata-rata =
3
71
Perhitungan Penetapan Kadar Abu tidak Larut Asam dari Serbuk Simplisia pecut kuda (Lanjutan)
Perhitungan penetapan kadar air ekstrak pecut kuda (Lanjutan)
72 Perhitungan penetapan kadar abu total ekstrak pecut kuda (Lanjutan)
73
Perhitungan penetapan kadar abu tidak larut asam ekstrak pecut kuda (Lanjutan) No Berat Sampel (g) Berat Abu (g)
% Kadar abu yang tidak larut dalam asam rata-rata
74
Lampiran 6. Alat yang digunakan
Modifikasi alat penampung urin
Alat AAS
75
Lampiran 7. Data volume urin (ml), pH urin, kadar natrium, dan kadar kalium
(meq/l) setelah pemberian ekstrak dan furosemid (pembanding) No Parameter Kontrol
CMC Na 0,5%
Furosemid 10 mg/kg
bb
76
Lampiran 8. Tabel konversi dosis hewan dengan manusia Konversi dosis
antara jenis hewan dengan manusia (Laurence and Bacharach, 1964).
Mencit 20 g
Tikus 200 g
Marmut 400 g
Kelinci 1,2 kg
Kera 4 kg
Anjing 12 kg
Manusia 70 kg Mencit
20g
1,0 7,0 12,25 27,8 64,1 124,2 387,9
Tikus 200g
0,14 1,0 1,74 3,9 9,2 17,8 56,0
Marmut 400 g
0,08 0,57 1,0 2,25 5,2 10,2 31,5
Kelinci 1,2 kg
0,04 0,25 0,44 1,0 2,4 4,5 14,2
Kera 4 kg
0,016 0,11 0,19 0,42 1,0 1,9 6,1
Anjing 12 kg
0,008 0,06 0,10 0,22 0,52 1,0 3,1
Manusia 70 kg
77
Lampiran 9. Contoh perhitungan dosis kontrol CMC Na 0,5%
- Pembuatan CMC 0,5% = 500 mg/ 100 ml = 5 mg/ml
- Perhitungan CMC Na 0,5% pada tikus 200 g = 1% × BB Tikus
=
ml 100
g 1
× 200 g
= 2 ml
78
Lampiran 10. Contoh Perhitungan Dosis Furosemid
Furosemid yang digunakan = 40 mg
Dosis Furosemid 10 mg/kg bb untuk tikus 200 g Furosemid yang diberikan =
g 1000
bb mg/kg 10
× 200 g
= 2 mg Volume yang diberikan =
mg 40
mg 2
× 10 ml
= 0,5 ml
79
Lampiran 11. Contoh perhitungan dosis dari ekstrak etanol pecut kuda 1%
1. Untuk dosis 100 mg/kg bb pada tikus 180,2 g =
Volume yang diberikan =
mg/ml 10
mg 18,02
= 1,802 ml
2. Untuk dosis 150 mg/kg bb pada tikus 179,5 g
=
Volume yang diberikan =
mg/ml 10
mg 26,92
= 2,692 ml
3. Untuk dosis 200 mg/kg bb pada tikus 188,9 g
=
Volume yang diberikan =
mg/ml 10
mg 37,78
80
Lampiran 12. Hasil pengujian AAS dari volume urin untuk kadar Na+ dan K+ No Kelompok pengujian Tikus Konsentrasi
Na+ K+
1. Kontrol CMC-Na 0,5%
1 1,5384 3,5221
2 1,8014 3,7006
3 1,4531 4,0022
4 1,8664 3,7044
5 1,9220 4,5113
2. Furosemid dosis 10 mg/kg bb
1 3,7151 6,4331
2 4,2884 8,3544
3 4,1803 7,9225
4 4,5468 7,5239
5 4,8321 8,5321
3. EEPK dosis 100 mg/kg bb
1 2,7504 4,4252
2 3,0080 4,6997
3 3,2051 5,1220
4 2,7671 4,8150
5 3,6228 5,9921
4. EEPK dosis 150 mg/kg bb
1 2,9204 4,7308
2 3,1005 5,5321
3 2,9884 5,6682
4 3,4260 5,1595
5 3,8846 6,8311
5. EEPK dosis 200 mg/kg bb
1 3,4821 5,0330
2 4,0111 6,8766
3 3,3550 5,8850
4 4,1250 6,9236
81
Lampiran 13. Contoh perhitungan kadar elektrolit (Lanjutan)
Kadar Na = x 500
Pembacaan pada AAS = 1,5384 mcg/ml
Kadar Na =
ml 1
mcg/ml 1,5384
x 500 = 769,2 mcg/ml
= 0,7692 mg/ml
meq/l = x 1 meq
=
23 mg/ml 0,7692
x 1 meq = 0,03344 meq/ml
82
Lampiran 14. Data kalibrasi natrium dengan AAS, perhitungan persamaan
garis regresi dan koefisien korelasi No. Konsentrasi (µg/ml)
(X)
15,0000 2,1147 7,7676 55,0000 1,09708249 = 2,5 = 0,35245 Dengan nilai r sebagai berikut :
83
Lampiran 15. Data kalibrasi kalium dengan AAS, perhitungan persamaan
garis regresi dan koefisien korelasi No. Konsentrasi (µg/ml)
(X) 30,0000 1,2709 9,366 220,0000 0,39881489
= 5 = 0,211817 Dengan nilai r sebagai berikut :
84
Lampiran 16. Skema pembuatan ekstrak etanol pecut kuda dan uji
aktivitas diuretik
Maserasi dengan etanol 96% selama 5 hari
Didiamkan selama 2 hari
Diuapkan dengan Rotary Evaporator
Dikeringkan dengan Freeze Dryer
Uji aktivitas diuretik
Dikondisikan selama 2 minggu
Dipuasakan selama ± 12 jam
Diberi ekstrak etanol Pecut kuda
(EEPK) dengan dosis berbeda
Diukur Diukur dengan pH meter dengan AAS
Nilai pH
Serbuk simplisia herba pecut kuda
Ampas Maserat
Ekstrak kental Etanol
Ekstrak etanol pecut kuda (EEPK)
Tikus
Urin
Volume urin
Maserat
Elektrolit
85
Lampiran 17. Hasil data statistik ANAVA dengan Uji Tukey Jam ke 1- 5
ANOVA
Post Hoc Tests
Multiple Comparisons
95% Confidence Interval
Lower
Bound
Upper
Bound
Kontrol CMC Na
86
mg/kg bb Furosemid 10 mg/kg bb -.5000 .2034 .141 -1.109 .109
EEPK 100 mg/kg bb -.1000 .2034 .987 -.709 .509
EEPK 150 mg/kg bb .3000 .2034 .589 -.309 .909
*. The mean difference is significant at the 0.05 level.
ANOVA
Post Hoc Tests
Multiple Comparisons
Volume_Urin_Jam_Ke_2
Tukey HSD
(I)
Kelompok_Pen
gujian (J) Kelompok_Pengujian
Mean
Difference
(I-J)
Std.
Error Sig.
95% Confidence Interval
87
*. The mean difference is significant at the 0.05 level.
ANOVA
Post Hoc Tests
Multiple Comparisons
Volume_Urin_Jam_Ke_3
Tukey HSD
(I)
Kelompok_Peng
ujian (J) Kelompok_Pengujian
Mean
Differenc
e (I-J)
Std.
Error Sig.
95% Confidence Interval
Lower
Bound
Upper
Bound
Kontrol CMC na
88
*. The mean difference is significant at the 0.05 level.
ANOVA
Post Hoc Tests
Multiple Comparisons
95% Confidence Interval
Lower
Bound
Upper
Bound
Kontrol CMC na
89 *. The mean difference is significant at the 0.05 level.
ANOVA
Post Hoc Tests
Multiple Comparisons
Volume_Urin_Jam_Ke_5
Tukey HSD
(I)
Kelompok_Peng
ujian (J) Kelompok_Pengujian
Mean
Differenc
e (I-J)
Std.
Error Sig.
95% Confidence Interval
Lower
Bound
Upper
Bound
Kontrol CMC na
0.5%
Furosemid 10 mg/kg bb -2.8200* .2868 .000 -3.678 -1.962
90
EEPK 150 mg/kg bb -1.5200* .2868 .000 -2.378 -.662 EEPK 200 mg/kg bb -2.6800* .2868 .000 -3.538 -1.822 Furosemid 10
mg/kg bb
Kontrol CMC na 0.5% 2.8200* .2868 .000 1.962 3.678 EEPK 100 mg/kg bb 1.5400* .2868 .000 .682 2.398 EEPK 150 mg/kg bb 1.3000* .2868 .002 .442 2.158 EEPK 200 mg/kg bb .1400 .2868 .988 -.718 .998
EEPK 100
mg/kg bb
Kontrol CMC na 0.5% 1.2800* .2868 .002 .422 2.138 Furosemid 10 mg/kg bb -1.5400* .2868 .000 -2.398 -.682 EEPK 150 mg/kg bb -.2400 .2868 .916 -1.098 .618
EEPK 200 mg/kg bb -1.4000* .2868 .001 -2.258 -.542 EEPK 150
mg/kg bb
Kontrol CMC na 0.5% 1.5200* .2868 .000 .662 2.378 Furosemid 10 mg/kg bb -1.3000* .2868 .002 -2.158 -.442 EEPK 100 mg/kg bb .2400 .2868 .916 -.618 1.098
EEPK 200 mg/kg bb -1.1600* .2868 .005 -2.018 -.302 EEPK 200
mg/kg bb
Kontrol CMC na 0.5% 2.6800* .2868 .000 1.822 3.538 Furosemid 10 mg/kg bb -.1400 .2868 .988 -.998 .718
91
Lampiran 18. Hasil data statistik ANAVA dengan Uji Tukey
Hasil perhitungan nilai pH urin secara ANAVA ANOVA
Post Hoc Tests
Multiple Comparisons
95% Confidence Interval
92
Hasil perhitungan kadar natrium secara ANAVA ANOVA
Post Hoc Tests
Multiple Comparisons
95% Confidence Interval
93
*. The mean difference is significant at the 0.05 level.
Hasil perhitungan kadar kalium secara ANAVA ANOVA
Post Hoc Tests
Multiple Comparisons
95% Confidence Interval
94
10mg/kg bb EEPK 100 mg/kg bb 16.93400* 3.10608 .000 7.6395 26.2285 EEPK 150 mg/kg bb 13.29200* 3.10608 .003 3.9975 22.5865 EEPK 200 mg/kg bb 8.64000 3.10608 .076 -.6545 17.9345
EEPK 100
mg/kg bb
CMC-Na 0,5% 7.21000 3.10608 .009 -2.0845 16.5045
Furosemid 10mg/kg bb -16.93400* 3.10608 .000 -26.2285 -7.6395 EEPK 150 mg/kg bb -3.64200 3.10608 .766 -12.9365 5.6525
EEPK 200 mg/kg bb -8.29400 3.10608 .095 -17.5885 1.0005
EEPK 150
mg/kg bb
CMC-Na 0,5% 10.85200* 3.10608 .017 1.5575 20.1465 Furosemid 10mg/kg bb -13.29200* 3.10608 .003 -22.5865 -3.9975 EEPK 100 mg/kg bb 3.64200 3.10608 .766 -5.6525 12.9365
EEPK 200 mg/kg bb -4.65200 3.10608 .576 -13.9465 4.6425
EEPK 200
mg/kg bb
CMC-Na 0,5% 15.50400* 3.10608 .001 6.2095 24.7985 Furosemid 10mg/kg bb -8.64000 3.10608 .076 -17.9345 .6545
EEPK 100 mg/kg bb 8.29400 3.10608 .095 -1.0005 17.5885
EEPK 150 mg/kg bb 4.65200 3.10608 .576 -4.6425 13.9465
60
DAFTAR PUSTAKA
Anna. (2011). Uji Efek Diuretik Ekstrak Etanol 70% Daun Ceplukan (Physalis angulate L.) [Skripsi]. Universitas Muhammadiyah Surakarta, Surakarta. Halaman. 2.
Apandi, F., dan Aminah, D. (2014). Uji Aktifitas Antihipertensi Ekstrak Etanol Daun Legundi (Vitex trifolia L.) Pada Tikus Hipertensi Yang Diinduksi Efinefrin. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman. 2.
Asif, M., Atif, M., Malik, A.S.A., Dan, Z.C., Ahmad, I., Ahmad, A. (2013). Diuretic Activity of Trianthema portulacastrum Crude Extract in Albino Rats. Tropical Journal of Pharmaceutical Research 12(6): 967-972
Basset, J., R. C. Denny, G.H Jeffry, J. Mendhom. (1994). Buku Ajar Vogel: Kimia Analisis Kuantitatif Anorganik. Penerjemah: Hadyana, A dan Setiono, L. Jakarta: EGC. Halaman. 234-245.
BPOM RI. (2012). Pedoman Teknologi Formulasi Sediaan Berbasis Ekstrak Volume 1. Jakarta: Badan Pengawasan Obat dan Makanan RI. Halaman 6. 12-14.
Calista. (2010). Ekstraksi senyawa aktif dari tumbuhan liar pecut kuda sebagai obat herbal antikanker menggunakan metode ramah lingkungan. Skripsi. Universitas Katolik Widya Mandala Surabaya. Halaman. 2.
Dalimartha, S. (2000). Atlas Tumbuhan Obat Indonesia. Jilid 2 Jakarta: Pustaka Bunda. Halaman. 146-148.
Darmono, S. (2011). Buku Ajar Farmakologi Eksperimental. Jakarta: Universitas Indonesia. Halaman 110-115.
Depkes RI. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Halaman 7. 744.748.
Depkes RI. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman. 9.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman. 1-11
61
Ditjen POM. (1989). Material Medika Indonesia. Jilid V. Jakarta: Dapartemen Kesehatan RI. Halaman. 169-171. 300-337.
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halalaman. 10-11.
Edwin, K.J. (2012). Diuretik Dalam Buku Goodman & Gulman’s Dasar Farmakologi Terapi. Edisi 10. Vol. 2. Jakarta: EGC. Halaman. 744
Farnsworth, N.R. (1966). Biological and Phytochemical Screenning of Plants. Journal of Pharmaceutical Science. 55(3): 257.
Foda, F.S., dan Aminah, D. (2015). Uji Aktivitas Diuretik Ekstrak Etilasetat Pecut Kuda (Stachytharpheta jamaicensis L.Vahl ) Pada Tikus. Skripsi. Medan : Fakultas Farmasi Universitas Sumatera Utara. Halaman. 25-30.
Foye, W.O. (1995). Prinsip-Prinsip Kimia Medisinal. Jilid II. Yogyakarta: UGM Press. Halaman 145-150.
Ganong, W.F. (2002). Buku Ajar Fisiologi Kedokteran. Edisi 20. Jakarta: EGC. Halaman. 671-680.
Guyton, A.C. (1994). Fisiologi Manusia dan Mekanisme Penyakit. Edisi III. Jakarta: EGC. Halaman. 287-289.
Guyton., dan Hall. (1997). Buku Ajar Fisiologi Kedokteran. Edisi IX. Jakarta: EGC. Halaman. 289-345.
Guyton dan Hall. (2006). Textbook of Medical Physiology. Edisi ke-11. Philadelphia: Elvesier. Halaman. 323-325
Hapsoh., dan Hasanah, Y. (2011). Budidaya Tanaman Obat dan Rempah. Medan: USU Press. Halaman. 4-8.
Harborne, J.B. (1987). Metode Fitokimia Penuntun cara Modern Menganalisa Tumbuhan. Edisi II. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Bandung: ITB. Halaman. 152.
Indrayani, L. (2006). Skrining Fitokimia Dan Uji Toksisitas Ekstrak Etanol Pecut Kuda (Stachytarpheta jamaicensis L.Val) terhadap larva udang artemia salina leach). Berk. Penel. Hayati: 12. (57 – 61). Universitas Kristen Satya Wacana. Salatiga. Halaman. 2.
62
Jonad, H., Lacaille-Dubois, M. A, Lyoussi, B dan Edduks, M. 2001. Effect of The Flavonoids Extract from Spregularia purpurea Pers. On Arterial Blood Pressure and Renal Fuction in Normal and Hypertensive Rats. Journal of Ethnopharmacology. (76): 156-163.
Khabibah, N. (2011). Uji Efek Diuretik Ekstrak Buncis (Phaseolus Vulgaris L.) Pada Tikus Putih Jantan Galur Wistar. [Skripsi]. STIKES Ngudi Waluyo. Ungaran. Halaman. 2.
Mukrima. (2008). Uji efek antifungi ekstrak n-Butanol akar Pecut Kuda terhadap Candida albicans dan analisa KLT- Bioautografi. Skripsi. Fakultas MIPA, Universitas Pancasakti, Makassar. Halaman. 2.
Mutschler. E. (1991). Dinamika Obat. Edisi V. Bandung: Institut Teknologi Bandung. Halaman. 565-568.
Idu, M., Ezenwa, C. K., Ovuakporie, O., dan Faustina, K. (2105). Evaluationof diuretic activity of Stachytarpheta Jamaicensis (L.) Vahl on wistar rats. Asian Journal Of Biochemical and Pharmaceutical Research. (5): 12 Parmar, N.S., dan Prakash, S. (2006). Screening Methods in Pharmacology.
Kawali: Institute of Pharmacheutical Science and Technology. Halaman. 241-245.
Permadi, A. (2006). Tanaman Obat Pelancar Air Seni. Cetakan I. Jakarta: Penebar Swadaya. Halaman. 16-20.
Rasyid, A. (2011). Ketidakseimbangan Cairan, Elektrolit dan Eliminasi. Tanggal akses: 4 Januari 2014. http://www.sisrom.blogspot.com/2006/
05/kebutuhan-cairan-dan elektrolit.html.
Rawlins, E.A. (2003). Bentley’s Textbook of Pharmaceutics. London: Bailierre Tindall. Halaman. 201.
Tan, H.J., dan Rahardja, K. (2008). Obat-Obat Penting. Edisi keenam. Jakarta: PT. Elex Media Komputindo. Halaman. 519. 522-52.
Widjayakusuma, H. (2009). Bebas Penyakit Ginjal & Saluran Kemih. Jakarta: Pustaka Bunda. Halaman. 29
14
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode eksperimental dengan tahapan penelitian yaitu identifikasi sampel, pengumpulan dan pengolahan sampel, pembuatan simplisia, pemeriksaan karakteristik simplisia, pembuatan ekstrak, pemeriksaan skrining fitokimia serbuk simplisia dan ekstrak, karakteristik ekstrak, pengujian efek diuretik menggunakan rancangan acak lengkap (RAL). Data yang diperoleh dianalisis secara ANAVA (analisis variansi) dan dilanjutkan dengan uji beda rata-rata Tukey menggunakan program statistical and product service solution (SPSS) 17.0.
3.1 Alat dan Bahan
3.1.1 Alat-Alat
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas, lemari pengering, blender, neraca listrik (Chyo 6000), timbangan hewan (Chyo JP2-6000), seperangkat alat destilasi, rotary evaporator (Heidolph vv-2000), waterbath, freeze dryer (Modulyo, Edwards serial no:3985), oral sonde, mortir dan stamper, seperangkat alat pengujian diuresis berupa modifikasi kandang metabolik, spuit, miskroskop (Model L-301), pH meter (Hanna) dan AAS (Shimadzu AA 62000).
3.1.2 Bahan-Bahan
Bahan tumbuhan yang digunakan dalam penelitian ini adalah herba pecut
15
natrium (CMC Na (Graha Jaya)), tablet furosemid (Indofarma), aqua bidestilata, kloralhidrat.
3.2 Pengumpulan Pecut Kuda
Pengambilan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Tumbuhan yang digunakan dalam penelitian ini adalah pecut kuda (Stachytarpheta jamaicensis L. Vahl). Sampel diperoleh dari daerah Bukit Simarsayang, Kota Padang Sidempuan, Provinsi Sumatera Utara.
3.3 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian dan Pengembangan Biologi Bogor.
3.4 Pembuatan Simplisia
16
3.5 Pembuatan Ekstrak Etanol Herba Pecut Kuda
Metode: Maserasi
Ekstrak etanol yang digunakan merupakan hasil dari ekstraksi n-heksan dan ekstrak etilasetat. Pembuatan ekstrak etanol pecut kuda dilakukan dengan cara maserasi bertahap (stepwise maceration) menggunakan pelarut n-heksan, etilasetat dan etanol 96% (Ditjen, POM., 1979).
Ekstraksi dilakukan dengan cara sebagai berikut, sebanyak 600 g serbuk simplisi direndam dengan pelarut etanol 96%, ditutup, dibiarkan selama 5 hari terlindung dari cahaya sambil sering diaduk, disaring, diperas. Ampas diremaserasi dengan etanol 96% secukupnya. Pindahkan kedalam bejana tertutup, dibiarkan di tempat terlindung dari cahaya selama 2 hari. Enap tuangkan atau saring. Maserat yang diperoleh dipekatkan dengan alat rotary evaporator. Kemudian diuapkan dengan freeze dryer sampai diperoleh ekstrak kental (Ditjen, POM., 1979).
3.6 Karakterisasi Simplisia dan Ekstrak
Pemeriksaan karakterisasi simplisia dan ekstrak meliputi pemeriksaan makroskopik dan mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam air, penetapan kadar sari larut dalam etanol, penetapan kadar abu total, penetapan kadar abu tidak larut dalam asam (Ditjen, POM., 1989).
3.6.1 Pemeriksaan Makroskopik dan organoleptik
Pemeriksaan makroskopik dan organoleptik dilakukan dengan mengamati bentuk, rasa, bau, dan warna dari pecut kuda.
3.6.2 Pemeriksaan Mikroskopik
17
kloralhidrat dan ditutup dengan kaca penutup kemudian diamati dibawah mikroskop.
3.6.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Alat terdiri dari labu alas bulat 500 ml, alat penampung, pendingin, tabung penyambung dan tabung penerima. Cara penetapannya, yaitu:
Pada labu bulat dimasukkan 200 ml toluen dan 2 ml air suling, didestilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air di dalam tabung penerima dibaca dengan ketelitian 0,05 ml. Kemudian ke dalam labu yang berisis toluen jenuh tersebut dimasukkan 5 g serbuk simplisia yang telah ditimbang seksama, lalu dipanaskan hati-hati selama 15 menit. Setelah toluen mulai mendidih, kecepatan tetesan diatur lebih kurang 2 tetes per detik hingga sebagian air tersuling. Kemudian kecepatan dinaikkan hingga 4 tetes per detik. Kemudian setelah semua air tersuling, destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin sampai suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO., 1998).
3.6.4 Penetapan kadar sari larut dalam air
18
kering dalam cawan penguap yang berdasar rata yang telah ditara dan sisa dipanaskan pada suhu 105oC sampai diperoleh bobot konstan. Kadar sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes, RI., 1979).
3.6.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai diperoleh bobot konstan. Kadar sari yang larut dalam etanol 96% dihitung terhadap bahan yang telah dikeringkan (Depkes, RI., 1979).
3.6.6 Penetapan kadar abu total
Sebanyak 2 g serbuk simplisia dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, jika arang masih tidak dapat dihilangkan, ditambahkan air panas, saring melalui kertas saring bebas abu. Pijarkan sisa dan kertas saring dalam krus yang sama. Masukkan filtrat ke dalam krus, uapkan, pijarkan hingga bobot tetap, timbang. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Depkes, RI., 1995).
3.6.7 Penetapan kadar abu tidak larut asam
19
kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan (Depkes, RI., 1979).
3.7 Skrining Fitokimia
Skrining fitokimia dilakukan menurut Depkes (1995), dan Farnsworth (1966), untuk mengetahui golongan senyawa alkaloid, flavonoid, glikosida, glikosida antrakuinon, saponin, tanin, dan steroida/triterpenoida. Di mana skrining fitokimia dilakukan terhadap simplisia dan ekstrak etanol pecut kuda.
3.7.1 Pemeriksaan Alkaloida
Simplisia atau ekstrak etanol pecut kuda ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloida: diambil 3 tabung reaksi, lalu kedalamannya dimasukkan 0,5 ml filtrat.
Pada masing-masing tabung reaksi:
a. ditambahkan 2 tetes pereaksi Mayer b. ditambahkan 2 tetes pereaksi Bouchardat c. ditambahkan 2 tetes pereaksi Dragendroff
Alkaloida positif jika terjadi endapan atau kekeruhan paling sedikit dua dari tiga percobaan diatas (Depkes, RI., 1995).
3.7.2 Pemeriksaan Flavonoida
20
jika warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.7.3 Pemeriksaan Glikosida
Simplisia dan ekstrak etanol pecut kuda ditimbang sebanyak 3 g, lalu disari dengan 30 ml campuran etanol 96% dengan air (7:3) dan 10 ml asam klorida 2 N, direfluks selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran isopropil dan kloroform (2:3), dilakukan berulang kali sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada temperatur tidak lebih dari 50ºC. Sisanya dilarutkan dalam 2 ml air dan 5 tetes pereaksi Molish. Kemudian secara perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan ikatan gula (Depkes, RI., 1995).
3.7.4 Pemeriksaan Saponin
Simplisia atau ekstrak etanol pecut kuda ditimbang sebanyak 0,5 g dan
dimasukkan ke dalam tabung reaksi, lalu ditambahkan 10 ml air panas, dinginkan kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1 - 10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Depkes, RI., 1995).
3.7.5 Pemeriksaan Tanin
Simplisia atau ekstrak etanol pecut kuda ditimbang sebanyak 1 g,
21
warna biru kehitaman atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.7.6 Pemeriksaan Steroida/Triterpenoida
Sebanyak 1 g simplisia atau ekstrak etanol pecut kuda dimaserasi dengan 20 ml n-heksan selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan beberapa tetes pereaksi Lieberman-Burchard. Timbulnya warna biru atau biru hijau menunjukkan adanya steroida, sedangkan warna merah, merah muda atau ungu menunjukkan adanya triterpenoida (Harborne, 1987).
3.8 Penyiapan Bahan Uji, Obat Pembanding dan Kontrol
Ekstrak etanol 96% simplisia pecut kuda dibuat dalam bentuk suspensi menggunakan CMC Na 0,5%. Obat pembanding furosemid dibuat dalam bentuk suspensi menggunakan CMC Na 0,5%. Kontrol negatif yang digunakan adalah suspensi CMC Na 0,5%.
3.8.1 Pembuatan suspensi CMC Na 0,5%
Sebanyak 0,5 g CMC Na ditaburkan dalam lumpang yang berisi 20 ml air
suling panas. Didiamkan selama 15 menit lalu digerus hingga diperoleh massa yang transparan, lalu digerus sampai homogen, diencerkan dengan air suling, dihomogenkan dan dimasukkan ke labu tentukur 100 ml, dicukupkan volumenya dengan air suling hingga 100 ml.
3.8.2 Pembuatan suspensi furosemid dosis 10 mg/kg bb
22
3.9 Penyiapan Hewan Percobaan
Hewan percobaan yang digunakan dalam penelitian ini adalah tikus putih jantan dengan berat 150 - 200 g. Sebelum pengujian dikondisikan terlebih dahulu selama satu minggu dengan kondisi lingkungan, makanan, dan minuman yang sama. Setelah satu minggu, dipilih tikus yang sehat ditandai dengan berat badan yang stabil atau meningkat.
3.10 Pengujian Efek Diuretik pecut kuda
Hewan yang digunakan sebanyak 25 ekor tikus putih jantan yang setiap
kelompok terdiri dari 5 ekor tikus. Tikus dipuasakan tidak diberi makan selama ± 12 jam dengan tetap diberi minum, kemudian bobot tikus ditimbang. Tikus diberikan NaCl 0,9% secara oral dengan dosis 20 ml/kg bb. Masing-masing tikus diberi perlakuan yang dibagi menjadi 5 kelompok yaitu kelompok kontrol negatif diberikan CMC-Na 0,5%, kontrol positif diberikan furosemid 10 mg/kg bb, dan pemberian bahan obat ekstrak etanol pecut kuda dosis 100, 150, 200 mg/kg bb. Tikus diletakkan di dalam kandang metabolik yang telah dimodifikasi. Volume urin yang diekskresikan dicatat setiap jam dan akumulasinya selama 5 jam sebagai urin total dan cek pH urin serta ditentukan kadar elektrolit natrium dan kalium dalam urin (Parmar dan Prakash, 2006).
3.10.1 Pengukuran pH urin
23
1% yaitu ditimbang 1 gram sampel dan dilarutkan dalam 100 ml air suling. Kemudian elektroda dicelupkan dalam larutan tersebut. Dibiarkan alat menunjukkan harga pH konstan. Angka yang ditunjukkan pH meter merupakan pH sampel (Rawlins, 2003).
3.10.2 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (konsentrasi 1000 µg/ml) dipipet sebanyak 2,5 ml,
dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 50 µg/ml).
Larutan untuk kurva kalibrasi kalium dibuat dengan memipet (1; 2; 3; 4; dan 5) ml dari larutan baku 50 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan hingga garis tanda dengan akuabides larutan ini mengandung (2,0; 4,0; 6,0; 8,0; 10,0) µg/ml dan diukur absorbansinya pada panjang gelombang 766,5 nm dengan nyala udara-asetilen.
3.10.3 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (konsentrasi 1000 µg/ml) dipipet sebanyak 2,5 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 50 µg/ml).
24
3.10.4 Penentuan Kadar Natrium dan Kalium dengan Spektrofotometer Serapan Atom
Sebanyak 1 ml urin dimasukkan ke dalam labu tentukur 50 ml kemudian dicukupkan dengan akuades sampai 50 ml. Dipindahkan ke dalam erlemeyer dan ditambahkan 5 ml HNO3 pekat dan beberapa batu didih. Didihkan secara
perlahan-lahan kemudian diuapkan dengan hotplate hingga volume urin total tinggal 20 ml, saring. Filtrat dimasukkan ke dalam labu tentukur 100 ml dicukupkan dengan akuades sampai garis tanda. Faktor pengenceran untuk penentuan kadar natrium pada urin adalah 5 kali, faktor pengenceran untuk penentuan kadar kalium pada urin adalah 2,5 kali. Selanjutnya diukur menggunakan alat SSA (SNI, 2004).
3.11 Analisis Data
25
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Pusat Penelitian dan Pengembangan LIPI Bogor, menunjukkan bahwa tumbuhan yang diteliti adalah pecut kuda (Stachytarpheta jamaicensis (L.) Vahl), suku Verbenaceae (Lampiran 1 halaman 47).
4.2 Hasil Karakterisasi Simplisia dan Ekstrak
Hasil pemeriksaan makroskopik simplisia pecut kuda menunjukkan simplisia berwarna coklat, tekstur rapuh, berbau khas, berasa sepat, sifatnya pahit. Hasil pemeriksaan mikroskopik serbuk simplisia pecut kuda terlihat adanya rambut, rambut kelenjar, jaringan palisade, pembuluh kayu dengan penebalan jala, fragmen mesofil dan epidermis (Lampiran 4 halaman 51).
Menurut Ditjen POM (2000), standarisasi suatu simplisia dan ekstrak adalah pemenuhan terhadap persyaratan sebagai bahan obat dan menjadi penetapan nilai untuk berbagai parameter produk. Hasil pemeriksaan karakteristik simplisia dan ekstrak pecut kuda dapat dilihat pada Tabel 4.1.
Tabel 4.1 Hasil karakterisasi simplisia dan ekstrak pecut kuda
No Parameter Hasil (%)
Simplisia Ekstrak
1 Kadar air 8,61 7,82
2 Kadar sari larut dalam air 20,16 -
3 Kadar sari larut dalam etanol 28,31 -
4 Kadar abu total 5,44 2,08
26
secara umum dengan syarat yaitu tidak lebih dari 10% (Ditjen, POM., 1995). Penetapan kadar air dilakukan untuk memberikan batasan minimal atau rentang tentang besarnya kandungan air dalam ekstrak karena tingginya kandungan air menyebabkan ketidakstabilan sediaan obat, bakteri dan jamur cepat tumbuh dan bahan aktif yang terkandung didalamnya dapat terurai.
Karakterisasi simplisia lain seperti penetapan kadar abu total, penetapan kadar abu yang tidak larut dalam asam, penetapan kadar sari yang larut dalam etanol, dan penetapan kadar sari yang larut dalam air khusus untuk simplisia pecut kuda belum ada literatur yang mencantumkannya sehingga tidak mempunyai standarisasi. Penetapan kadar sari yang larut dalam air dan etanol dilakukan untuk mengetahui jumlah senyawa yang dapat tersari dalam air dan dalam etanol dari suatu simplisia. Senyawa yang bersifat polar dan larut dalam air akan tersari oleh air. Sedangkan senyawa-senyawa yang tidak larut dalam air dan larut dalam etanol akan tersari oleh etanol.
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral internal yang terdapat di dalam simplisia yang diteliti serta senyawa organik yang tersisa selama pembakaran. Abu total terbagi dua yang pertama abu fisiologis adalah abu yang berasal dari jaringan tumbuhan itu sendiri dan abu non fisiologis adalah sisa setelah pembakaran yang berasal dari bahan-bahan dari luar yang terdapat pada permukaan simplisia. Kadar abu tidak larut asam untuk menentukan jumlah silika, khususnya pasir yang ada pada simplisia dengan cara melarutkan abu total dalam asam klorida (WHO., 1998).
oksida-27
oksida anorganik. Kadar abu total yang tinggi menunjukkan adanya zat anorganik logam-logam (Ca, Mg, Fe, Cd dan Pb) yang sebagian mungkin berasal dari pengotoran. Kadar logam berat yang tinggi dapat membahayakan kesehatan, oleh sebab itu perlu dilakukan penetapan kadar abu total dan kadar abu tidak larut asam untuk memberikan jaminan bahwa ekstrak tidak mengandung logam berat tertentu melebihi nilai yang ditetapkan karena berbahaya (toksik) bagi kesehatan.
Herba pecut kuda yang digunakan pada penelitian ini sebanyak 2,9 kg, yang selanjutnya dikeringkan dalam lemari pengering pada temperatur ± 40ºC sampai buah kering dan diperoleh berat simplisia sebesar 1,1 kg.
Hasil penyarian 600 g serbuk simplisia pecut kuda dengan pelarut etanol 96% diperoleh ekstrak kental yang kemudian diuapkan dengan menggunakan rotary evaporator dan kemudian dikeringkan dengan menggunakan freeze dryer diperoleh 83,15 g ekstrak dengan rendeman sebesar 13,85%.
4.3 Hasil Skrining Fitokimia Simplisia dan EEPK
Skrining fitokimia serbuk simplisia dan ekstrak etanol pecut kuda dilakukan untuk mengetahui senyawa kimia yang terdapat pada simplisia tersebut, dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil skrining fitokimia serbuk simplisia dan ekstrak etanol pecut kuda
(EEPK)
No Parameter Pecut kuda
Serbuk simplisia Ekstrak Etanol
1 Alkaloida + +
2 Flavonoida + +
3 Saponin - -
4 Tanin + +
5 Glikosida + +
6 Steroida/Triterpenoida + +
28
Berdasarkan hasil skrinning fitokimia serbuk simplisia dan ekstrak etanol pecut kuda (Stachytarpheta jamaicensis (L.) Vahl mengandung alkaloid, flavonoid, tanin, glikosida dan steroida/triterpenoida.
4.4 Hasil Pengujian Efek Diuretik
Pengujian efek diuretik ekstrak etanol pecut kuda dengan parameter volume urin, pH urin, kadar natrium dan kadar kalium dalam urin terhadap tikus putih jantan.
4.4.1 Hasil volume urin
46
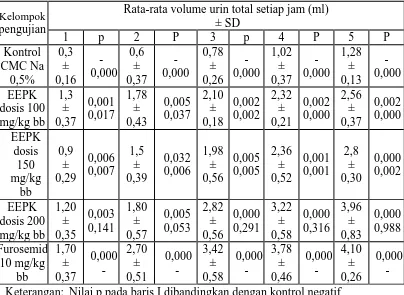
Tabel 4.3 Hasil pengukuran volume urin rata-rata setiap jam selama 5 jam
Kelompok
pengujian
Rata-rata volume urin total setiap jam (ml) ± SD Keterangan: Nilai p pada baris I dibandingkan dengan kontrol negatif
Nilai p pada baris II dibandingkan dengan kontrol positif p (Signifikan)
Pada Tabel 4.3 menunjukkan bahwa kelompok uji yang diberikan EEPK dosis 100, 150 dan 200 mg/kg bb terjadi peningkatan volume urin dan terdapat perbedaan yang signifikan terhadap kelompok kontrol negatif yang diberikan CMC Na 0,5% dengan nilai signifikan (p < 0,05). Hal ini menunjukkan adanya efek diuretik dari EEPK.
Pada kelompok uji yang diberikan EEPK dosis 100,150 dan 200 mg/kg bb diperoleh hasil yang menunjukkan bahwa peningkatan pemberian dosis EEPK dapat meningkatkan pengeluaran volume urin dan terdapat perbedaan yang signifikan antara kelompok uji dengan nilai signifikan (p < 0,05).
47
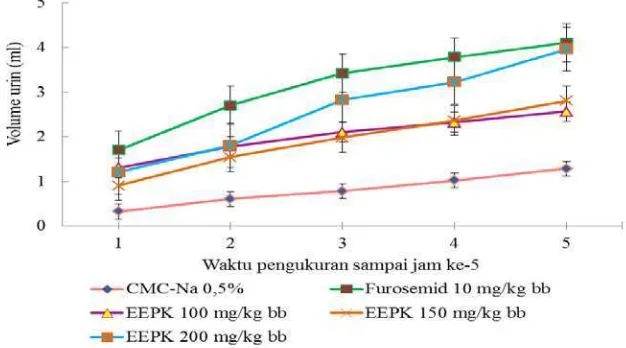
statistik menunjukkan bahwa EEPK dosis 200 mg/kg bb tidak terdapat perbedaan yang signifikan terhadap kelompok kontrol positif yang diberikan furosemid 10 mg/kg bb dengan nilai signifikan (p ≥ 0,05). Profil volume urin terhadap waktu ditunjukkan pada Gambar 4.1.
Gambar 4.1 Volume urin rata-rata terhadap waktu setiap jam selama 5 jam
48
150 dan 200 mg/kg bb. Pada jam ke-3 terjadi proses dimana senyawa yang ada dalam ekstrak etanol pecut kuda telah berikatan dengan reseptor sehingga menghasilkan efek diuretik. Senyawa yang berpengaruh pada aktivitas diuretik ekstrak etanol pecut kuda ini adalah alkaloid dan flavonoid. Menurut (Jabar, 2011), bahwa alkaloid dan flavonoid dapat meningkatkan pengeluaran volume urin dan pengeluaran elektrolit pada tikus. Selain itu kandungan kalium berfungsi sebagai diuretik sehingga pengeluaran natrium cairan meningkat, jumlah natrium rendah, tekanan darah turun.
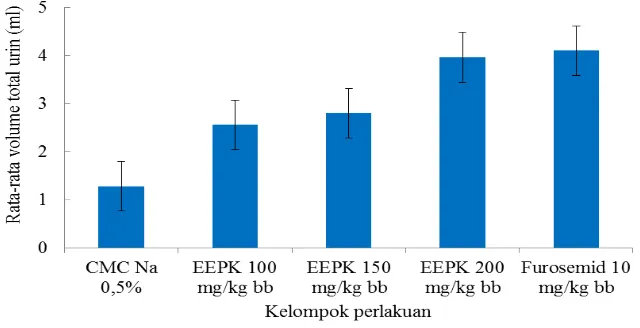
Gambar 4.2 Volume total urin pada tikus
Pada Gambar 4.2 dapat dilihat bahwa volume total urin dengan rata- rata untuk kontrol negatif 1,28±0,130 ml, EEPK dosis 100 mg/kg bb 2,56±0,378 ml, EEPK dosis 150 mg/kg bb 2,8±0,308 ml, EEPK dosis 200 mg/kg bb 3,96±0,838 ml, furosemid 10 mg/kg bb 4,10±0,264 ml. Berdasarkan data volume urin total yang dihasilkan maka dapat dikatakan bahwa EEPK memberikan efek diuretika dimana terjadi peningkatan jumlah volume urin yang dikeluarkan oleh tubuh dibandingkan volume urin total kelompok kontrol negatif.
49
Hal tersebut sesuai dengan hasil yang diperoleh pada penelitian Idu, et. al., (2015) dan Foda, dkk., (2015) bahwa pemberian ekstrak dengan dosis yang meningkat terhadap hewan uji maka semakin banyak mempengaruhi pengeluaran volume urin.
Berdasarkan hasil statistik yang diperoleh, EEPK dengan dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan efek diuretik terhadap volume urin. Dari ketiga dosis tersebut, EEPK dengan dosis 200 mg/kg bb mempunyai efek diuretik yang paling baik terhadap volume urin dengan nilai signifikan (p ≥ 0,05) dibandingkan dengan kontrol negatif. Peningkatan pemberian dosis EEPK dapat meningkatkan pengeluaran volume urin terhadap tikus.
50
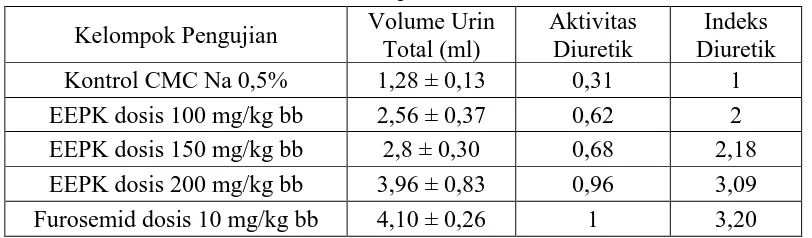
Indeks diuretik dari hasil penelitian ekstrak etanol pecut kuda dapat ditunjukkan pada Tabel 4.4.
Tabel 4.4 Indeks diuretik ekstrak etanol pecut kuda
Kelompok Pengujian Volume Urin Total (ml)
Aktivitas Diuretik
Indeks Diuretik
Kontrol CMC Na 0,5% 1,28 ± 0,13 0,31 1
EEPK dosis 100 mg/kg bb 2,56 ± 0,37 0,62 2 EEPK dosis 150 mg/kg bb 2,8 ± 0,30 0,68 2,18 EEPK dosis 200 mg/kg bb 3,96 ± 0,83 0,96 3,09 Furosemid dosis 10 mg/kg bb 4,10 ± 0,26 1 3,20
Menurut Asif (2013), bahwa nilai indeks diuretik lebih besar 1,50 adalah aktivitas diuretik kuat. Sedangkan nilai indeks diuretik mulai dari 1,00-1,50 menunjukkan aktivitas diuretik sedang dan 0,72-0,99 menunjukkan aktivitas diuretik ringan, nilai indeks diuretik lebih kecil 0,72 menunjukkan tidak ada aktivitas diuretik. Dalam penelitian ini, nilai indeks diuretik dari ketiga kelompok perlakuan adalah 2, 2,18 dan 3,09 menunjukkan bahwa ekstrak memiliki aktivitas diuretik kuat. Berdasarkan tabel diatas EEPK dosis 200 mg/kg bb menunjukkan aktivitas diuretik sebesar 96% dibandingkan dengan furosemid.
4.4.2 Hasil nilai pH
51
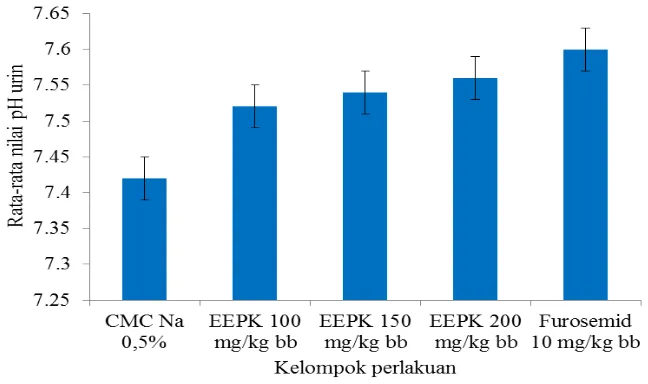
Berdasarkan hasil pengukuran nilai pH urin dari volume urin pada jam ke-5 sebagai pH urin total pada setiap kelompok uji dapat dilihat pada Tabel 4.5 dan Gambar 4.3.
Tabel 4.5 Hasil pengukuran nilai pH urin tikus pada kelompok uji
No Kelompok Pengujian
Nilai pH Rata-rata
± SD Keterangan: Nilai p pada baris I dibandingkan dengan kontrol negatif Nilai p pada baris II dibandingkan dengan kontrol positif
p (Signifikan)
T.I – T.V (Tikus 1 - Tikus 5)
52
Pada Tabel 4.5 dan Gambar 4.3 dapat dilihat bahwa nilai pH urin rata- rata untuk kontrol negatif 7,42±0,130, EEPK dosis 100 mg/kg bb 7,52±0,08, EEPK dosis 150 mg/kg bb 7,54±0,114, EEPK dosis 200 mg/kg bb 7,56±0,134, furosemid dosis 10 mg/kg bb 7,6±0,1.
Berdasarkan hasil statistik nilai pH urin total yang diperoleh, semua kelompok kontrol negatif, kelompok kontrol positif serta kelompok uji menunjukkan bahwa tidak terdapat perbedaan yang signifikan antara kelompok dengan nilai signifikansi (p ≥ 0,05), dengan demikian dapat disimpulkan bahwa EEPK memiliki nilai pH yang sama dan tidak ada pengaruh antara kelompok pengujian.
Pada hasil pengukuran pH urin menunjukkan bahwa nilai pH pada semua kelompok pengujian berada dalam rentang pH normal. Pengukuran pH urin dilakukan untuk mengetahui apakah ekstrak yang diuji termasuk dalam golongan diuretik penghambat karbonik anhidrase. Golongan diuretik penghambat karbon anhidrase dapat menyebabkan pH urin menjadi basa. Penghambatan karbon anhidrase menyebabkan ekskresi HCO3- yang cepat di urin. Hal ini seiring dengan
penghambatan terhadap titrable acid dan adanya sekresi ammonia di sistem duktus pengumpul yang mengakibatkan pH urin menjadi basa dan menimbulkan asidosis (Edwin, 2012).
4.4.3 Hasil kadar Natrium
53
ekstraseluler. Elektrolit natrium ini akan membantu pengeluaran air seni yang disebut efek diuresis (Rasyid, 2011).
Berdasarkan pengukuran kurva kalibrasi untuk natrium diperoleh persamaaan garis regresi yaitu Y=0,141763x–0,00196 dengan nilai r = 0,9999. Hal ini menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi). Hasil pengukuran kadar natrium dapat dilihat pada Tabel 4.6 dan Gambar 4.4.
Tabel 4.6 Kadar natrium dalam urin tikus pada kelompok uji
N o
Kelompok Pengujian
Kadar Natrium (meq/l)
Rata-rata Keterangan: Nilai p pada baris I dibandingkan dengan kontrol negatif
Nilai p pada baris II dibandingkan dengan kontrol positif p (Signifikan)
54
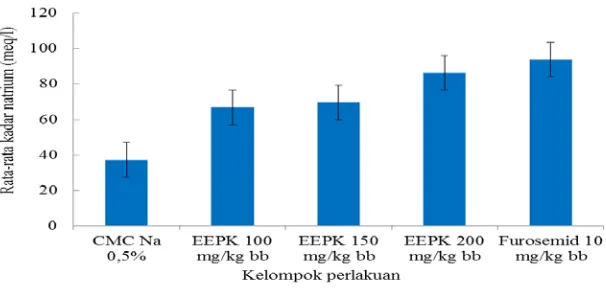
Gambar 4.4 Kadar Natrium pada urin tikus putih jantan
Pada Tabel 4.6 dan Gambar 4.4 dapat dilihat bahwa dari hasil rata-rata yang diperoleh untuk CMC Na 0,5% 37,13±4,38 meq/l; EEPK dosis 100 mg/kg bb 64,25±7,84 meq/l, EEPK dosis 150 mg/kg bb 69,56±10,06 meq/l, dan EEPK dosis 200 mg/kg bb 74,55±1,84 meq/l; furosemid dosis 10 mg/kg bb 93,74±9,09 meq/l.
Berdasarkan hasil yang diperoleh, EEPK dengan dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan efek diuretik terhadap kadar natrium dalam urin. Dari ketiga dosis tersebut, EEPK dengan dosis 200 mg/kg bb mempunyai efek pengeluaran natrium yang paling baik terhadap volume urin dengan nilai signifikan (p ≥ 0,05).
55
dalam urin mengindikasikan adanya efek diuretik yang dihasilkan dari ekstrak pecut kuda.
4.4.5 Hasil kadar Kalium
Kalium merupakan salah satu mineral makro yang berperan dalam pengaturan keseimbangan cairan tubuh. Masukan natrium yang tinggi dapat meningkatkan ekskresi kalium. Hubungan ini diperkirakan disebabkan sebagian oleh reabsorbsi kalium secara pasif mengikuti natrium dan air pada tubulus proksimal dan sepanjang lengkung Henle.
Berdasarkan pengukuran kurva kalibrasi untuk kalium diperoleh persamaaan garis regresi yaitu Y=0,211817x-0,00329 dengan nilai r = 0,9998. Hal ini menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi). Hasil pengukuran kadar kalium dalam urin tikus putih jantan pada kelompok uji dapat dilihat pada Tabel 4.7 dan Gambar 4.5.
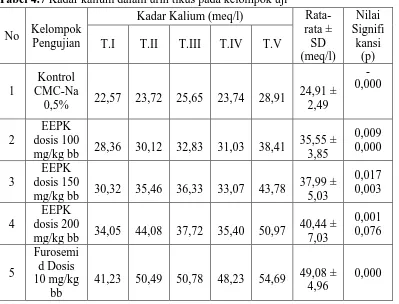
Tabel 4.7 Kadar kalium dalam urin tikus pada kelompok uji
No Kelompok Pengujian
56
Keterangan: Nilai p pada baris I dibandingkan dengan kontrol negatif Nilai p pada baris II dibandingkan dengan kontrol positif
p (Signifikan)
T.I – T.V (Tikus 1 - Tikus 5)
Gambar 4.5 Kadar Kalium pada urin tikus putih jantan
Pada Tabel 4.7 dan Gambar 4.5 dapat dilihat bahwa dari perolehan hasil rata-rata untuk kontrol negatif 24,91±2 , 4 9 meq/l; EEPK dosis 100 mg/kg bb 35,55±3,85 meq/l; EEPK dosis 150 mg/kg bb 37,99±5,03 meq/l; EEPK dosis 200 mg/kg bb 40,44±7,03 meq/l; furosemid 10 mg/kg bb 49,08±4,96 meq/l.
Berdasarkan hasil yang diperoleh, EEPK dengan dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan efek diuretik terhadap kadar kalium dalam urin. Dari ketiga dosis tersebut, EEPK dengan dosis 200 mg/kg bb mempunyai efek pengeluaran kalium yang paling baik terhadap volume urin dengan nilai signifikansi (p ≥ 0,05).
57
tikus sedangkan CMC Na 0,5 % adalah sebagai kontrol negatif dalam penelitian ini. Penelitian ini menunjukkan bahwa semakin banyak dosis ekstrak yang diberikan maka semakin banyak mempengaruhi pengeluaran volume urin dan ekskresi kalium sama halnya dengan peneliti sebelumnya bahwa peningkatan dosis dapat mempengaruhi pengeluaran kalium (Foda, dkk., 2015).
Berdasarkan hasil pengukuran kadar elektrolit natrium dan kalium dalam urin yang diekskresikan oleh tikus, maka dapat dihitung rasio Na+/K+. Nilai rasio Na+/K+ dapat dilihat pada Tabel 4.8.
Tabel 4.8 Rasio kadar elektrolit Natrium dan Kalium dalam urin tikus
Kelompok pengujian Elektrolit (meq/l) ± SD
Na+ K+ Na+/ K+
Kontrol CMC Na 0,5% 37,13 ± 4,38 24,91 ± 2,49 1,49 EEPK dosis 100 mg/kg bb 64,25 ± 7,84 35,55 ± 3,85 1,80 EEPK dosis 150 mg/kg bb 69,56 ± 10,06 37,99 ± 5,03 1,83 EEPK dosis 200 mg/kg bb 74,55 ± 1,87 40,44 ± 7,03 1,84 Furosemid dosis 10 mg/kg bb 93,74 ± 9,09 49,08 ± 4,96 1,90
58
Menurut Kebamo, et. al., (2015) rasio Na+/K+ dihitung untuk mengetahui indeks pengeluaran aldosteron (aktivitas natriuretik). Aldosteron berfungsi menjaga keseimbangan ion natrium dalam darah. Menurut Guyton (1994), apabila konsentrasi aldosteron meningkat maka sisa natrium akan direabsorbsi dari bagian dalam tubulus distal dan duktus koligens sehingga pada dasarnya tidak ada natrium keluar ke dalam urin, sebaliknya jika konsentrasi aldosteron dikurangi maka sisa natrium tidak direabsorbsi dari tubulus distal sehingga natrium keluar bersama urin.
Penelitian ini menunjukkan bahwa dengan peningkatan nilai rasio Na+/K+ dari semua kelompok pengujian terjadi peningkatan efek diuretik. Berdasarkan hasil statistik terdapat perbedaan yang signifikan antara kelompok uji dengan nilai signifikan (p < 0,05). Hal ini diduga pemberian ekstrak etanol pecut kuda menyebabkan peningkatan pengeluaran zat-zat terlarut dalam urin akibat adanya kandungan flavonoid.
59
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian ini dapat disimpulkan bahwa ekstrak etanol pecut kuda dosis 100, 150 dan 200 mg/kg bb memiliki aktivitas diuretik dengan meningkatkan volume urin, kadar natrium dan kadar kalium dalam urin tikus serta terdapat perbedaan yang signifikan dibandingkan kontrol negatif (p < 0,05). Dosis yang paling baik untuk efek diuretik pada penelitian ini yaitu EEPK dosis 200 mg/kg bb yang tidak berbeda signifikan dengan furosemid dosis 10 mg/kg bb (p ≥ 0,05) serta tidak ada pengaruh terhadap nilai pH. Dengan meningkatnya dosis maka terjadi peningkatan efek diuretik ekstrak etanol pecut kuda pada tikus.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk meneliti efek farmakologi yang
5
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Pecut kuda tumbuh liar di tepi jalan, tanah lapang dan tempat-tempat terlantar lainnya. Tanaman yang berasal dari Amerika ini dapat ditemukan di daerah cerah, sedang, terlindung dari sinar matahari dan pada ketinggian 1-1500 m dpl. Pecut kuda merupakan terna tahunan, tumbuh tegak, tinggi ±50 cm, tumbuh liar disisi jalan daerah pinggir kota, tanah kosong yang tidak terawat. Daun letak berhadapan, bentuk bulat telur, tepi bergerigi, tidak berambut. Bunga duduk tanpa tangkai pada bulir-bulir yang berbentuk pecut, panjang 4-20 cm. bunga mekar tidak berbarengan, kecil-kecil warna ungu, putih (Dalimartha, 2000).
2.1.1 Sistematika Tumbuhan
Kedudukan kategori taksa untuk jenis pecut kuda di dalam sistematika tumbuhan adalah sebagai berikut :
Divisi : Spermatophyta Sub divisi : Angiospermae Class : Dicotyledoneae Ordo : Lamiales Famili : Verbenaceae Genus : Stachytarpheta
Spesies : Stachytarpheta jamaicensis (L.) Vahl (Depkes, RI., 2000).
2.1.2 Nama Lokal
6
2.1.3 Nama Asing
Yu long Bian (Cina), Snakeweed (Inggris) (Dalimartha, 2000).
2.1.4 Kandungan Kimia
Pecut kuda mengandung glikosida, flavonoid dan alkaloid (Dalimartha, 2000).
2.1.5 Khasiat Tumbuhan
Herba pecut kuda (Stachytarpheta jamaicensis (L.) Vahl) digunakan sebagai obat infeksi dan batu saluran kencing, rematik, sakit tenggorokan, pembersih darah, haid tidak teratur, keputihan, hepatitis A. Bunga dan tangkainya untuk pengobatan radang hati sedangkan akarnya untuk pengobatan keputihan (Dalimartha, 2000).
2.2 Metode Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Depkes, RI., 2000). Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani menurut cara yang cocok, diluar pengaruh cahaya matahari langsung (BPOM, RI., 2012).
7
memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan (Syamsuni, 2006).
Metode ekstraksi dapat dilakukan dengan berbagai cara (Ditjen, POM., 2000), yaitu:
a. cara dingin
i. maserasi
Maserasi adalah proses ekstraksi dengan cara merendam simplisia dalam pelarut yang sesuai pada temperatur ruangan dan terlindung dari cahaya yang disertai pengocokan atau pengadukan.
ii. perkolasi
Perkolasi adalah penyarian dengan pelarut baru sampi sempurna yang dilakukan pada temperatur ruangan. Proses terdiri dari tahap pengembangan bahan, perendaman dan perkolasi sebenarnya (penetesan/penampungan ekstrak).
b. cara panas
i. refluks
Refluks adalah proses penyarian simplisisa dengan menggunakan pelarut pada temperatur titik didihnya selama waktu tertentu dan jumlah pelarut terbatas relatif konstan dengan adanya pendingin balik.
ii. sokletasi
8
pendingin balik dengan alat khusus sehingga terjadi ekstraksi kontiniu dengan jumlah pelarut relatif konstan.
iii. digesti
Digesti merupakan maserasi kinetik (dengan pengadukan kontinu) pada temperatur yang lebih tinggi dari temperatur kamar, umumnya dilakukan pada suhu 40-50oC. Infus
iv. infundasi
Infundasi merupakan suatu cara ekstraksi dengan menggunakan pelarut air pada temperatur 90oC selama 15 menit.
v. dekoktasi
Dekoktasi merupakan suatu cara ekstraksi pada suhu 90oC dengan menggunakan pelarut air selama 30 menit.
2.3 Ginjal
Ginjal merupakan organ utama untuk membuang produk sisa metabolisme yang tidak diperlukan tubuh. Peran penting ginjal adalah membuang sisa metabolit tubuh dari hasil pencernaan dan fungsi lainnya mengontrol volume dan komposisi cairan tubuh. Fungsi pengaturan ginjal ini untuk memelihara kestabilan lingkungan sel-sel yang diperlukan untuk melakukan berbagai aktivitas (Guyton dan Hall, 1997).
9
asam urat dan ion-ion natrium, kalium, klorida serta ion-ion hidrogen dalam jumlah yang berlebihan (Guyton, 1990).
2.4 Mekanisme Pembentukan Urin
Proses pembentukan urin dimulai dengan filtrasi sejumlah besar cairan yang bebas protein dari kapiler glomerolus ke kapsula Bowman. Kebanyakan zat dalam plasma, kecuali protein, difiltrasi secara bebas sehingga konsentrasinya pada filtrat glomerolus dalam kapsula Bowman hampir sama dengan dalam plasma. Ketika cairan yang telah difiltrasi ini meninggalkan kapsul Bowman dan mengalir melewati tubulus, cairan diubah oleh reabsorbsi air dan zat terlarut spesifik yang kembali ke dalam darah atau oleh sekresi zat-zat lain dari kapiler peritubulus ke dalam tubulus (Guyton dan Hall, 1997).
10
Gambar 2.1 Organ – organ yang membentuk saluran urin (Ganong, 2002)
2.5 Diuretik
Diuretik adalah obat yang dapat menambah kecepatan pembentukan urin. Istilah diuretik mempunyai dua pengertian, pertama menunjukan adanya penambahan volume urin yang diproduksi dan kedua menunjukan jumlah pengeluaran (kehilangan) zat-zat terlarut dan air (Foye, 1995).
Tempat kerja diuretik umumnya terletak pada sepanjang nefron yaitu pada tubulus proksimal, ansa Henle, tubulus distal atau pada tubulus penampung. Nefron merupakan suatu kesatuan fungsional yang membentuk ginjal. Mengetahui tempat kerja diuretik sangat bermanfaat karena yang menentukan potensi kerja dan efek samping diuretik adalah tempat kerja.
11
Tabel 2.1 Penggolongan diuretik berdasarkan mekanisme kerja dan tempat kerja
No Diuretik Contoh Obat Mekanisme Kerja Tempat Kerja 1. Karbonat
5. Thiazida Hidroklortiazida Klortiazida
Furosemid adalah turunan sulfonamida yang berdaya diuretik kuat dan bertitik kerja di lengkung Henle bagian menaik. Sangat efektif pada keadaan udema di otak dan paru–paru yang akut .
Kelarutan praktis tidak larut dalam air dan dalam kloroform, larut dalam 75 bagian etanol (95%) dan dalam 850 bagian eter, larut dalam larutan alkali hidroksida (Depkes, RI, 1979).
12
kurang 50%, plasma t1/2-nya 30–60 menit, ekskresinya melalui kemih secara utuh,
pada dosis tinggi juga lewat empedu.
Efek sampingnya secara umum, pada injeksi i.v terlalu cepat dan terjadi ketulian (reversibel) dan hipotensi, hipokalemia reversibel dapat terjadi pula.
Dosis pada udema: oral 40–80 mg pagi p.c., jika perlu atau insufisiensi ginjal jarang sampai 250–4000 mg sehari dalam 2–3 dosis. Injeksi i.v (perlahan) 20–40 mg, pada keadaan hipertensi sampai 500 mg (Tan dan Rahardja, 2002).
2.7 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah suatu spektrofotometri serapan yang digunakan untuk mendeteksi uap atom logam. Cara kerja alat ini berdasarkan penguapan larutan sampel, kemudian logam yang terkandung di dalamnya diubah menjadi atom bebas. Atom tersebut mengabsorpsi radiasi dari sumber cahaya yang dipancarkan dari lampu katoda (hallow cathode lamp) yang mengandung unsur yang akan ditentukan. Banyaknya penyerapan radiasi kemudian diukur pada panjang gelombang tertentu menurut jenis logamnya.
Alat–Alat Spektrofotometer Serapan Atom: a. sumber sinar ( hallow cathode lamp )
13 b. burner dan nyala
Nyala, burner dan nebulizer pada alat AAS menyebabkan kation – kation logam dalam larutan menghasilkan atom–atom logam. Alat AAS membuat penyerapan pada keadaan dasar. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara suhunya sebesar 2200ºC. Sumber nyala asetilen-udara ini merupakan sumber nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai bahan pembakar, sedangkan udara sebagai bahan pengoksidasi.
c. monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum sesuai dengan panjang gelombang yang digunakan dalam analisis dari sekian banyak spektrum yang dihasilkan lampu katoda berongga.
d. detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman.
e. alat penunjuk ( Readout Device )
1
BAB I
PENDAHULUAN
1.1Latar Belakang
Diuretik adalah zat-zat yang dapat memperbanyak pengeluaran kemih (diuresis) melalui kerja langsung terhadap ginjal. Diuretik bekerja pada ginjal untuk mengeluarkan kelebihan elektrolit dalam darah. Prinsip kerja diuretik secara umum adalah menurunkan reabsorbsi elektrolit oleh tubulus ginjal, di mana peningkatan ekskresi elektrolit akan disertai dengan peningkatan ekskresi air yang diperlukan untuk mencapai keseimbangan osmotik. Senyawa yang dapat merangsang pengeluaran air sangat potensial untuk digunakan dalam keadaan seperti: udema, gagal jantung, gagal ginjal, dan hipertensi (Permadi, 2006).
Indonesia merupakan negara agraris yang memiliki keanekaragaman hayati yang berlimpah, yaitu memiliki sekitar 30.000 jenis tanaman dan sekitar 9.600 di antaranya berkhasiat obat. Sampai saat ini, jumlah tanaman yang telah dimanfaatkan sebagai bahan obat tradisional oleh industri obat baru mencapai 300 jenis. Obat tradisional adalah bahan atau ramuan bahan yang berasal dari tumbuhan, hewan, mineral, sediaan sarian (galenik), atau campuran dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (Depkes, RI., 2000).
2
tidak teratur. Bunga dan tangkainya untuk pengobatan radang hati sedangkan akarnya untuk pengobatan keputihan (Dalimartha, 2002). Penelitian sebelumnya telah menunjukkan bahwa senyawa dari tumbuhan pecut kuda memiliki aktivitas biologis antara lain uji efek antifungi (Mukrima, 2008), antibakteri (Ningrum, 2003) dan antikanker (Calista, 2013).
Adapun suku yang sama dengan tumbuhan pecut kuda adalah legundi (Vitex trifolia) di mana legundi berdasarkan penelitian memiliki khasiat sebagai obat tekanan darah tinggi dan diuretik (Frans, 2014; Dian, 2015). Penelitian tentang tumbuhan legundi menunjukkan bahwa senyawa flavonoid dalam tumbuhan tersebut berperan sebagai antihipertensi, antibakteri, analgetik, diuretik, dan antioksidan (Widyaningrum, 2011). Oleh karena spesies tumbuhan tersebut merupakan satu suku dengan Stachytharpheta jamaicensis kemungkinan mempunyai kandungan dan aktivitas yang hampir sama dengan Stachytharpheta jamaicensis.
Berdasarkan penelitian oleh Calista tahun 2013 menyatakan bahwa tumbuhan pecut kuda memiliki kandungan senyawa metabolit sekunder salah satunya adalah flavonoid. Flavonoid merupakan senyawa yang mempunyai aktivitas biologis sebagai diuretik (Anna, 2011). Mekanisme kerja flavonoid jenis flavonol yang diduga sebagai diuretik yang disebutkan oleh Khabibah (2012), yaitu dengan menghambat reabsorbsi Na+, K+, dan Cl- sehingga terjadi peningkatan elektrolit di tubulus sehingga terjadilah diuresis.
3
1.2 Perumusan Masalah
Perumusan masalah pada penelitian ini adalah apakah ekstrak etanol pecut kuda mempunyai efek diuretik terhadap tikus?
1.3 Hipotesis
Hipotesis pada penelitian ini yaitu ekstrak etanol pecut kuda mempunyai efek diuretik terhadap tikus.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui efek diuretik dari ekstrak etanol pecut kuda dengan parameter volume urin, pH urin, kadar natrium dan kadar kalium dalam urin tikus.
1.5 Manfaat Penelitian
Manfaat dari penelitian ini adalah sebagai berikut:
a. mengembangkan tanaman pecut kuda menjadi suatu sediaan herbal terstandar dengan efek diuretik.
b. menambah inventaris tanaman obat yang berkhasiat sebagai diuretik.
1.6 Kerangka Pikir Penelitian
4
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Diagram kerangka pikir penelitian
Simplisia pecut
kuda
Ekstrak etanol pecut
kuda (EEPK) dosis 100,
150, 200 mg/kg bb
CMC Na 0,5 %
Volume urin (ml)
Kadar Na+ (meq/l)
Kadar K+ (meq/l) Waktu
pengamatan setiap jam
selama 5 jam Furosemid
10 mg/kg bb
efek
diuretik pH urin
vi
UJI AKTIVITAS DIURETIK EKSTRAK ETANOL PECUT KUDA (Stachytharpheta jamaicensis L. Vahl)
PADA TIKUS
ABSTRAK
Penggunaan tanaman obat semakin berkembang di masyarakat, salah satunya adalah pecut kuda (Stachytharpheta jamaicensis L. Vahl) yang mempunyai kandungan flavonoid yang diduga mampu menimbulkan efek diuretik. Tujuan penelitian ini adalah untuk mengetahui aktivitas diuretik ekstrak etanol pecut kuda (EEPK).
Hewan yang digunakan adalah tikus putih jantan. Tikus dipuasakan selama ± 12 jam kemudian diberikan NaCl 0,9% secara oral dengan dosis 20 ml/kg bb. Tikus dibagi menjadi 5 kelompok yaitu kelompok kontrol negatif diberikan CMC-Na 0,5%, kontrol positif diberikan furosemid 10 mg/kg bb, dan pemberian ekstrak etanol pecut kuda dosis 100, 150, 200 mg/kg bb. Tikus diletakkan di dalam kandang metabolik yang telah dimodifikasi. Volume urin yang diekskresikan dicatat setiap jam dan akumulasinya selama 5 jam sebagai urin total, diukur nilai pH serta ditentukan kadar elektrolit natrium dan kalium dalam urin menggunakan SSA (Spektrofotometri Serapan Atom) .
Hasil penelitian menunjukkan bahwa pemberian EEPK dengan dosis 100, 150 dan 200 mg/kg bb meningkatkan volume urin, kadar natrium dan kalium serta tidak ada pengaruh terhadap nilai pH dan hasil statistik menunjukkan perbedaan yang tidak berbeda signifikan terhadap kontrol positif yang diberikan furosemid dosis 10 mg/kg bb dengan tingkat signifikan p ≥ 0,05. Dosis 200 mg/kg bb menunjukkan efek diuretik paling baik dibandingkan dengan dosis lain. Volume urin total EEPK dosis 100 mg/kg bb: 2,56±0,378 ml; EEPK dosis 150 mg/kg bb: 2,8±0,308 ml; EEPK dosis 200 mg/kg bb: 3,96±0,838 ml. Nilai pH EEPK dosis 100 mg/kg bb: 7,42±0,08; EEPK dosis 150 mg/kg bb: 7,56±0,134; EEPK 200 mg/kg bb: 7,6±0,1. Kadar natrium EEPK dosis 100 mg/kg bb: 61,15±2,18 meq/l; EEPK dosis 150 mg/kg bb: 64,07±3,95 meq/l; EEPK dosis 200 mg/kg bb: 74,55±1,87 meq/l. Data kadar kalium dosis EEPK 100 mg/kg bb: 30,56±0,39 meq/l; dosis 150 mg/kg bb: 31,67±1,06 meq/l; dosis 200 mg/kg bb: 34,04±1,17 meq/l.
Berdasarkan hasil di atas, dapat disimpulkan bahwa EEPK dosis 100, 150 dan 200 mg/kg bb memberikan aktivitas diuretik dengan meningkatkan volume urin, kadar natrium dan kadar kalium terhadap tikus putih jantan.
vii
DIURETIC ACTIVITY TEST OF PORTERWEED ETHANOL EXTRACT (Stachytarpheta jamaicensis L. Vahl)
IN RATS
ABSTRACT
Currently people widely use medicinal plants, one of which is porterweed (Stachytharpheta jamaicensis L. Vahl). It contains flavonoids that are capable of causing a diuretic effect. The purpose of this study is to determine the diuretic activity of porterweed ethanol extract (EEPK).
Animals used were white male rats. The rats were fasted for ± 12 hours prior to orally administrating them 0.9% NaCl on a dose of 20 ml/kg bodyweight. They were divided into 5 groups: the negative control group was given CMC-Na 0.5%, the positive control was given furosemide 10 mg/kg bodyweight, and the ethanol extract of porterweed was at doses of 100, 150, 200 mg/kg bodyweight. The rats were placed in modified metabolic cages. Excreted urine volume was recorded every hour and so was its accumulation for 5 hours as a urine total. Its pH value was measured and its levels of electrolytes sodium and potassium in the urine was determined by using AAS (Atomic Absorption Spectrophotometry).
The results show that administration of EEPK at doses of 100, 150 and 200 mg/kg bodyweight increased urine volume, sodium and potassium, but no influence on the pH value. The statistical results did not show a significant difference to the positive control that was given furosemide at dose of 10 mg/kg bodyweight with a significant level p ≥ 0,05. The dose of 200 mg/kg bodyweight showed the most excellent diuretic effects compared to other doses. EEPK urine volume total with dose of 100 mg/kg bodyweight: 2.56 ± 0.378 ml; EEPK dose of 150 mg/kg bodyweight: 2.8±0.308 ml; EEPK dose of 200 mg/kg bodyweight: 3.96±0.838 ml. The pH value of EEPK at dose of 100 mg/kg bodyweight: 7.42±0.08; EEPK dose of 150 mg/kg bodyweight: 7.56±0.134; EEPK 200 mg/kg bodyweight: 7.6±0.1. EEPK sodium value on dose of 100 mg/kg bodyweight: 61.15 ± 2.18 mEq/l; EEPK dose of 150 mg/kg bodyweight: 64.07±3.95 mEq/l; EEPK dose of 200 mg/kg bodyweight: 74.55±1.87 mEq/l. Potassium level on EEPK dose of 100 mg/kg bodyweight: 30.56±0.39 mEq/l; at dose of 150 mg/kg bodyweight: 31.67 ± 1.06 mEq/l; on dose of 200 mg/kg bodyweight: 34.04±1.17 mEq/l.
Based on the above results, it can be concluded that EEPK doses of 100, 150 and 200 mg/kg bodyweight showed diuretic activity by increasing urine volume, sodium and potassium levels to white male rats.
Uji Aktivitas Diuretik Ekstrak Etanol Pecut Kuda
(Stachytharpheta Jamaicensis L. Vahl)
Pada Tikus
SKRIPSI
OLEH:
Melida Kristina Baringbing
NIM 121524194
PROGRAM STUDI EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI AKTIVITAS DIURETIK EKSTRAK ETANOL PECUT
KUDA (Stachytharpheta jamaicensis L. Vahl)
PADA TIKUS
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
MELIDA KRISTINA BARINGBING
NIM 121524194
PROGRAM STUDI EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI AKTIVITAS DIURETIK EKSTRAK ETANOL PECUT
KUDA (Stachytharpheta jamaicensis L. Vahl)
PADA TIKUS
OLEH:
MELIDA KRISTINA BARINGBING
NIM 121524194
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 18 Desember 2015
Disetujui oleh:
Pembimbing I, Panitia Penguji,
Prof. Dr. UripHarahap, Apt Prof. SumadioHadisahputra, Apt.
NIP 195301011983031004 NIP 1 11281983031002
Medan, Januari 2016 Fakultas Farmasi
Universitas Sumatera Utara Pejabat Dekan,
Dr. Masfria, M.S., Apt. NIP 195707231986012001
Pembimbing I,
Aminah Dalimunthe, S.Si., M.Si., Apt. NIP 197806032005012004
Panitia Penguji,
Prof. Dr. Urip Harahap, Apt. NIP 195301011983031004
Pembimbing II,
Marianne, S.Si., M.Si., Apt. NIP 198005202005012006
Dr. Poppy Anjelisa Z. Hasibuan, S.Si., M.Si., Apt. NIP 197506102005012003
Yuandani, S.Farm., M.Si., Ph.D., Apt. NIP 198303202009122004
iv
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat dan karunia kepada penulis sehingga dapat menyelesaikan skripsi ini yang berjudul “Uji Aktivitas Diuretik Ekstrak Etanol Pecut Kuda (Stachytharpheta jamaicensis L.Vahl) Pada Tikus”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
v
Penulis juga mengucapkan terima kasih dan penghargaan yang tak terhingga kepada Ayahanda Frencius Baringbing dan Ibunda Rosita Marpaung tercinta, serta kepada kakanda tercinta Fitra Devi Baringbing, S.Pd, abangda tercinta Rony, Marno, Melki dan adinda tercinta Nora Oktavia, yang tiada hentinya berkorban dengan tulus ikhlas bagi kesuksesan penulis, juga kepada teman-teman Farmasi Ekstensi 2012/2013 yang selalu setia memberi dukungan dan motivasi selama melakukan penelitian.
Penulis menyadari skripsi ini masih belum sempurna. Oleh karena itu, diharapkan saran dan kritik yang membangun untuk penyempurnaanya. Harapan penulis semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan kefarmasian.
Medan, Januari 2016 Penulis
Melida Kristina Baringbing