PEMBUATAN KOMPOSIT
POLIMER-KALSIUM FOSFAT KARBONAT :
KARAKTERISASI
X-RAY DIFFRACTION
(XRD) DAN
SCANNING ELECTRON MICROSCOPY
(SEM)
PRIYO PUJI WALUYO
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
PRIYO PUJI WALUYO (G74103031). Pembuatan Komposit Polimer-Kalsium Fosfat Karbonat: Karakterisasi X-Ray Diffraction (XRD) dan Scanning Electron Microscopy (SEM). Dibimbing oleh KIAGUS DAHLAN dan YESSIE WIDYA SARI
Dilakukan penelitian pembuatan biomaterial komposit polimer-kalsium fosfat karbonat. Polimer matriks terbuat dari reaksi kering sodium chloroacetate pada suhu 192°C yang menghasilkan polyglycolide yang berpori. Larutan kalsium fosfat karbonat ditumbuhkan pada matriks polyglycolide dengan cara tetes-tetes, yaitu meneteskan 1 ml larutan ion Ca2+, PO43- dan
CO32- dengan konsentrasi masing-masing 1 M secara bersamaan. Penetesan dilakukan sebanyak
10 kali dengan setiap tetesnya + 0,1 ml larutan ion. Selang waktu antara tiap tetesan + 3 – 4 detik. Hasil karakterisasi menunjukkan apatit karbonat tipe A, apatit karbonat tipe B, hidroksiapatit, dan NaCl hadir dalam komposit polimer-kalsium fosfat karbonat. Hasil mikrogaf SEM menunjukkan kristal hidroksiapatit dan apatit karbonat tumbuh disamping matriks polyglicolide dengan ukuran kristal mendekati tulang manusia.
PEMBUATAN KOMPOSIT
POLIMER-KALSIUM FOSFAT KARBONAT :
KARAKTERISASI
X-RAY DIFFRACTION
(XRD) DAN
SCANNING ELECTRON MICROSCOPY
(SEM)
PRIYO PUJI WALUYO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Fisika
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
RIWAYAT HIDUP
Judul :
Pembuatan Komposit Polimer - Kalsium Fosfat Karbonat :
Karakterisasi
X-Ray Diffraction
(XRD) dan
Scanning Electron
Microscopy
(SEM)
Nama : Priyo Puji Waluyo
NRP : G 74103031
Menyetujui,
Dr. Kiagus Dahlan
Pembimbing I
Yessie Widya Sari, M. Si
Pembimbing II
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Instutut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, M.S.
NIP. 131 473 999
PRAKATA
Alhamdulillahhirobbil’alamin, puji dan syukur penulis panjatkan kepada Allah SWT atas segala izin, rahmat, kekuatan dan karunia-Nya sehingga penulis dapat menyelesaikan Skripsi yang berjudul “Komposit Polimer-Kalsium Fosfat Karbonat : Karakterisasi X-ray Diffraction (XRD) dan Scanning Electron Microscopy (SEM)” sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains (S.Si) pada Departemen Fisika.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Bapak Dr. Kiagus Dahlan dan Ibu Yessi Widya Sari, M. Si. atas waktu yang telah diberikan untuk membimbing, dan memberikan masukan yang sangat berharga. Kepada Bapak Dr. Irzaman dan Ibu Mersi Kurniati,M. Si sebagai penguji yang banyak memberikan saran demi kebaikan penulis. Terima kasih juga diucapkan kepada kedua orang tua tercinta yang banyak berkorban demi keberhasilan penulis serta kakak (Arif dan Miftah), adikku dan seluruh family dimanapun berada. Rekan seperjuangan (Taofik, Mbak Arsi, Kak Jumali), teman-teman fisika 39, 40, 41 dan 42. Rekan-rekan di IPB yang senantiasa mendukung dan membantu penulis untuk menyelesaikan penulisan skripsi ini.
Penulis menyadari akan keterbatasan yang dimiliki, segala kritik dan saran sangat dibutuhkan untuk mencapai hasil yang lebih baik.
Bogor, Mei 2007
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... viii
DAFTAR TABEL ... viii
DAFTAR LAMPIRAN ... ix
PENDAHULUAN Latar Belakang ... 1
Tujuan Penelitian ... 1
Waktu dan Tempat Penelitian ... 1
TINJAUAN PUSTAKA Senyawa Kalsium Fosfat ... 1
Matriks Polimer Berpori ... 2
Pengaruh Ion CO32- dalam Kristal Apatit ... 2
Identifikasi Senyawa Kalsium Fosfat dengan X-ray Diffraction (XRD) ... 3
Identifikasi Senyawa Kalsium Fosfat dengan Scanning Electron Microscopy (SEM) ... 3
BAHAN DAN METODE Bahan dan Alat ... 4
Pembuatan Matriks Berpori ... 4
Komposit Polimer-Kalsium Fosfat Karbonat ... 4
HASIL DAN PEMBAHASAN Matriks Berpori ... 4
Komposit Polimer-Kalsium Fosfat Karbonat ... 6
SIMPULAN ... 11
DAFTAR PUSTAKA ... 11
DAFTAR GAMBAR
Halaman
1 Unit sel struktur hidroksiapatit ... 2
2 Subsel prisma segitiga rombik ... 2
3 Proses terjadinya difraksi oleh kisi kristal ... 3
4 Skema SEM ……….……….. 4
5 Spektra Differential Scanning Calorimetry (DSC) sodium chloroacetate ……….………..……… 5
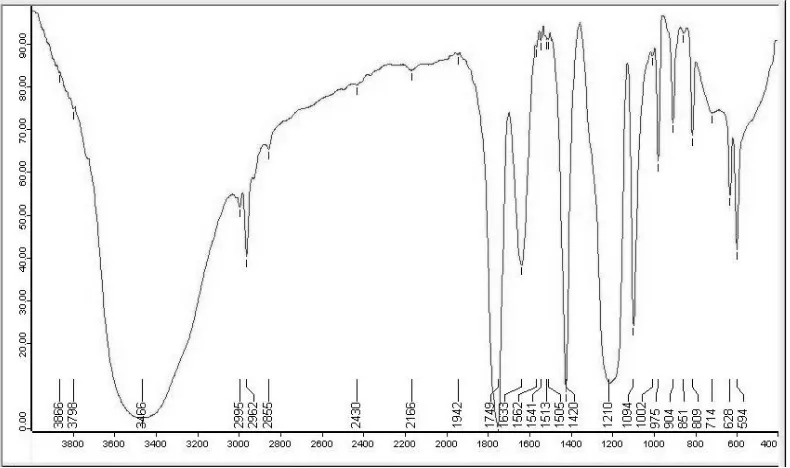
6 Spektra Fourier Transform Infrared (FTIR) reaksi kering sodium chloroacetate dengan onset suhu 192 0C ... 5
7 Pelet yang diperoleh secara mekanik dan standar IR. a). Tampak atas, b). Tampak samping ... 6
8 Profil XRD sampel kalsium fosfat karbonat yang ditumbuhkan pada matriks polyglycolide berpori dengan cara; a.presipitasi, b.celup-celup, c.tetes-tetes, d.celup-tetes ……….……… 7
9 MikrografSEM Sampel A ... 7
10 MikrografSEM Sampel B ... 7
11 MikrografSEM Sampel C ... 8
12 MikrografSEM Sampel D ... 8
13 Profil XRD sampel D1 dan D2 ... 9
14 Profil XRD sampel D3 dan D4 ... 10
15 MikrografSEM Sampel D1 ... 10
16 MikrografSEM Sampel D2 ... 10
17 MikrografSEM Sampel D3 ... 11
18 MikrografSEM Sampel D4 ... 11
DAFTAR TABEL
Halaman 1 Perbandingan spektra FTIR antara sodium chloroacetate dan polyglycolide .... 62 Nilai dl kristal apatit yang ditumbuhkan pada sampel A, B, C dan D ... 7
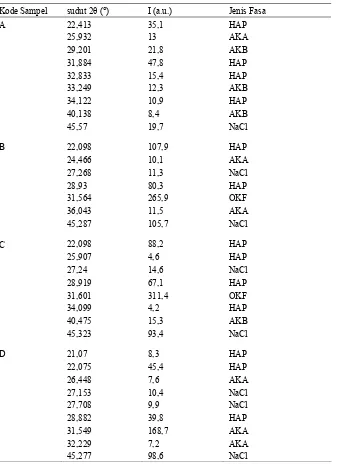
3 Nilai sudut difraksi (2θ) beberapa puncak pada profile XRD sampel A, B, C dan D ... 8
4 Variasi larutan ion kalium fosfat karbonat (D1 dan D2) ... 9
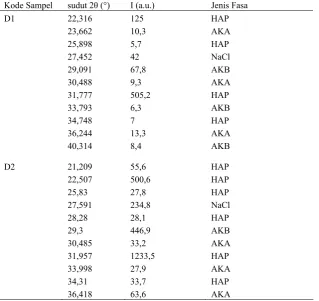
5 Nilai sudut difraksi (2θ) beberapa puncak pada profile XRD sampel D1 dan D2 ... 9
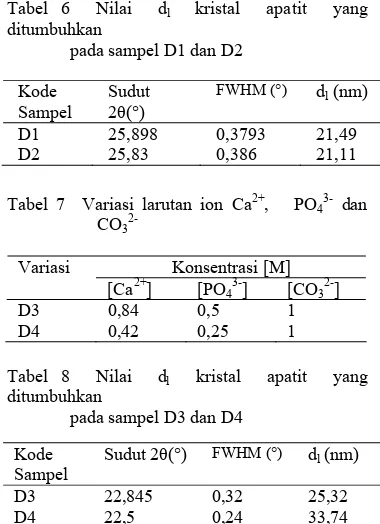
6 Nilai dl kristal apatit yang ditumbuhkan pada sampel D1 dan D2 ... 10
7 Variasi larutan ion kalium fosfat karbonat (D3 dan D4) ... 10
8 Nilai dl kristal apatit yang ditumbuhkan pada sampel D3 dan D4 ... 10
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian …..……….………..……….. 14
2 Data X-ray Diffraction (XRD) sampel A ………. 15
3 Data X-ray Diffraction (XRD) sampel B ………. 16
4 Data X-ray Diffraction (XRD) sampel C ... 17
5 Data X-ray Diffraction (XRD) sampel D ... 18
6 Data X-ray Diffraction (XRD) sampel D1 ………..………. 19
7 Data X-ray Diffraction (XRD) sampel D2 ……… 20
8 Data X-ray Diffraction (XRD) sampel D3 ……… 21
9 Data X-ray Diffraction (XRD) sampel D4 ……… 22
10 Sudut difraksi (2θ) beberapa puncak pada profil XRD kristal okta kalsium fosfat, hidroksiapatit, apatit karbonat tipe A dan tipe B[JCPDS] ... 23
11 Probabilitas kandungan kalsium fosfat dalam sampel (%) ... 24
12 Perhitungan ukuran kristal kalsium fosfat karbonat pada sampel ... 25
PENDAHULUAN
Latar Belakang
Biomaterial didefinisikan sebagai bahan inert yang diimplantasi ke dalam sistem hidup sebagai pengganti fungsi dari jaringan hidup atau organ[1]. Perkembangan teknologi biomaterial dalam implantasi salah satunya adalah plat tulang. Teknologi ini diperkenalkan pada awal 1990-an untuk menstabilkan keretakan pada tulang dan mempercepat penyembuhan.
Tubuh manusia tersusun oleh jaringan keras dan lunak. Tulang dan gigi termasuk jaringan keras yang merupakan organ biologi dinamik yang tersusun oleh sel aktif metabiologi yang terintegrasi ke dalam rangka yang kaku[2]. Pertumbuhan tulang memerlukan banyak senyawa mineral. Senyawa ini diperoleh dari makanan dan susu. Senyawa mineral yang berada di dalam tulang pada umumnya berbentuk senyawa kalsium. Kalsium pada tulang berikatan dengan gugus-gugus diantaranya fosfat, hidroksida, dan karbonat. Kalsium banyak berikatan dengan fosfat, oleh karenanya dikenal juga sebagai senyawa kalsium fosfat.
Senyawa kalsium fosfat pada tulang memberikan sifat keras, sehingga senyawa kalsium fosfat sangat penting di dalam tulang. Kalsium fosfat dalam jaringan keras akan semakin teratur susunan atomnya seiring dengan pertambahan umur. Tulang muda memiliki fase amorf, yang menunjukan bahwa tulang masih tumbuh, sedangkan pada usia mencapai tua, tulang memiliki lebih banyak senyawa kalsium fosfat dalam fase kristal.
Senyawa kalsium fosfat dalam tulang hadir dalam dua fase, yaitu fase amorf dan kristal. Pada fase kristal senyawa kalsum fosfat yang paling stabil adalah hidroksiapatit yang mempunyai formula Ca10(PO4)6(OH)2. Selain gugus fosfat,
hidroksida, dan karbonat di dalam tulang juga terdapat ion lain seperti Mg2+, F-, Na+, dan Cl-, dengan hadirnya ion tersebut akan mengganggu kestabilan hidroksiapatit.
Kerusakan pada tulang karena retak atau patah sering terjadi pada manusia. Material komposit kalsium fosfat dibutuhkan untuk memperbaiki atau mengganti tulang yang rusak. Pemilihan biomaterial yang tepat sangat diperlukan dalam proses implantasi. Tentunya biomaterial yang dipilih adalah yang mudah diperoleh, biokompatibel atau sesuai dengan jaringan keras dalam komposisi dan morfologi.
Tujuan Penelitian
1. Membuat matriks polimer berpori dari
sodium chloroacetate melaui proses reaksi kering.
2. Pembuatan komposit polimer kalsium fosfat karbonat.
3. Karakterisasi komposit menggunakan
X-Ray Diffraction (XRD) dan Scanning
Electron Microscope (SEM). Waktu dan Tempat Penelitian
Waktu penelitian dimulai dari bulan Mei 2006 sampai April 2007. Penelitian ini dilaksanakan di Laboratorium Biofisika, Departemen Fisika Kampus IPB Darmaga. Karakterisasi menggunakan X-Ray Diffraction
(XRD) di BATAN PUSPITEK Serpong dan
Scanning Electron Microscopy (SEM) di
Departemen Teknik Metalurgi Universitas Indonesia.
TINJAUAN PUSTAKA
Senyawa Kalsium Fosfat
Secara umum penyusun dasar komponen anorganik dalam tulang adalah kalsium fosfat. Kalsium fosfat hadir dalam dua bentuk yaitu fase amorf dan kristal. Hidroksiapatit merupakan fase kalsium fosfat yang paling stabil. Hidroksiapatit mempunyai struktur kristal heksagonal dengan parameter kisi a = b = 9,4160 Å dan c = 6,8830 Å[3]. Selain fase kristal, kalsium fosfat juga dapat hadir dalam fase amorf. Kalsium fosfat amorf (KFA) bersifat nonstokiometri. Fase ini terjadi akibat masuknya ion sederhana maupun ion kompleks ke dalam kisi kristal, akibatnya komposisi kristal menjadi sangat bervariasi.
Ion CO32- merupakan salah satu contoh ion
kompleks yang dapat menggantikan ion kisi dalam kristal. Selain ion karbonat, terdapat unsur-unsur lain yang dapat menggantikan ion kisi dari Ca2+, PO43- ataupun OH- dalam struktur
kristal stabil hidroksiapatit seperti ion Na+, H+, F+, Sr2+, dan Mg2+ yang cenderung menghasilkan kristal apatit dengan komposisi dan kristalinitas bervariasi[4].
Unit sel terdiri dari 2 subsel prisma segitiga rombik (Gambar 2). Atom Ca ditunjukkan oleh lingkaran hijau, atom O oleh lingkaran biru dan atom P ditunjukkan oleh lingkaran merah. Terdapat 2 kaca datar horizontal yaitu pada z = ¼ dan z = ¾ dan sebagai tambahan terdapat bidang tengah inversi tepatnya di setiap tengah muka vertikal dari setiap subsel. Unit sel kristal hidroksiapatit memiliki 2 jenis atom Ca yang disebut Ca1 dan Ca2. Perbedaannya terletak pada lokasi atom Ca.
Setiap subsel memiliki 3 pusat. Atom Ca1 puncak dan dasar masing-masing
dihitung sebagai ½ Ca1, sementara Ca1
tengah dihitung sebagai satu Ca1 sehingga
masing-masing subsel tersebut memiliki 2 atom Ca dari Ca1. Setiap unit sel memiliki 6
atom Ca2. Total atom Ca setiap unit sel
adalah 10 yang terdiri dari 4 atom Ca1 dan 6
atom Ca2. Atom-atom Ca2 membentuk 2
segitiga normal hingga sumbu c dan berotasi sebesar 600[6].
Gambar 1 Unit sel struktur hidroksiapatit [6].
Gambar 2 Subsel prisma segitiga rombik [6].
Matriks Polimer Berpori
Matriks polimer berpori didapatkan dari reaksi polimerisasi halogenoacetate melaui reaksi kering dan digunakan sebagai media tempat tumbuh apatit karbonat untuk membentuk biomaterial komposit polimer-kalsium fosfat karbonat yang bisa langsung diimplankan ke dalam tulang. Matriks polimer berpori harus dapat diterima oleh tubuh dan tidak beracun. Polimer tersebut juga harus mudah terdegradasi karena keberadaannya dalam tubuh tidak diperlukan selamanya sepanjang manusia itu hidup. Setelah hidroksiapatit bersatu di dalam tulang dan membentuk tulang yang sehat, maka polimer akan terdegradasi.
Terdapat berbagai jenis halogenoacetate di alam yang dapat menghasilkan polyglycolide
dengan pori yang bervariasi. Pemilihan prekursor dan perlakuan mekanik yang tepat akan menghasilkan ukuran pori rata-rata yang terdistribusi dengan diameter 0,3 sampai 1 m[7]. Polyglycolide merupakan poliester sederhana yang bisa didapatkan dengan mengeliminasi logam halida dari
halogenoacetate pada suhu tertentu. Reaksi
eliminasi halida halogenoacetate dinyatakan sebagai
M+ -OOC-CH2-X
MX + 1/n [-OOC-CH2-]n (1)
Sodium chloroacetate merupakan salah satu jenis halogenoacetate. Sodium chloroacetate
mengalami reaksi polemerisasi pada suhu 1980C. Hasil penelitian menunjukan pada suhu di atas 1500C struktur pori pada polyglycolide
mencapai sempurna[7]. Diantara beberapa polimer yang ada, polyglycolide (PGA) merupakan polimer yang lebih biokompatibel dan paling mudah terdegredasi di dalam tubuh dengan air, reaksi enzim, dan proses metabolisme tubuh[8].
Pengaruh Ion CO32- dalam Kristal Apatit Fraksi mineral dalam jaringan keras selalu mengandung persentase karbonat berbentuk ion CO32- atau HCO3- walaupun dalam jumlah
yang sedikit[3]. Ion CO32- dapat menggantikan
ion fosfat (PO43-) atau ion hidroksil (OH-).
Jika yang digantikan adalah ion OH-,
maka akan terbentuk kristal apatit karbonat tipe A, sedangkan jika yang
digantikan adalah ion PO43-, maka akan
terbentuk kristal apatit karbonat tipe B. Apatit
suhu rendah didominasi oleh apatit karbonat tipe B sedangkan apatit yang diproduksi dari reaksi padat dan suhu tinggi didominasi apatit karbonat tipe A[4]. Pada prinsipnya dominasi apatit biologis didalam tubuh merupakan karbonat tipe B dan sejumlah kecil tipe A [9].
Kehadiran ion karbonat dalam kristal apatit karbonat tipe B akan memperpendek parameter kisi a. Kontraksi parameter kisi a pada kristal apatit karbonat tipe B terjadi karena ion karbonat berbentuk planar menggantikan ion fosfat yang berbentuk tetrahedral dan relatif lebih besar[10]. Kehadiran karbonat pada sintetik apatit akan menyebabkan menurunnya proses kristalisasi terhadap meningkatnya konsentrasi karbonat[11].
Pembuatan senyawa kalsium fosfat dengan temperatur diantara 60–100 oC menunjukkan ion karbonat mengisi kisi kristal apatit dengan menggantikan ion fosfat. Penggantian ion hidroksil dengan ion karbonat dari sintesis apatit harus dilakukan pada kondisi sangat kering yaitu 1000 oC [3].
X-ray Diffraction (XRD)
X-ray Diffraction (XRD) digunakan
untuk mengetahui nilai parameter kisi, struktur kristal, dan derajat kekristalan. Derajat kekristalan adalah besaran yang menyatakan banyaknya kandungan kristal dalam suatu materi dengan membandingkan luasan kurva puncak dengan total luasan amorf dan kristal[12].
Sinar-X ditembakkan pada bahan sehingga terjadi interaksi dengan elektron dalam atom. Ketika foton sinar-X bertumbukan dengan elektron, beberapa foton hasil tumbukan akan mengalami pembelokan dari arah awal datang.
Gambar 3 Proses terjadinya difraksi oleh kisi kristal[13].
Jika panjang gelombang hamburan sinar-X tidak berubah (foton sinar-X tidak kehilangan banyak energi) dinamakan hamburan elastik dan terjadi transfer momentum dalam proses hamburan. Sinar-X ini yang membawa informasi distribusi atom dalam material. Gelombang yang terdifraksikan dari atom-atom berbeda dapat saling mengganggu dan distribusi intensitas resultannya termodulasi kuat oleh interaksi ini. Syarat terjadinya difraksi harus memenuhi hukum Bragg yaitu :
2d sin θ = n (2) Jika atom-atom tersusun periodik dalam kristal, gelombang terdifraksi akan terdiri dari interferensi maksimun tajam (peak).
Scanning Electron Microscopy (SEM)
Scanning Electron Microscope (SEM)
Gambar 4 Skema SEM[14].
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan CaCl2.2H2O(s)
pro analisis, NaHPO4.2H2O(s) pro analisis,
NaHCO3(s) pro analisis, NH4OH(l),aquades,
sodium chloroacetate dan N2.
Peralatan yang digunakan adalah buret,
beaker glass, statip, pengaduk, crucible
(cawan keramik), alumunium foil, pipet
mohr, hotplate, neraca analitik, pH meter digital, furnace, termometer digital, bulb, sampel holder kaca.
Metode Penelitian
Pembuatan Matriks Berpori
Matriks berpori dibuat dari sodium chloroacetate dalam bentuk pelet. Dilakukan karakterisasi menggunakan Differential
Scanning Calorimetry (DSC) pada
sodium chloroacetate sebelum dibuat
pelet untuk mengetahui pada suhu berapa terjadi reaksi polimerisasi.
Pemanasan sodium chloroacetate sesuai hasil Differential Scanning Calorimetry
(DSC) dilakukan supaya terbentuk
polyglycolide dan kemudian dibuat pelet
dengan standar Infra Red (IR). Dilakukan pencucian menggunakan aquades sebanyak 3x untuk menghilangkan NaCl. Reaksi ini akan menghasilkan matrik polyglycolide yang berpori[7].
Komposit Polimer-Kalsium Fosfat Karbonat
Penumbuhan senyawa kalsium fosfat karbonat pada matriks berpori dilakukan dengan empat cara, yaitu presipitasi, celup-celup, celup-tetes dan tetes-tetes. Presipitasi (Sampel A) dilakukan dengan mencampurkan
polyglycolide berpori ke dalam larutan ion PO4
3-dan CO32- dan meneteskan ion Ca2+ dengan
buret. Celup-celup (Sampel B) dilakukan dengan mencelupkan polyglycolide berpori ke dalam 1 ml larutan ion PO43- dan CO3
2-kemudian dilanjutkan dengan pencelupan ke dalam 1 ml larutan ion Ca2+. Celup-tetes (Sampel C) dilakukan dengan mencelupkan sample kedalam 1 ml larutan ion PO43- dan
CO32- tetapi ion Ca2+ sebanyak 1 ml diberikan
dengan cara diteteskan. Tetes-tetes (Sampel D) dilakukan dengan menetesi
polyglycolide berpori dengan larutan ion PO4
3-dan CO32- serta larutan ion Ca2+ secara
bersamaan. Penetesan 1 ml larutan ion PO43,
CO32- serta Ca2+ diteteskan dalam 10 kali
penetesan sehingga tiap kali penetesan matriks + 0,1 ml larutan ion. Selang waktu antara tiap tetesan + 3 -4 detik. Hasil komposit biomaterial tersebut dipanaskan di dalam furnace dengan suhu 1100C selama 10 jam selanjutnya dikarakterisasi menggunakan Difraksi Sinar-X
(XRD) dan Scanning Electron Microscopy
(SEM).
HASIL DAN PEMBAHASAN
Matriks Berpori
Pembuatan matriks berpori harus dapat diterima oleh tubuh dan tidak beracun. Polimer tersebut harus mudah terdegradasi karena keberadaannya dalam tubuh tidak diperlukan selamanya. Matriks berpori dibuat dari polyglygolide. Polyglycolide merupakan polimer yang lebih biokompatibel dan paling mudah terdegredasi di dalam tubuh dengan air, reaksi enzim, dan proses metabolisme tubuh[8].
Polyglycolide dapat dihasilkan dari berbagai jenis halogenoacetate di alam.
Matriks berpori dibuat dari reaksi kering
sodium chloroacetate. Reaksi eliminasi halida
Gam
Na+ -OOC-CH2 - Cl
bar 5 Spektra Differential Scanning Calorimetry (DSC) sodium chloroacetate.
Gambar 6 Spektra Fourier Transform Infrared (FTIR) reaksi kering sodium chloroacetate dengan onset suhu 192 0C.
NaCl + 1/n [-OOC-CH2-]n (3)
Garam (NaCl) dilarutkan dalam air sehingga meninggalkan pori dengan ukuran
submicron[7].
Residual sodium chloroacetate
menghasilkan puncak polimerisasi eksotermik pada suhu 190 0C, sedangkan puncak leleh endotermik dari residual
chloroacetate acid terjadi pada suhu
600C[7]. Hasil Differential Scanning
Calorimetry ( DSC ) sodium
chloroacetate (gambar 5) menunjukkan bahwa reaksi polimerisasi terjadi pada suhu 191,50 0C.
Hasil reaksi kering sodium chloroacetate pada suhu 192 0C dikarakterisasi menggunakan
Hasil reaksi kering sodiumchloroacetate dibuat menjadi pelet. Pembuatan pelet dilakukan dengan dua metode, yaitu secara mekanik dan standar pembuat pelet
Infra Red (IR). Hasil yang diperoleh
menunjukkan bahwa pelet yang dibuat dengan standar pembuat pelet Infra Red (IR) lebih baik dibandingkan secara mekanik (gambar 7). Pelet yang dibuat secara mekanik bersifat sangat rapuh dan mudah larut. Matriks berpori yang digunakan diperoleh dengan metode standar pembuat pelet Infra Red (IR).
hidroksiapatit, AKA, dan AKB terhadap data
Joint Committee on Powder Diffraction
Standards (JCPDS). Kristal HAP, AKA, dan
AKB hadir dalam keempat jenis sampel. Okta kalsium fosfat hadir pada sampel B dan C yang menunjukkan kristal hidroksiapatit yang belum stabil. Sampel A, polyglycolide berpori larut dalam larutan ion Ca
Komposit Polimer-Kalsium Fosfat Karbonat
Penumbuhan senyawa kalsium fosfat karbonat pada matriks berpori dilakukan dengan empat cara, yaitu presipitasi (Sampel A), celup-celup (Sampel B), celup-tetes (Sampel C), tetes-tetes (Sampel D). Konsentrasi larutan ion Ca2+, PO43- dan CO32- masing -masing sebanyak
1 M. Hasil dari keempat sampel tersebut dikarakterisasi menggunakan X-ray Diffraction (XRD) dan Scanning Electron Microscope (SEM).
Keempat profil XRD masing-masing sampel (gambar 8) dipilih beberapa puncak yang memiliki sudut difraksi mendekati nilai karakter hidroksiapatit (HAP), apatit karbonat tipe A (AKA) dan apatit karbonat tipe B (AKB) (tabel 3). Probabilitas terbesar didapatkan berdasarkan ketepatan yang paling tinggi dari nilai karakter
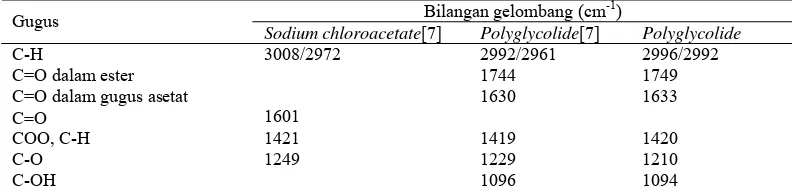
Tabel 1 Perbandingan spektra FTIR antara sodium chloroacetate dan polyglycolide
Bilangan gelombang (cm-1) Gugus
Sodium chloroacetate[7] Polyglycolide[7] Polyglycolide
C-H 3008/2972 2992/2961 2996/2992
C=O dalam ester 1744 1749
C=O dalam gugus asetat 1630 1633
C=O 1601
COO, C-H 1421 1419 1420
C-O 1249 1229 1210
C-OH 1096 1094
Mekanik
2+
, PO43- dan
CO32- sehingga senyawa kalsium fosfat
karbonat tidak bisa ditumbuhkan pada
polyglycolide berpori. Hasil mikrograf SEM
(gambar 9) menunjukkan polyglycolide berpori dengan struktur mikro sudah tidak tampak lagi.
Polyglycolide sampel B, C dan D tidak larut dalam larutan ion Ca2+, PO43- dan CO32-.
Hasil (XRD) pada sudut difraksi 2θ = 22,0980 , sampel B memiliki intensitas tertinggi yang menunjukkan hidroksiapatit pada sampel B lebih tinggi dari sampel C dan D, tetapi hasil mikrograf (SEM) sampel B (gambar 10) menunjukkan senyawa kalsium fosfat karbonat hanya di permukaan. Intensitas tertinggi terjadi pada sudut difraksi (2θ) sekitar 31,549° – 31,884°, yang mendekati nilai sudut difraksi puncak maksimum AKA (31,529°), sehingga kemungkinan dalam semua sampel kandungan AKA relatif lebih tinggi dibanding dengan kandungan AKB. Kenaikan kandungan karbonat sudut difraksi untuk refleksi 002 meningkat dan untuk refleksi 300 menurun [15].
Standar IR
a b
Tabel 2 menunjukkan ukuran kristal pada bidang 002 (dl) sebagai hasil kalkulasi
mengikuti persamaan berikut
cosθ β
K D
⋅ ⋅
= (4)
K = 0,9 , λ =1,54Å untuk sinar X karakteristik CuKα, dan β = (FWHM) dalam satuan radian[16].
(a)
(b)
Gambar 9 Mikrograf SEM sampel A.
Tabel 2 Nilai dl kristal apatit yang ditumbuhkan
pada sampel A, B, C, D
Kode Sampel
Sudut 2θ (°)
(c)
(d)
Gambar 10 Mikrograf SEM sampel B. FWHM (°) dl (nm)
A 25,932 0,596 13,7
B - - -
C 25,907 0,705 11,7
D 26,448 0,379 21,5
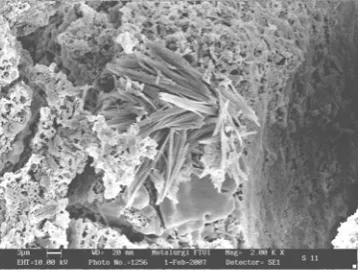
Gambar 11 Mikrograf SEM sampel C. Gambar 12 Mikrograf SEM sampel D.
Kode Sampel sudut 2θ (°) I (a.u.) Jenis Fasa
A 22,413 35,1 HAP
25,932 13 AKA
21,8 AKB 47,8 HAP 15,4 HAP 12,3 AKB 10,9 HAP 8,4 AKB 19,7 NaCl
22,098 107,9 HAP 10,1 AKA 11,3 NaCl 80,3 HAP
265,9 OKF
11,5 AKA
105,7 NaCl
22,098 88,2 HAP
4,6 HAP 14,6 NaCl 67,1 HAP
311,4 OKF
4,2 HAP 15,3 AKB 93,4 NaCl
8,3 HAP 45,4 HAP 7,6 AKA 10,4 NaCl 9,9 NaCl 39,8 HAP
31,549 168,7 AKA
32,229 7,2 AKA
45,277 98,6 NaCl
29,201 31,884 32,833 33,249 34,122 40,138 45,57 B 24,466 27,268 28,93 31,564 36,043 45,287 C 25,907 27,24 28,919 31,601 34,099 40,475 45,323 D 21,07 22,075 26,448 27,153 27,708 28,882
Hasil mikrograf SEM sampel C dan D (gambar 11 dan 12) menunjukkan bahwa kristal hidroksiapatit maupun apatit karbonat tumbuh disamping matriks polyglycolide
namun sampel D memiliki ukuran kristal relatif lebih besar dan mendekati ukuran kristal tulang manusia (tabel 3) sehingga sampel D menjadi pilihan untuk penumbuhan senyawa kalsium fosfat karbonat. Sampel B tidak memiliki sudut difraksi yang mendekati bidang 002 hidroksiapatit.
Kehadiran karbonat pada sintetik apatit akan menyebabkan menurunnya proses kristalisasi terhadap meningkatnya konsentrasi karbonat[11]. Dilakukan variasi konsentrasi ion CO32- (tabel 4). Dilakukan
pemilihan beberapa puncak yang memiliki sudut difraksi mendekati nilai karakter hidroksiapatit, apatit karbonat tipe A dan tipe B (tabel 5). Kristal HAP, AKA, dan AKB hadir dalam keempat jenis sampel. Tabel 4 Variasi larutan ion Ca2+, PO43- dan
CO3
2-Konsentrasi [M] Kode
sampel [Ca2+] [PO43-] [CO32-]
D1 0,5 0,5 1
D2 0,25 0,25 1
(D1)
(D2)
Gambar 13 Profil XRD sampel D1 dan D2.
Tabel 5 Nilai sudut difraksi (2θ) beberapa puncak pada profile XRD sampel D1 dan D2
Kode Sampel sudut 2θ (°) I (a.u.) Jenis Fasa
D1 22,316 125 HAP
23,662 10,3 AKA
25,898 5,7 HAP
27,452 42 NaCl
29,091 67,8 AKB
30,488 9,3 AKA
31,777 505,2 HAP
33,793 6,3 AKB
34,748 7 HAP
36,244 13,3 AKA
40,314 8,4 AKB
D2 21,209 55,6 HAP
22,507 500,6 HAP
25,83 27,8 HAP
27,591 234,8 NaCl
28,28 28,1 HAP
29,3 446,9 AKB
30,485 33,2 AKA
31,957 1233,5 HAP
33,998 27,9 AKA
34,31 33,7 HAP
Tabel 6 Nilai dl kristal apatit yang
ditumbuhkan
pada sampel D1 dan D2
Tabel 7 Variasi larutan ion Ca2+, PO43- dan
CO3
2-Konsentrasi [M] Variasi
[Ca2+] [PO43-] [CO32-]
D3 0,84 0,5 1
D4 0,42 0,25 1
Tabel 8 Nilai dl kristal apatit yang
ditumbuhkan
pada sampel D3 dan D4
Sampel D1 memiliki ukuran kristal lebih besar dari pada sampel D2 (tabel 6). Ion CO32- berperan sebagai inhibitor dalam
pembentukan kristal apatit sehingga probabilitas penggantian PO43- oleh CO3
2-pada sampel D2 lebih besar dari sampel D1. Ion karbonat berbentuk planar menggantikan ion fosfat yang berbentuk tetrahedral dan relatif lebih besar[10]. Konsentrasi CO32- yang terlalu besar akan
menyebabkan kristalinitas kristal apatit menurun. Hasil mikrograf SEM sampel D1 dan D2 (gambar 15 dan 16) menunjukkan bahwa kristal apatit tumbuh berdampingan bersama pori. Dilakukan variasi konsentrasi CO32- berdasarkan perbandingan Ca/P =
1,67 yang merupakan karakter dari kristal hidroksiapatit (tabel 7).
Dilakukan pemilihan beberapa puncak dari profil XRD sampel D3 dan D4 yang memiliki sudut difraksi mendekati nilai karakter hidroksiapatit, apatit tipe A dan tipe B (tabel 9). Kristal HAP, AKA, dan AKB hadir dalam sampel D3 dan D4. Dilakukan pengukuran ukuran kristal pada bidang 111 (tabel 8). Sampel D3 dan D4 memiliki ukuran kristal lebih besar dari sampel D1 dan D2. Perbedaan ukuran kristal bisa disebabkan karena pengukuran pada bidang yang berbeda. Hasil mikrograf SEM sampel D3 dan D4 (gambar 17 dan 18) menunjukkan kristal apatit yang tumbuh berdampingan bersama pori.
Kode Sampel
Sudut 2θ(°)
(D3)
(D4)
Gambar 14 Profil XRD sampel D3 dan D4.
Gambar 15 Mikrograf SEM sampel D1.
Gambar 16 Mikrograf SEM sampel D2. FWHM (°) dl (nm)
D1 25,898 0,3793 21,49
D2 25,83 0,386 21,11
Kode Sampel
Sudut 2θ(°) FWHM (°) dl (nm)
D3 22,845 0,32 25,32
af SEM sampel D3.
SIMPULAN
Pemanasan sodium chloroacetate pada suh
besar, namun tidak dapat mengetahui proses Gambar 17 Mikrogr
u 1920C menghasilkan polyglycolide.
Pencucian hasil reaksi kering sodium chloroacetate pada suhu 1920C yang telah dibuat pelet dengan standar IR menghasilkan
porous polyglycolide. Senyawa kalsium
fosfat karbonat ditumbuhkan dengan metode tetes-tetes dengan ukuran kristal pada bidang 002 sebesar 21,11 nm sampai 21,50 nm. Meningkatnya konsentrasi karbonat menyebabkan probabilitas penggantian ion fosfat oleh karbonat lebih
Gambar 18 Mikrograf SEM sampel D4.
enggantian karbonat terhadap fosfat. Terdapat andungan AKA, AKB, HAP dan NaCl pada
DAFTAR PUSTAKA
1. Bh aterials.
Pangboune Engl nd : Alpha Science 2.
Healing. Neurosurg. .
cture of the
p k
komposit polimer-kalsium fosfat karbonat.
at, Sujata V. 2002. Biom
a International Ltd.
Kalfas, Ian H., M. D., F. A. C. S. 2001.
Principles of Bone
Focus. Vol 10. April.
Elliott, J. C. 1973. The Problem of Composition on Stru
3 Tabel 9 Nilai sudut difraksi (2θ) beberapa puncak pada
sudut 2θ (°) I (a.u.) Jenis Fasa
profile XRD sampel D3 dan D4
Kode Sampel
D3 22,845 211,6 HAP
25,26 16,1 HAP
27,977 90,4 NaCl
29,621 243,9 AKB
32,336 1417,2 AKA
34,745 26,6 HAP
36,741 46,7 AKA
46,005 1320,6 HAP
D4 21,361 75,1 HAP
22,5 649,2 HAP
27,542 105 NaCl
28,159 76,8 HAP
29,175 534,5 AKB
31,828 1336 HAP
32,872 27,1 AKA
34,141 42,7 HAP
36,357 80,5 AKA
45,614 1014,4 NaCl
Material Components of the Hard Tissue, Clin Orthop Rel Res 93:313-345.
Bigi, A.,E. Foresti, R. Gregorini, A. Ripam
4.
onti, n. Noveri, anf J. S. Shah.
5.
ch K750X &
6. atite. 7 with Controlled 8. 6. 9.
Structures of Biological
se
10.
roskopi Inframerah dan
11.
12.
Kalsium Fosfat Hasil
13.
Jakarta : Erlangga. 1992. The Role of Magnesium on the Structure of Biological Apatite, Calc. Tiss. Int. 50:439 – 444.
Emitech. 2005. Technical Brief of Freeze drying for Emite
K775X. England. Emitech Corp. Hanson, Bob. 2005. 150000000:1 Model of Hydroxyap www.stolaf.edu/people/hansonr (23 Agustus 2006).
Eapple, M,. and O. Herzberg.
Polyglycolide
Porosity: and Improved Biomaterial. J. Master. Chem. 7(6), 1037-1042. Rezwan K., Q.Z. Chen., J.J. Blaker., Aldo Roberto Boccaccini. 200
Biodegradable and Bioactive porous Polymer/Inorganic Composite Scaffolds for Bone tissue Engineering. Biomterials 27. 3413-3431.
Mathew Mathai, Shozo Takagi. 2001.
Minerals in DentalResearch. Journal of Re arch of The National of Standard and Technology. 106 : 1035-1044.
Notonegoro, H. A. 2003. Analisis Hasil Spekt
difraksi Sinar X Pertumbuhan Kristal
Apatit Pada Mucoza Ampela Ayam,
Sekripsi S1 Jurusan Fisika FMIPA UI (Pembimbing D. S. Soejoko), Depok. Saptari, S. A. 1999. Karbonat Sebagai Inhibitor dalam Pembentukan Hidroksiapatite Hasil Presipitasi, Skripsi S1 Jurusan Fisika UI (Pembimbing D. S. Soejoko), Depok.
Riyani, E. 2004. Karakterisasi Senyawa
Presipitasi Menggunakan XRD (X-ray Diffraction) dan SEM (Scanning Elektron Microscope). Skripsi S1 Departemen Fisika FMIPA IPB ( Pembimbing A. Maddu, dan D. S. Soejoko), Bogor.
Vlack, Van. 1995. Ilmu dan Teknologi Bahan.
14. __. 2002. Scanning Electron Microscope. Oxford Univ.
http://www.unl.edu/CMRAcfem/sem optic. [23 Agustus 2006]
LeGeros RZ, Trautz OR, LeGeros JP, Klein E, Apatite Cry
15.
stallites: Effects of
16.
, Energy Dispersive
carbonate on morphology. Science 155, 1967, 1409-1411
Widya, Sari Y. 2005. A Scanning Electron Microscopy
Lampiran 1 Diagram alir penelitian
Penyediaan Alat dan Bahan
Siap ?
Karakter asi DSC is
Pengambilan Data dan Analisis
Penyusunan Laporan Karakterisasi SEM dan XRD
Tidak
Karakterisasi FTIR
Pembuatan Matrix
Variasi Konsentrasi Kalsium Fosfat Karbonat Metode Tetes-Tetes D1. 0,5-0,5-1
D2. 0,25-0,25-1 D3. 0,84-0,5-1 D4. 0,42-0,25-1 Penumbuhan Senyawa Kalsium Fosfat Karbonat
ampiran 2 Data X-ray Diffraction (XRD) sampel A L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°)
20,905 4,24601 5,9 73,2 0,65
22,413 23,059
3,96359 3,85388
35,1 383,4 0,596
7,6 28,1 0,217
0,542 24,779 3,59025 5,8 52,8
25,932 3,4331 13 141,6 0,596
28,129 3,16976 8,2 58,9 0,434
29,201 3,0558 21,8 262 0,651
30,824 2,89847 9,3 72,3 0,434
31,884 2,80448 2,72559
47,8 539,3 0,651
32,833 15,4
12,3
84,5 0,271
33,249 2,69243 67,1 0,325
34,122 2,62553 10,9 120 0,596
35,959 2,49546 4,9 44 0,488
38,427 2,34073 5,3 37,3 0,379
39,113 2,3012 6,2 39,7 74,3
0,379
40,138 2,24476 8,4 0,488
42,159 2,14174 2,11611
6,4 53,8 0,487
42,694 5,2 36,4 0,379
45,57 1,98905 19,7 190 0,542
46,308 1,95902 7 74,6 0,704
48,519 49,602
1,87482 5,1 48,9 0,542
1,83637 6,8 6,6
36,4 0,434
50,151 1,81755 42,7 0,38
51,37 1,77724 6,1 48 0,487
53,07 1,72424 5,7 45,6 0,542
0,596 56,596 1,62489 8,1 79,6
41,7
60,09 1,53851 4,6 0,488
61,725 1,50162 5,8 46,5 0,487
63,978 69,253
1,45406 6,6 44,9 0,434
1,35563 6,4 47,9 0,433
74,65 1,27042 5,5 37,6 0,379
75,579 1,25709 6,8 40,7 0,433
ampiran 3 Data X-ray Diffraction (XRD) sampel B L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°) 22,098 4,01927 107,9 2152,6 1,084 24,466
7
,3
3,6354 10,1 134 0,975
27,268 3,26791 11,3 108,9 0,651
28,93 3,08382 80,3 1604 1,084
31,564 2,83257 265,9 3189,2 1,138
33,953 2,63818 6 150 1,517
36,043 2,48985 11,5 190 1,246
38,867 2,31523 5,1 158,3 1,571
42,216 2,13895 9,5 251,8 1,788
45,287 2,00079 105, 2128,2 1,138
51,697 1,76676 6,7 124,3 1,246
54,333 1,68711 6,5 62,5 0,975
56,348 1,63146 24,3 435,4 1,137
62,457 1,48576 5 92,7 1,029
66,116 1,41213 17,3 320,1 1,084
ampiran 4 Data X-ray Diffraction (XRD) sampel C L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°) 22,098 4,01942 88,2 1637,2 1,03 24,506
25,907
3,62951 3,43639
8,8 149,2 0,921
4,6 57 0,705
0,704 27,24 3,2712 14,6
9,6
6 83 28,919 3,085 67,1
311,4
118 0,975
31,601 34,099
2,82899 3427,5
74,2
1,029 2,62723
2,50014
4,2 0,975
35,89 7 150,1 1,192
40,475 2,22687 15,3 75,2 1,083
42,31 2,13442 10,9 93,4
216 1,137
45,323 1,99929 1664, 0,975
47,48 1,91336 7,1 135,3 78,2
1,029
52,373 1,74555 7,1 0,976
53,801 56,326
1,70255 6,1 68,3 0,921
1,63207 25,4 476,4 1,029
60,158 1,53693 3,8 53,1 0,813
66,085 1,41271 16,1 252,3 0,976
69,691 1,34816 4,9 55,5 0,813
75,147 1,26324 27,8 415,7 0,975
ampiran 5 Data X-ray Diffraction (XRD) sampel D L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°)
21,07 4,21303 8,3 57,8 0,379
22,075 3
7 8
4,0235 45,4 453 0,542
26,448 3,36732 7,6 49,2 0,379
27,153 3,28143 10,4 72,7 0,379
27,708 3,21702 9,9 69,2 0,379
28,882 3,08884 39,8 397,8 0,541
31,549 2,83355 168, 1516, 0,488
32,229 2,77525 7,2 55,1 0,433
36,289 2,47354 6 113,6 1,03
42,337 2,13311 8,2 65,8 0,434
42,955 2,10387 8,1 71 0,488
45,277 2,00123 98,6 871,5 0,488
46,035 1,97001 7,1 41,5 0,325
56,339 1,63172 27,6 248,1 0,488
66,068 1,41304 16,6 160,8 0,542
ampiran 6 Data X-ray Diffraction (XRD) sampel D1 L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°) 22,316 3,98052 125 2054,5 0,4408 23,662
7
7
,1
8
3,7571 10,3 2254,5 0,2523
24,739 3,59597 9,4 240,4 0,6502
25,898 3,43761 5,7 84,4 0,3793
27,452 3,24644 42 473,9 0,3195
29,091 3,06711 67,8 1493, 0,5875
30,488 2,92967 9,3 81,2 0,2709
31,777 2,81375 505,2 4305,1 0,2548
33,159 2,69949 6,1 3662, 1,8694
33,793 2,65033 6,3 439,2 0,6231
34,748 2,57963 7 58,7 0,2438
36,244 2,4765 13,3 360,9 0,7315
37,635 2,3881 8 260,4 0,9998
38,941 2,31096 8,7 498,4 1,3275
39,429 2,28347 12 388,5 0,9482
40,314 2,23541 8,4 84,5 0,2709
41,226 2,18801 9,2 617,1 0,6773
42,618 2,11973 10,2 909,1 2,2757
43,667 2,07121 9,1 651,5 0,5148
44,65 2,02783 8,7 4696 1,0566
45,574 1,98885 259, 2711,2 0,2986
47,49 1,91301 7,2 141,1 0,5418
49,942 1,82466 5,8 56,5 0,2365
51,183 1,78329 6,7 265,3 1,1379
52,382 1,74527 7,5 250,3 0,894
53,246 1,71895 6,3 91,5 0,3522
54,03 1,69587 17,5 215,2 0,3127
55,111 1,66514 6,3 524,8 0,2438
56,556 1,62597 136,4 1601,7 0,3066
58,131 1,5856 5,3 92,2 0,4877
66,401 1,40677 20 286,9 0,3983
67,288 1,39036 6,1 89 0,3741
69,83 1,34583 5,5 48,7 0,2167
72,547 1,30197 5,4 61,7 0,2818
73,226 1,29156 9,5 141,8 0,3793
ampiran 7 Data X-ray Diffraction (XRD) sampel D2 L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°) 21,209 4,18569 55,6 3653,7 0,7823
22,507 7
7
5 3
6
7
3,9471 500,6 9670 0,386
25,83 3,44643 27,8 2460,1 0,386 27,591 3,23036 234,8 2470 0,2222 28,28 3,15317 28,1 9369,8 0,2222
29,3 3,04565 446,9 11580 0,504
30,485 2,92998 33,2 4654,6 0,504 31,95 2,79824 1233,5 15564,1 0,2679 33,998 2,63483 27,9 2552,3 1,46 34,31 2,61155 33,7 2793,4 1,46 36,418 2,46505 63,6 3689,7 1,191 38,36 2,34463 81,7 1443,1 0,367 39,718 2,26756 67,6 3430,1 1,0417 42,659 2,11777 78 7731,9 1,0417 42,981 2,10265 89,1 7661,8 1,5633 43,311 2,08737 79,3 6345,1 1,0745 44,573 2,03119 445,7 6360,3 0,2837 45,665 1,9851 1820, 25019,4 0,2864 47,867 1,89881 53,1 2700,5 1,0288 52,373 1,74554 44,2 4337,9 1,0288 52,873 1,73021 48,2 3649,4 1,1 54,122 1,69319 68,3 3625 0,4501 54,801 1,67382 51,8 4466,3 1,19 56,656 1,62334 364 9373,8 0,5268 60,564 1,52758 27,6 956,2 0,6696 64,961 1,43442 113,6 2264,5 0,4001 66,401 1,40676 93,2 2900,9 0,6107 73,299 1,29046 32,4 848,3 0,5255 75,637 1,25627 448,9 11328,1 0,4937
ampiran 8 Data X-ray Diffraction (XRD) sampel D3 L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°) 22,845 3,89571 211,6 4314,3 0,32 25,26 3,52284
7
2
1 6
16,1 453,2 0,5379
27,977 3,18662 90,4 1320,3 0,301 29,621 3,01345 243,9 6247,1 0,504 32,336 2,76636 1417, 17483 0,2605 34,745 2,57983 26,6 1015,7 0,8652 36,741 2,44413 46,7 1783 0,7714 38,346 2,34547 74,3 940,6 0,2611 39,905 2,25734 44,3 2631,5 1,32 43,189 2,09299 73,5 9702,5 1,9375 44,569 2,03135 384,5 5340,6 0,286 46,005 1,97122 1320, 23628,3 0,3553 48,139 1,88872 41,3 1468,9 0,7195 52,558 1,73983 41,9 3598,1 1,62 54,383 1,68568 59,8 1624,8 0,5753 57,002 1,61429 440,6 6946,6 0,325 58,268 1,5822 15,5 584,7 0,7458 60,932 1,51926 27,9 1239,4 0,9795 64,957 1,4345 114,5 2267,2 0,4061 66,741 1,40041 159,8 3772,2 0,5032 73,472 1,28784 35,1 1069,2 0,6331 75,727 1,25501 506 9392,6 0,3964
ampiran 9 Data X-ray Diffraction (XRD) sampel D4 L
2θ (°) d (A) Height (a.u.) Area (a.u. °) FWHM (°) 21,361 4,15638 75,1 14124 1,3134 22,5 3,95819
2 5
,4
8
61
649,2 14554,7 0,24
Lampiran 10 Sudut difraksi (2θ) beberapa puncak pada profil XRD kristal okta kalsium fosfat, hidroksiapatit, apatit karbonat tipe A dan tipe B[JCPDS]
Apatit karbonat sudut 2θ (°) I/I0 h k l
okta kalsium fosfat 4,722 100 0 1 0
9,441 15 0 2 0
9,765 13 1 1 0
25,871
ydroksiapatit
atit tipe A
17 2 2 1
31,554 33 2 6 0
31,703 32 2 4 1
33,523 17 0 7 0
h
21,819 10 2 0 0
22,902 25,879 10 40 1 0 1 0 1 2
28,966 18 2 1 0
31,773 100 2 1 1
32,196 60 1 1 2
32,902 60 3 0 0
34,048 25 2 0 2
46,711 30 2 2 2
ap
23,376 40 2
1
6 1 25,972 30,510 35 10 0 0
0 2
1
31,529 100 3 3 0
32,214 70
2
0 232,596 50
2
3 2
atit tipe B
1 2
33,917 19 4 0
36,370 10 6 1
ap
25,748 25 0 0 2
29,380 32,199 10 100 2 1 1 1 0 2
33,435 40 3 0 0
40,430 16 3 1 0
Lampiran 11 Probabilitas kandungan kalsium fosfat dalam sampel (%)
AKB NaCl
Kode Sampel 2θ(°) OKF HAP AKA
A 25,932 99,76 99,79 99,85 99,29
31,884 98,95 99,65 98,87 99,39
33,249 99,18 98,03 99,44
B 9,34 9,59
9,38
9,72
7,28
9,55
1 9,89
9,73
2 9,81
9,16
3 7,61
4 9,13 9,57
7,91
31,564 99,97 9 99,89 9
C 25,907 99,86 99,89 99,75 9
31,601 99,85 99,46 99,77 9
D 26,448 97,77 97,80 98,17 9
31,549 32,229
99,98 99,29
99,89
99,94 99,95
9 99,91
D 25,898 9 99,93 99,72 99,42
31,777 33,793
99,29 99,19
99,99 99,21
99,63
9 98,93
D 25,83 99,34 9 99,45 99,68
31,957 33,998
98,72 98,58
99,42 98,64
99,76
9 98,32
D 25,26 97,15 9 97,26 98,10
32,336 99,57 99,62 99,57
D 31,828 9 99,83 99,05 9
Lampiran 12 Perhitungan ukuran kristal kalsium fosfat karbonat pada sampel
D[m] D[nm] Kode
Sampel 2θ (°) θ (°) COS θ FWHM (°) FWHM (rad)
A 25,932 12,966 0,975 0,596 0,0104 1,368E-08 13,675
C 25,907 12,954 0,975 0,705 0,0123 1,156E-08 11,56
D 26,448 13,224 0,974 0,379 0,0066 2,153E-08 21,528
D1 25,898 12,949 0,975 0,379 0,0066 2,149E-08 21,487
D2 25,83 12,915 0,974 0,386 0,0067 2,111E-08 21,111
D3 22,845 11,423 0,980 0,32 0,0056 2,532E-08 25,322
![Gambar 1 Unit sel struktur hidroksiapatit [6].](https://thumb-ap.123doks.com/thumbv2/123dok/539789.336732/11.595.120.284.571.689/gambar-unit-sel-struktur-hidroksiapatit.webp)
![Gambar 3 Proses terjadinya difraksi oleh kisi kristal[13].](https://thumb-ap.123doks.com/thumbv2/123dok/539789.336732/12.595.113.298.612.699/gambar-proses-terjadinya-difraksi-kisi-kristal.webp)
![Gambar 4 Skema SEM[14].](https://thumb-ap.123doks.com/thumbv2/123dok/539789.336732/13.595.122.295.93.388/gambar-skema-sem.webp)