PERBANDINGAN METODE ANALISIS SENYAWA NITROGEN
DENGAN KCl DAN CaCl
2DI BEBERAPA KEDALAMAN
TANAH YANG DITANAMI BAWANG DAUN
SARI UMARIAH
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
PERBANDINGAN METODE ANALISIS SENYAWA NITROGEN
DENGAN KCl DAN CaCl
2DI BEBERAPA KEDALAMAN
TANAH YANG DITANAMI BAWANG DAUN
SARI UMARIAH
Skripsi
sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
SARI UMARIAH. Perbandingan Metode Analisis Senyawa Nitrogen dengan KCl dan CaCl2 di Beberapa Kedalaman Tanah yang Ditanami Bawang Daun. Dibimbing oleh
MUCHAMMAD SRI SAENI dan DIAH SETYORINI.
Penggunaan pupuk yang berlebihan menyebabkan berbagai masalah, di antaranya ialah pencemaran lingkungan. Pengaturan dosis pupuk organik sangat penting pada budidaya intensif tanaman sayuran di dataran tinggi. Nitrogen merupakan salah satu unsur hara esensial dengan tingkat ketersediaan yang rendah di dalam tanah. Perilaku nitrogen di dalam tanah sangat dinamis dan mudah berubah sehingga dilakukan penelitian untuk mengetahui perilaku nitrogen pada tanah di pertanaman bawang daun dengan dosis pemupukan petani dan pemupukan introduksi menggunakan metode KCl dan CaCl2.
Penelitian ini dilakukan dalam dua tahap. Pada tahap pertama, contoh tanah diambil pada kedalaman 0−25, 25−50, 50−75, dan 75−100 cm yang ditanami bawang daun di Wonosobo, Jawa Tengah. Contoh tanah diambil secara berkala sejak tanam hingga panen dengan selang waktu 3 minggu di lokasi penelitian. Contoh tanah dikumpulkan dari sepuluh titik pegambilan contoh di atas guludan di antara tanaman bawang daun. Pada tahap kedua, kadar amonium dan nitrat pada tanah tersebut dianalisis dengan menggunakan metode KCl dan CaCl2 secara spektrofotometri. Berdasarkan hasil
pengamatan, metode CaCl2 tidak dapat digunakan pada penentuan kadar amonium dan
dapat digunakan pada penentuan nitrat. Pola distribusi kadar amonium pada dosis petani hampir sama dengan dosis introduksi dan kadar nitrat pada dosis petani lebih besar dibandingkan dengan dosis introduksi.
ABSTRACT
SARI UMARIAH. Comparison of Analysis Methods on Nitrogen Compounds using KCl and CaCl2 in Some Soil Depth Cultivated with Onion Leaves. Supervised by
MUCHAMMAD SRI SAENI and DIAH SETYORINI.
Excessive fertilizing causes various problems such as pollution to the environment. Dosage control of organic fertilizer is very important in an intensive vegetable cultivation an plateau. Nitrogen is one of the essential nutrient elements with low availability in the soil. Nitrogen behavior is very dynamic and always fluctuating, so research has to be carried out to study its behavior in the soil cultivated with onion leaves with farmer dose fertilization and introduction dose fertilization using KCl and CaCl2 methods.
This research was conducted in two phases. In the first phase, soil samples were taken from 0−25, 25−50, 50−75, and 75−100 cm of depth at onion leaves cultivation area in Wonosobo, Central Java. Soil samples were taken periodicaling since plant until harvesting every 3 weeks. Soil samples were collected from 10 sampling spots of above guludan among onion leaves plants. In the second phase, the ammonium and nitrate contents in those soils were determined by KCl and CaCl2 methods
spectrophotometrically. Based on the observation results, CaCl2 method could not be used
Judul : Perbandingan Metode Analisis Senyawa Nitrogen dengan KCl dan CaCl2
di Beberapa Kedalaman Tanah yang Ditanami Bawang Daun Nama : Sari Umariah
NIM : G44203038
Disetujui,
Pembimbing I, Pembimbing II,
Prof. Dr.Ir. M. Sri Saeni.MS
Dr. Diah Setyorini
NIP 130256339
NIP 080077872
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor,
Prof. Dr. Ir. Yonny Koesmaryono, MS NIP 131 473 999
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT yang telah melimpahkan rahmat dan karuniaNya sehingga penulis dapat menyelesaikan skipsi berdasarkan hasil penelitian yang dilaksanakan pada bulan Januari-Juni 2007 dengan judul Perbandingan Metode Analisis Senyawa Nitrogen dengan KCl dan CaCl2 di Beberapa Kedalaman Tanah yang Ditanami Bawang Daun. Terima kasih penulis ucapkan teramat besar kepada Prof.Dr.Ir.Muchammad Sri Saeni, MS selaku pembimbing I atas saran, kritik, masukan ilmu dan pengetahuan, serta kesabaran dalam membimbing. Terima kasih juga penulis sampaikan kepada Dr.Diah Setyorini selaku pembimbing II atas kesabaran dan bimbingannya. Terima kasih juga diberikan kepada kegiatan penelitian N-Balance yang kerja sama antara Ghent University, Belgia dengan Balai Penelitian Tanah, Bogor, pak Ibrahim atas masukan ilmu dan kesabarannya, Pak Mulyadi dan Pak Didi atas masukan ilmunya, beserta teman-teman kimia angkatan 40 khususnya Diah, Feri, Widya, Tika, dan Ayu dari D3 Ilmu Tanah, Kak Budhi, kosan B 2 dan B 14. Penghargaan dan terima kasih juga ditujukan kepada Mama, Bapa, my sisters and brothers, atas kasih sayang, perhatian, dan dukungannya.
Semoga laporan ini bermanfaat bagi pembaca pada umumnya dan bagi penulis pada khususnya.
Bogor, Juli 2007
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 8 November 1985 dari ayah bernama Ir. Umar Hamzah (Alm) dan Ibu bernama Hj. Badriah. Penulis adalah anak ke-3 dari 4 bersaudara.
Tahun 2003 penulis lulus dari SMU Negeri 1 Tambun serta pada tahun yang sama lulus masuk IPB melalui jalur USMI (Undangan Seleksi Masuk IPB). Penulis memilih Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... vii
DAFTAR TABEL ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Tanah ... 1
Nitrogen dalam tanah ... 2
Metode Penetapan Nitrogen ... 3
Kadar air ... 3
Spektrofotometer UV-Vis ... 3
BAHAN DAN METODE Bahan dan Alat ... 3
Pengambilan Contoh ... 4
Penetapan Kadar Air ... 4
Ekstraksi Contoh ... 4
Penetapan Amonium dan Nitrat dengan KCl ... 4
Penetapan Amonium dan Nitrat dengan CaCl2 ... 4
Pengolahan Data ... 4
HASIL DAN PEMBAHASAN Sifat Tanah Awal ... 4
Uji Beda Nilai Tengah antara Metode KCl dan CaCl2 pada Penentuan Kadar Amonium ... 5
Uji Beda Nilai Tengah antara Metode KCl dan CaCl2 pada Penentuan Kadar Nitrat ... 5
Dosis Petani dan Introduksi ... 5
Pola Distribuís Kadar Amonium ... 6
Pola Distribusi Kadar Nitrat ... 7
SIMPULAN DAN SARAN Simpulan ... 7
Saran ... 8
DAFTAR PUSTAKA ... 8
DAFTAR GAMBAR
Halaman
1 Perubahan nitrogen dalam tanah... 2
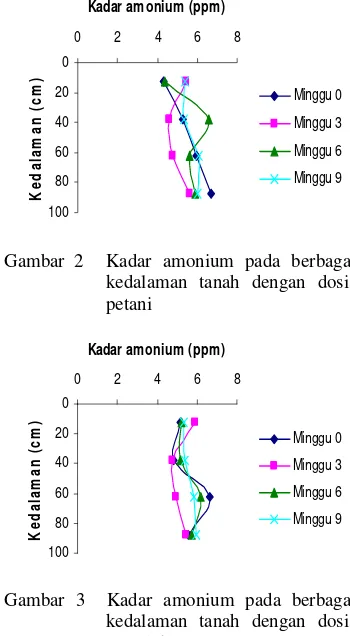
2 Kadar amonium pada berbagai kedalaman tanah dengan dosis petani... 6
3 Kadar amonium pada berbagai kedalaman tanah dengan dosis introduksi... 6
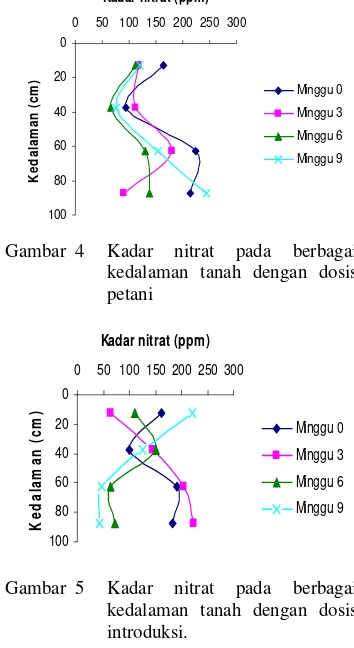
4 Kadar nitrat pada berbagai kedalaman tanah dengan dosis petani... 7
5 Kadar nitrat pada kedalaman tanah dengan dosis introduksi... 7
DAFTAR TABEL
Halaman 1 Sifat-sifat tanah Andisol Wonosobo, Jawa Tengah... 12 Dosis pemupukan petani dan introduksi ... 5
3 Kadar N pada pupuk dan tanaman ... 6
DAFTAR LAMPIRAN
Halaman 1 Pembuatan pereaksi ... 102 Pembagian kelas tekstur tanah ... 12
3 Kriteria penilaian sifat-sifat tanah (Pusat Penelitian Tanah, 2005) ... 13
4 Perhitungan statistik dengan uji beda nilai tengah dua populasi ... 14
5 Kurva standar amonium dan nitrat pada dua metode ... 15
6 Diagram alir penelitian ... 17
7 Contoh Perhitungan ... 18
8 Data analisis penentuan amonium pada metode KCl 1 N (ulangan 1) ... 19
9 Data analisis penentuan amonium pada metode KCl 1 N (ulangan 2) ... 20
10 Data analisis penentuan amonium pada metode KCl 1 N (ulangan 3)... 21
11 Data analisis penentuan amonium pada metode CaCl2 0.01 M (ulangan 1) ... 22
12 Data analisis penentuan amonium pada metode CaCl2 0.01 M (ulangan 2) ... 23
13 Data analisis penentuan amonium pada metode CaCl2 0.01 M (ulangan 3) ... 24
14 Data analisis penentuan nitrat pada metode KCl 1 N (ulangan 1)... 25
15 Data analisis penentuan nitrat pada metode KCl 1 N (ulangan 2) ... 26
16 Data analisis penentuan nitrat pada metode KCl 1 N (ulangan 3) ... 27
17 Data analisis penentuan nitrat pada metode CaCl2 0.01 M (ulangan 1) ... 28
18 Data analisis penentuan nitrat pada metode CaCl2 0.01 M (ulangan 2)... 29
PENDAHULUAN
Peningkatan produksi tanaman sangat berkaitan dengan keadaan hara dalam tanah. Pupuk merupakan unsur hara yang dibutuhkan oleh tanaman, sehingga pemanfaatannya dibutuhkan untuk meningkatkan produksi pertanian. Penggunaan pupuk yang berlebihan menyebabkan berbagai masalah, di antaranya pencemaran lingkungan dan tanaman menjadi kurang sehat serta peka terhadap hama penyakit (Bonh et al. 1979).
Pemupukan dilakukan hanya untuk memenuhi kebutuhan unsur hara tanaman yang tidak dapat disediakan sepenuhnya oleh sistem tanah. Jenis dan jumlah unsur hara yang diberikan harus disesuaikan dengan kebutuhan tanaman untuk tingkat produksi tertentu. Untuk mencapai tujuan tersebut, ketersediaan unsur hara dalam tanah harus diketahui lebih dahulu melalui evaluasi status ketersediaan hara dalam tanah. Pengaturan dosis pupuk organik sangat penting pada budidaya intensif tanaman sayuran di dataran tinggi (Soepardi 1996).
Nitrogen merupakan salah satu unsur hara esensial dengan tingkat ketersediaan yang rendah di dalam tanah, karena mudah hilang melalui proses penguapan dan pencucian. Perilaku nitrogen di dalam tanah sangat dinamis dan mudah berubah. Kondisi ini berbahaya bagi lingkungan dan kesehatan manusia sehingga penggunaan pupuk harus diefisienkan (Resh 1983). Nitrogen dibutuhkan dalam jumlah besar untuk mendukung pertumbuhan tanaman (Soepardi 1996). Sumber utama nitrogen di dalam tanah adalah bahan organik, sehingga keberadaan bahan organik akan menentukan jumlah dan ketersediaannya di dalam tanah.
Penelitian ini bertujuan membandingkan dua metode penentuan amonium (NH4+) dan
nitrat (NO3
-) yang menggunakan KCl dan CaCl2 serta melihat pola distribusi amonium
dan nitrat di beberapa kedalaman tanah pada dosis pemupukan petani dan dosis pemupukan introduksi pada pertanaman bawang daun di dataran tinggi Wonosobo, Jawa Tengah. Hasil dari penelitian ini diharapkan dapat memberikan informasi mengenai metode yang baik serta efisien dalam menentukan amonium dan nitrat serta mengetahui dosis penggunaan pupuk yang baik.
TINJAUAN PUSTAKA
Tanah
Tanah merupakan hasil pelapukan batuan yang bercampur dengan sisa-sisa bahan organik dari organisme (vegetasi atau hewan) yang hidup di permukaan atau di dalamnya. Setiap jenis tanah mempunyai sifat dan karakteristik tertentu yang dicirikan melalui sifat fisik, kimia, dan biologi tanahnya (Tejoyuwono 1998)
Kemasaman dan kebasaan tanah dipengaruhi oleh macam kation yang terjerap pada permukaan zarah-zarah koloid. Kation-kation utama yang terjerap ialah Al3+, H+, Na+,
K+, Ca2+, dan Mg2+ (Tan Kim 1991). Setiap jenis tanah memiliki kandungan bahan organik yang berbeda-beda, tergantung dari tingkat ketinggian dan horizon tanah (Darmawijaya 1990).
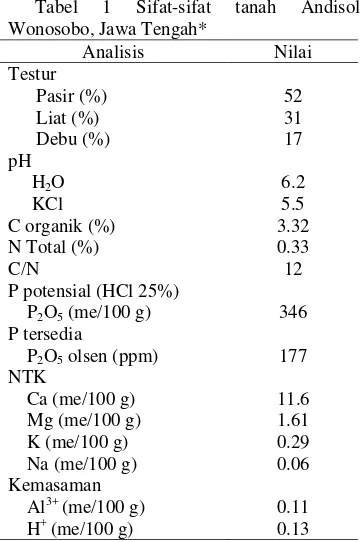
Tanah andisol merupakan tanah yang berkembang dari bahan vulkanik (Hardjowigeno 2003). Andisol secara umum mempunyai sifat-sifat kimia dan fisika yang penting (Anonim 1997). Menurut Tan (1984) menyatakan bahwa andisol di Indonesia dicirikan oleh kandungan bahan organik yang tinggi dengan nilai pH berkisar 3.8−6.4. Berikut ini sifat-sifat tanah andisol Wonosobo, Jawa Tengah.
Tabel 1 Sifat-sifat tanah Andisol Wonosobo, Jawa Tengah*
Analisis Nilai Testur Pasir (%) 52
Liat (%) 31 Debu (%) 17
pH
H2O 6.2
KCl 5.5 C organik (%) 3.32 N Total (%) 0.33
C/N 12 P potensial (HCl 25%)
P2O5 (me/100 g) 346
P tersedia
P2O5 olsen (ppm) 177
NTK Ca (me/100 g) 11.6
Mg (me/100 g) 1.61 K (me/100 g) 0.29 Na (me/100 g) 0.06 Kemasaman
Al3+ (me/100 g) 0.11
H+ (me/100 g) 0.13
2
Nitrogen dalam Tanah
Nitrogen merupakan salah satu unsur hara makro bagi pertumbuhan tanaman yang sangat diperlukan untuk pembentukan atau pertumbuhan seperti daun, batang dan akar (Hakim 1986).
Kekurangan nitrogen menyebabkan daun kasar dan berserat serta berwarna kekuningan (Ashari 1995). Kelebihan nitrogen pada tanaman dapat menyebabkan tanaman menjadi cepat layu dan rentan terhadap serangan penyakit (Douglas 1985).
Tanaman dapat menyerap nitrogen dalam bentuk amonium atau nitrat (Hakim 1986). Penyerapan amonium dan nitrat oleh tumbuhan memungkinkan tumbuhan untuk membentuk senyawa nitrogen (Harjadi & Sunaryono 1989). Nitrogen tanah dibagi dalam dua bentuk, yaitu bentuk organik dan anorganik. Bentuk organik merupakan bagian terbesar. Senyawa N organik dalam tanah pada umumnya terdapat dalam bentuk asam-asam amino (Leiwakabessy 1998).
Nitrogen anorganik dalam tanah dijumpai dalam bentuk seperti gas nitrogen (N2),
nitrous oksida (N2O), dan amonia (NH3), dan
dalam bentuk ion-ion seperti nitrat (NO3
-), nitrit (NO2-), dan amonium (NH4+) (Bockman et al. 1990).
Menurut Soepardi (1996), ion-ion nitrat, nitrit dan amonium jumlahnya tergantung dari jumlah pupuk yang diberikan dan kecepatan dekomposisi bahan organik tanah. Proses dekomposisi ini terjadi melalui tiga tahap, yaitu Aminisasi ialah pemecahan protein dan senyawa serupa menjadi senyawa amino. Reaksi yang terjadi sebagai berikut:
Protein R-NH2 + CO2 + Energi
Amonifikasi ialah proses enzimatik yang mengubah senyawa amino menjadi amonium. Reaksi yang terjadi sebagai berikut:
R-NH2 + HOH R-OH + NH3 + Energi
NH3 + H2O NH4OH NH4 +
+ OH−
Nitrifikasi yaitu proses oksidasi enzimatik yang mengubah amonium menjadi nitrat. Reaksi yang terjadi sebagi berikut:
2NH4+ + 3O2 2NO2−+ 2H2O + 4H+ + Energi
2NO2
+ O2 2NO3
−
+ Energi
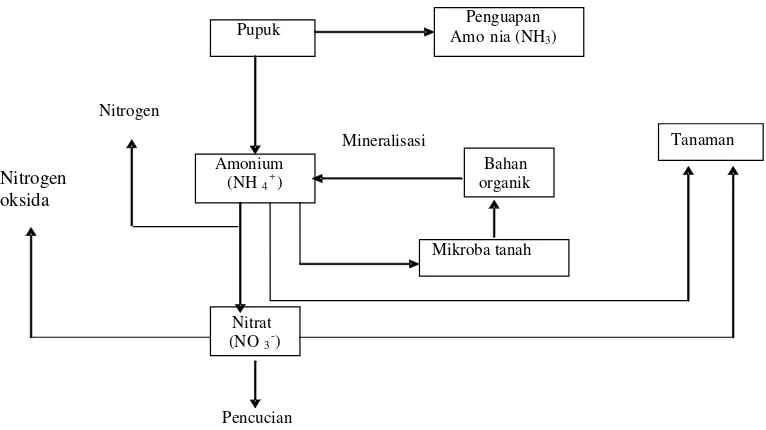
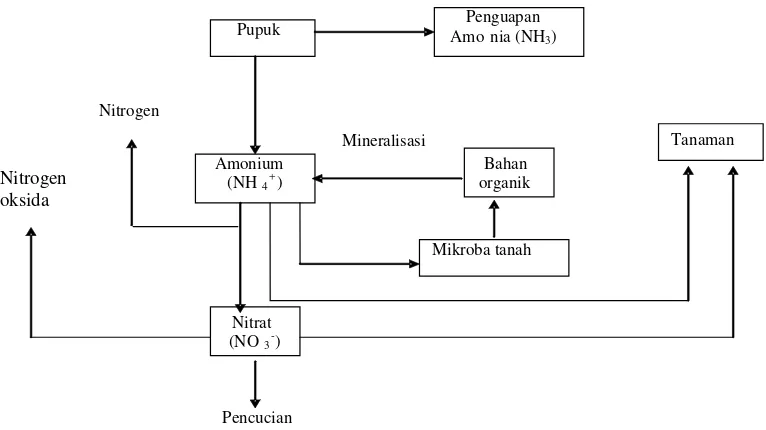
Gambar 1 Perubahan senyawa nitrogen dalam tanah (Bockman et al. 1990).
Penguapan Amo nia (NH3) Pupuk
Tanaman
Mikroba tanah
Nitrat (NO3-)
Bahan organik Amonium
(NH4+)
Denitrifikasi
Mineralisasi
Nitrogen Hidrolisis
Nitrogen oksida
PERBANDINGAN METODE ANALISIS SENYAWA NITROGEN
DENGAN KCl DAN CaCl
2DI BEBERAPA KEDALAMAN
TANAH YANG DITANAMI BAWANG DAUN
SARI UMARIAH
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
PERBANDINGAN METODE ANALISIS SENYAWA NITROGEN
DENGAN KCl DAN CaCl
2DI BEBERAPA KEDALAMAN
TANAH YANG DITANAMI BAWANG DAUN
SARI UMARIAH
Skripsi
sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
SARI UMARIAH. Perbandingan Metode Analisis Senyawa Nitrogen dengan KCl dan CaCl2 di Beberapa Kedalaman Tanah yang Ditanami Bawang Daun. Dibimbing oleh
MUCHAMMAD SRI SAENI dan DIAH SETYORINI.
Penggunaan pupuk yang berlebihan menyebabkan berbagai masalah, di antaranya ialah pencemaran lingkungan. Pengaturan dosis pupuk organik sangat penting pada budidaya intensif tanaman sayuran di dataran tinggi. Nitrogen merupakan salah satu unsur hara esensial dengan tingkat ketersediaan yang rendah di dalam tanah. Perilaku nitrogen di dalam tanah sangat dinamis dan mudah berubah sehingga dilakukan penelitian untuk mengetahui perilaku nitrogen pada tanah di pertanaman bawang daun dengan dosis pemupukan petani dan pemupukan introduksi menggunakan metode KCl dan CaCl2.
Penelitian ini dilakukan dalam dua tahap. Pada tahap pertama, contoh tanah diambil pada kedalaman 0−25, 25−50, 50−75, dan 75−100 cm yang ditanami bawang daun di Wonosobo, Jawa Tengah. Contoh tanah diambil secara berkala sejak tanam hingga panen dengan selang waktu 3 minggu di lokasi penelitian. Contoh tanah dikumpulkan dari sepuluh titik pegambilan contoh di atas guludan di antara tanaman bawang daun. Pada tahap kedua, kadar amonium dan nitrat pada tanah tersebut dianalisis dengan menggunakan metode KCl dan CaCl2 secara spektrofotometri. Berdasarkan hasil
pengamatan, metode CaCl2 tidak dapat digunakan pada penentuan kadar amonium dan
dapat digunakan pada penentuan nitrat. Pola distribusi kadar amonium pada dosis petani hampir sama dengan dosis introduksi dan kadar nitrat pada dosis petani lebih besar dibandingkan dengan dosis introduksi.
ABSTRACT
SARI UMARIAH. Comparison of Analysis Methods on Nitrogen Compounds using KCl and CaCl2 in Some Soil Depth Cultivated with Onion Leaves. Supervised by
MUCHAMMAD SRI SAENI and DIAH SETYORINI.
Excessive fertilizing causes various problems such as pollution to the environment. Dosage control of organic fertilizer is very important in an intensive vegetable cultivation an plateau. Nitrogen is one of the essential nutrient elements with low availability in the soil. Nitrogen behavior is very dynamic and always fluctuating, so research has to be carried out to study its behavior in the soil cultivated with onion leaves with farmer dose fertilization and introduction dose fertilization using KCl and CaCl2 methods.
This research was conducted in two phases. In the first phase, soil samples were taken from 0−25, 25−50, 50−75, and 75−100 cm of depth at onion leaves cultivation area in Wonosobo, Central Java. Soil samples were taken periodicaling since plant until harvesting every 3 weeks. Soil samples were collected from 10 sampling spots of above guludan among onion leaves plants. In the second phase, the ammonium and nitrate contents in those soils were determined by KCl and CaCl2 methods
spectrophotometrically. Based on the observation results, CaCl2 method could not be used
Judul : Perbandingan Metode Analisis Senyawa Nitrogen dengan KCl dan CaCl2
di Beberapa Kedalaman Tanah yang Ditanami Bawang Daun Nama : Sari Umariah
NIM : G44203038
Disetujui,
Pembimbing I, Pembimbing II,
Prof. Dr.Ir. M. Sri Saeni.MS
Dr. Diah Setyorini
NIP 130256339
NIP 080077872
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor,
Prof. Dr. Ir. Yonny Koesmaryono, MS NIP 131 473 999
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT yang telah melimpahkan rahmat dan karuniaNya sehingga penulis dapat menyelesaikan skipsi berdasarkan hasil penelitian yang dilaksanakan pada bulan Januari-Juni 2007 dengan judul Perbandingan Metode Analisis Senyawa Nitrogen dengan KCl dan CaCl2 di Beberapa Kedalaman Tanah yang Ditanami Bawang Daun. Terima kasih penulis ucapkan teramat besar kepada Prof.Dr.Ir.Muchammad Sri Saeni, MS selaku pembimbing I atas saran, kritik, masukan ilmu dan pengetahuan, serta kesabaran dalam membimbing. Terima kasih juga penulis sampaikan kepada Dr.Diah Setyorini selaku pembimbing II atas kesabaran dan bimbingannya. Terima kasih juga diberikan kepada kegiatan penelitian N-Balance yang kerja sama antara Ghent University, Belgia dengan Balai Penelitian Tanah, Bogor, pak Ibrahim atas masukan ilmu dan kesabarannya, Pak Mulyadi dan Pak Didi atas masukan ilmunya, beserta teman-teman kimia angkatan 40 khususnya Diah, Feri, Widya, Tika, dan Ayu dari D3 Ilmu Tanah, Kak Budhi, kosan B 2 dan B 14. Penghargaan dan terima kasih juga ditujukan kepada Mama, Bapa, my sisters and brothers, atas kasih sayang, perhatian, dan dukungannya.
Semoga laporan ini bermanfaat bagi pembaca pada umumnya dan bagi penulis pada khususnya.
Bogor, Juli 2007
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 8 November 1985 dari ayah bernama Ir. Umar Hamzah (Alm) dan Ibu bernama Hj. Badriah. Penulis adalah anak ke-3 dari 4 bersaudara.
Tahun 2003 penulis lulus dari SMU Negeri 1 Tambun serta pada tahun yang sama lulus masuk IPB melalui jalur USMI (Undangan Seleksi Masuk IPB). Penulis memilih Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... vii
DAFTAR TABEL ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Tanah ... 1
Nitrogen dalam tanah ... 2
Metode Penetapan Nitrogen ... 3
Kadar air ... 3
Spektrofotometer UV-Vis ... 3
BAHAN DAN METODE Bahan dan Alat ... 3
Pengambilan Contoh ... 4
Penetapan Kadar Air ... 4
Ekstraksi Contoh ... 4
Penetapan Amonium dan Nitrat dengan KCl ... 4
Penetapan Amonium dan Nitrat dengan CaCl2 ... 4
Pengolahan Data ... 4
HASIL DAN PEMBAHASAN Sifat Tanah Awal ... 4
Uji Beda Nilai Tengah antara Metode KCl dan CaCl2 pada Penentuan Kadar Amonium ... 5
Uji Beda Nilai Tengah antara Metode KCl dan CaCl2 pada Penentuan Kadar Nitrat ... 5
Dosis Petani dan Introduksi ... 5
Pola Distribuís Kadar Amonium ... 6
Pola Distribusi Kadar Nitrat ... 7
SIMPULAN DAN SARAN Simpulan ... 7
Saran ... 8
DAFTAR PUSTAKA ... 8
DAFTAR GAMBAR
Halaman
1 Perubahan nitrogen dalam tanah... 2
2 Kadar amonium pada berbagai kedalaman tanah dengan dosis petani... 6
3 Kadar amonium pada berbagai kedalaman tanah dengan dosis introduksi... 6
4 Kadar nitrat pada berbagai kedalaman tanah dengan dosis petani... 7
5 Kadar nitrat pada kedalaman tanah dengan dosis introduksi... 7
DAFTAR TABEL
Halaman 1 Sifat-sifat tanah Andisol Wonosobo, Jawa Tengah... 12 Dosis pemupukan petani dan introduksi ... 5
3 Kadar N pada pupuk dan tanaman ... 6
DAFTAR LAMPIRAN
Halaman 1 Pembuatan pereaksi ... 102 Pembagian kelas tekstur tanah ... 12
3 Kriteria penilaian sifat-sifat tanah (Pusat Penelitian Tanah, 2005) ... 13
4 Perhitungan statistik dengan uji beda nilai tengah dua populasi ... 14
5 Kurva standar amonium dan nitrat pada dua metode ... 15
6 Diagram alir penelitian ... 17
7 Contoh Perhitungan ... 18
8 Data analisis penentuan amonium pada metode KCl 1 N (ulangan 1) ... 19
9 Data analisis penentuan amonium pada metode KCl 1 N (ulangan 2) ... 20
10 Data analisis penentuan amonium pada metode KCl 1 N (ulangan 3)... 21
11 Data analisis penentuan amonium pada metode CaCl2 0.01 M (ulangan 1) ... 22
12 Data analisis penentuan amonium pada metode CaCl2 0.01 M (ulangan 2) ... 23
13 Data analisis penentuan amonium pada metode CaCl2 0.01 M (ulangan 3) ... 24
14 Data analisis penentuan nitrat pada metode KCl 1 N (ulangan 1)... 25
15 Data analisis penentuan nitrat pada metode KCl 1 N (ulangan 2) ... 26
16 Data analisis penentuan nitrat pada metode KCl 1 N (ulangan 3) ... 27
17 Data analisis penentuan nitrat pada metode CaCl2 0.01 M (ulangan 1) ... 28
18 Data analisis penentuan nitrat pada metode CaCl2 0.01 M (ulangan 2)... 29
PENDAHULUAN
Peningkatan produksi tanaman sangat berkaitan dengan keadaan hara dalam tanah. Pupuk merupakan unsur hara yang dibutuhkan oleh tanaman, sehingga pemanfaatannya dibutuhkan untuk meningkatkan produksi pertanian. Penggunaan pupuk yang berlebihan menyebabkan berbagai masalah, di antaranya pencemaran lingkungan dan tanaman menjadi kurang sehat serta peka terhadap hama penyakit (Bonh et al. 1979).
Pemupukan dilakukan hanya untuk memenuhi kebutuhan unsur hara tanaman yang tidak dapat disediakan sepenuhnya oleh sistem tanah. Jenis dan jumlah unsur hara yang diberikan harus disesuaikan dengan kebutuhan tanaman untuk tingkat produksi tertentu. Untuk mencapai tujuan tersebut, ketersediaan unsur hara dalam tanah harus diketahui lebih dahulu melalui evaluasi status ketersediaan hara dalam tanah. Pengaturan dosis pupuk organik sangat penting pada budidaya intensif tanaman sayuran di dataran tinggi (Soepardi 1996).
Nitrogen merupakan salah satu unsur hara esensial dengan tingkat ketersediaan yang rendah di dalam tanah, karena mudah hilang melalui proses penguapan dan pencucian. Perilaku nitrogen di dalam tanah sangat dinamis dan mudah berubah. Kondisi ini berbahaya bagi lingkungan dan kesehatan manusia sehingga penggunaan pupuk harus diefisienkan (Resh 1983). Nitrogen dibutuhkan dalam jumlah besar untuk mendukung pertumbuhan tanaman (Soepardi 1996). Sumber utama nitrogen di dalam tanah adalah bahan organik, sehingga keberadaan bahan organik akan menentukan jumlah dan ketersediaannya di dalam tanah.
Penelitian ini bertujuan membandingkan dua metode penentuan amonium (NH4+) dan
nitrat (NO3
-) yang menggunakan KCl dan CaCl2 serta melihat pola distribusi amonium
dan nitrat di beberapa kedalaman tanah pada dosis pemupukan petani dan dosis pemupukan introduksi pada pertanaman bawang daun di dataran tinggi Wonosobo, Jawa Tengah. Hasil dari penelitian ini diharapkan dapat memberikan informasi mengenai metode yang baik serta efisien dalam menentukan amonium dan nitrat serta mengetahui dosis penggunaan pupuk yang baik.
TINJAUAN PUSTAKA
Tanah
Tanah merupakan hasil pelapukan batuan yang bercampur dengan sisa-sisa bahan organik dari organisme (vegetasi atau hewan) yang hidup di permukaan atau di dalamnya. Setiap jenis tanah mempunyai sifat dan karakteristik tertentu yang dicirikan melalui sifat fisik, kimia, dan biologi tanahnya (Tejoyuwono 1998)
Kemasaman dan kebasaan tanah dipengaruhi oleh macam kation yang terjerap pada permukaan zarah-zarah koloid. Kation-kation utama yang terjerap ialah Al3+, H+, Na+,
K+, Ca2+, dan Mg2+ (Tan Kim 1991). Setiap jenis tanah memiliki kandungan bahan organik yang berbeda-beda, tergantung dari tingkat ketinggian dan horizon tanah (Darmawijaya 1990).
Tanah andisol merupakan tanah yang berkembang dari bahan vulkanik (Hardjowigeno 2003). Andisol secara umum mempunyai sifat-sifat kimia dan fisika yang penting (Anonim 1997). Menurut Tan (1984) menyatakan bahwa andisol di Indonesia dicirikan oleh kandungan bahan organik yang tinggi dengan nilai pH berkisar 3.8−6.4. Berikut ini sifat-sifat tanah andisol Wonosobo, Jawa Tengah.
Tabel 1 Sifat-sifat tanah Andisol Wonosobo, Jawa Tengah*
Analisis Nilai Testur Pasir (%) 52
Liat (%) 31 Debu (%) 17
pH
H2O 6.2
KCl 5.5 C organik (%) 3.32 N Total (%) 0.33
C/N 12 P potensial (HCl 25%)
P2O5 (me/100 g) 346
P tersedia
P2O5 olsen (ppm) 177
NTK Ca (me/100 g) 11.6
Mg (me/100 g) 1.61 K (me/100 g) 0.29 Na (me/100 g) 0.06 Kemasaman
Al3+ (me/100 g) 0.11
H+ (me/100 g) 0.13
2
Nitrogen dalam Tanah
Nitrogen merupakan salah satu unsur hara makro bagi pertumbuhan tanaman yang sangat diperlukan untuk pembentukan atau pertumbuhan seperti daun, batang dan akar (Hakim 1986).
Kekurangan nitrogen menyebabkan daun kasar dan berserat serta berwarna kekuningan (Ashari 1995). Kelebihan nitrogen pada tanaman dapat menyebabkan tanaman menjadi cepat layu dan rentan terhadap serangan penyakit (Douglas 1985).
Tanaman dapat menyerap nitrogen dalam bentuk amonium atau nitrat (Hakim 1986). Penyerapan amonium dan nitrat oleh tumbuhan memungkinkan tumbuhan untuk membentuk senyawa nitrogen (Harjadi & Sunaryono 1989). Nitrogen tanah dibagi dalam dua bentuk, yaitu bentuk organik dan anorganik. Bentuk organik merupakan bagian terbesar. Senyawa N organik dalam tanah pada umumnya terdapat dalam bentuk asam-asam amino (Leiwakabessy 1998).
Nitrogen anorganik dalam tanah dijumpai dalam bentuk seperti gas nitrogen (N2),
nitrous oksida (N2O), dan amonia (NH3), dan
dalam bentuk ion-ion seperti nitrat (NO3
-), nitrit (NO2-), dan amonium (NH4+) (Bockman et al. 1990).
Menurut Soepardi (1996), ion-ion nitrat, nitrit dan amonium jumlahnya tergantung dari jumlah pupuk yang diberikan dan kecepatan dekomposisi bahan organik tanah. Proses dekomposisi ini terjadi melalui tiga tahap, yaitu Aminisasi ialah pemecahan protein dan senyawa serupa menjadi senyawa amino. Reaksi yang terjadi sebagai berikut:
Protein R-NH2 + CO2 + Energi
Amonifikasi ialah proses enzimatik yang mengubah senyawa amino menjadi amonium. Reaksi yang terjadi sebagai berikut:
R-NH2 + HOH R-OH + NH3 + Energi
NH3 + H2O NH4OH NH4 +
+ OH−
Nitrifikasi yaitu proses oksidasi enzimatik yang mengubah amonium menjadi nitrat. Reaksi yang terjadi sebagi berikut:
2NH4+ + 3O2 2NO2−+ 2H2O + 4H+ + Energi
2NO2
+ O2 2NO3
−
+ Energi
Gambar 1 Perubahan senyawa nitrogen dalam tanah (Bockman et al. 1990).
Penguapan Amo nia (NH3) Pupuk
Tanaman
Mikroba tanah
Nitrat (NO3-)
Bahan organik Amonium
(NH4+)
Denitrifikasi
Mineralisasi
Nitrogen Hidrolisis
Nitrogen oksida
3
Jumlah yang dibebaskan dari bahan organik ditentukan oleh keseimbangan antara faktor yang mempengaruhi mineralisasi, mobilisasi, dan kehilangan N dari tanah (Sanchez 1976; Tisdale et al. 1985). Berikut ini adalah siklus perubahan senyawa nitrogen di dalam tanah (Gambar 1).
Kehilangan nitrogen pada pertanian dapat terjadi melalui denitrifikasi, volatilisasi amonia, dan kehilangan NO3− karena proses
memperlihatkan bahwa pencucian (Hidayat et al. 1984). Gambar 1 nitrogen tercuci di dalam tanah sebagai nitrat (NO3
−
) sedangkan amonium (NH4
+
) mudah terjerap pada kompleks pertukaran kation. Pencucian nitrat merupakan masalah pencemaran yang potensial terjadi pada air permukaan dan air bawah tanah yang sangat berbahaya bagi lingkungan dan kesehatan manusia (Bonh et al. 1979).
Nitrogen dalam bentuk NO3
−
lebih mobil. Pada kondisi curah hujan yang tinggi atau irigasi, NO3− tercuci dari horizon atas tanah
(Sibuea 1993). Selama musim kemarau yang hebat dan pergerakan air kapiler memungkinkan ke atas dan ke bawah, akibatnya nitrat akan terakumulasi pada bagian atas horizon tanah bahkan di permukaan tanah (Tisdale et al. 1985). Menurut Ponnamperuma (1976) penguapan amonia (NH3) dari pupuk-pupuk dipengaruhi
oleh suhu, kelembaban, jenis dan dosis pupuk amonium, serta dalamnya penempatan.
Metode Penetapan Senyawa Nitrogen
Nitrogen total dalam tanah dapat ditentukan dengan metode Kjedahl, sementara nitrogen yang tersedia dapat ditetapkan dengan metode KCl dan Morgan Wolf. Penetapan nitrogen total dengan metode Kjeldahl didasarkan ketetapan bahwa senyawa nitrogen organik dan anorganik dapat dioksidasi dalam lingkungan asam sulfat (H2SO4) membentuk amonium sulfat.
Amonium sulfat yang terbentuk disuling dengan penambahan NaOH yang akan membebaskan NH3. NH3 yang tersuling akan
diikat oleh asam borat dan dapat dititar dengan H2SO4 dengan menggunakan conway
(Wijdjik & Hardjono 1996). Reaksi yang terjadi sebagai berikut:
N-Tanah + H2SO4→ (NH4)2SO4
(NH4)2SO4 + 2NaOH → 2NH3 + Na2SO4 + 2H2O
NH3 + H3BO3→ NH4H2BO3
2NH4H2BO3 + H2SO4→ (NH4)2SO4 + 2H3BO3
Metode ekstraksi dengan KCl dasar penetapan ialah senyawa nitrogen (NH4+ dan
NO3−) dalam tanah dapat dibebaskan oleh KCl
1 N menjadi amonium klorida dan kalium nitrat. Sementara N-organik tidak terekstrak. Untuk mengukur NH4+ dan NO3− yang
dibebaskan tersebut dapat dengan cara spektrofotometer atau distilasi dapat digunakan (Wijdjik & Hardjono 1996).
Kadar Air
Air ini kurang tersedia untuk tanaman karena penjerapan secara fisik maupun kimia air oleh bahan-bahan organik, Untuk menetapkan kandungan komponen lain dari bahan penentuan kadar air dilakukan agar kandungan komponen-komponen tersebut dapat dinyatakan sebagai % bahan kering dan nilainya konstan (Harjadi 1993). Kadar air dapat ditetapkan dengan metode gravimetri. Gravimetri merupakan cara penentuan jumlah zat berdasarkan pada penimbangan hasil reaksi setelah bahan yang dianalisis direaksikan (Harjadi 1993).
Spektrofotometri Ultraviolet -Tampak
Suatu spektrofotometer tersusun dari sumber spektrum tampak yang kontinyu, monokromator, sel pengabsorpsi untuk larutan sampel atau blangko dan satu alat untuk mengukur perbedaan absorpsi antara sampel dan blangko ataupun pembanding (Khopkar 2003). Prinsip kerja alat spektrofotometer ultraviolet-tampak (UV-Vis) adalah sumber radiasi yang merupakan sinar polikromatis dilewatkan melalui monokromator, kemudian sinar ini oleh monokromator diteruskan melalui sel yang berisi sampel. Sinar sebagian diserap oleh sel dan sebagian diteruskan ke fotosel yang berfungsi mengubah energi cahaya menjadi energi listrik. Energi listrik yang dihasilkan oleh fotosel memberikan sinyal pada detektor yang kemudian diubah menjadi nilai serapan (Day & Underwood 1989).
BAHAN DAN METODE
Waktu dan Tempat
4
dengan Balai Penelitian Tanah, Bogor tahun 2005−2010.
Bahan dan Alat
Bahan-bahan yang digunakan di antaranya adalah pupuk urea, pukan ayam, SP−36, KCl, K−Na tartrat, fenol, natrium hipoklorit (NaOCl 5%), H2SO4 pekat, brusin 2%, serbuk
KNO3, air bebas ion, dan serbuk CaCl2. Alat
yang digunakan adalah ombrometer, meteran, bor tanah, kantong plastik, ember, neraca analitik, alat-alat kaca, dan spektrofotometer.
Metode
Pengambilan Contoh Tanah
Contoh tanah diambil secara periodik sejak tanam hingga panen dengan selang waktu 3 minggu di lokasi penelitian (Wonosobo, Jawa tengah). Contoh tanah dikumpulkan dari 10 titik pengambilan contoh di atas guludan diantara tanaman bawang daun dengan empat kedalaman, yaitu 0−25, 25−50, 50−75, dan 75−100 cm.
Penetapan Kadar Air
Sebanyak 5 g contoh dimasukan ke dalam cawan dan dikeringkan dalam oven pada suhu 105 oC selama 4 jam, Setelah di oven selama 4 jam dimasukan ke dalam eksikator kemudian ditimbang dengan neraca analitik.
Ekstraksi contoh
Sebanyak 5 g contoh tanah masing-masing ditimbang ke dalam botol kocok. 25 ml pengekstrak KCl 1 N dan pengekstrak CaCl2
0.01 M ditambahkan kemudian dikocok selama 30 menit lalu disaring hingga didapatkan ekstrak.
Penetapan Amonium dan Nitrat dengan KCl 1 N (Wijdjik & Hardjono 1996)
Penentuan amonium dalam contoh
Sebanyak 1 ml ekstrak contoh dan deret standar (Lampiran 1) dipipet ke dalam tabung reaksi ditambahkan 2 ml larutan bufer tartrat dan 2 ml Na−fenolat, dikocok dan dibiarkan selama 10 menit. Sebanyak 1 ml natrium hipoklorit 5% ditambahkan, dikocok selama 10 menit dan serapan diukur pada panjang gelombang 630 nm.
Penentuan nitrat dalam contoh
Sebanyak 5 ml ekstrak contoh dan deret standar (Lampiran 1) dipipet ke dalam tabung reaksi. Sebanyak 0.5 ml brusin 2% dan 5 ml H2SO4 pekat ditambahkan sambil dikocok,
dibiarkan selama 30 menit hingga dingin. Kemudian serapan diukur pada panjang gelombang 432 nm.
Penetapan Amonium dan Nitrat dengan CaCl2 0.01 M (Goldman & Jacobs 1991)
Penentuan amonium dalam contoh
Sebanyak 2 ml filtrat dan deret standar (Lampiran 1) dipipet ke dalam tabung reaksi, ditambahkan berturut-turut 4 ml larutan bufer tartrat dan 4 ml larutan Na−fenolat, dikocok dan dibiarkan selama 10 menit. Sebanyak 2 ml natrium hipoklorit 5% ditambahkan kemudian dikocok selama 10 menit. Setelah itu diukur serapannya pada panjang gelombang 630 nm.
Penentuan nitrat dalam contoh
Sebanyak 10 ml ekstrak dan deret standar dipipet ke dalam tabung reaksi dan kemudian diukur serapannya pada panjang gelombang 202 dan 275 nm sebagai koreksi.
Pengolahan data
Pengolahan data dilakukan dengan menggunakan uji beda nilai tengah dua populasi pada dua contoh bebas dengan ragam tidak sama. Bentuk hipotesis untuk kedua kondisi sama. Dengan persamaan sebagai berikut:
1. Ho :μ1−μ2=δ0
2. Hi : μ1−μ2≠δ0
Hal ini menyatakan bahwa bila Ho diterima
maka metode KCl dan CaCl2 dapat dikatakan
tidak berbeda. Sebaliknya bila Ho ditolak
maka metode KCl dan CaCl2 dapat dikatakan
berbeda.
HASIL DAN PEMBAHASAN
Sifat Tanah Awal
5
memiliki sifat tanah agak masam berdasarkan kriteria hasil analisis tanah yang digunakan Pusat Penelitian Tanah (Lampiran 3). Kandungan C organik tinggi, yaitu sebesar 3.32% serta N total yang sedang sebesar 0.33% dengan perbandingan C dan N yang sedang sebesar 12%. Nilai tukar kation (NTK) Ca dan Mg-nya yang rendah, masing-masing 11.6 dan 1.61 me/100 g. Selain itu, kandungan Na dan K juga terbilang rendah, yaitu 0.06 dan 0.29 me/100 g, sehingga dapat dikatakan bahwa tanah tersebut memiliki serapan N yang rendah.
Umumnya, sifat-sifat tanah Andisol Wonosobo, Jawa Tengah kurang begitu baik, dilihat dari nilai pHnya yang agak masam (Tan 1984). Curah hujan dan suhu yang tinggi memungkinkan terjadinya pencucian terhadap basa-basa, sehingga dalam periode relatif pendek menyebabkan reaksi tanah menjadi masam.
Uji Beda Nilai Tengah antara Metode KCl dan CaCl2 pada Penentuan Kadar
Amonium
Nitrogen di dalam tanah dapat dilihat dari perilaku perubahan NH4
+
yang terjadi lebih cepat karena sifatnya yang lebih kering dan memacu laju proses oksida menjadi NO3
-(Sibuea 1993). Hal ini kemudian diuji menggunakan dua metode, yaitu KCl dan CaCl2. Data yang diperoleh menunjukkan
bahwa penentuan amonium menggunakan metode KCl dan CaCl2 memiliki nilai
hipotesis yang mendukung untuk menolak Ho.
Hipotesis ini dinyatakan dengan menggunakan uji beda nilai tengah pada dua contoh bebas yang terlihat pada Lampiran 4.
Lampiran 4 menyajikan nilai uji t-hitung pada perhitungan statistik yang menyatakan bahwa kedua metode berbeda, dengan kata lain metode CaCl2 tidak dapat menggantikan
penentuan kadar amonium karena nilai p yaitu 5.80 Χ 10-6 jauh lebih kecil dari nilai α, yaitu 0.05 sehingga mendukung untuk menolak Ho
dan menerima Hi.
Uji Beda Nilai Tengah antara Metode KCl dan CaCl2 pada Penentuan Kadar Nitrat
Penentuan kadar nitrat mengunakan metode KCl dan CaCl2 cukup berbeda.
Perbedaan ini terlihat dari efisiensi penggunaan pereaksi, baik dari KCl maupun CaCl2. Pada metode KCl digunakan pereaksi
yang cukup banyak dan tidak efisien bila dibandingkan dengan CaCl2. Pereaksi KCl
yang digunakan, yaitu brusin dan H2SO4 pekat
sedangkan pada CaCl2 tidak menggunakan
brusin dan H2SO4 pekat sehingga penentuan
kadar nitrat lebih efisien menggunakan metode CaCl2. Hasil pengujian kadar nitrat
menggunakan metode KCl dan CaCl2 pada uji
nilai beda tengah menunjukkan bahwa penentuan kadar nitrat pada metode KCl dan CaCl2 tidak berbeda, sehingga metode CaCl2
pada penentuan nitrat dapat digunakan sebagai pengganti metode KCl. Hasil ini dapat terlihat pada Lampiran 4.
Lampiran 4 menyajikan nilai uji t-hitung dan nilai p dengan menggunakan perhitungan statistik. Hasil ini menyatakan bahwa kedua metode tidak berbeda dengan kata lain bahwa metode CaCl2 dapat menggantikan penentuan
kadar nitrat karena nilai p yaitu 0.25jauh lebih besar dari nilai α yaitu 0.05 sehingga mendukung untuk tidak menolak Ho.
Dosis Petani dan Introduksi
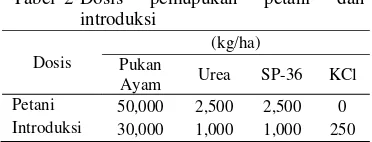
Penggunaan pupuk yang digunakan oleh petani tidaklah sama dengan pupuk yang digunakan pada introduksi. Tabel 2 menunjukkan dosis pemupukan oleh petani dan dosis introduksi yang telah direkomendasikan dari penelitian sebelumnya.
Tabel 2 Dosis pemupukan petani dan introduksi
Dosis
(kg/ha) Pukan
Ayam Urea SP-36 KCl
Petani 50,000 2,500 2,500 0
Introduksi 30,000 1,000 1,000 250
Dosis pemupukan yang digunakan oleh petani dan introduksi cukup berbeda jauh. Terlihat bahwa petani menggunakan pupuk yang cukup banyak dibandingkan dengan introduksi. Umumnya petani menggunakan dosis ini agar hasil yang didapatkan lebih baik. Namun, penggunaan pupuk yang berlebih dapat menimbulkan pencemaran terhadap lingkungan. Khususnya pada air karena salah satu senyawa nitrogen yaitu nitrat dapat tercuci di dalam air. Pencucian nitrat merupakan masalah pencemaran yang potensial terjadi pada air permukaan dan air bawah tanah (Bonh et al. 1979).
6
adalah dengan menghitung komponen kadar N di setiap tanah dan pupuk yang digunakan hingga dihasilkan dosis pupuk introduksi. Adapun kadar N pada dosis petani dan introduksi terhadap pupuk dan tanaman disajikan pada Tabel 3.
Tabel 3 Kadar N pada pupuk dan tanaman
Dosis
Kadar N (kg/ha) Pukan Ayam (a) Urea (b) Total
(a + b) Tanaman
Petani 595 1125 1720 289
Introduksi 357 450 807 289
Tabel 3 menunjukkan bahwa kadar N yang tersedia pada dosis petani sangat tinggi dibandingkan pada dosis introduksi. Data kadar N pada pupuk yang didapat dari perhitungan jumlah kadar N yang tersedia dalam pupuk sedangkan data nilai kadar N yang diserap oleh tanaman baik dosis petani maupun dosis introduksi didapatkan dari puslittanak. Hasil ini menunjukkan bahwa penggunaan pupuk yang berlebihan atau tidak berlebihan memiliki jumlah kadar N yang diserap tanaman relatif sama. Dosis introduksi merupakan rekomendasi efisiensi N pada tingkat 50% dari dosis petani yang berdasarkan pada penelitian sebelumnya.
Pola Distribusi Kadar Amonium
Gambar 2 menyajikan hasil analisis penentuan amonium menggunakan dosis petani sementara pada Gambar 3 menyajikan hasil analisis penentuan kadar amonium pada dosis introduksi. Kadar amonium pada dosis introduksi merupakan hasil penggunaan pupuk rekomendasi efisiensi 50% dari dosis petani. Kadar amonium pada dosis petani dan dosis introduksi di dalam tanah dipengaruhi oleh beberapa faktor diantaranya proses dekomposisi (Soepardi 1996). Kadar amonium pada dosis petani dan introduksi, yakni pada minggu ke−0 dan ke−6 di kedalaman 0−25 cm hampir sama, begitu pula pada minggu ke−3 dan ke−9 di kedalaman 0−25 cm menunjukkan kadar amonium yang relatif sama, yaitu berada disekitar 4−7 ppm NO3− (Gambar 2 dan 3). Kadar amonium pada
dosis petani dan introduksi secara keseluruhan pada minggu ke−0 sampai ke−9 pada kedalaman 0−100 cm, menunjukkan terjadinya proses dekomposisi (Soepardi
1996). Terlihat dengan kadar amonium yang fluktuatif. 0 20 40 60 80 100
0 2 4 6 8
Kadar amonium (ppm)
Ke da la m a n ( c m ) Minggu 0 Minggu 3 Minggu 6 Minggu 9
Gambar 2 Kadar amonium pada berbagai kedalaman tanah dengan dosis petani 0 20 40 60 80 100
0 2 4 6 8
Kadar amonium (ppm)
Ke da la m a n ( c m ) Minggu 0 Minggu 3 Minggu 6 Minggu 9
Gambar 3 Kadar amonium pada berbagai kedalaman tanah dengan dosis introduksi
Proses dekomposisi yang terjadi yaitu amonifikasi dan nitrifikasi. Amonifikasi di dalam tanah merubah asam amino menjadi amonium. Hal ini menyebabkan kadar amonium di dalam tanah meningkat sedangkan proses nitrifikasi dapat menyebabkan kadar amonium menurun karena terjadi tranformasi amonium menjadi nitrat (Soepardi 1996). Nitrifikasi di dalam tanah dibantu oleh bakteri. Perubahan nitrit dilakukan oleh bakteri nitrosomonas yang tergolong dalam bakteri obligat outotrop, sedangkan perubahan nitrit menjadi nitrat dilakukan oleh golongan bakteri obligat autotrop yang lain yaitu nitrobakteri.
7
Pola Distribusi Kadar Nitrat
Gambar 4 menyajikan hasil analisis penentuan nitrat menggunakan dosis petani sementara pada Gambar 5 menyajikan hasil analisis penentuan kadar nitrat pada dosis introduksi. Nitrat di dalam tanah bersifat mobil dibandingkan amonium (Tisdale et al.
1985) sehingga nilai kadar nitrat pada dosis petani dan introduksi berbeda. Kadar nitrat pada dosis petani terlihat lebih besar dibandingkan dengan kadar nitrat pada dosis introduksi, yakni pada minggu ke−9 di kedalaman 50-100 cm (Gambar 4 dan 5).
0 20 40 60 80 100
0 50 100 150 200 250 300 Kadar nitrat (ppm )
K e d a la ma n ( c
m) Minggu 0
Minggu 3
Minggu 6
Minggu 9
Gambar 4 Kadar nitrat pada berbagai kedalaman tanah dengan dosis petani 0 20 40 60 80 100
0 50 100 150 200 250 300
Kadar nitrat (ppm)
K e d a la ma n ( c
m) Minggu 0
Minggu 3
Minggu 6
Minggu 9
Gambar 5 Kadar nitrat pada berbagai kedalaman tanah dengan dosis introduksi.
Terlihat juga bahwa kadar nitrat pada dosis petani pada minggu ke−0 dari kedalaman 0−100 cm menunjukan nilai yang fluktuasi. Pada kedalaman 50−75 cm tertinggi dibandingkan dengan kedalaman yang lainnya. Kadar nitrat tertinggi ini disebabkan pada kedalaman tersebut nitrat tercuci dari kedalaman 0−50 cm serta terjadinya perubahan nitrifikasi yang cukup besar dibandingkan dengan kedalaman lain. Begitu pula pada minggu ke−3 kadar nitrat tertinggi
terdapat pada kedalaman 50−75 cm. Kadar nitrat minggu ke−6 menurun dibandingkan dengan minggu ke−3 dan meningkat pada kedalaman 75−100 cm. Hal ini disebabkan kondisi nitrat di dalam tanah tersebut meningkat dari nitrat yang tercuci dan proses nitrifikasi yang besar. Pada minggu ke−9 kadar nitrat mulai semakin meningkat dari kedalaman 25−100 cm. Hal ini terlihat bahwa penggunaan dosis yang digunakan oleh petani cenderung lebih banyak yang tercuci di minggu ke−9 dibandingkan pada dosis introduksi.
Kadar nitrat pada dosis introduksi, yakni pada minggu ke−0 tertinggi terdapat pada kedalaman 50−75 cm. Hal ini dimungkinkan pada kedalaman tanah tersebut terjadi nitrifikasi yang cukup besar, sedangkan kadar nitrat minggu ke−3 pada kedalam 75−100 cm merupakan kadar tertinggi. Dapat diketahui bahwa terjadi peningkatan nitrat karena nitrat bersifat mobil yang biasanya tercuci (Tisdale
et al. 1985) di dalam tanah. Namun, kadar nitrat pada minggu ke−6 dan ke−9 cenderung menurun dari kedalaman 25−100 cm. Hal ini memperlihatkan bahwa kadar nitrat di dalam tanah hampir sebagian besar terserap oleh tanaman dan hanya sebagian kecil yang tercuci di dalam tanah. Terkait dengan penggunaaan dosis introduksi yang merupakan rekomendasi efisiensi 50% dari dosis petani.
Secara keseluruhan bahwa kadar nitrat pada dosis petani lebih besar dibandingkan pada dosis introduksi. Kadar nitrat juga dipengaruhi oleh proses dekomposisi di dalam tanah, sehingga nilai kadar nitratnya fluktuatif (Soepardi 1996). Kadar nitrat pada dosis introduksi memungkinkan tidak terjadi pencemaran lingkungan karena kadar nitrat yang dihasilkan cenderung tidak tercuci di dalam tanah dibandingkan dengan kadar nitrat pada dosis petani serta penggunaan dosis introduksi yang sedikit dibandingkan dengan dosis petani.
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian dapat disimpulkan bahwa metode CaCl2 berbeda
dengan metode KCl pada penentuan amonium sementara pada penentuan nitrat tidak berbeda sehingga metode CaCl2 dapat digunakan pada
8
petani hampir sama dengan dosis introduksi, yaitu 4−7 ppm. Kadar nitrat pada dosis petani lebih besar dibandingkan dengan dosis introduksi.
Saran
Untuk mengetahuinya secara terperinci, metode CaCl2 dapat digunakan untuk
pengamatan pada jenis tanah yang berbeda dengan ragam dosis pupuk.
DAFTAR PUSTAKA
Anonim. 1997. Kriteria Kesesuaian Tanah dan Iklim Tanaman Pertanian. Jakarta: Departemen Pertanian.
Ashari S. 1995. Hortikultura, Aspek, dan Budidaya. Jakarta: UI Pr. hlm 89-90.
Bockman OC, Kaarstad O, Lie OH, Richard I. 1990. Agriculture and Fertilizers. Oslo-Norway: Agriculture Group.
Bonh HL, McNeal BL, O’Connor GA. 1979.
Soil Chemistry. New York: J Wiley
Darmawijaya. 1990. Klasifikasi Tanah.
Yogyakarta: University Gajah Mada Pr.
Day RA, Underwood AL. 1989. Analisis Kimia Kuantitatif. Ed ke-5. Jakarta: Erlangga.
Douglas JS. 1985. Advanced Guide to Hydroponics. London: Pelhman Books. hlm 333.
Goldman E, Jacobs R. 1991. Determination of nitrates by ultraviolet absorption. J.Amer. Water Works Assoc. 53:187
Hakim N. 1986. Dasar-Dasar Ilmu Tanah
(Terjemahan). Yogyakarta: Gajah Mada University Pr.
Hardjowigeno S. 2003. Ilmu Tanah. Jakarta: Akademika Pressindo.
Harjadi SS, Sunaryono H. 1989. Dasar-dasar
Hortikultura. Bogor: Fakultas
Pertanian, IPB. hlm 506.
Harjadi W. 1993. Ilmu kimia Analitik Dasar. Jakarta: Gramedia Pustaka Utama.
Hidayat A, Fujimoto T, Ismunadji M. 1984. Perilaku nitrogen pada tanah kering.
Penelitian Pertanian 4(1):35-40.
Khopkar SM. 2003. Konsep Dasar Kimia Analitik. Jakarta: UI Pr.
Leiwakabessy FM, Sutandi A. 1998. Pupuk dan Pemupukan. Bogor: Fakultas Pertanian., IPB
Ponnamperuma FA. 1976. Spesific Soil Chemical Characteristic of Rice
Production in Asia. IRRI.
Resh HM. 1983. Hydroponic Food Production. Ed ke-2. California: Woodbridge Pr. hlm 335.
Sanchez FA. 1976. Properties and Management of Soils in the Tropics. New York: J Wiley.
Sibuea LH. 1993. Pengaruh suhu dan lenggas tanah terhadap ketersediaan dan serapan hara serta hasil tanaman pada tiga jenis tanah sawah. [tesis]. Bogor: Fakultas Pertanian, IPB.
Soepardi G. 1996. Sifat dan Ciri Tanah. Bogor: Fakultas Pertanian, IPB.
Tan KH. 1984. Andosols. Georgia: Benchmark Book Van Nostrand
Tan KH. 1991. Dasar-dasar Kimia Tanah. Didiek HG, Penerjemah. Yogyakarta: Gajah Mada University Pr.
Tejoyuwono N. 1998. Tanah dan Lingkungan.
Jakarta: Direktorat Jendral Pendidikan Tinggi Departemen Pendidikan dan Kebudayaan.
Tisdale SL, Nelson WL, Beaton JD. 1985.
Soil Fertility and Fertilizers. New York: Macmillan
10
Lampiran 1 Pembuatan pereaksi
Ekstrak KCl 1 N : Sebanyak 74.55 g kristal KCl dilarutkan k edalam labu berukuran 1 liter dengan air bebas ion hingga homogen.
Standar pokok 1000 ppm NH4+: Sebanyak 4.7143 g serbuk (NH4)2SO4 pekat (kering 105 oC)
dilarutkan ke dalam labu ukur 1 liter dengan air bebas ion hingga homogen.
Standar 20 ppm NH4 +
dalam KCl 1 N: Sebanyak 2 ml standar pokok 1000 ppm NH4 +
dipipet ke dalam labu ukur 100 ml dan diencerkan dengan ekstrak KCl 1 N hingga tanda tera.
Larutan brusin 2% : Sebanyak 2 g brusin dilarutkan dengan 100 ml air bebas ion hingga homogen.
Standar pokok 1000 ppm NO3−-: Sebanyak 1.6290 g serbuk KNO3 pekat dilarutkan ke dalam
labu 1 liter dengan air bebas ion hingga homogen.
Standar pokok 50 ppm NO3 −
: Sebanyak 5 ml standar 1000 ppm NO3
−
dipipet kedalam labu ukur 100 ml dengan air bebas ion hingga homogen.
Standar pokok 5 ppm NO3 −-
dalam KCl 1 N : Sebanyak 10 ml standar 50 ppm NO3
−
dipipet ke dalam labu ukur 100 ml kemudian diencerkan dengan pengekstrak KCl 1 N hingga tanda tera.
Ekstrak CaCl2 0.01 M : Sebanyak 1.48 g CaCl2 dilarutkan kedalam labu ukur 1 liter dengan air
bebas ion sampai tanda tera
Standar pokok 1000 ppm NH4+ : Sebanyak 4.7143 g serbuk (NH4)2SO4 pekat (kering 105 o
C) dilarutkan ke dalam labu ukur 1 liter dengan air bebas ion hingga tanda tera.
Standar pokok 20 ppm NH4 +
: Sebanyak 2 ml standar pokok 1000 ppm dipipet ke dalam labu ukur 100 ml dengan ekstrak CaCl2 0.01 M hingga tanda tera.
Standar pokok 1000 ppm NO3−- : Sebanyak 1.6290 g serbuk KNO3 pekat dilarutkan ke dalam
labu 1 liter dengan air bebas ion hingga homogen
Standar pokok 50 ppm NO3−- : Sebanyak 5 ml standar 1000 ppm NO3−- dipipet ke dalam labu
ukur 100 ml dengan air bebas ion hingga homogen.
Standar pokok 5 ppm NO3
dalam CaCl2 0.01 M : Sebanyak 10 ml standar 50 ppm NO3
dipipet ke dalam labu ukur 100 ml dengan pengekstrak CaCl2 0.01 M hingga tanda tera.
Deret standar amonium pada KCl
Penetapan nitrat dilakukan pembuatan deret standar (0−20 ppm N−NH4 +
). Standar 20 ppm N−NH4+ dalam KCl 1 N dipipet 0; 0.1; 0.2; 0.4; 0.6; 0.8; dan 1 ml ke dalam tabung reaksi
kemudian ditambahkan ekstrak KCl 1 N hingga menjadi 1 ml. Deret standar ini memiliki kepekatan 0, 2, 4, 6, 8, 12, 16, dan 20 ppm N−NH4
+
. Kemudian deret standar ini ditambahkan 2 ml larutan sangga tartrat dan 2 ml larutan Na-fenolat, kocok dan biarkan selama 10 menit. Tambahkan 1 ml natrium hipoklorit 5% kemudian kocok selama 10 menit setelah itu diukur serapannya pada panjang gelombang 630 nm.
Deret standar nitrat pada KCl
Penetapan nitrat dilakukan pembuatan deret standar (0−5 ppm N−NO3−-). Standar 5 ppm
NO3−- dalam KCl 1 N dipipet 0; 0.5; 1; 2; 3; 4; dan 5 ml kedalam tabung reaksi kemudian
ditambahkan dengan penambahan ekstrak CaCl2 hingga volumenya 5 ml. Deret standar ini
memiliki kepekatan 0, 0.5, 1, 2, 3, 4, 5 ppm NO3
−
-. Kemudian deret standar ini ditambahkan 0,5 ml brusin 2% dan 5 ml H2SO4 pekat sambil dikocok kemudian dibiarkan selama 30 menit hingga
11
Deret standar amonium pada CaCl2
Penetapan nitrat dilakukan pembuatan deret standar (0−-20 ppm N-NH4+). Standar 20 ppm
N-NH4+ dalam CaCl2 0.01 M dipipet 0, 1, 2, 4, 6, 8, dan 10 ml kedalam tabung reaksi kemudian
ditambahkan estrak CaCl2 0.01 M hingga menjadi 10 ml hingga homogen. Deret standar ini
memiliki kepekatan 0, 2, 4, 6, 8, 12, 16, dan 20 ppm N-NH4 +
. Kemudian deret standar ini ditambahkan 4 ml larutan sangga tartrat dan 4 ml larutan Na−fenolat, kocok dan biarkan selama 10 menit. Tambahkan 2 ml natrium hipoklorit 5% kemudian kocok selama 10 menit setelah itu diukur serapannya pada panjang gelombang 630 nm.
Deret standar nitrat pada CaCl2
Penetapan nitrat dilakukan pembuatan deret standar (0−5 ppm N−NO3−-). Standar 5 ppm
NO3
−
dipipet 0, 1, 2, 4, 6, 8, dan 10 ml kedalam tabung reaksi kemudian ditambahkan dengan penambahan ekstrak CaCl2 hingga volumenya 10 ml hingga homogen. Deret standar ini memiliki
kepekatan 0, 0.5, 1, 2, 3, 4, 5 ppm NO3−-. Kemudian diukur serapannya pada panjang gelombang
202 nm dan 275 nm sebagai koreksi.
Pereaksi 1 dan 2 pada KCl
Pereaksi 1 (larutan bufer tartrat) yaitu 50 g NaOH dilarutkan 500 ml air bebas ion secara perlahan-lahan ke dalam labu ukur 1000 ml kemudian ditambahkan 50 g serbuk K−Na tartrat dan air bebas ion sampai tanda tera. Pereaksi 2 (larutan fenolat), yaitu sebanyak 36 g serbuk NaOH ditambahkan perlahan-lahan dengan 500 ml air bebas ion ke dalam labu ukur ukur 1 liter, kemudian ditambahkan 82 g fenol dan air bebas ion sampai tanda tera.
Pereaksi 1 dan 2 pada CaCl2
12
Lampiran 2 Pembagian kelas tekstur tanah
Keterangan gambar:
1. Pasir 7. Lempung liat berpasir
2. Pasir berlempung 8. Lempung berliat
3. Lempung berpasir 9. Lempung liat berdebu
4. Lempung 10. Liat berpasir
5. Lempung berdebu 11. Liat berdebu
13
Lampiran 3 Kriteria penilaian sifat-sifat tanah (Pusat Penelitian Tanah 2005)
Jenis Analisis Nilai
Sangat rendah Rendah Sedang Tinggi Sangat tinggi C organik (%) < 1.00 1−2.0 2.01−3 3.01−5 > 5 N Total (%) < 0.1 0.1−0.2 0.21−0.5 0.51−0.75 > 0.75 C/N < 5 5−10 11−15 16−25 > 25 P2O5 HCl 25% (mg/100 g) < 15 15−20 21−40 41−60 > 60
P2O5 Bray I (ppm) < 4 5−7 8−10 11−15 > 15
P2O5 Olsen (ppm) < 5 5−10 11−15 16−20 > 20
K2O HCl 25% < 10 10−20 21−40 41−60 > 60
KTK (me/100 g) < 5 5−16 17−24 25−40 > 40 Susunan kation (me/100 g)
Ca < 2 2−5 6−10 11−20 > 20 Mg < 0.4 0.4−1.0 1.1−2.0 2.1−8.0 > 8 K < 0.1 0.1−0.3 0.4−0.5 0.6−1.0 > 1 Na < 0.1 0.1−0.3 0.4−0.7 0.8−1.0 > 1 KB (%) < 20 20−40 41−60 61−80 > 80 Kemasaman
Al (me/100 g) < 5 5−10 11−20 20−40 > 40
Sangat
masam Masam
Agak
14
Lampiran 4 Perhitungan statistik dengan uji beda nilai tengah antara metode KCl dan CaCl2
Ulangan 1 Amonium Ulangan 1 Nitrat
t-Test: Paired Two Sampel for Means t-Test: Paired Two Sampel for Means
KCl CaCl2 KCl CaCl2
Mean 14.590513 5.0950482 Mean 184.77351 145.16161 Variance 46.230749 0.9467646 Variance 39353.507 11118.571
Observations 32 32 Observations 32 32 Pearson Correlation 0.4526068 Pearson Correlation 0.1344753
Hypothesized Mean
Difference 0
Hypothesized Mean
Difference 0
df 31 df 31
t Stat 8.3695465 t Stat 1.058127 P(T<=t) one-tail 9.36E-10 P(T<=t) one-tail 0.1490867 t Critical one-tail 1.6955187 t Critical one-tail 1.6955187 P(T<=t) two-tail 1.87E-09 P(T<=t) two-tail 0.2981735 t Critical two-tail 2.0395134 t Critical two-tail 2.0395134
Ulangan 2 Amonium Ulangan 2 Nitrat
t-Test: Paired Two Sampel for Means t-Test: Paired Two Sampel for Means
KCl CaCl2 KCl CaCl2
Mean 9.7784655 4.6824854 Mean 131.49923 201.09962 Variance 10.595771 1.2438151 Variance 11739.846 93038.438 Observations 32 32 Observations 32 32
Pearson Correlation 0.504228 Pearson Correlation
-0.0683081 Hypothesized Mean
Difference 0
Hypothesized Mean
Difference 0
df 31 df 31
t Stat 10.080079 t Stat
-1.1909397 P(T<=t) one-tail 1.32E-11 P(T<=t) one-tail 0.1213583 t Critical one-tail 1.6955187 t Critical one-tail 1.6955187 P(T<=t) two-tail 2.65E-11 P(T<=t) two-tail 0.2427167 t Critical two-tail 2.0395134 t Critical two-tail 2.0395134
Ulangan 3 Amonium Ulangan 3 Nitrat
t-Test: Paired Two Sampel for Means t-Test: Paired Two Sampel for Means
KCl CaCl2 KCl CaCl2
Mean 9.121828 5.0950482 Mean 159.45148 126.19657 Variance 19.847385 0.9467646 Variance 16361.034 5193.9514 Observations 32 32 Observations 32 32 Pearson Correlation 0.2284405 Pearson Correlation -0.238514
Hypothesized Mean
Difference 0
Hypothesized Mean
Difference 0
df 31 df 31
15
Lampiran 5 Kurva standar amonium dan nitrat pada dua metode
Ulangan 1 Amonium pada metode CaCl2 Ulangan 2 Amonium pada metode CaCl2
y = 69.071x - 112.71
R2 = 0.9591
-100 0 100 200 300 400 500
0 2 4 8 12 16 20
Kadar am onium (ppm )
A
b
so
rb
an
y = 21.919x - 9.4249
R2 = 0.9983
-100 0 100 200 300 400 500
0 5 10 15 20 25
Kadar am onium (ppm )
Ab s o rb a n
Ulangan 1 Nitrat pada metode CaCl2 Ulangan 2 Nitrat pada metode CaCl2
y = 138.57x - 15.27
R2 = 0.9939
-200 0 200 400 600 800
0 2 4 6
Kadar nitrat (ppm )
A
b
so
rb
an
y = 136.49x - 28.224
R2 = 0.9927
-200 0 200 400 600 800
0 2 4 6
Kadar am onium (ppm )
Ab s o rb a n
Ulangan 1 Amonium pada metode KCl Ulangan 2 Amonium pada metode KCl
y = 8.4147x - 4.8157
R2 = 0.9973
-50 0 50 100 150 200
0 5 10 15 20 25
Kadar Amonium (ppm)
A
b
s
o
rban
y = 8.192x - 4.4147 R2 = 0.9951
-50 0 50 100 150 200
0 5 10 15 20 25
Kadar am onium (ppm )
Ab
so
rb
an
Ulangan 1 Nitrat pada metode KCl Ulangan 2 Nitrat pada metode KCl
y = 122.02x - 9.0529 R2 = 0.9941
-100 0 100 200 300 400 500 600 700
0 2 4 6
Kadar nitrat (ppm )
Ab s o rb a n
y = 124.43x + 12.048 R2 = 0.9813
0 200 400 600 800
0 2 4 6
Kadar nitrat (ppm )
Ab
so
rb
16
Lanjutan lampiran 5
Ulangan 3 Amonium pada metode CaCl2
y = 20.469x - 13.014
R2 = 0.996
-100 0 100 200 300 400 500
0 5 10 15 20 25
Kadar am onium (ppm )
A
b
so
rb
an
Ulangan 3 Nitrat pada metode CaCl2
y = 140.22x - 2.198 R2 = 0.9988
-200 0 200 400 600 800
0 1 2 3 4 5 6
Kadar nitrat (ppm )
Ab
s
o
rb
a
n
Ulangan 3 Amonium pada metode KCl
y = 6.5026x - 3.1655 R2 = 0.9973
-20 0 20 40 60 80 100 120 140
0 5 10 15 20 25
Kadar am onium (ppm )
Ab
s
o
rb
a
n
Ulangan 3 Nitrat pada metode KCl
y = 121.55x - 26.995
R2 = 0.9708
-200 0 200 400 600 800
0 1 2 3 4 5 6
Kadar nitrat (ppm)
A
b
so
rb
17
Lampiran 6 Diagram alir penelitian
Contoh sampel tanah (0−25, 25−50, 50−75, 75−100 cm)
Ekstrak KCl 1 N Ekstrak CaCl2 0.01 M
Analisis NH4
+ Analisis
NH4+
Analisis NO3
− Analisis NO
18
Lampiran 7 Contoh perhitungan
Kadar air (%) = a − b Χ 100% b
Faktor koreksi (fk) = (100 + kadar air) 100
Kadar NH4 +
(ppm) = ppm standar Χ ml ekstrak Χ fk gram contoh
Kadar NO3−-(ppm) = ppm standar Χ ml ekstrak Χ fk Χ fp
gram contoh
ppm standar = Absorban – Intersept kemiringan
Keterangan :
Persamaan kurva standar: y = a + bΧ
Dari persamaan a = Intersept sumbu Χ
b = kemiringan kurva
a = Bobot bahan sebelum dikeringkan
b = Bobot bahan setelah dikeringkan
fk = Faktor koreksi
Lampiran 8 Data analisis penentuan amonium pada metode KCl 1 N (Ulangan 1)
Minggu Dosis Kedalaman
(cm) A Kemiringan Intersep ppm standar
Bobot kosong cawan (g)
Bobot contoh (g)
Bobot contoh kering + cawan (g)
Bobot contoh kering (g)
Kadar air (%) fka
Kadar NH4+
(ppm)
0
Petani
0-25 10.00 8.4147 -4.8157 1.7607 3.1400 5.0600 6.5200 1.6800 25.7669 1.2577 11.0718 25-50 7.00 8.4147 -4.8157 1.4042 3.1000 5.0600 5.9600 2.2000 36.9128 1.3691 9.6125 50-75 10.00 8.4147 -4.8157 1.7607 3.1400 5.0600 5.2800 2.9200 55.3030 1.5530 13.6720 75-100 35.00 8.4147 -4.8157 4.7317 3.1400 5.0200 5.2400 2.9200 55.7252 1.5573 36.8421
Introduksi
0-25 12.00 8.4147 -4.8157 1.9984 3.1000 5.0400 6.1200 2.0200 33.0065 1.3301 13.2898 25-50 7.00 8.4147 -4.8157 1.4042 3.0800 5.0200 6.3800 1.7200 26.9592 1.2696 8.9136 50-75 11.00 8.4147 -4.8157 1.8795 3.1000 5.0000 5.3600 2.7400 51.1194 1.5112 14.2017 75-100 10.00 8.4147 -4.8157 1.7607 3.1400 5.0200 5.2600 2.9000 55.1331 1.5513 13.6571
3
Petani
0-25 17.00 8.4147 -4.8157 2.5926 3.1000 5.0400 6.3200 1.8200 28.7975 1.2880 16.6958 25-50 18.00 8.4147 -4.8157 2.7114 3.1400 5.0400 6.0200 2.1600 35.8804 1.3588 18.4214 50-75 10.00 8.4147 -4.8157 1.7607 3.1400 5.0000 5.6600 2.4800 43.8163 1.4382 12.6608 75-100 10.00 8.4147 -4.8157 1.7607 3.1400 5.0200 5.5200 2.6400 47.8261 1.4783 13.0138
Introduksi
0-25 8.00 8.4147 -4.8157 1.5230 3.1600 5.0200 6.4600 1.7200 26.6254 1.2663 9.6426 25-50 8.00 8.4147 -4.8157 1.5230 3.1400 5.0400 5.9600 2.2200 37.2483 1.3725 10.4516 50-75 10.00 8.4147 -4.8157 1.7607 3.1000 5.0400 5.7000 2.4400 42.8070 1.4281 12.5720 75-100 11.00 8.4147 -4.8157 1.8795 3.0800 5.0200 5.5200 2.5800 46.7391 1.4674 13.7900
6
Petani
0-25 9.00 8.4147 -4.8157 1.6419 3.1000 5.0400 6.4600 1.6800 26.0062 1.2601 10.3442 25-50 13.00 8.4147 -4.8157 2.1172 3.0800 5.0400 5.9600 2.1600 36.2416 1.3624 14.4226 50-75 2.00 8.4147 -4.8157 0.8100 3.1200 5.0000 5.5000 2.6200 47.6364 1.4764 5.9791 75-100 1.00 8.4147 -4.8157 0.6911 3.1400 5.0200 5.2600 2.9000 55.1331 1.5513 5.3609
Introduksi
0-25 12.00 8.4147 -4.8157 1.9984 3.1000 5.0400 6.4800 1.6600 25.6173 1.2562 12.5515 25-50 4.00 8.4147 -4.8157 1.0477 3.1000 5.0400 6.2000 1.9400 31.2903 1.3129 6.8773 50-75 0.00 8.4147 -4.8157 0.5723 3.0800 5.0400 5.2200 2.9000 55.5556 1.5556 4.4512 75-100 4.00 8.4147 -4.8157 1.0477 3.1200 5.0000 5.3200 2.8000 52.6316 1.5263 7.9953
9
Petani
0-25 9.00 6.5026 -12.3652 3.2856 3.1200 5.0200 6.5800 1.5600 23.7082 1.2371 20.3230 25-50 11.00 6.5026 -12.3652 3.5932 3.0800 5.0400 6.0800 2.0400 33.5526 1.3355 23.9941 50-75 8.00 6.5026 -12.3652 3.1319 3.1600 5.0000 5.7200 2.4400 42.6573 1.4266 22.3391 75-100 10.00 6.5026 -12.3652 3.4394 3.1400 5.0200 5.6400 2.5200 44.6809 1.4468 24.8809
Introduksi
Lampiran 9 Data analisis penentuan amonium pada metode KCl 1 N (Ulangan 2)
Minggu Dosis Kedalaman
(cm) A Kemiringan Intersep ppm standar
Bobot kosong cawan (g)
Bobot contoh (g)
Bobot contoh kering + cawan (g)
Bobot contoh kering (g)
Kadar air (%) fka
Kadar NH4+
(ppm)
0
Petani
0-25 3.00 8.1920 -4.4147 0.9051 3.1400 5.0000 6.5400 1.6000 24.4648 1.2446 5.6327 25-50 4.00 8.1920 -4.4147 1.0272 3.0800 5.0400 5.9800 2.1400 35.7860 1.3579 6.9739 50-75 7.00 8.1920 -4.4147 1.3934 3.1200 5.0200 5.4400 2.7000 49.6324 1.4963 10.4249 75-100 15.00 8.1920 -4.4147 2.3700 3.1400 5.0200 5.2400 2.9200 55.7252 1.5573 18.4531
Introduksi
0-25 9.00 8.1920 -4.4147 1.6375 3.1000 5.0400 6.6400 1.5000 22.5904 1.2259 10.0373 25-50 3.00 8.1920 -4.4147 0.9051 3.0800 5.0200 6.2000 1.9000 30.6452 1.3065 5.9124 50-75 8.00 8.1920 -4.4147 1.5155 3.1000 5.0000 5.5200 2.5800 46.7391 1.4674 11.1189 75-100 4.00 8.1920 -4.4147 1.0272 3.1200 5.0000 5.4600 2.6600 48.7179 1.4872 7.6380
3
Petani
0-25 5.00 8.1920 -4.4147 1.1493 3.1200 5.0400 6.3600 1.8000 28.3019 1.2830 7.3726 25-50 5.00 8.1920 -4.4147 1.1493 3.1400 5.0200 6.1000 2.0600 33.7705 1.3377 7.6868 50-75 9.00 8.1920 -4.4147 1.6375 3.1400 5.0200 5.9000 2.2600 38.3051 1.3831 11.3240 75-100 6.00 8.1920 -4.4147 1.2713 3.1600 5.0200 5.6200 2.5600 45.5516 1.4555 9.2522
Introduksi
0-25 4.00 8.1920 -4.4147 1.0272 3.1600 5.0400 6.7200 1.4800 22.0238 1.2202 6.2671 25-50 5.00 8.1920 -4.4147 1.1493 3.1200 5.0200 6.1000 2.0400 33.4426 1.3344 7.6680 50-75 5.00 8.1920 -4.4147 1.1493 3.1000 5.0000 5.7400 2.3600 41.1150 1.4111 8.1089 75-100 5.00 8.1920 -4.4147 1.1493 3.0600 5.0200 5.6400 2.4400 43.2624 1.4326 8.2323
6
Petani
0-25 10.00 8.1920 -4.4147 1.7596 3.0800 5.0000 6.6000 1.4800 22.4242 1.2242 10.7709 25-50 4.00 8.1920 -4.4147 1.0272 3.0800 5.0200 5.9600 2.1400 35.9060 1.3591 6.9800 50-75 6.00 8.1920 -4.4147 1.2713 3.1200 5.0400 5.7000 2.4600 43.1579 1.4316 9.1000 75-100 5.00 8.1920 -4.4147 1.1493 3.1200 5.0000 5.5200 2.6000 47.1014 1.4710 8.4529
Introduksi
0-25 5.00 8.1920 -4.4147 1.1493 3.1000 5.0000 6.5200 1.5800 24.2331 1.2423 7.1388 25-50 3.00 8.1920 -4.4147 0.9051 3.1200 5.0000 6.2400 1.8800 30.1282 1.3013 5.8890 50-75 4.00 8.1920 -4.4147 1.0272 3.0800 5.0400 5.3800 2.7400 50.9294 1.5093 7.7516 75-100 4.00 8.1920 -4.4147 1.0272 3.1000 5.0000 5.4400 2.6600 48.8971 1.4890 7.6472
9
Petani
0-25 6.00 8.9283 -12.3652 2.0570 3.1400 5.0400 6.5200 1.6600 25.4601 1.2546 12.9034 25-50 6.00 8.9283 -12.3652 2.0570 3.1400 5.0200 6.1200 2.0400 33.3333 1.3333 13.7131 50-75 5.00 8.9283 -12.3652 1.9450 3.1600 5.0000 5.7200 2.4400 42.6573 1.4266 13.8732 75-100 4.00 8.9283 -12.3652 1.8330 3.1800 5.0000 5.6600 2.5200 44.5230 1.4452 13.2452
Introduksi
Lampiran 10 Data analisis penentuan amonium pada metode KCl 1 N (Ulangan 3)
Minggu Dosis Kedalaman
(cm) A Kemiringan Intersep ppm standar
Bobot kosong cawan (g)
Bobot contoh (g)
Bobot contoh kering + cawan (g)
Bobot contoh kering (g)
Kadar air (%) fka
Kadar NH4+
(ppm)
0
Petani
0-25 10.00 6.5026 -3.1655 2.0247 3.1400 5.0400 6.6000 1.5800 23.9394 1.2394 12.5467 25-50 4.00 6.5026 -3.1655 1.1019 3.1000 5.0200 5.9600 2.1600 36.2416 1.3624 7.5065 50-75 5.00 6.5026 -3.1655 1.2557 3.1400 5.0200 5.4800 2.6800 48.9051 1.4891 9.3492 75-100 12.00 6.5026 -3.1655 2.3322 3.1400 5.0200 5.2400 2.9200 55.7252 1.5573 18.1593
Introduksi
0-25 2.00 6.5026 -3.1655 0.7944 3.1000 5.0200 6.6400 1.4800 22.2892 1.2229 4.8572 25-50 4.00 6.5026 -3.1655 1.1019 3.0800 5.0200 6.2600 1.8400 29.3930 1.2939 7.1292 50-75 6.00 6.5026 -3.1655 1.4095 3.0800 5.0000 5.5400 2.5400 45.8484 1.4585 10.2788 75-100 4.00 6.5026 -3.1655 1.1019 3.1400 5.0200 5.4600 2.7000 49.4505 1.4945 8.2343
3
Petani
0-25 6.00 6.5026 -3.1655 1.4095 3.1000 5.0000 6.4200 1.6800 26.1682 1.2617 8.8918 25-50 -2.00 6.5026 -3.1655 0.1792 3.1400 5.0200 5.9800 2.1800 36.4548 1.3645 1.2229 50-75 2.00 6.5026 -3.1655 0.7944 3.1600 5.0200 5.7000 2.4800 43.5088 1.4351 5.7000 75-100 1.00 6.5026 -3.1655 0.6406 3.1600 5.0000 5.7200 2.4400 42.6573 1.4266 4.5692
Introduksi
0-25 5.00 6.5026 -3.1655 1.2557 3.1600 5.0400 6.6000 1.6000 24.2424 1.2424 7.8007 25-50 6.00 6.5026 -3.1655 1.4095 3.1200 5.0000 6.1400 1.9800 32.2476 1.3225 9.3202 50-75 1.00 6.5026 -3.1655 0.6406 3.1200 5.0400 5.6600 2.5000 44.1696 1.4417 4.6177 75-100 -1.00 6.5026 -3.1655 0.3330 3.0800 5.0400 5.7000 2.4200 42.4561 1.4246 2.3720
6
Petani
0-25 2.00 6.5026 -3.1655 0.7944 3.0800 5.0200 6.5000 1.6000 24.6154 1.2462 4.9496 25-50 2.00 6.5026 -3.1655 0.7944 3.0600 5.0200 6.