1. Judul Skripsi : UJI DAYA HAMBAT ISOLAT BAKTERI USUS ITIK (Anas domestica) TERHADAP BAKTERI GRAM POSITIF DAN PERTUMBUHAN ISOLAT BAKTERI USUS ITIK PADA MEDIA MRS BROTH
2. Nama Mahasiswa / NPM : DIAH RAHMAWATI / 0717021030 3. Komisi Pembimbing Skripsi
Pembimbing I : Dra. CN. Ekowati, M.Si Pembimbing II : Dr. Ir. Rudy Sutrisna, M.S Pembahas : Kusuma Handayani, M.Si 4. Jurusan / Prog. Studi : Biologi / S1 Biologi
5. Fakultas : Matematika dan Ilmu Pengetahuan Alam 6. Bidang Keilmuan (a) : Mikrobiologi
7. Abstrak Skripsi (b)
ABSTRAK
UJI DAYA HAMBAT ISOLAT BAKTERI USUS ITIK (Anas domestica) PADA BAKTERI GRAM POSITIF DAN POLA PERTUMBUHAN ISOLAT BAKTERI USUS ITIK PADA
MEDIA MRS BROTH
Oleh Diah Rahmawati
Telah diketahui bahwa 13 isolat bakteri yang berasal dari usus itik diduga bakteri Lactobacillus dapat menghambat pertumbuhan bakteri patogen Gram negatif Salmonella pullorum. Tetapi saat ini belum diketahui kemampuan daya hambat isolat bakteri usus itik tersebut terhadap bakteri Gram positif antara lain Bacillus subtilis dan Staphylococcus aureus. Selain itu, juga belum diketahui pola pertumbuhan isolat bakteri tersebut pada media tumbuh MRS Broth. Penelitian ini bertujuan untuk mengetahui daya hambat ekstrak antibakteri isolat bakteri usus itik terhadap bakteri Gram positif dan mengetahui pola pertumbuhan isolat bakteri usus itik yang terpilih pada media MRS Broth.
Penentuan uji daya hambat isolat bakteri usus itik dengan menggunakan metode sumuran, sedangkan untuk penentuan pola pertumbuhan isolat bakteri usus itik dengan menghitung langsung jumlah sel bakteri secara mikroskopis.
Hasil penelitian menunjukkan bahwa isolat bakteri usus itik mampu menghambat pertumbuhan bakteri Gram positif. Isolat yang menghasilkan diameter terbesar dari hasil penelitian ini yaitu isolat B4 dan B9 sebesar 20,2 mm dan 17,9 mm dengan lama waktu produksi 4 hari. Pertumbuhan isolat bakteri usus itik B4 menunjukkan fase lag selama 2 jam dan fase logaritmik selama 17 jam,
sedangkan isobat B9 menunjukkan fase lag selama 3 jam dan fase logaritmik selama 10 jam.
Kata Kunci (c) : Isolat bakteri asam laktat, karakterisasi, antibakteri, Escherichia coli, Salmonella pullorum.
(a) bidang keilmuan diisi sesuai dengan konsentrasi bidang ilmu skripsi (b) abstrak diisi sesuai dengan yang tercantum diskripsi. Minimal 500 kata.
(c) kata kunci diisi kata-kata yang berhubungan dengan abstrak skripsi. Minimal 5 kata kunci.
ABSTRAK SKRIPSI MAHASISWA
UJI DAYA HAMBAT ISOLAT BAKTERI USUS ITIK
(
Anas domestica
) TERHADAP BAKTERI GRAM POSITIF
DAN PERTUMBUHAN ISOLAT BAKTERI USUS ITIK
PADA MEDIA MRS
BROTH
(Skripsi)
Oleh :
Diah Rahmawati
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
I. PENDAHULUAN
A. Latar Belakang
Dalam saluran pencernaan unggas khususnya sekum dan tembolok, terdapat
populasi mikrobia dengan berbagai ukuran dan kompleksitas. Bakteri
tersebut umumnya bersifat fermentatif. Jumlah bakteri pada sekum sebanyak
109/g isi sekum, dan bakteri yang mendominasi adalah E. coli, Sterptococci
sp, dan Lactobacilli sp. Bakteri tersebut mampu berkembang dalam sekum karena pH dan temperatur sekum mendukung perkembangan bakteri secara
baik (Gabriel et al., 2006).
Saluran pencernaan unggas merupakan tempat hidup bagi mikroflora yang
segera dibentuk setelah dilahirkan. Mikroflora indigenous dewasa akan
menjadi barrier (pembawa) koloni mikroorganisme patogen seperti
Salmonella dan E. coli sedangkan mikroflora yang menyokong kesehatan unggas terdiri dari berbagai macam spesies mikroorganisme seperti
Lactobaccilus, Bifidobacterium dan Bacteroides yang sebagian besar merupakan mikroorganisme yang predominan. Penggunaan probiotik dapat
mempengaruhi keberhasilan produksi mikroflora kompetitif dalam
2
Fuller (1991) menjelaskan bahwa bakteri probiotik harus memiliki
persyaratan yaitu memberikan efek yang menguntungkan pada host, tidak
patogenik dan tidak toksik. Disamping itu mengandung sejumlah besar sel
hidup, mampu bertahan dalam kondisi yang tidak menguntungkan dan
melakukan kegiatan metabolisme dalam usus. Persyaratan lain adalah dapat
tetap hidup selama dalam penyimpanan sampai waktu digunakan,
mempunyai sifat sensori yang baik, dan diisolasi dari host. Salah satu kelompok bakteri yang mampu menghambat bakteri patogen dan
dimanfaatkan sebagai probiotik yaitu Lactobacillus. Beberapa Lactobacillus
yang biasa dijadikan sebagai probiotik antara lain Lactobacillus casei, L. acidophilus, L. casei Shirota, Lactobacillus GG, dan L. plantarum 299 (Young, 1998).
Napitupulu(2000) melaporkan bahwa Lactobacillus menghasilkan
antibakteri. Filtrat Lactobacillus dapat menghambat pertumbuhan bakteri patogen Gram positif antara lain Streptococcus dan Staphylococcus aureus
serta bakteri Gram negatif seperti Escerchia coli. Pada penelitian Abun (2008) diketahui bahwa Lactobacillus yang terdapat dalam usus ayam broiler dapat menghambat kolonisasi bakteri Gram negatif Salmonella
Berdasarkan penelitian Sutrisna dan Nurjanah (2010) telah ditemukan 20
isolat bakteri usus itik yang memiliki beberapa karakterisasi, diantaranya
adalah berbentuk batang, tidak berspora, Gram positif, bersifat motil. Selain
3
bakteri tersebut diduga merupakan Lactobacillus. Sebanyak 20 isolat, 13 diantaranya merupakan isolat yang dapat menghambat bakteri Gram negatif
Salmonella pullorum. Ketiga belas bakteri tersebut adalah : B1 : Isolat usus itik “Bulat Besar” (CI BB)
B2 : Isolat usus itik “Besar Kuning” (CI BK)
B3 : Isolat usus itik “Kecil Kuning” (CI KCK)
B4 : Isolat usus itik “Kecil Pipih” (CI KP)
B5 : Isolat usus itik “Kuning Kecil Pipih” (CI KKP)
B6 : Isolat usus itik “ Kecil Pipih Kuning” (CI KPK)
B7 : Isolat usus itik “ Pipih Kecil” (CI PKC)
B8 : Isolat usus itik “Putih Sedang Bulat” (CI PTSBL)
B9 : Isolat usus itik “Sangat Kecil Pipih” (CI SGKP)
B10 : Isolat usus itik “Tak Beraturan Besar” (CI TBRB)
B11 : Isolat usus itik “ Besar Bulat” (JK BSRBLT)
B12 : Isolat usus itik “Kecil Bulat” (JK KCLBLT)
B13 : Isolat usus itik “Tak Beraturan Besar” (JK TBRBSR)
Isolatbakteri usus itik mampu menghambat bakteri Gram negatif Salmonella pullorum namun kemampuan menghambat isolat bakteri usus itik terhadap bakteri patogen Gram positif belum jelas. Selain itu perlu dikaji lebih dalam
juga tentang pertumbuhan isolat usus itik dengan media MRS Broth yang diduga media tersebut merupakan media khusus untuk pertumbuhan
4
B. Tujuan Penelitian
Penelitian ini bertujuan untuk:
1. Mengetahui daya hambat ekstrak antibakteri isolat bakteri usus itik
terhadap bakteri Gram positif.
2. Mengetahui perbedaan besarnya diameter daya hambat ekstrak
antibakteri isolat bakteri usus itik terhadap bakteri Gram positif.
3. Mengetahui pola pertumbuhan isolat bakteri usus itik yang terpilih
(terbesar diameter daya hambatnya) pada media MRS Broth.
C. Kerangka Pemikiran
Lactobacillus mempunyai kemampuan untuk menghasilkan bakteriosin (Pridmore et al., 1996). Bakteriosin yang dihasilkan oleh bakteri Gram positif biasanya merupakan polipeptida bermuatan positif yang dapat
menembus membran sel dan tersusun kurang dari 60 residu asam amino.
Bakteriosin merupakan zat antimikroba berupa polipeptida, protein, atau
senyawa yang mirip protein (Kone dan Fung 1992; Jack et al., 1995).
Menurut Nester et al., (2009) mekanisme aksi antimikroba ada 4 cara yaitu dengan menghambat sintesis dinding sel, menghambat sintesis protein,
menghambat sintesis asam nukleat, atau menghambat jalur metabolisme
utama. Bakteriosin mencegah sintesis peptidoglikan yang utuh sehingga
5
Selain itu, bakteriosin yang menyelubungi sel mikroba target akan masuk
melalui membran sel mikroba target menyebabkan ketidakseimbangan fungsi
membran sitoplasma (mempengaruhi sintesa energi dan permeabilitas),
menghambat sintesa asam nukleat, sintesa protein dan mengubah mekanisme
translator sel.
Selain bakteriosin, Lactobacillus juga mampu menghasilkan asam laktat. Efek bakterisidal dari asam laktat berkaitan dengan penurunan pH lingkungan
menjadi 3 sampai 4,5 sehingga pertumbuhan bakteri lain termasuk bakteri
pembusuk akan terhambat. Pada umunya mikroorganisme dapat tumbuh
pada kisaran pH 6-8 (Buckle et al., 1987).
Bakteri asam laktat (Lactobacillus)dapat ditumbuhkan dengan media MRS (deMan et al., 1960). Kandungan yang terdapat dalam media MRS
diantaranya adalah ekstrak daging sapi dan ekstrak ragi sebagai sumber
karbon, nitrogen, dan vitamin. Sodium asetat berperan sebagai agen
penghambatan. Sodium asetat dan amonium sitrat bertindak sebagai selektif
agen serta sebagai sumber energi. Manganase mangan sulfat menyediakan
kation yang digunakan dalam metabolisme. Polisorbat 80 sebagai surfaktan
6
D. Hipotesis
Hipotesis yang diajukan pada penelitian ini adalah
1. Isolat bakteri usus itik dapat menghasilkan zona hambat yang mampu
menghambat bakteri Gram positif .
2. Terdapat perbedaan besarnya diameter daya hambat oleh ekstrak
antibakteri isolat bakteri usus itik terhadap bakteri Gram positif.
3. Isolat bakteri usus itik menunjukkan pola pertumbuhan tertentu pada
media MRS Broth.
E. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi kepada peneliti
hewan ternak itik mengenai kemampuan isolat bakteri usus itik dalam
menghambat pertumbuhan bakteri Gram positif dan merekomendasikan isolat
yang terpilih dalam penelitian ini untuk dijadikan probiotik bagi hewan
II. TINJAUAN PUSTAKA
A. Mikroflora Usus Itik
Proses pencernaan serat kasar pada itik terjadi pada sekum. Sekum adalah
ruang fermentasi pada itik yang memiliki panjang berkisar 10-29 cm
(Srigandono, 1997). Menurut Gabriel et al., (2006); dalam saluran
pencernaan terdapat populasi mikroorganisme dengan berbagai ukuran dan
kompleksitas. Mikroorganisme yang melekat pada saluran usus tersebut
dinamakan mikroflora usus (Nakazawa, 1992). Mikroflora usus merupakan
ekosistem yang kompleks terdiri dari sejumlah besar bakteri. Dijelaskan
lebih lanjut bahwa mikroorganisme yang ada dalam sekum bersifat anaerob
obligat, sedangkan yang ada di tembolok bersifat anaerob fakultatif. Tipe,
jumlah, dan aktivitas metabolik mikroorganisme tersebut sangat dipengaruhi
oleh faktor individu, umur ternak, lingkungan, dan pakan yang dikonsumsi.
(Gabriel et al., 2006).
Mikroflora normal usus mempunyai sifat (1) dapat tumbuh dalam kondisi
anaerobik, (2) terdapat pada saluran pencernaan dewasa normal, (3) dapat
mengkolonisasi pada bagian spesifik saluran pencernaan, (4) dapat
8
(6) dapat melekatkan diri dengan permukaan epitel usus. Kemampuan bakteri
ini untuk melekat pada jaringana epitel usus (lapisan lendirnya), dapat
dibuktikan dengan kemampuannya mengkolonisasi saluran usus dan menjaga
polpulasi tetapnya (Nakazawa, 1992).
B. Antibakteri
Antibakteri adalah suatu senyawa yang dalam konsentrasi kecil mampu
menghambat bahkan membunuh proses kehidupan suatu mikroorganisme
(Jawetz et al., 2001). Beberapa istilah yang digunakan untuk menjelaskan proses pembasmian bakteri yaitu:
a. Germisid adalah bahan yang dipakai untuk membasmi mikroorganisme
dengan mematikan sel-sel vegetatif, tetapi tidak selalu mematikan
bentuk sporanya.
b. Bakterisid adalah bahan yang dipakai untuk mematikan bentuk-bentuk
vegetatif bakteri.
c. Bakteriostatik adalah suatu bahan yang mempunyai kemampuan untuk
menghambat pertumbuhan bakteri tanpa mematikannya.
d. Antiseptik adalah suatu bahan yang menghambat atau membunuh
mikroorganisme dengan mencegah pertumbuhan atau menghambat
aktivitas metabolisme, digunakan pada jaringan hidup.
e. Desinfektan adalah bahan yang dipakai untuk membasmi bakteri dan
mikroorganisme patogen tapi belum tentu beserta sporanya, digunakan
9
Berdasarkan sifat toksisitas selektif, ada antibakteri yang bersifat menghambat
pertumbuhan bakteri yang dikenal sebagai bakteriostatik, dan ada yang
bersifat membunuh bakteri dikenal sebagai bakterisid. Kadar minimal yang
diperlukan untuk menghambat atau membunuh bakteri, masing-masing
dikenal sebagai kadar hambat minimal (KHM) dan kadar bunuh minimal
(KBM). Antibakteri tertentu aktivitasnya dapat meningkat menjadi bakterisid
bila kadar antimikrobanya ditingkatkan melebihi KHM (Ganiswara, 1995).
Efektivitas senyawa antimikroba dapat dilihat pada pengujian antimikroba
dengan menentukan konsentrasi terkecil agar pertumbuhan organisme uji
dapat terhambat. Pengujian antimikroba dengan menentukan konsentrasi
terkecil dilakukan dengan metode Minimum Inhibitory Concentration (MIC). Metode MIC ini terdiri dari dua teknik, yaitu teknik tabung pengenceran dan
teknik difusi agar (Middelbeek dan Drijver de Haas, 1992).
Kriteria zat ideal yang digunakan sebagai zat antimikroba adalah aktivitasnya
yang cukup luas, tidak bersifat racun, ekonomis, sebaiknya bersifat
membunuh daripada hanya menghambat pertumbuhan mikroba (Pelczar dan
Chan, 1988). Keadaan-keadaan yang dapat mempengaruhi kerja antimikroba
antara lain konsentrasi antimikroba yang digunakan, jumlah mikroorganisme,
suhu dan waktu kontak, spesies atau jenis mikroorganisme, keberadaan bahan
organik dan pH (Frazier dan Wessthof, 1988). Cara kerja zat antimikroba
10
dinding sel, merubah molekul protein dan asam nukleat serta menghambat
sintesis asam nukleat dan protein (Pelczar dan Chan, 1988)
C. Uji Aktivitas Antibakteri
Pengujian terhadap aktivitas antibakteri dapat dilakukan dengan berbagai cara,
yaitu:
1. Agar difusi, media yang dipakai adalah agar Mueller Hinton. Pada
metode difusi ini ada beberapa cara, yaitu:
a. Cara Kirby Bauer
b. Cara Sumuran
c. Cara Pour Plate
2. Dilusi cair/ dilusi padat
Pada prinsipnya antibakteri diencerkan sampai diperoleh beberapa
konsentrasi. Pada dilusi cair, masing-masing konsentrasi obat ditambah
suspensi kuman dalam media. Pada dilusi padat tiap konsentrasi obat
dicampur dengan media agar, kemudian ditanami bakteri. Metode dilusi
cair adalah metode untuk menentukan konsentrasi minimal dari suatu
antibakteri yang dapat menghambat atau membunuh mikroorganisme.
Konsentrasi terendah yang dapat menghambat pertumbuhan bakteri
ditunjukkan dengan tidak adanya kekeruhan disebut Kadar Hambat
11
mikroba apabila nilai konsentrasi minimum hambatannya rendah tetapi
mempunyai daya hambat yang besar (Hayati, 1999).
Perhitungan hasil pengamatan dilakukan dengan cara mengukur diameter
hambatan senyawa yang diperiksa dibandingkan dengan diameter hambatan
senyawa standar pada konsentrasi yang sama (Sherley, 1998).
Potensi = Diameter hambatan senyawa antimikroba x 100 % Diameter senyawa baku dengan konsentrasi sama
D. Bakteri Gram Positif
Secara garis besar berdasar pengecatan Gram, bakteri dikelompokkan
menjadi 2, yaitu gram positif dan Gram negatif. Bakteri gram positif adalah
bakteri yang mempertahankan zat warna Gram A yang mengandung kistal
violet, sewaktu proses pewarnaan gram. Bakteri jenis ini akan berwarna ungu
di bawah mikroskop, sedangkan bakteri Gram negatif akan berwarna merah
atau merah muda, karena warna ungu dapat dilunturkan kemudian mengikat
cat Gram D sebagai warna kontras. Perbedaan klasifikasi antara kedua jenis
bakteri ini terutama didasarkan pada perbedaan struktur dinding sel bakteri
(Jawetz, 1996).
Pada bakteri gram positif susunan dinding selnya lebih sederhana terdiri atas 2
lapis namun memiliki lapisan peptidoglikan yang tebal sementara pada
dinding sel bakteri gram negatif lebih kompleks terdiri atas 3 lapis namun
12
1. Staphylococcus aureus (S. aureus)
S. aureus berbentuk bulat atau lonjong, merupakan jenis yang tidak bergerak, tidak berspora, bakteri gram positif dan tersusun dalam
kelompok (seperti buah anggur). Pembentukan kelompok ini karena
pembelahan sel-sel anaknya cenderung tetap berada di dekat sel induknya
(Gupte, 1990). S. aureus merupakan kuman penyebab penyakit yang sering terjadi di masyarakat maupun sebagai infeksi nosokomial.
Kolonisasi S. aureus seringkali tidak bergejala dan hidup secara komensal pada hidung manusia (Fournier, 2005). S. aureus dapat menyebabkan penyakit berkat kemampuannya melakukan pembelahan, dan menyebar
luas ke dalam jaringan serta mampu memproduksi bahan ekstra seluler
seperti katalase, koagulase, eksotoksin, lekosidin, toksin eksfoliatif,
Toksin Sindroma Syok Toksik (Toxic Shock Syndrome Toxin),
enterotoksin dan enzim lain (Jawetz et al., 2001).
2. Bacillus subtilis
Bakteri Bacillus sp merupakan mikroba flora normal pada saluran pencernaan ayam (Green et al., 2006). Ciri-ciri bakteri ini adalah
organisme saprophytik, berbentuk batang, gram positif membentuk spora
non-patogen yang biasanya ditemukan dalam air, udara, debu, tanah dan
sedimen. Terdapat beberapa jenis bakteri yang bersifat saprofit pada
tanah, air, udara dan tumbuhan seperti Bacillus cereus dan Bacillus subtilis
13
lincheniformis, Bacillus clausii, Bacillus megaterium, Bacillus firmus,
kelompok Bacillus cereus (Barbosa et al.¸ 2005).
E. Bakteri Asam Laktat (BAL)
Menurut Jenie (2006) produk bakteri asam laktat yang bersifat
heterofermentatif adalah asam laktat, asam asetat, CO2 dan etanol dalam
jumlah yang besar. Bakteri asam laktat yang bersifat homofermentatif
mengubah 95% glukosa atau heksosa menjadi asam laktat dan sejumlah kecil
CO2 serta asam-asam volatil. Hasil fermentasi Lactobacillus yang berupa senyawa asam organik dan alkohol berpotensi dapat menghambat
pertumbuhan bakteri lain.
Bakteri yang termasuk kelompok bakteri asam laktat adalah Aerococcus, Allococcus, Carnobacterium, Enterococcus, Lactobacillus, Lactococcus, Leuconostoc, Pediococcus, Streptococcus, Tetragenococcus, dan Vagococcus
(Ali dan Radu, 1998).
Bakteri asam laktat (BAL) merupakan kelompok besar bakteri
menguntungkan yang memiliki sifat relatif sama. Saat ini bakteri asam laktat
digunakan untuk pengawetan dan memperbaiki tekstur dan cita rasa bahan
pangan. Bakteri asam laktat mampu memproduksi asam laktat sebagai produk
akhir perombakan karbohidrat, hidrogen peroksida, dan bakteriosin (Afrianto
14
pertumbuhan bakteri pathogen seperti Salmonella dan E. coli akan dihambat (Silalahi, 2000). Efektivitas bakteri asam laktat dalam menghambat bakteri
pembusuk dipengaruhi oleh kepadatan bakteri asam laktat, strain bakteri asam
laktat, dan komposisi media. Selain itu, produksi substansi penghambat dari
bakteri asam laktat dipengaruhi oleh media pertumbuhan, pH, dan
temperature lingkungan (Stiles, 1990).
F. Pertumbuhan Mikroorganisme
Pertumbuhan merupakan proses bertambahnya ukuran atau subtansi atau masa
zat suatu organisme, misalnya kita makhluk makro ini dikatakan tumbuh
ketika bertambah tinggi, bertambah besar atau bertambah berat. Pada
organisme bersel satu pertumbuhan lebih diartikan sebagai pertumbuhan
koloni, yaitu pertambahan jumlah koloni, ukuran koloni yang semakin besar
atau subtansi atau massa mikroba dalam koloni tersebut semakin banyak,
pertumbuhan pada mikroba diartikan sebagai pertambahan jumlah sel mikroba
itu sendiri. Pertumbuhan merupakan suatu proses kehidupan yang irreversible
artinya tidak dapat dibalik kejadiannya. Pertumbuhan didefinisikan sebagai
pertambahan kuantitas konstituen seluler dan struktur organisme yang dapat
dinyatakan dengan ukuran, diikuti pertambahan jumlah, pertambahan ukuran
sel, pertambahan berat atau massa dan parameter lain. Sebagai hasil
pertambahan ukuran dan pembelahan sel atau pertambahan jumlah sel maka
terjadi pertumbuhan populasi mikroba (Iqbalali, 2008). Pertumbuhan mikroba
15
disebut dengan fase lag, fase eksponensial, fase stasioner dan fase kematian.
Pada fase kematian eksponensial tidak diamati pada kondisi umum
pertumbuhan kultur bakteri, kecuali bila kematian dipercepat dengan
penambahan zat kimia toksik, panas atau radiasi. Kejadian di atas apabila
digambarkan dalam bentuk kurva adalah sebagai berikut:
Gambar 1. Kurva pertumbuhan bakteri pada umumnya
Ada empat fase pada pertumbuhan bakteri pada kurva diatas, yaitu
Tabel 1. Ciri dan fase pada kurva pertumbuhan
Fase Pertumbuhan Ciri
Lag (lambat)
Tidak ada pertumbuhan populasi karena sel mengalami perubahan komposisi kimiawi dan ukuran serta bertambahnya substansi
intraseluler sehingga siap untuk membelah diri.
Logaritma atau eksponensial
Sel membelah diri dengan laju yang konstan, massa menjadi dua kali lipat, keadaan
pertumbuhan seimbang.
Stationary (stasioner/tetap)
Terjadinya penumpukan racun akibat
16
Death (kematian)
Sel menjadi mati akibat penumpukan racun dan habisnya nutrisi, menyebabkan jumlah sel yang mati lebih banyak sehingga mengalami penurunan jumlah sel secara eksponensial.
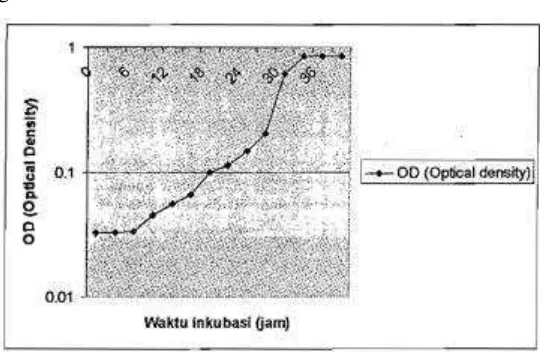
Pada bakteri Lactobacillus sp kurva pertumbuhannya sedikit berbeda seperti gambar berikut.
Gambar 2. Kurva pertumbuhan bakteri Lactobacillus
Diketahui bahwa inkubasi hingga 12 jam menunjukkan fase adaptasi
sedangkan inkubasi hingga 24 jam menunjukkan fasae logaritmik, kemudian
pada inkubasi yang dilanjutkan hingga 33 jam menunjukkan fase logaritmik
diperlambat akhirnya statis pada inkubasi 36 jam (Natsir dan Sartini, 2008).
Pengetahuan akan kurva pertumbuhan bakteri sangat penting untuk
menggambarkan karakteristik pertumbuhan bakteri, sehingga akan
mempermudah di dalam kultivasi (menumbuhkan) bakteri ke dalam suatu
media, penyimpanan kultivasi dan penggantian media.
Pertumbuhan dapat diamati dari meningkatnya jumlah sel atau massa sel
17
pembelahan biner,yaitu dari satu sel membelah menjadi 2 sel baru, maka
pertumbuhan dapat diukur dari bertambahnya jumlah sel. Waktu yang
diperlukan untuk membelah diri dari satu sel menjadi dua sel sempurna
disebut waktu generasi. Waktu yang diperlukan oleh sejumlah sel atau massa
sel menjadi dua kali jumlah/massa sel semula disebut doubling time atau
waktu penggandaan. Waktu penggandaan tidak sama antara berbagai
mikrobia, dari beberapa menit, beberapa jam sampai beberapa hari tergantung
kecepatan pertumbuhannya. Kecepatan pertumbuhan merupakan perubahan
jumlah atau massa sel per unit waktu. Adapun perhitungan pertumbuhan
mikroba (Sumarsih, 2003):
Gambar 3. Pembelahan sel secara biner
1 sel menjadi 2 sel
2 sel menjadi 4 sel 21 menjadi 22 atau 2x2
4 sel menjadi 8 sel 22 menjadi 23 atau 2x2x2
Dari hal tersebut dapat dirumuskan menjadi:
N = N
02
nN: jumlah sel akhir,
18
Waktu generasi = t / n
t: waktu pertumbuhan eksponensial, n: jumlah generasi
Dalam bentuk logaritma, rumus N = N0 2n menjadi:
log N = log N0 + n log 2
Waktu generasi juga dapat dihitung dari slope garis dalam plot
semilogaritma kurva pertumbuhan eksponensial, yaitu dengan rumus,
slope = 0,301/ waktu generasi. Usaha pengendalian mikroorganisme
dapat dilaksanakan apabila faktor-faktor yang mempengaruhi
pertumbuhan atau perkembangbiakan mikroorganisme telah diketahui
sebelumnya.
Menurut Yudhabuntara (2003) faktor-faktor yang mempengaruhi
pertumbuhan umumnya dibagi ke dalam empat bahasan yaitu:
1. Faktor intrinsik
Faktor intrinsik meliputi pH, aktivitas air (activity of water, aw),
kemampuan mengoksidasi-reduksi (redoxpotential, Eh), kandungan
nutrien, bahan antimikroba dan struktur bahan makanan. Ukuran
keasaman atau pH adalah log10 konsentrasi ion hidrogen.
Lazimnya bakteri tumbuh pada pH sekitar netral (6,5 – 7,5).
19
pertumbuhan mikrobia dalam pangan. Kemampuan
mengoksidasi-reduksi (redoxpotential, Eh) adalah perbandingan total daya
mengoksidasi (menerima elektron) dengan daya mereduksi
(memberi elektron). Pertumbuhan mikroorganisme memerlukan air,
energi, nitrogen, vitamin dan faktor pertumbuhan, mineral. Air
yang tersedia untuk pertumbuhan mikroorganisme ditentukan oleh
aw bahan makanan. Sebagai sumber energi, mikroorganisme
memanfaatkan karbohidrat, alkohol dan asam amino yang terdapat
dalam bahan makanan. Faktor pertumbuhan yang diperlukan adalah
asam amino, purin dan pirimidin, serta vitamin. Struktur bahan
makanan yang dapat mempengaruhi pertumbuhan mikroorganisme
misalnya lemak karkas dan kulit pada karkas unggas dan karkas
babi dapat melindungi daging dari kontaminasi mikroorganisme.
2. Faktor ekstrinsik
Faktor ekstrinsik yang mempengaruhi pertumbuhan
mikroorganisme adalah suhu penyimpanan. Faktor luar lainnya
yang pada prinsipnya berhubungan dengan pengaruh atmosferik
seperti kelembaban, tekanan gas/keberadaan gas, juga cahaya dan
pengaruh sinar ultraviolet.
3. Faktor proses
Semua proses teknologi pengolahan bahan makanan mengubah
lingkungan mikro bahan makanan tersebut. Proses tersebut dapat
20
curing, pengasapan, iradiasi, tekanan tinggi, pemakaian medan
listrik dan pemberian bahan imbuhan pangan.
4. Faktor implisit
Faktor lain yang berperan adalah faktor implisit yaitu adanya
sinergisme atau antagonisme di antara mikroorganisme yang ada
dalam “lingkungan” bahan makanan. Ketika mikroorganisme
tumbuh pada bahan makanan, mikroorganisme tersebut akan
bersaing untuk memperoleh ruang dan nutrien. Dengan demikian
akan terjadi interaksi di antara mikroorganisme yang berbeda.
Interaksi ini dapat saling mendukung maupun saling menghambat
(terjadi sinergisme atau antagonisme).
Bakteri merupakan organisme kosmopolit yang dapat kita jumpai di
berbagai tempat dengan berbagai kondisi di alam ini. Mulai dari
padang pasir yang panas, sampai kutub utara yang beku kita masih
dapat menjumpai bakteri. Namun bakteri juga memiliki batasan suhu
tertentu dia bisa tetap bertahan hidup, ada tiga jenis bakteri berdasarkan
tingkat toleransinya terhadap suhu lingkungannya:
1. Mikroorganisme psikrofil yaitu mikroorganisme yang suka
hidup pada suhu yang dingin, dapat tumbuh paling baik pada
suhu optimum dibawah 200C.
2. Mikroorganisme mesofil, yaitu mikroorganisme yang dapat
hidup secara maksimal pada suhu yang sedang, mempunyai
21
3. Mikroorganisme termofil, yaitu mikroorganisme yang tumbuh
optimal atau suka pada suhu yang tinggi, mikroorganisme ini
sering tumbuh pada suhu diatas 400C, bakteri jenis ini dapat
hidup di tempat-tempat yang panas bahkan di sumber-sumber
mata air panas bakteri tipe ini dapat ditemukan, pada tahun 1967
di Yellow Stone Park ditemukan bakteri yang hidup dalam
sumber air panas bersuhu 93-940C.
Dalam pertumbuhannya bakteri memiliki suhu optimum dimana
pada suhu tersebut pertumbuhan bakteri menjadi maksimal.
Dengan membuat grafik pertumbuhan suatu mikroorganisme, maka
dapat dilihat bahwa suhu optimum biasanya dekat puncak range
suhu. Di atas suhu ini kecepatan tumbuh mikroorganisme akan
berkurang. Metode pengukuran pertumbuhan yang sering
digunakan adalah dengan menentukan jumlah sel yang hidup
dengan jalan menghitung koloni pada pelat agar dan menentukan
jumlah total sel/jumlah massa sel. Selain itu dapat dilakukan
dengan cara metode langsung dan metode tidak langsung. Dalam
menentukan jumlah sel yang hidup dapat dilakukan penghitungan
langsung sel secara mikroskopik, melalui 3 jenis metode yaitu
metode: pelat sebar, pelat tuang dan most-probable number (MPN).
Penentuan jumlah total sel bakteri dapat menggunakan alat yang
khusus yaitu bejana Petrof-Hausser atau hemositometer. Penentuan
22
yang menentukan: Volume sel mampat, berat sel, besarnya sel atau
III. METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Mikrobiologi Jurusan Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
Penelitian ini dilakukan pada bulan April 2011 hingga Agustus 2011.
B. Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini antara lain mikroskop, tabung
reaksi, gelas objek, tabung anaerobic jar, cawan petri dengan diameter 15 dan
30 cm, erlenmeyer ukuran 500 ml, 250 ml, 100ml dan 50 ml, gelas ukur, ose,
spatula, bunsen, voertex mixer, neraca analitik, kompor listrik, autoklaf,
laminar air flow, inkubator dengan suhu370C, mikrotube, tip, mikropipet, pH meter, pipet tetes, dan peralatan lainnya.
Bahan-bahan yang digunakan adalah isolat bakteri usus itik (B1, B2, B3, B4,
B5, B6, B7, B8, B9, B10, B11, B12 dan B13), biakan Staphylococcus aureus
dan Bacillus subtilis yang diperoleh dari koleksi biakan Laboratorium
24
media Nutrient Broth (NB), bacteriological agar, aquades, alumunium foil, kasa, kapas, minyak imersi.
C. Metode Penelitian
Penelitian ini dilakukan 2 tahapan. Pertama, penentuan uji daya hambat
dengan menggunakan metode difusi antibiotik sumuran. Kemampuan zat
antibakteri ditentukan berdasar diameter daya hambat yang dihasilkan.
Kedua, yaitu penentuan pola pertumbuhan isolat bakteri usus itik dengan
menghitung langsung jumlah sel bakteri selama 24 jam dengan interval waktu
1 jam.
D. Prosedur Kerja
1. Peremajaan Bakteri
Isolat bakteri usus itik dibiakkan dengan cara digores pada media MRS
agar miring diinkubasi pada anaerobic jar selama 48 jam, sedangkan untuk
bakteri uji dibiakkan dengan cara digores pada NA miring.
2. Pembuatan Starter
Isolat yang telah diinkubasi dari peremajaan, diambil masing-masing 1 ose
25
3. Produksi Senyawa Antibakteri
Sebanyak 10% dari starter diambil dan dimasukkan kedalam 10,8 ml MRS
Broth steril, kemudian diinkubasi selama 2 hari. Setelah 2 hari masa inkubasi, setiap harinya diambil kultur sebanyak 1 ml dimasukkan
kedalam microtube lalu sentrifuge. Kultur disentrifuge dengan kecepatan
11.000 rpm selama 10 menit. Supernatan yang diperoleh dari sentrifuge
merupakan ekstrak antibakteri yang diduga mengandung senyawa
antibakteri yang dapat menghambat bakteri Gram positif.
4. Uji Daya Hambat Antibakteri
Bakteri uji diinokulasi sebanyak 1 ose ke dalam tabung reaksi yang berisi
9 ml aquades steril sampai diperoleh kekeruhan yang sama dengan
StandarMac Farlan (3x108 CFU/ml). Kemudian sebanyak 1 ml bakteri uji
dimasukkan ke dalam cawan petri steril dan ditambahkan 25 ml media NA
steril. Cawan petri diputar sesuai angka delapan sebelum media NA
memadat agar bakteri menyebar rata pada media. Setelah media memadat,
di dalam media dibuat lubang membentuk sumur dengan diameter 1 cm.
Larutan antibakteri dimasukkan ke dalam sumur sebanyak 100 µl. Kultur
diinkubasi selama 24 jam pada suhu 370C. Kemudian diameter daya
hambat diukur sesuai dengan garis yang telah dibuat.
5. Perhitungan Sel Bakteri Secara Langsung (Mikroskopis)
Perhitungan bakteri dilakukan secara langsung di bawah mikroskop
dengan cara mengambil 1 ose isolat bakteri usus itik yang telah
26
1 cm
1 cm
cm x 1 cm dan dilakukan pengecatan gram. Perhitungan kepadatan sel
bakteri secara langsung dilakukan dengan melihat jumlah sel pada luas
lapang pandang mikroskop. Penentuan luas lapang pandang mikroskop
dilakukan dengan mengukur diameter areal pandang mikroskop
menggunakan mikrometer objektif yang mempunyai skala terkecil 0,01
mm. Setelah nilai diameter areal pandang mikroskop diketahui kemudian
dibagi 2 untuk mencari jari-jari dan dimasukkan ke dalam rumus berikut :
Luas areal pandang mikroskop = πr2 mm2
πr2 x 10-2 cm2
Dimana r = jari-jari areal pandang mikroskop dalam cm, sedangkan rumus
penentuan perhitungan kepadatan sel bakteri secara langsung yaitu sebagai
berikut :
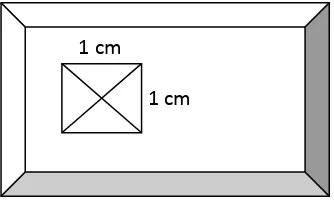
Konsentrasi sel = x
Luas lapang pandang mikroskop (cm2) x t (cm)
Keterangan = x : rata-rata jumlah bakteri dan t : tinggi
Gambar 4. Luas area perhitungan bakteri dalam objek glass
Setelah dilakukan perhitungan sel maka dilanjutkan dengan menghitung
waktu generasi sel bakteri agar dapat diketahui kecepatan sel bakteri dalam
membelah. Rumus dalam menentukan wakttu generasi sel adalah sebagai
27
Nt = N
02
nNt: jumlah sel akhir,
N0: jumlah sel awal, n: jumlah generasi
Waktu generasi = t / n
t: waktu pertumbuhan eksponensial, n: jumlah generasi
Dalam bentuk logaritma, rumus Nt = N0 2n menjadi:
log Nt = log N0 + n log 2
log Nt – log N0 = n log 2
n log 2 = log Nt – log N0
n = log Nt – log N0 Log 2
28
E. Diagram Alir
1. Uji Daya Hambat
1 Ose
Hasil peremajaan isolat
pada media miring 12 ml (MRS + Agar) MRS Broth
Starter Inkubasi 2 hari
(anaerobic jar)
1,2 ml
10,8 ml
MRS Broth Inkubasi (anaerobic jar)
Bahan Uji
Hari ke-2 Hari ke-3 Hari ke-4
1 ml 1 ml 1 ml Sentrifuge Sentrifuge Sentrifuge
100 µl 100 µl 100 µl
(Luas diameter dari masing-masing cawan dihitung dengan penggaris)
29
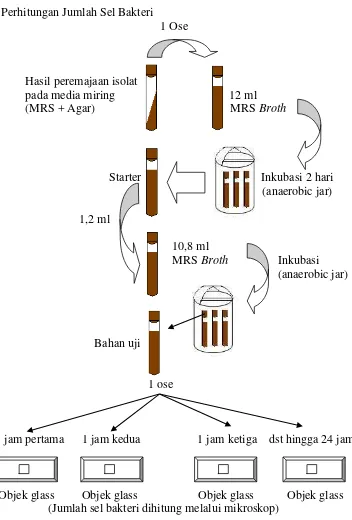
2. Perhitungan Jumlah Sel Bakteri
1 Ose (Jumlah sel bakteri dihitung melalui mikroskop)
RIWAYAT HIDUP
Penulis dilahirkan di kota Jakarta beberapa tahun
silam, tetapi besar dan menetap di kota Depok Jawa
Barat. Pendidikkan yang ditempuh penulis yaitu di
TK. Tunas Mekar, SD N Depok Baru 3, SMP N 2
Depok, SMA Muhammadiyah I Depok. Penulis
terdaftar sebagai mahasiswa Jurusan Biologi, Fakultas Matematika dan Ilmu
Pengetahuan, Universitas Lampung melalui jalur SPMB pada tahun 2007.
Selama menjadi mahasiswa penulis aktif di Badan Eksekutif Mahasiswa FMIPA
Unila sebagai Sekretaris Divisi Infokom Dinas Eksternal (2008/2009), Sekretaris
Dinas Eksternal (2009/2010), Ketua Bidang Hubungan Masyarakat Himpunan
Mahasiswa Biologi (2009/2010) dan Penyiar di a-Radio 101,1 FM Bandar
Lampung (2008-sampai akhir perkuliahan). Penulis juga pernah menjadi asisten
praktikum mata kuliah Mikrobiologi Umum STIKES.
Penulis melakukan kerja praktik di Balai Besar Penelitian Veteriner Bogor dengan
SANWACANA
Alhamdulillahirobbil’alamin, puji syukur penulis panjatkan kepada Allah SWT,
karena berkat kesempatan, kelancaran, kekuatan, rahmat dan hidayah-Nya
sehingga penulis dapat menyelesaikan skripsi ini dengan baik.
Skripsi dengan judul “Uji Daya Hambat Isolat Bakteri Usus Itik (Anas
domestica) Terhadap Bakteri Gram Positif Dan Pertumbuhan Isolat Bakteri Usus Itik Pada Media MRS Broth” adalah syarat untuk memperoleh gelar
sarjana sains di Universitas Lampung.
Dalam penyusunan skripsi ini banyak pihak yang telah membantu penulis sejak
memulai kegiatan sampai terselesaikannya skripsi ini, baik bantuan secara moril
ataupun materil, untuk itu dalam kesempatan ini penulis ingin menyampaikan
ucapan terimakasih yang sebesarnya kepada :
1. Kedua orang tua saya tercinta, yang telah membesarkan, mendidik dan
nasihat serta kasih sayang yang begitu besar, semangat serta do’a yang
tiada henti kepada penulis dalam mencapai cita-cita. Semoga Allah SWT
vi
2. Ibu C. N. Ekowati, M.Si selaku pembimbing I atas ide, saran, motivasi,
kritik, arahan, nasihat, perhatian dan bimbingan yang telah diberikan
dengan penuh kesabaran kepada penulis.
3. Bapak Rudy Sutrisna, MS selaku Pembimbing II yang telah memberikan
bimbingan, perhatian, arahan, saran, kritik dan membantu dengan penuh
kesabaran selama proses penyelesaian skripsi ini.
4. Ibu Kusuma Handayani, M.Si selaku Pembahas atas bimbingan, arahan,
saran, kritik, perhatian dan dukungan yang besar dalam menyelesaikan
skripsi ini.
5. Bapak G. Nugroho Susanto, M.Sc., selaku pembimbing akademik atas
dukungan, motivasi, dan bimbingan kepada penulis dalam menempuh
pendidikan di Jurusan Biologi.
6. Bapak Prof. Suharso, Ph.D selaku Dekan FMIPA Unila
7. Ibu Dra. Nuning Nurcahyani, M.Si. selaku ketua jurusan Biologi FMIPA
Unila atas dukungan sehingga penulis dapat menyelesaikan skripsi.
8. Mas Huda, Mba Isti (dan capo-nya), Mba Nurma, Adikku Gofur, Thofa
tersayang atas do’a, kasihsayang, semangat, dukungan yang telah
diberikan kepada penulis.
9. Panda, Sapi, Hamida, Bara, Tania, dan Andro (Small Family Of The
PaNda) terima kasih atas semangat, do’a, dukungan dan semoga ikatan
keluarga kecil ini senantiasa terjalin sampai akhirat kelak.
10.Teman - teman Microcholik, Dwi, Ratna dan Zahra teruslah berjuang dan
bersabarlah dengan kesabaran yang baik. Mba Debi, Mba Tika, Mba Win
vii
11.Penghuni Wisma Rizky tercinta, Bapak dan Ibu kost, kak Nova, Intan,
Mba Rofah, Icha, Lulu, Lusi, Mega, Fina, Azrin, Herti dan semua yang
mungkin saya lupa untuk menyebutnya.
12.Teman-teman seperjuangan di BEM The Pofessional Team, BEM The
Inspiration Team, teman-teman di HIMBIO dan A-Radio Crew 101,1 FM
Bandar Lampung.
13.Teman- teman satu angkatan Biologi FMIPA Unila.
14.Kakak kakak tingkat dari angkatan 2000 – 2006 dan adik tingkat 2008 –
2011 terimakasih atas kekeluargaan, kritikkan, canda tawa, semangat dan
dukungan yang diberikan kepada penulis.
15.Kepada semua pihak yang tidak dapat penulis satu per satu, yang dengan
tulus telah membantu penulis selama melakukan proses penyusunan
skripsi.
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan,
akan tetapi harapannya semoga Allah SWT memberikan keluasan ilmu dan
balasan pahala yang terbaik bagi semua pihak yang telah membantu penulis
selama ini dan semoga skripsi ini dapat bermanfaat bagi kita semua. Aaamiiin
allohumma aamiin ya Allah.
Bandar Lampung, Januari 2012
Penulis
V. SIMPULAN DAN SARAN
A. Simpulan
1. Isolat bakteri usus itik mampu menghambat pertumbuhan bakteri Gram
positif Bacillus subtilis dan Staphylococcus aureus.
2. Besarnya diameter daya hambat isolat bakteri usus itik berbeda-beda,
berdasarkan hasil analisis histogram dengan standar error bahwa isolat
yang menghasilkan diameter terbesar pada B. subtilis adalah B4 dan pada
S. autreus adalah B9.
3. Pertumbuhan isolat bakteri usus itik B4 menunjukkan fase lag selama 2
jam dan fase logaritmik selama 17 jam, sedangkan isobat B9 menunjukkan
fase lag selama 3 jam dan fase logaritmik selama 10 jam.
B. Saran
Perlu diadakan penelitian lanjutan tentang pola pertumbuhan untuk semua
jenis isolat bakteri usus itik agar dapat diketahui potensinya untuk dipilih