ISOLASI, KARAKTERISASI DAN UJI AKTIVITAS BIOLOGIS
SENYAWA STEROID DARI TERIPANG
SEBAGAI APRODISIAKA
ALAMI
KUSTIARIYAH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
BOGOR
ISOLASI, KARAKTERISASI DAN UJI AKTIVITAS BIOLOGIS
SENYAWA STEROID DARI TERIPANG
SEBAGAI APRODISIAKA ALAMI
KUSTIARIYAH
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Teknologi Industri Pertanian
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
BOGOR
© Hak cipta milik Kustiariyah, tahun 2006 Hak cipta dilindungi
Judul Tesis : Isolasi, Karakterisasi dan Uji Aktivitas Biologis Senyawa Steroid dari Teripang sebagai Aprodisiaka Alami
Nama : Kustiariyah
NIM : F351020211
Disetujui
Komisi Pembimbing
Prof. Dr. Ir. E. Gumbira Sa’id, M.ADev. Ketua
Dr. Ir. Khaswar Syamsu, M.Sc Dr. Ir. Kaseno, M.Eng
Anggota Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Teknologi Industri Pertanian
Dr. Ir. Irawadi Jamaran Dr. Ir. Khairil Anwar Notodiputro, M.S.
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis yang berjudul “Isolasi, Karakterisasi dan Uji Aktivitas Biologis Senyawa Steroid dari Teripang sebagai Aprodisiaka Alami“ adalah benar hasil karya saya sendiri dan belum pernah diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber
informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak
diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam
Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juni 2006
Kustiariyah
ABSTRAK
KUSTIARIYAH. Isolasi, Karakterisasi dan Uji Aktivitas Biologis Senyawa Steroid dari Teripang sebagai Aprodisiaka Alami. Dibimbing oleh E. GUMBIRA SA’ID, KHASWAR SYAMSU dan KASENO.
Teripang (Holothurian) merupakan salah satu komoditas perikanan yang mempunyai nilai ekonomis tinggi. Umumnya diperdagangkan dalam bentuk kering (beche-de-mer). Bioaktif dari teripang, yang umum disebut holothurin, menarik untuk diteliti karena spektrum aktivitas biologisnya yang luas, yaitu sebagai antibakteri, antikapang (antifungi), cytotoxic, haemolytic dan anti-inflamasi. Salah satu holothurin, yaitu senyawa steroid, sebagai aprodisiaka alami belum banyak diteliti. Oleh karena itu, tujuan penelitian ini adalah (1) Mendapatkan isolat senyawa steroid dan mengetahui kandungan steroid dalam jeroan dan daging teripang basah dan kering, (2) Mengetahui karakteristik ekstrak senyawa steroid dari teripang, (3) Mengetahui aktivitas biologis senyawa steroid dari teripang sebagai aprodisiaka alami, dan (4) Menguji coba membran nanofiltrasi untuk purifikasi awal senyawa steroid dari teripang.
ABSTRACT
KUSTIARIYAH. Isolation, Characterisation and Biological Activity Test of Sea
Cucumber Steroid Compound as Natural Aphrodisiac. Under direction of E. GUMBIRA SA’ID, KHASWAR SYAMSU and KASENO.
Sea cucumber (Holothurian) is one of fisheries commodities which has a high economic value. Generally sea cucumber is traded in the dried form ( beche-de-mer). Bioactive of sea cucumber, commonly known as holothurin, has drawn attention because of its wide spectrum of biological effects namely antibacterial, antifungal, cytotoxic, haemolytic and anti-inflammation. One of holothurins, steroid compounds, as natural aphrodisiac have not been observed yet. Therefore, the aims of this study were (1) to isolate steroid compounds of sea cucumber and their contents, (2) to characterise the compounds, (3) to know biological activity of the compounds as aphrodisiac, and (4) to do experiment of nanofiltration membrane for initial purification of steroid compounds.
PRAKATA
Puji syukur penulis panjatkan kehadirat Allah SWT, karena berkat rahmat dan karunia-Nya penulis dapat menyelesaikan tesis ini. Tesis ini merupakan salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Teknologi Industri Pertanian, Sekolah Pascasarjana Institut Pertanian Bogor. Tesis ini berjudul “Isolasi, Karakterisasi dan Uji Aktivitas Biologis Senyawa Steroid dari Teripang sebagai Aprodisiaka Alami”. Penelitian ini merupakan bagian dari Hibah Penelitian Tim Pasca (HPTP) yang didanai oleh Direktorat Jenderal Pendidikan Tinggi, Departemen Pendidikan Nasional.
Pada kesempatan ini penulis mengucapkan terima kasih banyak kepada para personalia di bawah ini:
1. Prof. Dr. Ir. E. Gumbira Sa’id, M.ADev., Dr. Ir. Khaswar Syamsu, M.Sc., dan Dr. Ir. Kaseno, M.Eng selaku ketua dan anggota komisi pembimbing, yang dengan penuh kesabaran membimbing penulis mulai dari penyusunan proposal sampai penulisan tesis ini.
2. Prof. Dr. Ir. Tridoyo Kusumastanto, MS, Kepala Pusat Kajian Sumberdaya Pesisir dan Lautan (PKSPL-IPB), atas dukungan dan motivasinya.
3. Dr. Ir. Linawati Hardjito, MSc, selaku Ketua Departemen Teknologi Hasil Perairan (THP-IPB), atas dukungannya.
4. Dr. Ir. Etty Riani, MS, selaku Penguji atas masukan dan sarannya.
5. Drs. Handoko Dwi Putro dari Balai Budidaya Laut Lampung, untuk penyediaan teripangnya.
6. Prof. Dr. Ulrike Lindequist, Direktur Institute of Marine Biotechnology-Greifswald, Jerman, atas motivasi dan dukungannya.
7. Dr. Gudrun Mernitz, Frau Beate Cuypers dan Nadine Ruderish atas masukan dan sarannya.
8. Dr. Nuttawut Saelim, Martha Aznury, MSi, Agung B. Santoso, MSi dan Tung Chau Thanh Nguyen, MSc, untuk motivasi, kritik dan sarannya.
9. Meydia, AMd, rekan-rekan di PKSPL dan THP-IPB, serta rekan-rekan di TIP-IPB atas dukungan dan persahabatannya.
10. Kedua orang tua dan keluarga di Malang atas doa dan dukungannya.
Harapan penulis semoga tesis ini bermanfaat bagi pembaca dan dapat menjadi amal shaleh bagi penulis. Atas masukan dan saran yang bersifat membangun penulis ucapkan terima kasih.
RIWAYAT HIDUP
Penulis dilahirkan di Malang pada tanggal 18 Agustus 1975 dari keluarga
Bapak Tarman dan Ibu Musannah. Penulis merupakan anak pertama dari tiga
bersaudara.
Penulis menyelesaikan pendidikan di SDN Karangnongko II,
Poncokusumo-Malang pada tahun 1988, Sekolah Menengah Pertama di SMPN
01 Poncokusumo-Malang pada tahun 1991 dan Sekolah Menengah Atas di
SMAN 01 Tumpang-Malang pada tahun 1994. Pada tahun tersebut penulis
diterima di Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB
dan tahun 1995 penulis memilih Program Studi Teknologi Hasil Perikanan,
Fakultas Perikanan IPB. Penulis memperoleh gelar Sarjana Perikanan pada
program studi tersebut pada tahun 1999.
Sejak lulus pada tahun tersebut hingga tahun 2001 penulis menjadi asisten
dosen pada matakuliah Bioteknologi Hasil Laut dan sejak tahun 2000 penulis
menjadi staf peneliti pada Pusat Kajian Sumberdaya Pesisir dan Lautan
(PKSPL-IPB). Pada tahun 2002 penulis melanjutkan pendidikan magister pada Program
Studi Teknologi Industri Pertanian, Sekolah Pascasarjana IPB. Tahun 2005
penulis mengikuti training Bioteknologi Industri yang diselenggarakan oleh
Internationale Weiterbildung und Entwicklung gGmbH (InWEnt) di Jerman selama satu tahun. Terhitung sejak bulan Januari 2005 penulis diterima sebagai
staf pengajar pada Departemen Teknologi Hasil Perairan, Fakultas Perikanan
DAFTAR ISI
1) Klasifikasi Membran ... 16
2) Filtrasi Membran ... 18
E. Teknologi Membran pada Filtrasi Steroid ... 19
F. Ayam sebagai Hewan Percobaan ... 19
2) Identifikasi Keberadaan Steroid ... 23
3) Filtrasi Steroid dengan Membran Nanofiltrasi ... 24
4) Pengukuran Kadar Testosteron dan Kolesterol dari Serum Darah ... 24
5) Analisis Kadar N Bahan Contoh (Bubuk Teripang dan Feses) ... 25
6) Analisis Serapan N pada Anak Ayam ... 25
7) Analisis Kadar Lemak pada Bubuk Teripang ... 26
8) Karakterisasi Senyawa Steroid dari Ekstrak Teripang ... 26
9) Uji Aktivitas Biologis/Bioassay pada Anak Ayam Jantan (Alwir 2001) 27 D. Rancangan Penelitian ... 30
2) Kromatografi Lapis Tipis/KLT (Thin Layer Chromatography/TLC) ... 35
3) Karakteristik Steroid Teripang ... 35
E. Purifikasi Awal dengan Membran Nanofiltrasi ... 36
Badan ... 39
2) Pengaruh Ekstrak Teripang terhadap Bobot Hati, Limpa dan Bursa Fabrisius ... 41
3) Pengaruh Ekstrak Teripang terhadap Kadar Kolesterol dan Testosteron ... 45
4) Pengaruh Ekstrak Teripang terhadap Panjang, Lebar, Tinggi dan Bobot Jengger ... 47
5) Pengaruh Ekstrak Teripang terhadap Bobot Testis ... 51
5. KESIMPULAN DAN SARAN ... 54
A. Kesimpulan ... 54
B. Saran ... 54
DAFTAR PUSTAKA ... 56
DAFTAR TABEL
Halaman
1. Produksi teripang di Indonesia pada tahun 2001 ... 6
2. Perkembangan produksi teripang di Indonesia ... 6
3. Paten bahan alami dari teripang ... 8
4. Hormon steroid pada manusia ... 11
5. Karakteristik teripang dari perairan Teluk Lampung ... 31
6. Hasil analisa proksimat daging dan jeroan teripang ... 32
7. Rendemen ekstraksi steroid dari teripang pasir ... 33
8. Hasil identifikasi keberadaan steroid dalam teripang ... 34
DAFTAR GAMBAR
Halaman
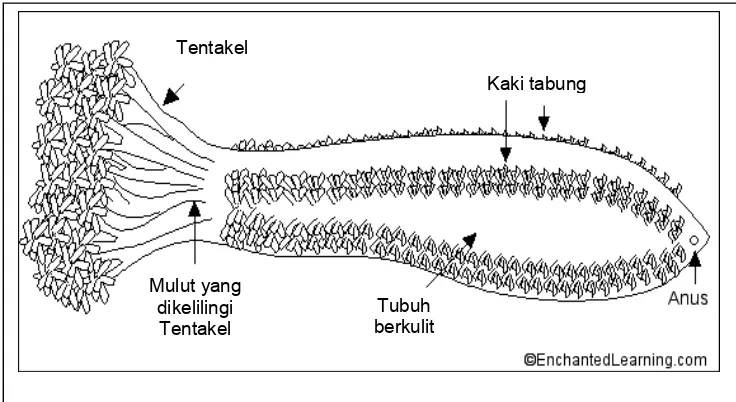
1. Morfologi teripang ... 3
2. Penampang melintang teripang ... 4
3. Kerangka inti steroid (cyclopentanoperhydrophenanthrene) ... 10
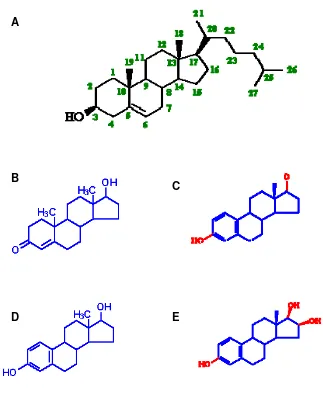
4. Struktur kolesterol (A) dan hormon kelamin, B. Testosteron, C. Estron, D. Estradiol dan E. Estriol ... 13
5. Konversi kolesterol menjadi hormon kelamin ... 14
6. Kerangka kerja penelitian ... 29
7. Teripang pasir yang digunakan dalam penelitian ... 31
8. Perbandingan kualitatif kandungan steroid pada ekstrak aseton (A dan B), metanol (C), heksan (D) dan etil asetat (E) ... 33
9. Agar diffusion assay pada C. maltosa ... 36
10. Proses filtrasi dengan menggunakan memran nanofiltrasi ... 37
11. A. Ekstrak sebelum proses filtrasi, B. Permeat setelah proses filtrasi ... 38
12. Busa terbentuk selama proses filtrasi ... 38
13. Anak ayam jantan sebagai hewan percobaan (umur 31 hari) ... 39
14. Kandungan N pada feses anak ayam jantan ... 40
15. Perkembangan bobot badan anak ayam jantan selama percobaan ... 41
16. Rataan bobot hati anak ayam jantan ... 42
17. Rataan bobot limpa anak ayam jantan ... 43
18. Rataan bobot bursa fabrisius anak ayam jantan ... 44
19. Rasio bobot bursa fabrisius dan bobot badan anak ayam jantan ... 45
20. Kadar kolesterol dan testosteron pada serum anak ayam jantan ... 46
21. Perkembangan panjang jengger anak ayam jantan selama percobaan ... 47
22. Perkembangan lebar jengger anak ayam jantan selama percobaan ... 48
23. Perkembangan tinggi jengger anak ayam jantan selama percobaan ... 49
24. Salah satu anak ayam jantan sebagai kontrol positif (A) dan kontrol negatif (B) ... 49
25. Rataan bobot jengger anak ayam jantan... 51
DAFTAR LAMPIRAN
Halaman
1. Pengukuran panjang, lebar dan tinggi jengger anak ayam jantan ... 62
2. Analisis keragaman pengaruh ekstrak teripang terhadap lebar jengger ... 62
3. Analisis keragaman pengaruh ekstrak teripang terhadap panjang jengger ... 63
4. Analisis keragaman pengaruh ekstrak teripang terhadap tinggi jengger ... 63
5. Uji lanjut pengaruh ekstrak teripang terhadap panjang jengger ... 64
6. Uji lanjut pengaruh ekstrak teripang terhadap lebar jengger ... 64
1. PENDAHULUAN
A. Latar Belakang
Dengan memiliki sekitar 17.504 pulau dan garis pantai lebih dari 81.000
km, Indonesia mempunyai potensi sumberdaya laut dengan keanekaragaman
hayati yang sangat besar (mega-biodiversity). Sumberdaya laut tersebut memiliki berbagai macam kegunaan dan manfaat, di antaranya untuk makanan,
farmasi dan kosmetik.
Ada berbagai organisme laut diantaranya adalah mikroorganisme, blue green algae, green algae, brown algae, red algae, sponges, coelenterates, bryozoans, moluska dan teripang (echinodermata) yang merupakan sumber bahan aktif yang sangat potensial. Biota laut tersebut dapat menghasilkan
berbagai bahan alami yang bermanfaat, antara lain untuk industri farmasi (seperti
antitumor, antikanker, antibiotik, anti-inflamasi), bidang pertanian (fungisida,
pestisida, growth stimulator), industri kosmetik dan makanan (seperti zat pewarna alami dan biopolisakarida). Disamping itu juga dapat dihasilkan protein
serta bahan diet sebagai sumber makanan sehat seperti asam lemak tidak jenuh
omega-3, vitamin, asam amino, dan berbagai jenis gula rendah kalori (Dahuri
2003).
Di antara berbagai organisme tersebut, teripang merupakan komoditi
perikanan yang bernilai ekonomis tinggi dan umumnya diperdagangkan dalam
bentuk kering. Teripang mengandung zat-zat aktif yang bermanfaat dalam
bidang farmasi dan kesehatan. Penelitian tentang bahan alami yang dihasilkan
oleh teripang telah dilaporkan oleh beberapa peneliti terdahulu. Kaswandi et al. (2000) dan Lian et al. (2000) melaporkan bahan aktif yang dihasilkan oleh
Holothuria sp. sebagai antibakteri dan antikapang. Beberapa penelitian teripang yang telah dilakukan umumnya mengenai bahan aktif sebagai antibakteri atau
anti-inflamasi, sedangkan penelitian tentang kandungan bahan aktif yang dapat
digunakan sebagai senyawa biofarmasi (biopharmaceutical substances) seperti aprodisiaka(penambah vitalitas laki-laki) belum banyak dilaporkan.
Pemisahan senyawa bioaktif, seperti steroid selama ini umumnya
dilakukan dengan teknik kromatografi. Namun teknik pemisahan tersebut sulit
diterapkan pada skala industri karena mahalnya biaya operasional dan
industri. Untuk memisahkan steroid yang mempunyai bobot molekul 300 Da
dapat digunakan membran nanofiltrasi. Membran nanofiltrasi adalah membran
yang mempunyai selektivitas pemisahan pada kisaran bobot molekul partikel
200-1000 Da. Dengan demikian, teknologi membran dapat digunakan untuk
pemurnian produk, sehingga merupakan teknologi alternatif yang menarik untuk
menggantikan proses konvensional yang telah ada.
B. Tujuan Penelitian
Tujuan penelitian ini adalah sebagai berikut:
1. Mendapatkan isolat senyawa steroid dan mengetahui kandungan steroid
dalam jeroan dan daging teripang basah dan kering
2. Mengetahui karakteristik ekstrak senyawa steroid dari teripang
3. Mengetahui aktivitas biologis senyawa steroid dari teripang sebagai
aprodisiaka alami
4. Menguji coba membran nanofiltrasi untuk purifikasi awal senyawa steroid
dari teripang
C. Ruang Lingkup Penelitian
Ruang lingkup penelitian ini adalah sebagai berikut:
1. Isolasi senyawa steroid dari jeroan dan daging teripang
2. Karakterisasi ekstrak senyawa steroid dari teripang
3. Uji aktivitas biologis senyawa steroid yang dihasilkan
4. Uji coba membran nanofiltrasi dalam purifikasi awal senyawa steroid dari
teripang
D. Hipotesis Penelitian
Hipotesis yang diuji dalam penelitian ini adalah sebagai berikut:
1. Teripang mengandung senyawa steroid yang dapat digunakan sebagai
aprodisiaka alami
2. Membran nanofiltrasi dapat digunakan untuk purifikasi awal senyawa
2. TINJAUAN PUSTAKA
A. Teripang
Teripang atau yang juga disebut dengan ketimun laut, merupakan hewan
tidak bertulang belakang yang termasuk dalam famili Holothuridae dan
Stichopodidae. Terdapat sebanyak 2000 spesies teripang di dunia
(www.gamatemas.dumei.com). Penyebaran hidup teripang sangat luas dan paling banyak ditemukan di wilayah Indo-Pasifik Barat. Panjang teripang sekitar
5-40 cm dan pada saat hidup bobotnya dapat mencapai 500 g (Wibowo et al.
1997), sedangkan menurut Bandaranayake dan Fosher (1999) panjang teripang
dapat mencapai 60 cm dengan bobot 2 kg. Adapun morfologi dan anatomi
teripang dapat dilihat pada Gambar 1 dan 2.
Teripang umumnya menempati ekosistem terumbu karang dengan
perairan yang jernih, bebas dari polusi, air relatif tenang dengan mutu air cukup
baik. Habitat yang ideal bagi teripang adalah air laut dengan salinitas 29-33‰
yang memiliki kisaran pH 6,5-8,5, kecerahan air 50-150 cm, kandungan oksigen
terlarut 4-8 ppm dan suhu air laut 20-25ºC (Wibowo et al. 1997).
Gambar 1 Morfologi teripang (Sumber: http://www.enchantedlearning.com) Kaki tabung
Tentakel
Mulut yang dikelilingi
Tentakel
Gambar 2 Penampang melintang teripang (Hegner dan Engemann 1968)
Klasifikasi teripang menurut Wibowo et al. (1997) dan Martoyo et al.
(2000) adalah sebagai berikut:
Filum : Echinodermata
Sub Filum : Echinozoa
Kelas : Holothuroidea
Sub Kelas : Aspichitotecea
Ordo : 1. Aspidoochirota
2. Dendrochirota
Famili : Aspidochirotae
Genus : 1. Holothuria
2. Stichopus
3. Thelonota
4. Actinopyga
5. Muelleria
Spesies : 1. Holothuria a. H. nobilis J.
b. H. scabra J.
2. Stichopus variegatus J.
3. Thelonota ananas J.
4. Actinopyga a. A. lecanora J.
b. A. miliaris
c. A. Echinites
Menurut Martoyo et al. (2000) teripang yang terdapat di perairan Indonesia adalah dari genus Holothuria, Muelleria dan Stichopus. Dari ketiga genus tersebut ditemukan 23 spesies, diantaranya baru lima spesies yang sudah
dimanfaatkan dan mempunyai nilai ekonomis penting, yaitu Holothuria scabra
(teripang putih atau pasir), Holothuria edulis (teripang hitam), Holothuria vacabunda (teripang getah atau keling), Holothuria vatiensis (teripang merah) dan Holothuria marmorata (teripang coklat).
Teripang ditemukan dengan berbagai warna, ada yang berwarna hitam,
putih, abu-abu, belang dan lain-lain. Tetapi menurut Ibrahim (2003), spesies
teripang yang benar-benar asli dan bermutu tinggi serta paling berkhasiat adalah
yang berwarna kuning keemasan. Di Malaysia dikenal dengan sebutan Gamat
Emas (Stichopus horrens).
Teripang telah dikenal sebagai makanan yang lezat sejak beberapa ribu
tahun yang lalu, terutama di Asia. Pada beberapa negara, telah ada industri
pengolahan teripang, terutama di RRC. Berbeda halnya dengan sejarahnya,
baru sedikit data ilmiah yang telah dikumpulkan. Hal ini dimungkinkan karena
studi ilmiah di beberapa negara belum dianggap begitu penting, karena jumlah
tangkapan alami cukup besar dan tidak ada ancaman terhadap kelangsungan
pasokannya (Bandaranayake dan Fosher 1999).
Potensi teripang dari perikanan tangkap di Indonesia cukup besar, yaitu
3.517 ton pada tahun 2001 (DKP 2003). Daerah penghasil utama teripang
adalah perairan pantai Sulawesi Tengah (1.134 ton) kemudian diikuti oleh
perairan pantai NTT (433 ton) dan Sulawesi Selatan (327 ton). Potensi teripang
Tabel 1 Produksi teripang di Indonesia pada tahun 2001*
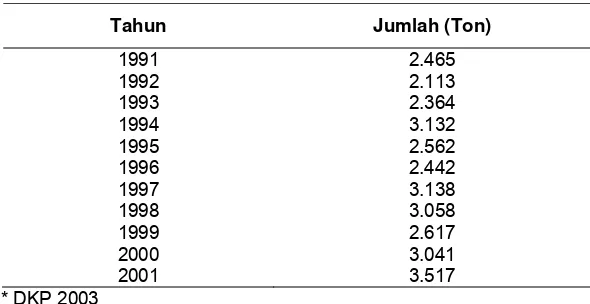
Sejak dasawarsa terakhir produksi teripang di Indonesia cenderung
meningkat dengan rata-rata peningkatan pada tahun 2000-2001 sebesar 5,06%
(DKP 2003). Perkembangan produksi teripang selengkapnya dapat dilihat pada
Tabel 2.
Tabel 2 Perkembangan produksi teripang di Indonesia*
Tahun Jumlah (Ton)
Saat ini perdagangan teripang telah meluas, terutama di Hongkong dan
Singapura, yang merupakan dua negara pusat perdagangan ekspor teripang
dunia. Teripang kering telah diolah dan diperdagangkan di USA, Kanada, Eropa,
Taiwan, Republik Korea, China, Australia, Malaysia, Thailand dan beberapa
negara lain. Pada tahun 1994, Indonesia mengekspor teripang ke Malaysia
China yang dapat memenuhi 37% kebutuhan teripang China (Baine dan Forbes
1997).
Teripang adalah hewan detritus yaitu makan secara menyapu pasir ke
dalam mulut. Pergerakan teripang yang lambat menyebabkannya perlu
mempunyai mekanisme pertahanan tubuh yang efisien, yaitu mengeluarkan
holothurin yang toksik dan dapat melumpuhkan hewan kecil. Holothurin
dikeluarkan oleh kelenjar khusus yang disebut sebagai kuvier (Michael 2003).
Penelitian tentang holothurin telah dimulai sejak awal tahun 1920an dan mulai
intensif pada tahun 1950an. Salah satu jenis holothurin utama dari teripang yang
berkhasiat dalam penyembuhan luka, perawatan sehabis bersalin dan sebagai
antifungi adalah saponin (www.gamatemas.dumei.com).
Bahan bioaktif di dalam teripang juga dikenal sebagai antioksidan yang
membantu mengurangi kerusakan sel dan jaringan tubuh. Kandungan antibakteri
dan antifungi teripang dapat meningkatkan kemampuannya untuk tujuan
perawatan kulit. Teripang juga diketahui mempunyai efek antinosiseptif
(penahan sakit) dan anti-inflamasi (melawan radang dan mengurangi
pembengkakan) (Wibowo et al. 1997). Penelitian yang telah dilakukan di beberapa daerah terutama di Malaysia terhadap penduduk di Kudat, Semporna,
Setiu, Kuantan, Pekan dan Pulau Pangkor membuktikan khasiat teripang sebagai
agen anti-hipertensi (www.gamatemas.dumei.com).
Kaswandi et al. (2000) dan Lian et al. (2000) melaporkan bahan aktif yang dihasilkan oleh Holothuria sp. sebagai antibakteri dan antifungi. Dari hasil penelitian tersebut disimpulkan bahwa bahan aktif dari teripang Holothuria tubolosa tersebut dapat menghambat pertumbuhan Saccharomyces cerevisiae. Disamping mengandung antibakteri, teripang juga dilaporkan mengandung
berbagai asam lemak tak jenuh seperti linoleat, oleat, eikosa pentaenoat (EPA),
dan docosaheksaenoat (DHA) (Fredalina et al. 1999). Beberapa kajian juga menunjukkan potensi teripang sebagai anti-tumor dan memberi khasiat positif
terhadap penyakit AIDS (Scheuer 1995; http://cybermed.cbn.net.id).
Cairan dan tubuh teripang mengandung protein lebih dari 44%,
karbohidrat antara 3-5% dan lemak 1,5% (Ibrahim 2003), sedangkan
Dharmananda (1998) menyebutkan kandungan protein teripang sebesar 55%.
Komponen-komponen lain yang dikandung teripang adalah asam amino
esensial, kolagen, vitamin E, zat-zat mineral seperti khromium, ferum, kadmium,
mangan, nikel, kobalt dan seng. Kandungan asam lemak penting seperti EPA
dan DHA turut memainkan peranan penting sebagai agen penyembuh luka dan
antithrombotik yaitu untuk mengurangi pembekuan darah di dalam saluran darah.
Hal ini dapat mengurangi resiko penyakit stroke dan jantung. Kedua asam di atas
juga dapat membantu memperlambat proses degenerasi sel disamping juga
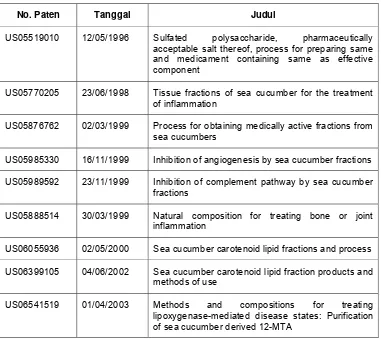
memperlambat proses penuaan (www.gamatemas.dumei.com). Saat ini telah terdapat sembilan paten berkaitan dengan bahan alami dari teripang seperti
disajikan pada Tabel 3.
Tabel 3 Paten bahan alami dari teripang*
No. Paten Tanggal Judul
US05519010 12/05/1996 Sulfated polysaccharide, pharmaceutically acceptable salt thereof, process for preparing same and medicament containing same as effective component
US05770205 23/06/1998 Tissue fractions of sea cucumber for the treatment of inflammation
US05876762 02/03/1999 Process for obtaining medically active fractions from sea cucumbers
US05985330 16/11/1999 Inhibition of angiogenesis by sea cucumber fractions
US05989592 23/11/1999 Inhibition of complement pathway by sea cucumber fractions
US05888514 30/03/1999 Natural composition for treating bone or joint inflammation
US06055936 02/05/2000 Sea cucumber carotenoid lipid fractions and process
US06399105 04/06/2002 Sea cucumber carotenoid lipid fraction products and methods of use
US06541519 01/04/2003 Methods and compositions for treating lipoxygenase-mediated disease states: Purification of sea cucumber derived 12-MTA
B. Hormon Steroid
Hormon adalah senyawa biologis aktif, bekerja dalam konsentrasi yang
kecil, yang dibentuk dalam jaringan atau organ tertentu dari organisme hewan
dan manusia, melalui aliran darah mencapai organ sasaran dan memperlihatkan
kerja spesifik (Schunack et al. 1990). Hormon juga merupakan senyawa yang secara normal dikeluarkan oleh kelenjar endokrin atau jaringan tubuh dan
dilepaskan ke peredaran darah, menuju jaringan sasaran, berinteraksi secara
selektif dengan reseptor khas dan menunjukkan efek biologis (Siswandono dan
Soekardjo 1995).
Secara kimiawi hormon dapat digolongkan menjadi tiga kelompok
berdasarkan bahan pembentuknya (Siswandono dan Soekardjo 1995), sebagai
berikut:
1. Hormon peptida: mempunyai residu asam amino 3-200, meliputi semua
hormon hypothalamus dan pituitary, insulin dan glukagon pada pankreas 2. Hormon amina: kecil, dapat larut dalam air, mengandung grup amina,
meliputi adrenalin pada medulla adrenal dan hormon tiroid
3. Hormon steroid: dapat larut dalam minyak, meliputi hormon adrenal cortical, androgen (hormon seks jantan) dan estrogen (hormon seks betina)
Steroid merupakan hormon turunan kolesterol yang mengandung 27 atom
karbon dan dihasilkan oleh testis, ovarium, korteks adrenalis dan placenta.
Steroid mempunyai bobot molekul sekitar 300 Da (Bischof dan Islami 2003).
Hormon steroid dibagi dalam tiga kelompok di bawah ini (Nogrady 1992).
1. Estrogen; merupakan hormon kelamin betina, diproduksi oleh ovarium,
plasenta dan korteks adrenalis. Terdapat tiga tipe hormon dalam kelompok
ini, yaitu estron, estradiol dan estriol.
2. Progesteron (Gestagen); merupakan hormon kelamin betina yang menjaga
kehamilan, diproduksi oleh korpus luteum dan plasenta.
3. Testosteron; merupakan hormon kelamin jantan, diproduksi oleh testis, dan
dalam jumlah yang lebih kecil oleh korteks adrenalis dan ovarium
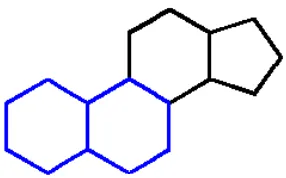
Hormon steroid merupakan turunan kolesterol, dengan struktur inti berupa
Gambar 3 Kerangka inti steroid (cyclopentanoperhydrophenanthrene) (Turner dan Bagnara 1976; Litwack dan Schmidt 2002)
Hormon steroid dibentuk dari jaringan tertentu di dalam tubuh dan dibagi
ke dalam dua kelas yaitu hormon adrenal dan hormon seks (testosteron,
esterogen dan progesteron) (Litwack dan Schmidt 2002). Hormon steroid
memiliki molekul yang berukuran kecil sehingga dapat masuk ke seluruh sel,
tetapi hanya sel-sel sasaran yang memiliki reseptor khusus yang dapat mengikat
hormon, yang selanjutnya akan terjadi sintesis protein baru. Beberapa jenis
hormon steroid pada manusia dapat dilihat pada Tabel 4.
Respon biologis dari suatu organ target terhadap suatu hormon
ditentukan oleh beberapa faktor diantaranya konsentrasi hormon, konsentrasi
reseptor dan afinitas dari interaksi hormon reseptor. Fungsi dari reseptor adalah
untuk mengenal suatu hormon tertentu di antara banyak molekul yang ditemukan
dalam waktu tertentu dan setelah berikatan dengan hormonnya akan
memberikan tanda-tanda yang dihasilkan oleh suatu respon biologis. Umumnya
hormon ada dalam sirkulasi darah dengan konsentrasi yang sangat rendah
(Schunack et al. 1990).
Fungsi androgen adalah menstimulasi tahap akhir dari proses
spermatogenesis, juga meningkatkan pertumbuhan dan aktivitas ekskresi dari
organ kelamin pelengkap, pemeliharaan dan kelamin sekunder dan sexual
Tabel 4 Hormon steroid pada manusia*
Hormon Sekresi dari Tanda
sekresia
Fungsi
Progesteron Corpus luteum LH Pemeliharaan endometrium
(dengan estradiol); diferensiasi kelenjar susu 17ß-Estradiol Folikel ovarium;
Corpus luteum; Sel Sertoli
FSH Wanita: Pengaturan sekresi gonadotropin pada siklus ovari; pemeliharaan endometrium (dengan progesteron); diferensiasi kelenjar susu.
Pria: Inhibitor umpan negatif dari sintesis testosteron oleh sel Leydig
Testosteron Sel Leydig testis; kelenjar adrenal, Ovarium
LH Pria: Setelah dikonversi menjadi dihydrotestosterone
Sel retikularis ACTH Pertahanan tubuh; androgen
lemah; dapat diubah menjadi estrogen; pengaturan koenzim NAD+
Cortisol Sel fasciculata ACTH Adaptasi terhadap stress
dengan ekspresi fenotipik seluler; peningkatan glikogen hati; pada dosis tinggi dapat membunuh sel T tertentu; meningkatkan tekanan darah Aldosteron Sel glomeru-losa dari
korteks adrenal
PTH Memfasilitasi absorpsi Ca2+ dan fosfat oleh sel epitel usus; mempengaruhi protein pengikat kalsium intraseluler
* Litwack dan Schmidt (2002)
a
Androgen ada yang terbentuk secara alami seperti testosteron, 11α
-ketotestosteron serta dihydrotestosteron dan ada pula yang disintesis seperti
17α-metiltestosteron dan testosteron propionate. Menurut (Schunack et al. 1990), hormon androgen terdiri dari androstanedion, androstenedion,
androstenediol dan trans-hidrosterin.
Testosteron dalam kelas steroid dikenal sebagai androgen. Dalam
sirkulasi darah, testosteron berikatan dengan α-globulin untuk ditransformasikan,
77-99% dari testosteron yang bersirkulasi terikat dengan globuli proteinnya, sisa
testosteron yang bebas dapat memasuki sel target dimana suatu enzim dalam
sitoplasma dapat merubah testosteron menjadi dihydrotestosteron yang
seterusnya dapat bereaksi dengan reseptor pada inti. Kompleks
hormon-reseptor memasuki inti sel dan menstimulasi sintesis RNA, akhirnya
meningkatkan biosintesis protein (Schunack et al. 1990).
Sebagai hormon steroid, testosteron merupakan hormon yang bersifat
anabolik dan androgenik. Dari kedua sifat itu yang lebih menonjol adalah sifat
androgenik karena sangat berpengaruh pada pertumbuhan organ reproduksi,
organ seksual sekunder dan kelenjar aksesoris kelamin, sedangkan untuk sifat
anabolik, berpengaruh pada pertumbuhan jaringan dan sel-sel seperti otot,
eritrosit serta pertumbuhan tulang (Rath et al. 1996).
Testosteron disintesis dari prekursor utamanya yaitu kolesterol (Gambar
4). Pada tahap awal kolesterol dikonversi menjadi Δ5-Pregnenolon, yang
merupakan senyawa antara dalam sintesis semua hormon steroid. Δ5
-Pregnenolon ini dapat diubah langsung menjadi progesteron atau menjadi
17ß-estradiol dengan dehydroepiandrosterone sebagai perantara. Selanjutnya progesteron diubah menjadi testosteron, yang merupakan produk utama sekresi
sel Leydig pada testis dan mengalami konversi menjadi dihydrotestosterone
sebelum terikat oleh reseptor androgen (Litwack dan Schmidt 2002). Konversi
Gambar 4 Struktur kolesterol (A) dan hormon kelamin, B. Testosteron, C. Estron, D. Estradiol dan E. Estriol (Montgomery et al. 1993)
A
B
C
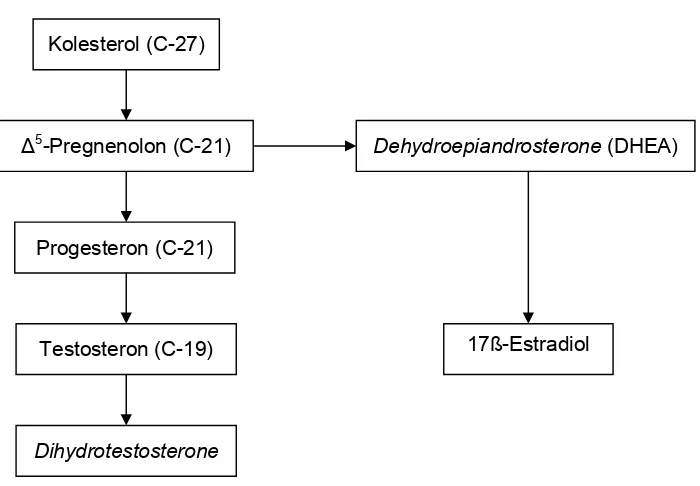
Gambar 5 Konversi kolesterol menjadi hormon kelamin (Litwack dan Schmidt 2002)
Sintesis testosteron pada tubuh hewan jantan terjadi dalam suatu jaringan
yang merespon androgen sehingga terbentuk metabolit androgenik yang
berperan dalam pengaturan tanda-tanda seks sekunder. Dalam hal ini, hipofisa
anterior mensekresi Follicle Stimulating Hormone (FSH) dan Luteinizing Hormone (LH) dimana LH mengatur aktivitas sel-sel leydig testis dalam memproduksi testosteron, sementara FSH merangsang spermatogenesis di
dalam tubuli seminiferi. Proses ini terjadi pada pejantan yang telah mencapai
kematangan seksual (Litwack dan Schmidt 2002).
C. Ekstraksi Steroid
Ekstraksi adalah pemisahan suatu komponen dengan menggunakan
pelarut (Austin 1986 seperti dikutip Heryani 2002). Ekstraksi dapat dilakukan
dengan tiga cara yaitu dengan metode maserasi, refluks (soxhlet) dan perkolasi.
Pada metode maserasi bahan didiamkan pada suhu rendah, sedangkan pada
metode refluks bahan dilarutkan dengan pelarut dan menggunakan suhu yang
lebih tinggi dari suhu kamar. Kolesterol (C-27)
Δ5
-Pregnenolon (C-21) Dehydroepiandrosterone (DHEA)
Progesteron (C-21)
Testosteron (C-19)
Dihydrotestosterone
Pelarut yang digunakan pada ekstraksi tergantung dari sifat komponen
yang akan diisolasi. Salah satu sifat yang penting dalam pemilihan pelarut
adalah sifat polaritas bahan. Polaritas bahan harus sama dengan polaritas
pelarut agar bahan dapat larut pada pelarut yang digunakan. Ada tiga jenis
pelarut yaitu pelarut polar (metanol, etanol dan air), pelarut semi polar (kloroform,
dietil eter dan etil asetat) dan pelarut non polar (heksan, sikloheksan dan toluen)
(Houghton dan Raman 1998).
Beberapa penelitian telah berhasil mengekstraksi senyawa steroid dari
senyawa alam dengan metode yang berbeda. Metode yang digunakan
Touchtone dan Kasparow yang dikutip Riris (1994), berhasil diterapkan untuk
mengekstraksi steroid dari kerang hijau (Riris 1994), lintah laut Discodoris sp (Ibrahim 2001), dan lintah laut Eunice siciliensis (Alwir 2001), sedangkan metode yang digunakan oleh Bahti et al. (1985) untuk mengekstraksi steroid dari daun kamboja juga telah berhasil diterapkan untuk mengekstraksi steroid dari tabat
barito dengan beberapa modifikasi (Heryani 2002). Pada metode yang
digunakan oleh Touchtone dan Kasparow (1970) dalam Riris (1994), pelarut yang digunakan adalah aseton dengan cara maserasi, sedangkan pada metode
yang digunakan oleh Bahti et al. (1985), pelarut yang digunakan adalah metanol dengan menggunakan soxhlet.
Metode yang digunakan oleh Stonik et al. (1998) dan Ponomarenko et al.
(2001) pada ekstraksi sterol bebas dari teripang, pelarut yang digunakan adalah
etanol dengan cara maserasi pada suhu ruang, kemudian dilanjutkan dengan
kloroform menggunakan soxhlet. Ekstraksi berikutnya menggunakan aseton
sebagai pelarut. Metode ekstraksi yang lain untuk mengisolasi steroid dari
teripang adalah menggunakan metanol pada suhu ruang (Moraes et al. 2004),
D. Teknologi Membran
Membran dapat diklasifikasikan berdasarkan material asal, morfologi, bentuk dan fungsinya (Wenten 1999). Berdasarkan material asal, membran dibedakan menjadi dua golongan, yaitu membran alamiah dan membran sintetis. Membran alamiah merupakan membran yang terdapat pada sel tumbuhan, hewan dan manusia. Membran ini memiliki perbedaan dasar dalam struktur dan fungsi dari membran sintetis. Membran ini berfungsi untuk melindungi isi sel dari pengaruh luar dan membantu proses metabolisme organisme dengan sifat permeabelnya.
Membran sintetis merupakan membran yang dibuat sesuai dengan
kebutuhan dan sifatnya disesuaikan dengan membran alamiah. Membran
sintetis dibagi lagi menjadi membran organik dan membran anorganik. Membran
sintetis ada yang terbuat dari polimer seperti selulosa asetat, selulosa triasetat,
polipropilen, polietilen, poliamida, polisulfon, polietersulfon, juga ada yang terbuat
dari keramik, gelas dan logam (Wenten 1999).
Berdasarkan morfologinya, membran dibagi menjadi dua golongan, yaitu
membran asimetrik dan simetrik (Wenten 1999). Membran asimetrik merupakan
suatu membran yang struktur porinya tidak seragam. Membran dengan struktur
asimetrik memiliki dua lapisan yaitu: (1) lapisan penyangga atau pendukung yang
memiliki ketebalan sebesar 20-100 um dan memiliki rongga pori yang makin ke
bawah makin besar, (2) lapisan aktif memiliki ketebalan 0,2-1,0 µm, ukuran pori
1,0-10 µm dan memiliki pori yang rapat serta lapisan ini mengadakan kontak
langsung dengan larutan. Membran asimetrik dibagi lagi menjadi dua bagian
yaitu membran inverse fasa dan membran komposit. Kedua membran di atas
memiliki perbedaan pada jumlah membrannya, dimana membran inverse fasa
terdiri dari satu jenis membran sedangkan membran komposit terdiri dari dua
jenis membran dengan perbandingan tertentu.
Membran simetrik merupakan suatu membran yang memiliki struktur pori
yang seragam. Pembuatan membran dilakukan pada ruangan tertutup dan jenuh
dengan non pelarut. Agar konsentrasi pelarut dapat berlangsung tetap maka
penambahan non pelarut dilakukan selambat mungkin sehingga struktur
membran yang diperoleh memiliki keseragaman dan homogen (Wenten 1999).
Berdasarkan bentuknya, membran dibagi menjadi dua golongan, yaitu
membran datar dan tubular (www.osmonics.com). Membran datar memiliki
bentuk melebar dan penampang lintang yang besar. Beberapa macam membran
datar, antara lain: (1) membran datar yang terdiri dari satu lembar, (2) membran
datar bersusun, terdiri dari beberapa lembar yang disusun bertingkat dengan
membran spiral bergulung, yaitu membran yang disusun bertingkat dan digulung
dengan pipa sentral membentuk spiral. Membran tubular terdiri dari tiga macam,
yaitu: (1) membran serat berongga (diameter < 0,5 mm), (2) membran kapiler
(diameter 0,5-5,0 mm), dan (3) membran tubular (diameter > 5 mm).
Berdasarkan fungsinya membran dibedakan seperti dijelaskan di bawah ini
(www.osmonics.com).
1) Membran mikrofiltrasi, dimana proses pemisahan antar partikel (bakteri dan
ragi) dan berfungsi untuk menyaring makromolekul > 500,000 g/mol atau
partikel berukuran 0,1-10 µm. Tekanan yang digunakan 0,5-2 atm. Tekanan
osmotik diabaikan dan tidak memperhitungkan adanya polarisasi konsentrasi.
Membran ini memiliki struktur simetrik dan asimetrik.
2) Membran ultrafiltrasi, yaitu proses pemisahan antar molekul dan berfungsi
untuk menyaring makromolekul > 5000 g/mol atau partikel berukuran
0.001-0.1 µm. Tekanan yang digunakan 1,0-3,0 atm. Tekanan osmotik diabaikan
dan tidak memperhitungkan adanya polarisasi konsentrasi. Membran di atas
memiliki struktur asimetrik.
3) Membran nanofiltrasi, mempunyai ukuran pori sekitar 1 nm. Banyak
diterapkan pada pemisahan garam dari air dan fraksinasi garam dan molekul
yang kecil di berbagai industri. Selektif untuk partikel dengan bobot molekul
200-1000 Da.
4) Membran osmosa balik (reverse osmosis/RO), berfungsi untuk menyaring garam-garam organik > 50 g/mol atau partikel berukuran 0,0001-0,001 µm.
Tekanan yang digunakan adalah antara 8,0-12,0 atm.
5) Membran dialisis, berfungsi untuk memisahkan larutan koloid yang
mengandung elektrolit dengan bobot molekul kecil. Zat terlarut pada larutan
yang konsentrasinya tinggi akan menembus membran kearah larutan yang
konsentrasinya rendah.
6) Membran elektrodialisis, berfungsi untuk memisahkan larutan dengan
membran melalui pemberian muatan listrik, atau gaya gerak listrik sebagai
pendorong.
2) Filtrasi Membran
cairan. Proses filtrasi dengan menggunakan membran sering digunakan untuk memisahkan padatan yang tidak terlarut dalam produk cair.
Proses filtrasi diklasifikasikan berdasarkan ukuran molekul dari komponen
yang tertahan oleh media filter. Filtrasi dibagi menjadi dua bagian yaitu filtrasi
partikel konvensional (dead-end filtration) dan proses filtrasi membran (cross-flow filtration) (Eykamp 1997). Pemisahan partikel besar yang tersuspensi berukuran lebih dari 10 μm dapat menggunakan filtrasi partikel konvensional, sedangkan
untuk memisahkan zat berukuran kurang dari 10 μm menggunakan filtrasi
membran (Wenten 1999).
Wenten (1999) menyatakan bahwa terdapat beberapa perbedaan antara
filtrasi partikel konvensional dan filtrasi membran, sebagai berikut:
1) Media filtrasi yang digunakan pada proses konvensional berstruktur terbuka
dan tebal, sedangkan pada membran tergantung ukuran pori dan tipis
2) Tekanan filtrasi membran yang digunakan adalah daya pendorong untuk
pemisahan dan pada filtrasi konvensional tekanan digunakan untuk
mempercepat proses
3) Desain proses. Aliran umpan pada filtrasi konvensional tegak lurus media penyaring dan dilakukan pada sistem terbuka, sedangkan filtrasi membran
menggunakan desain silang atau aliran tangensial dan dilakukan pada sistem
tertutup.
4) Derajat pemisahan. Pada filtrasi konvensional, material yang tersuspensi dapat dipisahkan secara sempurna dari cairan. Filtrasi membran hanya
dapat memekatkan material yang tertahan dalam jumlah kecil terhadap
cairan semula.
E. Teknologi Membran pada Filtrasi Steroid
Teknologi membran telah digunakan dalam proses penanganan air
limbah yang mengandung hormon steroid. Hasil penelitian Nghiem et al. (2002) dan Schaefer et al. (2003) menunjukkan bahwa membran nanofiltrasi dan RO dapat digunakan untuk memisahkan estron dari air limbah.
Pada penanganan air limbah secara konvensional masih dihasilkan air
air olahan (secondary effluent) ini masih cukup berbahaya bagi organisme perairan, khususnya ikan (Johnson dan Sumpter 2001 yang dikutipNghiem et al. 2002). Steroid yang terdapat pada air limbah tersebut berasal dari air limbah
rumah sakit dan air limbah rumah tangga. Steroid pada air limbah ini umumnya
disebut endocrine disrupters, karena steroid tersebut dapat masuk dalam sistem endokrin dan menyerupai hormon, sehingga dapat memicu atau menghambat
reseptor. Hal ini dapat mengganggu respon hormon pada manusia dan hewan
(Nghiem et al. 2002). Oleh karena itu, diperlukan teknologi yang lebih baik untuk memenuhi persyaratan yang ketat dalam penanganan air limbah, seperti
penggunaan membran nanofiltrasi dan RO untuk menghilangkan steroid
estrogen dari air limbah.
F. Ayam sebagai Hewan Percobaan
Hewan laboratorium atau hewan percobaan adalah hewan yang sengaja
dipelihara dan diternakkan untuk dimanfaatkan sebagai hewan model guna
mempelajari dan mengembangkan berbagai macam bidang ilmu dalam skala
penelitian atau pengamatan laboratorik (Malole dan Pramono 1989). Ayam
merupakan salah satu hewan yang sering digunakan dalam percobaan
aprodisiaka. Ha lini disebabkan ayam jantan memberikan respon yang sangat
cepat terhadap perlakuan hormon testosteron, selain itu ayam juga merupakan
hewan yang cepat berkembang, mudah dipelihara dalam jumlah banyak serta
sifat anatomis dan fisiologisnya terkarakterisasi dengan baik.
Pubertas atau dewasa kelamin merupakan suatu periode dalam
kehidupan makhluk jantan dan betina, dimana proses-proses reproduksi mulai
berlangsung (Hafez 1992). Periode tersebut ditandai dengan kemampuan
hewan untuk memproduksi benih pertama kali dan kemampuan untuk melakukan
perkembangbiakan.
Birahi merupakan kegiatan fisiologis pada hewan yang dimanifestasikan
dengan munculnya gejala keinginan untuk melakukan aktivitas kawin. Pada
hewan betina, pada kondisi birahi, folikel akan tumbuh dan berkembang menjadi
folikel de Graf dan ovum mengalami perubahan-perubahan ke arah pematangan.
Estradiol yang dihasilkan oleh folikel tersebut menyebabkan perubahan pada
saluran reproduksi (Tolihere 1981).
Pada hewan jantan kondisi birahi dipengaruhi oleh hormon jantan atau
tubulus seminiferus dan sel-sel interstitial seperti sel Leydig. Sel Leydig berperan
dalam biosintesa hormon testosteron, sehingga memungkinkan berlangsungnya
proses spermatogenesis di dalam testis (Turner dan Bagnara 1976).
Hormon testosteron dapat menginduksi peningkatan anabolisme protein
pada jaringan tubuh. Selain mempengaruhi kondisi birahi, jika plasma
testosteron cukup dalam tubuh, maka daya retensi nitrogen sebagai protein tetap
berlangsung sehingga memungkinkan terjadinya peningkatan bobot organ tubuh
(McDonald 1980). Hasil penelitian Riani (1990) menunjukkan bahwa pemberian
hormon metil testosteron dan ekstrak gonad jantan ikan mas pada anak ayam
jantan yang berusia tujuh hari, memperlihatkan munculnya ciri-ciri seksual
sekunder yang sangat dini, berupa munculnya jengger, munculnya taji pada kaki
serta munculnya sifat-sifat kejantanan seperti suara berkokok dan munculnya
keinginan untuk berlaga.
G. Aprodisiaka
Aprodisiaka (aphrodisiac) berasal dari bahasa Yunani, Aphrodite yaitu salah satu nama dewa dalam kepercayaan Yunani, Dewi Cinta. Aprodisiaka
adalah bahan, baik berupa obat ataupun makanan yang dapat meningkatkan
gairah seksual atau merangsang libido (Wikipedia 2004). Walker dalam Smith (2006) menyebut makanan sehat yang dapat meningkatkan libido di atas dengan
‘nutridisiac’.
Aprodisiaka dalam tubuh dapat menyebabkan pelebaran pembuluh darah
atau bersifat vasodilator, sehingga terjadi pembendungan darah yang
menyebabkan rangsangan lebih baik. Testosteron sebagai hormon steroid dapat
dijadikan bahan aktif aprodisiaka pada laki-laki. Di dalam tubuh manusia,
hormon steroid tersebut selain mengatur pertumbuhan organ kelamin juga dapat
meningkatkan libido.
Schoeder et al. (2003) menyatakan bahwa pemberian hormon jantan atau androgen yaitu testosteron juga dapat meningkatkan kekuatan dan massa otot.
Kadar testosteron dalam tubuh menurun seiring dengan pertambahan usia.
Pemberian testosteron pada laki-laki lanjut usia juga dapat meningkatkan
kekuatan otot, hal ini karena pemberian testosteron dapat meningkatkan sintesis
protein otot rangka (Urban et al. 1995).
Saat ini telah dikenal beberapa sumber penghasil senyawa alami yang
dapat dijadikan sebagai aprodisiaka, baik dari tumbuhan maupun hewan seperti
lebih dari 2000 tahun digunakan dalam pengobatan Cina. Selain dimanfaatkan
sebagai tonik, komponen aktif ginseng juga bermanfaat sebagai antikanker, anti-aging, dan anti-stress. Hal ini karena ginseng mengandung ginsenoside, polisakarida, peptida, polyacetylenic alcohol dan asam lemak (Gillis 1997 yang dikutipLee et al. 2003).
Selain tanaman obat, beberapa hewan laut juga digunakan sebagai
aprodisiaka, diantaranya adalah kuda laut dan kerang. Minyak kura-kura atau
yang biasa disebut minyak bulus juga dapat digunakan sebagai aprodisiaka
3. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan dari bulan Maret sampai Desember 2004 bertempat di Laboratorium Pengawasan Mutu, TIP-IPB; Balai Pengkajian Bioteknologi, Puspiptek-BPPT Serpong; Laboratorium Biokimia, THP-IPB; Laboratorium Biokimia, TPG-IPB; Laboratorium Terpadu, FKH-IPB; Kandang Percobaan, Fakultas Peternakan-IPB. Pada bulan Agustus sampai Oktober 2005 penelitian dilanjutkan di Institute of Marine Biotechnology-Greifswald, Jerman.
B. Bahan dan Alat
Sampel yang digunakan adalah teripang yang didapat dari Balai Budidaya Laut
(BBL), Lampung dan anak ayam jantan strain Ross 308 dengan nama dagang
“Jumbo 747” dari PT. Cibadak Indah Sari Farm, Leuwiliang untuk bioassay.
Bahan-bahan lain yang digunakan adalah Bahan-bahan-Bahan-bahan untuk analisis kadar N, kadar lemak,
testosteron dan kolesterol.
Peralatan yang digunakan adalah membran nanofiltrasi dengan ukuran 1000 Da yang
ada di Laboratorium Bioteknologi, Puspiptek, Serpong, Kromatografi Lapis Tipis
(Thin Layer Chromatography/TLC), High Performance Liquid Chromatography
(HPLC), water bath, sentrifuge, pH-meter, milimeter skrup dan peralatan gelas.
C. Prosedur Penelitian 1) Ekstraksi Steroid
Ekstraksi steroid dilakukan berdasarkan metode yang dilaporkan oleh
Touchstone dan Kasparow (1970) yang dikutip Riris (1994). Sebanyak 20 g
daging atau jeroan teripang dalam kondisi beku dan kering yang telah
dihomogenkan diblender, ditambahkan 45 ml aseton dingin, kemudian disimpan
selama 24 jam dalam ruang dingin. Selanjutnya disentrifugasi pada 5000 rpm
selama 15 menit. Endapan yang diperoleh dipisahkan dari fase cairnya. Fase
cairnya kemudian diuapkan dalam penangas air (water bath) pada suhu 40oC. Residu yang diperoleh diekstraksi dua kali dalam larutan etil asetat, kloroform
dan air (1:1:1) dengan menggunakan corong pemisah sehingga terbentuk dua
lapisan. Pelarut pengekstrak kemudian diuapkan pada penangas air pada suhu
40oC. Ekstrak tersebut kemudian digunakan untuk identifikasi keberadaan steroid, fraksinasi dengan TLC dan filtrasi membran serta bioassay.
2) Identifikasi Keberadaan Steroid
dan 0,5 ml khloroform pada ekstrak teripang, kemudian diaduk. Selanjutnya ditambahkan satu tetes asam sulfat pekat. Jika terbentuk warna hijau berarti ekstrak tersebut mengandung steroid (Cook 1958; Bahti et al. 1983; Harborne 1987).
Pemisahan steroid dilakukan dengan teknik TLC. Prosedur kerjanya
adalah sebagai berikut:
1. Sampel, beberapa fraksi standar dan lempeng tipis silika gel 60 F254 katalog
Art 5554 dengan ukuran panjang 10 cm dan lebar 5 cm disiapkan. Sampel
dan semua fraksi standar diambil sedikit (0,35 g) kemudian dilarutkan
kedalam 1,5 ml khloroform.
2. Eluen yang digunakan adalah etanol dan kloroform dengan perbandingan 3 :
7. Eluen dimasukkan ke dalam tabung kromatografi hingga 2 cm tingginya
dari dasar tabung dan diletakkan dengan kertas saring kemudian ditutup
rapat agar jenuh dengan uap eluen.
3. Larutan ekstrak sampel diteteskan dengan pipa kapiler pada lempeng silika
gel. Penetesan dilakukan pada jarak 1 cm dari salah satu ujung lempeng
tersebut. Di lain tempat diteteskan juga beberapa standar steroid yang
disediakan.
4. Ujung lempeng yang terdekat pada tempat penetesan dicelupkan ke dalam
tabung kromatografi yang sudah jenuh dengan eluen. Kemudian ditutup
rapat dan dibiarkan pelarut naik sampai batas yang ditentukan.
5. Setelah dielusi pada batas tertentu, lempeng tersebut diangkat dan
selanjutnya dikeringkan dalam oven selama beberapa menit.
6. Lempeng langsung dideteksi dengan sinar UV dengan panjang gelombang
254 nm dan 366 nm.
3) Filtrasi Steroid dengan Membran Nanofiltrasi
Ekstrak teripang yang didapat selanjutnya difiltrasi dengan membran nanofiltrasi yang mempunyai selektivitas untuk steroid. Permeat yang dihasilkan merupakan bioaktif target kemudian diamati kemurniannya secara kualitatif dengan uji Liebermann-Burchard.
4) Pengukuran Kadar Testosteron dan Kolesterol dari Serum Darah Pengukuran kadar testosteron dan kolesterol dalam serum darah anak
Chromatography (HPLC). Prosedur pengukuran dilakukan seperti berikut ini (Kurečková et al. 2002).
Prinsip prosedurnya didasarkan pada deteksi testosteron dan kolesterol
sampel pada panjang gelombang 240-242 nm. Analisis dilakukan dengan
menggunakan sistem HPLC yang terdiri dari beberapa peralatan, seperti: pompa
LCP 4000 Ecom bertekanan tinggi (Praha, Republik Cekoslovakia), gradient programmer GP 5 Ecom, kolom pengaman C18, 4 mm L x 3 mm I.D. Phenomenex (Torrance, CA, USA). Prosedur pengukuran selengkapnya adalah
sebagai berikut:
1. Dipersiapkan kolom HPLC analitik 125 x 4 mm dengan LiChrospher 100
RP-18e 5 µm (Merck) dengan detektor UV pada panjang gelombang 240-242
nm.
2. Dipersiapkan tabung ke-A, B, C, D, E dan F serta duplonya untuk sampel
serum darah yang akan dianalisis.
3. Dipipet 50 μl dari setiap sampel ke dalam tabung sampel yang telah
ditentukan (sampel pertama ke dalam tabung pertama, sampel kedua ke
dalam tabung kedua dan seterusnya). Masing-masing duplo. 4. Sebanyak 20 µl dari masing-masing sampel diinjeksikan.
5. Laju alir fase gerak adalah 0,7 ml/menit dan pemisahan dicapai dengan
menggunakan gradien pemisah (sequence), yaitu pelarut yang digunakan adalah metanol-air dengan komposisi yang diatur dari 45:55 (v/v) sampai
85:15 (v/v) selama 15 menit.
6. Steroid dideteksi pada panjang gelombang 240 nm dan 242 nm.
5) Analisis Kadar N Bahan Contoh (Bubuk Teripang dan Feses)
Analisis kadar N dilakukan dengan metoda makro-kjeldahl (Sudarmadji et al. 1984). Satu gram contoh (=x) ditimbang kemudian dimasukkan ke dalam labu destruksi dan ditambahkan sebanyak 6 gram katalis (campuran selen) serta 25
ml H2SO4 pekat (teknis) dan dicampur sampai homogen. Campuran tersebut
dipanaskan (mulai dengan nyala kecil) diatas nyala pembakar bunsen di dalam
lemari asam. Bila tidak berbuih lagi, barulah nyala diperbesar. Sampel terus
Setelah itu labu destruksi didinginkan dan larutan dimasukkan ke dalam
labu penyuling dan diencerkan dengan 300 ml air. Selanjutnya ditambah
beberapa butir batu didih dan larutan dijadikan basa dengan menambahkan
kira-kira 100 ml NaOH 33%, labu dipasang dengan cepat ke alat penyuling. Sulingan
(NH3 dan air) ditangkap dalam satu labu erlenmeyer yang terlebih dahulu telah
diberi sejumlah H2SO4 dengan titrasi tetentu (misalnya 0,3 N) yang jumlahnya
tergantung pada banyaknya N yang terikat dan 2 tetes indikator campuran.
Penyulingan diteruskan, hingga semua N dari cairan tertangkap oleh
H2SO4 yang ada dalam labu erlenmeyer (bila 2/3 dari cairan dalam labu
penyuling telah menguap). Labu erlenmeyer berisi sulingan diambil dan dititar
kembali dengan standar NaOH dengan titar tertentu (0,1 N) = Z ml. Perubahan
warna dari biru ke hijau menandakan titik akhir. Selanjutnya nilai titar
dibandingkan dengan titar blanko = Y ml.
( Y – Z ) x titar x 0,014 x 6.25 x 100%
Z
6) Analisis Serapan N pada Anak Ayam
Analisis serapan N pada anak ayam dilakukan dengan metode
makro-kjeldahl (Sudarmadji et al. 1984). Sebelumnya ayam dipuasakan selama 12 jam. Pakan yang akan diberikan ditimbang dahulu. Pakan ini diberikan untuk
konsumsi selama 24 jam. Selama 24 jam tersebut fesesnya ditampung,
kemudian ditimbang. Dilakukan pengeringan dengan oven, kemudian digerus.
Jumlah N yang terdapat dalam feses tersebut dianalisis seperti cara di atas.
%N Pakan - % N Feses x 100%
% N Pakan
7) Analisis Kadar Lemak pada Bubuk Teripang
Analisis kadar lemak dilakukan dengan metode yang dilaporkan oleh
Sudarmadji et al. (1984). Labu penyari dengan beberapa butir batu didih di dalamnya, dikeringkan dalam alat pengering pada suhu 105-110ºC selama 1
jam. Selanjutnya labu penyari didinginkan dalam eksikator, kemudian ditimbang
= a gram. Ditimbang sebanyak 5 gram contoh = X gram (banyak sedikitnya
contoh yang ditimbang tergantung pada kadar lemak bahannya) lalu dimasukkan Kadar N =
ke dalam selongsong penyari (dapat juga digunakan kertas saring yang dibuat
seperti kantong yang ditutup dengan kapas yang tidak berlemak).
Selongsong penyari dimasukkan ke dalam alat soxhlet dan diekstrak
dengan eter minyak tanah, etil eter atau kloroform di atas penangas air (water bath). Setelah ekstraksi selesai (24-48 jam sampai eter minyak tanah di dalam soxhlet jernih) labu penyari dibuka dan dikeringkan untuk menghilangkan eter
minyak tanah secepat mungkin. Kemudian labu penyari dikeringkan dalam alat
pengering pada suhu 105-1100C selama 1 jam.
Selanjutnya labu penyari didinginkan dalam eksikator dan ditimbang.
Pekerjaan mengeringkan dan menimbang diulangi, hingga tercapai bobot yang
tetap (b gram).
b - a
X
8) Karakterisasi Senyawa Steroid dari Ekstrak Teripang
Karakteristik ekstrak steroid dari teripang yang diamati adalah warna, derajat keasaman (pH), kelarutan, stabilitas, antibakteri dan antifungi. Warna ekstrak diamati secara visual dan pH diukur dengan menggunakan pH-meter. Kelarutan ekstrak steroid diamati dengan menggunakan pelarut aseton, etil asetat, kloroform, metanol dan air.
Pengujian stabilitas ekstrak steroid dari teripang dilakukan berdasarkan aktivitas antibakterinya setelah penyimpanan selama 10 bulan pada temperatur + 10oC. Pengujian aktivitas antibakteri dan antifungi dijelaskan seperti di bawah ini sebagaimana metode yang digunakan oleh Institute of Marine Biotechnology, Greifswald-Jerman.
a. Antibakteri
Pengujian aktivitas antibakteri dilakukan dengan metode difusi agar (agar
diffusion assay). Biakan bakteri uji diambil sebanyak dua ose kemudian
disuspensikan pada larutan buffer sebanyak 2 ml. Sebanyak 200 µl dari suspensi bakteri uji tersebut dimasukkan ke dalam 20 ml media agar yang masih cair lalu digoyang secara perlahan agar homogen. Selanjutnya media agar tersebut dituangkan ke dalam cawan petri yang steril dan dibiarkan pada suhu kamar dalam keadaan aseptik sampai media agar membeku. Setelah agar membeku, diletakkan di atasnya paper disc yang telah ditetesi ekstrak steroid. Paper disc yang digunakan berdiameter 6 mm.
Media agar yang telah membeku kemudian disimpan di refrigerator selama dua jam dengan posisi terbalik. Selanjutnya media agar diinkubasi selama 18 jam pada suhu 37oC dengan posisi terbalik. Setelah diinkubasi aktivitas bakteri dapat diamati yaitu dengan mengukur diameter hambatan yang terbentuk di sekeliling
paper disc. Besarnya diameter hambatan yang terbentuk diukur dalam mili meter.
b. Antifungi (antikapang)
Fungus (kapang) yang digunakan dalam uji aktivitas antikapang adalah
Candida maltosa. Pengujian aktivitas antikapang dilakukan sebagaimana
pengujian aktivitas antibakteri, hanya saja inkubasi dilakukan pada posisi tidak terbalik.
9) Uji Aktivitas Biologis/Bioassay pada Anak Ayam Jantan (Alwir 2001)
Sebelum perlakuan, anak ayam jantan divaksinasi ND (New Castle
Disease) secara tetes hidung dan ditimbang bobot badannya kemudian diukur panjang, lebar dan tinggi jengger. Anak ayam jantan diletakkan dalam kandang
percobaan yang dilengkapi dengan lampu listrik 25 watt. Sebelum perlakuan,
anak ayam jantan dibiarkan beradaptasi di dalam kandang selama seminggu.
Dalam setiap kandang terdapat enam ekor anak ayam jantan yang
masing-masing mendapat perlakuan yang sama.
Pemberian perlakuan ekstrak steroid dan kontrol pada anak ayam jantan
dilakukan secara oral setiap hari selama 18 hari pengamatan dimulai dari umur
10 hingga 27 hari. Selama beradaptasi dan pemberian pakan, masing-masing
anak ayam diberi ransum yang sama dan air minum secara ad libitum (tidak terbatas). Pemberian ransum bebas sterol dan air minum ini dilakukan dengan
cara menaruhnya dalam tempat-tempat yang diikatkan dalam kandang.
Setiap hari anak ayam jantan ditimbang bobot badannya dan tiap dua hari
sekali diukur panjang, lebar dan tinggi jenggernya. Proses pengukuran jengger
hewan percobaan dapat dilihat pada Lampiran 1.
Pada hari ke-28 hingga ke-30 dilakukan pengamatan serapan N, dimana
dua ekor anak ayam dari masing-masing perlakuan ditempatkan secara terpisah
pada kandang yang dilengkapi dengan alas untuk menampung feses anak ayam
tersebut. Pada hari ke-31, anak ayam disembelih dan diambil darahnya dari
leher. Selanjutnya anak ayam dibedah dan diambil jengger, hati, limpa, bursa
fabrisius dan testisnya, kemudian ditimbang. Serum darah dipersiapkan untuk
pengukuran kadar kolesterol dan testosteron. Secara garis besar, kerangka
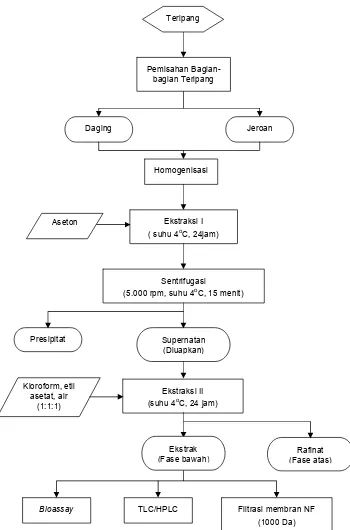
Gambar 6 Kerangka kerja penelitian (Modifikasi dari Alwir 2001) Pemisahan
Bagian-bagian Teripang
Daging Jeroan
Homogenisasi
Ekstraksi I ( suhu 4oC, 24jam)
Sentrifugasi
(5.000 rpm, suhu 4oC, 15 menit)
Supernatan (Diuapkan) Presipitat
Ekstraksi II (suhu 4oC, 24 jam)
Rafinat (Fase atas)
Filtrasi membran NF (1000 Da)
Bioassay TLC/HPLC Ekstrak (Fase bawah) Aseton
Kloroform, etil asetat, air
(1:1:1)
D. Rancangan Penelitian
Rancangan penelitian yang digunakan pada tahap bioassay adalah
Rancangan Acak Lengkap (RAL) dengan enam perlakuan dan enam ulangan,
dimana hewan uji yang digunakan adalah 36 ekor anak ayam jantan yang
dianggap homogen. Model matematis rancangan percobaan tersebut adalah
seperti di bawah ini (Steel dan Torrie 1995).
Yij = µ + Pi + εij
Keterangan:
Yij = Nilai pengamatan (respon) dari faktor perlakuan ke-i dan ulangan ke-j
µ = Nilai rata-rata yang sesungguhnya
Pi = Pengaruh perlakuan ke-i
εij = Pengaruh galat pada perlakuan ke-i dan ulangan ke-j
Percobaan dirancang untuk mendapatkan data pengaruh senyawa steroid
teripang terhadap bobot badan, serapan N, bobot testis, limpa, hati, kadar
kolesterol dan trigliserida darah anak ayam jantan. Perlakuan yang dicobakan
dijelaskan seperti di bawah ini (Modifikasi dari Alwir 2001).
1. Pemberian ransum basal tanpa senyawa steroid dan dicekok 0,5 ml minyak
jagung sebagai kontrol negatif setiap hari sekali
2. Pemberian ransum basal dan dicekok 0,5 ml senyawa steroid teripang
kering (ekstrak kasar) yang konsentrasinya 0,4 g/ml setiap hari sekali
3. Pemberian ransum basal dan dicekok 0,5 ml senyawa steroid teripang
basah (ekstrak kasar) yang konsentrasinya 0,4 g/ml setiap hari sekali
4. Pemberian ransum basal dan dicekok 0,5 ml metil testosteron (Argent Laboratories Inc.) dengan konsentrasi 0,4 mg/ml setiap hari sekali sebagai kontrol positif (a)
5. Pemberian ransum basal dan dicekok 0,5 ml aprodisiaka komersial (Levitra)
dengan konsentrasi 0,4 mg/ml setiap hari sekali sebagai kontrol positif (b)
6. Pemberian ransum basal dan dicekok 0,5 ml tepung teripang kering yang
konsentrasinya 1 g/ml setiap hari sekali.
Data yang diperoleh dianalisis dengan ANOVA (analysis of variance). Jika terdapat perbedaan yang nyata dilanjutkan dengan uji beda nyata terkecil,
4. HASIL DAN PEMBAHASAN
A. Bahan Baku
Teripang yang digunakan dalam penelitian ini adalah teripang pasir
(Holothuria scabra) yang diperoleh dari Balai Budidaya Laut (BBL), Lampung. Teripang tersebut yaitu sebanyak 123 ekor merupakan hasil tangkapan dari
alam, yakni perairan Teluk Lampung (Gambar 7). Umur teripang yang
digunakan menurut peneliti BBL diperkirakan berkisar antara 1,5-2 tahun.
Secara ringkas karakteristik teripang yang digunakan untuk penelitian ini dapat
dilihat pada Tabel 5.
Gambar 7 Teripang pasir yang digunakan dalam penelitian
Tabel 5 Karakteristik teripang dari perairan Teluk Lampung
Karakteristik Deskripsi
Bentuk tubuh Bulat panjang dengan permukaan tubuh
kasar
Warna Abu-abu sampai kehitaman dengan garis
melintang berwarna hitam
Umur (tahun) 1,5-2
Bobot (g) 124,55-136,52
Panjang (cm) 18,85-20,86
Proporsi antara daging dan jeroan adalah 2,6:1 (b/b). Proporsi bobot
kering dan bobot basah (segar beku) daging teripang adalah 1:6, sedangkan
B. Analisa Proksimat Daging dan Jeroan Teripang
Hasil analisa proksimat pada daging teripang, baik daging segar maupun
kering disajikan pada Tabel 6 berikut ini. Analisa proksimat dilakukan untuk
mengetahui kandungan protein, lemak, air dan abu.
Tabel 6 Hasil analisa proksimat daging dan jeroan teripang
Komponen
Kandungan (%) Daging basah Daging
kering
Jeroan kering
Protein 8,37+0,77 34,13+5,62 2,39+0,10 Lemak 0,87+0,01 2,17+0,03 1,52+0,01 Air 80,72+0,22 3,07+0,03 2,93+0,02 Abu 9,18+0,50 42,57+0,65 53,87+0,07
Tabel 6 di atas menunjukkan bahwa kandungan protein daging teripang
tergolong sedang, yaitu mencapai 8,37 % (dengan kadar air 80,72 %) dan 34,13
% untuk daging kering. Hasil analisa tersebut menunjukkan bahwa teripang
termasuk hasil perikanan berprotein sedang dan rendah lemak (kurang dari 5 %).
Kandungan protein hasil perikanan umumnya mencapai 15-25 % dari total bobot
daging (dengan kadar air 70-85 %) (Nurjanah et al. 2004).
C. Ekstraksi Steroid
Pemilihan aseton sebagai pelarut dalam ekstraksi mengacu pada metode
yang digunakan oleh Touchtone dan Kasparow (1970) seperti dikutip Riris
(1994). Namun demikian, karena bahan baku yang digunakan berbeda, yaitu
antara kerang hijau dan teripang, maka memungkinkan steroid yang terkandung
juga memiliki karakteristik yang berbeda. Oleh karena itu, selain aseton juga
digunakan metanol dan air (pelarut polar), kloroform dan etil asetat (pelarut semi
polar) serta heksan (pelarut non polar). Hasil pemilihan jenis pelarut tersebut
menunjukkan bahwa secara kualitatif (visual) ekstrak aseton lebih banyak
Gambar 8 Perbandingan kualitatif kandungan steroid pada ekstrak aseton (A dan B), metanol (C), heksan (D) dan etil asetat (E)
Ekstraksi steroid selanjutnya dilakukan berdasarkan metode yang
dilaporkan oleh Touchstone dan Kasparow (1970) seperti dikutip Riris (1994).
Hasil ekstraksi dari 1 kg daging teripang kering diperoleh ekstrak kasar 8,16 g;
dari 1 kg daging teripang basah diperoleh ekstrak kasar 12,96 g, sedangkan
ekstrak kasar dari 1 kg jeroan kering diperoleh 17,96 g dan dari 1 kg jeroan
basah diperoleh 21,28 g. Rendemen yang diperoleh dari proses ekstraksi
selengkapnya dapat dilihat pada Tabel 7.
Tabel 7 Rendemen ekstraksi steroid dari teripang pasir
Bahan (1 kg) Rendemen ekstrak kasar (g)
Persentase (%)
Daging kering 8,16+0,07 0,816
Jeroan kering 17,96+0,11 1,796
Daging basah 12,96+0,40 1,296
Jeroan basah 21,28+1,19 2,128
Tabel 7 di atas menunjukkan bahwa daging dan jeroan teripang basah
lebih banyak mengandung steroid dibandingkan sampel kering. Data ini
diperkuat dengan hasil analisis kadar testosteron pada ekstrak teripang dengan
HPLC. Daging teripang basah mengandung testosteron 4,890 ppm, daging
kering 4,347 ppm, jeroan kering 5,388 ppm dan jeroan basah 6,124 ppm. Hal ini
diduga karena sebagian senyawa steroid dalam sampel mengalami kerusakan
selama proses pengeringan yang diakibatkan oleh aktivitas bakteri. Hal ini
sesuai dengan pernyataan Litwack (2006) yang menyebutkan bahwa senyawa
steroid dapat terdegradasi karena proses enzimatis yang disebabkan oleh
bakteri. Dalam hal ini bakteri diduga tumbuh dan berkembang selama proses
pengeringan daging dan jeroan teripang berlangsung. Pada proses pengeringan
jeroan, sejumlah bakteri juga berasal dari alat pencernaan.
Kandungan steroid yang cukup tinggi (2,13 %) pada jeroan teripang
basah merupakan bukti bahwa jeroan tersebut mempunyai nilai manfaat yang
selama ini diabaikan. Dengan demikian, jeroan dari industri pengolahan teripang
yang selama ini dibuang dapat dimanfaatkan sebagai sumber steroid sehingga
dapat meningkatkan nilai tambah dari teripang tersebut.
D. Identifikasi dan Karakterisasi Steroid Hasil Ekstraksi
Identifikasi keberadaan steroid dilakukan pada daging dan jeroan
teripang. Sampel yang diuji adalah daging dan jeroan dalam keadaan segar
(beku) dan kering. Uji yang dilakukan ini merupakan uji kualitatif steroid dalam
daging dan jeroan teripang.
1) Uji Warna
Hasil uji warna steroid dalam daging dan jeroan teripang yang dilakukan
dengan uji Lieberman-Burchard menunjukkan bahwa ekstrak kasar daging dan
jeroan teripang positif mengandung steroid. Hal ini ditunjukkan dengan
terbentuknya warna hijau pada saat titrasi dengan asam sulfat pekat. Hasil uji
warna tersebut dapat dilihat pada Tabel 8 berikut ini.
Tabel 8 Hasil identifikasi keberadaan steroid dalam teripang
Sampel Kualitatif*
Daging basah +
Daging kering +
Jeroan basah +++
Jeroan kering ++
* Jumlah tanda (+) menunjukkan intensitas warna hijau
Tabel 8 menunjukkan bahwa secara kualitatif (visual) jeroan basah
mempunyai kandungan senyawa steroid yang lebih banyak dibandingkan dengan
steroid pada jeroan kering dan daging basah serta daging kering. Jeroan