OPTIMASI PROSES PRODUKSI DAN KARAKTERISASI MALTODEKSTRIN DERAJAT POLIMERISASI MODERAT (DP 3-9)
DARI PAT1 GANDUM
OLEH: BEN1 HIDAYAT
PROGRAM PASCA SARJANA INSTITUT PERTANIAN BOGOR
ABSTRAK
BEN1 HIDAYAT. Optimasi Proses Produksi
dan
Karakterisasi Maltodekstrin DP Moderat (DP 3-9) dari Pati Gandum. Dibimbing oleh ADlL BASUKI AHZA dan SUGIYONOMaltodekstrin sangat berpotensi digunakan sebagai sumber karbohidrat pada minuman olahraga, khususnya minuman olahraga isotonik. Penggunaan maltodekstrin tersebut, terutama ditujukan agar pelepasan energi saat pelaksanaan aktivitas, lebih lambat serta untuk menurunkan derajat osmolalitas dan derajat kemanisan produk. Berdasarkan tujuan penggunaan tersebut, maka diperlukan upaya untuk mengembangkan maltodekstrin dengan komposisi sakarida spesifik, sehingga memiliki karakteristik ideal untuk digunakan sebagai sumber karbohidrat pada minuman olahraga isotonik.
Penelitian ini ditujukan untuk melakukan optimasi proses produksi maltodekstrin DP moderat (DP 3-9)
dari
pati gandum, menggunakan teknik hidrolisis enzimatis dan separasi membran, serta karakterisasi maltodekstrin hasil optimasi proses yang berkaitan dengan potensi dan nilai tambah penggunaannya sebagai sumber karbohidrat pada minuman olahraga isotonik, dengan pembanding glukosa dan maltodekstrin komersial.Hasil penelitian ini menunjukkan bahwa optimasi proses hidrolisis terbaik berdasarkan kandungan dan rendemen oligosakarida DP 3-9 tertinggi dan kandungan sakarida DP 1-2
dan
DP > 9 terendah, dihasilkan dari kombinasi perlakuan konsentrasi pati 200 gll, konsentrasi enzim 1207,50 unitll, dengan lama hidrolisis 30 menit yang dilanjutkan dengan proses separasi membran (kon&si operasional : konsentrasi sampel 5 %, suhu sampel 4S°C, tekanan 2 atm, dan disertai perlakuan filtrasi pendahuluan).Berdasarkan karakteristik kimiawinya dibandingh maltodekstrin komersil, maltodekstrin DP 3-9 yang dihasilkan akan memiliki kandungan sakarida DP 1-2 yang lebih rendah (10,87 % berbanding 16,07 %, p i 0,05), kandungan oligosakarida DP 3-9 yang lebih tinggi (89,13 % berbanding 78,66 %, p < 0,05), kandungan oligosakarida DP > 9 yang lebih rendah (tidak terdeteksi berbanding 5,27 %, p < 0,05), serta tipe pembentukan kompleks warna dengan larutan Iodium (kuning berbanding ungu kemerahan).
Dibandingkan glukosa, penggunaan maltodekstrin DP 3-9 sebagai sumber karbohidrat pada minuman olahraga isotonik memiliki beberapa keunggulan ditinjau
Dibandingkan maltodekstrin komersil, maltodekstrin DP 3-9 &an lebib ideal digunakan sebagai sumber karbohidrat pada minuman olahraga isotonik, karena karakteristik laju absorpsinya lebih dari 2 kali lipat lebih cepat (60 menit berbanding lebih
dan
120 menit) dan stabilitas penyimpanan pada suhu rendah yang lebih baik berdasarkan hasil uji pembentukan endapan (perlakuan tanpa sterilisasi, lebih dari 8SURAT
PERNYATAAN
Dengan ini saya menyatakan bahwa tesis yang berjudul :
OPTIMASI PROSES PRODUKSI DAN KARAKTERISASI MALTODEKSTRIN DERAJAT POLIMERISASI MODERAT (DP 3-9)
DARI PAT1 GANDUM
Adalah benar me~piikan hasil karya saya sendiri clan belum pernah dipublikasikan. Semua sumber data dan informasi yang digunakan telah dinyatakan secara jelas dan dapat diperiksa kebenarannya.
OPTIMASI PROSES PRODUKSI DAN KARAKTERISASI MALTODEKSTRIN DERAJAT POLIMERISASI MODERAT (DP 3-9)
DARI PAT1 GANDUM
BEN1 HIDAYAT
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program stud^ Ilmu Pangan
PROGRAM PASCA SARJANA INSTITUT PERTANIAN BOGOR
Judul Tesis : Optimasi Proses Produksi dan Karakterisasi Maltodekstrin Demjat Polimerisasi Moderat (DP 3-9) dari Pati Gandum
Nama : Beni Hidayat
NRP
: 99210Program Studi : Ilmu Pangan
Menyetujui 1. Komisi Pembimbing
,v
-
VDr.
Ir.
H. Adil Basuki Ahza. MS Dr. Ir. Sueivono. MAouScKetua AWgota
Prof Dr. Ir. Betty Sri Laksmi Jenie, M yafrida Manuwoto, MSc
RIWAYAT
HIDUP
Penulis dilahirkan di Tanjung Karang Bandar Lampung, pada tanggal 14 Januari 1967;
anak
kedua dari lima bersaudara dari pasangan Almarhum Bustami Jacub dan Rohaila.Pendidikan sarjana ditempuh penulis pada Jurusan Teknologi Hasil Pertanian, Fakultas Pertanian Universitas lampung, pada Tahun 1985-1989, dan sejak tahun 1992 penulis resmi diangkat sebagai staf pengajar pada Program Studi Telcnologi Pangan Politeknik Pertanian Negeri Bandar lampung. Pada tahun 1999, penulis memperoleh kesempatan untuk melanjutkan pendidikan magister di Program Studi Ilmu Pangan, Program Pasca Sarjana, lnstitut Pertanian Bogor.
Penulis menikah dengan Ratu Dewi Anggraini, tahun 1986, dan saat ini telah dikaruniai tiga orang putra-putri, yaitu Alpha Akbar Raditya, Ratu Betha Instania, dan Ratu Chaterine Fajri.
Sejak bertugas sebagai staf pengajar, penulis telah berhasil meraih berbagai penghargaan di bidang akademis, antara lain Dosen Teladan Politeknik Pertanian Universitas Lampung tahun 1997, juara pertama Lomba Cipta Produk Pangan Tingkat Nasional Tahun 1999, serta penerima anugerah Bogasari Nugraha Tahun 2001. Sebagai staf pengajar, penulis juga diberi amanah sebagai Kepala Laboratorium Teknologi Pangan 1994-1999, Ketua Koperasi 1997-2000, serta pembina Komisi I Senat Mahasiswa Politeknik Pertanian Negeri Bandar Lampung
1997-1999.
Selain bertugas sebagai staf pengajar, penulis juga berprofesi sebagai konsultan pengolahan pangan di beberapa industri pangan kecil-menengah, antara lain di CV Putra Lampung, Lampung (1998-1999), dan di PT Trimatra, Jakarta (1999).
PRAKATA
Puji syukur penulis panjatkan ke hadirat Allah SWT, yang telah melimpahkan
rahmat serta hidayah-Nya sehingga penulisan laporan penelitian ini dapat
diselesaikan tepat pada waktunya.
Pada kesempatan ini, penulis ingin menyarnpaikan ucapan terima kasih yang
setulus-tulusnya kepada
(1) Istri penulis, Ratu Dewi Anggraini, serta putra-putri tercinta : Alpha Akbar
Raditya, Ratu Betha Instania, dan Ratu Chaterine Fajri, atas pengorbanan dan
pengertiannya selama penulis menyelesaikan pendidikan magister.
(2) Bapak Dr. Ir. H. Adil Basuki Ahza, M.S. dan Dr. Ir. Sugiyono, M.App.Sc. selaku
ketua clan anggota komisi pembimbing atas saran dan perbaikannya yang sangat berarti pada penyusunan laporan penelitian ini.
(3) Bapak Roland Taunay dan Ibu Rafaini selaku Ketua dan Sekretaris Panitia
Bogasari Nugraha 2001, yang telah memberikan apresiasi positif selama
pelaksanaan kegiatan penelitian.
(4) Pimpinan PT ISM Bogasari Flour Mills, atas bantuan dana dan komitmen yang
tinggi untuk menjalin kerja sama kegiatan penelitian dengan institusi peryuuan
tinggi.
(5) Tim juri penilai proposal Bogasari Nugraha 2001 atas kepercayaan yang
(6) Seluruh pihak, baik teknisi-teknisi laboratorium, rekan-rekan LPN angkatan
1999, rekan-rekan dosen Politeknik Pertanian, dan rekan-rekan seprofesi, yang
telah tumt menyumbang saran dan membantu penyelesaian kegatan penelitian;
khususnya kepada Ir. Syamsu Udayana Nurdin, M.Si, atas bantuan dan saran-
sarannya saat pelaksanaan pengujian laju absorpsi produk pada tikus percobaan.
Akhimya penulis menyadari bahwa dengan segala keterbatasan yang ada,
laporan penelitian ini di sana-sini masih memerlukan penyempumaan lebih lanjut. Oleh karenanya, saran dan kritik membangun dari semua pihak sangat pendis
harapkan.
Bogor, Juli 2002
DAFTAR IS1
Halaman
DAFTAR TABEL ... i
...
DAFTAR GAMBAR ... 111
...
DAFTAR LAMPIRAN v
I
.
PENDAHULUAN ... 11.1 Latar Belakang ... 1 1.2 Tujuan Penelitian ...
.
.
... 4n
.
TINJAUAN PUSTAKA ....
.
...2.1 Pati Gandum ... 2.2 Sifat Fisik dan Kimia Pati Gandum ...
2.3 Hidrolisis Pati ... 2.4 Sifat-sifat Fungsional Maltodekstrin ... 2.5 Aplikasi Maltodekstrin pada Produk Minuman
Olahraga ... 2.6 Paktor-faktor yang Mempengaruhi Komposisi
Sakarida Maltodekstrin ... 2.7 Separasi Membran ...
.
.
...111
.
METODOLOGI PENELITIAN ... 3.1 Lokasi dan Waktu Penelitian ... 3.2 Bahan dan Alat Penelitian ...3.2.1 Bahan ... 3.2.2 Alat ... 3.3 Metode Penelitian ...
.
.
...3.3.1 Penelitian Pendahuluan ... ... 3.3.2 Optimasi Proses Separasi Membran
3.3.3 Optimasi Parameter Hidrolisis ... 3.3.4 Karakterisasi Maltodekstrin ...
...
3.4 Metode Pengujian dan Pengamatan
3.4.1 Pengujian Aktivitas Enzim a-amylase ...
3.4.2 Pengujian Selektifitas Membran ... 3.4.3 Pengujian Permeabilitas Membran ... 3.4.4 Pengamatan Produktivitas Membran ...
...
3.4.5 Pengujian Komposisi Maltodekstrin
3.4.7 Pengujian Viskositas Maltodekstrin DP 3-9 ...
3.4.8 Penpuiian Stabilitas Maltodekstrin DP 3-9 ...
3.4.9 ~ e n g u j i a n Warna Maltodekstrin DP 3-9 ...
3.4.10 Pengujian Derajat Osmolalitas Maltodekstrin DP 3-9 3.4.11 Pengujian Derajat Kemanisan Maltodekstrin DP 3-9 3.4.12 Pengujian Laju Absorpsi Maltodekstrin DP 3-9
I V
.
HASIL DAN PEMBAHASAN ... 4.1 Komposisi Kimia Pati Gandnm ...4.2 Pengujian Aktivitas Enzim a-amylase ...
4.3 Pengamatan Struktur Membran dan Prinsip Pemisahan Sampel ...
...
4.4 Pengujian Selektifitas Membran
4.5 Pengujian Driving Force Separasi Membran ...
...
4.6 Optimasi Proses Separasi Membran
... 4.6.1 Optimasi permeabilitas membran
... 4.6.2 Optimasi produktivitas membran
...
4.7 Optimasi Parameter Proses Hidrolisis
4.7.1 Optimasi Berdasarkan Kandungan Sakarida DP 1-2 4.7.2 Optimasi Berdasarkan Kandungan Sakarida DP > 9 4.7.3 Optimasi Berdasarkan Kandungan Sakarida DP 3- 9
4.7.4 Ootimasi Berdasarkan Rendemen Maltodekstrin
...
4.7.5 Pemilihan Perlakuan Terbaik
...
4.8 Karakterisasi Maltodekstrin DP 3-9
4.8.1 Karakterisasi Kimia ...
4.8.2 Karakterisasi Fisik ... ...
4.8.3 Karakterisasi Biologis
V
.
KESIMPULAN DAN SARAN ... 5.1 Kesimpulan ...5.2 Saran ...
DAFTAR PUSTAKA ...
DAFTAR
TABEL
No Judul halaman
1 Komposisi pati gandum (dalam basis berat kering)
... . ..
... . . 52 Rasio amilosa dan amilopektin pati gandurn dlbandingkan pati
Lainnya . . . , , . . , ,
.
,. . .
, , . .. .
. . ..
.. . . .
73 Tipe pembentukan kompleks warna pati-iodin pada berbagai derajat
polimerisasi . . .
.
. .. . .
..
. . ..
. . ..
..
..
.. . . ..
94 Pengaruh lama proses liquifikasi terhadap komposisi akhir produk
h a i l liquifikasi . . . , , , , . , ,
. . . .
, . . . ..
. . . 105 Perbandingan beberapa parameter fisik mtara proses liquifikasi dan
sakarifikasi . . .
.
.. . .
. . .. . .
. . . 116 Klasifikasi proses separasi membran . . .
. .
, , , , . .. .
. . ..
. . . . 207 Aplikasi teknik separasi membran untuk pengolahan produk pangan 22
8 Kondisi operasional pengujian komposisi maltodekstrin dengan HPLC 36
9 Komposisi kimia pati gandum h a i l ekstraksi . . .
. . .
44 10 Hasil uji selektifitas membran MWCO 1000 dan 3000 pada pemisahansenyawa oligosakarida DP 1-2, DP 3-9, dan DP > 9
.. .
... . .. . 48 11 Hubungan antara besar tekanan dan permeabilitas membran MWCO3000 dan 1000 . . .
. .
, ,.
, . ..
. . .. . .
. . . . 5112 Hubungan antara besar tekanan, konsentrasi sampel, dan suhu sampel
terhadap permeabilitas membran MWCO 1000 .
. . .
. . . ..
5413 Kandungan sakarida DP 1-2 pada berbagai perlakuan parameter
hidrolisis
. . . .
. . .. . .
. . .. . .
. . ..
. 5715 Perbedaan komposisi sakanda antara maltodekstrin h a i l penelitian
dan maltodekstrin komersil ... 66 16 Perbedaan karakteristik tipe pembentukan kompleks warna dengan larutan
Iodium antara maltodekstrin DP 3-9 (maltodekstrin hasil penelitian) dan maltodekstrin komersil ... 68
17 Kondisi pembentukan endapan maltodekstrin DP 3-9 (maltodekstrin hasil penelitian) dibandingkan dengan glukosa dan maltodekstrin komersil
selama penyimpanan ... 69
18 Hasil pengukuran derajat putih maltodekstrin DP 3-9 (maltodekstrin
hasil penelitian) dibandingkan dengan maltodekstrin komersil
...
7019 Hasil penentuan berat molekul rata-rata maltodekstrin DP 3-9
(maltodekstrin hasil penelitian) dan maltodekstrin komersil ... 71 20 Hasil penentuan nilai osmolalitas maltodekstrin DP 3-9 (maltodekstrin
hasil penelitian dan maltodekstrin komersil dengan menggunakan basis lmol glukosa sebagai standar ...
...
72 21 Hasil pengujian viskositas maltodekstrin DP 3-9 dibandingkan glukosa danmaltodekstrin komersil pada dua konsentrasi berbeda
...
74 22 Rekapitulasi penilaian 20 panelis terhadap tingkat kemanisan glukosa,maltodekstrin DP 3-9, dan maltodekstrin komersil pada berbagai
konsentrasi dengan menggunakan larutan sukrosa 2 % sebagai standar ... 76 23 Perbedaan tingkat kemanisan relatif maltodekstrin DP 3-9 dibandingkan
dengan maltodekstrin komersil dan glukosa, dengan menggunakan Gngkat kemanisan sukrosa (100) sebagai standar
...
.
.
... 7724 Kondisi kadar glukosa darah Tikus Sprague Dawley jantan berumur
2,5 bulan, tanpa dan dengan perlakuan puasa ...
.
.
....
79 25 Karakteristik laju absorpsi maltodekstrin DP 3-9 dibandingkan denganDAFTAR GAMBAR
Judul
...
Proses produksi tepung gluten dan pati gandum
...
Struktur amilosa dan amilopektin
Mekanisme pemutusan rantai polimer pati oleh enzim a-amylase dan glucoamylase ...
.
.
...Prinsip dasar mekanisme pemisahan komponen dengan teknik
...
separasi membran
Mekanisme ekstraksi produk maltodekstrin dengan menggunakan
... ...
teknik separasi membran
.
.
...
Alat separasi membran skala laboratorium
Metode ekstraksi pati gandum skala laboratorium ...
Proses produksi maltodekstrin pati gandum dengan menggunakan teknik hidrolisis enzimatis dan separasi membran ...
Susunan penyajian sampel per booth pada pengujian derajat kemanisan ...
.
.
...Kurva standar pati untuk penentuan aktivitas enzim a-amylase
Kromatograf maltodekstrin standar yang telah diseparasi dengan membran MWCO 1000 ...
Pola perubahan permeabilitas membran MWCO 1000 akibat perlakuan filtrasi pendahuluan pada sampel ...
Histogram perbedaan kandungan sakarida DP 1-2 pada perlakuan hasil optimasi ...
15 Histogram perbedaan kandungan sakarida DP 3- 9 pada perlakuan
hasil optimasi ... 6 1 16 Histogram perbedaan rendemen maltodekstrin DP 3- 9 pada perlakuan
hasil optimasi ... 63 17 Pola perubahan kadar glukosa darah Tikus Sprague Dawley jantan
berumur 2.5 bulan sebagai respon terhadap pemberian larutan
maltodekstrin DP 3- 9 dlbandingkan dengan glukosa dan maltodekstrin ...
DAFTAR LAMPIRAN
Judul halaman
Data hasil pengamatan kandungan sakarida DP 1-2 maltodekstrin
(% kromatograf, sebelum normalisasi) ... 92 Data hasil pengamatan kandungan sakarida DP 1-2 maltodekstrin
(% kromatograf, setelah normalisasi) ... 93 Tabel hasil analisis sidik ragam pengaruh parameter hidrolisis terhadap kandungan sakarida DP 1-2 maltodekstrin ... 94
Tabel hasil analisis beda nyata terkecil terhadap kandungan sakarida
DP 1-2 perlakuan hasil optirnasi ... 95
Data hasil pengamatan kandungan oligosakarida DP 3-9 maltodekstrin
(% kromatograf, sebelum normalisasi) ... 96 Data hasil pengamatan kandungan oligosakarida DP 3-9 maltodekstrin
(% kromatograf, setelah normalisasi) ... 97
Tabel hasil analisis sidik ragam pengaruh parameter hidrolisis terhadap kandungan oligosakarida DP 3-9 maltodekstrin
...
98Tabel hasil analisis beda nyata terkecil terhadap kandungan
oligosakarida DP 3-9 perlakuan hasil optimasi ... 99
Data hasil pengamatan kandungan oligosakarida DP > 9 maltodekstrin
(% kromatograf, sebelum normalisasi) ... 100 Data hasil pengamatan kandungan oligosakarida DP > 9 maltodekstrin
(% kromatograf, setelah normalisasi)
...
101Tabel hasil analisis sidik ragam pengaruh parameter hidrolisis terhadap
kandungan oligosakarida DP > 9 maltodekstrin ... 102
Tabel hasil analisis beda nyata terkecil terhadap kandungan
...
oligosakarida DP > 9 perlakuan hasil optimasi 103
Tabel hasil analisis si&k ragam pengaruh parameter proses hidrolisis
terhadap rendemen maltodekstrin DP 3-9
...
105Tabel hasil analisis beda nyata terkecil rendemen maltodekstrin DP 3-9
perlakuan hasil optimasi ... 106
Contoh cara perhitungan konsentrasi DP 1 (glukosa) pada pengujian
...
komposisi sakarida maltodekstrin DP 3-9 107
Contoh cara perhitungan rendemen maltodekstrin DP 3-9 pada
perlakuan AIBICl ulangan 1 ... 108
Data perubahan volume dan total padatan perlakuan. pada tahap
optimasi parameter hidrolisis ... 109 Data hasil pengamatan kadar glukosa darah tikus (mgidl) ... 110
Susunan perlakuan pada pengujian laju absorpsi produk ... 111 Contoh cara penyusunan ransum tikus ... 112
Data pertambahan berat badan tikus selama pemeliharaan
di laboratorium (3 minggu) ...
....
... 114 Contoh cara seleksi tikus berdasarkan pertambahan berat badan ... 116Foto perubahan aktivitas tikus yang dipuasakan dan tidak dipuasakan 117
Foto alat untuk memberikan larutan secara oral pada tikus percobaan 1 18
Foto tabung reaksi steril-vakum
+
pengawet Na+. yang digunakanuntuk menampung darah tikus perwbaan ... 118 Foto metode pemberian larutan secara oral pada tikus percobaan ... 119
Foto metode pengambilan darah melalui vena abdominal pada
tikus percobaan ... 120 Foto pati gandum hasil ekstraksi ... 121 Foto bahan-bahan utama pada proses hidrolisis pati ... 121
33 Foto perbedaan reaksi pembentukan
warna
dengan larutan Iodiurnantara maltodekstrin DP 3-9 dm maltodekstrin komersil ... 123 34 Foto hasil uji stabilitas pada penyimpanan suhu dmgin ... 123 35 Foto maltodekstrin DP 3-9 setelah dikeringkan dibandingkan dengan
...
I.
PENDAHULUAN
1.1 LATAR BELAKANG
Pada industri pengolahan gluten, pati gandum merupakan hasil samping
(by product) yang memiliki potensi untuk lebih ditingkatkan nilai tambahnya.
Salah satu upaya pe~ngkatan nilai tambah pati gandum adalah pengolahan pati
giuidum dalam bentuk produk-produk hidrolisis pati seperti dekstrin,
maltodekstrin, cyclodekstrin, sirup maltosa, sirup glukosa, dan sirup fruktosa.
Maltodekstrin I yellow dekstrin merupakan bahan baku penting bagi
inclustri pangan dan industri lainnya. Pada industri pangan, penggunaan
ma,ltodekstrin terutama ditujukan untuk memperbaiki tekstur produk, mengontrol
kristalisasi selama proses pembekuan (freezing), pengganti lemak, pembentuk
film, serta berfungsi sebagai penyuplai gizi pada suatu produk (Kearsley and
Ddedzic, 1995).
Maltodekstrin merupakan produk hasil hidrolisis pati tidak sempurna,
yzng umumnya memiliki nilai DE (Dextrose Equivalent) kurang dari 20 (Kearsley
an,$ Dziedzic, 1995). Kisaran nilai DE pada produk maltodekstrin akan sangat
ditentukan oleh tinggi rendahnya derajat hidrolisis pati. Menurut Marchal el al.
(1!)99), komposisi sakarida sebagai hasil proses hidrolisis pati pada produk
maltodekstrin akan sangat menentukan sifat-sifat fungsionalnya. Sehingga dapat
terjadi produk maltodekstrin dengan hsaran nilai DE yang sama akan memiliki
sif'at-sifat fungsional yang berbeda (Kearsley and Dziedzic, 1995).
Salah satu bentuk aplikasi maltodekstrin yang sedang dikembangkan saat
olahraga, khususnya minuman olahraga isotonik (Ford, 1995). Penggunaan
maltodekstrin tersebut, terutarna ditujukan agar pelepasan energi terjadi lebih
lambat, serta untuk menurunkan derajat osmolalitas dan derajat kemanisan produk
(A~~stin and Pierpoint, 1998; Kearsley and Dziedzic, 1995). Berdasarkan tujuan
penggunaan tersebut, maka diperlukan upaya untuk mengembangkan
maltodekstrin dengan komposisi sakanda yang spesifik.
Komposisi maltodekstrin ideal yang dibutuhkan untuk produk minuman
olahraga isotonik adalah maltodekstrin yang tidak mengandung oligosakarida
dengan rantai linier yang pendek (DP 1-2), karena akan meningkatkan kemanisan
produk, derajat osmosis, dan laju absorpsi produk oleh tubuh. Sebaliknya,
perlggunaan maltodekstrin yang mengandung oligosakarida dengan rantai linier
yang panjang (DP > lo), akan menyebabkan produk memiliki laju absorpsi, kelarutan, dan stabilitas yang rendah. Menurut Storey and Zumbe (1995), secara
w ~ u m pada produk minuman olahraga, maltodekstrin yang dibutuhkan adalah
oligosakarida dengan rantai linier yang pendek (DP 3-6), agar produk dapat
terabsorpsi pada laju tinggi tetapi tetap memililu osmolalrty pada tingkat yang
moderat. Sedangkan menurut Marchal et al. (1999), untuk produk-produk
beverages, spesifikasi ideal maltodekstrin yang diinginkan adalah maltodekstrin
yang memiliki DP tertentu yang bersifat tidak manis, kental (vrscous), dan tetap
stabil selama penyimpanan.
Berdasarkan karakteristik minuman isotonik dan tujuan penggunaan
maltodekstrin pada produk minuman tersebut, maka mperlukan upaya untuk
mengembangkan produk maltodekstrin yang komposisi utamanya adalah
3
Dibandingkan dengan produk maltodekstrin yang mengandung oligosakarida
rar~tai linier pendek (DP 1-2) dengan konsentrasi yang tingg, maka maltodekstrin
DF' moderat diharapkan akan terabsorpsi pada laju lebih rendah, lebih bersifat
tidak manis, serta memiliki derajat osmolalitas yang lebih rendah pula.
Sebaliknya, dibandingkan dengan produk maltodekstrin yang mengandung
oligosakarida rantai linier panjang (DP > 10) dengan konsentrasi yang tinggi,
ma.ka maltodekstrin DP moderat diharapkan
akan
memiliki laju absorpsi yang lekih tinggi, bersifat tidak terlalu kental (viscous), kelarutan yang lebih baik, dan lek~ih stabil selarna penyimpanan.Menurut Marchal et al. (1999), upaya untuk menghasilkan maltodekstrin
dengan komposisi sakarida yang spesifik, antara lain dapat dilakukan dengan
mengefektihn teknik ekstraksi produk. Salah satu metode yang dapat digunakan
untuk mengektraksi produk dari campurannya adalah teknik separasi membran (Cheryan, 1986).
Melalui penggunaan membran dengan karakteristik tertentu, dapat
diupayakan agar hanya sakarida dengan DP tertentu pada produk maltodekstrin
ya-ng dominan dapat melewati membran sedangkan campuran-campuran lainnya
ak.an tertahan oleh membran (Cheryan, 1986). Agar penggunaan teknik separasi
membran mampu menghasilkan produk maltodekstrin dengan komposisi sakarida
yang spesifik, maka diperlukan pula upaya untuk mengkondisikan larutan hasil
hitlrolisis pada komposisi yang ideal. Salah satu upaya yang dapat dilakukan
untuk mengontrol proses hidrolisis pati adalah penggunaan metode hidrolisis enzimatis yang akan memutus rantai polimer pati secara spesifik (Schwardt,
yang spesifik dan optimal untuk dipisahkan pada proses separasi membran.
Penelitian lebih lanjut diperlukan untuk melakukan optimasi proses, agar
mslltodekstrin yang dihasilkan memiliki karakteristik sesuai yang diharapkan.
1.1: TUJUAN PENELITIAN
(1) Melakukan optimasi proses produksi maltodekstrin DP moderat (DP 3-9)
dari pati gandum menggunakan teknik hidrolisis enzimatis dan separasi
membran.
(2) Melakukan karakterisasi maltodeksbin hasil optimasi proses, berkaitan
dengan penggunaannya sebagai sumber karbohidrat pada minuman
olahraga isotonik, dengan pembankng glukosa dan maltodekstrin
11.
TINJAUAN PUSTAKA
2.li PAT1 GANDUM
Berbeda dengan industri pati dari komoditi lainnya, pati gandum
unlumnya tidak diproses secara khusus, tetapi merupakan hasil samping (by
product) dari industri pengolahan gluten (Kearsley and Dziedzic, 1995).
Walaupun pati gandum tersebut merupakan hasil samping, upaya pengolahan pati
gandum lebih lanjut tetap penting guna memberikan nilai tambah pada proses
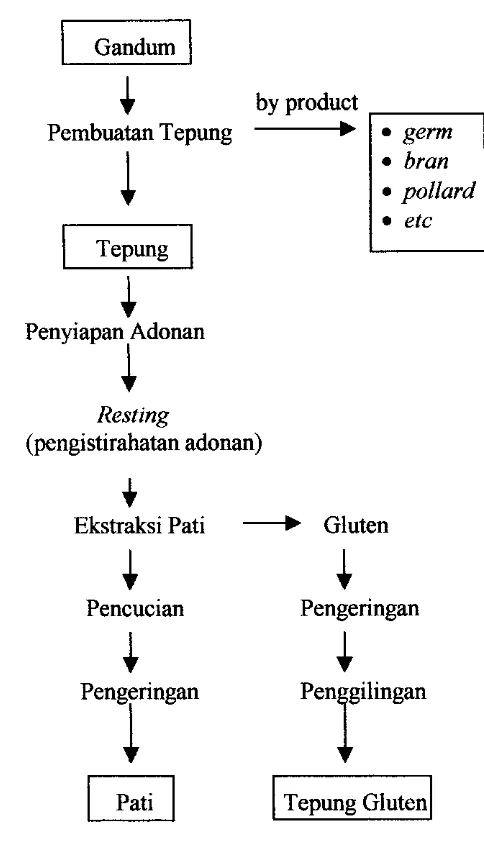
pengolahan gandum secara keseluruhan. Proses pengolahan pati gandum sebagai
bagian dari industri pengolahan gluten dapat dilihat pada Gambar 1.
2.2 SWAT FISIK DAN KIMIA PAT1 GANDUM
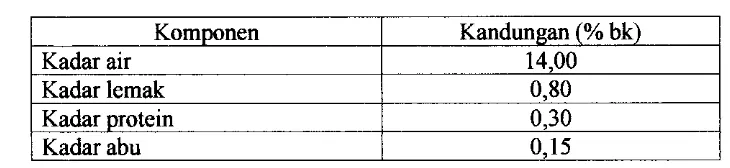
Seperti halnya pati-pati lainnya (pati kentang, jagung, dan ubi kayu), pati gandum juga masih mengandung komponen-komponen lain dalam jumlah yang
relatif kecil (Tabel 1).
Tabel 1. Komposisi pati gandum (dalam basis berat kering)
Kadar air 14,OO
Kadar lemak
0,30
Kadar abu 0,15
Sumber: Kearsley and Dziedzic (1995)
Selain berdasarkan komposisinya, pati gandum juga dapat dibedakan dari
pati lainnya berdasarkan bentuk dan ukuran granula pati, serta rasio amilosa dan
arnilopektin. Menurut Kearsley and Dziedzic (1995), granula pati gandum
[image:176.572.106.471.489.573.2]Jidleani et al. (1996), semakin kecil clan seragam ukuran granula suatu pati maka
ak,m semakin cepat laju hidrolisis pati tersebut.
by product
Pembuatan Tepung
-
I
+
Resting
(pengistirahatan adonan)
+
Ekstraksi Pati
+
Glutengerm bran pollard
Pencucian Pengeringan
Pengeringan
1
[image:177.572.230.472.115.536.2]I
patiI
I
Tepung ~ l u t e n lGambar 1. Proses produksi tepung gluten dan pati gandum (Sumber : Kearsley and Dziedzic, 1995)
Dibandingkan jenis pati lainnya, terutama pati kentang dan pati ubi kayu,
palti gandum memiliki rasio amilosa dan amilopektin yang lebih besar (Tabel 2).
dengan kandungan amilosa yang tinggi sangat sesuai digunakan untuk bahan baku
proses hidrolisis. Selain lebih mudah larut, pati dengan kandungan amilosa yang
tinggi juga akan lebih mudah terhidrolisis oleh asam dan enzim, karena jurnlah
bagian amorfiya yang lebih tinggi dan ikatan antar moleMnya lebih lemah.
Tabel 2. Rasio amilosa dan amilopektin pati gandurn mbandingkan pati lainnya
Surnber: Kearsley and Dziedzic (1995) Jenis pati
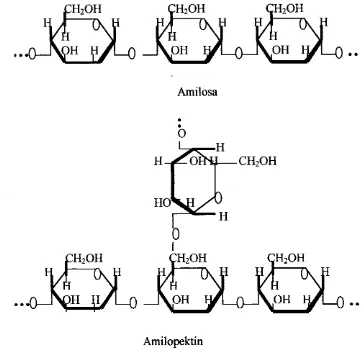
Amilosa merupakan polimer glukosa berantai lurus dengan ikatan a-
1,4. glukosida, sedangkan amilopektin merupakan polimer glukosa bercabang
deilgan ikatan a-1,4 glukosida pada rantai lurusnya serta ikatan a-1,6 glukosida
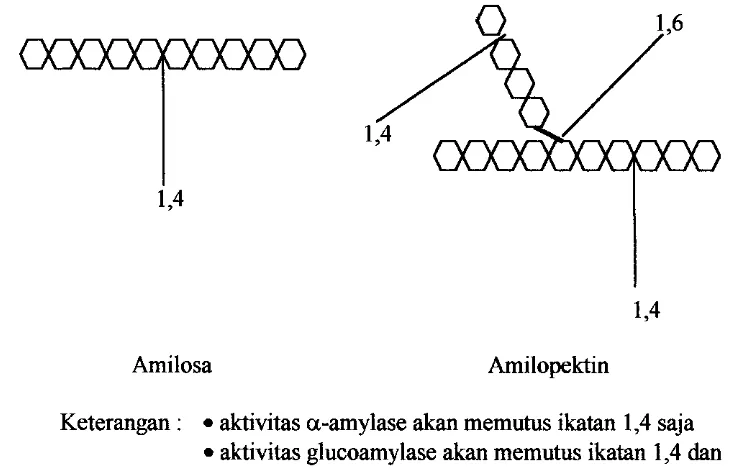
palla percabangannya (Gambar 2).
Amilosa dan amilopektin memiliki sifat fisik yang berbeda. Amilosa
let~ih mudah larut dalam air (air panas) dan kurang kental dibandingkan dengan
anilopektin. Amilosa akan menghasilkan warna biru bila direaksikan dengan
larutan iodium, sedangkan amilopehn akan menghasilkan wama ungu. Kearsley
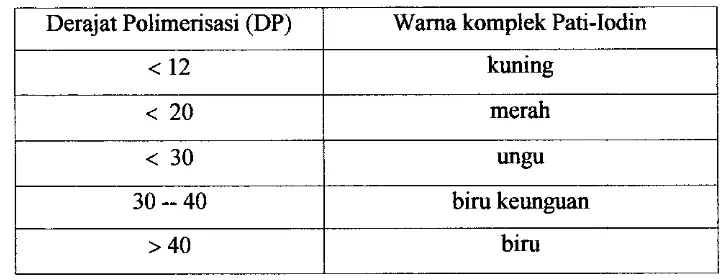
and Dziedzic (1995), menggunakan wama dari kompleks pati-iodin sebagai intiikator derajat polimerisasi yang secara tidak langsung akan menunjukkan
panjang rantai polimer glukosa suatu pati (Tabel 3). Pada tabel tersebut terlihat
bahwa amilosa memiliki derajat polimerisasi yang tinggi (> 40 DP), sedangkan
an~ilopektin memiliki derajat polimerisasi yang rendah (< 30 DP). Amilosa (%)
27 2 1
27 14
Amilopektin (%)
[image:178.579.104.474.203.278.2]Amilosa
[image:179.572.97.460.47.399.2]Amilopektin
Gambar 2. Struktur amilosa dan amilopektin
2.3 HIDROLISIS PAT1
Proses hidrolisis pati pa& dasarnya adalah pemutusan rantai polimer pati
(C,;HIOOS), menjadi unit-unit dekstrosa ( C a 1 2 0 6 ) . Produk-produk hasil hdrolisis
pati umumnya dikarakterisasi berdasarkan tingkat derajat hidrolisisnya dan
hnyatakan dengan nilai DE ( D e m s e Equivalent) yang menunjukkan persentase
dar-i dekstrosa murni dalam basis berat kering pada produk hidrolisis. Menurut
Kearsley and Dziedzic (1995), dekstrosa murni adalah dekstrosa dengan derajat
DE. 15, menunjukkan bahwa persentase dekstrosa murni pada pr& kurang lebih
setlesar 15 % (bk).
Tal3el3. Tipe pembentukan warna kompleks pati-iodin pada berbagai derajat polimerisasi (Kearsley and Dziedzic, 1995)
I
Derajat Polimerisasi (DP)/
Wama komplek Pati-Iodin< 12 kuning
< 20
< 30 30
--
40Pemutusan rantai polimer pati dapat dilakukan dengan berbagai metode,
misalnya secara enzimatis, kimiawi, ataupun kombinasi keduanya. Hidrolisis
secara enzimatis memiliki perbedaan mendasar dibanhngkan hidrolisis secara
kirniawi dan fisik dalam ha1 spesifitas pemutusan rantai polimer pati. Hidrolisis
secara lumiawi dan fisik akan memutus rantai polimer secara acak, sedangkan hitlrolisis enzimatis akan memutus rantai polimer secara spesifik pada
peircabangan tertentu (Schwardt, 1990). Sebagai contoh, disajkan mekanisme
[image:180.572.111.475.163.303.2]pemutusan rantai polimer pati oleh enzim a-amylase dan glucoamylase pada
Gambar 3.
Akibat pemutusan rantai polimer secara acak tersebut, maka proses
htlrolisis secara kimiawi clan fisik akan menyebabkan tejadinya peningkatan kandungan produk reversi, sehingga kualitas produk hasil htdrolisis akan lebih
merah
ungu
biru keunguan
> 40
Amilosa Amilopektin
Keterangan : aktivitas a-amylase akan memutus ikatan 1,4 saja aktivitas glucoamylase akan memutus ikatan 1,4 dan 1,6
Gambar 3. Mekanisme pemutusan rantai polimer pati oleh enzim a-amylase dan glucoamylase (Sumber: Schwardt, 1990)
Proses liquifikasi merupakan tahap proses awal pada proses-proses
hiclrolisis pati, misalnya pada pembuatan dekstrin, glukosa, dan sirup fruktosa.
Pada tahap liquifikasi ini, akan terjadi pemutusan ikatan a-1,4 oleh aktifitas
exdm a-amylase. Menurut Dziedzic and Kearsley (1984), kesempumaan dan
lanna proses liquifikasi akan menentukan komposisi akhir produk basil liquifikasi
(Tiibel4).
Tabel 4. Pengaruh lama proses liquifikasi terhadap komposisi akhir produk hasil liquifikasi (Dziedzic and Kearsley, 1984)
I
'Lama Proses (jam) 1 2 4 DE 12 20 29
DP 1
(%)
0,4 0,7
2,9
D P 2
(%) 2,1 5,5 14,l DP5
(%I
3,9 8 3 17,3 DP3 (%) 5,O 10,O 17,lDP 6+ (%)
85,2
69,7
40,l D P 4
("A)
3,4
[image:181.572.103.468.71.306.2]Hidrolisis hasil liquifikasi lebih lanjut, umumnya Qlakukan dengan
pellambahan enzim glucoamylase (proses sakarifikasi) yang akan memutus
rar~tai a-1,4 dan a-1,6 sekaligus. Melalui proses sakarifikasi ini, polimer pati
akan mengalami pernutusan ikatan lebih lanjut dan nilai DE produk hasil hiclrolisis akan meningkat. Perbandingan beberapa parameter fisik antara proses
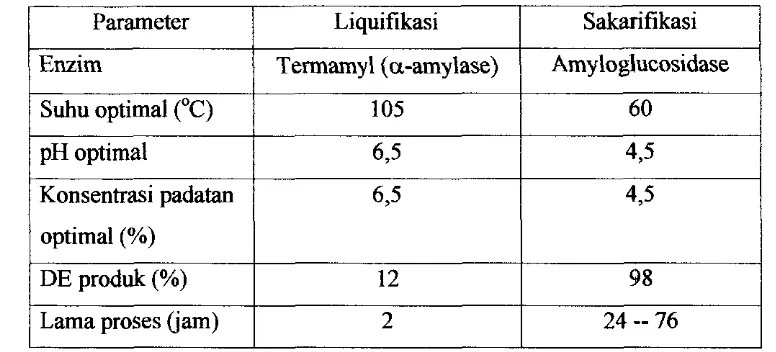
liquifikasi dan sakarifikasi dapat dilihat pada Tabel 5
Tabel 5. Perbandingan beberapa parameter fisik antara proses liquifikasi dan sakarifikasi
1 I
Enzim
1
Termamyl (a-amylase)1
Amyloglucosidase Sakarifikasi Parameteroptimal (%)
I
I
Liquifikasi
Suhu optimal ("C)
pH optimal
Konsentrasi padatan
DE produk (%) 12 98
1
105
6,5
6,5
Sumber : Dziedzic and Kearsley (1984)
60
4,5
4 3
I I
2.4 SWAT-SWAT FUNGSIONAL MALTODEKSTRIN
Maltodekstrin merupakan produk hasil hidrolisis pati tidak sempurna yang Lama proses (jam)
I
2diintrodusir pertama kali pada tahun 1959 oleh American Maize Product
Company. Badan FDA (Food and Drug Administration) Amerika Serikat, 24
--
76mendefinisikan maltodekstrin sebagai produk non pemanis, polimer sakarida yang
terciiri dari unit-unit D-glukosa yang umumnya terangkai dengan ikatan a-1,4 dan
[image:182.579.99.487.278.454.2]Sebagai contoh, maltodekstrin antara lain telah digunakan sebagai bahan pengisi
dan pembawa (carrier), senyawa untuk memperhaiki tekstur suatu produk, bahan
pe~nbantu pada proses spray dryer, bahan pengganti lemak, senyawa untuk
me:ngontrol proses pembekuan, senyawa untuk mencegah terjadinya proses
knstalisasi, dan sebagai penyuplai gizi pada suatu produk.
Penggunaan maltodekstrin terutama berkaitan dengan sifat-sifat
fungsional fisik dan biologsnya. Menurut Marchal el ul. (1999), sifat-sifat fur~gsional fisik dan biologis maltodekstrin akan sangat ditentukan oleh komposisi
sairaridanya. Beberapa aspek yang berkaitan dengan sifat-sifat fungsional fisik
da11 biologis maltodekstrin adalah
a. Derajat higroskopis (hygroscopicity)
Hygroscopicity adalah kemampuan suatu produk untuk menyerap air d m
lingkungan atmosfer sekitarnya. Menurut Johnson and Srisuthep (1975),
glukosa (DP 1) dan dan maltosa (DP2) memiliki hygroscopicity yang sangat
rendah dibandingkan sakarida lainnya yang memiliki nilai DP lebih tinggi.
Sebaliknya hasil penelitian Donnelly et al. (1973), menunjukkan bahwa
maltotriose (DP3) memiliki hygroscopicity yang tertinggi dibandingkan
sakarida lainnya, seperti dapat dilihat pada perbandmgan berikut :
DP3 > DP4 = DP7 > DP5 > DP6 > DPl 1 > DP2
Walaupun mekanisme p e n m a n derajat higroskopis belurn banyak diketahui,
tapi sebagian besar hasil-hasil penelitian menunjukkan bahwa oligosakarida
dengan nilai DP > 9 dan I 2 memiliki hygroscopicity lebih rendah
b. Kemampuan untuk terfermentasi pada produk-produk pangan (fermentability
in foodproduct)
Hasil penelitian Shieh et al. (1973) terhadap kemampuan terfermentasi dari
oligosakarida dengan DP 2-8, menunjukkan bahwa Saccharomyces
carlbergensis dan Saccharomyces cerevisiae, hanya dapat memfermentasi maltosa dm maltotriose.
c. Viscositas (viscosity)
Hasil penelitian Johnson and Srisuthep (1975), terhadap derajat viskositas
oligosakarida dengan DP 2--10, menunjukkan bahwa s a m p DP 7, derajat
viskositas akan meningkat secara linier seiring dengan peningkatan nilai DP
oligosakarida; sedangkan pada DP 8-10, hubungan antara peningkatan derajat
viskositas dengan nilai DP oligosakarida akan terjadi secara kuadratik.
d. Derajat kemanisan (sweetness)
Hasil penelitian Birch et al. (1991), menunjukkan bahwa derajat kemanisan
(sweetness) akan semakin menurun seiring dengan peningkatan nilai DP
oligosakarida.
e. Stabilitas (stability)
Hasil penelitian Gidley and Bulpin (1987) dan Johnson and Srisuthep (1975),
menunjukkan bahwa oligosakarida dengan nilai DP > 7 akan memiliki stabilitas lebih rendah selama penyimpanan.
f. Derajat osmolalitas (osmolality)
Hasil penelitian Birch et al. (1991), menunjukkan bahwa derajat osmolalitas
g. Kemampuan terabsorpsi oleh tubuh (absorption by human)
Kemampuannya oligosakarida untuk terabsorpsi oleh tubuh terutama berkaitan
dengan derajat osmolalitas dan kelarutannya. Secara umum, oligosakarida
yang lebih mudah larut akan lebih mudah terabsorbsi aleh tubuh.
Berdasarkan sifat-sifat fungsional fisik dan biologis maltodekstrin
terrsebut, terlihat bahwa dibandngkan nilai DE, nilai DP maltodeshitrin lebih dapat
digunakan untuk memprediksi penampilan produk yang akan dihasilkan pada
be~,bagai keperluan aplikasi (Marchall et dl. , 1999).
2.5 APLIKASI MALTODEKSTRIN PADA PRODUK MINUMAN OLAHRAGA
(SPORT
DRINK)Aplikasi maltodekstrin sebagai bahan tarnbahan pada produk minuman
(beverages) berkembang makin pesat sejalan dengan semakin populernya produk
miiiuman olahraga dan energ (sport and energy drink) di tengah masyarakat.
Mc:nurut Ford (1995), komposisi utarna minuman olahraga adalah karbohidrat dan
miiieral; dan sebagai sumber karbohtdrat antara lain dapat berupa sukrosa,
glukosa, maltodekstrin, dan karbohidrat yang bersumber dari buah-buahan.
Melalui proses karbonasi pada konsentrasi rendah, produk-pr~duk minuman
olahraga dirancang untuk mengatasi efek kehilangan mineral clan dehidrasi selama
aktivitas berolahraga (Austin dan Pierpoint, 1998), serta berfungsi sebagai sumber
energi untuk mempertahankan stamina selama aktivitas (Ford, 1995).
Tiga tipe utama dari minurnan olahraga adalah hypotonic, hypertonic, dan
isotonic. Pada dasarnya timbulnya istilah ketiga tipe minuman tersebut
disebabkan perbedaan kandungan partikel terlarutftekanan osmotiknya (Ford,
mi numan yang mengandung partikel terlarut lebih tinggi dibandingkan
ko~~sentrasi partikel terlarut pada cairan tubuh. Menurut Austih dan Pierpoint,
(1998), ketiga jenis produk minuman olahraga tersebut, an@ra lain dapat
dikledakan berdasarkan kandungan karbohidrat pada produk, waktu untuk
mengkonsumsinya, dan laju absorpsi (penyerapan) produk oleh tubuh. Minuman
hipotonik (hypoton~c drmk), dldesain untuk dikonsumsi setelah aktivitas olahraga
kar.ena akan terserap tubuh lebih cepat dan mengandung karhohidrat dengan
konsentrasi yang rendah (2-3%). Sebaliknya, minuman hipertqnik (hypertonic
drink) urnumnya mengandung karbohidrat dengan konsentrasi ymg tinggi (10%
atau lebih) dan akan terabsorpsi tubuh pada laju yang lebih larnbqt sehingga akan
lebih sesuai untuk dikonsumsi sebelum aktivitas. Dari ketiga jenis minurnan
olahraga tersebut, minurnan isotonic (isotonic drink) merupakan tipe produk yang paling sering dijumpai. Minuman isotonik yang memililu tqkanan osmotik
sei~mbang dengan tekanan osmotik cairan tubuh, dirancang untuk menggantikan
enr:rgi secara cepat baik sebelum, selama dan setelah aktifitas.
Berdasarkan karakteristik minuman isotonik tersebut, maha maltodekstrin
merupakan komponen yang paling sesuai digunakan sebagai @ahan tambahan
untuk produk m i m a n olahraga isotonik (Austin clan Pierpoint, 1998; Kearsley
ancl Dziedzic, 1995). Adanya komponen maltodekstrin, akw menyebabkan ene:rgi dilepaskan secara lambat dan juga mengurangi osmolalitas produk (Austin
dark Pierpoint, 1998). Selain itu, penggunaan maltodekstrin pada produk
mi~~uman olahraga juga diharapkan akan mengurangi kemanisab produk tanpa
serta memungkinkan untuk meningkatkan kandungan kalori dap mineral pada
prc~duk (Ford, 1995).
Hasil penelitian beberapa peneliti menunjukkan bahwa diperlukan
ko~nposisi yang spesifik untuk aplikasi maltodesktrin pada produk-produk
minuman olahraga khususnya untuk minuman isotonic (isotonic drink). Pada
prc~duk minuman isotonik, maltodekstrin yang dibutuhkan adalah maltodekstrin
yarlg tidak mengandung oligosakarida dengan rantai linier yang ppndek (DP 1-2),
karena akan meningkatkan kemanisan produk, meningkatkan tdkanan osmotik,
dari menyebabkan produk terabsorpsi dengan laju yang sangat cepat. Sebaliknya,
penggunaan maltodekstrin yang mengandung oligosakarida dengan rantai linier
yang panjang (DP>10), akan menyebabkan produk memiliki laju absorpsi,
sta bilitas, dan kelarutan yang rendah. Menurut Storey and Zumbq (1995), secara
urnurn pada produk minuman olahraga, maltodekstrin yang diblutuhkan adalah
olijpsakarida dengan rantai linier yang pendek (DP 3-6), agar produk dapat teriibsorpsi pada laju dengan tinggi tetapi tetap memiliki osmolaMy pada tingkat
yarlg moderat. Sedangkan menurut Marchal et al. (1999), untuk produk-produk
beverages, spesifikasi ideal maltodekstrin yang diinginkan a d a l 4 maltodekstrin
yang memiliki DP tertentu yang bersifat tidak manis, kental (viscdus), tetapi tetap
stal~il selama penyimpanan.
2.6 FAKTOR-FAKTOR YANG MEMPENGARUHI KOMPaSISI SAKARIDA MALTODEKSTRIN
Komposisi sakarida pada maltodekstrin akan sangat meneqtukan sifat-sifat
fungsional fisik dan biologis. Berikut adalah faktor-faktor utapa yang dapat
a. Jenis enzim hdrolitik yang digunakan
Perbedaan jenis enzim terutama berkaitan dengan aktivitas spesifik enzim
tersebut pada pemutusan ikatan a- 1,4 molekul pati (Kearsleiy and Dziedzic, 1995).
b. Jenis dan konsentrasi pati
Perbedaan jenis pati terutama berkaitan dengan kandungan amilosa, distribusi
panjang rantai pati, dan berat molekulnya. Hasil penelitian Reeve (1992),
menunjukan bahwa reaksi transglycosylation relatif lebih mudah terjadi pada
konsentrasi pati yang tinggi.
c. Temperatur hidrolisis
Hasil penelitian Dobreva el ul. (1994) dan Ramesh and Lonsane (1989),
menunjukkan bahwa laju reaksi hidrolisis, spesifitas produk yang Ihasilkan,
dan reaksi transglycosylation akan sangat dipengaruhi oleh temperatur selama
proses hidrolisis.
d. Penambahan pelarut-pelarut organik
Hasil penelitian Blakeney and Stone (1985), menunjukkan bahwa penambahan
pelarut organik akan menurunkan jumlah oligosakarida bjerantai pendek
selama proses hidrolisis
e. Penggunaan enzim terimobilisasi
Hasil penelitian Hisamatsu et al. (1994), menunjukkan bahwa penggunaan
enzim terimobilisasi akan meningkatkan spesifitas kerja enzim.
f. Proses a h r (down stream processmng)
Penelitian yang telah dilakukan antara lain adalah perpisahan secara
penggunaan metode kromatografi untuk menghasilkan olieosakarida yang
lebih spesifik (Sakai et al., 1987), dan fermentasi untqk memisahkan
komponen sakarida berantai pendek (Yoo et ul., 1995)
g. Ekstraksi produk selama proses hidrolisis
Penelitian-penelitian untuk mengefektifkan teknik ek$traksi produk
maltodekstrin belurn banyak dilakukan. Sebagai perbqndingan, hasil
penelitian yang dilakukan Sims and Cheryan (1992) menupjukkan bahwa
penggunaan membran ultrafiltrasi pada proses produksi sirup glukosa akan
meningkatkan kemurnian produk yang dihasilkan.
2.7 SEPARASI MEMBRAN
Proses separasi membran Qdasarkan pada prinsip pemis+an komponen
berdasarkan perbedaan berat dan ukuran molekul komponen melalui suatu
membran semi-perrneabel (Morris and Morris, 1976). Melalui dnggunaan suatu
membran dengan karakteristik dan ukuran pori-pori tertenfu, komponen-
kolnponen dengan ukuran molekul lebih besar dari ukuan pod-pori membran
&in tertahan (retentate) sedangkan komponen-komponen dengan ukuran molekul
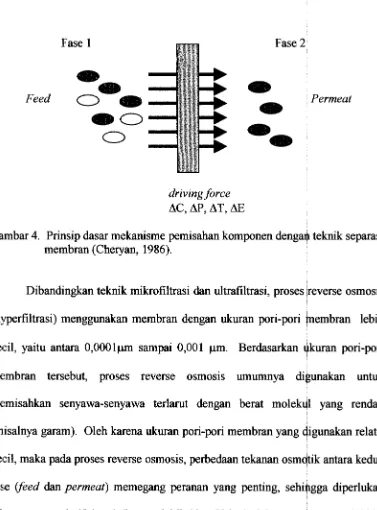
lebih kecil akan melewati membran (permeate). Pada GamQar 4, disajikan
pri nsip dasar mekamsme pemisahan komponen dengan teknik sepqasi membran.
Berdasarkan perbedaan kisaran ukuran molekul kompoben yang akan
dipisahkan dan prinsip driving force yang digunakan untuk untw mengalirkan
b a l m melalui membran, maka proses separasi membran dapat dibedakan atas
milu-ofiltrasi, ultrafiltrasi, reverse osmosis/hyperfiltrasi, elektkoQalysis, dan
dy~disis (Matsuura and Sourirajan, 1994; Cheryan, 1986). Klasifikasi berbagai
Feed
Fase 1 Fase
Permeat
driving force AC, AP, AT, AE
Gambar 4. Prinsip dasar mekanisme pemisahan komponen d e n g a ~ teknik separasi membran (Cheryan, 1986).
Dibandingkan teknik mikrofiltrasi dan ultrafiltrasi, proses reverse osmosis
(hyperfiltrasi) menggunakan membran dengan ukuran pori-pori hembran lebih
kecil, yaitu antara 0,0001pm sampai 0,001 pm. Berdasarkan &wan pori-pori
membran tersebut, proses reverse osmosis umumnya digunakan untuk
memisahkan senyawa-senyawa terlarut dengan berat molekd yang rendah
(misalnya garam). Oleh karena ukuran pori-pori membran yang 4gunakan relatif
kecil, maka pada proses reverse osmosis, perbedaan tekanan osmcjtik antara kedua
fase veed clan permeat) memegang peranan yang penting, sehiqgga lperlukan tek:anan yang relatif tinggi (kurang lebih 10
--
50 bar). Menurut Rerguson (1989),proses reverse osmosis umumnya dilakukan untuk tujuan-tujqan mengurangi
ka~idungan air bahan (terutama jika konsentrat l d u g a dapat ruqak atau bersifat
lahi1 oleh panas), dan untuk tujuan pemurnian air (terutama pengolahan air laut
[image:190.572.106.483.41.551.2]Tallel 6. Klasifikasi proses separasi membran
Mi krofiltrasi GradienTekanan 10 - 0,l ym Jellis proses Driving force
- Ultrafiltrasi - Reverse osmosis (hyperfiltration) mikroba Kisaran ukuran pori
-pori membran
Gradien tekanan
-
N;mofiltrasi*
Emulsi, kdloid, makro- Contoh kom#nen
Yang dipisa&an
< O,1 ym
-
5 nm Gradien tekananmolekul, prodein
Garam-garanj terlarut,
< 5 nm Gradien tekanan
Bahan-bahanl organik
< 1 nm
berukuran kebil ~aram-garad terlarut
Smnber: Cheryan (1986) ;
*
Hartomo clan Wibatmoko (1994)Pada proses ultrafiltrasi, membran yang digunakan memillki ukuran pori-
Garam-garaq terlarut
menggantik& fbngsi ginjal untuk memisahkan komponen-kqmponen tertentu bada sistem metabolisme tubuh
poi-i antara 0,001 pm sampai 0,l pm. Berdasarkan karaktqristik pori-pori
< 5 nm < 5 n m
- I
Electrodialysis
-
Dialysis
melmbran tersebut, maka proses ultrafiltrasi menjadi lebih bersifat selektif dan
I
Gradien medan listrik
Gradien konsentrasi
digunakan untuk memisahkan komponen-komponen dengan ber* molekul besar
(1.000-10.000). Menurut Ferguson (1 989), membran ultrafiitrasi urnumnya
digunakan untuk memisahkan padatan-padatan tersuspensi, kbloid (misalnya
protein), padatan-padatan teremulsi (misalnya cat), dan badatan-padatan
malkromolekular terlarut. Melalui proses ultrafiltrasi, komponen&omponen yang
me:miliki berat molekul besar akan menjadi konsentrat (retentdzte component),
pelarut, garam, gula, dan air) akan melewati membran, dan disebut filtrat
(permeate component).
Pada proses mikrofiltrasi, membran yang digunakan memiliki ukuran pori-
p o ~ i antara 0,s - 10 pm. Berdasarkan karakteristik p~ri-pori meimbran tersebut,
maka proses mikrofiltrasi hanya digunakan untuk memisahkan komponen-
ko~nponen dengan berat molekul yang sangat besar. Menurut Ftrguson (1989),
prclses mikrofiltrasi antara lain digunakan untuk memisahkan globula lemak
beiukuran besar, dan partikel tersuspensi berukuran besar (misalnya sel mikroba).
Dari berbagai teknik separasi membran tersebut, proses mikrofiltrasi dan
ultrafiltrasi merupakan teknik yang paling banyak dikembangkan untuk
pengolahan produk-produk pangan. Pada Tabel 7, dapat dilihqt bahwa kedua
proses, umumnya digunakan untuk memisahkan komponen-kohponen dengan
berat molekul tinggi (seperti pektin dan protein). Pen$gunaan teknik
mikrofiltrasi dan ultrafiltrasi tersebut, dilakukan untuk meningkatkan efisiensi
proses, menyederhanakan proses, dan mengembangkan produktproduk pangan
balu.
Aplikasi teknik separasi membran pada proses dan prod* hidrolisis pati
antara lain hkembangkan pada proses liquifikasi berupa produlqsi maltotetraosa
(Kimura et al., 1988), dan pemurnian produk sakarifikasi (Siqs and Cheryan,
19'32).
Sims and Cheryan (1992), menggunakan reaktor membran pada proses
sal~arifikasi. Pada proses tersebut, digunakan substrat hasil liquiflkasi, dan proses
sdcarifikasi dilakukan dengan menggunakan enzim glucoamylase. Teknik
separasi membran yang digunakan berupa proses ultrafiltrast menggun
"
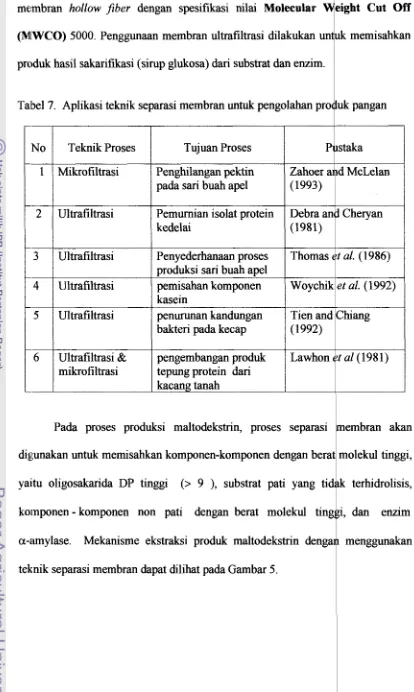
22 membran hollow Jiber dengan spesifikasi nilai Molecular eight Cut Off (MWCO) 5000. Penggunaan membran ultrafiltrasi dilakukan un uk memisahkan produk hasil sakarifikasi (sirup glukosa) dari substrat dan enzim.Tabel 7. Aplikasi teknik separasi membran untuk pengolahan proQuk pangan
Pada proses produksi maltodekstrin, proses separasi
digunakan untuk memisahkan komponen-komponen dengan
yaitu oligosakarida DP tinggi (> 9 ), substrat pati ko~nponen
-
komponen non pati dengan berata-amylase. Mekanisme ekstraksi produk
teknik separasi membran dapat dilihat pada Gambar 5. Tujuan Proses
Penghilangan pektin pada sari buah apel
Pemurnian isolat protein kedelai
Penyederhanaan proses produksi sari buah apel pemisahan komponen kasein
penurunan kandungan bakteri pada kecap
pengembangan produk tepung protein dari kacang tanah No 1 2 3 4 5 6 P-lstaka Teknik Proses Mikrofiltrasi Ultrafiltrasi Ultrafiltrasi Ultrafiltrasi Ultrafiltrasi
Ultrafiltrasi &
mikrofiltrasi Debra and (1981) Thomas Woychik Tien and (1992) Lawhon Cheryan
?t al. (1 986)
et al. (1992)
Chang
[image:193.576.81.495.49.741.2]Liquifikasi Substrat
-
Komponen non pati-+
Suk)strat Produk
Pat i (maltodekstrin)
-
a-amylase a-amylase -b
+ Maltodekstrin
DP19
[image:194.576.122.489.45.191.2]Membran
In.
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilaksanakan di Laboratorium Rekayasa Proses Pangan dan Pilot
Plant Pusat Studi Pangan dan Gizi (PSPG) Institut Pertanian Bogor; Laboratorium Kirr~ia Pangan dan Laboratoriurn Biokimia Pangan Jurusan Teknologi Pangan dan
G i z ~ Institut Pertanian Bogor; serta Laboratorium Teknologi Pangan Politeknik
Pertanian Negeri Bandar Lampung. Penelitian dilaksanakan pa& bulan Nopember
200 1 hlngga bulan April 2002.
3.2 BAHAN DAN ALAT PENELITIAN
3.2.1
Bahan
Bahan utarna yang digunakan dalam penelitian diantararlya adalah tepung
terilp lencana merah produksi PT ISM Bogasari Flour Mills, melmbran ultrafiltrasi
tipe PLAC MWCO 1000 dan PLBC MWCO 3000 yang diperoleh dari PT Hartech
Indonesia, Jakarta; serta enzim a-amylase (Termamyl 120 L) produksi NOVO
Industries yang lperoleh dari UPT EPG (Ethanol, Protein Sel Tmggal, dan Gula) Slusuban, BPP Teknologi Larnpung. Bahan lainnya yang digunakan selama kegiatan
penelitian antara lain adalah arang aktif, filter whatrnan No 42, &n membran filter
0,2 mikron serta bahan-bahan untuk menyusun ransum standar tiku$ percobaan.
Bahan kimia yang akan digunakan antara lain adalah NiaOH, CaCl?, pati
standar, maltodekstrin komersial, maltodekstrin standar, maltocbligokarida HPLC
25
Unit Pelayanan T e h s Laboratoriurn Politeknik Pertanian Negeri Bandar Lampung,
Jurusan Pangan dan Gizi Institut Pertanian Bogor, Toko Bahan Kimia Setia Guna, serta~ PD Fresconina Bogor.
3.2.;!
AlatAlat-alat utama yang digunakan dalam penelitian antara lain adalah alat
separasi membran skala laboratorium merk Sartorius (Gambar 6), sugar hand
refraktometer, spektrofotometer merk Hach tife DR/2010, advanced digimatic milk
cryoscope model 4D2, pengering semprot Merk Bucchi, High Petformance Liquid
Chromatography (HPLC), detektor differensial refiaktometer, chramameter Minolta
tipe Cr 200, ultra sentrifius, penangas air, pemanas vakum, pH-meter, timbangan analiitik, serta alat-alat gelas untuk analisis.
Keterangan
A. Tutup bagiah atas B. Salwan tekqnan
C. Pengukur teikanan
D. Tempat smpel
E. Disk penyangga membran
F. Saluran vakum
G. Tempat perbeate
[image:196.580.72.489.363.705.2]3.3 METODE PENELITIAN
Penelitian dilaksanakan secara bertahap dalam empat tahap utama, yaitu
penemlitian pendahuluan, optimasi proses separasi membran, optimasi parameter
proses hidrolisis, dan karakterisasi maltodekstrin DP 3-9 hasil penelitian.
3.3.11 Penelitian Pendahuluan
Pada penelitian pendahuluan, Qlakukan kegiatan ekstraksi pati gandurn
(Garnbar 7) dan pengujian terhadap komposisi kimia pati gandm hasil ekstraksi
(kadar air, kadar pati, dan kadar protein), pengujian aktivitas volmetrik enzim a-
amylase, pengamatan komposisi membran ultrafiltrasi dan prinsip pemisahan sampel,
pengujian selektifitas membran, serta pengujian driving force proses separasi menibran.
3.3.2 Optimasi Proses Separasi Membran
Optimasi proses separasi membran dilakukan untuk menentukan konQsi
ope~.asional proses. Kegiatan yang dilakukan berupa optimasi permeabilitas dan
procluktivitas membran pada pemisahan komponen oligosakarida DP > 9. Optimasi
pernieabilitas membran dilakukan berdasarkan penentuan besw tekanan, serta
konsentrasi sampel dan suhu sampel yang akan diseparasi. Adapun optimasi
procluktivitas akan diamati melalui penggunaan tahap filtrasi pendahuluan sebelum
Tepung terigu
Pembentukan adonan (pengulenan)
Air
(60 % bterat tepun