PENGARUH KADAR ZAT PENGOTOR SILIKON (Si) DAN BESI
(Fe) PADA ALUMINIUM CAIR YANG DIHASILKAN DI
TUNGKU REDUKSI TERHADAP KESESUAIAN
STANDAR GRADE ALUMINIUM
DI PT INALUM
KARYA ILMIAH
HARRY NUGRAHA
092401056
PROGRAM D-3 KIMIA INDUSTRI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATRA UTARA
PENGARUH KADAR ZAT PENGOTOR SILIKON (Si) DAN BESI (Fe) PADA ALUMINIUM CAIR YANG DIHASILKAN DI TUNGKU REDUKSI
TERHADAP KESESUAIAN STANDAR GRADE ALUMINIUM DI PT INALUM
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Ahli Madya
HARRY NUGRAHA 092401056
PROGRAM D-3 KIMIA INDUSTRI DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATRA UTARA
PERSETUJUAN
Judul : PENGARUH KADAR ZAT PENGOTOR SILIKON (Si) DAN BESI (Fe) PADA
ALUMINIUM CAIR YANG DIHASILAKAN DI TUNGKU REDUKSI TERHADAP KESESUAIAN STANDAR GRADE ALUMINIUM DI PT
INALUM
Kategori : TUGAS AKHIR
Nama : HARRY NUGRAHA
Nomor Induk Mahasiswa : 092401056
Program studi : DIPLOMA TIGA (D-III) KIMIA INDUSTRI Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (MIPA)
UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Juni 2012
Diketahui
PERNYATAAN
PENGARUH KADAR ZAT PENGOTOR SILIKON (Si) DAN BESI (Fe) PADA ALUMINIUM CAIR YANG DIHASILKAN DI TUNGKU REDUKSI
TERHADAP KESESUAIAN STANDAR GRADE ALUMINIUM DI PT INALUM
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2012
PENGHARGAAN
Bismillahirrahmanirrahim,
Puji dan syukur penulis panjatkan Ke hadirat ALLAH SWT Yang Maha
Pengasih dan Maha Penyayang, atas rahmat dan karunia-Nya penulis dapat
menyalesaikan karya ilmiah ini mulai dari awal penulisan sampai selesai. Karya
ilmiah ini merupakan salah satu syarat untuk meraih gelar Ahli madya pada program
diploma 3 kimia industri di Fakultas Matematika dan Ilmu Pengetahuan Alam,
Universitas Sumatera Utara.
Dalam penyusunan karya ilmiah ini penulis menyadari sepenuhnya bahwa
karya ilmiah ini jauh dari kesempurnaan karena keterbatasan penulis baik dari segi
kemampuan, waktu dan pengetahuan. Hal ini disebabkan karena keterbatasan penulis,
baik dalam penguraian ilmu maupun keterbatasan dalam pengalaman yang sejauh ini
belum dapat tercapai sebagaimana diharapkan. Oleh karena itu, penulis menerima
kritikan dan saran-saran yang bersifat membangun dari para pembaca.
Pada kesempatan ini penulis bersyukur dan ingin mengucapkan terima kasih
secara tertulis, kepada :
1. Kedua orang tua saya Suryo Domo dan Rosilawati yang telah membesarkan
dan melimpahkan kasih sayang kepada saya hingga akhirnya sampai seperti
saat ini. Serta abang saya Agyasta Yudha, dan adik saya Ria Az’zahra dan
Alfa Rizi.
2. Bapak Dr. Mimpin Ginting, MS, yang telah membimbing dengan kesabaran
kepada penulis dalam menyelesaikan karya ilmiah ini.
3. Dr. Rumondang Bulan MS, sebagai ketua Departeman Kimia FMIPA-USU
Medan.
4. Dra. Emma Zaidar Nasution, MSi. selaku Ketua dan Dra. Herlince Sihotang,
MSi. selaku sekretaris Program Studi Kimia Industri FMIPA-USU Medan.
5. Seluruh Dosen Kimia Industri, FMIPA-USU Medan.
6. Bapak Damianus Siregar dan Faishal Hidayat selaku pembimbing Praktek
Mahadi Fahrozi, Januar Sasmitra, Ariansyah Perangin-angin, Didi Febrian, Ali
Nassaruddin, Arif Kurniawan, Lisa Usmalyana, Riki Get-Get, Dede Subarqah.
Terima kasih kawan atas segala bentuk bantuan yang telah diberikan, sukses
buat kita semua. “HIDUP IMAKIN”
8. Teman-teman seperjuangan di Program Studi Kimia Industri FMIPA-USU
angkatan 09.
9. Adik-adik di Kimia Industri stambuk 2010 dan 2011, terus semangat untuk
menyelesaikan studinya.
Medan, Juni 2012
ABSTRAK
Telah dilakukan pengujian pengaruh kadar zat pengotor silikon (Si) dan besi (Fe) yang terdapat dalam aluminium cair untuk menghasilkan standar grade aluminium. Aluminium yang dihasilkan masih banyak mengandung zat pengotor seperti besi dan silikon yang menyebabkan korosi (pengaratan) dan warna aluminium menjadi kuning. Apabila kadar zat pengotor banyak terdapat dalam aluminium dapat dilakukan dengan pengadukan ulang, penambahan aluminium cair, pencetakan sebagian aluminium dan penurunan grade. Dari hasil pengamatan yang diperoleh, aluminium yang dihasilkan di PT INALUM ternyata sesuai standar grade yang telah ditetapkan, untuk grade S2 dengan kadar pengotor Si = 0,08 dan Fe = 0,12 dengan kemurnian 99,85% dan grade
RATES INFLUENCE LEVELS OF SILICON (Si) AND IRON (Fe) OF LIQUID ALUMINUM PRODUCED IN THE POT REDUCTION TO STILL THE
STANDARD OF GRADE ALUMINUM IN PT INALUM
ABSTRACT
DAFTAR ISI
BAB 4. HASIL DAN PEMBAHASAN 30
4.1. Hasil 30
4.1.1. Data Percobaan 30
4.2. Pembahasan 32
BAB 5. KESIMPULAN DAN SARAN 33
5.1. Kesimpulan 33
5.2. Saran 33
DAFTAR TABEL
Halaman
Tabel 2.1. Spesifikasi AlF3 11
Tabel 2.2. Spesifikasi Alumina yang Digunakan di PT Inalum 14
Tabel 2.3. Standar Kualitas Aluminium Batangan (Ingot) 23
Tabel 4.1. Pengukuran Kadar Si dan Fe di Potline 2 28
ABSTRAK
Telah dilakukan pengujian pengaruh kadar zat pengotor silikon (Si) dan besi (Fe) yang terdapat dalam aluminium cair untuk menghasilkan standar grade aluminium. Aluminium yang dihasilkan masih banyak mengandung zat pengotor seperti besi dan silikon yang menyebabkan korosi (pengaratan) dan warna aluminium menjadi kuning. Apabila kadar zat pengotor banyak terdapat dalam aluminium dapat dilakukan dengan pengadukan ulang, penambahan aluminium cair, pencetakan sebagian aluminium dan penurunan grade. Dari hasil pengamatan yang diperoleh, aluminium yang dihasilkan di PT INALUM ternyata sesuai standar grade yang telah ditetapkan, untuk grade S2 dengan kadar pengotor Si = 0,08 dan Fe = 0,12 dengan kemurnian 99,85% dan grade
RATES INFLUENCE LEVELS OF SILICON (Si) AND IRON (Fe) OF LIQUID ALUMINUM PRODUCED IN THE POT REDUCTION TO STILL THE
STANDARD OF GRADE ALUMINUM IN PT INALUM
ABSTRACT
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Industri peleburan aluminium mulai berkembang sejak Charles Hall dan Paul
Heroult yang secara terpisah menemukan proses produksi aluminium yang lebih
sederhana pada tahun 1866, yaitu dengan cara mereduksi aluminium (Al) dari bahan
baku alumina (Al2O3) melalui proses elektrolisis. Dalam proses ini, bahan karbon (C)
dipakai sebagai elektroda, kriolit (Na3AlF6) sebagai pelarut dan arus listrik searah
(DC) sebagai sumber energi pemisah Al dari senyawa alumina (Al2O3), dan menjaga
agar elektrolit maupun metal cair yang terbentuk tetap terjaga dalam fase cair didalam
tungku reduksi (Austin,1996).
Aluminium mempunyai titik lebur 20000C, namun dengan proses elektrolisa
metode Hall Heroult yang menggunakan larutan kriolit (Na3AlF6), aluminium dapat
diperoleh pada temperatur 10000C, dan dengan memasukkan zat additif seperti AlF3,
CaF2 dan bahan-bahan lain yang terdapat didalam bahan baku, maka aluminium dapat
diperoleh pada temperatur 9600C sampai 9700C.
Adapun aluminium yang dihasilkan adalah aluminium yang berbentuk batangan
(ingot) dengan berat perbatangnya 22,7 kg. Desain produksi PT INALUM adalah
225.000 ton per tahun. Aluminium yang dihasilkan merupakan bahan baku industri
hilir yang dapat menghasilkan barang-barang seperti : bahan bangunan, alat rumah
Aluminium mempunyai sifat penghantar panas yang tinggi dan juga mempunyai daya
tahan terhadap karat yang sangat baik. Oleh karena itu permintaan akan aluminium
dari tahun ke tahun terus mengalami peningkatan. Hal ini ditandai dengan semakin
banyaknya permintaan aluminium di kalangan konsumen.
Dalam proses peleburan aluminium pastilah tidak dapat dihasilkan aluminium yang
100% murni, terdapat zat pengotor didalam hasilnya. Zat pengotor tersebut dapat
berupa silikon (Si), besi (Fe), tembaga (Cu), timbal (Pb) dan sebagainya. Tetapi dalam
hal ini, zat pengotor yang lebih dicermati adalah silikon (Si) dan besi (Fe). Karena
dengan adanya zat pengotor ini akan mempengaruhi kualitas dari aluminium yang
dihasilkan, dimana PT Inalum memberikan beberapa standar terhadap kemurnian dari
aluminium. Untuk mengurangi kelebihan atau menyeimbangkan kadar zat pengotor
yang terdapat dalam aluminium yaitu dengan cara pemberian aluminium murni
(PT.Inalum,2010).
Dari uraian diatas, maka dapat dijadikan suatu alasan bagi penulis untuk memilih
1.2. Identifikasi Masalah
Apakah pengaruh kadar zat pengotor berupa silikon (Si) dan besi (Fe) yang
terdapat dalam aluminium cair (molten) dapat mempengaruhi kualitas aluminium yang
akan dihasilkan terhadap standar grade aluminium yang telah ditetapkan.
1.3. Tujuan
Untuk mengetahui standar kadar zat pengotor yang dapat dicetak menjadi
aluminium batangan (ingot) dengan menyesuaikan standarisasi grade aluminium yang
telah ditentukan oleh PT.Inalum.
1.4. Manfaat
Dengan diketahui berapa banyak persentase (%) kadar zat pengotor silikon (Si)
dan besi (Fe) yang terkandung dalam aluminium cair dapat dilakukan analisa terhadap
aluminium cair (molten), sehingga ketika kadar zat pengotor berlebih dilakukan
perlakuan berupa mencampurkan aluminium cair dengan kadar zat pengotor tinggi ke
dalam aluminium cair dengan kadar zat pengotor rendah sehingga dapat dilakukan
BAB 2
TINJAUAN PUSTAKA
2.1. Alumina dan Aluminium
2.1.1 Aluminium
Aluminium adalah logam yang ringan dan cukup penting dalam kehidupan
manusia. Aluminium merupakan unsur kimia golongan IIIA dalam sistim periodik
unsur, dengan nomor atom 13 dan berat atom 26,98 gram per mol. Didalam udara
bebas aluminium mudah teroksidasi membentuk lapisan tipis oksida (Al2O3) yang
tahan terhadap korosi. Aluminium juga bersifat amfoter yang mampu bereaksi dengan
larutan asam maupun basa (Hartono,1992).
Aluminium merupakan logam ringan yang mempunyai ketahanan korosi yang
baik dan hantaran listrik yang baik serta sifat-sifat baik yang lainnya sebagai sifat
logam (Surdia,2005).
2.1.2. Sejarah Aluminium
Aluminium ditemukan kira-kira sekitar 160 tahun yang lalu dan mulai
diproduksi skala industri sekitar 90 tahun yang lalu. Berikut sejarah perkembangan
1. Pada tahun 1782, seorang ilmuwan Prancis bernama Lavoiser telah
menduga bahwa aluminium merupakan logam yang terkandung didalam
alumina.
2. Pada tahun 1807, ahli kimia inggris bernama Humphrey Davy berhasil
memisahkan alumina secara elektrokimia logam dan yang diperoleh dari
pengujian tersebut adalah aluminium.
3. Pada tahun 1821, biji sumber aluminium ditemukan di Prancis Selatan,
tepatnya dikota Lesbaux, yang dinamakan bauksit.
4. Pada tahun 1825, ahli kimia Denmark, Orsted berhasil memisahkan
aluminium murni dengan cara memanaskan aluminium chloride dengan
kalium amalgam dan kemudian memisahkan merkuri dengan cara destilasi.
5. Pada tahun 1886, mahasiswa Oberlin College di Ohio, Amerika Serikat
bernama Charles Martin-Hall menemukan dengan cara melarutkan alumina
(Al2O3) dalam lelehan kriolit (Na3AlF6) pada temperatur 9600C dalam
bentuk kotak yang dilapisi logam karbon dan kemudian melewatkan arus
listrik melalui ruang tersebut. Cara ini dikenal dengan proses Hall-Heroult,
karena ini terjadi pada tahun yang sama dengan seorang Prancis yang
bernama Paul Heroult.
6. Pada tahun 1888, ahli kimia Jerman Karlf Josef Bayer menemukan cara
memperoleh alumina dari bauksit secara pelarutan kimia. Sampai saat ini
cara Bayer masih digunakan untuk memproduksi alumina dari bauksit
secara industri dan disebut proses Bayer (Davis,1993).
Aluminium adalah logam yang terbanyak didunia. Logam 8% dari bagian pada
mengandung aluminium, tetapi proses untuk mendapatkan aluminium logam dari
kebanyakan bahan itu masih belum ekonomis. Logam aluminium pertama kali dibuat
dalam bentuk murni oleh Oersted pada tahun 1825, yang memanaskan ammonium
klorida (NH4Cl) dengan amalgam kalium-raksa (K-Hg).
Pada tahun 1854, Henri Sainte-Claire Deville membuat aluminium dari
natrium-aluminium klorida dengan jalan memanaskan dengan logam natrium. Proses
ini beroperasi selama 35 tahun dan logamnya dijual dengan harga $ 220 per kilogram.
Pada tahun 1886 Charles Hall mulai memproduksi aluminium dengan skala besar
seperti sekarang, yaitu melalui elektrolisis alumina didalam kriolit (Na3AlF6) lebur.
Pada tahun itu pula, Paul Heroult mendapat hak dari prancis untuk proses serupa
dengan proses Hall. Hingga pada tahun 1893, produksi aluminium menurut cara Hall
ini sudah sedemikian meningkat, sehingga harganya sudah jatuh menjadi $ 4,40 per
kilogram. Industri ini berkembang dengan baik, berdasarkan suatu pasaran yang sehat
dan berkembang atas dasar penelitian mengenai sifat-sifat aluminium dan cara-cara
pemakaian yang ekonomis bagi bahan ini (Austin,1990).
2.1.3. Sifat-sifat Aluminium
Dalam tiga dasawarsa terakhir ini aluminium telah menjadi salah satu logam
industri yang paling luas penggunaannya didunia. Aluminium banyak digunakan
didalam semua sektor utama industri seperti angkutan, konstruksi, listrik, peti kemas
Penggunaan aluminium yang luas disebabkan aluminium memiliki sifat-sifat yang
lebih baik dari logam lainnya seperti :
a. Ringan : memiliki bobot sekitar 1/3 dari bobot besi dan baja, atau tembaga dan karenanya banyak digunakan dalam industri transportasi seperti angkutan
udara.
b. Kuat : terutama bila dipadu dengan logam lain. Digunakan untuk pembuatan produk yang memerlukan kekuatan tinggi seperti : pesawat terbang, kapal laut,
bejana tekan, kendaraan dan lain-lain.
c. Mudah dibentuk dengan semua proses pengerjaan logam. Mudah dirakit karena dapat disambung dengan logam/ material lainnya melalui pengelasan,
brazing, solder, adhesive bonding, sambungan mekanis, atau dengan teknik
penyambungan lainnya.
d. Tahan korosi : sifatnya durabel sehingga baik dipakai untuk lingkungan yang dipengaruhi oleh unsur-unsur seperti air, udara, suhu dan unsur-unsur kimia
lainnya, baik diruang angkasa atau bahkan sampai ke dasar laut.
e. Konduktor listrik : setiap satu kilogram aluminium dapat menghantarkan arus listrik dua kali lebih besar jika dibandingkan dengan tembaga. Karena
aluminium relatif tidak mahal dan ringan, maka aluminium sangat baik untuk
kabel-kabel listrik overhead maupun bawah tanah.
f. Konduktor panas : sifat ini sangat baik untuk penggunaan pada mesin/ alat pemindah panas sehingga dapat membersihkan penghematan energi.
g. Memantulkan sinar dan panas : dapat dibuat sedemikian rupa sehingga memiliki kemampuan pantul yang tinggi yaitu sekitar 95% dibandingkan
dengan kekuatan pantul sebuah cermin. Sifat pantul ini menjadikan aluminium
h. Non magnetik : dan karenanya sangat baik untuk penggunaan pada peralatan listrik/ elektronik, pemancar radio/ TV, dan lain-lain, dimana diperlukan faktor
magnetisasi negatif.
i. Tak beracun : dan karenanya sangat baik untuk penggunaan pada industri makanan, minuman dan obat-obatan, yaitu untuk peti kemas dan pembungkus.
j. Memiliki ketangguhan yang baik : dalam keadaan dingin dan tidak seperti logam lainnya yang menjadi getas bila didinginkan. Sifat ini sangat baik untuk
penggunaan pada pemrosesan maupun transportasi LNG dimana suhu gas cair
k. Menarik : dan karena itu aluminium sering digunakan tanpa diberi proses pengerjaan akhir. Tampak permukaan aluminium sangat menarik dan karena
itu cocok untuk perabot rumah (hiasan), bahan bangunan dan mobil.
Disamping itu aluminium dapat diberi surface treatment, dapat dikilapkan,
disikat atau dicat dengan berbagai warna, dan juga diberi proses anodisasi.
Proses ini menghasilkan lapisan yang juga dapat melindungi logam dari
goresan dan jenis abrasi lainnya.
l. Mampu diproses ulang-guna : yaitu dengan mengolahnya kembali melalui proses peleburan dan selanjutnya dibentuk menjadi produk seperti yang
diinginkan. Proses ulang-guna ini dapat menghemat energi, modal dan bahan
baku yang berharga (Daryus,2008).
A. Bahan baku utama
1. Alumina
Alumina diperoleh dari bauksit melalui beberapa proses Bayer. Bauksit
merupakan bahan baku Al yang terdiri dari Al2O3 (aluminium oksida) dan
memiliki kemurnian yang berbeda seperti besi oksida, aluminium silika dan
titanium oksida. Aluminium oksida (Al2O3) atau alumina biasanya berupa kristal
ion. Tetapi ion oksida (O-2) dipolarisasi oleh ion aluminium sehingga sebagian
ikatannya bersifat kovalen. Aluminium oksida meleleh pada 20350C. Zat ini tidak
larut dalam air, stabil dan keras. Aluminium oksida adalah amfoter. Zat ini
melarut dengn lambat dalam asam encer maupun basa encer.
Al2O3 (s) + 6H+(aq) 2Al3+(aq) + 3H2O(l)
Al2O3(s) + 2OH-(aq) + 3H2O 2Al(OH)-4
2. Anoda
Anoda adalah elektroda bermuatan listrik positif. Jenis anoda yang dipakai adalah
jenis anoda prebaked, anoda yang digunakan diseksi reduksi dibuat digedung
karbon dengan bahan kokas dan hard pitch.
3. Katoda
Katoda adalah elektroda bermuatan listrik negatif. Ditinjau dari bahan bakunya
a. Blok katoda amorphous, bahan bakunya antrasit, dipanggang pada suhu
12000C
b. Blok katoda semi graphitic, bahan bakunya grafit, dipanggang pada suhu
23000C
c. Blok katoda graphitic, bahan bakunya kokas mengalami proses grafitasi suhu
30000C (Jody,1992).
B. Bahan baku penunjang
a. Kriolit
Kriolit dapat mengandung CaF2 dan AlF3 yang dapat membentuk kriolit Na3AlF6.
Sifat-sifat kriolit adalah :
1) Konduktivitas listrik baik
2) Memiliki berat jenis yang rendah
3) Temperatur kristalisasi primer rendah
4) Stabil dalam keadaan cair
5) Dapat melarutkan alumina dalam jumlah besar
Untuk memperbaiki sifat-sifat kriolit tersebut, bath biasanya ditambah dengan
beberapa bahan tambahan seperti fluorida, alkil metal, AlF3 dan CaF2.
b. Soda abu (Na2CO3)
untuk membantu proses pembentukan kerak samping. Selain mencegah erosi oleh
bath, soda abu berfungsi sebagai isolasi termal.
c. Aluminium florida (AlF3)
Aluminium florida berfungsi menjaga keasaman bath dan merupakan bahan yang
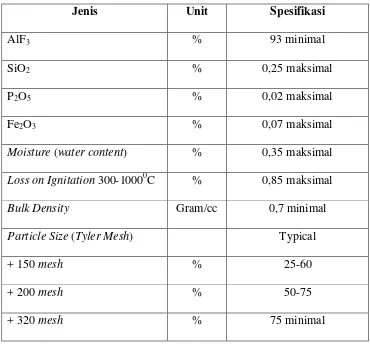
dituangkan secara manual jika kelebihan AlF3 kurang didalam bath. Spesifikasi
AlF3 yang digunakan oleh PT INALUM adalah :
Tabel 2.1. Spesifikasi AlF3
Jenis Unit Spesifikasi
AlF3 % 93 minimal
SiO2 % 0,25 maksimal
P2O5 % 0,02 maksimal
Fe2O3 % 0,07 maksimal
Moisture (water content) % 0,35 maksimal
Loss on Ignitation 300-10000C % 0,85 maksimal
Bulk Density Gram/cc 0,7 minimal
Particle Size (Tyler Mesh) Typical
+ 150 mesh % 25-60
+ 200 mesh % 50-75
+ 320 mesh % 75 minimal
2.1.5. Kegunaan Aluminium
Dilihat dari segi kuantitas dan kualitas, kegunaan aluminium dapat mengatasi
kegunaan logam lain kecuali besi. Karena itu aluminium sangat penting dalam
kehidupan sehari-hari dan berpengaruh terhadap perkembangan ekonomi dunia,
dikarenakan aluminium diprediksi akan menjadi komoditi ekspor dunia.
Aluminium murni mempunyai kekuatan tegangan yang rendah, tetapi
mempunyai kemampuan untuk membentuk alloy bersama dengan banyak unsur
seperti tembaga, seng, magnesium, mangan dan silikon. Pada saat ini hampir semua
bahan yang dianggap aluminium adalah sebenarnya sejenis alloy aluminium bukan
aluminium murni.
Apabila digabung secara proses termomekanikal, alloy aluminium menunjukkan
peningkatan kekuatan dari segi sifat mekanikal. Alloy aluminium membentuk
komponen penting dalam pesawat udara dan roket, ini dikarenakan kekuatan yang
meningkat.
Sebagian dari kegunaan-kegunaan aluminium yaitu :
1) Pengangkutan (kendaraan, kapal terbang, kendaraan landasan, kapal laut, dsb)
2) Pembungkus (tin aluminium, keranjang aluminium, dsb)
3) Perawatan air
4) Pembinaan (tingkap, pintu, dwai binaan, dsb)
5) Barang pengguna tahan lama (perkakas, peralatan dapur, dsb)
6) Talian penghantaran elektrik (berat pengalir aluminium adalah setengah dari
8) Aluminium murni
9) Serbuk aluminium, yang mempunyai bentuk perak yang bisa digunakan dalam
cat. Serpihan aluminium juga dimasukkan dalam cat alas, terutama kayu cat
(Oxtoby,2003).
2.2. Alumina
Adapun pembagian dari alumina berdasarkan ukuran partikelnya adalah :
1. Alumina sandy (¥-Al2O3)
Alumina sandy banyak ditemukan di Amerika, yang berbentuk serbuk yang
diproduksi pada pembakaran yang lebih rendah dari alumina floury. Alumina
sandy yang terbentuk digunakan pada tungku peleburan karena sifat dari alumina
tersebut yang bergerak bebas dan tidak dipengaruhi oleh gaya dari luar.
2. Alumina floury (α-Al2O3)
Alumina floury banyak ditemukan di Eropa, dimana alumina jenis ini diperoleh
melalui proses Bayer, selanjutnya diproses lagi untuk memperoleh aluminium
cair. Proses yang digunakan adalah Hall-Heroult, prinsip yang dipakai melalui
reduksi alumina. Reduksi dilakukan secara elektrolisa terhadap alumina yang
dilarutkan dalam larutan elektrolit cair dan dialirkan arus listrik. Dengan
mengalirkan arus listrik tersebut pada kedua elektroda (anoda dan katoda) maka
akan terjadi proses elektrolisa, sehingga terbentuk endapan aluminium cair pada
Tabel 2.2. Spesifikasi alumina yang digunakan di PT INALUM
Item Satuan Spesifikasi
Loss on Ignition (300-10000C) % 1,00 maksimal
SiO2 % 0,03 maksimal
Fe2O3 % 0,03 maksimal
TiO2 % 0,005 maksimal
Na2O % 0,600 maksimal
CaO % 0,060 maksimal
Al2O3 % 98,40 minimal
Spesific Surface Area M2/g 40-80
Particle Size
+ 100 mesh % 12,0 maksimal
+ 150 mesh % 25 minimal
- 325 mesh % 12,0 maksimal
Angle of Refuse Deg 30-34
(PT INALUM,2009).
2.2.1. Kebutuhan Alumina
Selama beroperasinya sel, terjadi pembentukan kerak diatas permukaan
penangas lebur. Alumina ditambahkan ke atas kerak ini dan alumina akan mengalami
pemanasan selanjutnya melepaskan kandungan airnya. Kerak itu dipecahkan secara
aluminium. Tetapi dalam prakteknya, angkanya kira-kira 1,91. Bila kadar alumina
didalam penangas itu sudah berkurang dan efek anoda berlangsung pada anoda itu
terbentuk suatu lapisan tipis karbon tetrafluorida dipenangas itu tidak dapat lagi
membatasi permukaan anoda. Dalam hal ini voltase sel akan naik dan ini terlihat dari
lampu peringatan atau lonceng yang dihubungkan dengan sel dan hanya bekerja jika
sel beroperasi tidak normal. Bila ini terjadi, alumina kemudian diadukkan ke dalam
sel, walaupun waktunya bukanlah waktu penambahan berkala yang direncanakan.
Mengenai mekanisme yang sebenarnya dari pelarutan alumina didalam penangas dan
bagaimana mekanisme dekomposisi elektrolitnya masih belum jelas. Tetapi pada
akhirnya adalah pembebasan oksigen pada anoda dan pengendapan logam aluminium
pada katoda. Oksigen itu bergabung dengan anoda karbon menghasilkan CO dan CO2
tetapi kebanyakan adalah CO2 (Austin,1990).
2.3. Elektrolisa
Hampir semua logam aluminium primer dihasilkan dengan proses elektrolisa
Hall-Heroult. Bahan baku yang digunakan terdiri dari alumina, karbon, kriolit, CaF2,
HF, AlF3 dan tenaga listrik. Terdapat dua jenis tungku reduksi yang dipergunakan
dalam industri peleburan aluminium yaitu Prebaked Anode Furnace (PAF) dan
Soderberg Anode Furnace (SAF). Perbedaan kedua tipe tungku tersebut terletak pada
cara pemanggangan anodanya, dalam sistem PAF anoda dipanggang terlebih dahulu
(prebaked) sebelum dipergunakan. Sedangkan pada sistem SAF tidak dilakukan
pemanggangan pendahuluan, melainkan dimasukkan langsung kedalam tungku
Reaksi kimia yang terpenting yang terjadi ditungku reduksi, adalah reaksi
elektrolisa untuk menghasilkan logam aluminium. Dengan mengalirkan listrik arus
searah, terjadi elektrolisa alumina menjadi ion-ion positif dan ion-ion negatif Al2O3
2Al3+ + 3O2-. Ion aluminium tertarik ke katoda dan dinetralisir sehingga terbentuk
aluminium. Demikian juga ion zat asam mendekati anoda kemudian dinetralisir.
Selain itu terjadi juga reaksi reduksi, dimana karbon yang berasal dari anoda berfungsi
sebagai reduktor mengikat asam :
2Al2O3 + 3C 4Al + 3CO2
Aluminium cair yang terkumpul dibagian bawah tungku selanjutnya dihisap dan
dibawa ke pabrik penuangan. Pada proses Hall-Heroult, logam aluminium diperoleh
dari alumina dengan menggunakan cairan kriolit (Na3AlF6), (titik lebur 10000C) yang
digunakan sebagai pelarut. Sejumlah besar alumina (Al2O3) dilarutkan dalam kriolit,
dimana larutan kriolit dapat menurunkan titik lebur alumina. Campuran kriolit dan
aluminium oksida dielektrolisa dalam sel dan sel lapisan karbon yang berfungsi
sebagai katoda tersimpan didalam cairan aluminium. Pada operasi sel, cairan
aluminium berada pada bagian bawah sel. Dari waktu ke waktu aluminium cairakan
disedot dan selanjutnya akan dibawa ke bagian casting untuk dicetak. Pada operasi sel
ini diperlukan tegangan sebesar 4,0 sampai 5,5 volt, dan arus yang digunakan dari
50.000 sampai 150.000 kA (Kelvin,1994).
2.4. Proses Hall-Heroult
dengan proses reduksi elektrolitik. Proses peleburan ini memakai metode
Hall-Heroult.
Alumina dilarukan dalam larutan kimia yang disebut kriolit pada sebuah
tungku yang disebut pot. Pot ini mempunyai dinding yang dibuat dari karbon. Bagian
luar pot terbuat dari baja. Aliran listrik diberikan melalui anoda dan katoda. Proses
reduksi memerlukan karbon yang diambil dari anoda. Pada proses ini dibutuhkan arus
listrik searah sebesar 190 kA.
Arus listrik akan mengelektrolisa alumina menjadi aluminium dan oksigen
bereaksi membentuk senyawa CO2. Aluminium cair dari hasil elektrolisa akan turun
ke dasar pot dan selanjutnya dialirkan dengan prinsip siphon ke krusibel yang
kemudian diangkut menuju tungku-tungku pengatur (holding furnace).
Kebutuhan listrik yang dihabiskan untuk menghasilkan 1 kg aluminium berkisar
sekitar 12-15 kWh. 1 kg aluminium dihasilkan dari 2 kg alumina dan ½ kg karbon.
Reaksi pemurnian alumina menjadi aluminium adalah sebagai berikut :
9700C
2Al2O3 + 3C 4Al + 3CO2
Na3AlF6 (Daryus,2008).
2.5. Proses Elektrolisis Aluminium
Aluminium terutama masih sekedar menjadi bahan penelitian dilaboratorium
sampai tahun 1886, ketika Charles Hall di Amerika Serikat (lulusan Oberlin College
sendiri-sendiri menemukan proses yang efisien untuk memproduksinya. Pada tahun
1990-an produksi aluminium diseluruh dunia yang menggunakan proses Hall-Heroult
mencapai 1,5 x 107 ton metrik.
Proses Hall-Heroult melibatkan pengendapan aluminium secara katodik, dari
lelehan kriolit (Na3AlF6) yang mengandung Al2O3 terlarut, dalam sel elektrolisis.
Setiap sel terdiri dari kotak baja persegi panjang yang panjangnya sekitar 6 m, lebar 2
m, dan tinggi 1 m, yang berfungsi sebagai katoda, dan grafit pejal sebagai anoda yang
mencuat melewati atap sel hingga ke bak lelehan kriolit. Arus yang sangat besar
(50.000 sampai 100.000 A) dilewatkan dalam sel dan sebanyak 100 sel seperti ini
disusun secara seri.
Lelehan kriolit yang berdisosiasi sempurna menjadi ion-ion Na+ dan AlF63-,
merupakan pelarut yang baik untuk aluminium oksida, menghasilkan distribusi
kesetimbangan dari ion-ion seperti Al3+, AlF2+, AlF2+, AlF3+, AlF4-, AlF52-, AlF63-, dan
O2- dalam elektrolit. Kriolit meleleh pada suhu 10000C, tetapi titik lelehnya turun
dengan adanya aluminium oksida terlarut, sehingga suhu sel operasi hanya 9500C.
Dibandingkan dengan titik leleh Al2O3 murni (20500C), suhu tersebut merupakan suhu
yang rendah, dan ini sebabnya proses Hall-Heroult biasa berhasil. Lelehan aluminium
memiliki kerapatan yang sedikit lebih besar sehingga materi ini mengumpul didasar
sel, untuk selanjutnya disadap secara berkala. Oksigen merupakan produk anoda yang
utama, tetapi zat ini bereaksi dengan elektroda grafit menghasilkan karbon dioksida.
C(s) + O2 (g) CO2 (g) 2C(s) + O2 (g) 2CO(g)
Jika potensial sel elektrolisis lebih besar dari 1,02 Volt maka reaksi yang dapat
terjadi adalah :
Al2O3 + 3C(s) 4Al(l) + 3CO2 (g)
b. Reaksi Katodik
Reaksi yang dapat terjadi disekitar katoda adalah dekomposisi ion AlF4- dari
kriolit menjadi ion Al3+ dan F- :
AlF4- Al3+ + 4F-
Reaksi Al3+ pada katoda;
Al3+ + 3e Al(l)
Dan reaksi antara natrium dari kriolit dengan Al :
Al(l) + 3Na+ 3Na + Al3+
c. Reaksi Utama Elektrolisis Alumina
Reaksi keseluruhan pada industri elektrolisis alumina dengan menggunakan
2Al2O3 (l) + 3C(s) 4Al(l) + 3CO2 (g)
Reaksi ini berlangsung pada temperatur sekitar 9770C, beda potensial 1,18 Volt.
Mekanisme reaksi yang paling sering terjadi adalah reduksi Al2O3 secara langsung
dengan reaksi :
Al2O3 2Al3+
+ 3O
2-Reaksi katodik : 2Al3+ + 6e- 6Al(l)
Reaksi anodik : 3O2- 3/2 O2 + 6e-
2.6 Besi dan Silika
a. Besi
Besi merupakan logam industri terpenting sudah dikenal sejak zaman purba.
Besi merupakan unsur terbanyak keempat dalam litosfer bumi (setelah oksigen,
silikon, aluminium). Kegunaan besi terpenting ialah pembuatan baja (alloy). Besi
yang murni adalah logam berwarna putih-perak, yang kukuh dan liat. Besi melebur
pada temperatur 15350C. Zat-zat pencemar ini memegang peranan penting dalam
kekuatan struktur besi.
Sifat besi yang mudah mengalami korosi pada berbagai keadaan, sifat
elektrokimia besi menjadi bahan kajian sejak lama. Terlihat bahwa oksidasi lebih
tereduksi ke ferro, tetapi dalam keadaan alkali justru ferro berubah menjadi ferri. Agar
Fe(OH)3 tidak mengendap, suasananya harus asam.
Reaksi besi dan oksidasi rumit karena didorong dengan adanya kelembaban.
Produk karatnya non-stoikiometri dan sifatnya dapat protektif maupun tidak. Besi
dapat larut dalam asam mineral encer. Bila asam non-oksidator (tidak ada udara)
terbentuk ferro sedangkan biala ada udara atau asam nitrat dan kromat memasifkan
besi.
Ion ferro dan ferri dalam larutan mudah saling diubah dengan reaksi redoks
ferro hidroksida yang baru diendapkan berwarna putih dengan adanya udara menjadi
hijau atau hitam, kemudian membentuk ferri hidroksida merah cokelat. Amoniak
hanya mengendapkan besi sebagian karena terbentuk kompleks amina.
Ion ferri biasanya merah cokelat akibat bentukan kompleks, sedangkan ion
ferrinya sendiri tidak berwarna. Ferri mengkompleks dengan sianida. Besi merupakan
logam termurah karena sifat fisik menarik, mudah dielektroplating dari berbagai
elektrolit, tetapi besi tidak bernilai dekoratif, tetap terkena korosi, ia hanya dipakai
secara terbatas termasuk electroforming pada cetakan karet, gelas, plastik, pada alloy
nikelnya dan sebagainya.
b. Silika
Silika terdapat luas dialam, seperti pasir, kuarsa, batu api. Kristal silika tidak
berwarna atau merupakan bubuk putih, bau dan tidak berasa, silika tidak larut dalam
akhirnya dipisahkan yang halus dan yang tidak terbentuk. Senyawa SiO2 adalah yang
paling melimpah dari senyawaan dalam kerak bumi.
Asal mula silika adalah dapat dibuat dari larutan silika (air kaca), dengan
asam, kemudian dicuci dan dengan pembakaran. Bunga api silika dibuat dari pasir,
menguap pada temperatur 30000C dengan menggunakan pancaran energi listrik.
Bubuk silika digunakan untuk pembuatan gelas, keramik, alat pengelasan, saringan
air, mikroskop, kertas, komponen dari beton pengisi kosmetik insektisida.
Silika dan oksigen merupakan penyusun sebagian besar kerak bumi, dengan
oksigen meliputi 47% dan silikon 28% dari massanya. Ikatan silikon oksigen kuat dan
bersifat ionic parsial. Ikatan ini membentuk dasar untuk golongan mineral yang
disebut silikat, yang merupakan golongan terbesar dari batuan, lempung, pasir dan
tanah pada kerak bumi. Silikat menyediakan berbagai macam bahan bangunan seperti
batu bata, semen, beton dan kaca (Oxtoby,2003).
2.7. Pengaruh Pengotor Besi dan Silika dalam Produk Aluminium
Aluminium batangan (ingot) yang diproduksi sangat ditentukan oleh
unsur-unsur kimia yang terkandung didalam aluminium itu sendiri. Aluminium yang
dihasilkan masih banyak mengandung zat-zat pengotor dalam jumlah yang kecil,
seperti besi (Fe), silikon(Si), dan pengotor lainnya. Ini dipengaruhi atas bahan baku
yang digunakan untuk menghasilkan aluminium. Disamping adanya pengaruh bahan
apabila kondisi didalam pot kurang baik, sehingga ada pengikisan atau ikut larutnya
dinding pot pada saat proses elektrolisa berlangsung.
Jika kadar besi dalam aluminium cair yang akan dicetak masih terlalu tinggi,
maka aluminium yang dihasilkan akan lebih mudah terkorosi dan mudah berubah
menjadi warna kuning. Sebaliknya, jika kadar silikon didalam aluminium terlalu
tinggi, maka akan menyebabkan aluminium batangan (ingot) yang dihasilkan akan
menjadi keras, rapuh dan susah ditempah. Itulah beberapa pengaruh ketika kadar besi
dan silikon didalam aluminium berlebih atau tidak sesuai dengan standar yang ada.
2.8. Faktor-Faktor yang Mempengaruhi Kualitas Aluminium Batangan (Ingot) dan Cara Penanggulangannya
Faktor yang mempengaruhi kualitas ingot antara lain :
1. Kadar Fe dan Si
Kadar Fe dan Si dapat berpengaruh terhadap kualitas produk, karena
merupakan faktor utama penentu mutu grade yang dihasilkan. Kemurnian dari
aluminium ingot yang dihasilkan dilihat dari kadar besi (Fe) dan silikon (Si).
Maka kadar zat pengotor yang terkandung dalam aluminium cair harus dijaga
sesuai dengan grade produk yang diinginkan. Apabila kadar Fe dan Si masih
banyak terkandung didalam aluminium maka haruslah dikendalikan.
Pemberian flux pada aluminium cair di furnace (dapur) harus sesuai dengan
jumlah molten aluminium sehingga pemisahan oksida-oksida yang terkandung
dalam molten tersebut dapat terpisah secara sempurna, agar aluminium ingot
yang dihasilkan lebih murni.
2.9. Standar Pengendalian Grade Produk
Pengendalian grade produk dilakukan agar ada kesesuaian antara kadar Fe dan
Si terhadap produk, sehingga produk yang dihasilkan bisa mencapai target yang telah
ditetapkan di PT INALUM. Standar pengendalian grade produk berpatokan pada
Quality Standard of Aluminium Ingot (QSAI). QSAI merupakan variabel-variabel
yang ditetapkan agar produk yang dihasilkan tidak menyimpang dari jadwal operasi
pencetakan.
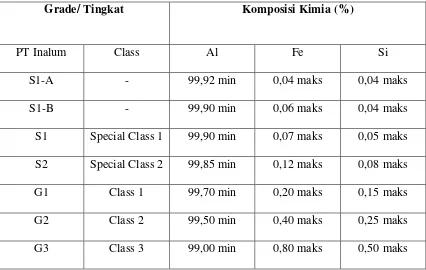
Tabel 2.3. Standar Kualitas Aluminium Batangan (Ingot)
Grade/ Tingkat Komposisi Kimia (%)
PT Inalum Class Al Fe Si
S1-A - 99,92 min 0,04 maks 0,04 maks
S1-B - 99,90 min 0,06 maks 0,04 maks
S1 Special Class 1 99,90 min 0,07 maks 0,05 maks
S2 Special Class 2 99,85 min 0,12 maks 0,08 maks
G1 Class 1 99,70 min 0,20 maks 0,15 maks
Aluminium (ingot) yang dihasilkan PT INALUM sekarang ini adalah grade S1-B dan
G1, yaitu dengan kemurnian aluminium, S1-B 99,90% dan G1 99,70%.
Apabila masih tetap tidak sesuai dengan standarisasi di PT INALUM, maka dapat
dilakukan dengan beberapa cara :
a. Pengadukan ulang
Pengadukan ulang aluminium cair (molten), yang bertujuan agar molten dapat
bercampur secara homogen. Setelah dilakukan pengadukan, lalu dilakukan
pengambilan sampel dan dibawa ke Smelter Quality Assurance (SQA) untuk
dianalisa kembali. Apabila hasil dari Test Product Metal (TPM) menyatakan
kadar Fe dan Si didalam molten masih tinggi dari standar yang diinginkan,
maka dilakukan pengurangan atau penambahan molten.
b. Pengurangan dan penambahan aluminium cair (molten)
Pengurangan molten yang berkadar Fe dan Si yang tinggi kemudian
ditambahkan molten yang memiliki kadar Fe dan Si yang rendah. Sehingga
akan dicapai keseimbangan diantara keduanya. Apabila penambahan dan
pengurangan molten tidak dapat menurunkan kadar Fe dan Si sesuai yang
diinginkan, maka dapat dilakukan cara brikutnya, yaitu pencetakan sebagian
molten.
c. Pencetakan sebagian molten
Dicetak sebagian molten yang berkadar Fe dan Si tinggi sebanyak 1/3 bagian
dicetak, maka molten yang tersisa didalam dapur ditambahkan molten yang
berkadar Fe dan Si yang rendah. Apabila masih tidak dapat memenuhi standar
yang ada, maka dilakukan perubahan grade. Misalnya dari grade S1-B
menjadi grade G1.
Dalam pengambilan sampel produk dapat dilakukan dalam 3 tahap, yaitu :
- Sampel yang pertama diambil pada awal pencetakan, yaitu setelah mencetak
30 ton.
- Sampel yang kedua diambil pada pertengahan pencetakan, yaitu setelah
mencetak 15 ton.
- Sampel ketiga diambil pada akhir pencetakan, yaitu 3 ton terakhir
(PT.INALUM,2010).
BAB 3
BAHAN DAN METODE
3.1. Bahan
- Aluminium Cair
- De-Inclusion Flux
3.2. Alat
- Alat Penciduk Sampel
Digunakan untuk mengambil sampel aluminium cair didalam dapur
- Optical Emission Spectrofotometer (OES)
- Mesin Bubut
Digunakan untuk menghaluskan sampel yang akan dianalisa
3.3. Prosedur Kerja
A. Pengisian Aluminium Cair
- Aluminium cair yang dibawa dari pabrik reduksi dituangkan kedalam
dapur peleburan kemudian diberikan de-inclusion flux untuk mengangkat
- Kemudian dilakukan skimming off untuk membersihkan kotoran-kotoran
yang mengapung diatas permukaan aluminium cair.
B. Pengambilan Sampel Test Product Metal (TPM) Aluminium Cair
- Pengambilan sampel test product metal dilakukan 30 menit sebelum
pencetakan aluminium. Pengambilan sampel dilakukan melalui pintu
samping dapur dengan menggunakan alat penciduk sampel yang diambil ½
meter dari kedalaman aluminium cair didalam dapur.
- Sampel aluminium yang diambil kemudian didinginkan diruangan terbuka
hingga membeku. Setelah dingin, diberi nomor lot terhadap sampel.
- Kemudian sampel dikirim ke bagian Smelter Quality Assurance (SQA)
untuk mengetahui kemurnian dan kandungan zat pengotor, antara lain
silikon (Si) dan besi (Fe).
C. Penganalisaan Produk
- Sampel yang didatangkan dari bagian casting terlebih dahulu dibubut, agar
permukaan dari sampel rata, halus dan bersih.
- Setelah dibubut, sampel dibawa ke ruang OES (Optical Emission
Spectrofotometer).
- Dibuka ruang eksitasi, lalu diletakkan sampel diatas meja eksitasi.
- Kemudian pintu ruang eksitasi ditutup, lalu tekan tombol “enter” pada
keyboard komputer, maka alat OES akan bekerja dengan sendirinya.
- Setelah selesai, buka kembali ruang eksitasi dan sampel dapat dikeluarkan
dari ruang eksitasi.
- Lakukan pengerjaan eksitasi sebanyak 3 kali pengerjaan pada setiap
sampel
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
4.1.1. Data Percobaan
Tabel 4.1. Pengukuran Kadar Si dan Fe di potline 2
Tgl No.Pot Si (%) Fe (%)
02-Jan-2012 301 0.034 0.095
02-Jan-2012 302 0.034 0.101
02-Jan-2012 303 0.046 0.173
02-Jan-2012 304 0.035 0.095
02-Jan-2012 305 0.044 0.088
02-Jan-2012 306 0.163 0.082
02-Jan-2012 307 0.036 0.109
02-Jan-2012 308 0.036 0.108
02-Jan-2012 309 0.038 0.072
02-Jan-2012 310 0.105 0.492
02-Jan-2012 311 0.039 0.202
02-Jan-2012 312 0.053 0.181
02-Jan-2012 313 0.035 0.099
02-Jan-2012 314 0.035 0.076
Tabel 4.1. merupakan hasil pengukuran dibeberapa pot (tungku reduksi), dari
beberapa pot akan dilakukan Metal Tapping (pengambilan metal), lalu dicampur
didalam gedung Smelter Casting (pencetakan). Pencampuran dilakukan berdasarkan
kadar zat pengotornya, sehingga bisa sesuai standar yang ditetapkan di PT INALUM.
Didalam gedung Smelter Casting terdapat dapur pencetakanyang berkapasitas 30 Ton.
Dari gedung Smelter Casting akan diambil sampel, untuk dianalisa dibagian SQA
sebelum akhirnya dicetak.
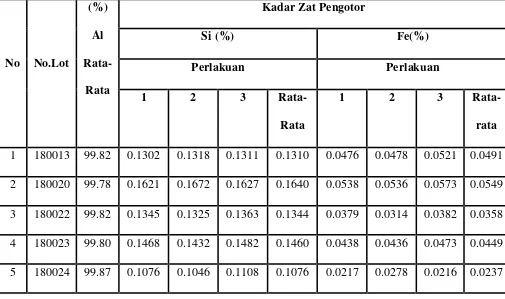
Tabel 4.2. Hasil Analisa Kadar Si Dan Fe di SQA
No No.Lot
4.2. Pembahasan
Dari Tabel 4.1. dipaparkan tentang kandungan zat pengotor silikon (Si) dan besi (Fe)
didalam pot (tungku reduksi), dari beberapa pot tersebut akan dilakukan pencampuran
kedalam dapur pencetakan. Misalnya pot nomor 601, 603, 604, dicampur menjadi
satu, lalu diambil sampel dan dianalisa hingga didapat data seperti dalam tabel 4.2.
Sesuai dengan grade yang telah ditentukan di PT INALUM, aluminium cair yang
akan dicetak berdasarkan data yang ada harus sesuai dengan kemurnian dan grade
yang telah ditentukan, yaitu S2 (special class 2) dan G1 (pada tabel 2.3). Sementara
pencetakan grade S1 belum memungkinkan, dikarenakan kondisi pot yang tidak
maksimal untuk mencapai grade tersebut.
Berdasarkan data, aluminium yang memungkinkan dicetak adalah grade S2 dengan
kadar aluminium 99,85% dan G1 dengan kadar aluminium 99,70%. Sebagai contoh
untuk nomor lot 180024 dengan kemurnian 99,87% harus dicetak untuk grade S2.
Sedangkan nomor lot 180020 dengan kemurnian aluminium 99,78% tidak
memungkinkan dicetak untuk grade S2 atau G1. Karena jika dicetak untuk grade S2,
masih terlalu banyak zat pengotor yang terdapat didalamnya. Sementara untuk grade
G1 masih terlalu tinggi kemurniannya. Hal ini perlu dilakukan penyesuaian terhadap
grade yang ditentukan dengan melakukan pengadukan ulang (re-stirring),
pengurangan atau penambahan aluminium cair (molten) dan pencetakan sebagian
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil analisa yang dilakukan terhadap kadar Si dan Fe dari bahan aluminium cair
di PT INALUM ternyata ada pengaruh terhadap standar kualitas aluminium batangan
yang dihasilkan. Sementara dari hasil data yang diperoleh, kadar zat pengotor tersebut
juga telah sesuai dengan standar yang ditetapkan yaitu untuk nomor lot 180013,
180020, 180022 dan 180023 dapat dicetak untuk grade G1 dengan kemurnian
99,70%. Sedangkan untuk nomor lot 180024 dapat dicetak untuk grade S2 dengan
kemurnian 99,85%.
5.2. Saran
Diusahakan untuk kembali mengamati pengaruh zat pengotor lain seperti tembaga
(Cu) dan timbal (Pb) yang terdapat dalam aluminium cair (molten) sehingga hasil dari
DAFTAR PUSTAKA
Austin, G. T., 1990. Industri Proses Kimia. Jilid I. Edisi Kelima. Jakarta: Erlangga.
Daryus, A., 2008. Proses Produksi. Jakarta: Universitas Darma Persada.
Davis, J. R., 1993. Aluminium and Aluminium Alloys. USA: Davis and Chargin Falls.
Grjotheim, K and Welc, B.L., 1998. Aluminium Smelter Technology. Second Edition.
Desserldorf: Aluminium Verlag.
Hartono, A. J., 1992. Mengenal Lapisan Logam. Yogyakarta: Andi Offset.
Jody, B. J., 1992. Recyling of Aluminium Salt Cake. London: J. Res Management and
Technology.
Kelvin, G. V., 1994. The Chemical World Concept and Aplication. 8th Edition.
Orlondo: Harcourt Brace & Company.
Oxtoby, W. D., 2003. Kimia Modern. Edisi Keempat. Jilid II. Jakarta: Erlangga.
PT Inalum., 2010. Modul OJT SRC Operasi Tungku Reduksi dan Pendukungnya.
Asahan: PT Inalum.
Surdia dan Saito., 2005. Pengetahuan Bahan Teknik. Cetakan Keenam. Jakarta: