PERBEDAAN EKSPRESI RESEPTOR ESTROGEN
DAN RESEPTOR PROGESTERON
PADA JARINGAN MIOMA DAN MIOMETRIUM NORMAL
TESIS
OLEH :
NOVRIAL
DEPARTEMEN OBSTETRI DAN GINEKOLOGI
FAKULTAS KEDOKTERAN
PENELITIAN INI DI BAWAH BIMBINGAN TIM 5
PEMBIMBING :
Prof. dr. Budi R. Hadibroto, SpOG.K
dr. Edy Ardiansyah, M.Ked(OG), SpOG.K
PENYANGGAH :
dr. Christoffel L.Tobing, SpOG.K
Dr. dr. Binarwan Halim, M.Ked(OG), SpOG.K
dr. Riza Rivany, SpOG.K
Diajukan untuk melengkapi tugas
KATA PENGANTAR
LEMBAR PENGESAHAN
Penelitian ini telah disetujui oleh TIM-5 :
PEMBIMBING :
Prof. dr. Budi R. Hadibroto, SpOG.K
...
Pembimbing I
Tgl :
dr. Edy Ardiansyah, M.Ked(OG), SpOG.K
...
Pembimbing II
Tgl :
PENYANGGAH :
dr. Christoffel L.Tobing, SpOG.K
...
Divisi Feto Maternal
Tgl :
Dr. dr. Binarwan Halim, M.Ked(OG), SpOG.K
...
Divisi Fertilitas Endokrinologi dan Reproduksi
Tgl :
dr. Riza Rivany, SpOG.K
…………..….
KATA PENGANTAR
“Bismillaahirrahmaanirrahiim”
Segala Puji dan Syukur saya panjatkan kepada Allah SWT, Tuhan Yang Maha Esa. Hanya atas izin dan kemurahan-Nya lah penulisan tesis ini dapat diselesaikan.
Tesis ini disusun untuk melengkapi tugas-tugas dan memenuhi salah satu syarat untuk memperoleh keahlian dalam bidang Obstetri dan Ginekologi. Sebagai manusia biasa, saya menyadari bahwa tesis saya ini masih banyak kekurangannya dan masih jauh dari sempurna, namun demikian besar harapan saya kiranya tulisan sederhana ini dapat bermanfaat dalam menambah perbendaharaan pustaka, khususnya tentang :
“ PERBEDAAN EKSPRESI RESEPTOR ESTROGEN DAN RESEPTOR PROGESTERON PADA JARINGAN MIOMA DAN MIOMETRIUM NORMAL “
Dengan selesainya laporan penelitian ini, perkenankanlah saya menyampaikan rasa terima kasih dan penghargaan yang setinggi-tingginya kepada yang terhormat :
1. Rektor Universitas Sumatera Utara Prof.Dr.dr.Syahril Pasaribu, DTM&H, MSc (CTM), SpA(K) dan Dekan Fakultas Kedokteran Universitas Sumatera Utara, Prof. dr. Gontar Alamsyah Siregar, SpPD (K-GEH) yang telah memberikan kesempatan kepada saya untuk mengikuti Program Pendidikan Dokter Spesialis di Fakultas Kedokteran USU Medan.
2. Prof. dr. Delfi Lutan, MSc, SpOG(K) dan Dr. dr. M. Fidel Ganis Siregar, M.Ked(OG), SpOG(K), selaku ketua dan sekretaris Departemen Obstetri dan Ginekologi FK-USU, Medan.
4. Kepada Prof. dr. Delfi Lutan, MSc, SpOG(K), Prof. dr. Hamonangan Hutapea, SpOG(K), Prof. Dr. dr. H.M.Thamrin Tanjung, SpOG(K), Prof. dr. R. Haryono Roeshadi, SpOG(K), Prof. dr. T.M.Hanafiah, SpOG(K), Prof. dr. Budi R. Hadibroto, SpOG(K), Prof. dr. Daulat H.Sibuea, SpOG(K), Prof. dr. M. Fauzie Sahil, SpOG (K), dan dr. Deri Edianto, M.Ked(OG), SpOG(K), yang secara bersama-sama telah berkenan menerima saya untuk mengikuti pendidikan dokter spesialis di Departemen Obstetri dan Ginekologi. Semoga Allah SWT membalas kebaikan budi guru-guru saya tersebut.
5. Kepada dr. Henry Salim Siregar, SpOG(K) selaku orang tua angkat saya selama menjalani masa pendidikan, yang telah banyak mengayomi, membimbing dan memberikan nasehat yang bermanfaat kepada saya selama dalam pendidikan.
6. Prof. dr. Budi R. Hadibroto, SpOG(K), dan dr. Edy Ardiansyah, M.Ked(OG), SpOG(K), selaku pembimbing tesis ini, serta dr. Christoffel L.Tobing, SpOG(K), Dr. dr. Binarwan Halim, M.Ked(OG), SpOG(K), dan dr. Riza Rivany, SpOG(K) selaku penyanggah. Terimakasih kepada para guru saya di tim 5 ini, atas segala koreksi, kritik yang membangun, serta atas segala bantuan, bimbingan, juga waktu dan pikiran yang telah diluangkan dengan penuh kesabaran, dalam rangka melengkapi dan menyempurnakan penulisan dan penyusunan tesis ini hingga dapat terselesaikan dengan baik.
7. dr. Muhammad Rusda, M.Ked(OG), SpOG (K) dan dr. Elida R.
Sidabutar, SpOG sebagai pembimbing tesis magister saya bersama Dr. dr. M. Fidel Ganis Siregar M. Ked(OG), Sp.OG (K), dr. Muslich Perangin Angin, SpOG, dan dr. Jenius L. Tobing, SpOG selaku penyanggah dan narasumber dalam penulisan tesis magister saya.
dan Ginekologi saya yang berjudul: “Office Hysteroscopy (Histeroskopi di Klinik Rawat Jalan)”, kepada dr. Ichwanul Adenin, M.Ked(OG), SpOG(K) selaku pembimbing minirefarat Fertilitas Endokrinologi dan Reproduksi saya yang berjudul
“Kegawatdaruratan pada Ginekologi”, dan kepada dr. Roy Yustin Simanjuntak, SpOG(K) selaku pembimbing minirefarat
Onkologi-Ginekologi saya yang berjudul “Penatalaksanaan Toksisitas
Hematologi pada Kemoterapi”.
9. Seluruh staf pengajar Departemen Obstetri dan Ginekologi Fakultas Kedokteran Universitas Sumatera Utara yang tidak dapat saya sebutkan satu persatu, baik di RSUP H. Adam Malik, RSUD dr. Pirngadi, RS Tembakau Deli, RSU Sundari dan RS KESDAM II Putri Hijau, Medan, yang telah banyak membimbing dan mendidik saya sejak awal hingga akhir pendidikan.
10. dr. Jamaludin SpPA dan Ketua Departemen Patologi Anatomi FK USU Medan beserta staf, atas kesempatan dan bimbingan yang telah diberikan selama saya melakukan penelitian dan bertugas di Departemen tersebut.
11. dr. Putri C. Eyanoer, MSEpi, Phd sebagai pembimbing statistik yang telah banyak membantu saya dalam penyelesaian tesis ini.
12. Ketua Departemen Anastesiologi dan Reanimasi FK USU Medan beserta staf, atas kesempatan dan bimbingan yang telah diberikan selama saya bertugas di Departemen tersebut.
13. Direktur RSUP H. Adam Malik Medan yang telah memberikan kesempatan dan sarana kepada saya selama mengikuti pendidikan di Departemen Obstetri dan Ginekologi.
15. Direktur RS Haji Mina Medan dan kepala SMF Kebidanan dan Penyakit Kandungan, dr. H. Muslich Perangin angin, SpOG beserta staf yang telah memberikan kesempatan dan sarana serta bimbingan kepada saya selama bertugas di Rumah Sakit tersebut.
16. Direktur RSU PTPN II Tembakau Deli dan kepala SMF Kebidanan dan Penyakit Kandungan, dr. H. Sofian Abdul Ilah, dr. Nazaruddin Jaffar, SpOG(K) beserta staf yang telah memberikan kesempatan dan sarana serta bimbingan kepada saya selama bertugas di Rumah Sakit tersebut.
17. Direktur RSU Sundari dan kepala SMF Kebidanan dan Penyakit Kandungan, dr. H. M. Haidir, MHA, SpOG beserta staf yang telah memberikan kesempatan dan sarana serta bimbingan kepada saya selama bertugas di Rumah Sakit tersebut.
18. Ka. RUMKIT KesDam II / Bukit Barisan Puteri Hijau dan kepala SMF Kebidanan dan Penyakit Kandungan, Mayor CKM dr. Gunawan Rusuldi, SpOG, dr.Yazim Yacub, SpOG, dr. Agnes SpOG(K) dr. Santa Martha, SpOG, beserta staf yang telah memberikan kesempatan dan sarana serta bimbingan kepada saya selama bertugas di Rumah Sakit tersebut.
19. Direktur RSUD Pandan Kabupaten Tapanuli Tengah beserta staf yang telah memberikan kesempatan untuk bekerja dan sarana selama saya bertugas di Rumah Sakit tersebut.
SpOG, dr. Andri P. Aswar, SpOG, dr. Alfian Z Siregar, SpOG, dr. Errol Hamzah, SpOG, dr. T. Johan Avicena, M.Ked(OG), SpOG, dr. Tigor P Hasugian, M.Ked(OG), SpOG, dr. Elvira M. Shungkar M.Ked(OG), SpOG, dr. Hendry Adi, M.Ked(OG), SpOG, dr. Heika N Silitonga, M.Ked(OG), SpOG, dr. Riske Eka Putri, M.Ked(OG), SpOG, dr. Ali Akbar, M.Ked(OG), SpOG, dr. Arjuna Saputra, M.Ked(OG), SpOG, dr. Janwar Syahnanda, M.Ked(OG), SpOG, dr. Irwansyah Putra, M.Ked(OG), SpOG, dr. Ulfah W Kusuma, M.Ked(OG), SpOG, dr. Ismail Usman, M.Ked(OG), SpOG, dr. Aries Misrawany, dr. Hendri Ginting, M.Ked(OG), SpOG, dr. Robby pakpahan, M.Ked(OG), dr. Meity Elvina, M.Ked(OG), SpOG, dr. M. Yusuf, M.Ked(OG), SpOG, dr. Fatin Ativa, M.Ked(OG), SpOG, dr. Dany Ariyani M.Ked(OG), SpOG, dr. Pantas S Siburian, M.Ked(OG), dr. Morel Sembiring, M.Ked(OG), SpOG, dr. Sri Damayana Harahap, M.Ked(OG), SpOG, dr. Eka Handayani, M.Ked(OG), SpOG, dr. Liza Marosa, M.Ked(OG), dr. M. Rizky P Lubis, M.Ked(OG), dr. M. Arief, M.ked(OG),SpOG, dr. Ferdiansyah Putra, M.Ked(OG), SpOG, dr. Yudha Sudewo, M.Ked(OG), SpOG, dr. Henry Gunawan, M.Ked(OG), saya berterima kasih atas segala bimbingan dan dukungan selama ini.
21. Kepada teman-teman seangkatan saya : dr. Ika Sulaika, dr. Edi Rizaldi, M.Ked(OG), dr. Hotbin Purba, M.Ked(OG), dr. Edward S Manurung, M.Ked(OG), SpOG, dr. Kiko Marpaung, M.ked(OG), SpOG, dr. Erwin Edi Syahputra, dr. Abdurrohim Lubis, M.ked(OG), SpOG, dr. Ricca Puspita Rahim, M.Ked(OG), dr. M. Rizal Sangadji, M.Ked(OG), dr. Julita A Lubis, M.Ked(OG), SpOG, dr. Wahyu Wibowo, M.Ked(OG), SpOG, dr. Ivo Firtian Chanitry, M.Ked(OG), SpOG, dr. Ray Christy Barus, M.Ked(OG), SpOG, dr. Nureliani Amni, dr. Fifianti P Adela, dr.Hiro Hidayah D Nst, M.Ked(OG), SpOG, dr. Anindita Novina, M.Ked(OG), SpOG serta kebersamaan yang indah yang tidak akan terlupakan.
dr. Gamal Darus, dr. Yufi Permana, dr. Nafon Zaitun, dr. Wahyu Utomo, dr. Irliansyah Putra, dr. Reny Junitasari, dr. Ahmad Safik, dr. Yusrizal, dr. Hendri Silaen, dr. Anisa, dr. Qisti dan rekan-rekan junior yang pernah menjadi satu tim jaga yang tidak bisa saya sebutkan semuanya dan telah banyak memberi dukungan, bantuan atas kebersamaan kita selama ini. Terima kasih sebanyak-banyaknya saya ucapkan.
23. Seluruh rekan sejawat PPDS yang tidak dapat saya sebutkan satu persatu, baik para senior maupun junior. Terima kasih atas kerjasama, bantuan, kebersamaan, dorongan semangat dan doa yang telah diberikan.
24. Kepada Almh. Ibu Hj. Asnawati Hsb, Ibu Hj. Sosmalawaty, Ibu Zubaedah, Ibu As, Mimi, Vina, Asih, Anggi, Dewi, Yus, Tuti, Ibu Mawan, kak Nani, dan seluruh pegawai di lingkungan Departemen Obstetri dan Ginekologi RSHAM dan RSPM, terima kasih atas bantuannya selama ini.
25. Seluruh pasien, rekan dokter muda, staf medis, paramedis maupun non medis-paramedis pada seluruh instansi ditempat saya pernah mengikuti pendidikan maupun bertugas. Terimakasih banyak atas segala kerjasama, bantuan, bimbingan, serta kebaikan yang diberikan selama masa pendidikan yang saya jalani.
Tiada kata yang dapat saya ucapkan selain rasa syukur kepada Allah SWT dan Sembah sujud serta terima kasih yang tidak terhingga saya sampaikan kepada kedua orang tua saya yang sangat saya cintai H. Bagindo Syafri dan Hj. Nuriani yang telah membesarkan, membimbing, mendoakan, serta mendidik saya dengan penuh kesabaran dan kasih sayang dari sejak kecil
hingga kini. Terimakasih saya ucapkan kepada Bapak mertua H.
Tiada kata yang bisa mengungkapkan rasa terima kasih kepada Istri saya, Elfira Wahyuni Putri, SE dan teramat khusus untuk Buah hatiku tercinta, Rafif Atharial Fasya dan Farisya Almeira Novri, te r im a ka s ih a tas ka s ih sa yan g, semangat serta doanya dan diiringi permohonan maaf yang sebesar-besarnya karena kesibukan saya dalam menyelesaikan tugas-tugas pendidikan ini, sehingga tugas saya sebagai suami dan ayah sedikit terabaikan, tanpa pengorbanan, doa dan dukungan dari istri saya tercinta, tidak mungkin tugas-tugas ini dapat saya selesaikan. Semoga Allah SWT selalu memberikan kebahagiaan kepada keluarga kita.
Kepada: Adik – adikku, drg. Ivo Asfria, Ilham Syafri S.H, dan
Fajrul Syafri, serta adik iparku, Kamil Fajri, Fahri Firas, Irfansyah, Annisa Fitri, Rizaldi Umar SH, Mkn, terima kasih atas dukungan kepada saya selama menjalani pendidikan.
Kepada seluruh Keluarga yang tidak dapat saya sebutkan namanya satu persatu, baik secara langsung maupun tidak langsung, yang telah banyak memberikan bantuan, dukungan dan doa, saya ucapkan terima kasih yang sebesar-besarnya.
Sem o ga A ll ah SW T sena nt ia sa m em be r i kan r ahm a t- N ya k epad a ki ta semua.
Medan, Juli 2014
DAFTAR ISI
KATA PENGANTAR ……….. i
DAFTAR ISI ………..… viii
DAFTAR GAMBAR ………...…. x
DAFTAR TABEL ……….…… xi
DAFTAR SINGKATAN ………..…... xii
ABSTRAK ………...……xiv
ABSTRACT ……… xv
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ……... 1
1.2. Rumusan Masalah ……... 4
1.3. Tujuan Penelitian ... 5
1.3.1. Tujuan Umum …... 5
1.3.2. Tujuan Khusus ……... 5
1.4. Manfaat Penelitian ... 5
1.4.1. Manfaat teoritis ……… 5
1.4.2. Manfaat metodologis ………. 6
BAB II TINJAUAN PUSTAKA...…………... 7
2.1. Mioma Uteri ……… ... 7
2.2. Patogenesis …………..………..……….… 9
2.3. Hormon Steroid ……....………... 14
2.4 Reseptor Estrogen ………...…... 18
2.5. Reseptor Progesteron ………... 23
2.6. Peranan faktor pertumbuhan pada mioma uteri ………..….24
2.7 Imunohistokimia reseptor estrogen dan reseptor Progesteron ……….. 25
2.8 Hipotesis Penelitian ………...……….………... 28
2.9 Kerangka Teori ……….. 29
BAB III METODE PENELITIAN ... 31
3.1. Rancangan Penelitian ………... 31
3.2. Tempat dan Waktu Penelitian ………... 31
3.3. Subjek Penelitian ………... 31
3.4. Sampel dan besar sampel ... 31
3.4.1 Sampel …………...…... 31
3.4.2 Besar sampel ………... 32
3.5. Kriteria Penelitian ... 33
3.5.1 Kriteria Eksklusi ………... 33
3.6 Cara kerja dan teknik pengumpulan data ... 33
3.7 Prosedur Pemeriksaan Imunohistokimia ………. 34
3.7.1 Alat penelitian ……….. 34
3.7.2 Bahan penelitian ………. 34
3.7.3 Cara kerja ……… 34
3.7.4 Instrumen penelitian ………...… 35
3.8 Defenisi operasional ………... 36
3.9 Analisis Data ………... 37
3.10 Alur Penelitian ………... 38
BAB IV HASIL DAN PEMBAHASAN ………... 39
BAB V KESIMPULAN DAN SARAN ... 48
5.1 Kesimpulan ………...……… 48
5.2 Saran ………..……….. 49
DAFTAR PUSTAKA ... 50
DAFTAR GAMBAR
Gambar 1 Tumorigenesis mioma uteri ...………...… 12 Gambar 2 Interaksi antara hormon ovarium , β-Catenin dan jalur TGF-β, dan MED12 pada sel mioma ...…... 14 Gambar 3 Regulasi hormon steroid terhadap faktor pertumbuhan ... 16 Gambar 4 Efek biologis dari estrogen dan progesteron pada jaringan mioma ………. 19 Gambar 5 Super famili reseptor nukleus ………... 20 Gambar 6 Ekspresi reseptor estrogen dan reseptor progesteron pada
DAFTAR TABEL
Tabel 2.1 Faktor pertumbuhan dan protein yang berhubungan pada miometrium dan mioma manusia : keberadaan, kerja dan
pengaturan seks steroid ………... 27 Tabel 3.1 Penilaian proportion score (PS) dan intensity score (IS) …...… 35 Tabel 3.2 Skor total imunohistokimia RE dan RP ………..….. 36 Tabel 4.1 Distribusi frekuensi mioma dan miometrium normal
berdasarkan karakteristik ………….……… 39 Tabel 4.2 Distribusi Jenis Mioma ……….… 43 Tabel 4.3 Perbedaan rerata skor ekspresi RE dan RP
pada mioma dan miometrium normal ………..………….… 44 Tabel 4.4 Perbedaan rerata skor ekspresi RE dan RP berdasarkan
DAFTAR SINGKATAN
bFGF : basic Fibroblast Growth Factor
DNA : Deoxyribonucleic Acid
EGF : Epidermal Growth Factor
EGFR : Epidermal Growth Factor Receptor
GnRH : Gonadothrophin Releasing Hormone HMGA2 : High Mobility Group A2
IGF : Insulin-like Growth Factor
IGFBP : Insulin-like Growth Factor Binding Protein
IHC : Immunohistochemistry
IMT : Indeks Massa Tubuh
IS : Intensity Score
MAPK : Mitogen-activated Protein Kinase
mRNA : messenger Ribonucleic Acid
MED 12 : Mediator Complex Subunit 12 PDGF : Platelet-derived Growth Factor
PPAR : Peroxisome Proliferator Activated Receptor
PS : Proportion Score
RE : Reseptor Estrogen
RP : Reseptor Progesteron
RG : Reseptor Glukokortikoid
RA : Reseptor Androgen
RM : Reseptor Mineralokortikoid
RVD : Reseptor Vitamin D
RT : Reseptor Tiroid
SMAD : Mothers Against Decapentaplegic
SERMs : Selective Estrogen Receptor Modulators SPRMs : Selective Progesterone Receptor Modulators
TGF : Transforming Growth Factor
TCF : T-cell Transcription Factor
TS : Total Score
VEGF : Vascular Endothelial Growth Factor
WNT : Wingless Type
PERBEDAAN EKSPRESI RESEPTOR ESTROGEN DAN RESEPTOR PROGESTERON
PADA JARINGAN MIOMA DAN MIOMETRIUM NORMAL
Novrial
Christoffel L Tobing, Binarwan Halim, Riza Rivany , Budi R Hadibroto, Edy Ardiansyah,
Departemen Obstetri dan Ginekologi Fakultas Kedokteran Universitas Sumatera Utara Abstrak.
Tujuan : Untuk mengetahui perbedaan ekspresi reseptor estrogen dan reseptor progesteron pada jaringan mioma dan miometrium normal
Metode : Penelitian ini bersifat analitik dengan studi case-control. Melalui pemilhan acak sederhana diperoleh pasien yang memenuhi kriteria penelitian pada masing-masing kelompok mioma uteri dan miometrium normal. Penelitian ini dilakukan dengan melihat catatan rekam medis dan menilai ekspresi reseptor estrogen dan reseptor progesteron terhadap blok parafin jaringan mioma uteri dan miometrium normal yang diperoleh dari miomektomi atau histerektomi pada pemeriksaan imunohistokimia.
Hasil : Berdasarkan usia, sebagian besar pederita mioma uteri dan miometrium normal berada pada usia diatas 40 tahun, indeks massa tubuh normoweight pada kedua kelompok dan status paritas adalah multipara pada mioma uteri dan grandemultipara pada miometrium normal. Berdasarkan jenis mioma, yang terbanyak adalah jenis mioma intramural (50% kasus). Ekspresi reseptor estrogen dan reseptor progesteron lebih tinggi secara bermakna pada mioma uteri (5.83 ± 1.14; 6.50 ± 1.43) daripada miometrium normal (3.93 ± 1.59; 4.27 ± 1.94), dengan nilai p=0.000 dan p=0.000. Namun, tidak terdapat perbedaan yang bermakna berdasarkan jenis mioma pada skor eskpresi reseptor estrogen (p=0.301), dan juga skor ekspresi reseptor progesteron (p=0.257).
Kesimpulan : Terdapat perbedaan ekspresi reseptor estrogen dan reseptor progesteron yang bermakna antara jaringan mioma uteri dan miometrium normal, namun tidak terdapat perbedaan yang bermakna berdasarkan jenis mioma uteri.
DIFFERENCE OF ESTROGEN AND PROGESTERONE RECEPTOR
EXPRESSION IN LEIOMYOMA AND NORMAL MYOMETRIAL TISSUE
Novrial
Christoffel L Tobing, Binarwan Halim, Riza Rivany , Budi R Hadibroto, Edy Ardiansyah,
Department of Obstetrics and Gynecology Faculty of Medicine Universitas Sumatera Utara
Abstract
Objective : To describe the difference of estrogen and progesterone receptor in leiomyoma and normal myometrial tissue.
Methods : This study is analityc study with case-control approach. Through simple random sampling, 30 patients who satisfied study criteria were obtained for each group of leiomyoma and normal myometrial tissue. This study was performed by collecting data from medical record and assesing estrogen and progesterone receptor expression of cells derived from paraffin block from hysterectomy or myomectomy procedure on immunohistochemical examination.
Results : Based on ages, majority of leiomyoma and normal myometrial patients are most ≥ 40 years old, normoweight body mass index are in both of groups, and from parity, are most multipara in leiomyoma patients and grandemultipara in normal myometrial patients. Based on type of leiomyoma, the most is intramural type (50% of cases). Estrogen and progesterone receptor expression significantly higher in leiomyoma group (5.83 ± 1.14; 6.50 ± 1.43) than normal myometrial group (3.93 ± 1.59; 4.27 ± 1.94), with p value 0.000 and 0.000. However, there are no significant differences based on type of leiomyoma in estrogen receptor expression score (p=0.301) and progesterone receptor expression score (p=0.257).
Conclusion : There are significant differences of estrogen and progesterone receptor expression between leiomyoma and myometrial tissue, however there are no significant differences based on type of leiomyoma.
PERBEDAAN EKSPRESI RESEPTOR ESTROGEN DAN RESEPTOR PROGESTERON
PADA JARINGAN MIOMA DAN MIOMETRIUM NORMAL
Novrial
Christoffel L Tobing, Binarwan Halim, Riza Rivany , Budi R Hadibroto, Edy Ardiansyah,
Departemen Obstetri dan Ginekologi Fakultas Kedokteran Universitas Sumatera Utara Abstrak.
Tujuan : Untuk mengetahui perbedaan ekspresi reseptor estrogen dan reseptor progesteron pada jaringan mioma dan miometrium normal
Metode : Penelitian ini bersifat analitik dengan studi case-control. Melalui pemilhan acak sederhana diperoleh pasien yang memenuhi kriteria penelitian pada masing-masing kelompok mioma uteri dan miometrium normal. Penelitian ini dilakukan dengan melihat catatan rekam medis dan menilai ekspresi reseptor estrogen dan reseptor progesteron terhadap blok parafin jaringan mioma uteri dan miometrium normal yang diperoleh dari miomektomi atau histerektomi pada pemeriksaan imunohistokimia.
Hasil : Berdasarkan usia, sebagian besar pederita mioma uteri dan miometrium normal berada pada usia diatas 40 tahun, indeks massa tubuh normoweight pada kedua kelompok dan status paritas adalah multipara pada mioma uteri dan grandemultipara pada miometrium normal. Berdasarkan jenis mioma, yang terbanyak adalah jenis mioma intramural (50% kasus). Ekspresi reseptor estrogen dan reseptor progesteron lebih tinggi secara bermakna pada mioma uteri (5.83 ± 1.14; 6.50 ± 1.43) daripada miometrium normal (3.93 ± 1.59; 4.27 ± 1.94), dengan nilai p=0.000 dan p=0.000. Namun, tidak terdapat perbedaan yang bermakna berdasarkan jenis mioma pada skor eskpresi reseptor estrogen (p=0.301), dan juga skor ekspresi reseptor progesteron (p=0.257).
Kesimpulan : Terdapat perbedaan ekspresi reseptor estrogen dan reseptor progesteron yang bermakna antara jaringan mioma uteri dan miometrium normal, namun tidak terdapat perbedaan yang bermakna berdasarkan jenis mioma uteri.
DIFFERENCE OF ESTROGEN AND PROGESTERONE RECEPTOR
EXPRESSION IN LEIOMYOMA AND NORMAL MYOMETRIAL TISSUE
Novrial
Christoffel L Tobing, Binarwan Halim, Riza Rivany , Budi R Hadibroto, Edy Ardiansyah,
Department of Obstetrics and Gynecology Faculty of Medicine Universitas Sumatera Utara
Abstract
Objective : To describe the difference of estrogen and progesterone receptor in leiomyoma and normal myometrial tissue.
Methods : This study is analityc study with case-control approach. Through simple random sampling, 30 patients who satisfied study criteria were obtained for each group of leiomyoma and normal myometrial tissue. This study was performed by collecting data from medical record and assesing estrogen and progesterone receptor expression of cells derived from paraffin block from hysterectomy or myomectomy procedure on immunohistochemical examination.
Results : Based on ages, majority of leiomyoma and normal myometrial patients are most ≥ 40 years old, normoweight body mass index are in both of groups, and from parity, are most multipara in leiomyoma patients and grandemultipara in normal myometrial patients. Based on type of leiomyoma, the most is intramural type (50% of cases). Estrogen and progesterone receptor expression significantly higher in leiomyoma group (5.83 ± 1.14; 6.50 ± 1.43) than normal myometrial group (3.93 ± 1.59; 4.27 ± 1.94), with p value 0.000 and 0.000. However, there are no significant differences based on type of leiomyoma in estrogen receptor expression score (p=0.301) and progesterone receptor expression score (p=0.257).
Conclusion : There are significant differences of estrogen and progesterone receptor expression between leiomyoma and myometrial tissue, however there are no significant differences based on type of leiomyoma.
BAB I PENDAHULUAN
1.1. Latar Belakang
Mioma uteri merupakan neoplasma jinak yang berasal dari otot polos
uterus dan bersifat monoklonal.1,2 Prevalensi mioma uteri di Amerika
serikat sekitar 35-50%.1 Namun, dengan inspeksi patologi uterus yang
seksama, prevalensi mioma uteri meningkat lebih dari 70%, karena mioma
uteri dapat terjadi tanpa gejala pada banyak wanita.3 Di Indonesia kasus
mioma uteri ditemukan sebesar 2,39% - 11,70% dari semua penderita
ginekologi yang dirawat.4 Insidensi mioma uteri di RS Dr. RD Kandou
Manado dijumpai sekitar 30.6%, sedangkan di RS Pirngadi Medan selama
tahun 2009-2011 ditemukan kasus mioma uteri sebanyak 152 kasus.5,6
Puncak insidensi mioma uteri berada pada dekade keempat dan menurun
setelah menopause.3,7
Mioma uteri memberikan gejala pada 20 – 30% wanita usia
reproduktif dan menyebabkan berbagai gangguan klinis seperti
perdarahan uterus abnormal, anemia, gangguan implantasi embrio,
abortus berulang, persalinan prematur, hambatan persalinan,
ketidaknyamanan pelvis, dan inkontinensia urin serta gejala yang
berhubungan dengan adanya massa pelvis yang besar.2,8 Sebanyak
71.4% penderita mioma uteri yang dirawat di RS H Adam Malik Medan
menderita anemia.9 Di Amerika Serikat, mioma uteri murupakan indikasi
prosedur miomektomi dan ribuan prosedur embolisasi arteri uterina setiap
tahunnya, sementara histerektomi dan miomektomi dilakukan pada 50%
dan 13.2% kasus mioma uteri di RS Pirngadi Medan.2,6,10
Meskipun insidensi mioma uteri cukup tinggi, sedikit yang diketahui
tentang penyebabnya. Aspek yang paling penting dari penyebab mioma
ini masih belum diketahui. Beberapa teori telah diajukan, salah satu
hipotesa menyatakan bahwa peningkatan kadar estrogen dan progesteron
menyebabkan peningkatan tingkat mitosis yang dapat berkontribusi pada
terjadinya mioma dengan meningkatkan kemungkinan mutasi somatik.3
Bukti lain yang mendukung konsep bahwa estrogen dan progesteron
dapat berpengaruh pada biologi miometrium dan mioma adalah dengan
memberikan up-regulating dan down-regulating dari berbagai faktor
pertumbuhan. Beberapa faktor pertumbuhan yang teridentifikasi yang
berhubungan dengan mioma adalah Transforming Growth Factor-β (TGF -β), basic Fibroblast Growth Factor (bFGF), Epidermal Growth Factor
(EGF), Platelet-derived Growth Factor (PDGF), Vascular Endothelial
Growth Factor (VEGF), Insulin-like Growth Factor (IGF) dan Prolaktin.3,11 Hal lain yang menyokong suatu abnormalitas bawaan pada
miometrium pada individu dengan mioma adalah adanya temuan
peningkatan kadar reseptor estrogen (RE) yang bermakna pada jaringan
mioma.3 Pada berbagai studi, konsentrasi RE dan reseptor progesteron
(RP) lebih tinggi pada jaringan mioma daripada miometrium normal.
Terdapat dua bentuk dari RP yaitu RP-A dan RP-B, yang diekspresikan
dominan pada kedua jaringan.12 Sedangkan pengaruh estrogen pada
pertumbuhan dan perkembangan mioma dimediasi oleh dua ligan yaitu
RE-α dan RE-β.10 Interaksi antara kedua hormon steroid dan kadar
reseptornya telah menjadi bahan penelitian yang menarik yang
berhubungan dengan pertumbuhan mioma. Terdapat bukti yang kuat
bahwa pengaruh estrogen akan meningkatkan kadar RE dan RP pada
miometrium, sedangkan pengaruh progesteron akan menurunkan kadar
RE.12
Karena estrogen mempengaruhi pertumbuhan mioma, maka segala
molekul yang menghambat aktivitas estrogen mempunyai aktivitas
terapeutik yang potensial terhadap mioma. Begitu juga halnya pengaruh
progesteron pada jaringan target dimediasi melalui RP, sedangkan
antagonis RP menurunkan kerja biologi progesteron dengan menghambat
aktivasi RP. Berdasarkan hal tersebut, kemungkinan bahwa antiprogestin
dan agonis/antagonis RP dapat dipakai dalam manajemen medis mioma
uteri.13
Wango dkk (2002) mendapatkan bahwa kadar RE dan RP lebih
tinggi pada mioma dibandingkan dengan miometrium normal.14 Hasil yang
sama juga diperoleh dari penelitian Englund dkk (1998) bahwa ekspresi
RE dan RP lebih tinggi secara bermakna pada mioma daripada
miometrium normal.15 Penelitian oleh Benassayag dkk (1999) serta oleh
Bakas dkk (2008) menemukan bahwa ekspresi dari mRNA RE lebih tinggi
Sebaliknya, studi yang dilakukan oleh Grings dkk (2012)
menunjukkan bahwa ekspresi protein RE-α dan RE-β tidak berbeda pada
mioma dan miometrium normal yang menunjukkan bahwa jika
dibandingkan dengan miometrium, over ekspresi RE-α dan RE-β pada
mioma uteri tidak menyebabkan pertumbuhan tumor.18 Namun, Nisolle
dkk (1999) menemukan terdapat peningkatan yang bermakna dari
ekspresi RE pada mioma uteri daripada miometrium, tetapi tidak terdapat
perbedaan yang bermakna dari ekspresi RP.19
Berdasarkan hal diatas dapat dilihat bahwa patogenesis dan etiologi
mioma uteri masih sangat kompleks dan dipengaruhi oleh berbagai faktor,
dan belum ada penelitian yang meneliti hal ini sebelumnya di Departemen
Obstetri dan Ginekologi FK USU, maka peneliti ingin meneliti bagaimana
ekspresi dari reseptor estrogen dan reseptor progesteron pada jaringan
mioma dan miometrium normal.
1.2. Rumusan masalah
Prevalensi mioma uteri yang masih cukup tinggi dan pengaruhnya
yang sangat mengganggu pada wanita usia reproduktif, sementara itu
penelitian tentang etiopatogenesa mioma uteri yang berkaitan dengan
ekspresi reseptor estrogen dan reseptor progesteron masih terdapat
pertentangan, maka rumusan masalah pada penelitian ini adalah apakah
terdapat perbedaan ekspresi reseptor estrogen dan reseptor progesteron
1.3. Tujuan Penelitian 1.3.1. Tujuan Umum
Mengetahui perbedaan ekspresi reseptor estrogen dan reseptor
progesteron pada mioma dan miometrium normal
1.3.2. Tujuan Khusus
1. Mengetahui distribusi frekuensi penderita mioma dan miometrium
normal berdasarkan karakteristik (usia, IMT, paritas)
2. Mengetahui distrubusi jenis mioma pada penderita mioma uteri.
3. Mengetahui perbedaan ekspresi reseptor estrogen pada mioma
dan miometrium normal.
4. Mengetahui perbedaan ekspresi reseptor progesteron pada mioma
dan miometrium normal.
5. Mengetahui perbedaan ekspresi reseptor estrogen pada tiap jenis
mioma.
6. Mengetahui perbedaan ekspresi reseptor progesteron pada tiap
jenis mioma.
1.4. Manfaat Penelitian 1.4.1 Manfaat teoritis
Memberikan informasi tambahan tentang patogenesis dari mioma
uteri yang berkaitan dengan ekspresi reseptor estrogen dan
reseptor progesteron, dan dapat menjadi dasar pada penelitian
1.4.2 Manfaat Metodologis
Dapat mengetahui bagaimana pemeriksaan ekspresi reseptor
estrogen dan reseptor progesteron pada mioma dan miometrium
BAB II
TINJAUAN PUSTAKA
2.1. Mioma uteri
Mioma uteri merupakan tumor pelvis yang paling sering pada
wanita. Tumor jinak ini berasal dari miometrium uterus dan secara
histopatologi ditandai dengan sel-sel otot polos seperti kumparan yang
membentuk nodul dengan batas yang tegas. Mioma uteri mempunyai
onset puncak pada dekade ketiga dan keempat kehidupan dan
menyebabkan gejala pada 20-25% wanita usia reproduktif.20 Prevalensi
mioma uteri pada wanita kulit adalah sebesar 9% dan pada wanita
Afrika-Amerika 16%. Tetapi hanya sepertiga wanita yang didiagnosa pada saat
operasi yang memang sebelumnya sudah didiagnosa sebagai mioma
uteri, yang menunjukkan bahwa mioma tersebut tidak terdeteksi
sebelumnya atau tidak adanya gejala yang dialami oleh pasien.21 Insidensi
kumulatif mioma uteri pada usia 50 tahun adalah 70% pada wanita kulit
putih dan 80% pada wanita Afrika-Amerika.20 Angka kejadian mioma uteri
di Amerika Serikat sebesar 8 orang per 1000 wanita tiap tahunnya.22
Sedangkan di Indonesia kasus mioma uteri ditemukan sebesar 2,39% -
11,70% dari semua penderita ginekologi yang dirawat.4
Studi pertama dari patologi tumor ini dilakukan pada tahun 1793,
dan miomektomi abdominal pertama dilaporkan pada tahun 1838. Dengan
kemajuan dalam pembedahan dan anastesia, pada awal tahun 1900-an
Insidensi mioma uteri meningkat dengan bertambahnya usia. Pada
usia 25 – 30 tahun insidensi mioma uteri hanya 0.31 per 1000 wanita,
tetapi pada usia 45 – 50 tahun insidensinya meningkat 20 kali menjadi 6.2
per 1000 wanita. Kesempatan untuk terdiagnosa mioma uteri meningkat
sejalan dengan usia sampai usia 50 tahun, kemudian setelah itu menurun
dengan tajam. Selain usia Obesitas juga meningkatkan resiko mioma uteri
sebesar 18% setiap peningkatan berat badan 10 kg dan terdapat
peningkatan resiko mioma sebanyak 2.3 pada wanita dengan indeks
massa tubuh diatas kuartil.21
Risiko terjadinya mioma uteri menurun dengan peningkatan paritas
dan peningkatan usia saat kehamilan aterm. Nulli paritas merupakan
faktor resiko untuk terjadinya mioma uteri dan dengan adanya kehamilan,
akan mengurangi waktu paparan terhadap unopposed estrogen. Data
menunjukkan bahwa penurunan resiko berkisar dari 20 sampai 50% pada
wanita yang melahirkan minimal 1 kali.7 Wanita dengan 2 kali hamil cukup
bulan mempunyai resiko setengah kali menjadi mioma. Merokok
menurunkan resiko (dengan menurunkan kadar estrogen), dan obesitas
meningkatkan resiko (dengan meningkatkan kadar estrogen). Walaupun
resiko mioma yang lebih rendah berhubungan dengan faktor yang
menurunkan kadar estrogen, termasuk kurus, merokok, dan latihan,
pemakaian kontrasepsi oral tidak berhubungan dengan peningkatan
resiko mioma uteri.22 Terdapat anggapan sedikit peningkatan resiko
mioma berhubungan dengan usia menars yang dini (7-9 tahun). Siklus
dialami miometrium selama usia reproduktif, yang menyebabkan
peningkatan resiko terjadinya mutasi gen yang mengontrol proliferasi
miometrium.3
Diperkirakan sekitar lebih dari 40% saudara tingkat pertama dari
wanita yang menderita mioma akan menderita mioma uteri juga dalam
kehidupannya.23 Hal ini mungkin tanpa gejala, dan jumlah serta lokasinya
sulit diprediksi. Sementara mioma umum terjadi pada semua ras,
tampaknya wanita kulit hitam memiliki insidensi yang sedikit lebih tinggi
daripada etnis lain. Di Amerika, wanita kulit hitam mempunyai resiko 3-9
kali lebih tinggi menderita mioma uteri.4,23,24 Mioma uteri ini menimbulkan
masalah besar dalam kesehatan dan terapi yang paling efektif belum
ditemukan, karena sedikit sekali informasi mengenai etiologi mioma uteri
itu sendiri.1
2.2 Patogenesis
Mioma uteri merupakan neoplasma jinak yang muncul dari otot
polos uterus. Penyebab pasti mioma uteri sampai saat ini masih belum
ditemukan. Meyer dan De Snoo mengajukan teori Cell Nest atau teori genitoblas. Menurut Meyer asal mioma uteri adalah sel imatur, bukan dari
sel-sel otot yang matur. Mioma uteri dipercaya berasal dari mutasi somatik
pada sel miometrium, hasil dari kegagalan proses pertumbuhan. Beberapa
penelitian Glucose-6-phospate dehydrogenase menunjukkan bahwa
mioma uteri berasal dari monoklonal. Tumor tumbuh sebagai klon
abnormal secara genetik muncul dari sel progenitor tunggal (tempat asal
Perbedaan kecepatan pertumbuhan dapat menunjukkan
perbedaan sitogenetik yang muncul pada masing-masing tumor. Mioma
uteri multipel dalam satu uterus tidak berkaitan secara klonal satu dengan
yang lainnya, masing–masing mioma tumbuh secara individual. Kehadiran
mioma uteri multipel (dimana memiliki tingkat kekambuhan yang lebih
tinggi dibandingkan yang tunggal) dianggap merupakan predisposisi
genetik terhadap pembentukan mioma uteri. Namun, warisan mioma uteri
dalam keluarga masih belum diteliti dengan baik. Tidak pasti apakah
mioma uteri tumbuh secara individu atau berasal dari mioma yang lain.22
Asal dari mioma uteri belum sepenuhnya dipahami, studi
sitogenetik telah menghasilkan beberapa petunjuk tentang bagaimana dan
mengapa mioma ini berkembang. Tiap tumor berkembang dari sel otot
tunggal, yaitu progenitor miosit, dengan demikian tiap mioma adalah
monoklonal. Analisis sitogenetik telah menunjukkan bahwa mioma
mempunyai kelainan kromosom multipel. Semakin besar mioma, semakin
banyak akan terdeteksi kelainan kariotip. Menariknya, kelainan kromosom
dari mioma mempunyai perubahan kluster yang luar biasa. Duapuluh
persen kelainan melibatkan translokasi antara kromosom 12 dan 14. Tujuh
belas persen melibatkan delesi kromosm 7. Duabelas persen melibatkan
delesi kromosom 12. Regio yang terkena pada kromosom 12 juga
abnormal pada banyak jenis tumor solid lainnya.28
Salah satu teori yang diajukan sabagai penyebab mioma uteri
adalah adanya peningkatan kadar estrogen dan progesteron yang
kemungkinan mutasi somatik. Hal lain yang menyokong adalah adanya
temuan peningkatan kadar RE dan RP yang bermakna pada jaringan
mioma daripada miometrium normal.3,12
Jaringan mioma manusia mengandung jumlah sel stem yang lebih
sedikit daripada miometrium normal. Namun, sel stem yang berasal dari
jaringan mioma, dengan mutasi MED 12 (suatu mediator yang mengkode
gen), yang menunjukkan bahwa minimal diawali dengan satu genetic hit
yang merubah sel stem miometrium, dan interaksi selanjutnya dengan
jaringan miometrium disekitrarnya untuk membentuk mioma.2
Model eksperimen in vivo menunjukkan bahwa pertumbuhan
mioma manusia bergantung pada estrogen dan progesteron yang
memerlukan adanya sel stem somatik multipoten. Dibandingkan dengan
populasi sel mioma atau dengan sel miometrium normal, sel stem mioma
mengekspresikan kadar RE dan RP yang rendah. Pertumbuhan sel stem
mioma memerlukan adanya sel-sel miometrium dengan kadar RE dan RP
dan ligannya yang lebih tinggi, yang menunjukkan bahwa kerja hormon
streroid pada sel stem mioma diperantarai oleh sel-sel miometrium dalam
pengaruh parakrin. Kemungkinan bahwa interaksi parakrin ini dengan
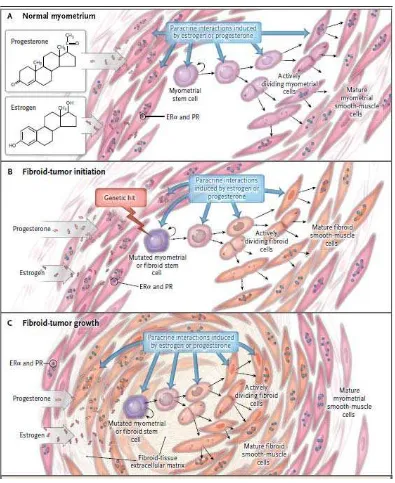
sel-sel sekitarnya mendukung kemampuan self-renewal dari sel stem mioma.2 Jaringan miometrium normal dan mioma mengandung pool sel dengan kapasitas untuk self-renewal, yang disebut dengan sel stem.
Suatu populasi sel stem bertanggung jawab terhadap proliferasi sel-sel
otot polos miometrium normal (Gambar 1A) yang tampak pada proses
yang matur mengekspresikan kadar RE-α dan RP yang lebih tinggi
daripada sel-sel stem. Dengan demikian kemungkinan proliferasi sel-sel
yang bergantung pada estrogen dan progesteron secara primer di
perantarai oleh RE-α dan RP yang ada pada sel-sel yang matur. Faktor
parakrin seperti ligan WNT, yang dikeluarkan oleh sel-sel matur bekerja
pada sel stem untuk merangsang self-renewal dan proliferasi mereka.
Suatu benturan genetik (genetic hit) seperti mutasi dari MED 12 atau pengaturan ulang kromosom mempengaruhi HMGA2 (suatu protein
yang dapat mempengaruhi proses pada sel seperti difrensiasi, kematian,
pertumbuhan dan proliferasi), yang dapat merubah sel-sel stem
miometrum menjadi sel-sel stem mioma (Gambar 1B). Sel-sel mioma ini
dapat memperbarui diri sendiri dan mulai membelah secara tidak
terkendali sampai berdifrensiasi menjadi sel otot polos mioma. Selama
proses ini sel-sel otot polos mioma memperoleh banyak abnormalitas
epigenetik dan fenotipik. RE-α dan RP terkonsentrasi secara primer pada
sel-sel mioma yang matur dan melewatkan sinyal estrogenik atau
progestogenik pada sel stem melalui mekanisme parakrin. Sel stem
mioma tunggal yang bertransformasi pada akhirnya menjadi mioma yang
jinak dengan batas yang tegas, dimana meluas dalam jaringan
miometrium (Gambar 1C). Pembentukan matriks ekstraselular
berkontribusi terhadap ekspansi tumor.2
Karena konsentrasi RE-α dan RP sangat tinggi pada sel-sel
miometrium dan sel-sel mioma matur dibandingkankan dengan sel-sel
stem, kemungkinan sinyal estrogen dan progesteron dikirimkan ke sel-sel
stem mioma melalui reseptor hormon pada sel-sel matur dengan cara
parakrin. Estrogen dan progesteron dapat meningkatkan sekresi ligan
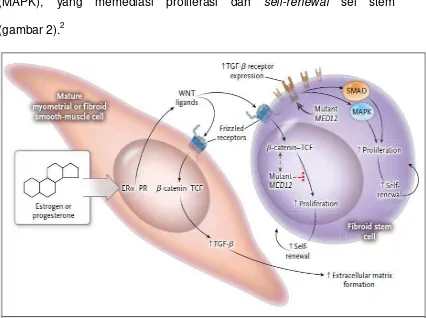
WNT, yang bekerja melalui famili frizzeled reseptor yang mengaktivasi jalur β-catenin-TCF (T-cell Transcription Factor), yang selanjutnya
menginduksi produksi dari TGF-β pada sel-sel matur dan menyebabkan
MED12 yang non-mutan bekerja sebagai modifier fisiologis dari kerja β -catenin, sedangkan MED12 yang mutan (atau absennya MED12) dapat
menyebabkan kegagalan untuk menyelesaikan fungsi ini. Absennya
MED12 atau adanya bentuk MED12 yang mutan pada sel-sel stem juga
dihubungkan dengan meningkatnya ekspresi reseptor TGF-β, yang
menyebabkan aktivasi dari downstream sinyalnya. Ini kemudian
mengaktivasi protein famili SMAD dan mitogen-activated protein kinase
(MAPK), yang memediasi proliferasi dan self-renewal sel stem
(gambar 2).2
Gambar 2.Interaksi antara hormon ovarium , β-Catenin dan jalur TGF-β, dan MED12 pada sel mioma (dikutip dari 2)
2.3 Hormon steroid
Secara umum estrogen, progesteron dan androgen merupakan
hormon ini diproduksi oleh ovarium. Bahan dasar pembentukan hormon–
hormon ini adalah kolesterol dan proses pembentukan hormon–hormon,
disebut juga steroidogenesis ini dibantu oleh beberapa enzim dan protein
regulator. Kemudian hormon steroid ini akan aktif dan bekerja pada organ
target.29
Gambaran yang mencolok dari mioma uteri adalah
ketergantungan mereka pada hormon steroid ovarium, estrogen dan
progesteron. Aktivitas ovarium penting untuk pertumbuhan mioma, dan
kebanyakan mioma menyusut setelah menopause. Peningkatan dan
penurunan yang tajam pada produksi estrogen dan progesteron yang
berhubungan dengan kehamilan yang sangat dini dan periode paska
melahirkan mempunyai pengaruh yang dramatis pada pertumbuhan
mioma. GnRH analog, yang menekan aktivitas ovarium dan mengurangi
kadar estrogen dan progesteron yang bersirkulasi, menyusutkan mioma
dan mengurangi perdarahan dari uterus.10
Umumnya reseptor-reseptor hormon steroid mempengaruhi
transkripsi gen. Reseptor steroid meregulasi transkripsi gen melalui
beberapa mekanisme, tidak semuanya membutuhkan interaksi langsung
dengan DNA. Peran estrogen yang penting adalah memodifikasi aktifitas
hormonnya sendiri dan yang lainnya dengan mempengaruhi konsentrasi
reseptor. Estrogen meningkatkan respon jaringan target untuknya sendiri
dan terhadap progesteron serta androgen dengan meningkatkan
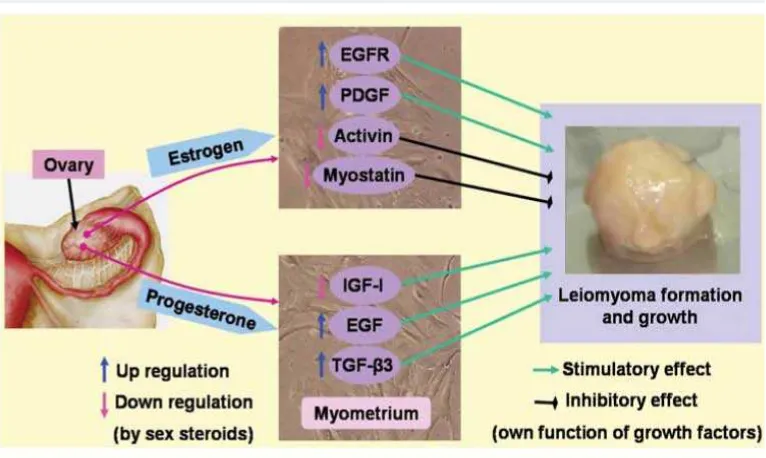
Estrogen dapat meningkatkan pertumbuhan mioma uteri memalui
up-regulation dari ekspresi EGFR dan PDGF dan dengan down-regulating
ekspresi aktivin dan miostatin. Demikian juga dengan progesteron dapat
mempengaruhi pertumbuhan mioma uteri dengan up-regulating ekspresi
EGF dan TGF-β3. Sebaliknya, progesteron juga dapat menghambat
pertumbuhan mioma dengan down-regulating ekspresi IGF-I. Peranan
sebenarnya dari steroid seks, bagaimana mereka berinteraksi dengan
faktor pertumbuhan dan bagaimana mereka mempengaruhi atau
mengatur pertumbuhan mioma belum dapat dimengerti. Namun, dengan
menggunakan konsep kemampuan seks steroid mempengaruhi
pertumbuhan, beberapa antagonis progesteron / anti progestin, SPRMs
(selective progesterone receptor modulators) dan SERMs (selective
estrogen receptor modulators) telah diajukan mempunyai potensi
terapeutik untuk penanganan mioma.11
Beberapa bukti klinis dan biokimiawi menunjukkan peranan
progesteron dalam patogenesis mioma uteri. Telah ditunjukkan bahwa
progesteron dapat merangsang aktivitas mitosis dan proliferasi mioma.
Kawaguchi dkk (1989) menemukan peningkatan aktivitas mitosis pada
mioma pada fase sekresi siklus menstruasi yang menunjukkan bahwa
pertumbuhan mioma dipengaruhi oleh kadar progesteron. Tiltman (1985)
melaporkan bahwa pemberian medroksiprogesteron asetat meningkatkan
aktivitas mitosis mioma secara bermakna dibandingkan dengan kelompok
yang tidak diobati. Pengobatan dengan antagonis progesteron RU-486
(mifepriston) telah dilaporkan untuk merangsang regresi mioma dengan
mengurangi immunoreaktivitas RP, yang menunjukkan pengaruh
langsung anti progesteron. Sebaliknya, progestin dapat menghambat
pengecilan mioma yang diinduksi GnRH agonis. Brandon dkk (1993)
menunjukkan peningkatan mRNA RP dan kadar protein pada mioma
bersamaan dengan peningkatan proliferasi yang berhubungan dengan
antigen Ki-67 dibandingkan terhadap miometrium normal, yang
menunjukkan hubungan dari sinyal yang diperantarai progesteron dengan
pertumbuhan mioma. Hasil ini mendukung pandangan bahwa progesteron
memegang peranan penting dalam pertumbuhan mioma uteri.30
Pada jaringan perifer (kulit dan jaringan lemak) dan ovarium,
aromatase mengkatalisasi pembentukan estrogen, yang mencapai
jaringan mioma melalui sirkulasi. Selain itu, aromatase pada jaringan
mioma mengubah androstenedion yang berasal dari adrenal atau ovarium
estradiol, menginduksi produksi dari RP dengan cara berikatan dengan
RE-α. RP penting sebagai respon dari jaringan mioma terhadap
progesteron yang disekresikan oleh ovarium. Progesteron dan RP sangat
diperlukan terhadap pertumbuhan tumor, meningkatkan proliferasi sel dan
survival dan meningkatkan pembentukan matriks ekstraselular. Pada
ketiadaan progesteron dan RP, estrogen dan RE-α tidak mencukupi untuk
pertumbuhan mioma. Pewarnaan imunuhistokimia pada jaringan mioma
menunjukkan lokalisasi nukleus dari RE-α atau RP pada sel-sel otot polos.
Faktanya bahwa aromatase inhibitor atau antiprogestin yang dapat
mengecilkan ukuran tumor menunjukkan dukungan dari mekanisme ini
dari pertumbuhan mioma (gambar 4).2
2.4 Reseptor Estrogen
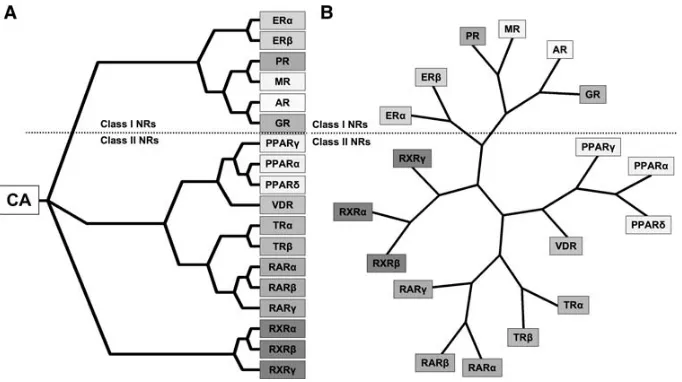
Reseptor estrogen (RE) merupakan anggota dari super famili
reseptor nukleus, dimana kebanyakan berasal dari sumber yang sama
(gambar 5). Super famili ini terdiri dari 18 anggota reseptor, yang dibagi
menjadi reseptor nukleus kelas I dan kelas II. Reseptor nukleus kelas I
termasuk reseptor hormon steroid : reseptor estrogen a dan b (RE a/b),
reseptor progesteron A dan B (RP A/B) reseptor glukokortikoid (RG),
Gambar 4. Efek biologis dari estrogen dan progesteron pada jaringan mioma (dikutip dari 2)
Yang termasuk reseptor nukleus kelas II, reseptor asam retinoat
(RAR a/b/c), reseptor retinoid X (RRX a/b/c), reseptor vitamin D (RVD),
reseptor peroxisome proliferator activated receptor (PPAR a/c/d) dan reseptor thyroid (RT a/b). Semua reseptor dari super famili reseptor
nukleus menghambat faktor transkripsi, dimana menjadi aktif saat
Gambar 5. Super famili reseptor nukleus (dikutip dari 31)
17β - estradiol (estrogen) merupakan ikatan ligan utama pada
RE-α/β. Estrogen disekresikan kedalam pembuluh darah oleh korteks
kelenjar adrenal dan gonad serta memegang peranan yang menonjol
dalam memperantarai perkembangan seksual, fungsi reproduksi,
proliferasi dan difrensiasi dari berbagai jaringan melalui RE. Sebagai
contoh, interaksi Estrogen/RE-α bertanggung jawab untuk proliferasi
payudara dan jaringan uterus yang dirangsang estrogen. RE-α pertama
sekali diisolasi pada tahun 1962, dan gen yang berhubungan di klon pada
tahun yang sama dan berlokasi pada lengan panjang dari kromosom 6
(6q24-q27; sekarang 6q25.1). Tiga dekade kemudian pada tahun 1993,
RE-α pertama tikus percobaan diciptakan dan menemukan bahwa
perkembangan mungkin tanpa RE-α. Pada waktu itu, hanya RE-α yang
difikirkan menjadi reseptor yang memperantarai respon pada estrogen, tetapi pada tahun 1996 telah di klon REβ dan berlokasi pada kromosom
Estrogen berikatan dengan afinitas yang tinggi pada RE, sementara
hasil metabolik estrogen seperti estron dan estriol, berikatan dengan
afinitas yang lebih rendah. Aksi estrogenik dapat dipengaruhi secara
farmakologi oleh anti estrogen dan SERMs. SERMs yang pertama sekali
di coba adalah tamoxifen pada tahun 1970 dan sampai sekarang
tamoxifen menunjukkan pengaruh pada terapi ajuvan dari kanker
payudara dengan RE (+) pada wanita premenopause.31
Uterus merupakan jaringan target yang sensitif terhadap estrogen
memiliki kedua reseptor dalam jumlah yang banyak. Namun reseptor ini
juga ditemukan di jaringan yang lain, contoh RE-α banyak dijumpai juga
pada ginjal, hati dan jantung. RE-β juga dijumpai pada jaringan otak, paru,
saluran pencernaan dan folikel ovarium.22,26
Pada seluruh sel endometrium dan miometrium, ekspresi RE
mencapai maksimum pada fase folikuler akhir. Selama fase luteal awal,
ekspresi RE menurun, diikuti dengan peningkatan pada pertengahan dan
akhir fase luteal. Perubahan ini menggambarkan perubahan siklus
estradiol. Walaupun RE-β dijumpai pada endometrium manusia, namun
kurang menonjol dibandingkan RE-α dan memperlihatkan perubahan yang
minimal selama siklus menstruasi.22
Lingkungan dalam mioma uteri bersifat hiperestrogenik dan
hipersensitif terhadap estrogen. Mioma uteri menciptakan lingkungan
hiperestrogeniknya sendiri, yang diperlukan untuk pertumbuhan dan
pemeliharaan mereka (mioma uteri). Mioma uteri memiliki RE dan RP
normal)18,25,26,27 sehingga mioma uteri mengikat estrogen lebih banyak
dan mioma uteri juga sangat sedikit merubah estradiol menjadi estron
lemah. Tidak dijumpai perbedaan RE yang signifikan berdasarkan ukuran
massa mioma uteri.32
Selain itu, teori mengenai kadar aromatase sitokrom 450 yang
lebih tinggi pada mioma dibandingkan dengan miosit normal. Aromatase
sitokrom 450 merupakan kelompok enzim yang terlibat dalam biosintesis
hormon steroid juga aktivasi metabolik karsinogen. Isoform sitokrom yang
spesifik ini mengkatalisasi konversi androgen menjadi estrogen pada
beberapa jaringan. Diduga sel-sel mioma uteri mensintesis estrogen
in-situ.18 Estrogen dapat menyebabkan pembesaran tumor dengan
meningkatkan produksi matriks ekstraseluler. 22,25
Bukti akumulatif mendukung konsep bahwa estrogen sangat
berhubungan dengan tumorigenesis dan pertumbuhan mioma. Estrogen
menggunakan efek fisiologinya pada sel-sel target dengan berikatan pada
reseptor nukleus spesifik yaitu RE-α dan RE-β. RE-β dapat dianggap
homolog dengan RE-α pada daerah ikatan DNA dan daerah ligand-binding. Beberapa studi telah menunjukkan bahwa baik mRNA RE-α dan
RR-β diekspresikan pada miometrium dan mioma. Sakaguchi dkk (2003)
melaporkan bahwa kadar mRNA RE-α dan RE-β pada miometrium
berubah selama siklus menstruasi, tetapi kadar mRNA RE-α lebih
menonjol daripada mRNA RE-β. Dua orang penulis telah melaporkan
bahwa kadar mRNA RE-α dan RE-β meningkat pada mioma dibandingkan
menstimulasi transkripsi dari gen target, walaupun aktivasi dari RE-β lebih
rendah daripada RE-α.30
2.5 Reseptor Progesteron
Reseptor progesteron (RP) terdapat dalam 2 bentuk yang berbeda
yang disebut dengan RP-A dan RP-B. Fungsi reseptor ini sebagai faktor
transkiripsi yang diaktivasi-ligan, tetapi isoform kedua reseptor
menunjukkan fungsi biologi yang berbeda. RP-B berfungsi sebagai
aktivator transkripsional dari gen yang responsif progesteron, sedangkan
RP-A bertindak sebagai repressor ligan dependen yang poten dari
aktivitas transkripsional B dalam promoter dan konteks sel dimana
RP-A tidak aktif sebagai aktivator transkripsional. Terdapat hubungan yang
kompleks antara jalur sinyal RE dan RP sebagaimana yang ditunjukkan
dengan observasi bahwa estrogen dapat menginduksi ekspresi RP pada
sel-sel miometrium pada monyet, dan mentransformasi miosit hamster,
serta meningkatkan transkripsi dari gen RP-B pada sel-sel kanker
payudara wanita, sementara isoform kedua RP dapat bertindak sebagai
represor ligan dependen yang poten dari aktivitas RE. kemudian,
progesteron men down-regulate transkripsi RP yang distimulasi
estrogen.30
RP-A dan RP-B telah diidentifikasi pada jaringan mioma dan
miometrium normal. Dua peneliti telah menunjukkan bahwa kandungan
RP-A dan RP-B lebih tinggi pada jaringan mioma daripada miometrium
normal dengan kandungan RP-A yang lebih dominan secara bermakna
antara konsentrasi mRNA yang mengkode RP-A dan RP-B pada mioma
dan miometrium normal, yang menunjukkan kontrol post translasi. Selain itu, GnRH agosis men down-regulate ekspresi imunoreaktif RP, RP-A dan
RP-B, dan kadar mRNA RP di jaringan mioma. Menariknya, Fujimoto dkk
(1998) menemukan over ekspresi relatif dari mRNA RP-B pada
permukaan mioma, yang menunjukkan bahwa ekspresi yang dominan dari
RP-B pada bagian ini menunjukkan fenotip yang diaktivasi untuk
proliferasi progestasional yang berhubungan dengan pertumbuhan
mioma. Namun, masih belum diketahui apakah tingginya RP-A
berhubungan dengan berkurangnya responsiveness progesteron terhadap
sel-sel mioma.30
2.6 Peranan faktor pertumbuhan pada mioma uteri
Pada uterus normal, pengaruh estrogen dan progestin pada mioma
diperantarai oleh faktor pertumbuhan. EGF diekspresikan berlebih pada
mioma, reseptor EGF terdapat pada mioma dan pengobatan dengan
GnRH agonis (dan hipogonadisme) menurunkan konsentrasi EGF pada
mioma (tetapi tidak pada miometrium normal). IGF-I dan IGF-II dan
reseptornya berlebihan pada miometrium dan secara aktif dieskpresikan
berlebih pada mioma. Mioma mengekspresikan lebih banyak IGF-II dan
sedikit IGFBP-3 daripada miometrium, suatu situasi yang akan
meningkatkan availabilitas dan aktivitas faktor pertumbuhan pada tumor.
Sel-sel mioma menseksresikan lebih banyak protein yang berhubungan
dengan hormon paratiroid (faktor pertumbuhan lainnya) daripada
mensekresikan prolaktin, dan prolaktin berfungsi pada uterus sebagai
faktor pertumbuhan.22
Salah satu konsekuensi dari perubahan ekspresi faktor
pertumbuhan pada mioma adalah abnormalitas vaskulatur, yang ditandai
dengan pleksus vena yang berdilatasi. Gambaran morfologi ini mungkin
hasil dari regulator vaskular spesifik dari angiogenesis, seperti faktor
pertumbuhan fibroblast dan vascular endothelial growth factor. Perubahan
ini mungkin berkontribusi terhadap perdarahan menstrual yang berat yang
berhubungan dengan mioma submukosa.22
2.7. Imunohistokimia reseptor estrogen dan reseptor progesteron
Imunohistokimia / Immunohistochemistry (IHC) adalah sebuah metoda pemeriksaan dengan menggunakan prinsip antibodi dengan
spesifikasi yang tinggi untuk menunjukkan lokasi dan keberadaan sebuah
protein dalam jaringan, yang biasanya dilakukan untuk penelitian, dan
tujuan diagnostik atau prognostik.33
Prinsip IHC meliputi langkah : 33
a. Deparafinisasi dan rehidrasi
b. Aktivasi antigen
c. Penghambatan peroksidase endogen
d. Inkubasi antibodi primer
e. Inkubasi antibodi skunder
f. Deteksi antibodi
g. Counter staining
i. Interpretasi slide.
Penilaian IHC diinterpretasikan berdasarkan gabungan antara
kualitas intensitas ikatan antigen dengan antibodi yang terbentuk di
sitoplasma atau inti sel dengan persentase sel yang terwarnai dalam
lapang pandang. Diantara metode penilaian IHC tersebut adalah : 34
1. H score, merupakan penjumlahan dari persentase sel yang terwarnai lemah, persentase sel yang terwarnai sedang dikalikan
dengan dua, dan persentase sel yang terwarnai kuat dikalikan
dengan tiga. Penilaian ini memberikan skor dari 0 – 300.34,35
2. Allred score, merupakan penjumlahan dari skor persentase sel
yang terwarnai (0 = tidak terwarnai, 1 = terwarnai < 1%, 2 = 1-10%,
3 = 10-33%, 4 = 33-67%, 5 = 67-100%) dan skor dari intensitas sel
yang terwarnai (0 = tidak terwarnai, 1 = terwarnai lemah, 2 =
terwarnai sedang, 3 = terwarnai kuat). Penilaian ini memberikan
skor dari 0 – 8.36,37
3. Intensitas warna pada sel, merupakan derajat intesitas sel yang
terwarnai, dengan nilai : negatif (-) jika tidak ada sel yang terwarnai,
(+) jika sel terwarnai lemah, (++) jika sel terwarnai sedang, dan
(+++) jika sel terwarnai kuat.38
Tabel 2.1. Faktor pertumbuhan dan protein yang berhubungan pada miometrium dan
2.8 Hipotesis Penelitian
Hipotesis pada penelitian ini adalah :
1. Ekspresi RE pada mioma lebih tinggi daripada miometrium normal.
2.9 Kerangka Teori
Miosit Normal
Mutasi somatik Inisiator tumor
(faktor genetik ?)
Mioma
Miosit yangbermutasi
Ekspansi Klonal
Induksi reseptor estrogen Induksi reseptor progesteron
Produksi faktor pertumbuhan
Induksi reseptor faktor pertumbuhan Produksi matriks esktraselular Mitogenesis
Estrogen
Progesteron Usia
2.10 Kerangka Konsep
Variabel tergantung
Variabel bebas
Variabel perancu (tidak diteliti) Ekspresi reseptor estrogen dan
reseptor progesteron pada miometrium
Miometrium
normal
Mioma uteri
BAB III
METODE PENELITIAN
3.1 Rancangan Penelitian
Penelitian ini merupakan penelitian analitik dengan pendekatan
case control dengan pemeriksaan imunohistokimia terhadap blok parafin
jaringan mioma penderita mioma uteri dan blok parafin miometrium
normal.
3.2 Tempat dan waktu Penelitian
Penelitian dilakukan di Departemen Obstetri dan Ginekologi.
Pemeriksaan imunohistokimia dilakukan di departemen Patologi Anatomi
RSUP H. Adam Malik Medan yang dilakukan pada bulan Juli 2014
sampai jumlah sampel terpenuhi.
3.3 Subjek Penelitian
Subyek penelitian kelompok kasus adalah blok parafin jaringan
mioma penderita mioma uteri yang diperoleh melalui miomektomi atau
histerektomi yang dibuktikan secara histopatologi. Sedangkan subjek
penelitian kelompok kontrol adalah blok parafin jaringan miometrium
normal yang dibuktikan dengan pemeriksaan histopatologi.
3.4 Sampel dan besar sampel 3.4.1 Sampel
Sampel penelitian adalah subjek penelitian yang diambil secara
3.4.2 Besar Sampel
Zα = nilai baku normal dari tabel Z yang besarnya bergantung pada nilai α yang ditentukan. Nilai α = 0,05 Zα=1.96
Zβ= nilai baku normal dari tabel Z yang besarnya bergantung pada nilai β
yang ditentukan. Nilai β = 0,20 Zβ=0.84
P1 = proporsi ekspresi RE dan RP (+) pada mioma = 0.83 38
P1 - P2 = perbedaan proporsi ekspresi RE dan RP pada mioma uteri dan
miometrium yang dianggap bermakna = 0.25
P2 = proporsi ekspresi RE dan RP (+) pada miometrium = 0.83 – 0.25 =
Bsar sampel untuk RE dan RP adalah sama yaitu 29.9, maka jumlah
sampel minimal untuk penelitian ini adalah 30 blok parafin untuk
3.5 Kriteria Penelitian 3.5.1 Kriteria Eksklusi
Kriteria eksklusi pada penelitian ini adalah :
− Sediaan yang tidak dapat dianalisa oleh sebab proses pembuatan
parafin blok yang tidak baik.
− Data dari rekam medis yang tidak lengkap.
3.6 Cara kerja dan teknik pengumpulan data
− Setelah mendapat persetujuan dari komisi etik untuk melakukan
penelitian, penelitian dimulai dengan mengumpulkan data pasien yang
didiagnosis dengan mioma uteri (kelompok kasus) yang telah menjalani
operasi miomektomi atau histerektomi, dan data pasien paska
histerektomi dengan miometrium normal yang jaringannya telah
dilakukan pemeriksaan histopatologi.
− Dilakukan pengumpulan blok parafin di Departemen Patologi Anatomi
RSUP H. Adam Malik Medan dan dicari data rekam medis pasien
tersebut.
− Pasien diseleksi berdasarkan kriteria inklusi dan eksklusi
− Pada blok parafin dilakukan pemeriksaan imunohistokimia untuk
menentukan ekspresi RE dan RP. Pemeriksaan imunohistokimia adalah
pemeriksaan jaringan yang telah dilabel dengan antibodi spesifik untuk
melihat ekspresi protein antigen spesifik dengan mikroskop.
− Pembacaan hasil pemeriksaan imunohistokimia dilakukan oleh dua
orang pengamat yaitu dua orang spesialis Patologi Anatomi.
3.7 Prosedur Pemeriksaan Imunohistokimia 3.7.1 Alat Penelitian
Alat-alat yang diperlukan untuk penelitian ini adalah: mikrotom,
waterbath, hot plate, freezer, incubator, staining jar, rak object glass, pipet mikro, kertas saring, tabung sentrifuge 15ml, coated object glass, kaca
penutup, entelan dan mikroskop cahaya, Bondmaxfull automatic.
3.7.2 Bahan Penelitian
− Blok parafin yang telah didiagnosa dengan pulasan Hematoksilin Eosin
− Pulasan imunohistokimia menggunakan alat Bondmax full automatic.
Antibodi primer yang digunakan adalah estrogen receptor dan
progesterone receptor(Leica), dengan pengenceran 1: 100.
3.7.3 Cara kerja
− Blok parafin yang telah dikumpulkan, disimpan dalam freezer sampai
cukup dingin, selanjutnya dipotong tipis dengan menggunakan mikrotom
dengan tebal 4µm dan ditempelkan pada coated object glass.
− Preparat yang siap dipulas dimasukkan dalam alat Bondmax full
automatic selama 4 jam.
− Setelah itu, dilakukan dehidrasi dengan cara : dicelupkan secara
berurutan pada cairan alcohol 70%, 80%, 90% dan etanol 98%
masing-masing 20 celup
− Masukkan dalam cairan xylol selama 3 menit
3.7.4 Instrumen Penilaian
Untuk penilaian, instrumen yang digunakan adalah hasil pulasan
imunohistokimia terhadap antibodi RE dan RP sebagai berikut:
• Kontrol positif : karsinoma mamae yang telah diketahui positif terhadap
RE dan RP
• Kontrol negatif : tonsil dengan antibodi primer yang digantikan dengan
serum normal
Penilaian imunihistokimia untuk RE dan RP menggunakan skor
Allred, karena sistem penilaian ini telah biasa dilakukan di Departemen
Patologi Anatomi RSUP H. Adam Malik Medan. Skor ini adalah hasil
penjumlahan skor persentase dari sel yang terwarnai/proportion score
(PS) dan skor intensitas pewarnaannya / intensity score (IS).37
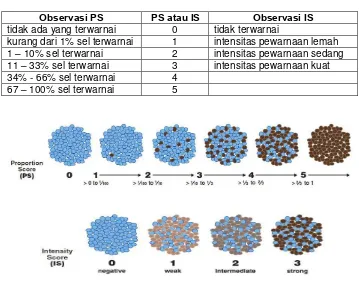
Tabel 3.1 Penilaian proportion score (PS) dan intensity score (IS) 37
Observasi PS PS atau IS Observasi IS
tidak ada yang terwarnai 0 tidak terwarnai
kurang dari 1% sel terwarnai 1 intensitas pewarnaan lemah
1 – 10% sel terwarnai 2 intensitas pewarnaan sedang
11 – 33% sel terwarnai 3 intensitas pewarnaan kuat
34% - 66% sel terwarnai 4
67 – 100% sel terwarnai 5
Skor total / total score (TS) adalah penjumlahan dari proportion score (PS) + intensity score (IS).37
Tabel 3.2 skor total imunohistokimia RE dan RP 37
Skor total Interpretasi
0 – 2 Negatif
≥3 Positif
3.8 Defenisi Operasional
Variabel Defenisi Alat ukur Skala ukur Kategori
Mioma uteri tumor jinak uterus
yang berasal dari
Miometrium Jaringan sel-sel
otot polos uterus
Paritas Jumlah kelahiran
yang pernah multipara : 2-3 kali melahirkan, grande multipara :
≥ 4 kali melahirkan
Indeks massa tubuh
Perhitungan lemak tubuh manusia berat badan dalam kilogram dibagi dengan kuadrat tinggi badan dalam meter (kg/m2)
Timbangan badan dan pengukur tinggi badan
Underweight : (< 18.5)
Normoweight : (18.5-24.9)
Overweight : (25-29.9)
Obese : (> 30)
Skala ordinal
3.9 Analisis Data
Hasil penelitian disajikan kedalam tabel distribusi frekuensi. Data
akan dianalisa secara deskriptif untuk melihat distribusi frekuensi dari
karakteristik sampel. Untuk menganalisa akurasi pembacaan RE dan RP,
nilai kappa dari dua observer akan dihitung dan dinyatakan valid bilai nilai > 75%. Uji T tidak berpasangan akan dilakukan untuk melihat perbedaan
ekspresi kedua reseptor, sedangkan Anova untuk melihat perbedaan
3.10 Alur Penelitian
Pemeriksaan imunohistokimia untuk melihat ekspresi RE dan RP
Pengolahan data dan uji hipotesis
Pengumpulan hasil histopatologi dan data rekam medis pasien yang menjalani operasi miomektomi atau histerektomi
Kriteria inklusi dan ekslusi
Blok parafin miometriumnormal
BAB IV
HASIL DAN PEMBAHASAN
Penelitian ini dilakukan dengan memeriksa blok parafin jaringan
mioma uteri dan jaringan miometrium normal berdasarkan hasil
pemeriksaan histopatologi di Departemen Patologi Anatomi RSUP. H.
Adam Malik Medan, dengan memilih secara acak sederhana dari blok
parafin yang tersedia dari tahun 2011 sampai tahun 2014, sehingga
diperoleh 30 blok parafin yang memenuhi kriteria penelitian pada
masing-masing kelompok.
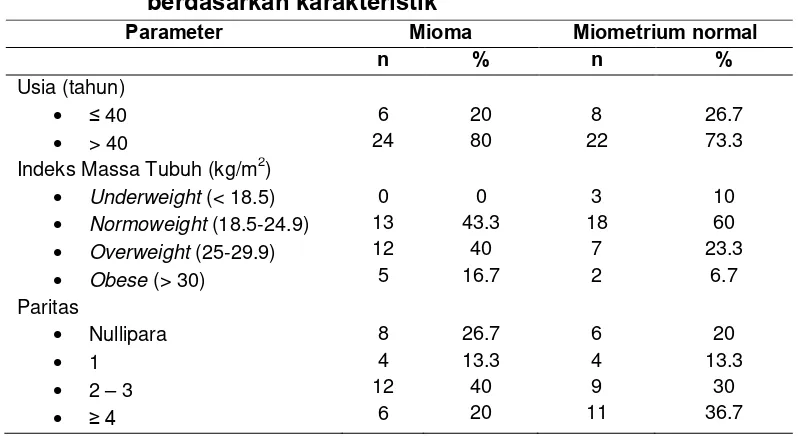
Tabel 4.1 Distribusi frekuensi mioma dan miometrium normal berdasarkan karakteristik
Parameter Mioma Miometrium normal n % n %
• Normoweight (18.5-24.9)
• Overweight (25-29.9)
• Obese (> 30)
Berdasarkan karakteristik usia seperti yang terlihat pada tabel 4.1,
pada kelompok kasus (mioma uteri) dan kelompok kontrol (non mioma),
yang terbanyak adalah kelompok usia > 40 tahun. Pada kelompok mioma
80% penderitanya berusia > 40 tahun, dengan rerata usia 44.8 ± 6.68