MIKROENKAPSULASI MINYAK IKAN
KAYA ASAM LEMAK OMEGA-3 SEBAGAI BAHAN
FORTIFIKASI PADA SUP KRIM KEPITING INSTAN
SANTIARA PUTRI PRAMESTIA
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul “Mikroenkapsulasi Minyak Kaya Asam Lemak Omega-3 sebagai Bahan Fortifikasi pada Sup Krim Kepiting Instan” adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan dan tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2015
Santiara Putri Pramestia
ABSTRAK
SANTIARA PUTRI PRAMESTIA. Mikroenkapsulasi Minyak Ikan Kaya Asam Lemak Omega-3 sebagai Bahan Fortifikasi pada Sup Krim Kepiting Instan. Dibimbing oleh BAMBANG RIYANTO dan WINI TRILAKSANI.
Asam lemak omega-3 memiliki peranan penting dalam meningkatkan kecerdasan dan kesehatan manusia, namun mudah teroksidasi dan berpotensi menghasilkan aroma rancid. Mikroenkapsulasi minyak ikan lemuru yang kaya akan asam lemak omega-3 merupakan suatu upaya untuk mempertahankan rasa, aroma, stabilitas, dan juga untuk mentransfer komponen bioaktif dari minyak ikan untuk tujuan fortifikasi pada makanan atau obat-obatan. Penelitian ini bertujuan untuk pengembangan metode mikroenkapsulasi minyak ikan kaya asam lemak omega-3 dan aplikasinya sebagai bahan fortifikasi pada sup krim kepiting instan. Mikrokapsul terbaik diperoleh dari perlakuan homogenisasi selama 10 menit, dengan efisiensi 90,41±0,64%, berbentuk bulat dengan ukuran rata-rata 6,52 µm, dan waktu induksi mencapai 26,09±0,01 jam. Sup krim kepiting instan terbaik diperoleh dari formula yang diperkaya mikrokapsul minyak ikan 3,30%, menghasilkan %AKG omega-3 8,19% termasuk %AKG EPA dan DHA 11,32% pada takaran saji 17,56 g.
Kata kunci: Asam lemak omega-3, fortifikasi, kepiting, mikroenkapsulasi, minyak ikan, sup krim instan.
ABSTRACT
SANTIARA PUTRI PRAMESTIA. Fish Oil Microencapsulation as Omega-3 Fatty Acids Fortification Material for Cream of Crab Soup. Supervised by BAMBANG RIYANTO and WINI TRILAKSANI.
Omega-3 fatty acids have important roles in improvement of human intelligent and health, but are susceptible to oxidation which potentially produce rancid aroma. Microencapsulation of Sardinella sp. fish oil which is rich in omega-3 fatty acids is an effort to maintain flavor, aroma, stability, and also to transfer bioactive component of the fish oil as fortification material for foods or medicines. The purpose of this research was to improve microencapsulation method for fish oil as source of omega-3 fatty acids and its application as fortification material for instant cream of crab soup. The best microcapsule was obtained from 10 minutes homogenization treatment with efficiency of 90.41±0.64%, the shape was spherical with average size 6.52 µm, and 26.09±0.01 hours of induction time. The best cream of crab soup formula was found at 3.30% fish oil microcapsule concentration, resulted 8.19% nutritional adequacy rate for omega-3 with 11.32% of EPA and DHA at 17.56 g serving size.
© Hak Cipta Milik IPB, tahun 2015
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
MIKROENKAPSULASI MINYAK IKAN KAYA ASAM
LEMAK OMEGA-3 SEBAGAI BAHAN FORTIFIKASI PADA
SUP KRIM KEPITING INSTAN
SANTIARA PUTRI PRAMESTIA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Teknologi Hasil Perairan
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Mikroenkapsulasi Minyak Ikan Asam Lemak Omega-3 sebagai Bahan Fortifikasi pada Sup Krim Kepiting Instan
Nama : Santiara Putri Pramestia
NIM : C34100003
Program Studi : Teknologi Hasil Perairan
Disetujui oleh
Bambang Riyanto SPi, MSi Dr Ir Wini Trilaksani, MSc Pembimbing I Pembimbing II
Diketahui oleh
Prof Dr Ir Joko Santoso, MSi Ketua Departemen
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Allah SWT atas limpahan rahmat dan berkat-Nya sehingga skripsi yang berjudul “Mikroenkapsulasi Minyak Ikan Kaya Asam Lemak Omega-3 sebagai Bahan Fortifikasi pada Sup Krim Kepiting Instan” ini dapat diselesaikan dengan baik. Skripsi disusun sebagai salah satu syarat penyelesaian studi di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
1 Bambang Riyanto, SPi, MSi dan Dr Ir Wini Trilaksani MSc selaku dosen pembimbing, yang telah memberikan banyak arahan dan masukan selama penyelesaian tugas akhir.
2 Dr Sugeng Heri Suseno, SPi, MSi selaku dosen penguji yang telah memberikan banyak informasi dan arahan dalam penulisan skripsi.
3 Dr Ir Iriani Setyaningsih, MS selaku Ketua Program Studi Teknologi Hasil Perairan.
4 Prof Dr Ir Joko Santoso, MSi selaku Ketua Departemen Teknologi Hasil Perairan.
5 PT. Indofood Sukses Makmur Tbk. yang telah mendanai penelitian ini dalam program Indofood Riset Nugraha 2014/2015.
6 PT. Globalindo Teknik Mandiri, Bogor atas bantuan penyediaan bentonit. 7 Keluarga penulis terutama mama (Nurjanah, SPd), bapak (Nasai, SE), kakak
(Rafli Reynaldi), dan adik (Regi Agustian).
8 Sahabat dan rekan Maya Sofia, Sonya Ayu Utari, Rahmawati, Asih Rahayu, Reza Febriyansyah, Ajeng Novvita Sary, Hardiana Rusmiati, Ukhti Sholihah, Aufa Khairunnisa, Himawan Prasetiyo, Bayu Irianto, Maydariana Ayuningtyas, Sheilla Amanda, I Wayan Kukuh Feryana, Nur Hidayah, I Wayan Darya Kartika, Dewi Ulfa Trisdiani, Pipih Mahmudah, Nia Kurniati, Fanji Sanjaya dan Zaky Abdullatif
9 Rizky Marcheria Ardiyanti, Eka Pujiyanti, Dian Eka Ramadhani, Lidya Agustina Budiarti, dan Nurul Izmah yang telah membantu penulis dalam dukungan moril.
Kritik dan saran yang membangun sangat diharapkan untuk perbaikan di masa depan. Demikian skripsi ini disusun, semoga bermanfaat.
Bogor, Agustus 2015
DAFTAR ISI
Mikroenkapsulasi dan karakterisasi minyak ikan... 5
Formulasi sup krim kepiting instan dengan metode Bayes ... 6
Fortifikasi mikrokapsul minyak ikan dan karakterisasi terhadap sup krim kepiting instan ... 7
Penentuan formula terbaik sup krim kepiting instan dan perhitungan kandungan gizi ... 7
Formula Terbaik Sup Krim Kepiting Instan dengan Fortifikasi Mikrokapsul Minyak Ikan Kaya Omega-3 ... 26
Angka kecukupan gizi sup krim instan terbaik ... 27
KESIMPULAN DAN SARAN ... 27
DAFTAR PUSTAKA ... 28
DAFTAR TABEL
1 Formula sup krim kepiting instan ... 6 2 Kualitas minyak ikan sebelum dan setelah pemurnian ... 14 3 Hasil analisis formula terpilih dengan metode Bayes ... 20 4 Karakteristik fisik sup krim kepiting instan dengan fortifikasi mikrokapsul
minyak ikan dan kontrol ... 23 5 Karakteristik kimia sup krim kepiting instan dengan fortifikasi
mikrokapsul minyak ikan dan kontrol ... 25 6 Hasil perankingan formula terbaik dengan metode Bayes ... 26 7 Informasi nilai gizi sup krim kepiting instan formula terbaik ... 27
DAFTAR GAMBAR
1 Diagram alir keterkaitan antar tahapan penelitian... 4 2 Reaksi oksidasi primer dan sekunder (Hamilton dan Rossell 1986)... 15 3 Perubahan ukuran globula mikroenkapsulat minyak ikan dengan
homogenisasi (a) 2 menit dan (b) 10 menit ... 16 4 Kenampakan globula mikroenkapsulat minyak ikan dengan mikroskop
polarisasi cahaya perbesaran 10×10, (a) t = 2 menit; (b) t =10 menit ... 17 5 Struktur globula mikroenkapsulat minyak ikan (Shahidi dan Han 1993)... 17 6 Struktur mikrokapsul minyak ikan dengan Scanning Electron Microscope
(a) perbesaran 10 000×, (b) perbesaran 5000× ... 18 7 Karakteristik sensori sup krim kepititng instan dengan fortifikasi
mikrokapsul minyak ikan kaya omega-3. (a) Tingkat kesukaan; (b) Karakteristik. Kontrol mikrokapsul 3,00%; mikrokapsul 3,30% mikrokapsul 3,60%. Angka- angka dengan huruf superskrip berbeda (a,b) menunjukkan berbeda nyata (p<0,05)... 21
DAFTAR LAMPIRAN
1 Hasil uji keragaan asam lemak minyak ikan, mikrokapsul minyak ikan, dan daging kepiting ... 39 2 Kromatogram keragaan asam lemak ... 40
3 Kuesioner penilaian kesukaan konsumen terhadap produk sup krim instan dan cara perhitungan metode Bayes ... 42 4 Lembar penilaian uji sensori sup krim kepiting instan dengan perlakuan
penambahan air... 44 5 Karakteristik sensori uji hedonik, uji Kruskal Wallis, dan uji sup krim
6 Penilaian metode Bayes terhadap parameter sensori sup krim kepiting instan
dengan perlakuan penambahan air... 48
7 Lembar penilaian uji sensori sup krim kepiting instan dengan fortifikasi mikrokapsul minyak ikan kaya omega-3 ... ... 50
8 Karakteristik sensori uji skoring dan uji Kruskal Wallis sup krim kepiting instan dengan fortifikasi mikrokapsul minyak ikan ... ... 52
9 Uji Kruskal Wallis dan uji lanjut Dunn parameter sensori sup krim kepiting instan dengan fortifikasi mikrokapsul minyak ikan kaya omega-3... 53
10 Uji kenormalan Kolmogorov-Smirnov, analisis ragam dan uji lanjut Duncan karakteristik fisik sup krim instan ... 56
11 Uji kenormalan Kolmogorov-Smirnov, analisis ragam dan uji lanjut Duncan karakteristik kimia sup krim instan ... 58
12 Perhitungan kandungan omega-3, EPA dan DHA... 63
13 Perhitungan Angka Kecukupan Gizi (AKG) ... 65
PENDAHULUAN
Latar Belakang
Asam lemak omega-3 berperan penting untuk pencegahan penyakit pada manusia sejak tahun 1929. Peran ini kembali populer pada awal tahun 1970 dalam kaitan dengan rendahnya pola plasma lipid dan lipoprotein terhadap penyakit kardiovaskular penduduk Eskimo pantai barat Greenland yang dominan mengkonsumsi ikan laut. Perannya dalam perkembangan otak manusia telah diketahui pada periode tahun yang sama, namun sebagai unsur utama peningkatan fungsi kecerdasan pada membran sel cerebral cortex, sejak janin dan masa pertumbuhan anak-anak, baru dilaporkan pada tahun 1990 (Hibbeln et al. 2007, Forchielli dan Walker 2012). Peran penting lain dari asam lemak omega-3 terutama DHA telah dilaporkan pula dalam pencegahan dan peningkatan daya ingat bagi penderita Alzheimer (Conquer et al. 2000), pengembangan psikologis klinis dan penyembuhan berbagai penyakit mental (American Psychiatric Association 1994), antara lain depresi (Hibbeln 1998), schizophrenia, deficit hyperactivity disorder, dan demensia (Freeman et al. 2006; Amminger et al. 2010).
Minyak ikan merupakan sumber asam lemak kaya omega-3 (Shamsudin dan Salimon 2006). Dewi (1996) melaporkan bahwa kandungan asam lemak omega-3 pada minyak ikan hasil pengalengan lemuru (Sardinella sp.) dapat mencapai 29,68%, namun menurut Shahidi dan Wanasundara (1998) kandungan asam lemak tidak jenuhnya yang tinggi merupakan penyebab kerusakan pada minyak ikan. Upaya pencegahan kerusakan telah banyak dilakukan, diantaranya dengan pemberian antioksidan (Kamal-Eldin dan Yanishlieva 2002; Jacobsen et al. 2008). Kerusakan minyak ikan akan semakin buruk apabila tidak ditangani dengan baik selama transportasi dan penyimpanan, karena sifatnya yang rentan terhadap panas, cahaya dan oksigen (Sathviel et al. 2003). Ketengikan mengindikasikan rendahnya kualitas minyak ikan, namun masih dapat diupayakan peningkatan mutunya melalui teknik pemurnian, salah satunya dengan penggunaan soda kaustik (alkali) dan
bleaching earth yang relatif murah dan mudah dilakukan (Rodriguez et al. 2009). Teknik lain dapat diupayakan untuk menjaga stabilitas, mencegah ketengikan dan memberikan nilai tambah pada minyak ikan adalah mikroenkapsulasi (Hogan et al. 2003).
Indonesia merupakan negara pengekspor kepiting-rajungan terbesar untuk pasar internasional (KKP 2013). Ekspor kepiting dan rajungan Indonesia sampai tahun 2012 hanya terdiri dari tiga jenis produk, yakni kepiting-rajungan kaleng (7164 ton), beku (2425 ton), dan segar (6.000 ton), dengan harga pasaran produk segar mencapai Rp. 100 000 - Rp. 200 000/kg. Bilgin dan Fidanbas (2011) melaporkan bahwa daging kepiting mengandung zat gizi penting, selain protein yang tinggi juga terdapat unsur mikronutrien, seperti niasin, folat, potassium, vitamin B12, fosfor, seng, dan selenium. Kurang beragamnya produk olahan kepiting dan potensi harga jualnya yang tinggi ini menjadi peluang yang besar untuk pengembangan produk olahan dari kepiting-rajungan, salah satunya sup krim kepiting.
Permintaan konsumen akan produk pangan selama satu dekade terakhir cenderung mengarah pada pangan yang memberikan kontribusi terhadap kesehatan atau penyediaan nutrisi, pencegah penyakit dan meningkatkan kesehatan fisik serta mental tanpa mengesampingkan kemudahan dan kepraktisan penyajian (Ohama 2006; Mathioudakis 2007). Sup instan merupakan suatu produk olahan pangan kering instan yang dapat dibuat dari daging, ikan, sayuran, serealia atau campurannya dengan atau tanpa penambahan bahan tambahan makanan yang diizinkan. Spesifikasi instan ditekankan pada komponen bahan penyusun kering yang bersifat instan (BSN 1996). Sup krim instan umumnya berupa dry soups yang terbuat dari daging (Krejcˇova et al. 2007), sayuran (Wang et al. 2010) atau jamur (Singh et al. 2003). Upaya pengkayaan sup krim instan masih terfokus pada fortifikasi protein. Milantisari (2006) dan Sangadah (2006) melaporkan mengenai pemanfaatan tepung daging-tulang leher ayam pedaging sebagai sumber protein pada sup krim instan jamur tiram putih dan jamur shitake, kemudian Haryasyah
et al. (2009) melaporkan tentang pemanfaatan pupa ulat sutra sebagai sumber protein sup krim instan, sehingga fortifikasi unsur atau pengkayaan gizi lainnya yang berperan penting terhadap kesehatan, misalnya asam lemak esensial (Kamal-Eldin dan Yanishlieva 2002) masih sangat perlu untuk dikembangkan.
Asam lemak omega-3 ditinjau dari manfaatnya yang banyak terdapat pada minyak ikan, serta potensi nilai jual kepiting dan olahannya dalam bentuk instan, maka pengembangan dan aplikasi mikroenkapsulasi minyak ikan kaya akan asam lemak omega-3 untuk fortifikasi pada produk sup krim kepiting instan menjadi sangat penting untuk dilakukan.
Tujuan Penelitian
Tujuan umum penelitian adalah pengembangan dan aplikasi mikroenkapsulasi minyak ikan lemuru kaya asam lemak omega-3 sebagai bahan fortifikasi pada sup krim kepiting instan.
Tujuan khusus dari penelitian yaitu:
1 Menentukan waktu homogenisasi mikrokapsul minyak ikan terbaik dan karaketristiknya.
2 Menentukan pengaruh fortifikasi mikrokapsul minyak ikan terhadap karakteristik sensori, fisika, dan kimia sup krim kepiting instan.
METODE PENELITIAN
Waktu dan Tempat
Penelitian dilaksanakan pada bulan Mei 2014 hingga Januari 2015. Penelitian bertempat di Institut Pertanian Bogor, yang meliputi Laboratorium Biokimia Hasil Perairan, Laboratorium Preservasi dan Pengolahan Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Laboratorium Terpadu Fakultas Kedokteran Hewan, Laboratorium Biokimia Gizi, Departemen Gizi Masyarakat, Fakultas Ekologi Manusia, Laboratorium Pilot Plant
Pusat Antar Universitas, SEAFAST Institut Pertanian Bogor, Laboratorium Kimia Terpadu Pascasarjana dan Laboratorium Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, serta Laboratorium Bahan Bangunan Puslitbang Permukiman Bandung.
Bahan
Bahan penelitian meliputi daging kepiting (berasal dari kepiting jantan jenis
Scylla serrata yang diangkut dalam keadaan hidup dari Tarakan, Kalimantan Utara, kadar protein 18,47% dan lemak 0,71%). Minyak ikan diperoleh dari pengalengan ikan lemuru (Sardinella sp.) di Pekalongan, Jawa Tengah (dikirimkan selama 12 jam). Attapulgit (pH 6), bentonit (kandungan montmorilonit 80%, pH <8,2), NaOH 20 ºBe (dipilih berdasarkan kadar asam lemak bebas minyak ikan sebelum pemurnian yaitu 5,27%, dibuat dari 14,36% NaOH dalam 100 mL aquades mengacu Hodgson (1995)), gum arab (80 mesh), maltodekstrin (90 mesh, DE 10-15), tepung mocaf (modified cassava flour) merk Mocaf (kadar pati 73,29%), maizena merk Maizenaku (protein 1%, karbohidrat total 89%), susu skim merk Tropicana Slim (protein 26%, karbohidrat total 57,20%),Italian mix leaves (basil, oregano, dan rose marry), minyak jagung Tropicana Slim (PUFA 50%).
Alat
Peralatan yang digunakan meliputi sentrifuge Hitachi CR G Series (himac CR 21G), magnetic stirrer (Yamato MH-61, 200-1200 rpm, 100 V), homogenizer
Wiggen Hauser, Spray Dryer (Büchi 190 (Ø nozzle 0,7 mm), mikroskop polarisasi cahaya (Zeiss Primo Star dengan kamera Axio Cam Erc5s), timbangan (Sartorius BS 124 S), drum dryer (Buflovak drum ganda, Ø drum 0,5 m, panjang drum 1 m, suhu drum 100 ºC, kecepatan drum 1 putaran/31,68 detik), spektrofotometer (UV-Vis 2500 Shimadzu), Toki Sangyo Viscometer model TV-10 (spindel no. M4),
Scanning Electron Miscroscope (Phenom ProX) dan Gas Chromatography
Prosedur Penelitian
Penelitian ini terdiri atas lima tahap yaitu 1) pemurnian minyak ikan, 2) mikroenkapsulasi minyak ikan, 3) formulasi sup krim kepiting instan, 4) fortifikasi mikrokapsul minyak ikan terhadap sup krim kepiting instan, dan 5) penentuan formula terbaik sup krim kepiting instan yang difortifikasi mikrokapsul minyak ikan serta perhitungan kandungan gizinya. Garis besar keterkaitan antar tahapan penelitian dapat dilihat pada Gambar 1.
Gambar 1 Diagram alir keterkaitan antar tahapan penelitian
Pemurnian minyak ikan
Minyak ikan yang digunakan merupakan minyak ikan hasil samping pre-cooking pengalengan lemuru (Sardinella sp.) yang berasal dari PT.X Pekalongan, Jawa Tengah. Minyak disimpan dalam wadah gelap dan rapat pada suhu -4°C, kemudian dicairkan (thawing) saat akan diuji kualitasnya mengacu pada ketentuan atau standar Council for Responsible Nutrition (2010) dan Internatonal Fish Oil Standard (2010) untuk pangan dan obat-obatan, meliputi parameter kadar asam
lemak bebas (free fatty acid), bilangan peroksida, angka p-anisidin, dan nilai total oksidasi.
Teknik yang digunakan mengacu Sathivel et al. (2003) dengan modifikasi pada konsentrasi NaOH, serta Tambunan (2014) berupa penggunaan bentonit dan attapulgit sebagai bahan bleaching. Aktivitas pemurnian diawali dengan sentrifugasi minyak ikan pada kecepatan 12 499 × g suhu 10 ºC selama 30 menit, yang bertujuan menghilangkan partikel solid atau komponen oksidasi bebas, serta logam berat yang menyebabkan peningkatan nilai bilangan peroksida (Bhattacharya et al. 2008). Penambahan NaOH 20 ºBe dilakukan untuk mengikat asam lemak bebas melalui reaksi saponifikasi dengan teknik pengadukan menggunakan magnetic stirrer kecepatan 11 × g hingga homogen pada suhu 60 ºC selama 20 menit (kondisi optimal modifikasi Sathivel et al. (2003). Pemisahan sabun yang terbentuk dilakukan dengan sentrifugasi kecepatan 12 499 × g pada suhu 20 ºC selama 15 menit, kemudian endapan sabun dipisahkan dengan cara penuangkan minyak (terletak pada bagian atas wadah sentrifuse) ke dalam botol kaca gelap. Minyak ikan hasil alkali refining kemudian dicuci untuk menghilangkan sisa sabun dengan penambahan 5% (b/b) aquades, kemudian dikocok dan didiamkan 10 menit hingga air cucian terpisah. Minyak kemudian dipisahkan dari air dengan menggunakan pipet. Pencucian diulang sebanyak 3 kali hingga pH minyak netral sebagai tanda hilangnya sisa sabun (Sathviel et al. 2003).
Bleaching dilakukan untuk menyerap asam lemak bebas, komponen
teroksidasi, dan pigmen warna sehingga warna minyak menjadi lebih cerah (Maes et al. 2005, Eyub dan Celik 2005, Bhattacharya et al. 2005) dengan
penambahan attapulgit 3% dan bentonit 3% dan diaduk dengan magnetic stirrer
kecepatan 11 × g selama 20 menit pada suhu 29 ºC (kondisi optimal modifikasi Tambunan (2014); Sathivel et al. (2003)) hingga homogen (Maes et al. 2005; Sabah dan Celik 2005). Sentrifugasi kembali dilakukan dengan kecepatan 12 499 × g selama 30 menit pada suhu 10 ºC untuk memisahkan endapan absorben dengan minyak.
Minyak ikan setelah pemurnian dianalisis meliputi bilangan asam (American Oil Chemists Society 1998 butir Ca5a-40), asam lemak bebas (AOCS 1998 butir Ca 5a-40), bilangan peroksida (Association of Analytical Chemists 2000, No. Metode 965.33b), bilangan p-anisidin (IUPAC 1987, No. Metode 2.504), nilai total oksidasi (AOCS 1997), keragaan asam lemak dengan Gas Chromatography
(AOAC 2005 butir 969.33).
Mikroenkapsulasi dan karakterisasi mikrokapsul minyak ikan
Mikroenkapsulasi minyak ikan hasil pemurnian dilakukan dengan bahan penyalut maltodekstrin dan gum arab dengan perbandingan 2:3, yang dalam penggunaannya dilarutkan 30% dari bobot air yang ditambahkan (Rubilar et al.
2012). Maltodekstrin dan gum arab yang telah dicampurkan, ditambahkan aquades dan dipanaskan pada suhu 60 ºC hingga meleleh. Larutan penyalut didinginkan hingga suhu mencapai 45 ºC dan dihomogenisasi dengan kecepatan 40 498 × g selama 2 menit.
emulsi minyak diamati dengan mikroskop polarisasi cahaya Zeiss Primo Star dengan kamera Axio Cam Erc5s dengan perbesaran 10 × 10, yang dioperasikan menurut Kolanowski et al. (2004) dengan modifikasi penggunaan perbesaran.
Emulsi minyak ikan yang dihasilkan kemudian dikeringkan menggunakan pengering semprot (spray dryer) dengan kondisi pengeringan Tinlet = 140 °C dan
Toutlet = 95 °C, laju alir udara 73 m3/jam dan feed rate 5,3 g/menit. Mikrokapsul
kemudian disimpan pada suhu -20 °C untuk keperluan pengujian (Imagi et al.
1992).
Kualitas mikrokapsul diuji yang meliputi karakteristik efisiensi mikroenkapsulasi (Velasco et al. 2006), morfologi mikrokapsul dengan Scanning Electronic Microscope (SEM), keragaan asam lemak dengan Gas Chromatography
(AOAC 2005, No. metode 969.33) dan analisis indeks stabilitas oksidasi (OSI) mikrokapsul (AOCS 1997 butir Cd 12b-92 OSI, ISO6886:1996(E) Rancimat).
Formulasi sup krim kepiting instan dengan metode Bayes
Komposisi formula bahan sup krim kepiting instan mengacu Rubilar et al.
(2012) dengan modifikasi pada formulasi tepung mocaf, daging kepiting, minyak jagung, dan mix leaves. Formula sup krim instan dapat dilihat pada Tabel 1. Tabel 1 Formula sup krim kepiting instan
Pembuatan sup krim instan diawali dengan preparasi kepiting. Preparasi dilakukan sesuai SNI 01-6929.3-2002 untuk diambil dagingnya. Kepiting (Scylla serrata) yang telah dibersihkan, direbus dalam air selama 20 menit suhu 100 ºC, selanjutnya dilakukan pemisahan antara daging dengan karapas. Daging kemudian dihaluskan menggunakan grinder Fomac tipe G31. Bahan-bahan tepung berupa tepung mocaf, tepung maizena, dan susu skim masing-masing dilarutkan terlebih dahulu dengan air sebanyak 20 mL untuk mencegah koagulasi saat pemasakan.
Teknik pencampuran bahan dan pemasakan mengacu Sunyoto dan Futiawati (2012). Proses pemasakan diawali dengan penumisan (sauté frying) pada suhu 70 °C daging kepiting dengan minyak jagung dan seasoning. Larutan susu skim, tepung, mocaf, dan maizena ditambahkan berturut-turut sambil diaduk. Garam dan gula kemudian dimasukkan, sambil terus diaduk Italian mix leaves
ditaburkan terakhir ke dalam sup. Sup krim dimasak selama 3 menit pada suhu 80 ºC. Sup krim dibiarkan dingin dan dihaluskan dengan blender hingga homogen untuk memudahkan pada saat pengeringan. Sup dikeringkan dengan drum dryer
(suhu drum 100 ºC, kecepatan drum 1 putaran/ 31,68 detik). Produk yang dihasilkan berupa lembaran kering, kemudian dihaluskan dengan food processor dan disimpan dalam plastik alumunium foil untuk dianalisis dan di uji hedonik.
Komposisi bahan Jumlah (%)
Seasoning (garam, gula, bawang putih (Allium sativum), lada putih (Piper nigrum L.), Italian mix leaves (oregano, basil, dan rosemarry))
16,79
Formula sup krim terpilih didasarkan pada kesukaan konsumen terhadap karakteristik sensori dengan pembobotan (kenampakan, warna, aroma, kekentalan, dan rasa). Penentuan formula sup krim kepiting instan dilakukan dengan uji indeks kinerja (metode Bayes) dengan perlakuan penambahan air. Lembar kuesioner, metode perhitungan Bayes dapat dilihat pada Lampiran 3. Formula terpilih yang diperoleh kemudian digunakan sebagai formula yang akan diberi perlakuan mikrokapsul minyak ikan.
Fortifikasi mikrokapsul minyak ikan dan karakterisasi terhadap sup krim kepiting instan
Fortifikasi mikrokapsul minyak ikan terhadap sup krim kepiting instan diujikan dengan tiga perlakuan yaitu konsentrasi 3,00%, 3,30%, dan 3,60% dari bobot sup krim instan. Acuan didasarkan pada GRAS US FDA (2004), yaitu mengenai kadar maksimum minyak ikan dan mikrokapsulnya yang diperbolehkan pada produk sup krim instan masing masing 2,00% (b/b) dan 3,60% (b/b).
Analisis terhadap ketiga sup krim instan dengan penambahan atau fortifikasi mikrokapsul minyak ikan kaya omega-3 mengacu Rubilar et al. (2012); Sunyoto dan Futiawati (2012), yang meliputi karakteristik sensori (kenampakan, kekentalan, rasa, warna, dan aroma) (Lampiran 7); analisis data dengan uji Kruskal Wallis dan uji lanjut Dunn, kimia (kadar air, abu, protein, lemak, dan karbohidrat) dan fisika (indeks penyerapan air, indeks kelarutan air, dan viskositas), kemudian dibandingkan dengan sup krim instan kontrol (tanpa penambahan mikrokapsul minyak ikan).
Penentuan formula terbaik sup krim kepiting instan dan perhitungan kandungan gizi
Formula terpilih ditentukan berdasarkan karakteristik terbaik dari ketiga formula sup krim instan yang difortifikasi mikrokapsul minyak ikan dengan uji indeks kinerja (metode Bayes). Formula terpilih yang didapatkan, dihitung angka kecukupan gizinya (Almatsier 2006).
Prosedur Analisis
Analisis bilangan peroksida (AOAC 2000, No. Metode 965.33b)
Analisis bilangan peroksida dilakukan dengan penimbangan 5 g contoh dalam erlenmeyer 250 mL kemudian ditambahkan 30 mL larutan asam asetat glasial dan kloroform (3:2). Sebanyak 0,5 mL larutan KI jenuh ditambahkan ke dalam campuran, kemudian ditambah 30 mL aquades dan 0,5 mL indikator pati 1%. Warna campuran sebelum dititrasi adalah biru kehitaman, lalu campuran tersebut dititrasi dengan Na2S2O3 0,1 N hingga larutan menjadi kuning. Blanko dengan
Bilangan peroksida (meq/kg) = S-B ×GN×1000
Analisis bilangan asam dan kadar asam lemak bebas (AOCS 1998, No. Metode Ca 5a-40)
Prinsip bilangan asam dan asam lemak bebas adalah pelarutan contoh lemak atau minyak dalam pelarut organik tertentu (alkohol netral 96%) dilanjutkan dengan penitaran dengan basa KOH. Contoh yang akan diuji, ditimbang sebanyak 5 g di dalam erlenmeyer 250 mL, lalu ke dalam contoh ditambahkan alkohol netral 96% sebanyak 25 mL dan dipanaskan sampai mendidih. Larutan ditambahkan 2 mL indikator PP, kemudian dititrasi dengan larutan KOH 0,1 N hingga berwarna merah muda (konstan selama 15 detik).
M = Bobot molekul asam dominan (DHA, bobot molekul= 328,488 g/mol) m = Bobot contoh (gram)
56,1= Bobot molekul KOH
Analisis bilangan p-anisidin (International Union on Pure an Applied Chemistry 1987, No. Metode 2.504)
Penentuan bilangan p-anisidin dilakukan dengan metode IUPAC (1987). Larutan uji 1 dibuat dengan cara melarutkan 0,5 g sampel ke dalam 25 mL isooktan. Larutan uji 2 dibuat dengan cara menambahkan 1 mL larutan p-anisidin (2,5 g/L) ke dalam 5 mL larutan uji 1, kemudian dikocok dan dihindarkan dari cahaya. Larutan referensi dibuat dengan cara menambahkan 1 mL larutan p-anisidin (2,5 g/L) ke dalam larutan isooktan, kemudian dikocok dan dihindarkan dari cahaya. Larutan diukur nilai absorbansinya, larutan uji 1 pada 350 nm dengan menggunakan isooktan sebagai larutan kompensasi. Larutan uji 2 pada 350 nm tepat 10 menit setelah larutan disiapkan, dengan menggunakan larutan referensi sebagai standar. Angka anisidin dihitung dengan rumus sebagai berikut:
Angka anisidin = 5 × , As − Abm
Keterangan:
Ab = Absorbansi larutan uji 1 As = Absorbansi larutan uji 2
Penentuan nilai total oksidasi (AOCS 1997)
Nilai total oksidasi didapat dengan menjumlahkan nilai 2PV dengan PAV,
dimana PV (Peroxide Value) adalah bilangan peroksida dan PAV (P-anisidine Value) adalah bilangan p-anisidin.
Total Oksidasi = 2PV + PAV
Analisis keragaan asam lemak menggunakan gas kromatografi (AOAC 2005, No. metode 969.33)
Minyak 20 mg dalam tabung bertutup teflon ditambah dengan 1 mL NaOH 0,5 N dalam metanol, kemudian dipanaskan dalam penangas air selama 20 menit. Larutan BF3 20% 2 mL dan 5 mg/mL standar internal ditambahkan ke dalam
campuran, lalu campuran dipanaskan selama 20 menit. Campuran didinginkan, kemudian ditambahkan 2 mL NaCl jenuh dan 1 mL isooktan, lalu campuran dikocok dengan baik. Lapisan isooktan yang terbentuk dipindahkan dengan bantuan pipet tetes ke dalam tabung berisi sekitar 0,1 gram Na2SO4 anhidrat, dan dibiarkan
15 menit. Fasa cair yang terbentuk dipisahkan, sedangkan fasa minyak yang terbentuk diinjeksikan ke instrumen GC sebanyak 1 μL, setelah sebelumnya dilakukan penginjeksian 1 μL campuran standar FAME (Supelco 37 component fatty acid methyl ester mix). Laju alir N2 pada alat GC 20 mL/ menit, laju alir H2
30 mL/ menit, dengan suhu injektor 200 °C dan suhu detektor 230 °C. Waktu retensi dan puncak masing-masing komponen diukur lalu dibandingkan dengan waktu retensi standar untuk mendapatkan informasi mengenai jenis dan komponen-komponen dalam contoh. Kandungan komponen-komponen dalam contoh dihitung dengan rumus sebagai berikut:
Cstandar = Konsentrasi standar
Vcontoh = Volume contoh
Bentuk dan ukuran globula
Emulsi mikroenkapsulat diteteskan pada kaca preparat dan diposisikan pada meja objek. Bentuk dan ukuran spesimen diamati dengan perbesaran 10×10 pada mikroskop polarisasi cahaya Zeiss Primo Star dengan kamera Axio Cam Erc5s dan monitor Compaq S2021a.
Efisiensi mikroenkapsulasi (Rubilar et al. 2012)
Efisiensi mikrokapsul (%) merupakan perbandingan minyak yang terdapat di dalam mikrokapsul dengan berat minyak yang digunakan dalam pembuatan mikrokapsul atau diperoleh dengan rumus sebagai berikut:
Struktur mikrokapsul dengan Scanning Electron Microscope (Rubilar et al. 2012)
Struktur permukaan dan bentuk mikrokapsul diamati menggunakan SEM. Cuplikan mikrokapsul dihampaudarakan terlebih dahulu, lalu dilapisi campuran emas dan paladium dengan mesin auto coater hingga konduktif terhadap elektron. Struktur dan ukuran diamati pada perbesaran 5000× dan 10 000× atau bergantung pada ukuran mikrokapsul.
Stabilitas oksidasi mikrokapsul (AOCS 1997 butir Cd 12b-92 OSI, ISO6886:1996(E) Rancimat, Kobus et al. 2009)
Sampel 3,5 g sampel minyak ikan dan minyak ikan yang diekstrak dari mikrokapsul dimasukkan ke dalam rancimat pada suhu 100 ºC dan aliran oksigen ditetapkan sebanyak 20 L/jam terus-menerus hingga didapat waktu induksi atau indeks stabilitasnya. Waktu induksi kedua sampel kemudian dibandingkan untuk mengetahui stabilitas oksidasinya.
Indeks penyerapan air dan indeks kelarutan air (Anderson et al. 1984)
Sampel tepung sup krim instan 3 g dimasukkan ke dalam tabung sentrifuse. Aquades 30 mL ditambahkan, diaduk dengan menggunakan vortex sampai semua bahan terdispersi merata. Tabung disentrifugasi pada suhu ruang selama 15 menit. Supernatan dipisahkan, sedangkan tabung sentrifuse beserta residunya dikeringkan dalam oven. Tabung diletakkan dengan posisi miring (25º) dan oven diatur pada suhu 50 ºC selama 25 menit. Tabung sentrifuse ditimbang untuk menentukan berat residunya.
Supernatan yang diperoleh, diambil 2 mL sebagai contoh dan dimasukkan ke dalam cawan yang telah diketahui beratnya. Cawan dikeringkan di dalam oven pada suhu 110 ºC selama 24 jam. Cawan didinginkan dan ditimbang sebagai bahan kering yang terlarut dalam supernatan.
IPA (mL/g) = A + B-C + D
D
IKA g mL⁄ = Berat cawan setelah dikeringkan dalam oven2 mL Keterangan:
A = berat awal
B = berat residu setelah dikeringkan dalam oven C = berat tabung
D = berat tepung sup krim instan
Pengujian karakteristik sensori
sensori sup krim kepiting instan dengan fortifikasi mikrokapsul minyak ikan dapat dilihat pada Lampiran 10.
Viskositas
Pengukuran viskositas dilakukan dengan alat pengukur viskositas yaitu Viscometer Toki Sangyo model TV-10 (spindle no. M4, 0,08 × g). Sampel yang akan diukur dipersiapkan sebanyak 10 g, dimasak dengan menggunakan air sebanyak 50 mL selama ± 1,5 menit. Sampel diukur pada suhu 50 °C. Pengukuran viskositas dimulai sesaat setelah tombol daya ditekan dan spindle berputar dalam sampel, hingga nilai viskositas yang tertera pada alat stabil.
Analisis kadar lemak (AOAC 2005)
Sampel 0,5 g ditimbang, dibungkus dengan kertas saring dan diletakkan pada alat ekstraksi soxhlet yang dipasang di atas kondensor serta labu lemak di bawahnya. Pelarut heksan dituangkan ke dalam labu lemak secukupnya sesuai dengan ukuran soxhlet yang digunakan dan dilakukan refluks selama minimal 16 jam sampai pelarut turun kembali ke dalam labu lemak. Pelarut di dalam labu lemak didestilasi dan ditampung. Labu lemak yang berisi lemak hasil ekstraksi dikeringkan dalam oven pada suhu 105 °C selama 5 jam. Labu lemak didinginkan dalam desikator selama 20-30 menit dan ditimbang. Perhitungan kadar lemak dapat dihitung dengan rumus sebagai berikut:
Kadar lemak % = Bobot labu dengan lemak-labu kosongBobot sampel ×100%
Kadar air (AOAC 2000 butir 934.01)
Cawan porselen kosong dikeringkan dalam oven bersuhu 105 °C selama 15 menit. Cawan porselen tersebut didinginkan di dalam desikator. Setelah dingin, cawan porselen kosong ditimbang dan dicatat bobotnya. Sampel ditimbang 5 g dan diletakkan di dalam cawan porselen. Sampel dikeringkan dengan oven bersuhu 105 °C selama 3 jam. Setelah proses tersebut, sampel beserta cawan didinginkan kembali di dalam desikator. Sampel yang telah kering beserta cawan ditimbang kembali dan dicatat bototnya. Perhitungan persentase kadar air basis basah dapat dihitung dengan rumus sebagai berikut:
Kadar air % = Bobot cawan+ Bobot sampelsampel -Bobot setelah oven ×100%
Kadar protein (AOAC 2000 butir 981.10)
Analisis protein dilakukan dengan metode kjeldahl mikro. Sampel 0,1 g dimasukkan ke dalam labu kjeldahl 30 mL. Ditambahkan K2SO4 (1,9 g), HgO
(40 mg), H2SO4 (2,5 mL) serta beberapa tablet kjeldahl ke dalam sampel. Sampel
dididihkan sampai berwarna jernih (1-1,5 jam); didinginkan dan dipindahkan ke alat destilasi. Lalu dibilas dengan air sebanyak 5-6 kali dengan akuades (20 mL). Larutan NaOH 40 % ditambahkan ke dalam tabung reaksi 20 mL. Cairan dalam ujung kondensor ditampung dengan erlenmeyer 125 mL berisi larutan H3BO3 dan
dilakukan sampai diperoleh kira-kira 200 mL destilat yang bercampur dengan H3BO3 dan indikator dalam erlenmeyer. Destilat dititrasi dengan menggunakan HCl
0,1 N sampai terjadi perubahan warna menjadi warna merah. Kadar protein dapat dihitung dengan rumus sebagai berikut:
Nitrogen % = (mL HCl sampelmg sampel-mL HCl blanko)×100%
Kadar protein % =% Nitrogen×faktor koreksi (6,25)
Kadar abu (AOAC 2005 butir 938.08)
Cawan porselen kosong dikeringkan dalam oven bersuhu 105 °C selama 15 menit, dan didinginkan di dalam desikator. Setelah dingin, cawan porselen kosong tersebut ditimbang dan dicatat bobotnya. Sampel sebanyak 5 g ditimbang dan diletakkan di dalam cawan porselen. Cawan porselen yang berisi sampel dipijarkan diatas nyala api hingga tidak mengeluarkan asap. Cawan tersebut dimasukkan ke dalam tanur pengabuan dengan suhu 600 °C selama 6 jam. Cawan didinginkan di dalam desikator lalu ditimbang hingga mendapatkan berat yang konstan. Perhitungan persentase kadar abu basis basah dapat dihitung dengan rumus sebagai berikut:
Kadar abu % = Bobot setelah tanurBobot sampel-Bobot cawan ×100%
Kadar karbohidrat (AOAC 2000)
Analisis karbohidrat dilakukan secara by difference, yaitu hasil pengurangan dari 100 % dengan kadar air, kadar abu, kadar protein dan kadar lemak, sehingga karbohidrat tergantung pada faktor pengurangannya. Hal ini karena karbohidrat sangat berpengaruh terhadap zat gizi lainnya. Analisis karbohidrat dapat dihitung dengan menggunakan rumus sebagai berikut:
Kadar karbohidrat=100%- kadar air+kadar abu+kadar lemak+kadar protein
Rancangan Percobaan dan Analisis Data
Data hasil uji sensori sup krim kepiting instan dengan perlakuan penambahan air (rehidrasi) dan sup krim kepiting instan dengan perlakuan fortifikasi mikrokapsul minyak ikan diolah menggunakan uji statistik non parametrik yaitu uji Kruskal Wallis dengan software Statistical Process for Social Science (SPSS) versi 22.0. Hasil uji Kruskal Wallis yang berpengaruh nyata diuji lanjut dengan menggunakan uji Dunn. Perhitungan uji Kruskal Wallis secara manual menurut Steel dan Torrie (1993) meliputi langkah-langkah berikut:
a Perankingan dengan mengurutkan nilai dari yang terkecil hingga terbesar berdasarkan nilai hasil sensori untuk semua perlakuan
b Membuat tabel ranking
FK = −
∑ T n− n n+e Menghitung H yang merupakan kriteria uji
H =
Ni = jumlah pengamatan pada setiap perlakuan
K = perlakuan Z = peubah acak
Rancangan percobaan yang digunakan adalah rancangan acak lengkap dengan faktor penambahan mikrokapsul minyak ikan dengan tiga taraf dan tiga kali ulangan untuk analisis sifat fsik dan kimia sup krim kepiting instan. Model matematika rancangan acak lengkap menurut Steel dan Torrie (1993) adalah :
Yij = µ + Ai + ɛij
Keterangan :
Yij = respon percobaan karena pengaruh perlakuan penambahan mikrokapsul
minyak ikan taraf ke-i, ulangan ke-j µ = nilai rata-rata
Ai = pengaruh perlakuan penambahan mikrokapsul minyak ikan taraf ke-i
ɛij = pengaruh kesalahan percobaan karena pengaruh perlakuan penambahan
mikrokapsul minyak ikan taraf ke-i dan ulangan ke-j i = ulangan
j = perlakuan
Hipotesis yang diuji pada pembuatan sup krim kepiting instan dengan fortifikasi mikrokapsul minyak ikan adalah :
H0 : Perlakuan penambahan konsentrasi mikrokapsul minyak ikan tidak
memberikan pengaruh berbeda terhadap karakteristik sup krim kepiting instan.
H1 : Minimal ada satu perlakuan penambahan konsentrasi mikrokapsul minyak
ikan yang memberikan pengaruh berbeda terhadap karakteristik sup krim kepiting instan.
uji lajut dengan menggunakan uji berganda Duncan untuk melihat perbedaan nyata antara perlakuan yang diberikan.
HASIL DAN PEMBAHASAN
Karakteristik Mutu Minyak Ikan
Minyak ikan hasil samping pengalengan yang akan digunakan secara keseluruhan belum memenuhi standar Council for Responsible Nutrition (2010) dan
International Fish Oil Standard (2010), terutama kandungan asam lemak bebas, bilangan asam, dan bilangan peroksida. Pemurnian minyak ikan dengan metode
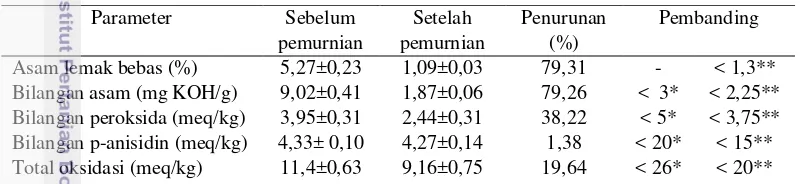
alkali refining dan bleaching terbukti dapat meningkatkan kualitas minyak ikan yang ada. Kualitas minyak ikan sebelum dan setelah pemurnian dapat dilihat pada Tabel 2.
Tabel 2 Kualitas minyak ikan sebelum dan setelah pemurnian
*Council for Responsible Nutrition (2010) ** International Fish Oil Standard (2010)
Tingginya kadar asam lemak bebas pada minyak sebelum pemurnian diduga karena masih tingginya kandungan air yang menyebabkan minyak ikan terhidrolisis. Pembentukan asam lemak bebas dapat terjadi karena adanya proses hidrolisis (Paul dan Mittal 1997). Minyak ikan dengan bilangan peroksida yang tinggi menunjukkan bahwa minyak tidak diproses dan disimpan dengan cara yang benar sehingga menyebabkan terjadinya oksidasi yang berlebihan. Beberapa faktor pemicu oksidasi ini antara lain keberadaan oksigen, enzim peroksidase, panas, radiasi cahaya, dan ion monovalen yang mempercepat terjadinya oksidasi pada minyak (Rustad 2010).
Nilai asam lemak bebas akan berbanding lurus dengan bilangan asam. Minyak yang mempunyai bilangan asam yang tinggi menunjukkan mutu rendah yang diakibatkan oleh pengolahan ataupun kerusakan minyak selama penyimpanan. Penurunan nilai asam lemak bebas pada proses pemurnian terjadi karena adanya pengikatan asam lemak bebas oleh senyawa alkali NaOH membentuk sabun dan air yang kemudian dipisahkan melalui proses sentrifugasi.
Peroksida merupakan produk indikasi dari oksidasi pada minyak ikan. Tingginya kandungan asam lemak jenuh majemuk pada minyak ikan dapat merangsang terjadinya kerusakan oksidatif (Serfert et al. 2010). Penurunan bilangan peroksida ini disebabkan sifat peroksida yang bersifat lebih polar dibandingkan minyak sehingga mudah diserap oleh sabun yang terbentuk pada proses penyabunan (Bimbo 1998).
Bilangan p-anisidin adalah bilangan yang memperkirakan adanya senyawa senyawa hasil dekomposisi hidroperoksida yang disebabkan oleh oksidasi lanjut (Hogan et al. 2003). Bilangan p-anisidin tidak selalu seiring dengan tingginya bilangan peroksida (Guillén dan Cabo 2002), namun tingginya bilangan peroksida dapat menyebabkan tingginya bilangan p-anisidin jika proses yang diberikan pada minyak ikan memungkinkan terjadinya degradasi lebih lanjut.
Bilangan total oksidasi merupakan parameter pengukur progresivitas dari proses deteriorasi yang terjadi pada minyak dan menyediakan informasi mengenai pembentukan produk oksidasi primer serta sekunder (Hamilton dan Rossell 1986). Reaksi oksidasi primer dan sekunder dapat dilihat pada Gambar 2.
Gambar 2 Reaksi oksidasi primer dan sekunder (Hamilton dan Rossell 1986)
Total oksidasi (totoks) adalah hasil penjumlahan antara dua kali bilangan peroksida dengan bilangan p-anisidin. Nilai total oksidasi dapat digunakan untuk mengukur progresivitas dari proses deteriorasi yang terjadi pada minyak dan menyediakan informasi mengenai pembentukan produk oksidasi primer serta sekunder (Hamilton and Rossell 1986). Nilai total oksidasi minyak hasil pemurnian mengalami penurunan yang menunjukkan bahwa jumlah peroksida dan hasil oksidasi sekunder menurun setelah proses pemurnian. Nilai total oksidasi ini berada dibawah batas maksimum menurut IFOS (2010) dan CRN (2010).
Karakteristik Mikrokapsul Minyak Ikan Stabilitas globula mikroenkapsulat minyak ikan
Stabilitas globula merupakan faktor penting dalam proses mikroenkapsulasi untuk mencegah atau mengurangi kecenderungan lemak bergabung kembali (coalescene) sebelum emulsi dikeringkan. Pengamatan globula mikroenkapsulat pada emulsi dilakukan untuk menentukan lama waktu terbaik yang dibutuhkan
Reaksi primer
27,67±3,99
dalam homogenisasi emulsi minyak ikan yang relatif stabil. Penyatuan bahan minyak dan air yang terbentuk pada suatu emulsi hanya dapat berlaku sementara karena perbedaan massa jenisnya (McClements 1999). Semakin kecil ukuran globula, stabilitas ukurannya akan semakin besar akibat daya dorong bahan yang terkapsul semakin kecil untuk mendorong dinding sel kapsul sehingga mencegah terjadinya coalescene. Upaya pengurangan kecenderungan sifat coalescene dapat dilakukan dengan proses homogenisasi dan penambahan bahan penyalut yang dapat berfungsi sebagai pengemulsi dan penstabil emulsi. Lebih jauh lagi pengukuran ukuran globula serta penyebarannya dalam emulsi akan mempengaruhi retensi minyak dan jumlah minyak bebas pada permukaan mikrokapsul kering (efisiensi mikroenkapsulasi) (Hogan et al. 2001).
Penggunaan maltodekstrin sebagai bahan penyalut dipilih karena menghasilkan kelarutan maltodekstrin yang cukup baik pada air dan memiliki kemampuan yang baik dalam melindungi minyak terhadap oksidasi (Westing dan Rennecius 1988), namun stabilitas emulsi dan retensi minyak yang dihasilkan rendah (Simanjuntak 2007). Penambahan gum arab digunakan karena sifatnya yang dapat menciptakan kestabilan yang sempurna dan sifat sebagai emulsifier ketika dicampur dengan sejumlah besar bahan insoluble. Gum arab memiliki sifat yang unik dibandingkan dengan jenis gum lainnya, karena hingga konsentrasi 40-50% tidak memberikan viskositas yang tinggi sedangkan gum yang lainnya hanya mampu ditambahkan dengan konsentrasi 1-5%. Gum arab merupakan agen pengemulsi yang efektif karena kemampuannya sebagai koloid pelindung. Gum arab juga sering digunakan dalam persiapan pangan emulsi minyak dalam air yang mampu menstabilkan sebagian besar minyak pada kisaran pH yang luas meskipun tanpa penambahan agen penstabil lainnya karena sifatnya yang hidrofilik (Gharsallaoui 2007). Perannya sebagai pembentuk gugus hidrofilik ini dapat dilihat pada Gambar 5.
Menurut McClements (1999) intensitas dan lama homogenisasi tergantung dari waktu yang dibutuhkan untuk melarutkan dan menyeragamkan distribusi globula lemak dalam emulsi. Yuliani et al. (2007) mengemukakan bahwa rentang ukuran partikel mikrokapsul adalah 0,2-5000 µm. Sementara Yoshizawa (2004) menyebutkan bahwa rata-rata ukuran mikrokapsul sangat kecil dengan diameter berkisar 15-20 mikron atau kurang dari setengah diameter rambut manusia.
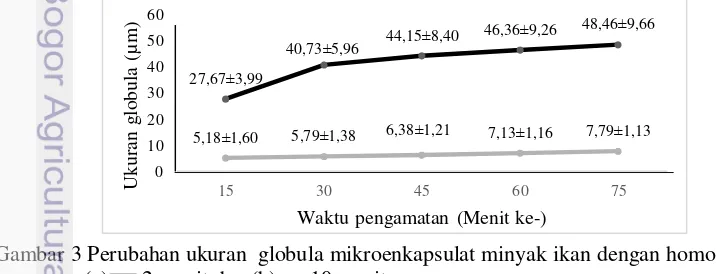
Lama pengadukan mempengaruhi ukuran dan stabilitas globula mikroenkapsulat. Stabilitas ukuran globula mikroenkapsulat minyak ikan dengan lama pengadukan berbeda dapat dilihat pada Gambar 3.
Gambar 4 Kenampakan globula mikroenkapsulat minyak ikan dengan mikroskop polarisasi cahaya perbesaran 10x10, (a) t = 2 menit; (b) t = 10 menit
Emulsi yang dihomogenkan selama 10 menit memiliki ukuran globula yang lebih kecil dan lambat perubahan ukurannya dibandingkan pengadukan selama 2 menit dengan kecepatan yang sama (Gambar 3). Hogan et al. (2001) menyatakan bahwa semakin lama proses homogenisasi berlangsung akan memperkecil ukuran globula lemak dan ukuran globula lemak yang berkisar antara 1-10 μm dan jumlah globula lemak yang relatif besar akan menyebabkan emulsi semakin stabil. Bentuk dan ukuran globula mikroenkapsulat dapat dilihat pada Gambar 4 dan struktur globula mikroenkapsulat minyak dalam air dapat dilihat pada Gambar 5.
Gambar 5 Struktur globula mikroenkapsulat minyak ikan (Shahidi dan Han 1993)
Emulsi minyak ikan yang dihomogenisasi selama 2 menit memiliki ukuran globula yang lebih besar dan tidak merata (Gambar 4a) sedangkan emulsi minyak ikan yang dihomogenisasi selama 10 menit dengan kecepatan sama memiliki globula yang berukuran lebih kecil dan relatif seragam serta kompak (Gambar 4b). Semakin lama proses homogenisasi juga berpengaruh terhadap jumlah globula lemak yang dihasilkan per volume produksi. Pengamatan dengan mikroskop polarisasi ditunjukkan dengan posisi globula yang semakin rapat teratur satu sama lain. Hal ini dikarenakan proses homogenisasi dapat meningkatkan jumlah droplet pada fase pendispersi (Tamjidi et al. 2013; Hogan et al. 2001). Ukuran globula lemak yang sangat kompak dan seragam pada lama pengadukan 10 menit mengindikasikan bahwa emulsi yang dihasilkan memiliki stabilitas yang lebih tinggi dibandingkan pengadukan selama 2 menit. Oleh karena itu perlakuan lama waktu yang digunakan dalam membuat emulsi minyak ikan pada pembuatan mikrokapsul ini adalah 10 menit dengan kecepatan 40 498 × g.
1
Gambar 6 Struktur mikrokapsul minyak ikan dengan Scanning Electron Microscope
(a) perbesaran 10 000×, (b) perbesaran 5000× Efisiensi mikroenkapsulasi
Pengukuran efisiensi mikroenkapsulasi diperlukan untuk mengetahui total minyak yang terenkapsulasi dan fraksi minyak bebasnya. Menurut Velasco et al.
(2006) efisiensi mikroenkapsulasi merupakan perbandingan minyak yang terdapat dalam mikrokapsul dengan berat minyak yang digunakan dalam pembuatan mikrokapsul dan dinyatakan dalam prosentase. Efisiensi mikroenkapsulasi yang dicapai adalah 90,41±0,64% yang tidak berbeda jauh dengan Rubilar et al. (2012) mengenai mikroenkapsulasi minyak linseed yang memiliki efisiensi 90,70±1,19%. Hal ini terjadi karena formula mikrokapsul yang digunakan sama berdasarkan penelitian Bhandari et al. (1992) yaitu penggunaan maltodekstrin dan gum arab sebagai bahan penyalut dengan komposisi 2:3 dan perbandingan antara bahan penyalut dengan minyak 1:2. Turchiuli et al. (2004) melaporkan kombinasi terbaik bahan penyalut dan mendapatkan perbandingan terbaik dalam penggunaan keduanya. Perbandingan antara maltodektsrin dan gum arab sebagai bahan penyalut yaitu 2:3 untuk proses penyalutan yang lebih efisien dan menyisakan fraksi minyak bebas yang rendah (<2% dari total minyak) pada proses mikroenkapsulasi minyak nabati.
Ukuran globula yang kecil dan tersebar merata pun menjadi penyebab tingginya efisiensi mikroenkapsulasi minyak ikan (Gambar 3b). Hal ini sesuai dengan penemuan McNamee et al. (1998) dalam penelitiannya bahwa diameter globula yang besar dari suatu emulsi akan meningkatkan jumlah minyak bebas pada permukaan mikrokapsul yang dikeringkan dengan spray dryer sehingga menghasilkan efisiensi yang rendah. Young et al. (1993) menyatakan bahwa efisiensi mikroenkapsulasi yang tinggi dapat dicapai dengan peningkatan konsentrasi bahan penyalut. Rendahnya proporsi minyak dibandingkan bahan penyalut dapat mengakibatkan retensi minyak yang tinggi dan menurunkan fraksi minyak bebas sehingga efisiensi mikroenkapsulasi menjadi tinggi.
Struktur mikrokapsul
Scanning Electron Microscope (SEM) dilakukan untuk melihat kualitas mikrokapsul. Hasil SEM menunjukkan bahwa mikrokapsul yang dihasilkan umumnya berbentuk bulat, baik itu berbentuk bulat sempurna maupun bulat dengan beberapa lekukan, serta permukaan yang halus tanpa retakan (Gambar 6).
Permukaan halus dan bebas retakan pada mikrokapsul akan mencegah oksidasi zat inti, dalam hal ini asam lemak, sehingga menjaga stabilitas oksidasi mikrokapsul. Mikrokapsul yang diamati pada perbesaran 10 000× memiliki bentuk yang bulat sempurna serta permukaan yang halus dengan ukuran rata-rata 6,52 µ m (Gambar 6a). Pengamatan dengan perbesaran 5000× memperlihatkan distribusi mikrokapsul yang berbentuk bulat dengan beberapa lekukan dan berdempetan satu sama lain. Pelekukan ini menandakan kandungan minyak yang lebih rendah dalam mikrokapsul sehingga mendorong terjadinya pelekukan pada awal proses pengeringan (Mongenot et al. 2001; Bertoloni et al. 2001). Hal inilah yag menyebabkan efisiensi mikroenkapsulasi tidak mencapai 100% dan dapat diatasi dengan peningkatan kecepatan dan waktu homogenisasi.
Keragaan asam lemak mikrokapsul
Keragaan asam lemak mikrokapsul minyak ikan dianalisis dan dibandingkan dengan keragaan minyak ikan sebelum pemurnian untuk mengetahui kualitas bahan dari segi kandungan asam lemaknya. Kandungan asam lemak pada minyak ikan sebelum pemurnian didominasi oleh kandungan asam lemak tak jenuh majemuk (Lampiran 1). Komposisi ini berkaitan dengan kerentanan dari minyak ikan mengalami kerusakan oksidatif (Shahidi dan Wanasundara 1998). Kandungan asam lemak tertinggi pada minyak ikan sebelum pemurnian adalah asam lemak dokosaheksaenoat (DHA), diikuti oleh asam palmitat dan asam lemak eikosapentaenoat (EPA). Tingginya kandungan asam lemak dokosahekasenoat (DHA) ini sejalan dengan hasil penelitian Khoddami et al. (2009) bahwa kandungan asam lemak pada lemuru didominasi oleh DHA (11,87%- 15,95%) dengan kandungan asam eikosapentaenoat 1,73%- 2,76%. Estiasih dan Ahmadi (2012) melaporkan bahwa minyak ikan Sardinella lemuru hasil samping pengalengan ikan mengandung 9,60% EPA dan 10,09% DHA.
Kandungan asam linolenat mengalami penurunan 50,56% (0,89±0,00% menjadi 0,44±0,00%). Asam lemak eikosapentanoat (EPA) mengalami penurunan 52,02%, (8,03±0,04% menjadi 3,85±0,04%). Asam lemak dokosaheksaenoat mengalami penurunan 49,58%, (17,48±0,13% menjadi 8,81±0,13%) (Lampiran 1). Penurunan kandungan asam lemak ini diduga disebabkan adanya panas saat pemurnian dan mikroenkapsulasi. Hal ini terkait dengan komponen asam lemak esensial omega-3 yang merupakan golongan asam lemak tak jenuh majemuk dengan banyak ikatan rangkap yang bersifat rentan terhadap panas dan oksidasi (Shahidi dan Wanasundara 1998). Menurut Serfert et al. (2009), penurunan persentase asam-asam lemak bebas disebabkan oleh oksidasi lemak yang terjadi saat proses mikroenkapsulasi, yakni homogenisasi dan spray drying.
Stabilitas oksidasi mikrokapsul
yang lebih lama mengindikasikan produk memiliki stabilitas oksidasi yang tinggi. Hasil ini menunjukkan tercapainya tujuan utama mikroenkapsulasi, yakni meningkatkan stabilitas minyak ikan terhadap oksidasi.
Formula Sup Krim Kepiting Instan
Formula sup krim kepiting instan ditentukan dengan uji indeks kinerja (metode Bayes) yang didasarkan pada hasil uji sensori dengan perlakuan penambahan air saat rehidrasi (Lampiran 6). Hasil analisis dengan metode Bayes dapat dilihat pada Tabel 3.
Tabel 3 Hasil analisis formula terbaik dengan metode Bayes
Parameter Formula Nilai Bobot
F01 F02 F03 F04 F05 F06 F07 kepiting instan terpilih yaitu formula F01 (perbandingan antara sup instan dan air 1:5), F04 (perbandingan antara sup instan dan air 1:8), dan F02 (perbandingan antara sup instan dan air 1:6). Sup krim kepiting instan dengan proporsi sup dan air 1:5 memiliki bobot nilai tertinggi sehingga sup krim dengan proporsi sup dan air 1:5 ini dinyatakan sebagai formula terpilih dan akan diberi perlakuan penambahan mikrokapsul minyak ikan.
Karakteristik Sup Krim Kepiting Instan Karakteristik sensori
4,85a
Gambar 7 Karakteristik sensori sup krim kepititng instan dengan fortifikasi mikrokapsul
minyak ikan kaya omega-3. (a) Tingkat kesukaan; (b) Karakteristik. Kontrol mikrokapsul 3,00%; mikrokapsul 3,30%; mikrokapsul 3,60%. Angka-
angka dengan huruf superskrip berbeda (a,b) menunjukkan berbeda nyata (p<0,05).
Hasil uji Kruskall Wallis menunjukkan bahwa penambahan mikrokapsul minyak ikan tidak berpengaruh secara nyata pada kenampakan sup krim kepiting instan (p>0,05) (Lampiran 9). Kenampakan sup krim cenderung seragam karena komposisi dan proses pada setiap formula dengan atau tanpa pengayaan mikrokapsul adalah sama. Selain itu mikrokapsul yang digunakan memiliki warna putih seperti tepung, yang kenampakannya cenderung menyerupai tepung bahan baku pembuatan sup krim, sehingga saat ditambahkan dalam jumlah yang relatif sedikit tidak mengakibatkan perbedaan secara visual.
Hasil uji Kruskall Wallis menunjukkan bahwa penambahan mikrokapsul minyak ikan tidak mempengaruhi kekentalan sup krim kepiting instan (p>0,05) (Lampiran 9). Kekentalan sup instan dipengaruhi oleh rasio bahan-bahan sup instan dengan atau tanpa penambahan mikrokapsul minyak ikan dan air yang digunakan untuk merehidrasi sup instan. Bahan yang digunakan pada sup krim kepiting instan memiliki rasio yang sama untuk setiap formulanya.
Nilai modus dan rataan dari penilaian panelis terhadap karakteristik warna sup krim cenderung agak kecoklatan untuk setiap perlakuan (Lampiran 8). Penilaian panelis menunjukkan bahwa penambahan mikrokapsul minyak ikan kaya omega-3 tidak memberikan pengaruh yang nyata terhadap warna sup krim kepiting (p>0,05). Perubahan warna kemungkinan besar disebabkan oleh reaksi pencoklatan non-enzimatis saat proses penginstanan sup menggunakan drum dryer. Warna mikrokapsul minyak ikan yang menyerupai tepung serta selisih penambahannya yang sedikit, tidak mengakibatkan adanya perbedaan warna antar perlakuan.
Tingkat kesukaan terhadap rasa sup krim instan berkisar antara 3,76 (agak tidak suka) hingga 5,82 (cukup suka). Tingkat kesukaan ini beriringan dengan modus hasil uji skoring karakteristik bahwa rasa sup krim ini cenderung agak tidak lezat hingga biasa atau netral (Lampiran 8), sedangkan rataanya berkisar antara tidak suka hingga netral (Gambar 7b). Hasil uji Kruskal Wallis menunjukkan bahwa penambahan mikrokapsul minyak ikan memberikan pengaruh yang berbeda nyata terhadap rasa sup krim kepiting instan (p<0,05). Hasil uji lanjut Dunn menunjukkan konsentrasi mikrokapsul minyak ikan 3,60% berbeda nyata dengan konsentrasi 3,00% dan 3,30%, namun tidak berbeda nyata dengan kontrol (Lampiran 9). Hasil pengujian menunjukkan bahwa panelis cenderung menyukai sup krim dengan konsentrasi mikrokaspul tertinggi yaitu 3,60%. Nilai kesukaan ini juga tidak berbeda nyata dengan sup krim tanpa penambahan mikrokapsul minyak ikan.
Nilai modus uji skoring terhadap karakteristik menunjukkan bahwa aroma sup krim netral atau biasa hingga cukup harum (Lampiran 8), sedangkan rataannya berkisar antara 4,15 (kurang harum) hingga 5,18 (netral). Penambahan mikrokapsul minyak ikan menurunkan tingkat kesukaan panelis terhadap aroma sup krim (Gambar 7a). Hasil uji Kruskal Wallis menunjukkan bahwa penambahan mikrokapsul minyak ikan mempengaruhi terhadap aroma sup krim kepiting instan (p<0,05) (Lampiran 9). Perlakuan konsentrasi 3,30% berbeda nyata terhadap konsentrasi 3,00% dan 3,60%, namun tidak berbeda nyata dengan kontrol. Penambahan konsentrasi mikrokapsul 3,30% terbukti meningkatkan nilai kesukaan aroma sup krim kepiting instan dibandingkan konsentrasi 3,00%, namun mengalami penurunan pada konsentrasi 3,60%. Minyak ikan memiliki bau khas yang dapat berubah menjadi tengik apabila tidak disimpan dan ditangani dengan baik. Sumbangan aroma yang ditimbulkan pada sup krim kepiting instan bukanlah bau tengik melainkan bau khas dari mikrokapsul minyak ikan murni yang ditambahkan. Hal ini dibuktikan dengan hasil pengujian karakteristik minyak ikan murni (Tabel 2) serta efisiensi mikroenkapsulasi minyak ikan yang mencapai 90,41±0,64%. Menurut Velasco et al. (2009) efisiensi mikroenkapsulasi menunjukkan total minyak yang terenkapsulasi dan fraksi minyak bebasnya.
bervariasi antara 3-20 (Kearsley dan Dziedzic 1995). Menurut Hull (2010) semakin tinggi nilai DE, semakin higroskopis pula maltodekstrin dan semakin rendah ketahananya terhadap panas. Nilai DE yang tinggi juga berbanding lurus dengan tingkat kemanisan maltodekstrin, sehingga maltodekstrin dengan DE rendah (<10-15) baik digunakan untuk mikroenkapsulasi yang diaplikasikan pada produk yang melibatkan panas dalam penyajiannya, dalam hal ini sup krim. Karel (1985) menyatakan bahwa kecepatan peluruhan matriks kapsul bergantung satu sama lain antara jumlah air dan temperaturnya. Suhu air yang tinggi meningkatkan energi kinetik sehingga gerak air dalam menembus matriks penyalut semakin cepat untuk proses pelunakkan (rubbery) dan pelepasan zat inti.
Karakteristik fisik
Karateristik fisik terhadap sup krim kepiting instan dengan fortifikasi mikrokapsul minyak ikan kaya omega-3 meliputi indeks penyerapan air (IPA), indeks kelarutan air (IKA), dan viskositas (Tabel 4).
Tabel 4 Karakteristik fisik sup krim kepiting instan dengan fortifikasi mikrokapsul minyak ikan dan kontrol
Parameter Konsentrasi Mikrokapsul Minyak Ikan Pembanding Kontrol 3,00% 3,30% 3,60%
IPA (mL/g) 4,620±0.070c 4,258±0,006b 4,197±0,001b 4,114±0,003a 2,824*
IKA (g/mL) 0,023±0,000c 0,022±0,000b 0,021±0,000b 0,019±0,000a -
Viskositas (cP) 600,00±0,00a 600,00±0,00a 600,00±0,00a 600,00±0,00a 850*
Keterangan: Angka-angka yang diikuti huruf superskrip berbeda (a, b, c) pada baris yang sama menunjukkan berbeda nyata (p<0, 05).
*Sunyoto dan Futiawati (2012)
Indeks penyerapan air (IPA) menunjukkan seberapa besar kemampuan suatu bahan makanan dalam menyerap air. Semakin besar nilai indeks penyerapan air, semakin besar pula kemampuan bahan tersebut dalam menyerap air apabila dilakukan rekonstitusi. Faktor-faktor yang mempengaruhi daya rehidrasi suatu bahan adalah sifat partikel bahan atau porositas dan polaritas bahan serta komposisinya. Daya rehidrasi juga tergantung pada ketersediaan gugus hidrofilik dan kapasitas pembentukan gel makromolekul, yaitu pati yang tergelatinisasi. Semakin banyak pati yang tergelatinisasi, semakin besar kemampuan produk menyerap air (Mestres et al. 1988).
dapat mempercepat proses penyerapan air. Lapisan lemak yang terbentuk pada permukaan granula pati dapat menghalangi penetrasi air terhadap pati sehingga menghambat gelatinisasi pati (Sunyoto dan Futiawati 2012).
Indeks Kelarutan Air (IKA) menyatakan banyaknya jumlah partikel (gram) terlarut dalam sejumlah air tertentu. Berdasarkan hasil analisis ragam, indeks kelarutan air sup krim kepiting instan dipengaruhi secara nyata (p<0,05) oleh penambahan mikrokapsul minyak ikan (Lampiran 10). Nilai IKA produk sup krim kepiting instan semakin menurun seiring peningkatan konsentrasi mikrokapsul minyak ikan yang ditambahkan (Tabel 4). Hal ini dikarenakan penambahan mikrokapsul minyak ikan akan meningkatkan kadar lemak sup krim instan. Menurut Schweizer et al. (1985), lemak yang terdapat pada bahan akan menyelubungi permukaan pati sehingga menghalangi molekul-molekul amilosa larut ke dalam air. Hal inilah yang menyebabkan indeks kelarutan air sup krim instan dengan penambahan konsentrasi mikrokapsul minyak 3,60% lebih rendah dibandingkan konsentrasi 3,30% dan 3,00%.
Viskositas merupakan salah satu sifat reologi yang penting dalam produk, sifat ini menggambarkan besarnya hambatan atau resistensi suatu cairan terhadap aliran dan pengadukan (Bourne 2002). Hasil pengukuran viskositas menunjukkan bahwa sup krim memiliki kekentalan yang tepat sama antar masing-masing perlakuan (Tabel 4). Hal ini menunjukkan bahwa perlakuan penambahan mikrokapsul minyak ikan dengan konsentrasi 3,00%, 3,30%, dan 3,60% tidak mempengaruhi viskositas sup krim kepiting sama sekali. Viskositas sup krim ini lebih rendah dibandingkan sup krim komersil yang ada di pasaran, yaitu 850 cP (Sunyoto dan Futiawati 2012). Menurut Pomeranz (1991), besarnya viskositas tergantung pada jenis dan konsentrasi pati. Semakin tinggi konsentrasi pati maka semakin tinggi viskositas yang dihasilkan. Granula pati akan membentuk pasta yang kental apabila dipanaskan hingga suhu gelatinisasinya. Bahan-bahan sup krim yang dibuat dalam penelitian ini memiliki komposisi yang sama, selain konsentrasi mikrokapsul minyak ikan, termasuk tepung mocaf dan tepung jagung sebagai sumber pati.
Karakteristik kimia
Karakteristik kimia dianalisis meliputi kadar air, abu, protein, lemak, serta karbohidrat (by difference). Pengujian tersebut dilakukan terhadap tiga konsentrasi sup krim kepiting instan dengan mikrokapsul minyak ikan dan sup krim kepiting instan kontrol (Tabel 5).
Tabel 5 Karakteristik kimia sup krim kepiting instan dengan fortifikasi mikrokapsul kadar air sup krim instan menurut Badan Standardisasi Nasional 01-4321-1996, yang berkisar 2%-7%. Nilai kadar air yang rendah ini dapat mengurangi pertumbuhan mikroorganisme perusak sehingga mengakibatkan produk tepung sup krim instan memiliki daya tahan yang lebih lama. Menurut Sunyoto dan Futiawati (2012) bahan dengan kadar air kurang dari 8% dapat mengurangi pertumbuhan mikroorganisme dan reaksi kimia yang merusak, seperti hidrolisis dan oksidasi lemak.
Kadar abu menunjukkan besarnya kandungan mineral dalam bahan. Perbedaan konsentrasi mikrokapsul memberikan pengaruh secara nyata (p<0,05) terhadap kadar abu sup krim kepiting instan ( Lampiran 11). Hasil uji lanjut Duncan menunjukkan bahwa kadar abu sup krim instan saling berbeda nyata antar konsentrasi penambahan mikrokapsulnya. Semakin besar penambahan mikrokapsul minyak ikan, kadar abu dari sup krim instan semakin meningkat (Tabel 5). Kadar abu dari mikrokapsul yang ditambahkan pada penelitian ini adalah 1,88±0,00%. Dugaan peningkatan ini karena adanya kontribusi kandungan abu pada maltodekstrin dan gum arab yang digunakan sebagai bahan penyalut mikrokapsul. FAO (1990) menyebutkan bahwa kadar abu dari gum arab berkisar antara 2% sampai 4%, sedangkan nilai standar maltodekstrin sendiri menurut DSN (1992) adalah ≤0,5%.
Hasil analisis ragam menunjukkan bahwa penambahan konsentrasi mikrokapsul minyak ikan memberikan pengaruh yang nyata (p<0,05) terhadap kadar protein sup krim kepiting instan (Lampiran 11). Uji Duncan menunjukkan bahwa kadar protein sup dengan penambahan mikrokapsul minyak ikan konsentrasi 3,00% tidak berbeda nyata dengan konsentrasi 3,30%, namun berbeda nyata dengan konsentrasi 3,60% dan kontrol, serta berbeda nyata dengan kesemua penambahan konsentrasi mikrokapsul minyak ikan. Kadar protein sup krim kepiting instan meningkat dengan adanya penambahan mikrokapsul minyak ikan, meskipun kadarnya menurun seiring dengan tingkat penambahannya (Tabel 5). Penurunan kadar protein ini adalah akibat pengaruh nisbah antar komponen kimia yang dipengaruhi oleh penambahan mikrokapsul minyak ikan, seperti kenaikan kadar abu, air, dan lemak. Kenaikan kadar protein ini dipengaruhi oleh kandungan protein pada mikrokapsul. Hasil pengujian kadar protein yang terdapat pada mikrokapsul minyak ikan adalah 0,24±0,04%. Sementara itu, menurut Shahidi dan Han (1993) gum arab memiliki komponen protein 5%.
Hasil analisis ragam menunjukkan bahwa penambahan konsentrasi mikrokapsul minyak ikan memberikan pengaruh yang nyata (p<0,05) terhadap kadar lemak sup krim kepiting instan (Lampiran 11). Uji lanjut Duncan menunjukkan bahwa kadar lemak sup krim kepiting instan saling berbeda nyata antar konsentrasi penambahan mikrokapsulnya. Kadar lemak sup krim instan semakin meningkat seiring dengan peningkatan konsentrasi mikrokapsul minyak ikan (Tabel 5). Kadar lemak pada produk sup krim instan ini memiliki kadar lemak yang lebih tinggi dibandingkan Rubilar et al. (2012) mengenai sup krim instan dengan penambahan mikrokaspul minyak linseed dan kadar lemak yang disyaratkan oleh Badan Standardisasi Nasional (1996) berturut-turut yaitu 11,51% dan ≤10%. Tingginya kadar lemak sup krim kepiting instan ini diduga disebabkan oleh penambahan minyak jagung yang digunakan pada saat penumisan daging kepiting saat pembuatan sup krim sebelum pengeringan.
Penentuan kadar karbohidrat secara by difference menghasilkan perkiraan jumlah karbohidrat secara keseluruhan, baik karbohidrat sederhana maupun yang kompleks. Hasil analisis ragam menunjukkan bahwa penambahan konsentrasi mikrokapsul minyak ikan memberikan pengaruh yang berbeda (p<0,05) terhadap kadar karbohidrat sup krim kepiting instan (Lampiran 11). Berdasarkan hasil uji lanjut Duncan, kadar karbohidrat sup krim kepiting instan dengan konsentrasi mikrokapsul 3,00% tidak berbeda nyata dengan 3,30%, namun berbeda nyata dengan konsentrasi 3,60% dan kontrol. Semakin besar konsentrasi mikrokapsul yang digunakan, maka kandungan karbohidrat dari sup krim instan semakin menurun.
Formula Terbaik Sup Krim Kepiting Instan dengan Fortifikasi Mikrokapsul Minyak Ikan Kaya Omega-3
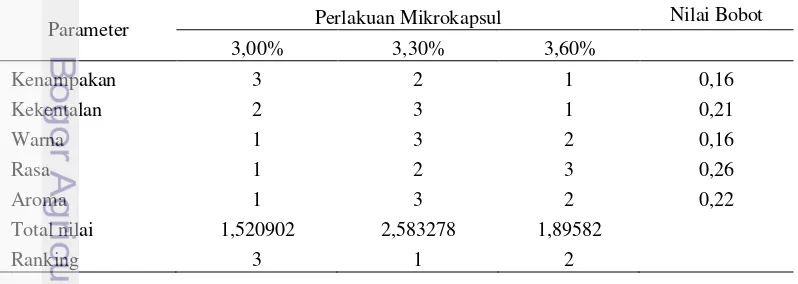
Formula terbaik sup krim kepiting instan yang difortifikasi mikrokapsul minyak ikan ditentukan berdasarkan hasil uji hedonik karakteristik sensori yang diolah dengan metode perankingan Bayes. Hasil analisis dengan metode Bayes dapat dilihat pada Tabel 6.
Tabel 6 Hasil perankingan formula terbaik dengan metode Bayes
Parameter Perlakuan Mikrokapsul Nilai Bobot
3,00% 3,30% 3,60%