EKSTRAKSI PROTEIN SERISIN DARI KOKON SUTERA
LIAR
Attacus atlas
DAN KARAKTERISASINYA
SEBAGAI BIOMATERIAL
YUNI CAHYA ENDRAWATI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
i
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Ekstraksi Protein Serisin dari Kokon Sutera Liar Attacus atlas dan Karakterisasinya sebagai Biomaterial adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juni 2012
ii
ABSTRACT
YUNI CAHYA ENDRAWATI. Sericin Protein Extraction from Attacus atlas Cocoon and Its Characterization as a Biomaterial. Under direction of DEDY DURYADI SOLIHIN and ANI SURYANI
The high sericin production is mostly determined by extraction method (degumming and serisin protein isolation). Sericin protein was extracted from silk wastewater by protein isolation with 75% (v/v) ethanol. Silk wastewaters was produced from degumming of cocoon Attacus atlas with 33,3% NaOH 0,25 N. Sericin protein extraction from Attacus atlas not only use a combination of temperature and time, but need a strong solvent for extracting sericin, strong bases such as NaOH. This research has been get the best extraction method to produce the highest sericin protein by optimization of protein extraction with response surface methodology (RSM). Stationary point at 129oC and 70,36 minute can produce maximum percentage of protein yields (± 19%). The molecular weight distribution of sericin was investigated by sodium dodecyl sulfate polyacrylamide gel electrophoresis (SDS PAGE). The results suggested that sericin represented wide ranging molecular weight distribution (8,24-73,30 kDa). The amino acid of sericin was investigated by high performance liquid chromatography (HPLC) analytical methods that result highest component of Attacus atlas sericin is glysine (24,64%). Amino acids of sericin contains polar groups (50,72%) and non polar groups (49,28%). Sericin has wide applications as a biomaterial in medical, pharmaceutical and cosmetic. One of them as a surfactant material with the ability to reduce water surface tension of 71,67 dyne/cm to 51,8 ± 1,3 dyne/cm on the sericin addition of 0,58 ± 0,01 mg/ml.
iii
RINGKASAN
YUNI CAHYA ENDRAWATI. Ekstraksi Protein Serisin dari Kokon Sutera Liar Attacus atlas dan Karakterisasinya sebagai Biomaterial. Dibimbing oleh DEDY DURYADI SOLIHIN dan ANI SURYANI
Serat sutera (fibroin) dihasilkan dari proses degumming kokon. Degumming adalah proses penguraian serat sutera (fibroin) dari bahan perekatnya yang disebut serisin (gum). Proses degumming kokon sutera menghasilkan larutan yang mengandung bahan organik tinggi (BOD 8219.6 mg/l) yang dapat memberikan dampak lingkungan kurang baik sehingga perlu pengolahan lebih lanjut. Pengolahan larutan hasil degumming dengan cara ekstraksi protein serisin dapat menurunkan kadar BOD hingga 86,7%. Hasil ekstraksi berupa protein serisin juga mempunyai manfaat luas sebagai biomaterial di berbagai bidang seperti dalam bidang medis dan kosmetik.
Metode ekstraksi protein serisin dari kokon dilakukan melalui degumming dan isolasi protein. Proses degumming dapat dilakukan dengan kombinasi fisik dan kimia pada suhu, waktu dan bahan pelarut kimia tertentu. Isolasi protein digunakan untuk mengisolasi protein target, salah satunya dengan cara pengendapan. Pada penelitian ini proses ekstraksi dilakukan secara bertahap untuk mendapatkan rendemen protein maksimal. Proses ekstraksi akan menghasilkan crude protein serisin. Kajian-kajian yang dilakukan adalah, 1) kajian pengaruh rasio volume NaOH 0,1 N dan jenis spesies ulat sutera terhadap rendemen protein serisin, 2) kajian pengaruh konsentrasi NaOH terhadap rendemen protein serisin, 3) kajian pengaruh kemurnian etanol terhadap rendemen protein serisin, dan 4) kajian optimasi rendemen protein serisin. Kajian optimasi menggunakan Response Surface Methodology (RSM) pada dua faktor yaitu suhu dan waktu. Titik pusat pada suhu 115oC dan waktu 40 menit. Ada tiga optimasi, yaitu optimasi 1 (O1) menggunakan 33,3% NaOH 0,25N dan etanol teknis 96%, optimasi 2 (O2) menggunakan 33,3% NaOH 0,25N tanpa etanol, dan optimasi 3 (O3) menggunakan etanol teknis 96% tanpa NaOH. Tahap terakhir dari penelitian ini adalah karakterisasi crude protein serisin dengan analisis bobot molekul menggunakan Sodium Dodecyl Sulphate Polyachrylamide Gel Electrophoresis (SDS PAGE), analisis asam amino dengan High Performance Liquid Chromatography (HPLC) dan uji tegangan permukaan dengan tensiometer.
Teknik pengendapan dengan etanol absolut dipakai dalam proses isolasi protein (Wu et al. 2007). Akan tetapi etanol absolut kurang efisien jika diterapkan dalam skala industri karena harganya cukup mahal. Perlu ada kajian tentang alternatif lain sebagai pengganti etanol absolut. Kajian isolasi protein pada tingkat kemurnian etanol berbeda dilakukan di awal penelitian ini untuk memberikan informasi tersebut. Pada kajian kemurnian etanol, etanol absolut dan etanol teknis 96% tidak berpengaruh nyata (P>0,05) terhadap rendemen protein serisin. Rendemen protein yang dihasilkan sebesar 1,03 ± 0,04% untuk etanol absolut dan 1,00 ± 0,16% untuk etanol teknis, sehingga etanol teknis 96% akan digunakan pada isolasi protein selanjutnya.
iv serisin. Hal ini menunjukkan bahwa degumming dengan rasio volume 50% dan 33,3% NaOH 0,1 N terhadap larutan tidak mempunyai pengaruh yang nyata pada rendemen protein serisin yang dihasilkan, sehingga volume 33,3 NaOH 0,1 N akan digunakan dalam kajian selanjutnya. Jenis spesies ulat sutera sangat berpengaruh terhadap rendemen protein serisin yang dihasilkan. Bombyx mori menghasilkan rendemen protein lebih tinggi dibanding Attacus atlas pada perlakuan ekstraksi yang sama, yaitu masing-masing sebesar 27%-32% dan 3%-4%. Hal ini berarti bahwa tahap ekstraksi yang dilakukan pada kajian ini belum dapat mengekstraksi protein serisin dari kokon Attacus atlas secara maksimal. Serat sutera Attacus atlas diduga lebih kuat dan lebih sulit diekstraksi serisinnya dibandingkan dengan Bombyx mori, karena makanan Attacus atlas mengandung tanin yang dapat mengikat protein dengan ikatan yang kuat (Hagerman 2002).
Tahap kajian selanjutnya adalah pengaruh konsentrasi NaOH terhadap rendemen protein serisin. Hasil analisis ragam berbeda nyata (P<0,05) pada konsentrasi NaOH 0,25-0,30 N dengan rendemen protein sekitar 11,69%-11,84%. Akan tetapi pada konsentrasi NaOH 0,30 N, fibroin terlihat mengalami kerusakan sehingga konsentrasi NaOH 0,25 N yang akan dipakai dalam kajian selanjutnya.
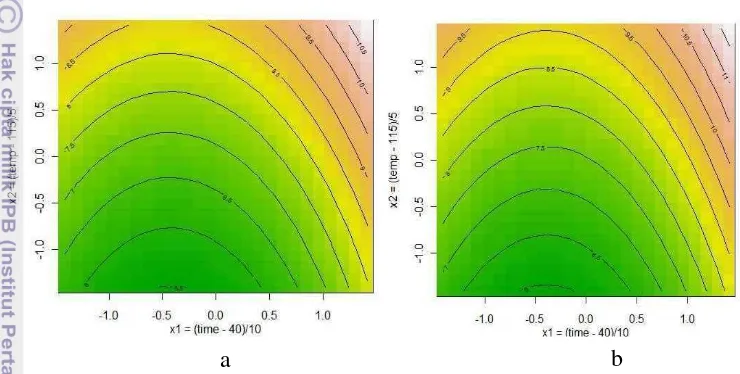
Optimasi terhadap variabel bebas suhu dan waktu (variabel bebas) dilakukan karena respon diduga belum optimum. Ada tiga optimasi dengan masing-masing dibagi dalam dua kelompok yaitu dengan dan tanpa air dalam fibroin basah (AFB). Respon terbaik ditunjukkan optimasi 2 (O2) menggunakan 33,3% NaOH 0,25 N tanpa etanol. Titik optimumnya tercapai pada suhu 129oC dan waktu 70,36 menit, dengan tipe optimasi maksimum. Hal ini berarti respon maksimum tercapai pada titik optimumnya, atau rendemen protein maksimal tercapai pada suhu dan waktu optimum. Penambahan AFB pada semua perlakuan menghasilkan respon yang lebih baik dibanding tanpa penambahan AFB.
Analisis bobot molekul dengan SDS PAGE secara keseluruhan menghasilkan tujuh fragmen bobot molekul protein serisin A. atlas dengan kisaran 8,24-73,30 kDa pada separating gel 12,5% dan stacking gel 4%. Lima fragmen pada kelenjar sutera Attacus atlas dengan kisaran bobot molekul (BM) 8,99-73,3 kDa, tiga fragmen pada crude protein serisin A. atlas dengan kisaran BM 8,24-10,25 kDa, dan dua fragmen pada crude protein serisin B. mori dengan kisaran BM 8,24-8,99 kDa. Teknik ekstraksi pada penelitian ini menyebabkan molekul protein serisinnya menjadi kecil karena adanya perlakuan basa kuat yang menyebabkan asam amino unit pembangunnya dibebaskan dari ikatan kovalen sehingga membentuk molekul yang relatif kecil. Hal ini ditunjukkan dengan munculnya fragmen bobot molekul kecil (8,24-10,25 kDa) dan tidak munculnya fragmen bobot molekul besar (34,86-73,30 kDa).
v tinggi kadar protein serisin yang ditambahkan maka semakin kecil tegangan permukaan yang dihasilkan.
vi
© Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan kutipan tersebut tidak merugikan kepentingan yang wajar IPB
vii
EKSTRAKSI PROTEIN SERISIN DARI KOKON SUTERA
LIAR
Attacus atlas
DAN KARAKTERISASINYA
SEBAGAI BIOMATERIAL
YUNI CAHYA ENDRAWATI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Biosains Hewan
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
ix Judul Tesis : Ekstraksi Protein Serisin dari Kokon Sutera Liar Attacus atlas
dan Karakterisasinya sebagai Biomaterial Nama : Yuni Cahya Endrawati
NIM : G352100081
Disetujui
Komisi Pembimbing
Dr. Ir. Dedy Duryadi Solihin, DEA Prof. Dr. Ir. Ani Suryani, DEA
Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Biosains Hewan
Dr. Bambang Suryobroto Dr. Ir. Dahrul Syah, MSc.Agr
x
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan November 2011 sampai Maret 2012 ini ialah ekstraksi protein serisin, dengan judul Ekstraksi Protein Serisin dari Kokon Sutera Liar Attacus atlas dan Karakterisasinya sebagai Biomaterial.
Terima kasih penulis ucapkan kepada Bapak Dr. Ir. Dedy Duryadi Solihin, DEA dan Ibu Prof. Dr. Ir. Ani Suryani, DEA selaku pembimbing, serta Dr. Ir. Dwi Setyaningsih, MSi. yang telah banyak memberi saran. Di samping itu, penghargaan penulis sampaikan kepada Ibu Ir. Rini Purwanti, M.Si dari Laboratorium Proses Departemen Teknologi Industri Pertanian, Ibu Devi Murtini, S.Pt dan saudari Febri dari Laboratorium Terpadu Departemen Ilmu Produksi dan Teknologi Peternakan, yang telah banyak membantu selama pengumpulan data. Terimakasih juga kepada seluruh teman-teman BSH 2010, staf dan pegawai Laboratorium Non Ruminansia dan Satwa Harapan yang banyak memberikan dukungan dan semangat. Ungkapan terimakasih juga disampaikan kepada suami, anak, bapak, ibu dan seluruh keluarga atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini menjadi jalan pembuka kebangkitan Persuteraan Indonesia.
Bogor, Juni 2012
xi RIWAYAT HIDUP
Penulis dilahirkan di Temanggung pada tanggal 9 November 1982 dari bapak Matnur dan ibu Endang Irawati. Penulis merupakan anak pertama dari dua bersaudara. Penulis juga merupakan istri dari bapak Antonius Hartono, ST dan ibu dari Axella Negyacahya Hartono.
Pada tahun 2000 penulis lulus dari SMA Negeri 1 Temanggung dan melanjutkan kuliah S1 di IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis masuk pada Program Studi Teknologi Produksi Ternak, Departemen Ilmu Produksi Ternak, Fakultas Peternakan IPB.
xii
Manfaat dan Aplikasi Serisin ………. 8
Ekstraksi Protein Serisin ………. 9
Karakterisasi Protein Serisin ……….. 11
Response surface methodology………... 14
BAHAN DAN METODE Ekstraksi Protein Serisin dari Kelenjar Sutera Tengah Attacus atlas (KSA) ………. 16
Kajian Pengaruh Rasio Volume NaOH 0,1 N dan Jenis Spesies Ulat Sutera terhadap Rendemen Protein Serisin ……… 17
Kajian Pengaruh Konsentrasi NaOH terhadap Rendemen Protein Serisin ………. 18
Kajian Pengaruh Kemurnian Etanol terhadap Rendemen Protein Serisin ………. 19
Kajian Optimasi Rendemen Protein Serisin ………... 20
Analisis Protein ……….. 22
Analisis Fibroin ……….. 22
Analisis Bobot Molekul (BM) ……… 23
Analisis Asam Amino ………. 23
Uji Tegangan Permukaan (Surface tension) ………... 24
HASIL DAN PEMBAHASAN Kajian Pengaruh Kemurnian Etanol terhadap Rendemen Protein Serisin Attacus atlas ………... 26
Kajian Pengaruh Rasio Volume NaOH 0,1 N dan Jenis Spesies Ulat Sutera terhadap Rendemen Protein Serisin ……… 27
Kajian Pengaruh Konsentrasi NaOH terhadap Rendemen Protein Serisin Attacus atlas ………... 29
Optimasi Rendemen Protein Serisin ………... 31
Bobot Molekul Protein Serisin (BM) ………. 37
Komposisi Asam Amino Protein Serisin ……… 40
Prospek Kedepan Protein Serisin sebagai Biomaterial ………. 41
KESIMPULAN DAN SARAN ……… 44
DAFTAR PUSTAKA ……….. 45
xiii DAFTAR TABEL
Halaman 1 Persentase asam amino protein serisin Bombyx mori dengan
ekstraksi berbeda (Aramwit et al. 2010) ………. 7 2 Persentase asam amino serisin dari beberapa spesies berbeda ……... 8
3 Tegangan permukaan berbagai cairan (Wikipedia 2012) …………... 14
4 Tabulasi data kajian pengaruh rasio NaOH 0,1 N dan jenis spesies ulat sutera terhadap rendemen protein serisin ……… 18
5 Tabulasi data kajian pengaruh variasi konsentrasi NaOH terhadap
rendemen protein serisin ………. 19
6 Tabulasi data kajian pengaruh kemurnian etanol terhadap rendemen protein serisin ………... 20 7 Desain rancangan percobaan dengan central composite design……. 21
8 Markerdari Fermentas Multicolor Broad Range Protein Ladder …. 23
9 Tabulasi data tegangan permukaan crude protein serisin …………... 25 10 Hasil kajian pengaruh kemurnian etanol terhadap rendemen protein
serisin ………... 26
11 Rendemen protein serisin hasil perlakuan rasio volume NaOH 0,1 N
dan jenis spesies ulat sutera ……… 28
12 Rendemen protein pada konsentrasi NaOH berbeda ……….. 30 13 Bobot molekul protein serisin hasil SDS PAGE (separating gel
12,5%, stacking gel 4%, Marker Fermentas Multicolor Broad
Range Protein Ladder 10-260 kDa) ………... 39
14 Komposisi asam amino protein serisin pada spesies yang berbeda … 41
xiv DAFTAR GAMBAR
Halaman
1 Siklus hidup Attacus atlas (Solihin & Fuah 2010) ………. 4
2 Kelenjar sutera (Brasla & Matei 1997) ………... 6
3 Skema susunan protein sutera (Gulrajani et al. 2008) ……… 8
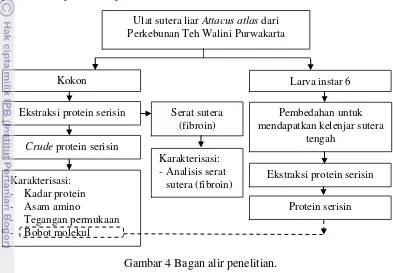
4 Bagan alir penelitian ………... 16
5 Penampang fibroin Attacus atlas hasil ekstraksi pada suhu 105oC selama 30 menit dengan, a) isolasi etanol absolut dan b) isolasi etanol teknis pada pembesaran 400 kali ………. 27
6 Penampang fibroin Attacus atlas (a. 50% NaOH 0,1 N; b. 33,3% NaOH 0,1 N), dan Bombyx mori (c. 50% NaOH 0,1 N; d. 33,3% NaOH 0,1 N) dengan 400 kali pembesaran ……… 29
7 Penampang fibroin Attacus atlas dengan 1000 kali pembesaran (a. 33,3% NaOH 0,05 N; b. 33,3% NaOH 0,10 N; c. 33,3% NaOH 0,15 N; d. 33,3% NaOH 0,20 N; e. 33,3% NaOH 0,25 N; f. 33,3% NaOH 0,30 N) ……… 31
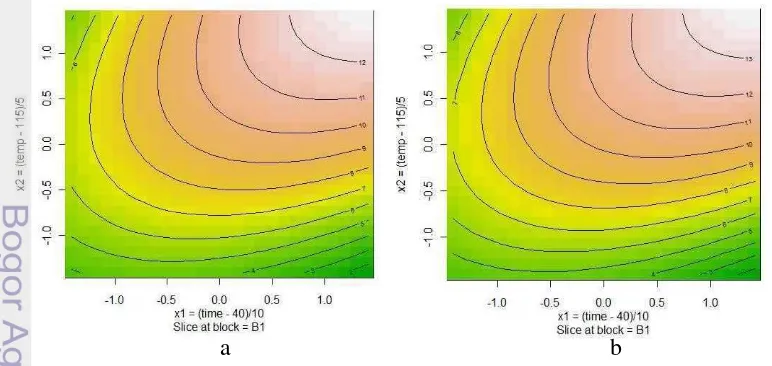
8 Kontur rendemen protein serisin (33,3% NaOH 0,25 N, berbagai suhu dan waktu, 75%(v/v) etanol 96%), a) tanpa AFB dan b) dengan AFB ……… 33
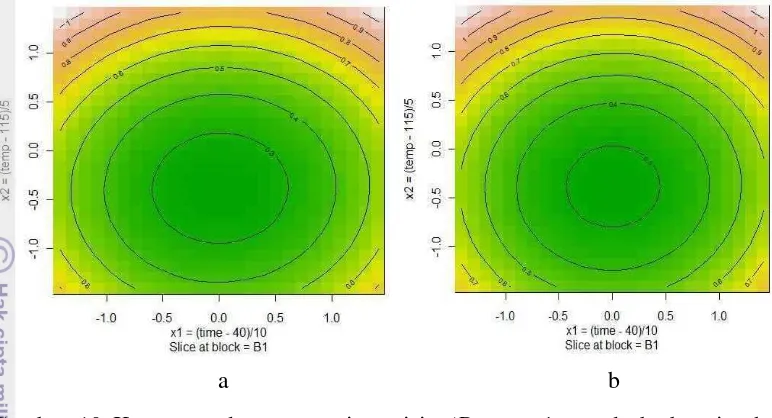
9 Kontur rendemen protein serisin (Degumming dengan 33,3% NaOH 0,25 N pada berbagai suhu, tekanan dan waktu tertentu), a) tanpa AFB dan b) dengan AFB ……… 34
10 Kontur rendemen protein serisin (Degumming pada berbagai suhu, tekanan dan waktu tertentu serta 75% (v/v) etanol teknis 96%), a) tanpa AFB dan b) dengan AFB ……….. 36
11 Rata-rata rendemen protein pada kajian optimasi teknik ekstraksi … 37
xv DAFTAR LAMPIRAN
Halaman 1 Tahapan ekstraksi protein serisin dari kelenjar sutera tengah Attacus
atlas (Invitrogen 2012) ………... 50
2 Preparasi sampel dan ekstraksi protein serisin dari kulit kokon
(Solihin & Fuah 2010) ……… 51
3 Tahapan uji tegangan permukaan ………... 53
4 Analisis ragam pengaruh kemurnian etanol terhadap rendemen
protein serisin ……….. 54
5 Analisis ragam pengaruh rasio volume NaOH 0,1 N dan jenis spesies terhadap rendemen protein serisin ……… 55
6 Analisis ragam pengaruh konsentrasi NaOH terhadap rendemen
protein serisin ……….. 56
7 Rendemen protein serisin pada optimasi 1 ………..………... 57
8 Analisis response surface methodology (RSM) pada optimasi 1
11 Rendemen protein serisin pada optimasi 2 ………... 61
12 Analisis response surface methodology (RSM) pada optimasi 2
15 Rendemen protein serisin pada optimasi 3 ………... 65 16 Analisis response surface methodology (RSM) pada optimasi 3
19 Kurva standar marker bobot molekul pada separating gel 12,5% dan
stacking gel 4% ………... 69
20 Perhitungan bobot molekul sampel ……… 70
xvi Halaman 22 Kromatogram analisis asam amino dengan hidrolisis basa ………… 72 23 Analisis ragam uji tegangan permukaan larutan dengan kadar
1
PENDAHULUAN
Latar Belakang
Bangsa Cina telah mengenal kain sutera sejak lama dan komoditas tersebut mulai menyebar luas melalui jalur perdagangan yang dikenal dengan nama “Jalur Sutera”. Kain sutera merupakan komoditas berkualitas tinggi dari tenunan (tradisional maupun modern) serat hasil pengokonan ulat sutera. Ada dua macam
ulat sutera, yaitu ulat sutera murbei dan non murbei. Ulat sutera murbei makan
daun murbei, contoh spesiesnya adalah Bombyx mori, sedangkan ulat sutera non
murbei (ulat sutera liar) jumlahnya cukup banyak diantaranya adalah Attacus
atlas, Cricula trifenestrata dan Antheraea spp. Ulat sutera liar ini termasuk jenis
polifagus, yaitu memakan banyak jenis makanan. Peigler (1989), jenis makanan
yang dapat dikonsumsi Attacus atlas sebanyak 90 genus tumbuhan dari 48 famili.
Beberapa ulat sutera liar dapat ditemukan di Indonesia, diantaranya Attacus atlas
dan Cricula trifenestrata. Hal ini kemungkinan karena sumber makanan dapat
tersedia sepanjang tahun di Indonesia.
Ulat sutera murbei maupun non murbei mempunyai siklus hidup sempurna
(metamorfosis holometabola) yaitu telur, larva (ulat), imago (ngengat) dan pupa.
Secara umum fase pupa merupakan fase yang bernilai ekonomis karena pada fase
ini kokon terbentuk dan selanjutnya dapat dimanfaatkan sebagai bahan dasar kain
sutera. Kain sutera banyak dikenal orang karena keunggulannya, diantaranya
karena sifatnya yang mudah menyerap keringat, anti mikroba, mengkilat, halus
(Sihombing 1999, Faatih 2005), eksotik, benang yang panjang, lembut, tidak
mudah kusut, tahan panas, dan tidak menimbulkan rasa gatal (Sutera Indonesia
2004).
Perkembangan zaman telah mengubah paradigma tentang sutera. Kokon ulat
sutera tidak lagi hanya dimanfaatkan sebagai bahan kain sutera (tekstil) namun
sudah mulai dimanfaatkan di berbagai bidang seperti kosmetik dan medis
(Padamwar & Pawar 2004) dengan memanfaatkan protein penyusun kokon yaitu
fibroin dan serisin (Fabiani et al. 1996). Fibroin adalah protein serat sedangkan
serisin merupakan perekatnya. Serisin membungkus filamen yang sangat kecil
(serat fibroin) pada kokon, bobotnya 20-30% dari bobot total kokon (Masahiro et
2 besar merupakan kelompok senyawa polar kuat seperti senyawa yang
mengandung gugus hidroksil, karboksil, dan kelompok amino (Wei et al. 2005).
Banyak penelitian terkait dengan protein sutera terutama serisin pada
Bombyx mori. Mulai dari cara ekstraksi, kerja gen serisin dan bahkan
pemanfaatannya sebagai biomaterial di bidang medis dan kosmetik. Hal ini
bermula dari melimpahnya hasil ikutan industri pengolahan kokon yang belum
bisa dimanfaatkan. Hasil ikutan tersebut menjadi masalah lingkungan yang cukup
serius karena mengandung bahan organik tinggi (BOD 8219.6 mg/l) sehingga
perlu pengolahan lebih lanjut. Gulrajani et al. (2008) menyatakan bahwa
pengolahan dengan cara ekstraksi protein serisin dapat menurunkan kadar BOD
hingga 86,7%.
Protein serisin mempunyai potensi tinggi sebagai biomaterial. Dalam bidang
kosmetik, protein serisin dapat digunakan sebagai cream dan lotion pada kulit
karena dapat meningkatkan elastisitas kulit, mencegah kekerutan dan penuaan dini
(Padamwar & Pawar 2004). Dalam medis, protein serisin dapat digunakan untuk
menyembuhkan luka dan menghambat penyebaran tumor (Zhaorigetu et al. 2003, Aramwit & Sangcakul 2007). Masakazu et al. (2003) menemukan bahwa aktivitas
serisin secara biologis dapat mencegah terbentuknya sel mati dan merangsang
pertumbuhan sel baru.
Hasil-hasil penelitian tentang serisin masih terbatas pada spesies Bombyx
mori. Hal ini karena sebagian besar industri pengolahan kokon menggunakan
kokon Bombyx mori sebagai bahan dasar, tidak terkecuali di Indonesia. Akan
tetapi selain Bombyx mori, Indonesia juga mempunyai potensi ulat sutera liar
Attacus atlas yang dapat dikembangkan lebih lanjut. Attacus atlas mempunyai
sifat polivoltin (banyak generasi dalam satu tahun), polifagus dan bobot kokon
yang relatif lebih besar dari kokon Bombyx mori. Bobot kokon Bombyx mori 1,5 – 2,5 g (Atmosoedarjo et al. 2000) sedangkan bobot kokon Attacus atlas sekitar 9 g (Solihin & Fuah 2010). Komposisi serat kokon Bombyx mori dan Attacus atlas
sama yaitu terdiri dari protein fibroin dan serisin, akan tetapi karakteristik
spesifiknya belum diketahui. Oleh karena itu perlu penelitian lebih lanjut
mengenai protein serisin pada Attacus atlas agar potensi dan pemanfaatannya
3 Protein serisin dapat diisolasi dari hasil ikutan (larutan) dari pengolahan
kokon (proses degumming) karena serisin merupakan protein larut air yang diduga
terlarut dalam hasil ikutan tersebut. Akan tetapi Indonesia belum mempunyai
industri pengolahan sutera Attacus atlas sehingga perlu adanya studi lebih lanjut
tentang teknik degumming yang dapat menghasilkan rendemen protein serisin
tertinggi dengan hasil fibroin yang masih baik juga. Hal ini selaras dengan tujuan
awal dari pengolahan kokon yaitu mendapatkan kualitas fibroin yang baik. Proses
degumming kokon Attacus atlas akan merujuk pada Aini (2009) dan Suriana
(2011).
Karakterisasi protein serisin dari Attacus atlas sangat diperlukan untuk
mengetahui sifat protein tersebut. Hal ini diperlukan dalam proses pemurnian
protein dan pemanfaatannya lebih lanjut di berbagai bidang terutama sebagai
biomaterial.
Tujuan
Penelitian ini bertujuan untuk:
- Menghasilkan teknik ekstraksi protein serisin dari kokon Attacus atlas
dengan rendemen protein serisin tertinggi
4
TINJAUAN PUSTAKA
Attacus atlas
Attacus atlas digolongkan sebagai ulat sutera liar yang dapat menghasilkan
serat sutera. Klasifikasi Attacus atlas, masuk dalam kelas insekta, ordo
lepidoptera, famili saturniidae, genus Attacus, dan spesies Attacus atlas (Solihin
& Fuah 2010). Attacus atlas merupakan serangga holometabola seperti halnya
Bombyx mori, yaitu serangga yang mengalami metamorfosis sempurna dengan
siklus hidup dimulai dari fase telur, larva (ulat), pupa dan imago (ngengat)
(Solihin & Fuah 2010, Peigler 1989). Perbedaan siklus hidup ulat sutera liar dan
domestikasi terletak pada jumlah instar dalam fase larva, Attacus atlas mengalami
enam instar sedangkan Bombyx mori lima instar. Attacus atlas pertama kali
ditemukan di Indonesia dan penyebarannya mulai dari Nanggroe Aceh
Darussalam (NAD) hingga ke Papua (Peigler 1989, Mahendran et al. 2006).
Gambar 1 Siklus hidup Attacus atlas (Solihin & Fuah 2010).
Ulat sutera liar Attacus atlas mempunyai banyak keunggulan karena
sifatnya yang polifagus yaitu dapat memakan banyak sumber makanan, dapat
memakan 90 genus tanaman dari 48 famili, dan polivoltin yaitu mengalami
beberapa generasi dalam satu tahun (Peigler 1989). Beberapa diantaranya adalah
5
sinensis), kina (Chincoma siccirubra), dadap (Erythrina sp.), mangga (Mangifera
indica L), jeruk (Citrus sp.), alpukat (Persea americana) dan lada (Piper sp.)
(Solihin & Fuah 2010). Daun teh segar mempunyai komposisi diantaranya
polipenol, kafein, asam amino, karbohidrat dan abu. Polifenol merupakan molekul
autoflouresence yang dapat menghasilkan warna sendiri seperti pada lignin dan
autoxidation seperti fenomena non enzymatic browning pada wortel. Polifenol
adalah komponen terbesar dari daun teh diantaranya seperti katekin dan tanin.
Tanin merupakan komponen sekunder dalam metabolisme yang dapat berinteraksi
dengan protein dengan cara mengendapkannya (Hagerman 2002). Fenomena ini
dimanfaatkan untuk penyamakan kulit dan pengawetan kayu karena tahan
terhadap rayap dan jamur (Risnasari 2002).
Kelenjar Sutera
Kelenjar sutera adalah kelenjar penghasil serat sutera yang merupakan organ
terbesar kedua dalam tubuh ulat sutera (Brasla & Matei 1997). Pada larva instar
akhir (instar kelima pada Bombyx mori dan instar keenam pada Attacus atlas),
kelenjar sutera menempati sebagian besar ventral lateral dari tubuh larva untuk
persiapan proses pembentukan kokon. Kelenjar sutera terbagi dalam tiga bagian
yaitu,
1. Kelenjar sutera posterior
Kelenjar ini berfungsi mensintesis serat sutera (fibroin). Kelenjar ini
membentuk lapisan di sekeliling posterior dari usus tengah sehingga kelenjar
posterior ini sangat panjang dan berputar-putar dengan ketebalan yang
seragam.
2. Kelenjar sutera bagian tengah
Kelenjar ini berada diantara kelenjar posterior dan anterior. Pada kelenjar
bagian tengah inilah protein serisin disekresikan.
3. Kelenjar sutera anterior
Kelenjar anterior merupakan saluran tipis yang berperan dalam penggulungan
protein sutera. Kelenjar anterior mempunyai tiga bagian yaitu depan, tengah
dan belakang. Bagian depan diawali dengan tipis kemudian menebal, bagian
tengah sangat tebal sedangkan bagian belakang mulanya tebal kemudian
6 Proses pembentukan filamen sutera dimulai dari sekresi protein di kelenjar
sutera dan ekskresi filamen pada spineret. Menurut Atmosoedarjo et al. (2000),
serat sutera terdiri dari protein serisin dan fibroin. Kedua protein ini saling
bergabung menghasilkan serat yang dikeluarkan oleh spineret dan telah dilapisi
lilin dari kelenjar filipi. Larva mengeluarkan cairan dengan merentang dan
menggelengkan kepala sampai spineret menyentuh titik yang lain. Gerakan
membentang dari kedua titik menghasilkan cairan menjadi serat. Gerakan ini
dilakukan secara berulang-ulang sehingga membentuk filamen yang panjang.
Filamen dikeluarkan larva untuk persiapan perlindungan pada fase pupa. Produk
filamen ini berupa kokon. Gambar 2merupakan gambar kelenjar sutera.
Gambar 2 Kelenjar sutera (Brasla & Matei 1997)
Protein Serisin
Serat sutera alami terdiri dari dua jenis protein yaitu fibroin dan serisin
(Fabiani et al. 1996). Protein fibroin merupakan protein serat sedangkan serisin
merupakan perekatnya. Informasi mengenai serisin masih terbatas pada protein
serisin Bombyx mori sehingga rujukan sebagian besar berasal dari jenis ulat sutera
domestikasi tersebut. Serisin membungkus filamen yang sangat kecil yaitu serat
fibroin pada kokon, bobotnya 20-30% dari bobot total kokon (Masahiro et al.
2000). Serisin merupakan jenis protein globular yang larut dalam air.
Protein tersusun dari asam amino dengan urutan yang khas (Lehninger
1982). Protein serisin Bombyx mori terdiri dari 18 jenis asam amino yang
sebagian besar merupakan kelompok senyawa polar kuat seperti senyawa yang
mempunyai gugus hidroksil, karboksil dan amino (Wei et al. 2005). Serisin dari
7
et al. 2003), akan tetapi Wu et al. (2007) menyatakan hasil serina sebesar 27,3%,
asam aspartat 18,8%, glisina 10,7% dan sedikit mengandung sistin 0,3% serta
triptofan 0,4%. Serisin merupakan protein dengan permukaan hidrofilik 70% dan
hidrofobik 30%. Ekstraksi protein serisin yang berbeda akan menghasilkan
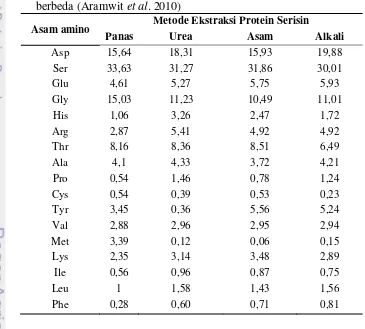
persentase asam amino yang berbeda pula (Tabel 1) (Aramwit et al. 2010).
Persentase asam amino protein serisin pada beberapa spesies berbeda ditampilkan
pada Tabel 2.
Tripoulas & Samols (1986) menyatakan bahwa RNA serisin melimpah pada
instar akhir yaitu instar 5, berbeda dengan RNA fibroin yang berlimpah sama
pada instar 4 dan 5 pada Bombyx mori. Okamoto et al. (1982), fibroin diproduksi
dibagian posterior kelenjar sutera sedangkan serisin dibagian tengah kelenjar
sutera.
Tabel 1 Persentase asam amino protein serisin Bombyx mori dengan ekstraksi berbeda (Aramwit et al. 2010)
Asam amino Metode Ekstraksi Protein Serisin
8 Tabel 2 Persentase asam amino serisin dari beberapa spesies berbeda
Asam amino
Gambar 3 Skema susunan protein sutera (Gulrajani et al. 2008)
Manfaat dan Aplikasi Serisin
Kosmetik
Kato et al. (1998) menyatakan serisin dapat menekan peroksidasi lemak,
menghambat aktifitas tirosinase secara in vitro (polifenol oksidase) dan membantu
aktifitas antioksidan pada kelompok senyawa yang mempunyai hidroksil.
Tirosinase adalah proses yang bertanggungjawab terhadap biosintesis melanin
kulit, sehingga serisin dapat dipergunakan dalam dunia kosmetik. Protein serisin
9 antioksidan, anti apoptotik dan anti inflamasi (Dash et al. 2008). Protein serisin
dapat digunakan sebagai cream dan lotion pada kulit karena dapat meningkatkan
elastisitas kulit, mencegah kekerutan dan penuaan dini (Padamwar & Pawar
2004). Padamwar et al. (2005), penggunaan serisin pada kulit dapat menurunkan
nilai transepidermal water loss (TEWL). TEWL adalah salah satu penyebab kulit
kering. Menurunnya nilai TEWL menyebabkan kadar air kulit terjaga karena tidak
terjadi kehilangan air pada lapisan kulit terluar sehingga tektur kulit menjadi lebih
halus. Hal ini menyebabkan kulit lebih elastis dan tidak mudah berkerut.
Medis
Masahiro et al. (2000) menyatakan bahwa serisin dapat meningkatkan
kemampuan secara biologis Zn, Fe, Mg and Ca pada tikus dan disarankan untuk
industri makanan karena mempunyai komposisi bahan alami penting. Serisin
dapat dipergunakan untuk menghambat aktifitas radiasi UV yang menimbulkan
bahaya akut pada tumor dengan menurunkan tekanan oksidatif pada kulit tikus
yang tidak berambut. Masakazu et al. (2003) menemukan bahwa aktifitas serisin
secara biologis dapat mencegah sel mati dan merangsang pertumbuhan sel baru.
Protein serisin dapat digunakan untuk menyembuhkan luka dan menghambat
penyebaran tumor (Zhaorigetu et al. 2003, Aramwit & Sangcakul 2007).
Ekstraksi Protein Serisin
Ekstraksi serisin dari hasil ikutan berupa air rebusan kokon perlu dilakukan
karena menyebabkan polusi dengan tingkat COD (Chemical Oxygen Demand)
dan BOD (Biological Oxygen Demand) tinggi. Protein serisin sebesar 6% per
tahun dapat dihasilkan dari ekstraksi air rebusan kokon Bombyx mori (Gulrajani et
al. 2008). Ekstraksi protein serisin dapat menurunkan kadar COD sebesar 8870
mg/l menjadi 260 mg/l dan BOD sebesar 4840 mg/l menjadi 158 mg/l
(Vaithanomsat et al. 2008).
Ada beberapa teknik ekstraksi serisin yang sudah dilakukan oleh para
peneliti. Teknik ekstraksi terdiri dari degumming dan isolasi protein. Aini (2009)
menyatakan bahwa degumming dengan penambahan NaOH 2 g/l (0,05 N), teepol
2 cc/l, sabun netral 2 g/l pada perebusan kokon Attacus atlas pada suhu 80oC
selama 2 jam akan menghasilkan karakter serat sutera yang lebih baik dari sisi
10
degumming yang menghasilkan fibroin terbaik Cricula trifenestrata (Suriana
2011). Metode Kato (2000) yaitu kokon Attacus atlas mula-mula dicelupkan ke
dalam air hangat dengan suhu sekitar 40oC untuk memisahkan partikel asing.
Kokon kemudian dicelupkan dalam air panas dengan suhu 95-98 oC, dan
selanjutnya direbus dalam larutan Na2CO3 2 g/l pada suhu 98-100 oC selama 3
jam. Kokon kemudian dicuci menggunakan air panas dengan suhu 95-98 oC,
kemudian dicuci kembali dengan air hangat pada suhu sekitar 40 oC. Kokon
diisolasi dengan etanol selama 5 hari sebelum digunakan untuk analisis
karakteristik seratnya. Metode yang dikerjakan Cui et al. (2009) dalam
mengekstraksi serisin kasar dari kokon Bombyx mori adalah dengan penambahan
metanol (70% v/v perbandingan terhadap air) yang kemudian didiamkan pada
suhu 25oC selama 10 hari. Hal ini untuk menghilangkan pigmen dan komponen
non organik. Tahap selanjutnya adalah perebusan kokon pada suhu 98oC selama 2
jam dengan penambahan 0,5% Na2CO3.Padamwar & Pawar (2004) menyatakan
bahwa ekstraksi kokon Bombyx mori dengan autoklaf pada suhu 105oC selama 30
menit akan menghasilkan properti gel dan rendemen yang baik.
Proses isolasi protein serisin yang berkembang pada dekade ini adalah
menggunakan pelarut organik dan membran filtrasi. Metode isolasi protein serisin
yang dilakukan Wu et al. (2007) adalah dengan menambahkan etanol absolut
dingin (-18 oC) kedalam air rebusan hasil degumming. Etanol bersifat semi polar
dengan gugus hidroksil yang dapat melarutkan beberapa senyawa ionik seperti
sodium dan potasium hidroksida dan magnesium klorit (Shakhashiri 2009).
Penambahan etanol absolut dilakukan sedikit demi sedikit sampai 75% (v/v)
perbandingan dengan volume air rebusan hasil degumming, selanjutnya
didiamkan semalaman pada suhu (-18 oC). Campuran serisin dan etanol kemudian
disentrifugasi selama 20 menit pada 3500 rpm (rotate per minute). Tahap akhir
adalah pengeringbekuan larutan dengan freeze drying. Gulrajani et al. (2008)
memurnikan protein serisin dengan membran filtrasi. Metode tersebut diawali
dengan sentrifugasi larutan hasil degumming pada 9000 rpm selama 60 menit.
Supernatan yang terbentuk akan dibuang sedangkan endapannya akan disaring
menggunakan filtrasi Wattman filter grade 1 (11 µm). Tahap selanjutnya adalah
11
drying dengan suhu inlet 180oC dan atomisasi 3 kg/cm2. Metode lain yang
menggunakan membran filtrasi adalah Cui et al. (2009), tahap pertama air rebusan
hasil degumming disimpan pada suhu 25oC selama 2 hari. Larutan tersebut
kemudian difiltrasi dengan filtrasi kertas nomor 1, selanjutnya didialisis pada
molecular weigth cut off (MWCO) 10.000 membran selama 3 hari. Isolat
kemudian dikeringbekukan dengan lyophilization.
Karakterisasi Protein Serisin
Karakterisasi sifat kimia dari protein serisin sangat berguna untuk aplikasi
serisin selanjutnya. Protein serisin dapat diekstraksi dari kokon (melalui proses
degumming) dan kelenjar sutera tengah. Degumming menggunakan bahan
pengurai seperti sabun, NaOH atau Na2CO3, sedangkan ekstraksi kelenjar sutera
menggunakan reagen tissue extraction. Beberapa sifat kimia dari protein serisin
adalah:
a. Kelarutan
Serisin dapat dibedakan berdasarkan kelarutannya, Padamwar & Pawar
(2004) membaginya menjadi serisin A, serisin B dan serisin C. Serisin A
merupakan lapisan terluar (outermost layer), tidak larut dalam air panas, dan
mengandung 17,5% nitrogen dan asam amino seperti serina, treonin, glisina dan
asam aspartat. Serisin B adalah lapisan tengah (middle layer), pada hidrolisis
asam akan menghasilkan asam amino serisin A dan triptofan serta mengandung
16,8% nitrogen. Hidrolisis adalah reaksi kimia yang memecah molekul air
menjadi atom hidrogen (H) dan gugus hidroksida (OH) melalui suatu proses
kimia. Serisin C adalah lapisan terdalam dari serisin (innermost layer) yang
berdekatan dengan fibroin. Serisin C tidak larut dalam air panas tapi akan larut
dalam alkali atau asam panas. Serisin C akan menghasilkan prolin dan asam
amino serisin B pada hidrolisis asam. Serisin C mengandung sulfur dan 16,6 %
nitrogen.
b. Bobot Molekul (BM)
Bobot molekul merupakan salah satu penentu kemurnian protein serisin.
Protein serisin mewakili kelompok protein dengan bobot molekul antara 10-310
12 yang berbeda akan menghasilkan BM yang berbeda pula. Aramwit et al. (2010),
ekstraksi dengan urea akan menghasilkan kisaran BM protein serisin antara
10-250 kDa, ekstraksi dengan asam menghasilkan kisaran 50-150 kDa, ekstraksi
dengan alkali menghasilkan kisaran 15-75 kDa, sedangkan ekstraksi dengan
temperatur dan tekanan tinggi akan menghasilkan BM dengan kisaran 25-150
kDa. Takasu et al. (2010), kisaran BM protein serisin dibagi menjadi empat
bagian yaitu, di atas 250 kDa pada Ser1, 250 kDa pada Ser3, 225-230 kDa pada
Ser2-large dan di bawah 130 kDa pada Ser2-small.
Wu et al. (2007) menyatakan bahwa bobot molekul serisin Bombyx mori
berkisar 6 kDa dengan resolving gel 12,5% dan stacking gel 4%. Salah satu
metode yang sering digunakan dalam menentukan bobot molekul adalah metode
elektroforesis dengan Sodium dodecyl sulfate polyacrylamide gel electrophoresis
(SDS–PAGE) dan pewarnaan silver (Laemmli 1970). Marker yang digunakan
adalah standar protein dengan ukuran bobot molekul tertentu seperti
phosphorylase B (97 kDa), bovine serum albumin (66 kDa), ovalbumin (43 kDa),
carbonic anhydrase (31 kDa), soy trypsin inhibitor (22 kDa), dan lysozyme (14
kDa) serta paket protein standar yang dikeluarkan suatu perusahaan.
c. Persentase Protein
Komposisi utama serisin Bombyx mori menurut Wu et al. (2007) adalah
protein (91,6%), abu (4,2%) dan gula (0,93%), sedangkan menurut Gulrajani et al.
(2008) adalah protein (58-62 %), nitrogen (9-10 %), dan abu (22%). Kedua
komposisi serisin di atas berbeda karena metode yang digunakan berbeda. Wu et
al. (2007) menggunakan pelarut organik dalam mendapatkan serisin murni,
sedangkan Gulrajani et al. (2008) menggunakan membran filtrasi.
Beberapa metode yang digunakan untuk pengukuran kadar protein adalah:
- Kjeldahl
Persentase nitrogen dalam serisin murni dapat digunakan untuk menduga
persentase proteinnya, yaitu dengan mengalikan persentase nitrogen dengan faktor
koreksi 6,25 (Apriyantono et al. 1989). Salah satu cara yang dilakukan untuk
mengetahui persentase nitrogen adalah dengan metode Kjeldahl yang terbagi tiga
13 - Lowry (Apriyantono et al. 1989)
Metode Lowry merupakan pengembangan dari metode Biuret tetapi
mempunyai sensitifitas 100 kali lebih baik dibandingkan dengan metode biuret.
Prinsip kerjanya adalah terjadi reaksi antara Cu2+ dengan ikatan peptida dan
reduksi asam fosfomolibdat dan asam fosfotungsat oleh tirosin dan triptofan
(merupakan residu protein) akan menghasilkan warna biru. Warna yang terbentuk
tergantung pada kadar tirosina dan triptofan dalam protein.
d. Analisis Asam Amino
High Performance Liquid Chromatography (HPLC) merupakan salah satu
teknik yang banyak digunakan dalam memisahkan asam amino penyusun protein.
HPLC menggunakan tekanan tinggi untuk merusak aktifitas biologis protein
dibagian struktur tersiernya. Kerja HPLC dimulai dengan memasukkan sampel
yang telah dipreparasi ke injektor. Sampel bersama fase bergerak akan masuk ke
bagian kolom. Pergerakan sampel dalam kolom akan diperlambat oleh bahan
kimia khusus sebagai fase diam di kolom. Kecepatan gerak sampel sangat
tergantung dari sifat sampel dan komposisi fase diam dalam kolom. Waktu yang
dibutuhkan sampel untuk keluar dari kolom disebut waktu tinggal (retention
time). Waktu retensi yang dihasilkan sampel merupakan identifikasi dari
karakteristik sampel tersebut. Penggunaan ukuran kolom yang lebih kecil akan
menciptakan back pressure yang lebih besar untuk menambah kecepatan linier
komponen sampel. Hal ini akan meningkatkan resolusi dari kromatogram (Cazes
2005).
Bahan kimia khusus yang digunakan bersifat meningkatkan homogenitas
larutan sampel, yang terdiri dari air dan bahan organik seperti metanol dan
asetonnitril. Air yang digunakan bersifat sebagai buffer untuk membantu
pemisahan komponen-komponen sampel.
e. Surface tension
Surface tension adalah tegangan permukaan dari fasa liquid (cair). Banyak
fenomena yang menggambarkan tentang surface tension, dan diantaranya yang
memanfaatkan fenomena tersebut adalah surfaktan (surface active agent) dengan
cara menurunkan tegangan permukaan. Surfaktan mempunyai dua sisi (ampifilik)
14 Tegangan permukaan yang kecil dapat dimanfaatkan untuk banyak hal. Suryani et
al. (2008), penambahan alkil poliglikosida (APG) sebanyak 10 mg/ml dapat
menurunkan tegangan permukaan air sampai 23,375 dyne/cm. APG adalah
surfaktan berbahan pati sagu dan alkohol lemak kelapa dengan mengubah sumber
patinya dari kentang menjadi pati sagu dan netralisasi dengan NaOH. APG
dipergunakan sebagai bahan tambahan pada herbisida untuk meningkatkan
penetrasi bahan aktif herbisida kedalam tanaman dan mengendalikan gulma jenis
rumput-rumputan. Tegangan permukaan dari beberapa bahan dapat dilihat pada
Tabel 3.
Tabel 3 Tegangan permukaan berbagai cairan (Wikipedia 2012)
Cairan Suhu (oC) Tegangan permukaan (dyne/cm)
Metodologi respon permukaan (Response Surface Methodology) adalah
suatu kumpulan teknik-teknik statistika dan matematika yang digunakan untuk
menganalisis permasalahan tentang variabel bebas yang berpengaruh terhadap
variabel tak bebas atau respon dengan tujuan untuk mengoptimasi respon
(Gasperz 1992). RSM dapat digunakan untuk mencari suatu fungsi pendekatan
15 bebas yang dapat mengoptimumkan respon. Hasil analisis RSM ditampilkan
dalam bentuk kontur yang menghasilkan titik optimum berupa optimasi
maksimum, minimum atau saddle point.
Tahap yang paling penting dalam RSM adalah menentukan daerah optimum
(Myers 1971). Daerah optimum dapat diperoleh dari data percobaan sebelumnya
tapi jika belum ada maka menggunakan steepest ascent methode (Gasperz 1992)
yang sering disebut dengan respon ordo pertama. Respon ordo pertama akan
menghasilkan daerah optimum yang dipakai sebagai titik pusat dari respon ordo
kedua. Desain respon ordo pertama dan kedua dapat dibantu dengan program
software seperti Design Expert, JMP dan Statgraphics. Akan tetapi baru-baru ini
ada program baru yang menyediakan semua menu penting untuk RSM seperti
pilihan desain, rsm’s ccd.pick (central composite design) yang dapat didesain
sendiri (Lenth 2010). Program tersebut adalah R versi 2.11.1 dengan packages
16
BAHAN DAN METODE
Penelitian dilaksanakan pada bulan November 2011 sampai Maret 2012
bertempat di Laboratorium Terpadu Departemen Ilmu Produksi dan Teknologi
Peternakan, Fakultas Peternakan IPB. Sampel kokon dan larva Attacus atlas
berasal dari Perkebunan Teh Walini Panglejar Purwakarta Jawa Barat. Tahapan
penelitian dapat dilihat pada Gambar 4.
Gambar 4 Bagan alir penelitian.
Ekstraksi Protein Serisin
Pada penelitian ini protein serisin diekstraksi dari kelenjar sutera tengah dan
kulit kokon. Kelenjar sutera tengah merupakan tempat sekresi protein serisin,
sedangkan kulit kokon adalah produk ulat sutera yang mengandung protein serisin
dan fibroin. Protein serisin merupakan perekat serat-serat fibroin pada kokon.
A.Ekstraksi Protein Serisin dari Kelenjar Sutera Tengah Attacus atlas (KSA) KSA adalah tempat protein serisin disekresi, sehingga hasil ekstraksi
protein serisin dari KSA digunakan sebagai standar protein serisin Attacus atlas.
Protein serisin dari KSA digunakan sebagai pembanding dari crude protein serisin
(hasil ekstraksi dari kokon). Tahapan ekstraksi dari KSA sesuai Brasla & Matei
(1997) dan Invitrogen 2012 (Lampiran 1). Hasil ekstraksi dianalisis bobot
molekulnya dengan SDS PAGE (Laemmli 1970).
Protein serisin Ulat sutera liar Attacus atlas dari
17 B.Ekstraksi Protein Serisin dari Kulit Kokon
B.1 Preparasi sampel kulit kokon (Lampiran 2) sesuai dengan Solihin & Fuah
(2010) yang telah dimodifikasi.
B.2 Ekstraksi protein serisin dari kulit kokon
Proses ekstraksi protein serisin dari kulit kokon terdiri dari dua tahap,
yaitu teknik degumming dan isolasi protein serisin. Degumming adalah proses
penguraian serat sutera (fibroin) dari perekatnya (gum atau serisin) secara fisik
yaitu dengan suhu dan tekanan tinggi (Padamwar & Pawar 2004), serta secara
kimia dengan NaOH 0,1 N (Suriana 2011). Tujuan degumming adalah
menghasilkan serat sutera (fibroin) yang siap untuk dijadikan benang sutera
dan mendapatkan serisin yang terlarut dalam larutan hasil degumming. Isolasi
protein serisin adalah tahapan mendapatkan protein target (serisin) dari larutan
hasil degumming, dan pada penelitian ini targetnya berupa crude protein
serisin. Isolasi protein pada penelitian ini menggunakan teknik pengendapan
dengan pelarut organik etanol 75% (v/v) terhadap larutan hasil degumming
(Wu et al. 2007).
Proses ekstraksi dilakukan secara bertahap untuk mengetahui pengaruh
setiap kajian terhadap rendemen protein serisin yang dihasilkan. Setiap kajian
sangat tergantung pada hasil kajian sebelumnya. Ada beberapa kajian yang
dilakukan, yaitu:
B.2.1 Kajian Pengaruh Rasio Volume NaOH 0,1 N dan Jenis Spesies Ulat Sutera terhadap Rendemen Protein Serisin
Ekstraksi protein serisin melalui teknik degumming secara fisik dan
kimia (Padamwar & Pawar 2004, Suriana 2011) yang telah dimodifikasi.
Teknik degumming pada suhu 115oC selama 40 menit dan tekanan 700 mbar,
serta variasi rasio NaOH 0,1 N (50% dan 33,3% terhadap distiled water/DW).
Isolasi protein dengan teknik pengendapan menggunakan etanol teknis 96%
sebesar 75% v/v terhadap larutan hasil degumming. Hasil isolasi berupa crude
protein serisin dalam bentuk cairan kental. Tahapan ekstraksi dapat dilihat pada
Lampiran 2.
Rancangan percobaan yang digunakan dalam kajian ini adalah rancangan
18 dan spesies ulat sutera (S) yang masing-masing pada dua taraf perlakuan yang
diulang dua kali (Tabel 4). Model matematikanya adalah:
Yijk = µ + Ri + Sj + (RS)ij + εijk
Keterangan :
Yijk = Pengamatan berupa rendemen protein serisin pada perlakuan ke-i (1,
2) dan ke-j (1, 2) pada ulangan ke-k (1, 2)
µ = Rataan umum
Ri = Pengaruh rasio NaOH 0,1 N ke-i (1, 2)
Sj = Pengaruh spesies ulat sutera ke-j (1, 2)
εijk = Pengaruh acak pada perlakuan ke-i dan ke-j pada ulangan ke-k. Analisis RALF menggunakan program Minitab 14 (Mattjik & Sumertajaya
2002).
Tabel 4 Tabulasi data kajian pengaruh rasio NaOH 0,1 N dan jenis spesies ulat sutera terhadap rendemen protein serisin
B.2.2 Kajian Pengaruh Konsentrasi NaOH terhadap Rendemen Protein Serisin
Ekstraksi protein serisin melalui degumming secara fisik dan kimia
(Lampiran 2) pada suhu 115oC selama 40 menit dan tekanan 700 mbar, serta
variasi konsentrasi NaOH (0,05 N; 0,1 N; 0,15 N; 0,20 N; 0,25 N dan 0,30 N)
pada rasio volume 33,3% terhadap DW. Isolasi protein dengan etanol teknis
(96%) pada perbandingan volume 75% v/v terhadap larutan hasil degumming.
Hasil isolasi protein berupa crude protein serisin.
Rancangan percobaan yang digunakan dalam kajian ini adalah rancangan
acak lengkap (RAL) satu faktor (konsentrasi NaOH) dengan dua kali ulangan
(Tabel 5). Model matematikanya adalah:
19 Keterangan:
Yij = Pengamatan berupa rendemen protein serisin pada perlakuan ke-i (1,
2, 3, 4, 5, 6) dan ulangan ke-j (1, 2)
µ = Rataan umum
Ni = Pengaruh konsentrasi NaOH ke-i (1, 2, 3, 4, 5, 6) εij = Pengaruh acak pada perlakuan ke-i dan ulangan ke-j.
Jika hasil analisis ragam berpengaruh nyata maka akan dilakukan uji lanjut
dengan Tukey. Analisis RAL dan Tukey menggunakan program Minitab 14
(Mattjik & Sumertajaya 2002).
Tabel 5 Tabulasi data kajian pengaruh variasi konsentrasi NaOH terhadap rendemen protein serisin Attacus atlas
B.2.3 Kajian Pengaruh Kemurnian Etanol terhadap Rendemen Protein Serisin
Pada kajian ini menggunakan proses ekstraksi dengan teknik degumming
secara fisik pada suhu 105oC selama 30 menit, dan tekanan 200 mbar. Isolasi
protein menggunakan teknik pengendapan dengan etanol absolut dan teknis
96% (masing-masing perbandingan volume terhadap larutan hasil degumming
sebesar 75% v/v). Hasil akhir isolasi berupa crude protein serisin dalam bentuk
cairan kental. Tahapan ekstraksi dapat dilihat pada Lampiran 2.
Rancangan percobaan yang digunakan dalam kajian ini adalah rancangan
acak lengkap (RAL) satu faktor (kemurnian etanol) dengan tiga kali ulangan
(Tabel 6). Model matematikanya adalah:
Yij = µ + Ei+ εij
Keterangan :
Yij = Pengamatan berupa rendemen protein serisin pada perlakuan ke-i (1,
20 µ = Rataan umum
Ei = Pengaruh kemurnian etanol ke-i
εij = Pengaruh acak pada kemurnian etanol ke-i dan ulangan ke-j.
Analisis RAL menggunakan program Minitab 14 (Mattjik & Sumertajaya
2002).
Tabel 6 Tabulasi data kajian pengaruh kemurnian etanol terhadap rendemen protein serisin Attacus atlas
Kajian optimasi rendemen protein serisin perlu dilakukan untuk
mengetahui rendemen protein serisin yang maksimal dari kokon Attacus atlas.
Rendemen protein yang maksimal dapat disebabkan oleh teknik ekstraksi yang
dilakukan atau kandungan protein serisin dalam kokon Attacus atlas.Ada tiga
perlakuan ekstraksi protein serisin yang dikerjakan pada kajian optimasi ini,
yaitu:
- Optimasi 3 (O3) menggunakan teknik degumming fisik pada kombinasi suhu
dan waktu (Tabel 7). Isolasi protein dengan etanol teknis 96%.
Analisis yang digunakan dalam optimasi rendemen protein serisinadalah
Response Surface Methodology (RSM) yang diolah dengan Program-R 2.11.1
(Lenth 2010). Hubungan antara respon dan variabel bebas adalah:
21 Keterangan:
Y = Respon (rendemen protein serisin)
Xi = Variabel bebas ( i = 1, 2, 3,...., k ) ε = error.
Daerah optimum (ordo pertama) ditentukan dari percobaan sebelumnya
sehingga analisis ordo pertama tidak dilakukan lagi. Analisis ordo kedua (titik
optimum) menggunakan model polinomial ordo kedua dengan fungsinya
kuadratik:
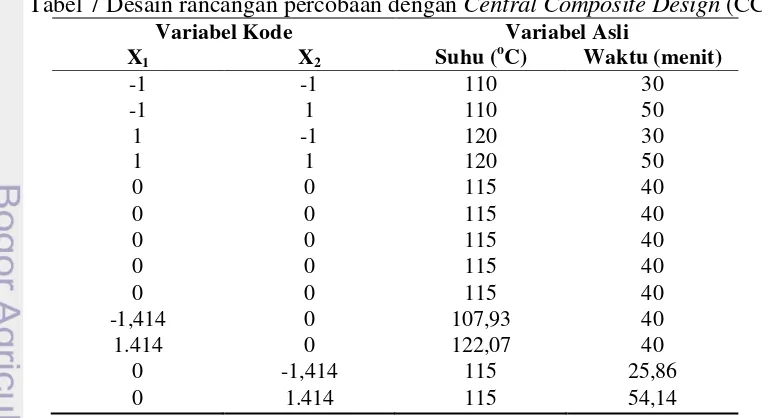
Rancangan percobaan pada penelitian ini menggunakan Central
Composite Design (CCD) seperti pada Tabel 7. Percobaan menggunakan dua
faktor (2k) yaitu suhu (X1) dan waktu (X2) sehingga α = 1,414. Titik pusat yang
digunakan adalah suhu 115oC dan waktu 40 menit.
Tabel 7 Desain rancangan percobaan dengan Central Composite Design (CCD)
22 B.3 Analisis Protein
Pada penelitian ini metode Lowry (Apriyantono et al. 1989) digunakan
untuk menganalisis crude protein serisin dan deteksi absorbansinya
menggunakan spektrofotometer tipe Gene Quant 1300 pada panjang
gelombang 750 nm. Crude protein serisin dihomogenisasi terlebih dahulu
dengan stirrer sebelum dianalisis dengan Lowry. Hasil analisis berupa kadar
protein serisin (mg/ml) digunakan untuk menghitung rendemen protein serisin.
Rendemen protein serisin dihitung dengan rumus:
Rendemen (%) = [ Bobot protein dalam crude protein serisin ] x 100% [Bobot kulit kokon]
Khusus untuk perhitungan rendemen protein serisin pada kajian optimasi,
ada dua perhitungan yang dilakukan yaitu tanpa penambahan air dalam fibroin
basah (AFB) dan dengan penambahan AFB. AFB adalah larutan hasil
degumming yang terikut dalam fibroin karena proses pemisahan antara larutan
dan fibroin belum sempurna. Penambahan AFB dalam perhitungan digunakan
untuk meminimalkan larutan yang terbuang karena keterbatasan kemampuan
alat pemisah. Tanpa penambahan AFB dinotasikan sebagai perlakuan 1,
sedangkan dengan penambahan AFB dinotasikan sebagai perlakuan 2 sehingga
masing-masing perlakuan optimasi terdiri dari dua perhitungan dengan notasi
O11, O12, O21, O22, O31 dan O32.
AFB dihitung dengan analisis kadar air fibroin untuk menghitung volume
larutan hasil degumming yang terikut dalam fibroin. Analisis kadar air
menggunakan oven Selecta Digitheat pada suhu 115oC selama 18 jam
(Apriyantono et al. 1989). Perhitungan kadar air fibroin hasil degumming
adalah:
AFB (ml) = [(Bobot basah fibroin – Bobot kering fibroin) x (BJ larutan)]
Keterangan: Berat jenis (BJ) larutan = 0,9889.
B.4 Analisis Fibroin
Analisis fibroin dilakukan untuk mengetahui pengaruh ekstraksi terhadap
penampang fibroin hasil degumming. Pengamatan fibroin menggunakan
mikroskop Optika Micro Image Analysis Versi 1.0 dengan pembesaran 400 kali
23 C. Karakterisasi Crude Protein Serisin
C.1 Analisis Bobot Molekul (BM)
Analisis bobot molekul dengan Sodium Dodecyl Sulphate
Polyachrylamide Gel Electrophoresis (SDS PAGE) merujuk pada Laemmli
(1970) yang telah dimodifikasi. Buffer gel yang digunakan adalah 2 M Tris
HCl pH 8,8 pada separating gel dan 1 M Tris HCl pH 6,8 pada stacking gel,
sedangkan buffer elektrodanya dengan Tris glisin (25 mM Tris dan 192 mM
glisin). Pada separating gel 12,5% dan stacking gel 4% dengan rasio
perbandingan panjang sebesar 5:1 antara separating gel dan stacking gel.
Analisis bobot molekul ini menggunakan pewarnaan silver (silver staining).
Elektroforesis menggunakan dual mini kit pada tegangan listrik konstan
60 volt dan kisaran arus listrik 24 ampere selama kurang lebih 4 jam. Marker
yang digunakan adalah Fermentas Multicolor Broad Range Protein Ladder
kode #SM1841 (Tabel 8).
Hasil analisis bobot molekul ditampilkan dalam bentuk fragmen atau pita
protein dalam gel. Bobot molekul protein target (terlihat sebagai pita protein)
dihitung berdasarkan kurva standar dari bobot molekul marker (Lampiran 20).
Tabel 8 Markerdari Fermentas Multicolor Broad Range Protein Ladder
Bobot molekul marker (kDa) Warna
Analisis asam amino menggunakan High Performance Liquid
Chromatography (HPLC) berdasarkan protokol HPLC Laboratorium Terpadu
IPB. Perangkat HPLC yang digunakan adalah Shimadzu HPLC dengan kolom
Thermo S Ods-Hypersil (laju aliran fase mobil 1 ml/menit). Analisis asam
amino dilakukan dengan memanfaatkan reaksi pra-kolom gugus amino dengan
24 Pereaksi OPA akan bereaksi dengan asam amino primer dalam suasana basa
yang mengandung merkaptoetanol membentuk senyawa yang berfluoresensi,
sehingga deteksinya dapat dilakukan dengan detektor flouresensi.
Hasil analisis asam amino dengan HPLC ditampilkan dalam bentuk
kromatogram. Konsentrasi asam amino dapat dihitung dengan rumus:
Asam amino (µmol) = [ Luas puncak sampel x konsentrasi standar] [Luas puncak standar]
Persentase asam amino dalam sampel dihitung dengan rumus:
Asam amino (%) = [ µmol asam amino x BM asam amino ] x 100% [µg sampel]
C.3 Uji Tegangan Permukaan (Surface Tension)
Struktur molekul surfaktan terdiri dari sisi hidrofilik pada bagian kepala
dan hidrofobik pada bagian ekor. Protein serisin mempunyai sisi hidrofilik dan
hidrofobik (Wu et al. 2007) sehingga diduga mempunyai sifat sebagai
surfaktan (surface active agent). Surfaktan merupakan zat yang mempunyai
kemampuan menurunkan tegangan permukaan suatu medium dan menurunkan
tegangan antarmuka dua fasa yang berbeda derajat polaritasnya (Salanger
2002). Uji tegangan permukaan pada penelitian ini dilakukan untuk
mengetahui kemampuan protein serisin dalam menurunkan tegangan
permukaan. Uji tegangan permukaan (surface tension) dilakukan menggunakan
tensiometer tipe Cole-Parmer Surface Tensiomat 21 dan tahapannya dapat
dilihat pada Lampiran 3.
Rancangan percobaan yang digunakan dalam uji tegangan permukaan
sampel adalah rancangan acak lengkap (RAL) satu faktor (kadar protein)
dengan tiga kali ulangan (Tabel 9). Model matematikanya adalah:
Yij = µ + TPi+ εij
Keterangan:
Yij = Pengamatan berupa nilai tegangan permukaan crude protein serisin
pada perlakuan ke-i (1, 2, 3) dan ulangan ke-j (1, 2, 3)
µ = Rataan umum
TPi = Pengaruh kadar protein ke-i
25 Jika hasil analisis ragam berpengaruh nyata maka akan dilakukan uji lanjut
dengan Tukey. Analisis RAL dan Tukey menggunakan program Minitab 14
(Mattjik & Sumertajaya 2002).
Tabel 9 Tabulasi data tegangan permukaan crude protein serisin
Ulangan
Perlakuan
Total
1 2 3
1 TP11 TP21 TP31
2 TP12 TP21 TP31
3 TP13 TP21 TP31
26
HASIL DAN PEMBAHASAN
1. Teknik Ekstraksi Protein Serisin
Hasil ekstraksi protein serisin dari kokon dipengaruhi oleh teknik
degumming dan isolasi protein yang dilakukan. Oleh karena itu perlu adanya
kajian tentang teknik ekstraksi yang tepat untuk menghasilkan respon (rendemen
protein) yang maksimal. Ada beberapa kajian yang dilakukan dalam penelitian ini
untuk mendapatkan teknik ekstraksi protein serisin.
Padamwar & Pawar (2004), menghasilkan protein serisin Bombyx mori
terbaik dari teknik ekstraksi serisin melalui degumming dengan kombinasi suhu,
waktu dan tekanan (105oC, 30 menit dan 200 mbar). Wu et al. (2007),
mengisolasi protein serisin Bombyx mori dengan teknik pengendapan
menggunakan etanol absolut. Akan tetapi etanol absolut harganya cukup mahal
sehingga kurang efisien untuk diterapkan dalam skala industri. Perlu ada kajian
tentang alternatif lain sebagai pengganti etanol absolut. Kajian isolasi protein pada
tingkat kemurnian etanol berbeda dilakukan di awal penelitian ini untuk
memberikan informasi tersebut. Berbeda dengan isolasi protein, teknik
degummingAttacus atlas pada awal penelitian ini masih merujuk pada Padamwar
& Pawar (2004), karena diduga kulit kokon Attacus atlas dan Bombyx mori
mempunyai karakteristik yang sama.
a. Kajian Pengaruh Kemurnian Etanol terhadap Rendemen Protein Serisin
Attacus atlas
Etanol digunakan sebagai pengendap dalam isolasi protein serisin. Wu et al.
(2007) menggunakan etanol absolut dengan volume 75% (v/v) untuk mengisolasi
protein serisin Bombyx mori. Pada kajian ini digunakan etanol dengan kemurnian
berbeda yaitu etanol absolut dan etanol teknis 96% dengan masing-masing
perbandingan volume terhadap larutan hasil degumming sebesar 75% (v/v). Hasil
kajian pengaruh kemurnian etanol disajikan pada Tabel 10.
Tabel 10 Hasil kajian pengaruh kemurnian etanol terhadap rendemen protein serisin Attacus atlas
Perlakuan Rendemen protein serisin dalam kulit kokon (%)
E1 1,03 ± 0,04
E2 1,00 ± 0,16
27 Hasil kajian menunjukkan bahwa E1 (etanol absolut) dapat mengisolasi
protein dengan rendemen sebesar 1,03 ± 0,04 %, sedangkan E2 (etanol teknis
96%) sebesar 1,00 ± 0,16 %. Analisis ragam dari data pengaruh kemurnian etanol
(Lampiran 4) menunjukkan bahwa kemurnian etanol tidak berpengaruh nyata
(P>0,05) terhadap rendemen protein serisin. Artinya tidak ada perlakuan yang
berbeda nyata akibat perbedaan kemurnian etanol. Hasil tersebut memberikan
informasi bahwa etanol teknis dapat digunakan untuk isolasi pada tahap kajian
selanjutnya.
Teknik ekstraksi hanya dengan degumming secara fisik pada suhu 105oC
selama 30 menit belum menghasilkan rendemen protein serisin (Tabel 10) yang
maksimal, yaitu hanya sebesar 1,03 ± 0,04 % dan 1,00 ± 0,16 % saja. Rendemen
protein serisin tersebut masih jauh dari informasi sebelumnya yang menyatakan
bahwa rendemen protein serisin sebesar 20%-30% dari bobot kulit kokon
(Masahiro et al. 2000). Hasil ekstraksi yang belum maksimal didukung oleh hasil
analisis penampang fibroin dengan mikroskop (Gambar 5). Kondisi fibroin
terlihat masih utuh dengan warna coklat tua pada kedua perlakuan. Hasil tersebut
memperlihatkan bahwa serisin belum terekstraksi maksimal.
Gambar 5 Penampang fibroin Attacus atlas hasil ekstraksi pada suhu 105oC selama 30 menit dengan, a) isolasi etanol absolut dan b) isolasi etanol teknis pada pembesaran 400 kali.
b. Kajian Pengaruh Rasio Volume NaOH 0,1 N dan Jenis Spesies Ulat Sutera terhadap Rendemen Protein Serisin
Basa kuat NaOH 0,1 N adalah bahan pelarut untuk degumming yang dapat
menghasilkan fibroin terbaik (Suriana 2011). Rasio volume NaOH 0,1 N
digunakan untuk mengkaji pengaruhnya terhadap rendemen protein serisin yang
dihasilkan. Suhu dan waktu yang digunakan pada kajian ini lebih tinggi daripada
kajian sebelumnya yaitu dari 105oC selama 30 menit menjadi 115oC selama 40
28 menit. Hal ini dilakukan karena rendemen protein serisin yang dihasilkan pada
kajian sebelumnya belum maksimal (Tabel 10).
Perlakuan jenis spesies juga digunakan pada tahap ini untuk mengetahui
perbedaan pengaruhnya terhadap rendemen protein serisin. Spesies yang
digunakan adalah Attacus atlas dan Bombyx mori.Rendemen protein serisin hasil
perlakuan rasio volume NaOH 0,1 N dan jenis spesies ulat sutera disajikan pada
Tabel 11.
Hasil analisis ragam (Lampiran 5) menunjukkan bahwa rasio volume NaOH
0,1 N tidak berpengaruh nyata (P>0,05), sedangkan spesies sangat berpengaruh
nyata (P<0,01) terhadap rendemen protein serisin. Hal ini menunjukkan bahwa
rasio volume NaOH 0,1 N baik 50% (1:1 terhadap DW) maupun 33,3% (1:2
terhadap DW) mempunyai pengaruh sama terhadap rendemen protein yang
dihasilkan. Oleh karena itu rasio volume yang lebih kecil yaitu 33,3% NaOH 0,1
N akan digunakan pada proses degumming selanjutnya.
Tabel 11 Rendemen protein serisin hasil perlakuan rasio volume NaOH 0,1 N dan jenis spesies ulat sutera 0,1 N. Huruf (a,b) adalah superscript dari hasil uji lanjut Tukey. Jika superscript sama hurufnya maka tidak berbeda nyata dan jika berbeda hurufnya maka berbeda nyata.
Perlakuan spesies mempunyai pengaruh nyata pada rendemen protein
serisin. Hal ini membuktikan bahwa dengan perlakuan yang sama setiap spesies
mempunyai potensi rendemen protein serisin yang berbeda. Perbedaan ini dapat
disebabkan oleh dua hal, yaitu pertama karena kandungan protein serisin dalam
kedua spesies kokon tersebut berbeda, kedua adalah akibat proses degumming
yang digunakan pada kokon Bombyx mori seluruh serisinnya berhasil diekstraksi
sedangkan pada Attacus atlas belum seluruhnya terekstraksi. Serat sutera Attacus
atlas diduga lebih kuat dan lebih sulit diekstraksi serisinnya dibandingkan dengan
Bombyx mori, karena makanan Attacus atlas mengandung tanin yang dapat