PEMANFAATAN LIMBAH KULIT BATANG KARET
SEBAGAI BIOSORBEN ION KROMIUM(VI)
DAN TIMBEL(II)
MARINA ASTRIAWI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul pemanfaatan limbah kulit batang karet sebagai biosorben ion kromium(VI) dan timbel(II) adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Mei 2013
Marina Astriawi
ABSTRAK
MARINA ASTRIAWI. Pemanfaatan Limbah Kulit Batang Karet sebagai Biosorben Ion Kromium(VI) dan Timbel(II). Dibimbing oleh ETI ROHAETI dan ADI SANTOSO.
Kulit batang karet merupakan limbah yang cukup melimpah di Sumatera Selatan dan potensial untuk dimanfaatkan. Penelitian ini memanfaatkan kulit batang karet sebagai biosorben ion kromium dan ion timbel di perairan. Metode yang digunakan adalah metode tumpak dengan parameter pengamatan meliputi pengaruh ukuran partikel, pH larutan, dan waktu kontak. Penetapan kondisi terbaik penjerapan menggunakan uji Duncan. Hasil penelitian menunjukkan kondisi terbaik biosorpsi Cr(VI) terjadi pada ukuran partikel 100 mesh, pH 2, dan waktu kontak selama 1 jam, sedangkan kondisi terbaik biosorpsi Pb(II) terjadi pada ukuran partikel 100 mesh, pH 7, dan waktu kontak selama 1 jam. Kesetimbangan biosorpsi kromium dan timbel mengikuti pola isoterm Freundlich (linearitas = 98.80% dan 93.92%). Kapasitas adsorpsi maksimum berdasarkan model isoterm Freundlich tersebut ialah 0.55 mg Cr(VI) dan 0.98 mg Pb(II) per gram adsorben.
Kata kunci: biosorben, biosorpsi, karet, kromium, timbel
ABSTRACT
MARINA ASTRIAWI. Utilization of Rubber Stem Bark Waste as Biosorbent of Chromium(VI) and Lead(II). Under the direction of ETI ROHAETI and ADI SANTOSO.
Rubber stem bark is a fair amount waste in South Sumatera which is potential to be utilized. This study utilized the rubber stem bark as chromium and lead ion heavy metal biosorbent in the water. The method used was batch method which observation parameters included the influence of biosorbent particle size, pH, and contact time. The optimum condition was determined by Duncan test. Results showed that the optimum condition of Cr(VI) biosorption occured at 100 mesh particle size, pH 2, and 1 hour contact time, whereas the optimum condition of Pb(II) biosorption occur at 100 mesh particle size, pH 7, and 1 hour contact time. Biosorption equilibrium of chromium and lead followed the Freundlich isotherm model (linearity = 98.80% and 93.92%). Maximum adsorption capacity based on the Freundlich equation was 0.55 mg Cr(VI) and 0.98 mg Pb(II) for one gram of adsorbent.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada Departemen Kimia
PEMANFAATAN LIMBAH KULIT BATANG KARET
SEBAGAI BIOSORBEN ION KROMIUM(VI)
DAN TIMBEL(II)
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2013
Judul Skripsi : Pemanfaatan Limbah Kulit Batang Karet sebagai Biosorben Ion Kromium(VI) dan Timbel(II)
Nama : Marina Astriawi
NIM : G44104018
Disetujui oleh
Dr Eti Rohaeti, MS Pembimbing I
Prof Dr Drs Adi Santoso, MSi Pembimbing II
Diketahui oleh
Prof Dr Ir Tun Tedja Irawadi, MS Ketua Departemen Kimia
PRAKATA
Puji syukur penulis panjatkan kepada Allah Subhanahu wa ta’ala atas segala berkat dan rahmat-Nya sehingga penulis dapat menyelesaikan karya tulis ini. Karya tulis ini disusun berdasarkan kegiatan penelitian dengan judul Pemanfaatan Limbah Kulit Batang Karet sebagai Biosorben Ion Kromium(VI) dan Timbel(II) yang dilaksanakan pada bulan Juli 2012 sampai dengan Januari 2013 di Laboratorium Kimia Analitik, Departemen Kimia, FMIPA, IPB, Bogor.
Penulis mengucapkan terima kasih kepada Dr Eti Rohaeti, MS dan Prof Dr Drs Adi Santoso, MSi selaku pembimbing yang telah memberikan bimbingan, arahan, dan waktu selama penelitian berlangsung. Penulis juga mengucapkan terima kasih kepada seluruh staf Laboratorium Kimia Analitik Fakultas MIPA, IPB, serta Badrun selaku rekan sepenelitian. Terima kasih takterhingga penulis sampaikan kepada keluarga tercinta Ibu, Ayah, Adik-adikku, Yogas, Geni, Mega, Ocep, Meli, Helga, Yuanita, Lia, Mbak Janti, dan teman-teman Program S1 Penyelenggaraan Khusus, Departemen Kimia angkatan 4 yang telah memberikan doa, semangat, kasih sayang, dan dukungan moral serta materi selama masa studi hingga prosees penyusunan karya ilmiah ini.
Semoga karya Ilmiah ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
Bogor, Mei 2013
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN vix
PENDAHULUAN 1
METODE 2
Bahan dan Alat 2
Preparasi Biosorben Kulit Batang Karet 3
Penentuan Kadar Air Kulit Batang Karet 3
Penentuan Konsentrasi Pb dan Cr dalam Sampel Biosorben 3
Penentuan Kondisi Adsorpsi Terbaik 3
Penentuan Isoterm dan Kapasitas Adsorpsi 4
HASIL DAN PEMBAHASAN 5
Biosorben Serbuk Kulit Batang Karet 5
Kondisi Terbaik Biosorpsi Cr(VI) 6
Kondisi Terbaik Biosorpsi Pb(II) 9
Pola Isoterm Adsorpsi 11
Pengaruh Konsentrasi pada Kapasitas dan Efisiensi Adsorpsi 13
Kapasitas Adsorpsi 13
SIMPULAN DAN SARAN 14
Simpulan 14
Saran 15
DAFTAR PUSTAKA 15
viii
DAFTAR TABEL
1 Kapasitas adsorpsi biosorben terhadap Cr(VI) 20 mg/L pada variasi kondisi ukuran partikel, pH larutan, dan waktu kontak 8 2 Kapasitas adsorpsi biosorben terhadap Pb(II) 20 mg/L pada variasi
kondisi ukuran partikel, pH larutan, dan waktu kontak 11 3 Perbandingan kapasitas adsorpsi pada berbagai biosorben mengikuti
mekanisme isoterm Freundlich 14
DAFTAR GAMBAR
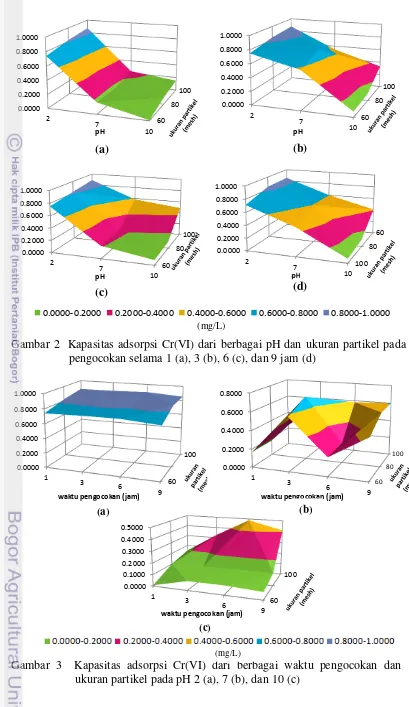
1 Serbuk kulit batang karet ukuran 100 (i), 80 (ii), dan 60 mesh (iii) 5 2 Kapasitas adsorpsi Cr(VI) dari berbagai pH, ukuran partikel pada
pengocokan selama 1 (a), 3 (b), 6 (c), dan 9 jam (d) 7 3 Kapasitas adsorpsi Cr(VI) dari berbagai waktu pengocokan dan
ukuran partikel pada pH 2 (a), 7 (b), dan 10 (c) 7 4 Kapasitas adsorpsi Cr(VI) dari berbagai waktu pengocokan dan pH
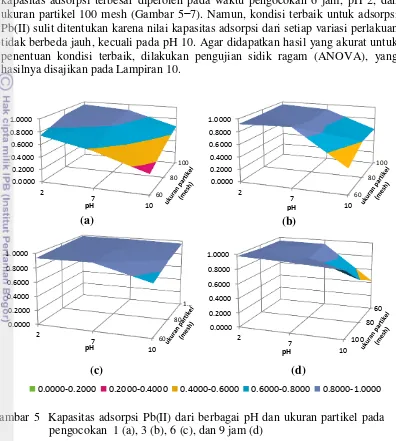
pada ukuran partikel 100 (a), 80 (b), dan 60 mesh (c) 8 5 Kapasitas adsorpsi Pb(II) dari berbagai pH, ukuran partikel pada
pengocokan selama 1 (a), 3 (b), 6 (c), dan 9 jam (d) 10 6 Kapasitas adsorpsi Pb(II) dari berbagai waktu pengocokan dan ukuran
partikel pada pH 2 (a), 7 (b), dan 10 (c) 9
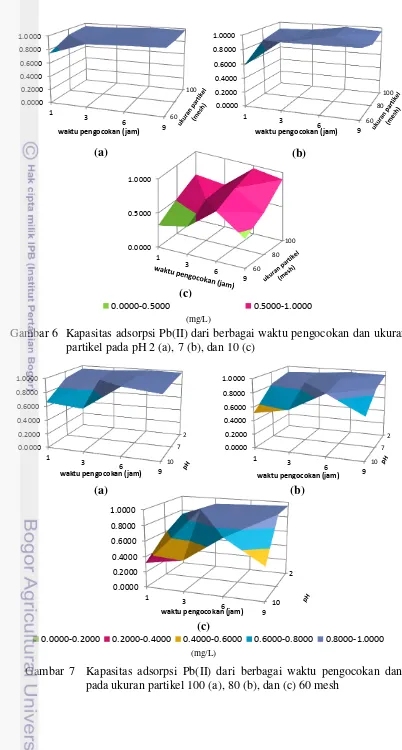
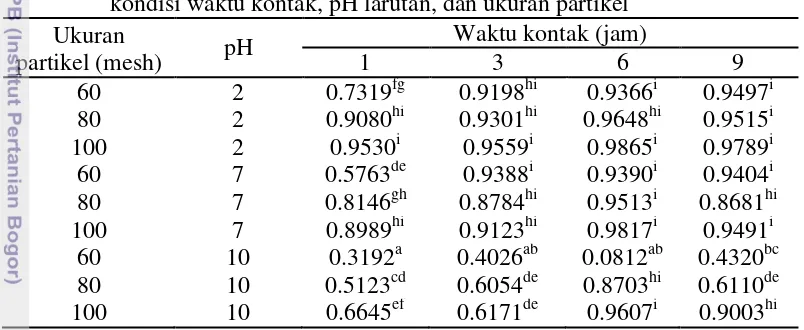
7 Kapasitas adsorpsi Pb(II) dari berbagai waktu pengocokan dan pH pada ukuran partikel 100 (a), 80 (b), dan (c) 60 mesh 10 8 Isoterm Langmuir (a) dan Freundlich (b) untuk adsorpsi Cr(VI) oleh
serbuk kulit batang karet 12
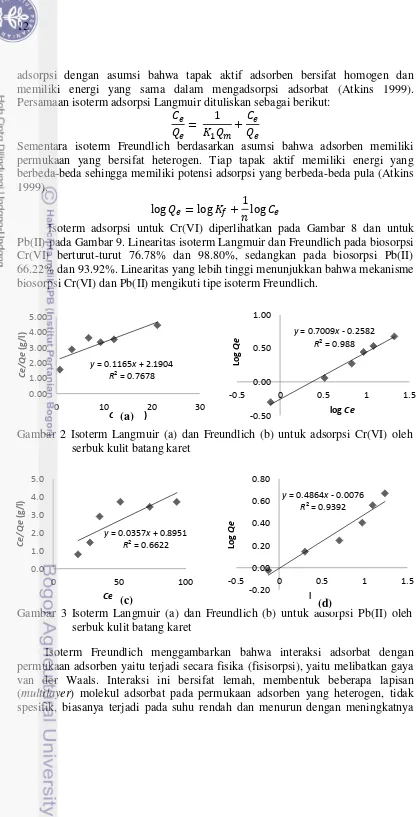
9 Isoterm Langmuir (a) dan Freundlich (b) untuk adsorpsi Pb(II) oleh
serbuk kulit batang karet 12
10 Pengaruh konsentrasi pada kapasitas dan efisiensi adsorpsi Cr(VI) (a)
DAFTAR LAMPIRAN
1 Diagram alir penelitian 18
2 Kurva kalibrasi Cr(VI) 19
3 Kurva kalibrasi Pb(II) 19
4 Penentuan kadar air serbuk kulit batang karet 20
5 Penentuan kadar kromium dan timbel di dalam kulit batang karet 20 6 Pengaruh waktu kontak, ukuran butir adsorben, dan pH pada biosorpsi
Cr(VI) 21
7 Sidik ragam kondisi terbaik adsorpsi Cr(VI) 24
8 Rerata nilai kapasitas adsorpsi Cr(VI) pada berbagai perlakuan 24 9 Pengaruh waktu kontak, ukuran butir adsorben, dan pH pada biosorpsi
Pb(II) 25
10 Sidik ragam kondisi terbaik adsorpsi Pb(II) 28
PENDAHULUAN
Karet merupakan tanaman tahunan yang tumbuh subur di daerah tropis dengan curah hujan yang cukup. Indonesia memiliki lahan perkebunan karet paling luas di dunia walaupun dari segi produksi, hanya menempati urutan kedua setelah Thailand (Dishutbun 2012). Tanaman ini merupakan sumber lateks yang kemudian akan diolah menjadi karet sintetik. Pada saat penyadapan lateks, kulit batang karet hanya dibuang tanpa pemanfaatan yang berarti dan akhirnya menjadi limbah pertanian.
Departemen Jenderal Pertanian Direktorat Perkebunan mencatat luas perkebunan karet di Sumatera Selatan pada tahun 2012 sebesar 662 686 ha. Jarak tanam antarpohon karet adalah 6×3 m2 sehingga jumlah pohon yang dapat ditanam untuk 1 ha sekitar 555 pohon. Pohon karet yang siap disadap adalah yang mempunyai lilit batang (diameter batang) minimum 45 cm dengan panjang irisan setengah diameter 22.5 cm. Tebal dan kedalaman sayatan setiap penyadapan ialah 2 dan 5 mm. Frekuensi penyadapan untuk 2 tahun pertama adalah 3 hari sekali dan untuk tahun berikutnya 2 hari sekali (SRAS 2005). Artinya, untuk 2 tahun pertama kulit yang terbuang sebanyak 218 467.7 m3 dan tahun ketiga 148 955.25 m3. Dengan demikian, rerata kulit batang karet yang terbuang di Sumsel per tahun sebanyak ± 122 474.32 m3. Data ini menunjukkan bahwa kulit karet limbah sadap cukup potensial dimanfaatkan.
Biosorben mempunyai keunggulan untuk mengatasi logam berbahaya dan beracun di lingkungan karena harganya yang relatif murah, mudah didapat, dan sifatnya yang ramah lingkungan (Shukla et al. 2002). Limbah pertanian yang sudah diteliti sebagai adsorben logam berat antara lain serbuk daun banyan (Ficus benghalensis L.) (Rao et al. 2013), kulit lada Ethiopia (Ajaelu et al. 2011), sabut kelapa (Kehinde et al. 2009), kulit buah Bauhinia racemosa (Chaudhari et al.
2012), dan kulit pisang (Ashraf et al. 2011).
Kulit batang efektif sebagai adsorben logam berat sebab di dalam kulit batang selain terdapat pori-pori, terkandung juga senyawa polihidroksi dari polifenol yang mampu mengelat ion logam berat (Gaballah dan Kilbertus 1998). Kulit batang merupakan lapisan luar kambium yang mengelilingi batang, cabang, dan akar. Susunan kimia kulit batang berbeda dari kayu karena adanya polifenol dan suberin (Sjӧstrӧm 1998). Suberin merupakan biopolimer kompleks dengan komponen polifenolik yang terikat pada dinding sel dan komponen polialifatik yang terletak di antara dinding sel dan membran plasma. Suberin bersama dengan lilin berfungsi melindungi permukaan tanaman dari kehilangan air dan serangan mikrob (Thomas et al. 2007).
Kulit batang tumbuhan telah dilaporkan dapat digunakan sebagai adsorben (biosorben) logam berat. Sarin dan Pant (2006) telah memanfaatkan kulit batang eukaliptus sebagai adsorben kromium. Biosorben lain berbasis pertanian untuk adsorben logam berat antara lain kulit batang pinus sebagai adsorben kadmium, timbel, dan kromium (Junior et al. 2012), kulit pinus termodifikasi-NaOH sebagai adsorben timbel (Argun dan Dursun 2007), dan kulit batang malapari (Pongamia pinata) untuk mengadsorpsi timbel (Mamatha et al. 2012).
2
penyamakan, metalurgi, dan manufaktur secara langsung maupun tidak langsung melepaskan kedua logam ini ke lingkungan, terutama ke perairan. Ketiadaan air bersih merupakan ancaman bagi keberlangsungan hidup manusia sebab timbel adalah logam berat yang beracun pada tingkat paparan sangat rendah dan memiliki efek akut dan kronis bagi kesehatan manusia. Paparan Pb(II) dapat menyebabkan kerusakan saraf/disfungsi saraf motorik, jantung, ginjal, kerusakan reproduksi, alergi lambung usus, hematologi, dan dampak perkembangan saraf pada anak-anak (UNEP 2010). Timbel juga menyebabkan asam urat, hipertensi, peningkatan risiko kardiovaskular, dan kanker (CDC 2012).
Kromium(VI) telah dilaporkan menimbulkan masalah kesehatan berupa muntah, nyeri perut, diare berdarah, dan gangguan peredaran darah pada awal terpapar (HPA 2007). Efek terhadap pernapasan dapat berupa iritasi hidung dan saluran pernapasan, kanker tenggorokan dan paru-paru. Jika terkena kulit dapat terjadi iritasi akut, sensasi terbakar dan ruam, dan alergi dermatitis, sedangkan jika terpapar pada saluran pencernaan, dapat menyebabkan gangguan perut dan pencernaan, bisul, kerusakan ginjal dan hati, kanker perut dan saluran pencernaan (OHA 2012).
Penelitian ini bertujuan menentukan kemampuan kulit batang karet yang diperoleh dari Tanjung Enim (Sumatera Selatan) sebagai biosorben larutan Cr(VI) dan Pb(II). Kondisi optimum adsorpsi ditentukan dengan parameter meliputi pH, ukuran partikel biosorben, dan waktu kontak, kemudian persamaan isoterm adsorpsi yang sesuai serta serta kapasitas adsorpsinya dihitung.
METODE
Tahapan penelitian meliputi preparasi adsorben kulit batang karet, optimasi adsorpsi Cr(VI) dan Pb(II), penetapan pola isoterm adsorpsi, dan penentuan kapasitas adsorpsi. Kulit batang karet dikeringkan dan dihancurkan, lalu diayak hingga ukuran partikel 60, 80, dan 100 mesh. Metode adsorpsi yang digunakan adalah metode tumpak, yaitu pengadukan adsorben dalam larutan ion adsorbat. Optimasi adsorpsi melibatkan parameter pH (2, 7, dan 10), ukuran partikel biosorben (60, 80, dan 100 mesh), serta waktu kontak (1, 3, 6, dan 9 jam), kemudian dilakukan penentuan isoterm adsorpsi dan kapasitas adsorpsi (Lampiran 1).
Konsentrasi Cr(VI) dan Pb(II) ditentukan dengan membuat kurva standar pada konsentrasi 0.2, 0.5, 1, dan 2 ppm untuk Cr(VI) (Lampiran 2) dan 0.3, 0.65, 1, 2, dan 3 ppm untuk Pb(II) (Lampiran 3). Konsentrasi sampel, meliputi larutan Cr(VI) dan Pb(II) sebelum dan sesudah diadsorpsi serta larutan standar, diukur menggunakan spektrofotometer serapan atom (SSA) pada panjang gelombang 248.3 nm untuk kromium dan 217 nm untuk konsentrasi timbel.
Bahan dan Alat
NaOH 1 M, HCl1 M, indikator universal, dan air bebas ion. Semua bahan kimia yang dipakai memiliki kualitas analisis (analytical grade).
Alat-alat yang digunakan dalam penelitian ini ialah SSA Shimadzu AA-7000, gerinda (mesin penggiling), alat kocok, ayakan ukuran 60, 80, dan 100 mesh, neraca analitik, dan alat-alat kaca.
Preparasi Biosorben Kulit Batang Karet (Mulgund et al. 2011)
Kulit batang karet dicuci dengan akuades kemudian dikering-udarakan di bawah sinar matahari selama 7 hari. Setelah itu, kulit batang karet dihaluskan, lalu diayak secara bertingkat dengan ayakan 60, 80, dan 100 mesh. Serbuk biosorben lolos ayakan 60, 80, dan 100 mesh telah siap digunakan dan disimpan dalam kantong plastik kedap udara. Serbuk biosorben terlebih dahulu ditentukan kadar air dan kadar logam beratnya (kromium dan timbel).
Penentuan Kadar Air Kulit Batang Karet (SNI 08-7070-2005)
Metode uji merujuk SNI 08-7070-2005 tentang cara uji kadar air pulp dan kayu. Wadah terlebih dahulu dipanaskan dalam oven pada suhu (105 ± 3) oC selama 1 jam, kemudian dipindahkan ke dalam desikator, didiamkan kira-kira 10 menit, dan ditimbang. Pemanasan dan penimbangan diulangi sampai diperoleh bobot tetap. Selanjutnya sampel sebanyak (2 ± 0.1000) g dimasukkan ke dalam wadah tersebut. Wadah berisi sampel lalu dipanaskan selama 3 jam pada suhu (105 ± 3) oC. Setelah itu, sampel didinginkan dalam desikator kira-kira 10 menit dan ditimbang. Pemanasan dan penimbangan diulangi sampai diperoleh bobot tetap.
Penentuan Konsentrasi Pb dan Cr dalam Sampel Biosorben
Larutan sampel terlebih dahulu disiapkan melalui proses destruksi basah (dalam SNI 01-3751-2006 tentang uji tepung terigu). Sampel serbuk batang karet sebanyak 5 g dimasukkan ke dalam erlenmeyer 250 mL dan ditambahkan HNO3(p)-HCl(p) 1:3 sebanyak 12 mL. Campuran dipanaskan di atas hot plate selama 30 menit sampai uapnya hilang dan campuran menjadi jernih, kemudian didinginkan dan disaring. Filtrat diencerkan dengan air bebas ion dalam labu takar 50 mL dan dibuat pH 2 sampai 4. Larutan filtrat diukur dengan SSA pada 248.3 nm (kromium) dan 217 nm (timbel). Perlakuan diulangi sebanyak 3 kali.
Penentuan Kondisi Adsorpsi Terbaik
4
Yijkl= μ + αi+ j+ k+ (α )ij+ (α )ik+ ( )jk+ (α )ijk+ εijkl
dengan
Yijkl = Nilai pengamatan pada masing-masing ukuran partikel ke-i, pH larutan
ke-j, dan pengaruh waktu kontak ke-k
μ = Rataan umum
αi = Pengaruh ukuran partikel ke-i j = Pengaruh pH larutan ke-j k = Pengaruh waktu kontak ke-k
(α )ij = Interaksi pengaruh ukuran partikel ke-i dengan pH larutan ke-j
(α )ik = Interaksi pengaruh ukuran partikel ke-i dengan waktu kontak ke-k
( )jk = Interaksi pengaruh pH larutan ke-j dengan waktu kontak ke-k
(α )ijk = Interaksi pengaruh ukuran partikel ke-i, pH larutan ke-j, dan waktu kontak ke-k
εijkl = Galat percobaan
Ke dalam botol plastik 100 mL dimasukkan 25 mL larutan Cr(VI) atau Pb(II) 20 ppm dengan variasi pH yang telah ditentukan, lalu ditambahkan (0.5 ± 0.01) g adsorben. pH diatur dengan penambahan HCl 1 M atau NaOH 1 M. Campuran kemudian diaduk dengan alat pengocok pada variasi waktu yang telah ditentukan. Campuran selanjutnya disaring dan filtratnya diambil untuk ditentukan konsentrasi Pb(II) dan Cr(VI) setelah adsorpsi. Konsentrasi awal adsorbat juga ditentukan menggunakan kurva standar. Kapasitas penjerapan biosorben terhadap Cr(VI) dan Pb(II) dihitung dengan rumus
dengan Q = kapasitas penjerapan bisosorben (µg/g)
V = volume larutan (mL)
C0 = konsentrasi awal larutan (µg/mL) C = konsentrasi akhir larutan (µg/mL)
m = bobot biosorben (g)
Data yang diperoleh diolah menggunakan perangkat lunak SPSS 16.0. Pengaruh faktor ukuran partikel, pH larutan, dan waktu kontak pada penjerapan Cr(VI) dan Pb(II) oleh biosorben ditentukan melalui analisis keragaman dengan kriteria apabila nilai-p< α (0.05), berarti pengaruh faktor pada respons yang diuji adalah nyata atau sangat nyata pada tingkat kepercayaan 95%. Perlakuan yang berpengaruh pada respons dalam analisis ragam diuji lebih lanjut dengan menggunakan uji kisaran berganda Duncan (DMRT) (Matjik dan Sumertajaya 2006).
Penentuan Isoterm dan Kapasitas Adsorpsi
dengan alat pengocok sesuai waktu terbaik yang diperoleh. Selanjutnya campuran disaring dan diambil filtratnya untuk penentuan konsentrasi Pb(II) dan Cr(VI) setelah adsorpsi.
Data yang diperoleh digunakan untuk penentuan pola isoterm adsorpsi dan kapasitas adsorpsinya. Pola isoterm adsorpsi diperoleh dengan membuat kurva regresi linear menggunakan persamaan Langmuir dan Freundlich. Kurva isoterm Langmuir menghubungkan konsentrasi (ppm) kesetimbangan adsorbat dalam larutan setelah adsorpsi (Ce) sebagai sumbu x dengan nisbah konsentrasi
kesetimbangan tersebut dengan jumlah adsorbat yang teradsorpsi per satuan bobot adsorben (Ce/Qe) dengan satuan g/L sebagai sumbu y, sedangkan kurva isoterm
Freundlich menghubungkan logaritma Ce sebagai sumbu x dan logaritma Qe
sebagai sumbu y.
HASIL DAN PEMBAHASAN
Biosorben Serbuk Kulit Batang Karet
Penyiapan adsorben dalam bentuk serbuk halus bertujuan meningkatkan kinerjanya. Getah sisa penyadapan yang masih menempel pada kulit batang karet harus dibersihkan terlebih dahulu agar tidak merusak mesin penggiling dan setelah itu dicuci dengan air sebanyak 3 kali. Pencucian dilakukan secara berulang untuk memastikan kulit bebas dari kotoran (seperti tanah dan lumut) dan ion-ion yang mungkin terkandung. Setelah dijemur, kulit karet digiling dan diayak dengan ayakan 60, 80, dan 100 mesh. Variasi tersebut diperlukan karena daya adsorpsi terhadap Cr(VI) dan Pb(II) sangat ditentukan oleh gugus aktif dan pori-pori yang dipengaruhi oleh luas permukaan adsorben. Secara umum, semakin kecil ukuran partikel, luas permukaan biosorben akan semakin besar yang menyebabkan daya adsorpsinya semakin besar. Setelah pencucian, penggilingan, dan pengayakan, kulit batang karet tidak mengalami perubahan fisik seperti warna dan tekstur. Hasil serbuk kulit batang karet dapat dilihat pada Gambar 1.
Kadar air ditentukan untuk menjaga mutu serbuk agar tidak berjamur dan berserangga. Di negara-negara beriklim sedang, kadar air penyimpanan biji-bijian yang ideal adalah di bawah 13% untuk penyimpanan lebih dari 9 bulan, sedangkan untuk penyimpanan yang singkat, kadar air dapat mencapai 14% (Maryam 2006). Pada penelitian ini, serbuk lolos ayakan 100 mesh yang digunakan untuk adsorpsi mempunyai kadar air sebesar 13.71% (Lampiran 4).
Biosorben dikemas dalam plastik kedap udara agar tidak terkontaminasi dari lingkungan luar baik faktor biotik maupun abiotik. Ruang simpan yang terbuka
(i) (ii) (iii)
6
berhubungan langsung dengan lingkungan sekitar dan dapat mencemari bahan baik berupa pencemar mikro (mikrob) maupun makro (serangga). Penyimpanan di ruang terbuka juga menyebabkan daya simpan bahan menjadi singkat akibat fluktuasi suhu dan kelembapan (Robi’in β007). Penelitian yang sama menunjukkan bahwa kemasan aluminum foil paling baik untuk menyimpan bahan
sampai periode simpan 4 minggu karena dapat mempertahankan kenaikan kadar
air lebih rendah (1–2% setiap 2 minggu) daripada kemasan plastik (sekitar 3% setiap 2 minggu). Namun, setelah 6 minggu, kadar air meningkat hingga 13% pada penyimpanan menggunakan aluminum foil, sedangkan kenaikan kadar air bahan pada kemasan plastik cenderung stabil. Penelitian ini membutuhkan waktu penyimpanan yang lama, maka kemasan plastik dipilih untuk menyimpan serbuk kulit batang karet.
Analisis kromium dan timbel pada biosorben ukuran 100 mesh bertujuan menentukan kadar kedua logam berat tersebut dalam bahan sehingga kapasitas adsorpsi biosorben dapat diukur dengan tepat. Kadar logam diukur dengan AAS nyala sehingga diperlukan proses pelarutan sampel yang diawali dengan proses destruksi basah. Hasil analisis menunjukkan bahwa tidak terkandung kromium dan timbel pada biosorben (Lampiran 5).
Kondisi Terbaik Biosorpsi Cr(VI)
Setiap biosorben mempunyai karakteristik yang berbeda bergantung pada bahan-bahan penyusun yang terkandung di dalamnya dan sifat adsorbat. Parameter yang digunakan pada penentuan kondisi terbaik meliputi pH larutan, waktu kontak, dan ukuran partikel yang menghasilkan biosorpsi logam berat secara optimum dan efisien. Data kapasitas adsorpsi Cr(VI) pada Lampiran 6 menunjukkan bahwa kapasitas adsorpsi terbesar terjadi pada waktu pengocokan selama 3 jam, pH 2, dan ukuran partikel 100 mesh (Gambar 3–5). Menurut Agarwal et al. (2006), pada pH rendah, ion HCrO4− paling dominan dan permukaan biosorben juga terprotonasi. Hal ini menyebabkan ion HCrO4− dengan mudah dipertukarkan dengan ion OH− dari permukaan biosorben. Kenaikan pH menurunkan kapasitas adsorpsi. Ketika pH meningkat, secara keseluruhan muatan permukaan biosorben menjadi negatif dan biosorpsi menurun.
100
8
Kapasitas adsorpsi dari interaksi antarperlakuan (Tabel 1) memperlihatkan kapasitas adsorpsi terbesar ialah 0.55 mg/g, terjadi pada waktu kontak 6 jam, pH 2, dan ukuran partikel 100 mesh. Agar lebih efisien dari segi waktu dan tenaga, nilai tersebut dibandingkan dengan nilai kapasitas adsorpsi dari kondisi lainnya. Pada waktu kontak 1 jam, pH 2, dan ukuran partikel 100 mesh, kapasitas adsorpsi yang dihasilkan tidak berbeda nyata (dilihat dari superskrip yang sama). Jadi, kondisi terbaik untuk biosorpsi Cr(VI) adalah waktu kontak selama 1 jam, pH 2, dan ukuran partikel 100 mesh.
Tabel 1 Kapasitas adsorpsi biosorben terhadap Cr(VI) 20 mg/L pada variasi kondisi ukuran partikel, pH larutan, dan waktu kontak
Ukuran
Keterangan: Superskrip yang berbeda pada baris yang sama menunjukkan perbedaan yang sangat
60
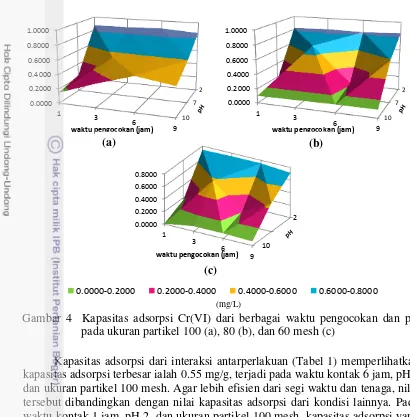
Data kapasitas adsorpsi Pb(II) pada Lampiran 9 menunjukkan bahwa kapasitas adsorpsi terbesar diperoleh pada waktu pengocokan 6 jam, pH 2, dan ukuran partikel 100 mesh (Gambar 5−7). Namun, kondisi terbaik untuk adsorpsi Pb(II) sulit ditentukan karena nilai kapasitas adsorpsi dari setiap variasi perlakuan tidak berbeda jauh, kecuali pada pH 10. Agar didapatkan hasil yang akurat untuk penentuan kondisi terbaik, dilakukan pengujian sidik ragam (ANOVA), yang hasilnya disajikan pada Lampiran 10.
10
Gambar 6 Kapasitas adsorpsi Pb(II) dari berbagai waktu pengocokan dan ukuran partikel pada pH 2 (a), 7 (b), dan 10 (c)
(mg/L)
Hasil sidik ragam tersebut menunjukkan bahwa variasi waktu kontak, pH larutan, ukuran partikel, dan interaksi ketiganya memberikan pengaruh nyata pada kapasitas adsorpsi Pb(II) dalam selang kepercayaan 95%. Oleh karena itu, dilakukan uji lanjut Duncan. Hasil uji Duncan (Lampiran 11) menunjukkan bahwa setiap tingkat perlakuan tunggal memberikan pengaruh yang sangat nyata pada kapasitas adsorpsi Pb(II). Artinya, setiap pengubahan tingkat menyebabkan nilai kapasitas adsorpsi Pb(II) berbeda nyata.
Kapasitas adsorpsi dari interaksi antarperlakuan (Tabel 2) menunjukkan kapasitas adsorpsi terbesar ialah 0.99 mg/g, terjadi pada waktu kontak 6 jam, pH 2, ukuran partikel 100 mesh. Interaksi antara waktu kontak (1, 3, 6, dan 9 jam), pH larutan (pH 2 dan 7), dan ukuran partikel (80 dan 100 mesh) tidak memberikan pengaruh yang nyata pada kapasitas adsorpsi Pb(II). Jadi, kondisi terbaik yang dipilih untuk biosorpsi Pb(II) adalah waktu kontak selama 1 jam, pH 7, dengan ukuran partikel 100 mesh.
Tabel 2 Kapasitas adsorpsi biosorben terhadap Pb(II) 20 mg/L pada variasi kondisi waktu kontak, pH larutan, dan ukuran partikel
Ukuran
partikel (mesh) pH
Waktu kontak (jam)
1 3 6 9
60 2 0.7319fg 0.9198hi 0.9366i 0.9497i
80 2 0.9080hi 0.9301hi 0.9648hi 0.9515i
100 2 0.9530i 0.9559i 0.9865i 0.9789i
60 7 0.5763de 0.9388i 0.9390i 0.9404i
80 7 0.8146gh 0.8784hi 0.9513i 0.8681hi
100 7 0.8989hi 0.9123hi 0.9817i 0.9491i
60 10 0.3192a 0.4026ab 0.0812ab 0.4320bc
80 10 0.5123cd 0.6054de 0.8703hi 0.6110de 100 10 0.6645ef 0.6171de 0.9607i 0.9003hi
Keterangan: superskrip yang berbeda pada baris yang sama menunjukkan perbedaan yang sangat
nyata (P < 0.05)
Penelitian menunjukkan pH 2 sebagai pH terbaik walaupun tidak berbeda nyata dengan pH 7. Menurut Kumar dan Gayathri (2009), biosorpsi Pb(II) terjadi pada pH sekitar 5 (pH asam). Pada pH rendah (di bawah 3), terjadi protonasi yang terlalu banyak pada permukaan biosorben sehingga adsorpsi Pb(II) oleh biosorben menurun. Sebaliknya, peningkatan pH hingga 6 menyebabkan ion H+ dilepaskan dari tapak aktif biosorben dan adsorpsi menjadi meningkat. Kenaikan pH yang lebih tinggi lagi menyebabkan ion OH− terlepas dari tapak aktif biosorben sehingga terjadi reaksi antara Pb2+ dan OH− menjadi Pb(OH)2 yang berupa endapan putih. Endapan ini akan menghalangi proses adsorpsi (Argun et al. 2006). Endapan tersebut teramati juga pada penelitian ini pada saat pengaturan pH 10
Pola Isoterm Adsorpsi
12
adsorpsi dengan asumsi bahwa tapak aktif adsorben bersifat homogen dan memiliki energi yang sama dalam mengadsorpsi adsorbat (Atkins 1999). Persamaan isoterm adsorpsi Langmuir dituliskan sebagai berikut:
Sementara isoterm Freundlich berdasarkan asumsi bahwa adsorben memiliki permukaan yang bersifat heterogen. Tiap tapak aktif memiliki energi yang berbeda-beda sehingga memiliki potensi adsorpsi yang berbeda-beda pula (Atkins 1999).
Isoterm adsorpsi untuk Cr(VI) diperlihatkan pada Gambar 8 dan untuk Pb(II) pada Gambar 9. Linearitas isoterm Langmuir dan Freundlich pada biosorpsi Cr(VI) berturut-turut 76.78% dan 98.80%, sedangkan pada biosorpsi Pb(II) 66.22% dan 93.92%. Linearitas yang lebih tinggi menunjukkan bahwa mekanisme biosorpsi Cr(VI) dan Pb(II) mengikuti tipe isoterm Freundlich.
Isoterm Freundlich menggambarkan bahwa interaksi adsorbat dengan permukaan adsorben yaitu terjadi secara fisika (fisisorpsi), yaitu melibatkan gaya van der Waals. Interaksi ini bersifat lemah, membentuk beberapa lapisan (multilayer) molekul adsorbat pada permukaan adsorben yang heterogen, tidak spesifik, biasanya terjadi pada suhu rendah dan menurun dengan meningkatnya
suhu. Kalor adsorpsinya berkisar 20−40 kJ/mol dan bersifat dapat balik (Saxena 2005).
Gugus aktif maupun pori-pori disebabkan oleh adanya selulosa, hemiselulosa, dan lignin. Selulosa tersusun atas unit-unit glukosa yang distabilkan oleh ikatan hidrogen yang kuat di sepanjang rantai. Gugus fungsi dalam rantai selulosa adalah gugus hidroksil yang merupakan tapak aktif untuk interaksi pengikatan logam pada adsorpsi logam. Rantai selulosa diikat bersama-sama membentuk mikrofibril yang sangat kristalin. Secara alami, selulosa berikatan dengan zat lain, yaitu hemiselulosa dan lignin yang berfungsi sebagai perekat antarsel selulosa dan trakeida (sekumpulan sel dengan dinding sel lateralnya). Susunan inilah yang menyebabkan struktur kulit kayu membentuk potongan-potongan serat yang memanjang, kontinu, berpori, dan saling menumpuk (Siquera et al. 2010).
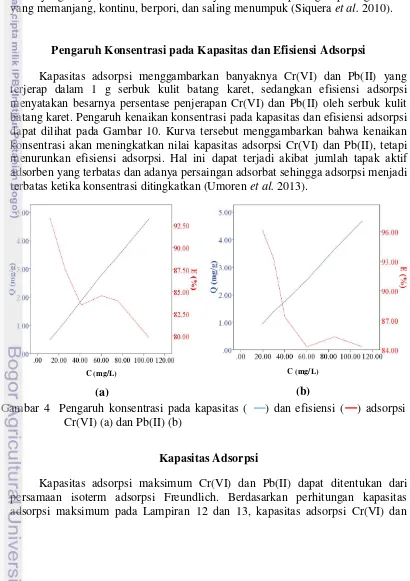
Pengaruh Konsentrasi pada Kapasitas dan Efisiensi Adsorpsi
Kapasitas adsorpsi menggambarkan banyaknya Cr(VI) dan Pb(II) yang terjerap dalam 1 g serbuk kulit batang karet, sedangkan efisiensi adsorpsi menyatakan besarnya persentase penjerapan Cr(VI) dan Pb(II) oleh serbuk kulit batang karet. Pengaruh kenaikan konsentrasi pada kapasitas dan efisiensi adsorpsi dapat dilihat pada Gambar 10. Kurva tersebut menggambarkan bahwa kenaikan konsentrasi akan meningkatkan nilai kapasitas adsorpsi Cr(VI) dan Pb(II), tetapi menurunkan efisiensi adsorpsi. Hal ini dapat terjadi akibat jumlah tapak aktif adsorben yang terbatas dan adanya persaingan adsorbat sehingga adsorpsi menjadi terbatas ketika konsentrasi ditingkatkan (Umoren et al. 2013).
Kapasitas Adsorpsi
Kapasitas adsorpsi maksimum Cr(VI) dan Pb(II) dapat ditentukan dari persamaan isoterm adsorpsi Freundlich. Berdasarkan perhitungan kapasitas adsorpsi maksimum pada Lampiran 12 dan 13, kapasitas adsorpsi Cr(VI) dan
C (mg/L) C (mg/L)
Gambar 4 Pengaruh konsentrasi pada kapasitas ( ) dan efisiensi ( ) adsorpsi Cr(VI) (a) dan Pb(II) (b)
14
Pb(II) berturut-turut sebesar 0.55 dan 0.98 mg/g. Telah banyak penelitian mengenai biosorpsi Cr(VI) dan Pb(II) dengan menggunakan limbah pertanian khususnya kulit pohon.
Jika biosorben serbuk kulit batang karet dibandingkan dengan biosorben yang lain tersebut (Tabel 3), kapasitas adsorpsi Cr(VI) terbesar diperoleh dari kulit batang eukaliptus. Hal ini dikarenakan adanya modifikasi pada kulit batang eukaliptus, yaitu penghilangan warna oleh formaldehida sehingga gugus aktif permukaannya semakin banyak dan kapasitas adsorpsinya menjadi semakin besar. Kapasitas adsorpsi Pb(II) terbesar diperoleh dari kulit pisang. Kulit pisang mengandung lebih banyak gugus fungsi dibandingkan dengan kulit batang karet. Menurut Castro et. al. (2011), kulit pisang mengandung karbohidrat, protein, lipid, dan serat, sedangkan kulit batang karet hanya mengandung selulosa, hemiselulosa, dan polifenol.
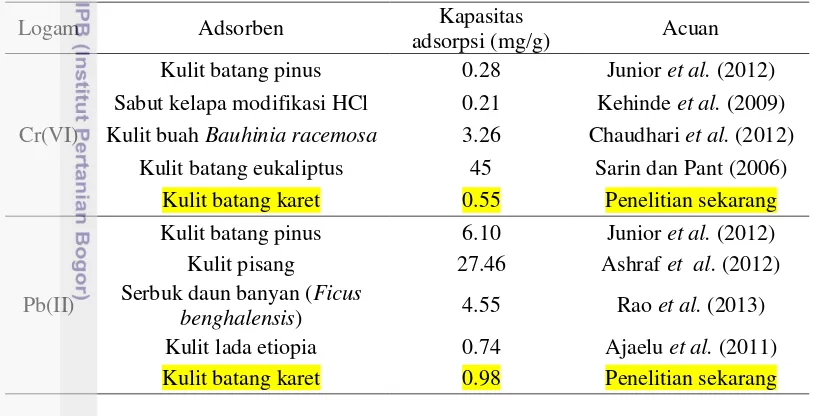
Tabel 3 Perbandingan kapasitas adsorpsi pada berbagai biosorben mengikuti mekanisme isoterm Freundlich
Logam Adsorben Kapasitas
adsorpsi (mg/g) Acuan
Cr(VI)
Kulit batang pinus 0.28 Junior et al. (2012)
Sabut kelapa modifikasi HCl 0.21 Kehinde et al. (2009) Kulit buah Bauhinia racemosa 3.26 Chaudhari et al. (2012)
Kulit batang eukaliptus 45 Sarin dan Pant (2006)
Kulit batang karet 0.55 Penelitian sekarang
Pb(II)
Kulit batang pinus 6.10 Junior et al. (2012)
Kulit pisang 27.46 Ashraf et al. (2012)
Serbuk daun banyan (Ficus
benghalensis) 4.55 Rao et al. (2013)
Kulit lada etiopia 0.74 Ajaelu et al. (2011)
Kulit batang karet 0.98 Penelitian sekarang
SIMPULAN DAN SARAN
Simpulan
Serbuk kulit batang karet dapat digunakan sebagai biosorben ion Cr(VI) dan Pb(II). Kondisi terbaik adsorpsi Cr(VI) terjadi pada waktu kontak selama 1 jam, pH larutan 2, ukuran partikel 100 mesh, sedangkan biosorpsi maksimum Pb(II) terjadi pada waktu kontak selama 1 jam, pH larutan 7, dan ukuran partikel 100 mesh.
Saran
Berdasarkan hasil penelitian ini, tahapan selanjutnya yang perlu dilakukan adalah menerapkan serbuk kulit batang karet sebagai biosorben pada limbah sebenarnya (limbah laboratorium atau pabrik). Modifikasi biosorben secara fisika atau kimia perlu dilakukan agar kapasitas dan efisiensi adsorpsi kedua logam tersebut dapat ditingkatkan. Desorpsi juga perlu dilakukan agar biosorben dapat dimanfaatkan kembali.
DAFTAR PUSTAKA
Agarwal GS, Bhuptawat HK, Chaudhari S. 2006. Biosorption of aqueous chromium (VI) by Tamarindus indica seeds. Biores Technol. 97:949-956. Ajaelu CJ, Ikotun AA, Olutona OO, Ibironke OL. 2011. Biosorption of aqueous
solutions of lead on Xylopia aethiopica (ethiopian pepper). J Appl Sci Environ Sanitation. 6(3):269-277.
Argun ME, Dursun S, Ozdemir C, Karatas M. 2006. Heavy metal adsorption by modified oak sawdust: thermodynamics and kinetics. J Hazardous Mat.
141:77-85. doi:10.1016/j.jhazmat.2006.06.095
Argun ME, Dursun S. 2007. Activation of pine bark surface with NaOH for lead removal. J Int Environ Appl Sci. 2(1&2):5-10.
Ashraf MA, Mahmood K, Wajid A. 2011. Study of low cost biosorbent for biosorption of heavy metals. Int Conf Food Eng Biotechnol. 9:60-68.
Atkins PW. 1999. Kimia Fisika. Ed Ke-4. Jilid I. Kartohadiprodjo II, penerjemah. Jakarta (ID): Erlangga. Terjemahan dari: Physical Chemistry.
[BSN] Badan Standardisasi Nasional. 2006. SNI 01-3751-2006. Tepung gandum. Jakarta (ID): BSN.
[BSN] Badan Standardisasi Nasional. 2005. SNI 08-7070-2005. Cara uji kadar air pulp dan kayu dengan metode pemanasan dalam oven. Jakarta (ID): BSN. Castro RSD, Caetano L, Ferreira G, Padilha PM, Saeki MJ, Zara LF, Martines
MAU, Castro GR. 2011. Banana peel applied to the solid phase extraction of copper and lead from river water: preconcentration of metal ions with a fruit waste. Ind Eng Chem Res. 50:3446-3451. doi: 10.1021/ie101499e. [CDC] Centers for Disease Control and Prevention. 2012. Lead in Drinking Water
and Human Blood Lead Levels in the United States. Atlanta (US): Morbidity and Mortality Weekly Report.
Chaudhari UE, Shekar RS, Wanjari AK. 2012. Studies in the adsorption of environmentally relevant Cr(VI) metal by using granulated particle of
Bauhinia racemosa fruit shell. Int J Chem Sci Technol.2(4):61-64.
16
Gaballah I, Kilbertus G. 1998. Recovery of heavy metals ions through decontamination of synthetics solutions and industrial effluents using modified barks. J Geochem Explor. 62:241-286.
Junior ACG, Strey L, Lindino CA, Nacke H, Schwantes D, Seidel EP. 2012. Applicability of the Pinus bark (Pinus elliottii) for the adsorption of toxic heavy metals from aqueous solutions. Acta Scientiarum Tech. 34(1):79-87. doi: 10.4025/actascitechnol.v34i1.9585
[HPA] Health Protection Agency. 2007. Chromium. Bedfordshire (UK): Cranfield Univ.
Kehinde OO, Oluwatoyin TA, Aderonke OO, 2009. Comparative analysis of the efficiencies of two low cost adsorbents in the removal of Cr(VI) and Ni(II) from aqueous solution.African J Environ Sci Technol. 3(11):360-369
Kumar PS, Gayathri R. 2009. Adsorption of Pb2+ ions from aqueous solutions onto bael tree leaf powder: isotherms, kinetics and thermodynamics study. J Eng Sci Tech. 4(4):381-399.
Mamatha M, Aravinda HB, Manjappa S, Puttaiah ET. 2012. Kinetics and mechanism for adsorption of lead in aqueous and industrial effluent from
Pongamia pinnata tree bark. J Environ Sci Toxicol Food Tech. 2(3):1-9. Maryam R. 2006. Pengendalian terpadu kontaminasi mikotoksin. Wartazoa.
16(1):21-30.
Matjik AA, Sumertajaya IM. 2006. Perancangan Percobaan dengan Aplikasi SAS dan Minitab. Bogor (ID): IPB Pr.
Mulgund MG, Kulal PM, Mulgund GV. 2011. Sorption kinetics and intraparticulate diffusivity of heavy metals biosorption by Cassia angustifolia from aqueous solution. Int J Chem Sci Appl. 2(3):194-199. [OHA] Oregon Health Authority. 2012. Health Effects Information: Chromium
Hexavalent. Portland (US): Oregon Government.
Rao LN, Prabhakar G, Shaik F. 2013. Biosorption of lead ions from aqueous solution by Ficus benghalensis L: equilibrium & kinetic studies. Asian J Biochem Pharmaceut Res. 3(1):158-167.
Robi’in. β007. Perbedaan bahan kemasan dan periode simpan dan pengaruhnya terhadap kadar air benih jagung dalam ruang simpan terbuka. Bul Teknik Pertanian. 12(1):7-9.
Sarin V, Pant KK.. 2006. Removal of chromium from industrial waste by using eucalyptus bark. Biores Technol. 97(1):15-20
Saxena PB. 1998. IIT Chemistry. Meerut (IN): Krishna Prakashan Media.
Shukla A, Zhang YH, Dubey P, Margravw JL, Shukla S. 2002. The role of sawdust in the removal of unwanted materials from water. J Hazardous Mat.
9:137-157.
Siqueira G, Bras J, Dufresne A. 2010. Cellulosic bionanocomposites: a review of preparation, properties and applications. Polymers. 2:728-765.
Sjӧstrӧm E. 1998. Kimia Kayu, Dasar-dasar dan Penggunaan. Ed ke-2. Sastrohamidjojo H, penerjemah. Yogyakarta (ID): Gadjah Mada Univ Pr. Terjemahan dari: Wood Chemistry, Fundamentals and Applications.
[SRAS] Smallholder Rubber Agroforestry System. 2005. Penyadapan Tanaman Karet. Sembawa (ID): Balit Sembawa.
and relationship to partial resistance to Phytophthora sojae. Plant Physiol.
144:299-311. doi: 10.1104/pp.106.091090
Umoren SA, Etim UJ, Israel AU. 2013. Adsorption of methylene blue from industrial effluent using poly(vinyl alcohol). J Mat Environ Sci. 4(1):75-86. [UNEP] United Nations Environment Programme. 2010. Final Review of
18
Lampiran 1 Diagram alir penelitian
Kulit batang karet
Serbuk kulit batang karet
Biosorben
Kapasitas adsorpsi pada pH 2, 7, dan 10
Kondisi optimum biosorpsi
Pola isoterm adsorpsi
Penentuan kapasitas adsorpsi Penentuan kapasitas
adsorpsi maksimum Kapasitas adsorpsi pada ukuran partikel
60, 80, dan 100 mesh
Kapasitas adsorpsi pada waktu kontak 1, 3, 6, dan 9 jam Penentuan kadar air
Penentuan kadar Cr(VI) dan Pb(II)
Dicuci
Dikeringkan
Dihaluskan
Lampiran 2 Kurva kalibrasi Cr(VI)
Lampiran 3 Kurva kalibrasi Pb(II)
20
Lampiran 4 Penentuan kadar air serbuk kulit batang karet
Ulangan Bobot Kadar air
m0 (g) m1 (g) (%)
1 2.0004 1.7247 13.7822
2 2.0005 1.7233 13.8565
3 2.0002 1.7304 13.4886
Rerata 13.7091
Keterangan: m0 = bobot sampel sebelum pemanasan (g)
m1 = bobot sampel setelah pemanasan (g)
Contoh perhitungan: adar air = 0 1
0 100
= β 000 1 7 β 0004 100 = 1γ 71
Lampiran 5 Penentuan kadar kromium dan timbel di dalam kulit batang karet Logam
berat Ulangan
Volume larutan
(mL)
Bobot sampel
(g)
Absorbans Konsentrasi (mg/L)
Kadar (mg/g)
Cr 1 50 5.0020 -0.0009 0.0000 0.00
2 50 5.0002 -0.0015 0.0000 0.00
3 50 5.0032 -0.0006 0.0000 0.00
Rerata 0.00
Pb 1 50 5.0009 -0.0008 0.0000 0.00
2 50 5.0015 -0.0010 0.0000 0.00
3 50 5.0011 -0.0007 0.0000 0.00
Rerata 0.00 Contoh perhitungan (konsentrasi Cr(VI)) :
y = 0.0432x + 0.0022 y = 0 04γβx + 0 00ββ -0 0009 = 0 04γβx+0 00ββ
0 04γβx = - 0 00γ1 x = -1γ 9γ
Lampiran 6 Pengaruh waktu kontak, pH, dan ukuran butir adsorben pada biosorpsi Cr(VI)
No Waktu
Ukuran
partikel pH Ulangan m C0 A C E Q
(jam) (mesh) ( g) (ppm) (ppm) (%) (mg/g)
1 6 100 2 1 0.5001 20.0000 0.0258 1.9798 90.10 0.9008
2 6 100 2 2 0.5001 20.0000 0.0305 2.2147 88.93 0.8891
3 6 100 2 3 0.5001 20.0000 0.0337 2.4832 87.58 0.8757
4 6 100 7 1 0.5000 20.0000 0.1046 8.4311 57.84 0.5784
5 6 100 7 2 0.5000 20.0000 0.1032 8.3137 58.43 0.5843
6 6 100 7 3 0.5000 20.0000 0.1035 8.3388 58.31 0.5831
7 6 100 10 1 0.4999 20.0000 0.1277 10.3690 48.15 0.4816
8 6 100 10 2 0.4999 20.0000 0.0531 10.2767 48.62 0.4863
9 6 100 10 3 0.4999 20.0000 0.0521 10.0670 49.66 0.4967
10 6 80 2 1 0.5000 20.0000 0.1563 3.5259 82.37 0.8237
11 6 80 2 2 0.5000 20.0000 0.1560 3.5191 82.40 0.8240
12 6 80 2 3 0.5000 20.0000 0.1570 3.5417 82.29 0.8229
13 6 80 7 1 0.5000 20.0000 0.6917 15.6496 21.75 0.2175
14 6 80 7 2 0.5000 20.0000 0.6954 15.7334 21.33 0.2133
15 6 80 7 3 0.5000 20.0000 0.6441 14.5717 27.14 0.2714
16 6 80 10 1 0.5000 20.0000 0.7837 15.1526 24.24 0.2424
17 6 80 10 2 0.5000 20.0000 0.7849 17.7600 11.20 0.1120
18 6 80 10 3 0.5000 20.0000 0.7862 17.7895 11.05 0.1105
19 6 60 2 1 0.5000 20.0000 0.2424 5.4756 72.62 0.7262
20 6 60 2 2 0.5000 20.0000 0.2073 4.6807 76.60 0.7660
21 6 60 2 3 0.5000 20.0000 0.2091 4.7215 76.39 0.7639
22 6 60 7 1 0.5000 20.0000 0.6763 15.3009 23.50 0.2350
23 6 60 7 2 0.5000 20.0000 0.6904 15.6202 21.90 0.2190
24 6 60 7 3 0.5000 20.0000 0.7002 15.8421 20.79 0.2079
25 6 60 10 1 0.5000 20.0000 0.8123 18.3805 8.10 0.0810
26 6 60 10 2 0.5000 20.0000 0.8115 18.3624 8.19 0.0819
27 6 60 10 3 0.5000 20.0000 0.8125 18.3850 8.07 0.0807
28 1 100 2 1 0.5000 20.0000 0.1059 2.3846 88.08 0.8808
29 1 100 2 2 0.5000 20.0000 0.1134 2.5545 87.23 0.8723
30 1 100 2 3 0.5000 20.0000 0.1150 2.5907 87.05 0.8705
31 1 100 7 1 0.5000 20.0000 0.7045 15.9394 20.30 0.2030
32 1 100 7 2 0.5000 20.0000 0.6955 15.7356 21.32 0.2132
33 1 100 7 3 0.5000 20.0000 0.7055 15.9621 20.19 0.2019
34 1 100 10 1 0.5000 20.0000 0.7192 16.2723 18.64 0.1864
35 1 100 10 2 0.5000 20.0000 0.7306 16.5305 17.35 0.1735
36 1 100 10 3 0.5000 20.0000 0.8075 18.2718 8.64 0.0864
37 1 80 2 1 0.5000 20.0000 0.1476 3.3289 83.36 0.8336
38 1 80 2 2 0.5000 20.0000 0.1698 3.8316 80.84 0.8084
lanjutan Lampiran 6
No Waktu
Ukuran
partikel pH Ulangan m C0 A C E Q
(jam) (mesh) ( g) (ppm) (ppm) (%) (mg/g)
82 9 100 2 1 0.5001 20.0000 0.1352 2.8604 85.70 0.8568
83 9 100 2 2 0.5000 20.0000 0.1346 2.8471 85.76 0.8576
84 9 100 2 3 0.4999 20.0000 0.1419 3.0092 84.95 0.8497
85 9 100 7 1 0.4999 20.0000 0.3391 7.3887 63.06 0.6307
86 9 100 7 2 0.5000 20.0000 0.3726 8.1327 59.34 0.5934
87 9 100 7 3 0.5000 20.0000 0.3834 8.3725 58.14 0.5814
88 9 100 10 1 0.5000 20.0000 0.5363 11.7682 41.16 0.4116
89 9 100 10 2 0.5000 20.0000 0.5340 11.7171 41.41 0.4141
90 9 100 10 3 0.5000 20.0000 0.5367 11.7771 41.11 0.4111
91 9 80 2 1 0.5001 20.0000 0.1540 3.2780 83.61 0.8359
92 9 80 2 2 0.5000 20.0000 0.1578 3.3623 83.19 0.8319
93 9 80 2 3 0.5000 20.0000 0.1345 2.8449 85.78 0.8578
94 9 80 7 1 0.5001 20.0000 0.4049 8.8500 55.75 0.5574
95 9 80 7 2 0.5000 20.0000 0.3720 8.1194 59.40 0.5940
96 9 80 7 3 0.5001 20.0000 0.3429 7.4731 62.63 0.6262
97 9 80 10 1 0.4999 20.0000 0.8068 17.7756 11.12 0.1112
98 9 80 10 2 0.5001 20.0000 0.8065 17.7689 11.16 0.1115
99 9 80 10 3 0.4999 20.0000 0.8061 17.7600 11.20 0.1120
100 9 60 2 1 0.5000 20.0000 0.1963 5.8755 70.62 0.7062
101 9 60 2 2 0.4999 20.0000 0.1675 4.9844 75.08 0.7509
102 9 60 2 3 0.5001 20.0000 0.2093 6.2777 68.61 0.6860
103 9 60 7 1 0.4999 20.0000 0.3709 11.2776 43.61 0.4362
104 9 60 7 2 0.5001 20.0000 0.3312 10.0493 49.75 0.4974
105 9 60 7 3 0.4999 20.0000 0.3777 11.4880 42.56 0.4257
106 9 60 10 1 0.4999 20.0000 0.6085 18.6289 6.86 0.0686
107 9 60 10 2 0.5001 20.0000 0.6092 18.6506 6.75 0.0675
108 9 60 10 3 0.4999 20.0000 0.6119 18.7341 6.33 0.0633
Keterangan: m = bobot biosorben. C0 = konsentrasi sebelum adsorpsi, C = konsentrasi
akhir, A = absorbans, E = efisiensi, dan Q = kapasitas adsorpsi
Contoh perhitungan:
Penentuan efisiensi Cr(VI) = 0
0 100
= β0 000 1 9798 β0 000 100
= 18 0β0ββ0 0000 100
= 90 10
= v 0
= β5 m (β0 000 1 9798) μg m 0 500 g ⁄
= 900 8 gg 0 9008 mg g
24
Lampiran 7 Sidik ragam kondisi terbaik adsorpsi Cr(VI) Sumber keragaman db Jumlah
kuadrat
Kuadrat
tengah F hitung P
Ukuran partikel (A) 2 0.577 0.289 578.018 0.000* pH larutan (B) 2 7.451 3.725 7.46 × 10-6 0.000* Waktu kontak (C) 3 0.483 0.161 322.344 0.000*
A*B 4 0.148 0.037 74.372 0.000*
A*C 6 0.183 0.031 61.185 0.000*
B*C 6 0.671 0.112 223.992 0.000*
A*B*C 12 0.164 0.014 27.337 0.000*
Galat 72 0.036 0.000
Total 108 33.662
Keterangan: *: berpengaruh nyata pada selang kepercayaan 95%
Lampiran 8 Rerata nilai kapasitas adsorpsi Cr(VI) pada berbagai perlakuan Perlakuan Tingkat Kapasitas adsorpsi (Q)
mg/g
Waktu (jam) 1 0.3627 ± 0.3290a
6 0.4695 ± 0.2973b
9 0.5165 ± 0.2753c
3 0.5349 ± 0.2874d
Ukuran partikel (mesh) 60 0.3908 ± 0.2936a
80 0.4544 ± 0.3297b
100 0.5675 ± 0.2572c
pH 10 0.1768 ± 0.1453a
7 0.4215 ± 0.2001b
2 0.8144 ± 0.0591c
lanjutan Lampiran 9
No Waktu
Ukuran
partikel pH Ulangan m C0 A C E Q
(jam) (mesh) (g) (ppm) (ppm) (%) (mg/g)
85 9 100 7 1 0.4999 20.0000 0.0304 1.1027 94.49 0.9451
86 9 100 7 2 0.4999 20.0000 0.0320 1.1584 94.21 0.9423
87 9 100 7 3 0.5000 20.0000 0.0217 0.8001 96.00 0.9600
88 9 100 10 1 0.5000 20.0000 0.0603 2.1429 89.29 0.8929
89 9 100 10 2 0.5000 20.0000 0.0564 2.0072 89.96 0.8996
90 9 100 10 3 0.5001 20.0000 0.0512 1.8263 90.87 0.9085
91 9 80 2 1 0.5001 20.0000 0.0308 1.1167 94.42 0.9440
92 9 80 2 2 0.5000 20.0000 0.0232 0.8523 95.74 0.9574
93 9 80 2 3 0.5000 20.0000 0.0257 0.9392 95.30 0.9530
94 9 80 7 1 0.5001 20.0000 0.0747 2.6438 86.78 0.8676
95 9 80 7 2 0.5001 20.0000 0.0819 2.8943 85.53 0.8551
96 9 80 7 3 0.5001 20.0000 0.0666 2.3620 88.19 0.8817
97 9 80 10 1 0.4999 20.0000 0.2211 7.7366 61.32 0.6133
98 9 80 10 2 0.4999 20.0000 0.2209 7.7296 61.35 0.6136
99 9 80 10 3 0.5000 20.0000 0.2251 7.8758 60.62 0.6062
100 9 60 2 1 0.5001 20.0000 0.0288 1.0471 94.76 0.9475
101 9 60 2 2 0.5001 20.0000 0.0262 0.9566 95.22 0.9520
102 9 60 2 3 0.5001 20.0000 0.0275 1.0019 94.99 0.9497
103 9 60 7 1 0.4999 20.0000 0.0224 0.8244 95.88 0.9590
104 9 60 7 2 0.5001 20.0000 0.0384 1.3810 93.09 0.9308
105 9 60 7 3 0.5000 20.0000 0.0382 1.3741 93.13 0.9313
106 9 60 10 1 0.5001 20.0000 0.3317 11.5840 42.08 0.4207
107 9 60 10 2 0.5001 20.0000 0.3228 11.2744 43.63 0.4362
108 9 60 10 3 0.5001 20.0000 0.3211 11.2153 43.92 0.4391
Keterangan: m = bobot biosorben. C0 = konsentrasi sebelum adsorpsi, C = konsentrasi
28
Lampiran 10 Sidik ragam kondisi terbaik adsorpsi Pb(II) Sumber
Keragaman db
Jumlah Kuadrat
Kuadrat
Tengah F Hitung P Ukuran partikel (A) 3 0.653 0.218 59.911 0.000*
pH larutan (B) 2 0.467 0.233 64.250 0.000*
Waktu kontak (C) 2 1.834 0.917 252.553 0.000*
A*B 4 0.217 0.054 14.939 0.000*
A*C 6 0.156 0.026 7.161 0.000*
B*C 6 0.276 0.046 12.680 0.000*
A*B*C 12 0.112 0.009 2.559 0.007*
Galat 72 0.261 0.004
Total 108 76.269
Keterangan: *: berpengaruh nyata pada selang kepercayaan 95%
Lampiran 11 Rerata nilai kapasitas adsorpsi Pb(II) pada berbagai perlakuan Perlakuan Tingkat Kapasitas adsorpsi (Q)
mg/g
Waktu (jam) 1 0.7099 ± 0.2157a
3 0.7956 ± 0.1946b
9 0.8423 ± 0.1828c
6 0.9247 ± 0.0999d
Ukuran partikel (mesh) 60 0.7357 ± 0.2211a 80 0.8221 ± 0.1979b 100 0.8966 ± 0.1206c
pH 10 0.6356 ± 0.2122a
7 0.8874 ± 0.1102b
2 0.9314 ± 0.0634c Keterangan: superskrip berbeda pada baris yang sama menunjukkan perbedaan yang sangat nyata (p <
Lampiran 12 Penentuan isoterm adsorpsi pada biosorpsi Cr(VI)
No
Volume larutan
(mL)
m C0
(ppm)
C
(ppm)
Ce
(ppm)
Isoterm Langmuir Isoterm
Freundlich
(g) Qe
(mg/g)
Ce/Qe (g/l)
log
Ce
log
Qe
1 0.025 0.5000 11.6545 0.7753 9.9298 0.4965 1.5616 -0.11 -0.30
2 0.025 0.5000 26.1767 3.2848 22.8926 1.1446 2.8691 0.52 0.06
3 0.025 0.4999 41.0747 6.7753 37.3595 1.8683 3.6264 0.83 0.27
4 0.025 0.4999 60.2017 9.3006 55.6795 2.7845 3.3401 0.97 0.44
5 0.025 0.4999 75.5184 12.0886 68.6766 3.4345 3.5197 1.08 0.54
6 0.025 0.4999 104.9368 21.1551 95.1741 4.7597 4.4447 1.33 0.68
Keterangan : m adalah bobot biosorben. C0 adalah konsentrasi sebelum adsorpsi. C adalah
konsentrasi akhir. Ce adalah konsentrasi kesetimbangan. dan Qe adalah kapasitas
adsorpsi.
Persamaan garis isoterm Freundlich yang diperoleh adalah y = 0.7009x – 0.2582 dengan R2 98.80%. Dari persamaan ini, diperoleh nilai kapasitas adsorpsi dengan cara
log = 1n log + log
y = 0.7009x – 0.β58β
log = - 0.β58β = 10 0.β58β
= 0.5518mg/g
30
Lampiran 13 Penentuan isoterm adsorpsi pada biosorpsi Pb(II)
No
Volume larutan
(mL)
m
C0
(ppm)
C
(ppm)
Ce
(ppm)
Isoterm Langmuir
Isoterm Freundlich
(g) Qe
(mg/g)
Ce/Qe
(g/l) log Ce
log
Qe
1 0,025 0,5001 19,6146 0,7517 18,8629 0,9430 0,7972 -0,12 -0,03
2 0,025 0,5001 29,8845 2,0207 27,8638 1,3929 1,4507 0,31 0,14
3 0,025 0,5001 40,2016 5,0931 35,1085 1,7551 2,9019 0,71 0,24
4 0,025 0,5001 60,2609 9,4552 50,8057 2,5398 3,7228 0,98 0,40
5 0,025 0,5000 85,3953 12,5310 72,8643 3,6432 3,4396 1,10 0,56
6 0,025 0,5000 110,6877 17,3414 93,3463 4,6673 3,7155 1,24 0,67
Keterangan : m adalah bobot biosorben. C0 adalah konsentrasi sebelum adsorpsi. C adalah konsentrasi akhir.
Ce adalah konsentrasi kesetimbangan. dan Qe adalah kapasitas adsorpsi.
Persamaan garis isoterm Freundlich yang diperoleh adalah y = 0.4864x – 0.0076 dengan R² = 93.92% Dari persamaan ini. diperoleh nilai kapasitas adsorpsi dengan cara :
log = 1n log + log
y = 0.4864x– 0.0076 log = – 0.0076
=
= 0.98β6mg/g
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 23 Februari 1990 di Tanjung Enim. Sumatera Selatan. Penyusun merupakan anak pertama dari 2 bersaudara. dari pasangan Bapak H. Mariadi dan Ibu Hj. Hermiyanah, BSc.
Tahun 2007 penulis lulus dari SMA PTBA Tanjung Enim dan pada tahun yang sama lulus seleksi masuk Direktorat Program Diploma, Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI).