METODE ELEKTROKOAGULASI
DISERTASI
Oleh
SUSILAWATI
058103007/KM
PROGRAM DOKTOR ILMU KIMIA
FAK. MATEMATIKA & ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MODEL PENGOLAHAN AIR GAMBUT UNTUK
MENGHASILKAN AIR BERSIH DENGAN
METODE ELEKTROKOAGULASI
DISERTASI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Doktor
dalam Program Studi Kimia, Konsentrasi Fisiko Kimia pada Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Oleh
SUSILAWATI
058103007/KM
PROGRAM DOKTOR ILMU KIMIA
FAK. MATEMATIKA & ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Judul Disertasi
:
MODEL PENGOLAHAN AIR GAMBUT
UNTUK MENGHASILKAN AIR BERSIH
DENGAN METODE ELEKTROKOAGULASI
NamaMahasiswa : Susilawati
Nomor Pokok
: 058103007
Program Studi
: Ilmu Kimia
Konsentrasi
: Fisiko Kimia
Menyetujui
Komisi Pembimbing
(Prof. Dr. Zul Alfian, MSc.)
Promotor
(Prof. Dr. Muhammad Zarlis, M.Sc.) (Dr. Hamonangan Nainggolan, M.Sc.)
Co Promotor
Co Promotor
Ketua Program Studi S3 Kimia
Dekan,
(Prof. Basuki Wirjosentono, M.S., Ph.D.) (Prof. Dr. Eddy Marlianto, M.Sc.)
PROMOTOR
Prof. Dr. Zul Alfian, M.Sc.
Guru Besar Tetap Ilmu Kimia Anorganik
Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
CO9PROMOTOR
Prof. Dr. Muhammad Zarlis, M.Sc.
Guru Besar Tetap Ilmu Fisika Komputasi
Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
CO9PROMOTOR
Dr. Hamonangan Nainggolan, M.Sc.
Staff Pengajar Tetap Ilmu Kimia Anorganik
Fakultas Matematika dan Ilmu Pengetahuan Alam
TIM PENGUJI
Ketua
: Prof. Dr. Zul Alfian, M.Sc.
Anggota
: Prof. Dr. Muhammad Zarlis, M.Sc.
Dr. Hamonangan Nainggolan, M.Sc.
Prof. Basuki Wirjosentono, M.S., Ph.D.
Guru Besar Tetap Ilmu Kimia Fisika Polimer
Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Prof. Dr. Eddy Marlianto, M.Sc.
Guru Besar Tetap Ilmu Fisika Superkonduktor
Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Prof. Dr. Yunazar Manjang
Guru Besar Tetap Ilmu Organik Bahan Alam
Fakultas Matematika dan Ilmu Pengetahuan Alam
PERNYATAAN ORISINALITAS
Disertasi ini adalah hasil karya penulis sendiri, dan semua sumber
baik yang dikutip maupun dirujuk telah penulis nyatakan dengan
benar.
Nama
: Susilawati
NIM
: 058103007
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
UNTUK KEPENTINGAN AKADEMIS
Sebagai sivitas akademik Universitas Sumatera Utara, saya yang bertanda tangan di bawah ini :
Nama : Susilawati
NIM : 058103007
Program Studi : Ilmu Kimia, Konsentrasi Fisiko Kimia Jenis Karya : Disertasi
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non9eksklusif (
)atas disertasi saya yang berjudul :
MODEL PENGOLAHAN AIR GAMBUT UNTUK MENGHASILKAN AIR
BERSIH DENGAN METODE ELEKTROKOAGULASI
beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non; eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media/formatkan, mengelola dalam bentuk , merawat dan mempublikasikan disertasi saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemilik hak cipta.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di : Medan
Pada Tanggal : Februari 2010 Yang Menyatakan
KATA PENGANTAR
Alhamdulillah, puji dan syukur penulis panjatkan ke hadirat Allah SWT, karena atas ridho, karunia dan rahmat;Nya penelitian dan disertasi ini dapat terlaksana dan selesai dengan baik. Disertasi ini merupakan tugas akhir penulis pada Program Studi Ilmu Kimia Konsentrasi Fisiko Kimia Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan.
Dengan selesainya disertasi ini, penulis ingin menyampaikan terima kasih yang setulus;tulusnya dan setinggi;tingginya kepada :
Rektor Universitas Sumatera Utara, Bapak Prof. Chairuddin P. Lubis, DTM&H.,Sp.A(K), atas kesempatan, bantuan biaya dan fasilitas yang diberikan kepada penulis untuk mengikuti dan menyelesaikan pendidikan program Doktor di Universitas Sumatera Utara, juga atas kesediaan beliau sebagai Ketua Tim Penguji Ujian Disertasi bagi penulis.
Dekan Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Bapak Prof. Dr. Eddy Marlianto, M.Sc. atas kesempatan menjadi mahasiswa dan mengikuti pendidikan program Doktor Pada Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Ketua Program Studi Ilmu Kimia Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Bapak Prof. Basuki Wirjosentono, M.S., Ph.D. atas dorongan dan arahan kepada penulis selama mengikuti pendidikan.
Terima kasih yang tak terhingga dan penghargaan yang setinggi;tingginya penulis ucapkan kepada komisi pembimbing, Bapak Prof. Dr. Zul Alfian, M.Sc. (Ketua), Bapak Prof. Dr. Muhammad Zarlis, M.Sc. (Anggota) dan Bapak Dr. Hamonangan Nainggolan, M.Sc. (Anggota) yang telah banyak menyumbangkan pikiran dan saran serta meluangkan waktu dalam proses penyelesaian disertasi ini. Dan dengan penuh kesabaran mendorong, memotivasi dan mengarahkan penulis sehingga disertasi ini dapat penulis selesaikan.
Prof. Basuki Wirjosentono, M.S., Ph.D., Bapak Prof. Dr. Eddy Marlianto, M.Sc., dan Bapak Prof. Dr. Yunazar Manjang, atas kesediaan mereka untuk menguji dan menilai penulis.
Terima kasih yang tek terhingga juga penulis ucapkan kepada Sekretaris Program Studi Ilmu Kimia Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Bapak Prof. Dr. Harry Agusnar, M.Sc. atas bantuan dan arahan kepada penulis selama mengikuti pendidikan.
Terima kasih yang tak terhingga juga penulis sampaikan kepada Staf Pengajar di Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara khususnya Program Studi Ilmu Kimia.
Terima kasih juga penulis sampaikan kepada rekan;rekan mahasiswa/I Program Studi Ilmu Kimia Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara angkatan 2005 khususnya konsentrasi Fisiko Kimia.
Penulis juga tak lupa mengucapkan terima kasih kepada Alexon Samosir dan Marcel, mahasiswa S1 Ilmu Kimia, Bapak Darmayanto, Ibu Jati Setiasih dan Ibu Nona mahasiswa S2 Ilmu Kimia yang telah membantu penulis dalam pengambilan Sampel ke Desa Hutabalang Kecamatan Badiri Kabupaten Tapanuli Tengah.
Secara khusus pada kesempatan ini penulis ingin menyampaikan terima kasih dan sayang yang mendalam kepada yang amat mulia kedua orang tua penulis, Bapak Achmadi dan Ibu Almarhumah Tumini yang telah bersusah payah membesarkan, menyekolahkan, membiayai dan mendidik penulis dengan penuh kasih sayang dan doa yang tiada hentinya. Demikian juga kepada bapak mertua saya, dan almarhumah ibu mertua saya yang menyayangi kami.
kalian selama mama menyelesaikan studi, terima kasih atas doa, motivasi, dorongan dan semangat yang kalian berikan kepada mama.
Akhirnya sekali lagi penulis menyampaikan terima kasih dan penghargaan yang setulus;tulusnya kepada mereka yang penulis sebutkan sebelumnya semoga Tuhan Yang Maha Esa selalu memberikan perlindungan, kesehatan, limpahan rahmat dan membalas semua kebaikan;kebaikan mereka.
Penulis menyadari bahwa disertasi ini tidak mungkin terlepas dari kesalahan yang ada di luar kemampuan penulis. Oleh sebab itu penulis dengan senang hati akan menerima kritik dan saran yang membangun demi kesempurnaannya.
Medan, Januari 2010
ABSTRAK
Metode Elektrokoagulasi telah banyak digunakan untuk pengolahan / pemurnian air (air limbah, air sungai maupun air gambut). Namun model pengolahan air gambut dalam skala pilot dengan metode elektrokoagulasi belum banyak dikembangkan. Dalam penelitian ini telah dirancang suatu model untuk pengolahan air gambut dalam skala pilot dengan metode elektrokoagulasi. Air gambut digunakan sebagai sampel mengingat air gambut merupakan sumber air baku yang sangat potensial terutama di sebagian besar pulau Kalimantan dan sebagian pulau Sumatera. Lokasi pengambilan sampel terletak di desa Hutabalang Kecamatan Badiri Kabupaten Tapanuli Tengah Propinsi Sumatera Utara. Penelitian dilakukan dalam dua tahap. Percobaan tahap pertama dilakukan dalam skala laboratorium menggunakan beaker glass untuk mengetahui parameter; parameter yang optimum, baik dari segi volume sampel, volume tawas dan waktu untuk elektrokoagulasi. Hasil percobaan tahap pertama ini digunakan sebagai acuan untuk mengkaji berapa banyak penambahan larutan tawas ke dalam sampel untuk proses elektrokoagulasi sehingga dapat menghasilkan air jernih. Tahap kedua adalah merancang suatu model pengolahan air gambut dalam skala pilot untuk menghasilkan air bersih yang menggunakan parameter;parameter optimum hasil percobaan tahap pertama. Model yang dirancang menggunakan beberapa bak, yaitu bak 1 sampel, bak 2 proses elektrokoagulasi, bak 3 filtrasi, bak 4 kontrol dan bak 5 air bersih, dengan kecepatan alir 1 liter/menit. Sebagai elektroda digunakan plat aluminium dengan jumlah plat adalah 4 buah (2 katoda dan 2 anoda) pada jarak 6 cm. Untuk mempercepat terjadinya koagulasi dan flokulasi, pada sampel ditambahkan larutan aluminium sulfat (tawas 17 %) sebanyak 10 ml/l sampel, dengan kadar 1000 ppm tawas yang telah dipasarkan. Hasil uji coba menggunakan model menunjukkan bahwa terdapat kenaikan pH mendekati netral dan penurunan warna, turbidity, COD, BOD, total organik dan kandungan logam Al, Fe, Mn, Zn, Cd dan Cu yang cukup signifikan.
ABSTRACT
Electrocoagulation method have used many for the processing of / purification of water (waste water, river water and also peat water). But model processing peat water in pilot scale with electrocoagulation method not yet many developed. In this research have been designed by a model for the processing of peat water in pilot scale with electrocoagulation method. Peat water used as sampel remember peat water represent the source standard water of very potential especially in this part of is big of Kalimantan island and some of Sumatra island. Location intake of sampel located in Hutabalang countryside District of Badiri Sub;Province Tapanuli Tengah of Province North Sumatra. Research done in two phase. Experiment of first Phase done in laboratory scale use glass beaker to know optimum parameter, either from facet sample volume, alum volume and time for the electrocoagulation. Result of experiment of this first phase used as reference to study how many addition of alum solution into sample for the process of electrocoagulation so that can yield clean water. Second is design a processing model peat water in pilot scale to yield clean water which use optimum parameter result of experiment of first phase. designed model use some basin, that is basin 1 sampel, basin 2 electrocoagulation process, basin 3 filtration, basin 4 control and basin 5 clean water, with speed emit a stream of 1 litre/minute. As electrode used aluminium plate with amount of plate is 4 ( 2 cathode and 2 anode) at distance 6 cm. To quicken the happening of coagulation and floculation, at sampel enhanced aluminium sulphate solution ( alum 17 %) counted 10 ml/ l sampel, with rate 1000 ppm alum which have been marketed. Result of test;drive use model indicate that there are increase of pH come near neutral and degradation of colour, turbidity, COD, BOD, organic total and content metal of Al, Fe, Mn, Zn, Cd and Cu which enough significant.
DAFTAR ISI
Halaman
ABSTRAK... i
... ii
KATA PENGANTAR... iii
DAFTAR ISI... vi
DAFTAR TABEL... viii
DAFTAR GAMBAR... ix
DAFTAR LAMPIRAN... x
BAB I PENDAHULUAN... 1
1.1 Latar Belakang... 1
1.2 Permasalahan... 6
1.3 Pembatasan masalah... 7
1.4 Tujuan Penelitian... 7
1.5 Manfaat Penelitian... 7
BAB II TINJAUAN PUSTAKA... 8
2.1 Air Gambut... 8
2.1.1 Karakteristik Air Gambut... 8
2.1.2 Pengolahan Air Gambut... 12
2.1.3 Alternatif Proses Pengolahan Air Gambut... 14
2.2 Proses Elektrokoagulasi... 16
2.2.1 Mekanisme Dalam Elektrokoagulasi... 20
2.2.2 Pelarutan Logam di Elektroda... 21
2.2.3 Reaksi Di Elektroda... 22
2.2.4 Sel Elektrokimia... 24
2.2.5 Proses Koagulasi... 25
2.2.6 Proses Flokulasi... 28
2.2.7 Faktor;Faktor Yang Mempengaruhi Koagulasi dan Flokulasi... 28
2.3 Tinjauan Koloid... 32
2.3.1 Kestabilan Koloid... 33
2.3.2 Destabilisasi Partikel Koloid... 33
2.3.3 Konsep Potensial Zeta... 37
2.4 Tawas (Alum)... 38
2.5 pH... 38
2.6 Warna... 39
2.7 Turbidity... 40
2.8 COD dan BOD... 41
2.9 Logam ; Logam Dalam Air... 43
2.9.1 Logam Al... 43
2.9.4 Logam Mn... 44
2.9.5 Logam Cu... 45
2.9.6 Logam Cd... 45
2.10 Total Organik... 46
BAB III METODE PENELITIAN... 47
3.1 Waktu dan Lokasi Penelitian... 47
3.2 Bahan dan Alat Penelitian... 48
3.3 Pengambilan Sampel... 50
3.4 Diagram Alir Penelitian... 53
3.5 Model Pengolahan Air Gambut... 57
3.6 Prosedur Penelitian... 60
BAB IV HASIL DAN PEMBAHASAN... 61
4.1 Skala Laboratorium... 61
4.2 Skala Pilot... 64
4.3 Proses Elektrokoagulasi Dengan Penambahan Larutan Tawas 68 4.4 Mekanisme Dalam Elektrokoagulasi... 70
4.5 Biaya Operasional Model... 72
BAB V KESIMPULAN DAN SARAN... 74
5.1 Kesimpulan... 74
5.2 Saran... 75
DAFTAR TABEL
Nomor Judul Halaman
2.1 Karakteristik Air Gambut Dari Berbagai Lokasi di Sumatera
dan Kalimantan……….. 12
4.1 Pengaruh Elektrokoagulasi terhadap pengolahan air gambut…… 62 4.2 Pengaruh larutan tawas terhadap pengolahan air gambut……….. 62 4.3 Elektrokoagulasi air gambut dengan penambahan larutan tawas.. 63 4.4 Karakteristik air gambut, sebelum dan sesudah diolah
dengan metode elektrokoagulasi + larutan tawas
(hasil ujicoba skala lab.)... 64 4.5 Pengolahan air gambut dengan elektrokoagulasi + larutan
Tawas 10 ml/L air gambut dengan kecepatan alir 1 L/menit
(hasil uji coba ke model, skala pilot)... 66 4.6 Karakteristik air gambut, sebelum dan sesudah diolah
dengan metode elektrokoagulasi + larutan tawas
(hasil ujicoba menggunakan model yang telah dirancang)... 67
DAFTAR GAMBAR
Nomor Judul Halaman
2.1 Struktur Model Asam Humat Berdasarkan Stevenson (1982)…… 10
2.2 Struktur Model Asam Fulvik Berdasarkan Buffle et al (1977)…... 10
2.3 Komponen Kimia Humus……… 11
2.4 Perinsip Proses Elektrokoagulasi………. 17
2.5 Diagram Venn……….. 18
2.6 Mekanisme dalam Elektrokoagulasi………. 21
2.7 Gaya ; Gaya Yang Terjadi Pada Interaksi Antar Partikel Koloid… 26 2.8 Pengurangan Gaya Tolak Menolak oleh Ion;Ion Aluminium…….. 27
2.9 Terjadinya proses ”Sweep;Floc” (Duan, 2003)... 36
2.10 Skema reaksi antar partikel koloid dengan poly elektrolit………… 37
3.1 Penentuan Titik;Titik Pengambilan Sampel………..… 51
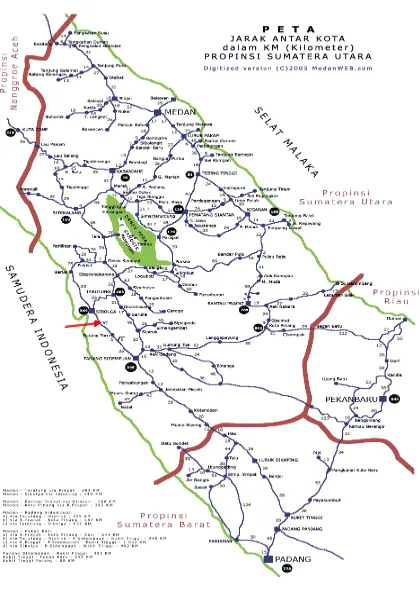
3.2 Peta Lokasi Pengambilan Sampel………. 52
3.3 Diagram Alir Penelitian Skala laboratorium………. 54
3.4 Diagram Alir Penelitian Skala Pilot……….. 56
3.5 Model Pengolahan Air Gambut Dalam Skala Pilot……….. 59
DAFTAR LAMPIRAN
Nomor Judul Halaman
1 pH……… 80
2 Turbidity (Kekeruhan)……….… 81
3 Total Organik………... 82
4 Warna………... 83
5 Hasil Analisa Logam (Cu, Zn, Fe, Mn, Cd, Pb) dengan SSA, Hasil Analisa COD dan BOD untuk pengambilan sampel I... 90
6 Hasil Analisa Logam (Cu, Zn, Fe, Mn, Cd, Pb) dengan SSA, Hasil Analisa COD dan BOD untuk Pengambilan Sampel II... 102
7 Hasil Analisa Logam (Fe, Zn, Mn, Cd, Cu) dengan SSA, Hasil Analisa COD dan BOD untuk Pengambilan Sampel III... 114
8 Hasil Analisa Logam Al dengan SSA untuk Pengambilan Sampel I, II, dan III... 126
9 KepMenKes RI No. 907/MENKES/SK/VII/2002 Tanggal 29 Juli 2002, Tentang PERSYARATAN KUALITAS AIR MINUM... 130
10 Peraturan Pemerintah Nomor 82 Tahun 2001 Tentang Pengelolaan Kualitas Air dan Pengendalian Pencemaran Air... 132
11 Peraturan Menteri Kesehatan Republik Indonesia Nomor : 416/MENKES/PER/IX/1990 Tanggal : 3 September 1990 Tentang Persyaratan Kualitas Air Minum dan Air Bersih... 134
ABSTRAK
Metode Elektrokoagulasi telah banyak digunakan untuk pengolahan / pemurnian air (air limbah, air sungai maupun air gambut). Namun model pengolahan air gambut dalam skala pilot dengan metode elektrokoagulasi belum banyak dikembangkan. Dalam penelitian ini telah dirancang suatu model untuk pengolahan air gambut dalam skala pilot dengan metode elektrokoagulasi. Air gambut digunakan sebagai sampel mengingat air gambut merupakan sumber air baku yang sangat potensial terutama di sebagian besar pulau Kalimantan dan sebagian pulau Sumatera. Lokasi pengambilan sampel terletak di desa Hutabalang Kecamatan Badiri Kabupaten Tapanuli Tengah Propinsi Sumatera Utara. Penelitian dilakukan dalam dua tahap. Percobaan tahap pertama dilakukan dalam skala laboratorium menggunakan beaker glass untuk mengetahui parameter; parameter yang optimum, baik dari segi volume sampel, volume tawas dan waktu untuk elektrokoagulasi. Hasil percobaan tahap pertama ini digunakan sebagai acuan untuk mengkaji berapa banyak penambahan larutan tawas ke dalam sampel untuk proses elektrokoagulasi sehingga dapat menghasilkan air jernih. Tahap kedua adalah merancang suatu model pengolahan air gambut dalam skala pilot untuk menghasilkan air bersih yang menggunakan parameter;parameter optimum hasil percobaan tahap pertama. Model yang dirancang menggunakan beberapa bak, yaitu bak 1 sampel, bak 2 proses elektrokoagulasi, bak 3 filtrasi, bak 4 kontrol dan bak 5 air bersih, dengan kecepatan alir 1 liter/menit. Sebagai elektroda digunakan plat aluminium dengan jumlah plat adalah 4 buah (2 katoda dan 2 anoda) pada jarak 6 cm. Untuk mempercepat terjadinya koagulasi dan flokulasi, pada sampel ditambahkan larutan aluminium sulfat (tawas 17 %) sebanyak 10 ml/l sampel, dengan kadar 1000 ppm tawas yang telah dipasarkan. Hasil uji coba menggunakan model menunjukkan bahwa terdapat kenaikan pH mendekati netral dan penurunan warna, turbidity, COD, BOD, total organik dan kandungan logam Al, Fe, Mn, Zn, Cd dan Cu yang cukup signifikan.
ABSTRACT
Electrocoagulation method have used many for the processing of / purification of water (waste water, river water and also peat water). But model processing peat water in pilot scale with electrocoagulation method not yet many developed. In this research have been designed by a model for the processing of peat water in pilot scale with electrocoagulation method. Peat water used as sampel remember peat water represent the source standard water of very potential especially in this part of is big of Kalimantan island and some of Sumatra island. Location intake of sampel located in Hutabalang countryside District of Badiri Sub;Province Tapanuli Tengah of Province North Sumatra. Research done in two phase. Experiment of first Phase done in laboratory scale use glass beaker to know optimum parameter, either from facet sample volume, alum volume and time for the electrocoagulation. Result of experiment of this first phase used as reference to study how many addition of alum solution into sample for the process of electrocoagulation so that can yield clean water. Second is design a processing model peat water in pilot scale to yield clean water which use optimum parameter result of experiment of first phase. designed model use some basin, that is basin 1 sampel, basin 2 electrocoagulation process, basin 3 filtration, basin 4 control and basin 5 clean water, with speed emit a stream of 1 litre/minute. As electrode used aluminium plate with amount of plate is 4 ( 2 cathode and 2 anode) at distance 6 cm. To quicken the happening of coagulation and floculation, at sampel enhanced aluminium sulphate solution ( alum 17 %) counted 10 ml/ l sampel, with rate 1000 ppm alum which have been marketed. Result of test;drive use model indicate that there are increase of pH come near neutral and degradation of colour, turbidity, COD, BOD, organic total and content metal of Al, Fe, Mn, Zn, Cd and Cu which enough significant.
BAB I PENDAHULUAN
I. 1 Latar Belakang
Air bersih merupakan salah satu kebutuhan pokok manusia yang diperoleh dari berbagai sumber, tergantung pada kondisi daerah setempat. Kondisi sumber air pada setiap daerah berbeda;beda, tergantung pada keadaan alam dan kegiatan manusia yang terdapat di daerah tersebut. Penduduk yang tinggal di daerah dataran rendah dan berawa seperti di Sumatera dan Kalimantan menghadapi kesulitan memperoleh air bersih untuk keperluan rumah tangga, terutama air minum. Hal ini karena sumber air di daerah tersebut adalah air gambut yang berdasarkan parameter baku mutu air tidak memenuhi persyaratan kualitas air bersih.
Air gambut mengandung senyawa organik terlarut yang menyebabkan air menjadi berwarna coklat dan bersifat asam, sehingga perlu pengolahan khusus sebelum siap untuk dikonsumsi. Senyawa organik tersebut adalah asam humus yang terdiri dari asam humat, asam fulvat dan humin. Asam humus adalah senyawa organik dengan berat molekul tinggi dan berwarna coklat sampai kehitaman, terbentuk karena pembusukan tanaman dan hewan, sangat tahan terhadap mikroorganisme dalam waktu yang cukup lama (Notodarmojo, 1994).
Air gambut di Indonesia merupakan salah satu sumber daya air yang masih melimpah, kajian pusat Sumber Daya Geologi Departemen Energi dan Sumber Daya Mineral melaporkan bahwa sampai tahun 2006 sumber daya lahan gambut di Indonesia mencakup luas 26 juta ha yang tersebar di pulau kalimantan (± 50 %), Sumatera (± 40 %) sedangkan sisanya tersebar di papua dan pulau;pulau lainnya. Dan untuk lahan gambut Indonesia menempati posisi ke – 4 terluas setelah Canada, Rusia dan Amerika Serikat (Tjahjono, 2007).
adalah warna, tingkat kekeruhan, dan zat organik yang tinggi sehingga sangat tidak layak untuk digunakan sebagai air bersih.
Kenyataan di atas dihadapi oleh masyarakat yang tinggal di area gambut yang masih cukup luas di daerah Tapanuli Tengah, khususnya di kecamatan Badiri. Masyarakat yang tinggal di areal gambut tersebut masih menggunakan air gambut untuk keperluan sehari;harinya tanpa melalui proses pengolahan terlebih dahulu.
Kondisi ini mendorong timbulnya penelitian;penelitian baru dalam pengolahan air gambut, sehingga dapat dimanfaatkan sesuai standar air bersih yang berlaku karena air gambut merupakan salah satu sumber air permukaan yang dapat digunakan sebagai air baku pengolahan air bersih. Air gambut baik sebagai air permukaan maupun air tanah umumnya memiliki kualitas yang tidak memenuhi persyaratan kualitas air bersih yang distandarkan oleh Departemen Kesehatan Republik Indonesia, karena :
1. Berwarna kuning/merah kecoklatan
2. Tingkat keasaman tinggi, sehingga kurang enak diminum. 3. Zat organik tinggi sehingga menimbulkan bau.
Air gambut yang berwarna kuning/merah kecoklatan disebabkan oleh kandungan organik yang merupakan partikel koloid bermuatan negatif dan sulit dipisahkan dari cairannya karena ukurannya sangat kecil dan mempunyai sifat muatan listrik pada permukaannya yang menyebabkan partikel stabil. Salah satu cara pendestabilisasian partikel koloid ini yaitu melalui proses koagulasi dengan bantuan garam;garam yang mengandung ion;ion logam bervalensi tiga, seperti besi dan aluminium sebagai koagulan, sehingga proses pengolahan air gambut ini dapat dilakukan dengan cara elektrolisa yang disebut dengan elektrokoagulasi (D. Ghernaout et al., 2009). Koagulasi adalah proses yang penting dalam proses pengolahan air secara konvensional, dimana proses ini bersamaan dengan proses lain seperti sedimentasi dan filtrasi. Tujuan utama proses koagulasi adalah untuk mendestabilisasi partikel sehingga dapat bergabung dengan partikel lain untuk membentuk agregat yang lebih besar yang akan lebih mudah mengendap.
bak persegi empat. Lempengan aluminium tersebut disusun secara paralel dengan suatu jarak tertentu dan dialiri dengan listrik arus searah. Dengan adanya arus listrik tersebut, aluminium akan dipisahkan dari anoda dan sedikit demi sedikit akan larut ke dalam air membentuk ion Al3+ yang akan bereaksi dengan air (hidrolisa) sebelum terjadi presipitasi Al(OH)3, sedangkan pada katoda terbentuk gas hidrogen.
Penelitian mengenai pengolahan air gambut sudah pernah dilakukan sebelumnya antara lain :
Pengolahan air gambut dengan menggunakan protein biji kelor sebagai koagulan untuk perjernihan warna air gambut (Chaidir, Z. et al., 1999).
Pemisahan berbasis membran yang sering digunakan untuk pengolahan air gambut adalah membran reverse osmosis (RO). Pemanfaatan ini merupakan teknologi baru dalam mengolah air gambut menjadi air minum. Salah satu keunggulan teknologi ini adalah kemurnian produk yang dihasilkan lebih baik dari proses konvensional (Syafran, 2005).
Mengolah air gambut asin dengan teknik dan proses filtrasi yang panjang dan dikombinasikan dengan unit desalinasi. Proses pertama terjadi di tangki clarifier yang berfungsi menjernihkan dan menaikkan pH menjadi 8;9 melalui pemberian abu soda atau kapur tohor yang dilarutkan. Untuk mempercepat proses pengendapan dapat digunakan tawas atau PAC dengan diaduk searah sekitar 5 menit. Air yang telah jernih dialirkan ke bak pengendap 1 dan 2. Pada tahap selanjutnya dilakukan proses oksidasi dengan kalium permanganat. Air yang telah jernih, tidak berbau dan berwarna, kemudian disaring lagi dengan menggunakan saringan mikro dengan ukuran 0,1 – 0,5 Mm. Air olahan yang telah jernih, tawar tidak berbau, dan bebas bakteri ditampung dalam bak penampung air bersih dan sudah dapat langsung diminum. Sistem pengolahan menelan biaya sekitar 350 juta ini mampu menghasilkan 170 galon air siap minum dalam 8 jam operasional (BPPT, 2006)
pengolahan lengkap (koagulasi – flokulasi – sedimentasi – filtrasi – netralisasi dan desinfektan) dapat digunakan untuk menghilangkan warna terutama pembentuk warna semu sekitar 80 %, efisiensi penghilangan warna akan lebih efektif jika dilakukan modifikasi dan tambahan proses seperti aplikasi karbon aktif, reaksi redoks, dan koagulan – flokulan aid (Pararaja, 2007).
Efektifitas proses elektrokoagulasi untuk memindahkan ( ) zat;zat organik dari limbah rumah potong hewan menggunakan sel;sel elektrolitik ( ) monopolar dan bipolar. Hasil menunjukkan bahwa pencapaian ( ) terbaik diperoleh menggunakan sistem elektroda baja ( ) bipolar yang dioperasikan pada intensitas arus 0,3 A selama 60;90 menit. Berhasil menurunkan BOD sebesar 86 ± 1%, lemak dan minyak sebesar 99 ± 1%, COD sebesar 50 ± 4%, TSS (total suspended solid) sebesar 89 ± 4% dan Turbidity sebesar 90 ± 4%. Total biaya yang dibutuhkan 0,71 USD $ / m3 limbah rumah potong hewan, (Asselin, M., 2008).
Menyelidiki efek pH awal untuk menurunkan unsur;unsur humus dari air limbah dengan proses elektrokoagulasi. Efek dari pH awal pada sistem elektrokoagulasi bisa duakali lipat, yaitu distribusi produk hidrolisis aluminium, transformasi unsur;unsur humus yang terkait ke pH awal dan akhirnya efek dari lapisan gel khususnya pada konsentrasi unsur;unsur humus yang tinggi dan pH awal yang tinggi yang dibentuk pada permukaan anoda. Hasil pengamatan menunjukkan bahwa konsentrasi awal unsur;unsur humus dan pH awal sangat efektif pada efisiensi dan tingkat penurunan. pH awal air limbah telah disesuaikan 5,0 dan efisiensi penurunan yang tinggi telah diamati. Sehingga sistem elektrokoagulasi akan dioperasikan pada pH rendah yaitu 5,0 pada konsentrasi unsur;unsur humus yang tinggi, (Koparal, A.S., 2008).
Dari penelitian;penelitian terdahulu yang telah dilakukan terhadap air baku air gambut dapat disimpulkan bahwa :
• Perlu pengolahan terlebih dahulu dalam pemanfaatan air gambut sebagai air bersih, karena pada umumnya kualitas air gambut mempunyai kandungan organik, warna dan derajat keasaman yang tinggi.
• Proses elektrokoagulasi dapat dipakai sebagai salah satu alternatif untuk memperbaiki kualitas air gambut karena dapat menurunkan kandungan organik, kekeruhan dan warna. Menurut Irianto bahwa air gambut sulit diolah secara koagulasi konvensional karena kandungan kation partikel tersuspensi yang rendah.
• Ditinjau dari persyaratan kualitas air yang ditetapkan pada dasarnya penelitian;penelitian terdahulu sudah dapat menurunkan beberapa karakteristik penting dari air gambut, namun ditinjau dari segi ekonomis masih kurang memuaskan.
Dari kendala;kendala yang ada maka prospek yang dianjurkan dalam penelitian ini yaitu sebagai salah satu alternatif pengganti beban kebutuhan bahan kimia dalam pengolahan air gambut dan lebih efisien dari segi operasi dan pemeliharaan. Dengan melihat hasil tersebut maka pada penelitian ini akan dirancang suatu model untuk pengolahan air gambut untuk menghasilkan air bersih dengan proses elektrokoagulasi dalam skala pilot.
Sebagai suatu alternatif pengganti proses yang ketergantungan terhadap bahan kimia, maka proses elektrokoagulasi ini perlu direncanakan dengan baik agar memberikan hasil yang optimum dan lebih efektif dengan mempertimbangkan faktor;faktor yang mempengaruhi reaksi elektroda yang akan menentukan pemakaian daya listrik, yaitu : variabel elektroda, meliputi : jenis, jumlah, dan jarak antar elektroda. Dan variabel listrik, meliputi : arus, tegangan, dan kecepatan alir.
I.2 Permasalahan
senyawa;senyawa organik. Senyawa organik tersebut bersifat asam sehingga umumnya logam;logam terlarut dalam bentuk mikroelement di dalam air gambut.
Berdasarkan identifikasi masalah di atas, maka permasalahan dalam penelitian ini adalah sebagai berikut :
1. Bagaimana mendapatkan air bersih di lahan gambut yang sesuai dengan persyaratan kualitas air bersih berdasarkan Peraturan Menteri Kesehatan RI No. 416/MENKES/PER/IX/1990 tanggal 3 September 1990, dengan sumber air baku dari air gambut.
2. Bagaimana merancang model yang praktis dan efisien yang dapat digunakan untuk mengolah air gambut menjadi air bersih di lahan gambut.
3. Apakah model yang dirancang dengan proses elektrokoagulasi dan penambahan larutan tawas dapat mengolah air gambut menjadi air bersih yang efektif dan efisien.
I.3 Pembatasan Masalah
Pengolahan air gambut menjadi air bersih yang dapat dikonsumsi sesuai dengan Peraturan Menteri Kesehatan RI No. 416/MENKES/PER/IX/1990 tanggal 3 September 1990 tentang persyaratan kualitas air bersih. Pada penelitian ini parameter yang akan dianalisis adalah : pH, Warna, Kekeruhan, COD, BOD, Total organik, Logam Al, Fe, Zn, Mn, Cd, dan Cu.
1.4 Tujuan Penelitian
Merancang suatu model pengolahan air gambut dengan menggunakan metode elektrokoagulasi untuk menghasilkan air bersih, yang sesuai dengan persyaratan kualitas air bersih berdasarkan Peraturan Menteri Kesehatan RI No. 416/MENKES/PER/IX/1990 tanggal 3 September 1990.
Khususnya :
1. Merancang suatu model pengolahan air gambut dalam skala pilot yang efektif dan efisien.
I.5 Manfaat Penelitian
1. Memberikan suatu alternatif pengolahan air gambut pada daerah;daerah atau kawasan yang sumber air bersih sulit diperoleh terutama dikawasan gambut. 2. Sebagai suatu studi untuk mengatasi masalah dalam pengadaan air bersih
melalui pengolahan air gambut khususnya di kabupaten Tapanuli Tengah. 3. model yang dirancang dapat mengolah air gambut dalam skala pilot untuk
menghasilkan air bersih dengan metode elektrokoagulasi dan penambahan larutan tawas dengan kecepatan alir 1 L/menit.
BAB II
TINJAUAN PUSTAKA
2.1 Air Gambut
2.1.1 Karakteristik Air Gambut
Air gambut adalah air permukaan yang banyak terdapat di daerah berawa maupun dataran rendah terutama di Sumatera dan Kalimantan, yang mempunyai ciri;ciri sebagai berikut (Kusnaedi, 2006) :
• Intensitas warna yang tinggi (berwarna merah kecoklatan) • pH yang rendah
• Kandungan zat organik yang tinggi
• Kekeruhan dan kandungan partikel tersuspensi yang rendah • Kandungan kation yang rendah
Warna coklat kemerahan pada air gambut merupakan akibat dari tingginya kandungan zat organik (bahan humus) terlarut terutama dalam bentuk asam humus dan turunannya. Asam humus tersebut berasal dari dekomposisi bahan organik seperti daun, pohon atau kayu dengan berbagai tingkat dekomposisi, namun secara umum telah mencapai dekomposisi yang stabil (Syarfi, 2007). Dalam berbagai kasus, warna akan semakin tinggi karena disebabkan oleh adanya logam besi yang terikat oleh asam;asam organik yang terlarut dalam air tersebut.
Struktur gambut yang lembut dan mempunyai pori;pori menyebabkannya mudah untuk menahan air dan air pada lahan gambut tersebut dikenal dengan air gambut. Berdasarkan sumber airnya, lahan gambut dibedakan menjadi dua yaitu (Trckova, M., 2005) :
1. Bog
Merupakan jenis lahan gambut yang sumber airnya berasal dari air hujan dan air permukaan. Karena air hujan mempunyai pH yang agak asam maka setelah bercampur dengan gambut akan bersifat asam dan warnanya coklat karena terdapat kandungan organik.
2. Fen
Berdasarkan kelarutannya dalam alkali dan asam, asam humus dibagi dalam tiga fraksi utama yaitu (Pansu, 2006) :
1. Asam humat
Asam humat atau humus dapat didefinisikan sebagai hasil akhir dekomposisi bahan organik oleh organisme secara aerobik. Ciri;ciri dari asam humus ini antara lain:
• Asam ini mempunyai berat molekul 10.000 hingga 100.000 g/mol (Collet, 2007).
• Merupakan makromolekul aromatik komplek dengan asam amino, gula amino, peptide, serta komponen alifatik yang posisinya berada antara kelompok aromatik (Gambar 2.1).
• Merupakan bagian dari humus yang bersifat tidak larut dalam air pada kondisi pH < 2 tetapi larut pada pH yang lebih tinggi.
• Bisa diekstraksi dari tanah dengan bermacam reagen dan tidak larut dalam larutan asam.
• Asam humat adalah bagian yang paling mudak diekstrak diantara komponen humus lainnya.
• Mempunyai warna yang bervariasi mulai dari coklat pekat sampai abu;abu pekat.
• Humus tanah gambut mengandung lebih banyak asam humat (Stevenson, 1982).
Gambar 2.1 Struktur model asam humat berdasarkan Stevenson (1982). 2. Asam fulvat
Asam fulvat merupakan senyawa asam organik alami yang berasal dari humus, larut dalam air, sering ditemukan dalam air permukaan dengan berat molekul yang rendah yaitu antara rentang 1000 hingga 10.000 (Collet, 2007). Bersifat larut dalam air pada semua kondisi pH dan akan berada dalam larutan setelah proses penyisihan asam humat melalui proses asidifikasi. Warnanya bervariasi mulai dari kuning sampai kuning kecoklatan. Struktur model asam fulvik dapat dilihat pada Gambar 2.2.
Gambar 2.2 Struktur model asam fulvik berdasarkan Buffle (1977)
3. Humin
juga menyatakan bahwa karakteristik humin adalah berwarna coklat gelap, tidak larut dalam asam dan basa, dan sangat resisten akan serangan mikroba. Tidak dapat diekstrak oleh asam maupun basa.
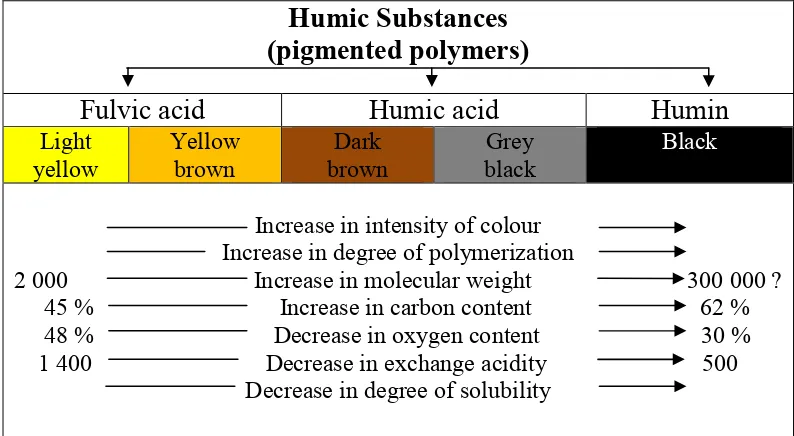
Perbedaan antara asam humat, asam fulvat dan humin bisa dijelaskan melalui variasi berat molekul, keberadaan group fungsional seperti karboksil dan fenolik dengan tingkat polimerisasi (Gambar 2.3)
Humic Substances
(pigmented polymers)
Fulvic acid
Humic acid
Humin
Light yellow
Yellow brown
Dark brown
Grey black
Black
Increase in intensity of colour Increase in degree of polymerization
2 000 Increase in molecular weight 300 000 ?
45 % Increase in carbon content 62 %
48 % Decrease in oxygen content 30 %
1 400 Decrease in exchange acidity 500
Decrease in degree of solubility
Chemical properties of humic substances (Stevenson, 1982) Gambar 2.3 Komponen Kimia Humus
Dari Gambar 2.3 diketahui bahwa kandungan karbon dan oksigen, asiditas dan derajat polimerisasi semuanya berubah secara sistematik dengan peningkatan berat molekul. Asam fulvik dengan berat molekul yang rendah memiliki kandungan oksigen yang lebih tinggi dan kandungan karbon yang rendah jika dibandingkan dengan asam humat dengan berat molekul yang tinggi. Warna juga akan semakin tinggi dengan semakin tingginya berat molekul.
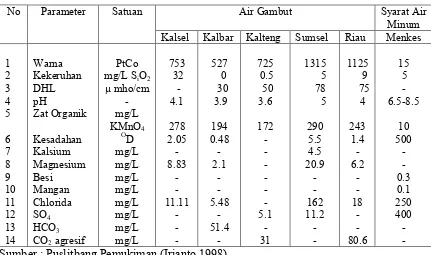
[image:30.595.119.516.223.441.2]Tabel 2.1 Karakteristik Air Gambut dari Berbagai Lokasi di Sumatera & Kalimantan.
No Parameter Satuan Air Gambut Syarat Air
Minum
Kalsel Kalbar Kalteng Sumsel Riau Menkes
1 2 3 4 5 6 7 8 9 10 11 12 13 14 Warna Kekeruhan DHL pH Zat Organik Kesadahan Kalsium Magnesium Besi Mangan Chlorida SO4 HCO3
CO2agresif
PtCo mg/L SiO2
M mho/cm ; mg/L KMnO4 OD mg/L mg/L mg/L mg/L mg/L mg/L mg/L mg/L 753 32 ; 4.1 278 2.05 ; 8.83 ; ; 11.11 ; ; ; 527 0 30 3.9 194 0.48 ; 2.1 ; ; 5.48 ; 51.4 ; 725 0.5 50 3.6 172 ; ; ; ; ; ; 5.1 ; 31 1315 5 78 5 290 5.5 4.5 20.9 ; ; 162 11.2 ; ; 1125 9 75 4 243 1.4 ; 6.2 ; ; 18 ; ; 80.6 15 5 ; 6.5;8.5 10 500 ; ; 0.3 0.1 250 400 ; ;
Sumber : Puslitbang Pemukiman (Irianto,1998).
Karakteristik air gambut bersifat spesifik, bergantung pada lokasi, jenis vegetasi dan jenis tanah tempat air gambut tersebut berada, ketebalan gambut, usia gambut, dan cuaca. Hal ini dapat dilihat pada Tabel 2.1 karakteristik air gambut dari sebagian wilayah Indonesia yang merupakan hasil penelitian Puslitbang Pemukiman bekerja sama dengan PAU ITB (Irianto, 1998).
2.1.2 Pengolahan Air Gambut
Karakteristik air gambut seperti yang telah disebutkan di atas menunjukkan bahwa air gambut kurang menguntungkan untuk dijadikan air minum bagi masyarakat di daerah berawa. Namun karena jumlah air gambut tersebut sangat banyak dan dominan berada di daerah tersebut maka harus bisa menjadi alternatif sumber air minum masyarakat. Kondisi yang kurang menguntungkan dari segi kesehatan adalah sebagai berikut :
[image:31.595.114.545.120.375.2]• Kandungan organik yang tinggi dapat menjadi sumber makanan bagi mikroorganisma dalam air, sehingga dapat menimbulkan bau apabila bahan organik tersebut terurai secara biologi, (Wagner, 2001).
• Apabila dalam pengolahan air gambut tersebut digunakan klor sebagai desinfektan, akan terbentuk trihalometan (THM’S) seperti senyawa argonoklor yang dapat bersifat karsinogenik (kelarutan logam dalam air semakin tinggi bila pH semakin rendah), (Wagner, 2001).
• Ikatannya yang kuat dengan logam (Besi dan Mangan) menyebabkan kandungan logam dalam air tinggi dan dapat menimbulkan kematian jika dikonsumsi secara terus menerus (Wagner, 2001).
Metode pertukaran ion menggunakan resin MEIXR dapat menghilangkan warna sejati air (asam humat dan fulvat) dari 109 Pt;Co menjadi 1 Pt;Co. Dengan mempertimbangkan sebagian besar pengolahan air di Indonesia masih menggunakan sistem konvensional. Cara pengolahan air secara konvensional / pengolahan lengkap (koagulasi – flokulasi – sedimentasi – filtrasi – netralisasi dan desinfektan) dapat digunakan untuk menghilangkan warna terutama pembentuk warna semu sekitar 80 %, efisiensi penghilangan warna akan lebih efektif jika dilakukan modifikasi dan tambahan proses seperti aplikasi karbon aktif, reaksi redoks, dan koagulan – flokulan aid, (Pararaja, 2007).
Efektifitas proses elektrokoagulasi untuk memindahkan ( ) zat;zat organik dari limbah rumah potong hewan menggunakan sel;sel elektrolitik ( ) monopolar dan bipolar. Hasil menunjukkan bahwa pencapaian ( ) terbaik diperoleh menggunakan sistem elektroda baja ( ) bipolar yang dioperasikan pada intensitas arus 0,3 A selama 60;90 menit. Berhasil menurunkan BOD sebesar 86 ± 1%, lemak dan minyak sebesar 99 ± 1%, COD sebesar 50 ± 4%, TSS (total suspended solid) sebesar 89 ± 4% dan Turbidity sebesar 90 ± 4%. Total biaya yang dibutuhkan 0,71 USD $ / m3 limbah rumah potong hewan, (Asselin, M., 2008).
lapisan gel khususnya pada konsentrasi unsur;unsur humus yang tinggi dan pH awal yang tinggi yang dibentuk pada permukaan anoda. Hasil pengamatan menunjukkan bahwa konsentrasi awal unsur;unsur humus dan pH awal sangat efektif pada efisiensi dan tingkat penurunan. pH awal air limbah telah disesuaikan 5,0 dan efisiensi penurunan yang tinggi telah diamati. Sehingga sistem elektrokoagulasi akan dioperasikan pada pH rendah yaitu 5,0 pada konsentrasi unsur;unsur humus yang tinggi, (Koparal, A.S., 2008).
Pengolahan air gambut yang dilakukan dengan mengkombinasikan larutan tawas dan metode elektrokoagulasi yang kemudian di ujicoba ke model. Sebelum proses elektrokoagulasi berlangsung, air gambut terlebih dahulu dicampur dengan larutan tawas (tawas yang dikomersialkan dengan mutu 17 %) sebanyak 10 ml/l air gambut (kadar 1000 ppm). Proses elektrokoagulasi berlangsung optimum dengan waktu elektrokoagulasi 45 menit dengan memberikan tegangan pada elektroda aluminium sebesar 12 volt dan kecepatan alir 1 L/menit. Hasil uji coba ke model diperoleh persentase penurunan warna sebesar 91,79 % (dari 94,295 Pt; Co menjadi 7,746 Pt;Co), dan kekeruhan sebesar 98,68 % (dari 72,43 NTU menjadi 0,953 NTU) (Susilawati, et al., 2009).
2.1.3 Alternatif Proses Pengolahan Air Gambut
Berdasarkan pada pengetahuan tentang penyebab dan kandungan warna pada air gambut dan sifat;sifatnya, maka proses dan metode pengolahan yang dapat diterapkan untuk mengolah jenis air berwarna alami adalah : Proses oksidasi, Proses adsorpsi, Proses Koagulasi – Flokulasi, dan Proses elektrokoagulasi.
1. Proses Oksidasi
CO2 dan H2O apabila oksidasinya sempurna. Namun dalam aplikasinya biaya operasi relatif mahal, dan perlu digunakan unit penghasil ozon.
2. Proses Adsorpsi
Adsorbsi merupakan fenomena fisika dimana molekul;molekul bahan yang diadsorpsi tertarik pada permukaan bidang padat yang bertindak sebagai adsorban. Dengan demikian jelas bahwa adsorpsi merupakan fenomena bidang batas, yang efisiensinya makin tinggi apabila luas bidang permukaan adsorban makin besar (Schnitzer, 1992). Ditinjau dari segi derajat adsorpsi pada suatu jenis adsorban secara umum mengikuti aturan sebagai berikut (Cahyana, 2009) :
• Adsorpsi berlangsung sedikit terhadap semua senyawa organik, kecuali senyawa berhalogen (F, Br dan Cl).
• Adsorpsi berlangsung baik pada semua senyawa berhalogen dan senyawa alifatik.
• Adsorpsi berlangsung sangat baik terhadap semua senyawa aromatik, makin banyak kandungan inti benzennya makin baik adsorpsinya.
Berdasarkan kriteria di atas maka, pengolahan air berwarna (air gambut) dapat dilakukan dengan cara adsorpsi karena asam humus mempunyai gugus senyawa aromatik. Namun secara umum proses inipun masih mahal.
Dalam pengolahan air gambut dengan proses adsorpsi pada perinsipnya adalah menarik molekul asam;asam humus ke permukaan suatu adsorben. Contoh adsorben yang biasa digunakan adalah karbon aktif (charcoal), zeolit, resin, dan tanah liat dari lokasi sumber air gambut.
3. Proses Koagulasi – Flokulasi
Proses koagulasi yang diiringi dengan proses flokulasi merupakan salah satu proses pengolahan air yang sudah lama digunakan. Proses ini penting untuk penyisihan warna dan organik (Amirtarajah dan O’melia, 1999). Definisi koagulasi sebagai proses cukup banyak tapi dari laporan Fearing et al, (2004) dapat disimpulkan menjadi tiga :
2. Proses penambahan bahan kimia ke dalam air untuk menghasilkan spesies kimia yang berperan dalam destabilisasi kontaminan dan meningkatkan kemungkinan penyisihan.
3. Proses untuk menggabungkan partikel koloid dan partikel kecil menjadi agregat yang lebih besar dan dapat mengadsorb material organik terlarut ke permukaan agregat sehingga dapat mengendap.
Partikel koloid yang terkandung dalam air alam umumnya mempunyai muatan negatif, sehingga koagulan yang diperlukan adalah yang bermuatan positif. Koagulan yang umum digunakan dalam pengolahan air adalah garam aluminium seperti alum.
Flok;flok yang terbentuk pada umumnya juga mempunyai kemampuan adsorpsi yang cukup besar. Sehingga pada saat yang bersamaan dengan pembentukan dan penggabungan mikroflok akan terjadi proses adsorpsi dan pemerangkapan bahan;bahan terlarut dalam air, dan akan ikut tersisih dalam proses pengendapan dan penyaringan. Sedangkan pada air berwarna alami atau air gambut konsentrasi bahan koloid atau partikel tersuspensi lainnya umumnya sangat rendah. Sehingga ada pendapat mengatakan bahwa sesungguhnya proses koagulasi dan flokulasi yang dilaksanakan pada air berwarna tidak lain adalah melaksanakan proses adsorpsi dengan bantuan penambahan bahan kimia (Notodarmojo, 1994).
2.2 Proses Elektrokoagulasi
pada bejana elektrolisis yang didalamnya terdapat dua penghantar arus listrik searah yang disebut elektroda, yang tercelup dalam larutan elektrolit.
Gambar 2.4 Perinsip proses elektrokoagulasi (Ni’am, 2007)
Apabila dalam suatu larutan elektrolit ditempatkan dua elektroda dan dialiri arus listrik searah, maka akan terjadi peristiwa elektrokimia yaitu gejala dekomposisi elektrolit, yaitu ion positif (kation) bergerak ke katoda dan menerima elektron yang direduksi dan ion negatif (anion) bergerak ke anoda dan menyerahkan elektron yang dioksidasi. Sehingga membentuk flok yang mampu mengikat kontaminan dan partikel;partikel dalam limbah.
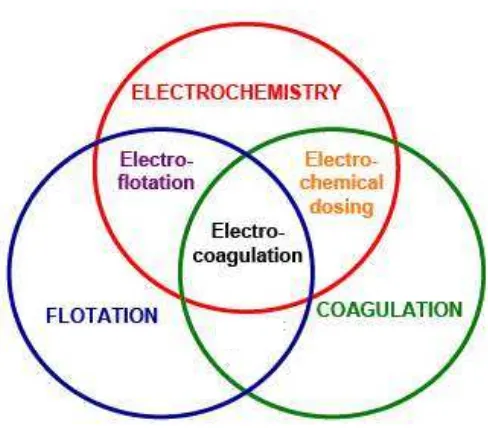
Diidentifikasikan terdapat tiga proses mendasar yang terjadi dalam elektrokoagulasi, yaitu elektrokimia, koagulasi dan flotasi. Ketiga proses ini dapat digambarkan dengan diagram Venn dimana kombinasi dari ketiganya menghasilkan teknologi elektrokoagulasi, sedangkan kombinasi yang lain menghasilkan teknologi yang berbeda (Gambar 2.5).
Gambar 2.5 Diagram Venn (Holt et al, 2004)
Sementara instalasi pengolahan lumpur secara elektrolisis dioperasikan dibeberapa tempat di Amerika Serikat pada awal tahun 1911 yang memiliki ukuran yang serupa dengan instalasi pengolahan air limbah pada masa tersebut (Vik et al., 1984 dalam Holt et al., 2004). Namun sejak tahun 1930;an semua instalasi tersebut tidak dioperasikan lagi dikarenakan biaya operasional yang tinggi dan adanya alternatif lain berupa penggunaan bahan kimia sebagai koagulan (Holt et al., 2004).
Pada massa sekarang penggunaan teknologi elektrokoagulasi mulai dikembangkan kembali untuk meningkatkan kualitas effluen air limbah. Elektrokoagulasi digunakan untuk mengolah effluen dari beberapa air limbah yang berasal dari industri makanan, limbah tekstil, limbah rumah makan, limbah yang mengandung senyawa arsenik, air yang mengandung flourida, dan air yang mengandung partikel yang sangat halus, bentonit dan kaolinit.
Untuk pertimbangan penentuan penggunaan elektrokoagulasi maka Mollah (2001) telah memberikan gambaran tentang keuntungan dan kerugiannya. Keuntungan dari penggunaan elektrokoagulasi adalah sebagai berikut :
[image:37.595.192.436.91.305.2]2. Air yang diolah dengan elektrokoagulasi menghasilkan effluen yang jernih, tidak berwarna dan tidak berbau.
3. Flok yang terbentuk pada elektrokoagulasi memiliki kesamaan dengan flok yang berasal dari koagulasi kimia. Perbedaannya adalah flok dari elektrokoagulasi berukuran lebih besar dengan kandungan air yang sedikit, lebih stabil dan mudah
dipisahkan secara cepat dengan filtrasi.
4. Effluen yang dihasilkan elektrokoagulasi mengandung TDS (
) dalam jumlah yang lebih sedikit dibandingkan dengan pengolahan kimiawi.
5. Proses elektrokoagulasi mempunyai keuntungan dalam mengolah partikel; partikel koloid yang berukuran sangat kecil, sebab diaplikasikan medan elektrik dengan gerak yang lebih cepat, sehingga proses koagulasi lebih mudah terjadi dan lebih cepat.
6. Proses elektrokoagulasi jauh dari penggunaan bahan kimia sehingga tidak bermasalah dengan netralisasi kelebihan bahan kimia, dan tidak ada polusi yang kedua yang disebabkan substansi;substansi kimia yang ditambahkan pada konsentrasi yang tinggi.
7. Produksi gelembung;gelembung gas selama elektrolisis dapat membawa polutan;polutan yang diolah untuk naik ke permukaan (flotasi) dimana flok tersebut dapat dengan mudah terkonsentrasi, dikumpulkan dan dipisahkan (
8. Perawatan reaktor elektrokoagulasi lebih mudah karena proses elektrolisis yang terjadi cukup dikontrol dari pemakaian listrik tanpa perlu memindahkan bagian;bagian didalamnya.
9. Teknologi elektrokoagulasi dapat dengan mudah diaplikasikan di daerah yang tidak terjangkau layanan listrik yakni dengan menggunakan panel matahari yang cukup untuk terjadinya proses pengolahan.
Sedangkan kerugian dari penggunaan elektrokoagulasi adalah :
1. Elektroda yang digunakan dalam proses pengolahan ini harus diganti secara teratur.
3. Penggunaan listrik kadangkala lebih mahal pada beberapa daerah.
4. Teknologi ini membutuhkan konduktivitas yang tinggi pada air limbah yang diolah.
2.2.1 Mekanisme Dalam Elektrokoagulasi
Reaktor elektrokimia merupakan sebuah sel elektrokimia dimana kutub anoda yang berupa logam (biasanya alumunium atau terkadang besi) dimana ion logam yang terlepas berfungsi sebagai agen koagulan. Dan secara simultan terjadi gelembung gas hidrogen di kutub katoda.
Elektrokoagulasi mempunyai kemampuan untuk mengolah berbagai macam polutan termasuk padatan tersuspensi, logam berat, tinta, bahan organik, minyak dan lemak, ion dan radionuklida. Karakteristik fisika kimia dari polutan mempengaruhi mekanisme pengolahan misalnya polutan berbentuk ion akan diturunkan melalui proses presipitasi sedangkan padatan tersuspensi yang bermuatan akan diabsorbsi ke koagulan yang bermuatan. Kemampuan elektrokoagulasi untuk mengolah berbagai macam polutan menarik minat industri untuk menggunakannya.
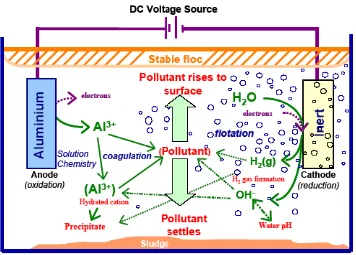
Gambar (2.6) memperlihatkan proses elektrokoagulasi yang sangat kompleks. Dimana koagulan dan produk hidrolisis saling berinteraksi dengan polutan atau dengan ion yang lain atau dengan gas hidrogen.
Menurut Holt et al. (2006) ada berbagai kemungkinan mekanisme yang terjadi dalam elektrokoagulasi (interaksi dalam larutan) yaitu :
1. Migrasi ke muatan elektroda yang berlawanan ( ) dan agregatisasi netralisasi muatan.
2. Kation atau ion OH;membentuk suatu presipitasi dengan polutan
3. Interaksi kation logam dengan OH; untuk membentuk suatu hidroksida yang mempunyai sifat;sifat adsorpsi yang tinggi sekaligus mengikat polutan (jembatan koagulasi).
4. Hidroksida membentuk struktur seperti kisi yang lebih besar dan
Gambar 2.6 Mekanisme dalam elektrokoagulasi (Holt, 2006)
Menurut Mollah (2004) mekanisme penyisihan yang umum terjadi di dalam elektrokoagulasi terbagi dalam tiga faktor utama yaitu : (a) terbentuknya koagulan akibat proses oksidasi elektrolisis pada elektroda, (b) destabilisasi kontaminan, partikel tersuspensi, dan pemecahan emulsi, dan (c) agregatisasi dari hasil destabilisasi untuk membentuk flok.
Sedangkan proses destabilisasi kontaminan, partikel tersuspensi, dan pemecahan emulsi terjadi dalam tahapan sebagai berikut :
• Kompresi dari lapisan ganda ( ) difusi yang terjadi di sekeliling spesies bermuatan yang disebabkan interaksi dengan ion yang terbentuk dari oksidasi di elektroda.
• Netralisasi ion kontaminan dalam air limbah dengan menggunakan ion berlawanan
[image:40.595.137.493.94.349.2]• Terbentuknya flok, dimana flok ini terbentuk akibat proses koagulasi sehingga terbentuk sludge blanket yang mampu menjebak dan menjembatani partikel koloid yang masih ada di air limbah.
2.2.2 Pelarutan Logam di Elektroda
Pada percobaan elektrokoagulasi, elektroda yang digunakan selalu dihubungkan dengan sumber listrik DC. Jumlah logam yang larut tergantung pada jumlah arus listrik yang mengalir pada elektroda tersebut. Hukum Faraday membuat hubungan antara kuat arus (I) yang mengalir dengan jumlah massa yang terlepas ke larutan, hal ini merupakan pendekatan secara teoritis untuk menghitung jumlah alumunium yang terlepas ke larutan. Adapun rumus dari hukum Faraday adalah sebagai berikut :
. . .
= (2.1)
Dimana : = Berat aluminium yang larut (g)
= Kuat arus listrik yang digunakan (Ampere) = Lamanya arus mengalir (detik)
= berat molekul plat logam (aluminium) / berat atom = valensi (aluminium = 3)
= Konstanta Faraday, (96500 C/mol)
Dengan menggunakan persamaan (2;1) kita dapat membandingkan antara jumlah logam yang larut secara teoritis dengan percobaan di lapangan. Seringkali diperoleh hubungan yang cukup baik antara hasil percobaan dengan teori. Walaupun kadangkala terdapat perbedaan/erorr yang signifikan yang dapat terjadi karena tidak memperhatikan ukuran dan bentuk elektroda yang tepat serta pemasangan elektroda yang kurang baik.
2.2.3 Reaksi di Elektroda
diperlukan beda potensial diantara elektroda. Perbedaan potensial ini diperlukan untuk menimbulkan reaksi elektrokimia pada masing;masing elektroda.
Dari berbagai penelitian yang ada telah didesain berbagai macam konfigurasi elektroda seperti pemakaian pellet aluminium dengan reaktor fluidized bed (Barkley et al., 1993), elektroda aluminium bipolar (Mameri et al., 1998), elektroda mesh (Matteson et al., 1995), baja bipolar berbentuk lingkaran (Ogutveren et al., 1992), dan juga elektroda sederhana berbentuk lempengan (Vik et al., 1984; Mameri et al., 1998 : Holt et al., 2001). Selain itu berbagai jenis elektroda telah dicoba seperti aluminium, besi, baja dan platinum. Bahan elektroda digunakan untuk mengetahui jenis koagulan yang timbul. Aluminium merupakan elektroda yang paling banyak digunakan, dimana pada proses elektrokogulasi reaksi yang terjadi adalah :
Reaksi Pada Katoda
Reaksi pada katoda adalah reduksi terhadap kation, jadi yang diperhatikan hanya kation saja.
1. Jika larutan mengandung ion;ion logam alkali, ion;ion logam alkalitana, ion Al3+ dan ion Mg2+, maka ion;ion logam ini tidak dapat direduksi dari larutan. Yang akan mengalami reduksi adalah pelarut (air), dan terbentuk gas hidrogen (H)2 pada katoda. Reaksi yang terjadi di katoda tergantung pada pH air yang diolah. Pada kondisi netral atau basa, gas hidrogen terjadi dengan reaksi :
2H2O + 2e → 2OH; + H2
Dari daftar E0 diketahui bahwa reduksi terhadap air lebih mudah berlangsung daripada reduksi terhadap ion;ion di atas.
2. Sedangkan pada kondisi asam, reaksi pembentukan gas hidrogen adalah sebagai berikut : 2H+ + 2e → H2
3. Jika larutan mengandung ion;ion lain, maka ion;ion logam ini akan direduksi menjadi masing;masing logamnya dan logam yang terbentuk itu diendapkan pada permukaan batang katoda.
Fe2+ + 2e → Fe Mn2+ + 2e → Mn Reaksi Pada Anoda
Al → Al3+ + 3e
Reaktor yang mempergunakan aluminium pada kedua elektroda yaitu anoda dan katoda dilaporkan proses pelarutan aluminium melebihi 100% (Przhegorlinskii et al., 1987 ; Bozin and Mikhailov, 1990 ; Donini et al., 1994 ; Mameri et al., 1998 dalam Holt, 2002). Untuk penggunaan aluminium pada kedua elektroda, reaksinya adalah sebagai berikut: Al3+ + 3 H2O → Al(OH)3 + 1.5 H2 Sedangkan proses pelepasan aluminium pada kutub katoda adalah sebagai berikut
Al3+ + 4 H2O + e → Al(OH);4 + 2 H2
Secara garis besar, faktor;faktor yang mempengaruhi reaksi elektroda dapat dibagi dalam 5 variabel, yaitu :
1. Variabel elektroda
(Jenis, luas permukaan, kondisi permukaan, jarak antar elektroda) 2. Variabel perpindahan massa
(Cara perpindahan, konsentrasi permukaan, adsorbsi) 3. Variabel larutan
(Konsentrasi spesi elektroaktif dalam bagian terbesar larutan, spesi;spesi lainnya,
sifat pelarut).
4. Variabel listrik (Potensial, arus, jumlah muatan coulomb) 5. Variabel luar (Temperatur, tekanan, waktu)
2.2.4 Sel Elektrokimia
yang dipisahkan oleh paling sedikit satu fase elektrolit. Elektroda tempat terjadinya oksidasi disebut anoda dan elektroda tempat terjadinya reduksi disebut katoda.
Oksidasi yaitu suatu perubahan kimia, jika (Hiskia, 1992) : • Suatu zat memberikan atau melepaskan elektron
• Suatu unsur mengalami pertambahan bilangan oksidasi atau tingkat oksidasi • Terjadi pada anoda atau elektroda positif suatu sel elektrokimia
Sedangkan reduksi ialah suatu perubahan kimia, jika : • Suatu zat menangkap atau menerima elektron
• Suatu unsur mengalami pengurangan bilangan oksidasi atau tingkat oksidasi • Terjadi pada katoda atau elektroda negatif suatu sel elektrokimia
2.2.5 Proses Koagulasi
Proses koagulasi merupakan faktor kunci dalam elektrokoagulasi, proses ini menggambarkan interaksi antara koagulan dengan bahan polutan yang hendak diolah. Perinsip dari koagulasi adalah destabilisasi partikel koloid dengan cara mengurangi semua gaya yang mengikat, kemudian menurunkan energi penghalang dan membuat partikel menjadi bentuk flok. Koagulasi merupakan proses destabilisasi partikel;partikel koloid untuk memfasilitasi pertumbuhan partikel;partikel selama flokulasi.
Koagulasi menurut Mackenzie L. Davis, adalah proses untuk membuat partikel;partikel kecil (koloid) dapat bergabung satu dengan yang lainnya sehingga membentuk flok yang lebih besar. Sedang menurut Reynold (1977), koagulasi adalah proses destabilisasi pada suatu sistem koloid yang berupa penggabungan dari partikel;partikel koloid akibat pembubuhan bahan kimia. Pada proses ini terjadi pengurangan besarnya gaya tolak menolak antara partikel; partikel koloid di dalam larutan.
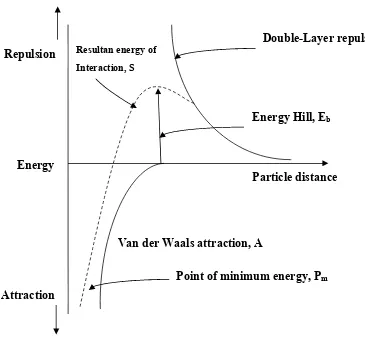
mendekat hingga jarak keduanya dapat mencapai jarak dalam dimensi atom, maka dalam keadaan seperti ini gaya Van der Waals akan berpengaruh pada kestabilan partikel koloid. Besarnya gaya tarik menarik Van der Waals berbanding terbalik dengan kuadrat jarak antara kedua partikel koloid, sedangkan besarnya gaya tolak menolak elektrostatis akan berkurang secara eksponensial dengan makin besarnya jarak antar partikel. Kedua gaya tersebut dapat dilukiskan dalam suatu grafik, seperti pada Gambar 2.7.
Kurva A menunjukkan gaya tarik menarik Van der Waals, sedangkan kurva R menunjukkan gaya tolak menolak elektrostatis. Resultan dari kedua gaya ini dilukiskan sebagai kurva S.
Gambar 2.7 Gaya;gaya yang terjadi pada interaksi antar partikel koloid (Fair, 1978)
Gambar 2.8 memperlihatkan bahwa makin besar konsentrasi ion;ion positif, maka besarnya gaya resultan maksimum akan mengecil sehingga pada akhirnya dapat mencapai nol.
Hal ini menunjukkan telah terjadi kesetimbangan antara kedua gaya tersebut. Berkurangnya gaya tolak menolak ini ditunjukkan dengan berkurangnya harga potensial zeta. Pada suatu konsentrasi aluminium sulfat tertentu harga potensial zeta akan mencapai harga kritis seperti yang telah dikemukakan di atas. Maka selanjutnya gaya;gaya Van der Waals akan mulai bekerja untuk memperkuat ikatan antar partikel dan terjadilah penggabungan dari partikel; partikel koloid tersebut.
Resultan energy of
Interaction, S
Particle distance
Double9Layer repulsion, R
Energy Hill, Eb
Van der Waals attraction, A
Point of minimum energy, Pm Repulsion
[image:46.595.124.489.80.419.2]Gambar 2.8 Pengurangan gaya tolak menolak oleh ion;ion aluminium (Fair et al, 1978)
2.2.6 Proses Flokulasi
Flokulasi adalah proses kontak diantara partikel;partikel koloid yang telah mengalami destabilisasi sehingga ukuran partikel;partikel tersebut tumbuh menjadi partikel;partikel yang lebih besar (Kiely, 1998). Dalam hal ini proses koagulasi harus diikuti flokulasi yaitu penggumpalan koloid terkoagulasi sehingga membentuk flok yang mudah terendapkan atau transportasi partikel tidak stabil, sehingga kontak antar partikel dapat terjadi (Sutrisno, 1991).
Koagulasi dan flokulasi diperlukan untuk menghilangkan material limbah berbentuk suspensi atau koloid. Koloid dihadirkan oleh partikel;partikel berdiameter sekitar 1 nm (10;7 cm) hingga 0.1 nm (10;8 cm). Partikel;partikel ini tidak dapat mengendap dalam periode waktu yang wajar dan tidak dapat dihilangkan dengan proses perlakuan fisika biasa.
Koloid yang tidak stabil cenderung untuk menggumpal, walaupun kecepatan penggumpalannya sangat lambat. Kecepatan penggumpalan ini ditentukan oleh
or concentration of electrolyte Increasing
charge Repulsion
Attraction
Particle distance R1
R2 R3
[image:47.595.137.490.88.358.2]Penggabungan partikel;partikel koloid dapat terjadi karena : 1. Gerak Brown (perikinetik)
2. Gradien kecepatan dalam media suspensi (ortokinetik) yang bergantung pada temperatur, kecepatan aliran air, jumlah partikel koloid, konsentrasi dan ukuran partikel koloid.
2.2.7 Faktor9Faktor Yang Mempengaruhi Koagulasi dan Flokulasi
Proses koagulasi;flokulasi optimum, dapat dicapai dengan pengaturan kondisi;kondisi yang saling berkaitan dan mempengaruhi proses tersebut, seperti : a. Pengaruh Temperatur Air
Apabila temperatur menurun maka viskositas air akan meningkat sehingga kecepatan mengendap flok akan menurun. Proses koagulasi – flokulasi lebih mudah dilakukan pada temperatur tinggi daripada temperatur rendah, karena viskositas air pada temperatur tinggi lebih rendah daripada viskositas air pada temperatur rendah. Hubungan antara temperatur dengan proses koagulasi – flokulasi adalah sebagai berikut :
1. pH optimum untuk proses koagulasi akan berubah;ubah karena pengaruh temperatur.
2. Dosis koagulan akan bertambah bila temperatur turun.
3. Untuk dosis koagulan tertentu, effluen dari proses koagulasi – flokulasi akan mempunyai kekeruhan yang lebih tinggi bila temperatur rendah.
b. Pengaruh derajat keasaman (pH) dan alkalinitas.
c. Pengaruh Jenis Koagulan
Koagulan adalah bahan kimia yang ditambahkan untuk membantu proses koagulasi. Pemilihan jenis koagulan pada pengolahan air seharusnya didasarkan kepada penelitian perbandingan performa koagulan dan setelah itu baru dilihat dari segi ekonomisnya. Jenis koagulan yang paling banyak dipakai di Indonesia adalah tawas atau alumunium sulfat.
d. Pengaruh Tingkat Kekeruhan Air Baku
Pada tingkat kekeruhan yang rendah, proses destabilisasi akan sukar terjadi. sebaliknya pada tingkat kekeruhan yang tinggi proses destabilisasi akan dapat berlangsung dengan cepat, tetapi bila pada kondisi tersebut dipakai dosis koagulan yang rendah maka pembentukan flok kurang efektif. Hubungan dosis koagulan dan tingkat kekeruhan secara garis besar dapat dijelaskan sebagai berikut :
1. Umumnya dosis koagulan akan naik bersamaan dengan meningkatnya kekeruhan, akan tetapi kenaikan dosis koagulan ini tidak berbanding lurus dengan peningkatan kekeruhan.
2. Apabila kekeruhan sangat tinggi akan diperlukan koagulan yang lebih sedikit karena besarnya tumbukan antar partikel;partikel koloid yang telah dikoagulasi. Dan bila kekeruhan rendah kemungkinan terjadinya tumbukan tidak terlalu besar sehingga sulit terkoagulasi.
3. Bervariasinya distribusi ukuran partikel lebih memudahkan terjadinya koagulasi, dibanding dengan suspensi yang hanya terdiri dari satu jenis ukuran partikel saja.
e. Pengaruh Jumlah Garam9Garam Terlarut Dalam Air
Secara garis besarnya pengaruh garam;garam terlarut adalah sebagai berikut :
1. Pengaruh anion lebih besar daripada kation, sehingga ion seperti Natrium, kalsium dan Magnesium tidak memberikan pengaruh yang berarti terhadap proses koagulasi.
2. Ion;ion negatif memperbesar daerah pH optimum koagulasi untuk koagulasi ke arah bagian yang sama, yang tergantung juga pada valensi ion;ion tersebut. Dengan kata lain ion;ion monovalen seperti chlorida, nitrat dan sebagainya tidak memberikan pengaruh yang berarti dibandingkan dengan pengaruh yang diberikan oleh ion;ion sulfat, fosfat dan anion;anion bervalensi lainnya.
f. Pengaruh Kondisi Pengadukan
Pengaturan kondisi pengadukan sangat penting untuk mencapai proses koagulasi;flokulasi yang baik. Pengaturan kondisi pengadukan dapat dilakukan dengan mengatur gradien kecepatan (G) dan lamanya waktu pengadukan (t). Pencampuran koagulan harus benar;benar merata, sehingga koagulan yang dibubuhkan akan bereaksi dengan partikel;partikel koloid atau ion;ion lain dalam suspensi. Disamping itu kecepatan pengadukan sangat mempengaruhi pertumbuhan flok dan bila terlalu besar kecepatan pengadukannya akan mengakibatkan pecahnya flok. Karena kecepatan koagulasi;flokulasi berbanding langsung dengan besarnya gradien kecepatan (G), maka proses koagulasi – flokulasi yang baik dari G.t yang tepat.
2.3 Tinjauan Koloid
Tinjauan koloid digunakan untuk menjelaskan suatu sistem dimana partikel;partikel padat baik organik maupun anorganik yang berukuran relatif kecil terdispersi di dalam suatu media yang homogen (Hartomo, 1994). Partikel; partikel koloid berada di suspensi karena ukurannya yang sangat kecil, keadaan hidrasi dan memiliki muatan listrik pada permukaannya. Partikel koloid mempunyai sifat;sifat antara lain :
Partikel koloid terdispersi dalam air dan merupakan partikel yang sangat kecil
(diameter 1m ; 1 ), selalu dalam keadaan melayang dan tidak mudah diendapkan. Partikel koloid akan bermuatan listrik apabila terjadi penyerapan ion pada permukaan partikel. Peristiwa penyerapan pada permukaan suatu zat disebut adsorpsi. Suatu koloid mempunyai kemampuan mengabsorpsi, sebab zat;zat dalam bentuk koloidal memiliki permukaan yang sangat luas sehingga terjadi gejala terikatnya atom, molekul atau ion pada permukaan zat padat dan bekerja suatu gaya tarik / gaya Van Der Waals (Chatterjee, 1979).
* Bermuatan Listrik
Pada permukaan partikel koloid terdapat muatan listrik sejenis yang menyebabkan keadaan stabil dimana muatan diantara partikel koloid saling tolak menolak sehingga tidak dapat membentuk partikel lebih besar.
* Sifat Hidrasi
Yaitu sifat koloid yang mempunyai gaya gabung yang besar terhadap media air. Berdasarkan sifat hidrasi, partikel koloid dapat dibagi dalam 2 golongan yaitu golongan koloid suka air (koloid hidrofil) dan golongan koloid tidak suka air (koloid hydropob).
2.3.1 Kestabilan Koloid
Kestabilan sistem koloid hidrofil adalah karena adanya fenomena hidrasi yaitu suatu peristiwa di mana molekul;molekul air tertarik oleh permukaan partikel zat padat (koloid) dan berfungsi sebagai penghalang untuk terjadinya kontak dengan partikel koloid lainnya (Hammer, 1977). Contoh : sabun, detergen sintetik dan protein terlarut.
2.3.2 Destabilisasi Partikel Koloid
Perinsip dasar untuk mengendapkan partikel koloid adalah menurunkan stabilitasnya dengan cara netralisasi gaya tolak menolak akibat adanya muatan listrik pada permukaan koloid. Setelah itu dilanjutkan dengan pengadukan agar terjadi penggabungan antara partikel;partikel, membentuk partikel yang lebih besar dan dapat diendapkan.
Agar partikel;partikel koloid dapat menggumpal, dua langkah harus terjadi yaitu : 2. Gaya tolak menolak harus dikurangi (destabilisasi)
3. Adanya transportasi partikel supaya terjadi kontak antara partikel (proses flokulasi), (Stum dan O’melia, 1968).
Empat macam mekanisme untuk menerangkan proses destabilisasi koloid yaitu : b. Pemampatan lapisan ganda.
c. Adsorbsi untuk menghasilkan netralisasi muatan. d. Penjaringan partikel dalam presipitat.
e. Adsorbsi dan pengikatan antar partikel.
a. Pemampatan Lapisan Ganda
Menurut Schulze;Hardy koagulasi disebabkan oleh ion;ion yang mempunyai muatan yang berlawanan dengan muatan partikel koloid. Kekuatan ion untuk mengkoagulasi ditentukan oleh valensi ion. Penambahan ion;ion yang berlawanan muatan dengan muatan partikel yang berasal dari koagulan akan menimbulkan destabilisasi partikel koloid sehingga lapisan difus akan mengecil (mampat) dan memungkinkan bekerjanya gaya tarik menarik antar partikel. Fenomena ini diterangkan dengan teori yang dikembangkan oleh Vervey dan Overbeek (1948).
Efek dari pamampatan ini adalah berkurangnya potensial permukaan. Apabila dosis elektrolit dinaikkan akan semakin berkurang pula potensial permukaan, sehingga memungkinkan terjadinya penggabungan partikel oleh gaya tarik menarik Van der Waals.
b. Adsorbsi dan netralisasi muatan
1. Spesi yang teradsorpsi dapat mendestabilisasi koloid dengan dosis yang jauh lebih
rendah dibanding dengan ion;ion pemampat lapisan ganda.
2. Destabilisasi adsorpsi adalah stoikiometris, yang berarti dosis koagulan bertambah dengan bertambahnya konsentrasi koloid. Sedang pada pemampatan lapisan ganda jumlah elektrolit yang dibutuhkan tidak stoikiometris dan tidak tergantung pada konsentrasi koloid.
3. Efek yang timbul bila dosis spesi yang diadsorpsi berlebihan adalah terjadinya restabilisasi, hasil dari pembalikan muatan pada partikel koloid.
Beberapa spesi kimia dapat diadsorpsi pada permukaan partikel koloid. Bila spesi yang diadsorpsi membawa muatan yang berlawanan dengan muatan partikel koloid, maka adsorpsi tersebut menyebabkan terjadinya pengurangan potensial permukaan dan menghasilkan destabilisasi partikel koloid. Ion;ion yang di adsorpsi dapat melebihi batas netralisasi hingga mencapai titik pembalikan muatan. Ini menunjukan bahwa interaksi kimiawi dapat melebihi efek tolak menolak elektrostatik pada beberapa kasus (Stumm dan O’melia, 1968).
c. Penjaringan Partikel Dalam Presipitat
Sejumlah garam yang berasal dari logam tertentu, seperti : Al2(SO4)2, FeCl3, dan MgCO3 dapat membentuk presipitat bila ditambahkan ke dalam dispersi koloid dalam jumlah yang cukup. Koloid dapat bertindak sebagai inti kondensasi bagi pembentukan presipitat tersebut, atau dapat juga terjaring sebagai endapan presipitat. Pengurangan koloid dengan cara demikian disebut ”
”.
Gambar 2.9 Terjadinya proses ”Sweep;Floc” (Duan, 2003)
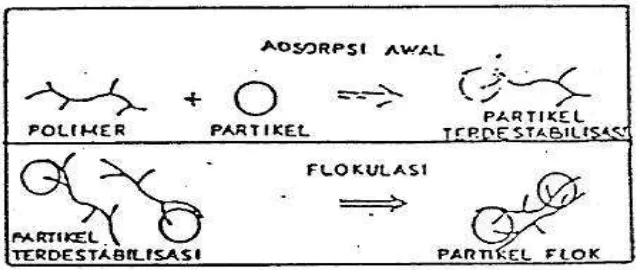
d. Adsorpsi dan pengikatan Antar Partikel
Destabilisasi dengan cara ini terjadi bila ke dalam dispersi koloid dimasukkan polimer dengan struktur rantai panjang dan bersegmen. Molekul polimer akan melekat pada permukaan partikel koloid pada satu tempat atau lebih, seperti terlihat pada Gambar 2.10. Ujung segmen polimer akan meluas ke bagian terbesar larutan dan menempel pada bagian partikel koloid lainnya membentuk jembatan kimia. Kekuatan ikatan ini menghasilkan partikel flok yang lebih kompak dan lebih mudah diendapkan.
[image:54.595.161.464.82.311.2] [image:54.595.164.485.558.693.2]Dalam proses elektrokoagulasi hanya ada dua mekanisme destabilisasi yang mungkin terjadi yaitu penyaringan dalam presipitat dan netralisasi muatan. Dua mekanisme yang lain yaitu pemampatan lapisan ganda dan pengikatan antar partikel tidak mungkin terjadi karena pada mekanisme pemampatan lapisan ganda dibutuhkan dosis koagulan yang tinggi agar terjadi destabilisasi koloid sedangkan pada proses elektrokoagulasi aluminium yang dibutuhkan masih relatif rendah. Untuk mekanisme pengikatan antar partikel karena tidak adanya penambahan polimer dalam proses elektrokoagulasi, maka mekanisme ini juga tidak dapat terjadi.
2.3.3 Konsep Potensial Zeta
Menurut Eckenfelder (1989), potensial listrik diantara bidang geser dan badan cairan dapat ditentukan dengan pengukuran elektroforesis (pengukuran laju partikel dalam suatu medan listrik) dan disebut potensial zeta. Konsep potensial zeta berasal dari teori lapisan rangkap listrik dan diterapkan untuk koloid hidrofob. Menurut kaedah Gouy, Champman dan Stern, partikel yang tersuspensi di dalam permukaan air mempunyai muatan listrik pada permukaannya. Muatan ini dapat meningkat jika terjadi ionisasi atom;atom pada permukaan partikel atau unsur;unsur yang berlawanan muatan dengan partikel dan adsorbsi ion;ion oleh partikel dalam air.
Ion;ion tersebut mengelilingi permukaan partikel dengan rapat dan menarik
ion;ion yang berlawanan muatan dari dalam larutan, sehingga sebagian partikel akan terimbangi. Lapisan muatan tersebut merupakan lapisan yang tidak bergerak (tetap) disebut lapisan rapat muatan (lapisan stern atau fixed layer). Fixed layer dilapisi lagi oleh lapisan dengan muatan berlawanan dengannya. Lapisan ini dapat bergerak dan disebut lapisan geser. Potensial zeta didefinisikan dalam persamaan
. . . 4π
= (2.2)
Kestabilan sistem koloid dapat dikurangi dengan memperkecil potensial zeta, dengan cara menambahkan ion yang berlawanan muatan sehingga perbedaan muatan pada permukaan dapat dikurangi. Dengan berkurangnya pe