GAMBAR ALAT
DAFTAR PUSTAKA
Darmong,(1995),“Logam Dalam Sistem Biologi Makhluk Hidup”,Cetakan Pertama, Penerbit UI-Press,Jakarta
Mukhlis,(2007),“Analisis Tanah Tanaman”,Cetakan Pertama,Penerbit USU press,Medan
Poerwowidodo,(2010),“Telaah Kesuburan Tanah”,Penerbit ANGKASA, Bandung Sarifuddin,(2011),“Kimia Tanah Teori Dan Aplikasi”,Cetakan Pertama,Penerbit
USU Press,Medan
Sudjadi,(2007),“Kimia Farmasi Analisis”,Cetakan Pertama, Penerbit PUSTAKA PELAJAR,Yogyakarta
BAB III
METODOLOGI PERCOBAAN
3.1 Alat-alat
Labu ukur 100 ml terkalibrasi Pyrex
Pipet tetes -
Pipet volume Pyrex
Bola karet -
Neraca analitik -
Gelas ukur Pyrex
Tabung reaksi plastik Pyrex
Botol aquadest -
Tabung bigest -
Kertas saring whatman No.42 -
Corong -
Gelas Piala Pyrex
Buret -
Penangas Air -
3.2 Bahan- bahan
HNO3 (p) 65%
3.3 Pembuatan Larutan Standar Pb
a. Pembuatan larutan standar Pb 100 ppm
Dipipet 10 ml larutan induk Pb 1000 ppm ke dalam labu ukur 100 ml di
encerkan dengan aquadest hingga garis batas, kemudian di homogenkan.
b. Pembuatan larutan seri standar Pb 0,1 ; 0,5 ; 1 ; 1,5 ; dan 2 ppm
Dipipet masing-masing 0,01 ml ; 0,05 ml ; 0,1 ml ; 0,15 ml ; 0,2 ml dan
dimasukkan kedalam labu ukur 100 ml, diencerkan dengan aquabides yang
telah diasamkan hingga garis tanda, dikocok.
c. Dimasukkan larutan standar ke masing-masing tabung bigest
d. Dimasukkan tabung bigest yang berisi larutan standar dan berisikan
sampel kedalam autosampler SSA
3.4 Prosedur Percobaan
3.4.1. Pembuatan Kurva Standar
a. Diukur masing-masing absorbansi larutan seri standar Pb 0,1 ; 0,5 ; 1 ;
1,5 ; dan 2 ppm dengan spektrofotometer serapan atom pada panjang
gelombang ( ) = 217 nm
3.4.2. Preparasi Sampel
a. Ditimbang 2,500 g tanah halus
b. Dimasukkan kedalam tabung bigest
c. Ditambahkan 5 ml HNO3(P) dibiarkan selama 1 malam
d. Dipanaskan pada suhu 1000c selama 1 jam 30 menit
e. Didinginkan
f. Ditambahkan 5ml HNO3(P)
g. Ditambahkan 1 ml HClO4(P)
h. Dipanaskan hingga suhu 1300C Selama 1 jam dan ditingkatkan
menjadi 1500C selama 2 jam 30 menit sampai uap kuning habis
i. Ditingkatkan suhu menjadi 1700C selama 1 jam, kemudian suhu
ditingkatkan menjadi 2000C selama 1 jam (hingga terbentuk uap putih) .
j. Dekstruksi selesai dengan terbentuknya endapan putih atau sisa larutan
k. Didinginkan ekstrak
l. Diencerkan dengan air bebas ion menjadi 25 ml
m. Dikocok hingga homongen
n. Dibiarkan semalam
o. Dianalisa ke SSA
3.4.3. Pengukuran Absorbansi Sampel
Hasil preparasi sampel di ukur dengan spektrofotometer serapan atom pada panjang gelombang ( ) = 217 untuk analisis Pb.
3.4.4. Instruksi Kerja Spekrofotometer Serapan Atom a. Pastikan bahwa power switch dalam posisi off.
b. Hubungkan steker voltage regulator dan kompresor ke stop kontak 220
volt.
c. Hidupkan voltage regulator ,komputer dan exhaust system.
d. Buka kran gas asetilen/nitrous oxyde (sesuai keperluan) dan hidupkan
alat spektrofotometer serapan atom.
e. Klik program kerja AAS GBC pada layar monitor, sehingga terbuka
lembaran kerja.
f. Setelah itu, klik “methode” dan pilih unsur yang akan dianalisa, catat
deretan larutan standart yang digunakan sesuai dengan unsur yang
g. Klik “samples” dan tuliskan sampel yang akan dianalisa pada label
sampel.
h. Klik “analysis” untuk menentukan pemilihan metoda dan sampel yang
sesuai.
i. Klik “instrument”, klik “properti” pastikan posisi lampu sudah benar kemudian klik “hardwere set-up”, sesuaikan model, asesoris, setting
dan communication, kembali close.
j. Klik “report” pilih apa saja yang diperlukan untuk pelaporan misalnya
grafik dan sebagainya.
k. Klik “result”, dan “gas flows optimatisations” pada sudut kanan atas
layar monitor.
l. Pastikan alat sudah dalam keaadaan “instrument ready” pada sebelah
bawah layar monitor.
m.Hidupkan flame dengan mengklik “ignite flame” pada gas flow
optimatisation atau memecet tombol warna kuning pada alat.
n. Lakukan optimatisation absorban dari salah satu larutan standart,
dengan menaikan atau menurunkan “ fuel flow”, pada gas flows optimatisation, setelah itu klik “perform instrument zero”
o. Buka lembaran “result”. Lakukan analisa dengan mengklik “start” pada
monitor, maka alat akan bekerja secara otomatis dan yang pertama
dilakukan adalah mengkalibrasi larutan standart, kemudian analisa
sampel.
p. Hasil kalibrasi larutan standart serta hasil analisa sampel dapat dibaca
q. Setelah analisa berakhir matikan flame dengan menekan tombol kuning
pada alat, tutup kran gas asetilen/nitrous oxyde.
r. Klik kembali “gas flows optimatisation”, keluarkan sisa gas yang masih ada pada alat dengan mengklik “bleed lines” berulang kali sehingga sisa
gas dianggap sudah habis.
s. Hidupkan printer dan cetak laporan hasil analisa sesuai keperluan.
t. Matikan alat, komputer dan kompresor serta voltage regulator dan cabut
4.2 Perhitungan
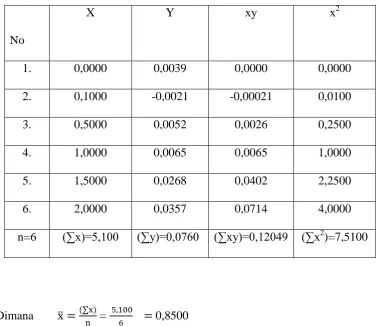
Untuk menentukan persamaan garis regresi dari kurva kalibrasi dapat
ditentukan dengan menggunakan metode Least Square sebagai berikut :
Tabel 4.3. Data Perhitungan persamaan garis regresi untuk analisis Pb
dengan Spektrofotometer Serapan Atom.
No
X Y xy x2
1. 0,0000 0,0039 0,0000 0,0000
2. 0,1000 -0,0021 -0,00021 0,0100
3. 0,5000 0,0052 0,0026 0,2500
4. 1,0000 0,0065 0,0065 1,0000
5. 1,5000 0,0268 0,0402 2,2500
6. 2,0000 0,0357 0,0714 4,0000
n=6 (∑x)=5,100 (∑y)=0,0760 (∑xy)=0,12049 (∑x2)=7,5100
Dimana ̅ = 0,8500
̅ = 0,01267
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan :
Dimana a = slope ; dan b = intersept
Harga a diperoleh dengan mensubstitusikan nilai-nilai yang terdapat pada tabel
4.3.
Tabel 4.3 kedalam persamaan berikut :
Untuk Pb :
0,0176
Sedangkan harga b adalah :
b = ̅ - a ̅
Untuk Pb :
b = 0,01267-((0,0176)(0,8500)
b = -0,00229
Sehingga persamaan garis regresinya adalah :
Untuk Pb : y = 0,0176x– 0,00229
Konsentrasi sampel dapat dihitung dengan menggunakan persamaan garis
Berdasarkan analisa yang dilakukakan diperoleh konsentrasi dari Pb
adalah 1,86307 mg/l dengan demikian tanah tersebut bagus untuk dilakukan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari data yang diperoleh analisa penentuan kadar Pb (Timbal) pada tanah
di Balai Besar Perbenihan dan Proteksi Tanaman Pekebunan (BBPPTP) Medan,
diperoleh kesimpulan sebagai berikut:
1. Metode analisa yang digunakan dalam penentuan kadar logam Pb (Timbal)
didalam tanah adalah dengan menggunakan spektrofotometer serapan atom
(SSA) pada panjang gelombang 217 nm.
2. Dari hasil pengukuran yang diperoleh, dinyatakan tanah yang dianalisa berada
dibawah standar mutu baku Pb dalam tanah 2-200 ppm yaitu dibawah 2 ppm
3. Kadar logam Pb yang diperoleh adalah 1,1642 mg/l
5.2 Saran
1. Dalam melakukan penganalisaan, prosedur percobaan yang dilakukan harus
benar dipahami dan teknik analisa yang dilakukan juga harus
benar-benar teliti dan konsentrasi agar didapat kan tingkat kesalahan yang lebih
2. Sebaiknya preparasi sampel dilakukan terlebih dahulu sebelum
BAB II
TINJAUAN PUSTAKA
2.1. Tanah
Tanah adalah suatu benda alam yang terdapat di permukaan kulit bumi,
yang tersusun dari bahan-bahan mineral sebagai hasil pelapukan batuan, dan
bahan-bahan organik sebagai hasil pelapukan sisa-sisa tumbuhan dan hewan, yang
merupakan medium atau tempat tumbuhnya tanaman dengan sifat-sifat tertentu,
yang terjadi akibat dari pengaruh kombinasi faktor-faktor iklim, bahan induk,
jasad hidup, bentuk wilayah dan lamanya waktu pembentukan.
(Yulipriyanto,2010)
Tanah tersusun atas mineral primer dan mineral sekunder serta bahan
organik. Mineral primer berasal dari batuan beku yang secara kimia belum
mengalami perubahan. Ini merupakan bahan sumber mineral utama sekaligus
sumber bahan organik. Pembebasan unsur haranya untuk tanaman sangat lambat
karena tergatung pada proses pelapukan sehingga tidak cukup membantu bagi
tanaman. Sedangkan mineral sekunder dan bahan organik terutama yang koloida
menyusun fraksi tanah aktif. Secara umum tanah tersusun atas lima komponen
yaitu, partikel mineral yang merupakan hasil perombakan batuan dipermukaan
bumi dan ini merupakan bagian terbesar tanah, bahan organik yang berasal dari
sisa tanaman dan kotoran binatang serta bangkainya, air ,udara dan kehidupan
tanah yaitu tanah mineral, yang meliputi tanah yang kandungan bahan organiknya
anorganik dan lapukan bahan organik), fase gas (udara), dan fase cair (air tanah).
2.2.1. Tekstur Tanah
Tektur tanah adalah perbandingan kandungan partikel tanah primer berupa
fraksi liat, debu dan pasir dalam suatu masa tanah. Sifat fisik ini berorientasi pada
besarnya butir-butir mineral, terutama pada perbandingan relatif berbagai
golongan dari tanah tertentu. Fraksi pasir mempunyai diameter 0,2 - 0,02 mm,
fraksi debu 0,02 - 0,002 mm dan fraksi liat lebih kecil dari 0,002 mm.
2.2.2 Struktur Tanah
Struktur tanah adalah susunan butir-butir tanah primer dan agregat primer
tanah yang secara alami menjadi bentuk tertentu yang dibatasi oleh bidang-bidang
yang disebut agregat. Agregat adalah butiran tanah yang banyak terikat menjadi
satu masa tanah atau bongkah tanah tunggal seperti gumpal kersai, kubus atau
prisma. Struktur tanah dibentuk dengan penggabungan butir-butir primer tanah
Penggabungan agregat-agregat primer ini disusun lagi menjadi bentukan-bentukan
yang masing-masing dibatasi oleh permukaan tertentu. Agregat primer dengan
struktur mikro (0,25 – 0,50 mm) , sedangkan agregat sekunder yang merupakan
struktur pada tanah olah disebut struktur makro (0,50 – 10 mm).
2.3 Sifat kimia Tanah
Sifat kimia tanah yang perlu diketahui adalah koloid tanah, susunan kimia
unsur tanah, dan pH tanah.
2.3.1. Koloid Tanah
Koloid tanah adalah butir – butir individu yang ukuranya sangat halus, luas
permukaanya setiap kesatuan luas sangat besar, dan pada permukaanya terdapat
muatan- muatan yang dapat menarik ion- ion dan air. Di dalam tanah ada koloid
liat lempung dan koloid humus. Koloid ini berperan sebagai pusat kegiatan tanah
yang disekitarnya terjadi persenyawaan-persenyawaan kimia. Oleh sebab itu sifat
fisik dan kimia tanah dipengaruhi oleh lempung dan humus.
2.3.2. Susunan Kimia Tanah
Unsur hara dalam tanah yang tersedia bagi tanaman terdapat dalam dua
keadaan yaitu dalam bentuk garam-garam yang terlarut menjadi ion dalam larutan
tanah, dalam bentuk unsur terikat pada permukaan koloid kompleks liat dan
humus atau kompleks abrasi. Koloid liat permukaanya bermuatan negatif atau
anion atau beberapa kation terdapat dalam larutan tanah atau pada permukaan
koloid tanah. Ion-ion yang terdapat dalam larutan tanah atau pada permukaan
koloid tanah adalah karbon, hidrogen, nitrogen, fosfor, kalium, kalsium
2.3.3. pH Tanah
Serenson (1909) mendefenisikan pH sebagai negatif logaritma dari
konsentrasi ion hidrogen dengan rumus :
pH = -log aH+
di mana : aH+ = aktivitas ion hidrogen.
Nilai pH tanah tidak sekedar menunjukkan suatu tanah asam atau alkali,
tetapi juga memberikan informasi tentang sifat-sifat tanah yang lain seperti,
ketersediaan fosfor, status kation-kation basa, dan unsur racun. Kebanyakan
tanah-tanah pertanian memiliki pH 4 hingga 8. Tanah yang lebih asam biasanya
ditemukan pada jenis tanah gambut dan tanah yang tinggi kandungan aluminium
atau belerang. Sementara tanah yang basa ditemukan pada tanah yang tinggi kapur
dan tanah yang berada didaerah arid dan di kawasan pantai.
pH tanah merupakan suatu ukuran intensitas kemasaman, bukan ukuran
total asam yang ada di tanah tersebut. Pada tanah-tanah tertentu, seperti tanah liat
berat, gambut yang mampu menahan perubahan pH atau kemasaman yang lebih
besar dibandingkan dengan tanah yang berpasir. (Mukhlis,2007)
2.4 Penetapan Kapasitas Tukar Kation
Kapasitas tukar kation (KTK) merupakan ukuran kemampuan suatu koloid
untuk mengadsorbsi dan mempertukarkan kation. KTK ini dapat didefenisikan
sebagai ukuran kualitas kation, yang segera dapat dipertukarkan dan yang
menetralkan muatan negatif tanah. Jadi penetapan KTK merupakan pengukuran
Kapasitas tukar kation (KTK) dinyatakan dalam satuan miliequivalen per
100 g tanah (me/100 g) atau centimol per kg tanah (cmol(+)/kg). Satuan yang
terakhir digunakan secara resmi di internasional. Istilah 1 me adalah 1 mg atau H+
yang teradsorbsi atau dipertukarkan, atau jumlah lainnya yang dapat
menggantikan atom H+. Besarnya KTK tergantung kepada tekstur tanah, tipe
mineral liat, dan kandungan bahan organik . Semakin tinggi kadar liat atau tekstur
semakin halus maka KTK tanah akan semakin besar. Demikian juga pada
kandungan bahan organik tanah, semakin tinggi bahan organik maka KTK tanah
akan semakin tinggi. Jenis mineral liat sangat mempengaruhi KTK tanah, karena
besarnya KTK dan masing- masing mineral liat juga berbeda. Beberapa metode
pengukuran KTK yang sering dipakai adalah:
a. Jumlah kation yang dapat dipertukarkan (KTK -8,2)
b. Penjumlahan kompleks pertukaran denagn kation indeks (penggantian
setelah pencucian). Biasanya digunakan amonium dalam NH4OAC
netral sebagai kation indeks (KTK-7)
c. Penjumlahan basa yang dapat dipertukarkan ditambah dengan
aluminium yang dapat dipertukarkan dengan ekstrak KCL (KTK
Efektif)
KTK -8,2 merupakan KTK total tanah atau KTK dari muatan parmanen
dan variabel, sedangkan KTK -7 merupakan KTK dari muatan parmanen.
Sehingga KTK dari muatan variabel dapat diperoeh dengan mempengaruhi KTK
2.5 Kandungan Unsur Hara
Tanaman memerlukan sejumlah anasir hara dalam takaran cukup,
seimbang dan sinambung untuk terus tumbuh dan berkembang , menyelesaikan
daur hidupnya. Anasir hara tanaman ini diambil dari atmosfir dan sistem tanah.
Paling sedikit 13 macam anasir hara yang diperlukan secara teratur untuk
pertumbuhan vaskular tanaman. Takaran dan jenis anasir hara yang dibutuhkan
setiap jenis tanaman adalah berbeda. Anasir hara yang dibutuhkan dalam takaran
banyak disebut anasir hara makro yaitu : N, P, K, S, Ca, dan Mg, sedangkan yang
dibutuhkan dalam takaran sedikit disebut anasir hara mikro yaitu : Mn, Fe, B, Zn,
Cu, Mo, dan Cl. (Poerwowidodo,2010)
Timbal (Pb)
Timbal (Pb) merupakan logam berat golongan IV-A dengan nomor atom
82 ,massa atom 207,2 dan massa jenis 11,34. Logam ini sangat populer dan
banyak dikenal disebabkan banyaknya timbal yang digunakan dipabrik dan paling
banyak menimbulkan keracunan pada makhluk hidup. Sifat-sifat dan kegunaan
logam ini adalah:
1.Mempunyai titik lebur yang rendah sehingga mudah digunakan dan
murah biaya operainya
2.Mudah dibentuk karena logam ini lunak
3.Mempunyai sifat kimia yang aktif sehingga dapat digunakan untuk
4.Bila dicampur dengan logam lain membentuk logam campuran ang lebih
bagus dari pada logam murninya
5.Kepadatannya melebihi logam lain
Timbal adalah sejenis logam yang lunak dan berwarna coklat kehitaman,
serta mudah dimurnikan dari pertambangan. Dalam pertambangan, logam ini
membentuk sulfida logam (PbS) yang sering disebut gelena. Bahaya yang
ditimbulkan oleh penggunaan timah hitam ini adalah sering menyebabkan
keracunan. Pencemaran logam berat dapat terjadi pada daerah lingkungan yang
bermacam-macam dan ini dapat dibagi tiga golongan, yaitu udara, tanah dan air.
Pencemaran udara oleh logam berat sangat erat hubunganya dengan sifat-sifat
logam itu sendiri, sedangkan pencemaran tanah atau air erat hubungannya dengan
penggunaan logam itu sendiri. Pencemaran tanah dan air biasanya terjadi karena
pembuangan limbah dari industri penggunaan logam yang bersangkutan secara
tidak terkontrol (pabrik aki/baterai) atau penggunaan bahan yang mengandung
logam itu sendiri (pestisida,insektisida)
2.6 Keracunan Timbal (Pb)
Keracunan logam paling sering disebabkan pengaruh pencemaran
lingkungan oleh logam berat, seperti penggunaan logam sebagai pembasmi hama
(pestisida), pemupukan maupun karena pembuangan limbah pabrik yang
Keracunan timbal dalam bentuk larutan diabsorpsi sekitar 1-10% melalui
dinding saluran pencernaan. Sistem darah porta hepatis( dalam hati) membawa
timbal tersebut dan dideposisi dan sebagian lagi dibawa darah dan didistribusikan
kedalam jaringan. Timbal kemudian diekskresikan melalui urine dan feses.
Kebanyakan ekskresi terjadi melalui cairan empedu kedalam intestinum dan ginjal
melalui dinding intestinum dan ginjal melalui air susu, keringat, dan rambut.
Timbal mungkin berpengaruh negatif pada semua organ yaitu dengan
mengganggu enzim oksidase sebagai akibatnya menghambat sistem metabolisme
sel, salah satu diantaranya adalah menghambat sistem Hb dalam sumsum tulang.
Timbal menghambat enzim sulfidril untuk mengikat delta-aminolevulinik asid
(ALA) menjadi porpobilinogen, serta protoforfirin-9 menjadi Hb. Hal ini
menyebabkan anemia dan adanya besofilik stipling dari eritrosit yang merupakan
ciri khas dari keracunan Pb. Baofilik stipling terjadi karena retensi dari DNA
ribosoma dalam sitoplasma eritrosit sehingga mengganggu sintesis protein.
(Darmong,1995)
2.7 Spektrofotometer Serapan Atom (SSA)
2.7.1 Prinsip dasar analisa SSA
Peristiwa serapan atom ini pertama kali diamati oleh fraunhofer, ketika
mengamati garis-garis hitam pada spektrum matahari. Spektroskopi serapan atom
pertama kali digunakan pada tahun 1995 oleh walsh. Spektroskopi serapan atom
digunakan untuk analisis kuantitatif unsur-unsur logam. Spektroskopi serapan
yang diserap biasanya sinar tampak atau ultraviolet. Dalam garis besarnya prinsip
spekroskopi serapan atom sama dengan spektrofotometri sinar tampak dan
ultraviolet . Perbedaannya terletak pada bentuk spektrum, cara pengerjaan sampel
dan peralatannya.
Metode spektrofotometer serapan atom (SSA) mendasarkan pada prinsip
absorbsi cahaya oleh atom. Atom-atom akan menyerap cahaya pada panjang
gelombang tertentu, tergantung pada sifat unsurnya. Sebagai contoh, natrium
menyerap pada 589 nm, uranium pada 358,5 nm, sementara kalium menyerap
pada panjang gelombang 766,5 nm. Cahaya pada panjang gelombang ini
mempunyai cukup energi untuk mengubah tingkat elektronik suatu atom yang
mana transisi elektronik suatu atom bersifat spesifik. Dengan menyerap suatu
energi maka atom akan memperoleh energi sehingga suatu atom pada keadaan
dasar dapat ditingkatkan energinya ke tingkat eksitasi. Misalkan, suatu unsur Na
mempunyai konfigurasi elektron 1s2,2s2,2p6,dan 3s1. Tingkat dasar untuk elektron
valensi 3s1 ini dapat mengalami eksitasi ketingkat 3p dengan energi 2,2 e.V atau
ketingkat 4p dengan energi 3,6 e.V yang masing –masing bersesuaian dengan
panjang gelombang 589,3 nm dan 330,2 nm.
2.7.2. Sketsa intrumentasi SSA
a c d
Keterangan :
Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau dilapisi
dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon dan argon)
dengan tekanan rendah (10-15 torr). Neon biasanya lebih disukai karena
memberikan intensitas pancaran lampu yang lebih rendah. Bila antara anoda dan
katoda diberi suatu tegangan yang tinggi (600 volt), maka katoda akan
memancarkan berkas-berkas elektron yang bergerak menuju anoda yang mana
kecepatan dan energinya sangat tinggi. Elektron-elektron dengan energi tinggi ini
dalam perjalanannya menuju anoda akan bertabrakan dengan gas-gas mulia yang
diisikan tadi.
B.Tempat Sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang akan
asas. Alat yang digunakan untuk mengubah suatu sampel menjadi uap atom -
atom yaitu : dengan nyala (flame) dan dengan tanpa nyala (flameless).
1. Nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan
menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Pada cara
spektrofotometri emisi atom, nyala ini berfungsi untuk mengeksitasikan atom dari
tingkat dasar ketingkat yang lebih tinggi. Suhu yang dicapai nyala tergantung
pada gas – gas yang digunakan, misalkan untuk gas batubara-udara , suhunya
kira-kira sebesar 18000C , gas alam-udara suhunya 17000C, asetilen-udara
suhunya 22000C, dan gas asetilen-dinitrogen oksida (N2O) sesar 30000C.
Sumber nyala yang paling banyak digunakan adalah campuran asetilen
sebagai bahan pembakar dan udara sebagai pengoksidasi. Propana-udara dipilih
untuk logam-logam alkali karena suhu nyala yang lebih rendah akan mengurangi
banyaknya ionisasi. Nyala hidrogen-udara lebih jernih dari pada nyala asetilen –
udara dalam daerah UV (dibawah 220 nm), dan juga karena sifatnya yang
mereduksi maka nyala ini sesuai untuk penetapan arsenik dan selenium.
2. Tanpa Nyala (flameless)
Teknik atomisasi dengan nyala dinilai kurang peka karena atom gagal
mencapai nyala, tetesan sampel yang masuk kedalam nyala terlalu besar, dan
proses atomisasi kurang sempurna, oleh karena itu muncullah suatu teknik
atomisasi yang baru yakni atomisasi tanpa nyala. Pengatoman dapat dilakukan
dalam tungku dari grafit seperti tungku yang dikembangkan oleh masmann.
Sistem pemanasan dengan tanpa nyala ini dapat melalui 3 tahap yaitu ;
(ashing) yang membutuhkan suhu yang lebih tinggi karena untuk menghilangkan
matriks kimia dengan mekanisme volatilasi atau pirolisis, dan pengatoman
(atomising).
C.Monokomator
Monokomator digunakan untuk memisahkan dan memilih panjang
gelombang yang digunakan dalam analisis. Disamping sistem optik, dalam
monokromator juga terdapat suatu alat yang digunakan untuk memisahkan radiasi
resonansi dan kontinyu yang disebut dengan chopper
D.Detektor
Detetor digunakan untuk mengukur intensitas cahaya yang melalui tempat
pengatoman. Biasanya digunakan tabung penggandaan foton. Ada2 cara yang
dapat digunakan dalam sistem deteksi yaitu : (a) yang memberikan respon
terhadap radiasi kontinyu, dan (b) yang hanya memberikan respon terhadap
radiasi resonansi.
Pada cara pertama, output yang dihasilkan dari radiasi resonan dan radiasi
kontinyu disalurkan pada sistem galvanometer dan setiap perubahan yang
disebabkan oleh radiasi resonan akan menyebabkan perubahan output. Pada cara
kedua , output berasal dari radiasi resonan dan radiasi kontinyu yang dipisahkan.
Dalam hal ini sistem penguat harus cukup selektif untuk dapat membedakan
radiasi. Cara tebaik adalah dengan menggunakan detektor yang hanya peka
terhadap radiasi resonan yang termodulasi.
5. Rekorder
Rekorder merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
terkalibrasi untuk pembacaan dapat berupa angka atau berupa kurva dari suatu
BAB I
PENDAHULUAN
1.1Latar Belakang
Logam berat adalah unsur-unsur yang memiliki kerapatan lebih dari 6
mg/m2. Logam berat juga didefenisikan sebagai logam yang memiliki berat atom
lebih besar dari 23 dan kerapatan lebih dari 5. Hingga saat ini logam berat hanya
didefenisikan atas dasar kerapatannya. Logam berat tidak terdegradasi, tetap stabil
di alam dalam waktu yang cukup lama dan bersifat meracun untuk organisme
hidup walaupun pada konsentrasi yang rendah. Sebagai contoh, waktu tinggal Cd
dalam tanah 75-380 tahun, Hg 500-1000 tahun dan untuk logam berat seperti Pb,
As, Ni, dan Zn memiliki waktu tinggal 1000-3000 tahun. Jadi polusi logam berat
dalam tanah memberikan pengaruh yang cukup lama. Saat ini mulai ada
peningkatan perhatian tentang keberadaan unsur mikro di lingkungan dalam
konsentrasi yang membahayakan kesehatan hewan. Banyak pupuk, terutama
pupuk P yang mengandung sejumlah unsur mikro seperti Pb, Hg, Ni, Cd, Co, Cr,
As, Mo, dan F.
Sumber antropogenik unsur mikro antara lain adalah industri peleburan
besi, limbah industri, lumpur buangan, limbah padat kota, pembakaran bahan
bakar fosil, air hujan dan lain sebagainya. Sumber antropogenik Pb dn As adalah
pembakaran bensin yang mengandung Pb dan penyemprotan pestisida yang
mengandung arsen. Pembakaran bensin yang ditambahkan timbal (Pb) merupakan
cukup tinggi. Pengamatan pada periode 1966-1988, ternyata terjadi penurunan
kandungan Pb dari atmosfir yang berasal dari bensin 1,7 g/ha/thn. Hal ini terjadi
karena mulai adanya kesadaran akan bahaya pencemaran udara terutama oleh Pb
sehingga penggunaan bensin yang bebas timbal mulai digalakkan. Untuk dapat
memastikan suatu tanah telah terkontaminasi oleh suatu logam harus ada suatu
acuan tentang kandungan logam dalam tanah yang dapat dianggap telah
terkontaminasi. Sayangnya tidak ada pedoman yang benar-benar pasti sebagai
antisipasi konsentrasi unsur mikro tanah yang secara alamiah variasinya sangat
tinggi. Sebuah hasil penelitian melaporkan bahwa kisaran normal dari As : <5-40,
Cd : <1-2, Cu : 2-60, Mo : <1-5, Ni : 2-100, Pb : 10-150, Se : <1-2 , dan Zn :
25-200 ppm. Disamping itu peneliti lainnya memperkirakan batas dasar jumlah total
Zn : 50, Cu : 20, Cd : 0,06 dan Pb : 10 ppm. (Sarifuddin, 2011)
Analisa kadar logam timbal (Pb) yang dipaparkan pada karya tulis ini
merupakan salah satu logam berat beracun yang menyebabkan kerusakan pada
tanah khususnya untuk tanah tanaman. Bagaimana cara menganalisa logam Pb,
dan apa saja akibat yang ditimbulkannya jika melebihi ambang batas yang telah
1.2Permasalahan
Tanah merupakan medium atau tempat tumbuhnya suatu tanaman untuk
dapat hidup. Apabila kadar unsur hara timbal (Pb) mengandung konsentrasi yang
tinggi akan mengakibatkan kerusakan pada tanaman.
1.3. Tujuan
- untuk mengetahui metode analisis yang dipergunakan untuk menentukan kadar
logam timbal (Pb) pada tanah
- untuk mengetahui apakah logam timbal (Pb) terdapat di dalam tanah
- untuk mengetahui kadar logam timbal (Pb) yang terkandung pada tanah
1.4 Manfaat
Manfaat dari pembuatan karya ilmiah ini adalah untuk memberikan
informasi bagaimana cara menganalisa kadar unsur timbal (Pb) pada tanah secara
laboratorium. Dan dengan mengetahui kadar timbal (Pb) dapat diketahui apakah
ANALISA KADAR TIMBAL (Pb) DALAM TANAH YANG
BERASAL DARI TANAH KARO SECARA
SPEKTROFOTOMETER SERAPAN ATOM (SSA)
ABSTRAK
Telah dilakukan analisa penentuan kadar logam timbal (Pb) didalam tanah, contoh tanah yang diambil dari tanah karo.
Penentuan kadar timbal (Pb) dilakukan dengan metode Spektrofotometer Serapan
Atom (SSA) dengan panjang gelombang = 271 nm, hasil yang diperoleh
DETERMINATION RATE OF RECIPROCAL (Pb) IN
SOIL DERIVED FROM KARO LAND IN ATOMIC
ABSORPTION SPECTROFOTOMETRI (AAS)
ABSTRACT
Have pervormed the analysis of lead metal (Pb) content determination in soil, soil samples taken from the soil karo.
Determining lead levels (Pb) conducted by the method atomic absorbtion
spectrofotometri wavelength = 271 nm, the results obtained indicate that lead
ANALISA KADAR TIMBAL (Pb) DALAM TANAH YANG
BERASAL DARI TANAH KARO SECARA
SPEKTROFOTOMETER SERAPAN ATOM (SSA)
TUGAS AKHIR
LESTARI YANTI SIMANUNGKALIT
122401067
PROGRAM STUDI D-3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
ANALISA KADAR TIMBAL (Pb) DALAM TANAH YANG
BERASAL DARI TANAH KARO SECARA
SPEKTROFOTOMETER SERAPAN ATOM (SSA)
Diajukan untuk melengkapi tugas akhir dan memenuhi syarat mencapai gelar Ahli Madya
Oleh:
LESTARI YANTI SIMANUNGKALIT
122401067
PROGRAM STUDI D-3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN
Judul : Analisa Kadar Timbal (Pb) Dalam Tanah Yang Berasal dari Tanah Karo Secara Spekrofotometer Serapan Atom (SSA)
Kategori : Tugas Akhir
Nama : Lestari Yanti Simanungkalit
Nomor Induk Mahasiswa : 122401067
Program studi : Diploma Tiga (D-3) Kimia
Departemen : Kimia
PERNYATAAN
ANALISA KADAR TIMBAL (Pb) DALAM TANAH YANG
BERASAL DARI TANAH KARO SECARA
SPEKTROFOTOMETER SERAPAN ATOM (SSA)
TUGAS AKHIR
Saya mengakui bahwa tugas akhir ini adalah hasil karya saya sendiri. Kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2015
PENGHARGAAN
Puji dan syukur penulis sampaikan kehadirat Tuha Yang Esa atas segala rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan penyusunan tugas akhir ini tepat pada waktunya dengan judul Analisa Kadar Timbal (Pb) Dalam Tanah Yang Berasal dari Tanah Karo Secara Spektfotometer Serapan Atom (SSA) .
Tugas akhir ini disusun sebagai persyaratan untuk menyelesaikan pendidikan Program Studi D-3 Kimia, Departemen Kimia, Fakultas Matematika Dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara. Dalam penyusunan tugas akhir ini penulis banyak menemukan kendala. Namun berkat bantuan, bimbingan dan dukungan dari berbagai pihak, akhirnya penulis dapat mengatasi berbagai kendala tersebut dengan baik.
Maka pada kesempatan ini dengan segala ketulusan dan kerendahan hati, penulis mengucapkan terima kasih kepada :
1. Kedua orang tua tercinta, Ayahanda Maradong Simanugkalit dan Ibunda Ermawani Siregar serta saudara penulis tersayang, Abang Charles Abbet Simanugkalit dan Adik-adik saya ( Richardo,Denni,Yunus,dan Aril ) yang telah memberikan bantuan moril dan materil serta doa restu demi kesuksesan penulis.
2. Bapak Dr. Sutarman, M.Sc selaku Dekan FMIPA USU.
3. Ibu Dr. Rumondang Bulan, MS selaku Ketua Departemen Kimia FMIPA USU.
4. Ibu Dra. Emma Zaidar Nst, M.Si selaku Ketua Program Studi D-3 Kimia FMIPA USU.
5. Ibu Dr. Minto Supeno, M.S selaku Dosen Pembimbing yang telah bersedia meluangkan waktu, tenaga, dan pikiran dalam membantu penulisan tugas akhir ini.
7. Bapak Miftah Elfahmi,S.TP. selaku Manager Teknis Di Laboratorium Analisa Pestisida di Balai Besar Perbenihan dan Proteksi Tanaman Perkebunan (BBPTP) Medan yang telah memberikan pengarahan dan membimbing penulis selama pelaksanaan PKL.
8. Bapak Fahri Riswal ,S.Si, Kakak Eva Yanti Manihuruk, ST, Kakak Nur Indah, S.Si, Kakak Elviani Sinaga, S.TP, Kakak Kartinatra P, A.md, Ibu Hasanah yang telah mengajari dan membimbing penulis selama pelaksanaan PKL.
9. Bapak Ir. Henry H.M Pardede selaku seksi jaringan Labortorium , Bapak Kusharyanto, S.Si,MP selaku kepala sub bagian tata usaha yang telah memberikan izin penulis melakukan kegiatan PKL di Balai Besar Perbenihan dan Proteksi Tanaman Perkebunan (BBPPTP) Medan.
10.Seluruh staff dan karyawan Balai Besar Perbenihan dan Proteksi Tanaman Perkebunan (BBPPTP) Medan yang telah memberikan dukungan, semangat dan ilmu baru kepada penulis.
11.Teman-teman seperjuangan D-3 Kimia stambuk 2012 dan seluruh pihak yang tidak dapt penulis sebutkan satu persatu yang turut adil dalam membantu penulis sehingga selesainya tugas akhir ini.
ANALISA KADAR TIMBAL (Pb) DALAM TANAH YANG
BERASAL DARI TANAH KARO SECARA
SPEKTROFOTOMETER SERAPAN ATOM (SSA)
ABSTRAK
Telah dilakukan analisa penentuan kadar logam timbal (Pb) didalam tanah, contoh tanah yang diambil dari tanah karo.
Penentuan kadar timbal (Pb) dilakukan dengan metode Spektrofotometer Serapan
Atom (SSA) dengan panjang gelombang = 271 nm, hasil yang diperoleh
DETERMINATION RATE OF RECIPROCAL (Pb) IN
SOIL DERIVED FROM KARO LAND IN ATOMIC
ABSORPTION SPECTROFOTOMETRI (AAS)
ABSTRACT
Have pervormed the analysis of lead metal (Pb) content determination in soil, soil samples taken from the soil karo.
Determining lead levels (Pb) conducted by the method atomic absorbtion
spectrofotometri wavelength = 271 nm, the results obtained indicate that lead
4.1. Data Percobaan 23 4.2. Perhitungan 24
4.2.1. Perhitungan Konsentrasi Sampel 25
4.3. Pembahasan 26
BAB V. KESIMPULAN DAN SARAN
5.1. Kesimpulan 30 5.2. Saran 30
DAFTAR TABEL
Halaman