STUDI SINTESIS MONOGLISERIDA MELALUI REAKSI ANTARA
GLISEROL KARBONAT
(4-HIDROKSIMETIL-1,3-DIOKSOLAN-2-ON) DENGAN PALM FATTY ACID DISTILLATE (PFAD)
MENGGUNAKAN KATALIS TRIETILAMIN (TEA)
SKRIPSI
MARIATI SIBUEA
050802054
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
STUDI SINTESIS MONOGLISERIDA MELALUI REAKSI ANTARA
GLISEROL KARBONAT
(4-HIDROKSIMETIL-1,3-DIOKSOLAN-2-ON) DENGAN PALM FATTY ACID DISTILLATE (PFAD)
MENGGUNAKAN KATALIS TRIETILAMIN (TEA)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana sains
MARIATI SIBUEA
050802054
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : STUDI SINTESIS MONOGLISERIDA MELALUI
REAKSI ANTARA GLISEROL KARBONAT (4-HIDROKSIMETIL-1,3-DIOKSOLAN-2-ON) DENGAN PALM FATTY ACID DISTILLATE (PFAD) MENGGUNAKAN KATALIS TRIETILAMIN (TEA)
Kategori : SKRIPSI
Nama : MARIATI SIBUEA
Nomor Induk Mahasiswa : 050802054
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
PERNYATAAN
STUDI SINTESIS MONOGLISERIDA MELALUI REAKSI ANTARA GLISEROL KARBONAT (4-HIDROKSIMETIL-1,3-DIOKSOLAN-2-ON) DENGAN PALM FATTY ACID DISTILLATE (PFAD) MENGGUNAKAN KATALIS TRIETILAMIN
(TEA)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasn yang masing-masing disebutkan sumbernya.
Medan, September 2010
PENGHARGAAN
Segala puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Kuasa, yang sudah memberikan kasih dan karunia-Nya bagi penulis sehingga dapat menyelesaikan penelitian dan penyusunan skripsi ini guna melengkapi syarat dalam memperoleh gelar sarjana kimia di FMIPA USU Medan.
Keberhasilan dalam menyelesaikan penelitian dan penyusunan skripsi ini juga tidak luput dari perhatian dan bantuan dari berbagai pihak. Dalam kesempatan ini, penulis dengan segala kerendahan hati mengucapkan terima kasih yang sebesar – besarnya kepada :
1. Ibu Juliati Tarigan, SSi, MSi selaku Dosen Pembimbing I dan Ibu Cut Fatimah Zuhra, SSI, MSi Dosen Pembimbing II yang telah meluangkan waktu dalam memberikan pemikiran, pengarahan, petunjuk, serta saran kepada penulis dari awal hingga akhir penelitian dan penyusunan skripsi ini.
2. Bapak Drs Adil Ginting, MSc selaku Kepala Laboratorium Kimia Organik serta para stafnya atas fasilitas yang telah diberikan kepada penulis selama melakukan penelitian sampai tersusunnya skripsi ini.
3. Ibu DR. Rumondang Bulan, MS selaku Ketua Departemen Kimia dan Bapak Drs. Firman Sebayang, MS selaku Sekretaris Departemen Kimia FMIPA USU yang turut memberikan pengarahan dan mengesahkan skripsi ini
4. Bapak dan Ibu Staf Dosen jurusan Kimia FMIPA USU yang telah mendidik selama penulis dalam masa perkuliahan. Khususnya kepada Drs.Minto Supeno, MS sebagai dosen wali Penulis yang selalu mendukung perkuliahan penulis. 5. Rekan – rekan kuliah dan asisten laboratorium Kimia Organik serta semua
angkatan 05 dan yang tidak dapat saya tuliskan yang telah membantu dan memberikan perhatiannya kepada penulis selama penelitian dan pengerjaan skripsi ini.
Akhirnya penulis mengucapkan rasa terima kasih yang sedalam – dalamnya kepada kedua orang tuaku, Ayahanda tercinta J.P Sibuea dan Ibunda R.Matondang serta kakak-kakak saya Maria Yohana Sibuea, Mariani Sibuea, Mariana Sibuea, dan Mariance Sibuea serta adik saya Maria Magdalena Sibuea yang telah memberikan doa, semangat serta dorongan baik secara materi maupun moril sehingga penulis dapat menyelesaikan perkuliahan, penelitian dan penyusunan skripsi ini. Penulis menyadari sepenuhnya bahwa skripsi ini masih jauh dari sempurna, oleh karena itu penulis mengharapkan saran – saran dan kritik yang membangun dari berbagai pihak agar skripsi ini dapat bermanfaat bagi kita semua.
Medan, September 2010 Penulis
ABSTRAK
Sintesis monogliserida dilakukan melalui reaksi antara gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2-on) dengan Palm Fatty Acid Distillate (PFAD) menggunakan katalis trietilamin (TEA). Gliserol karbonat (4-hidroksimetil-1,3dioksolan-2-on) disintesis melalui reaksi antara gliserol dengan dimetil karbonat menggunakan katalis K2CO3 pada
suhu 73 – 750C selama 3 jam. Hasil yang diperoleh berupa cairan kental berwarna kuning pucat sebanyak 12,012 gram (93,65%) dan dianalisis dengan spektrofotometer FT-IR dan
1
THE STUDY OF MONOGLYCERIDE SYNTHESIS BY REACTION BETWEEN GLYCEROL CARBONATE (4-HYDROXYMETHYL-1,3-DIOXOLAN-2-ON) WITH PALM FATTY ACID DISTILLATE (PFAD) USING TRIETHYLAMINE
(TEA) AS A CATALYST
ABSTRACT
The synthesis of monoglyceride by reaction of glycerol carbonate (4-hydroxymethyl-1 ,3-dioxolan-2-on) with Palm Fatty Acid Distillate (PFAD) using triethylamine (TEA) as a catalyst. Glycerol carbonate (4-hydroxymethyl-1,3-dioxolan-2-on) is synthesized by reaction of glycerol with dimethyl carbonate using K2CO3 as a catalyst at a temperature of
DAFTAR ISI
2.4 Monogliserida dan Digliserida 9
2.5 Trigliserida 10
2.6 Gliserol 11
2.7 Organik Karbonat 11
2.8 Metode Pembuatan Dimetil Karbonat 12
2.9 Gliserol Karbonat 14
Bab 3 Bahan dan Metode Penelitian
3.1 Alat-alat 17
3.2 Bahan-bahan 18
3.3 Prosedur Penelitian
3.3.1 Pembuatan Gliserol Karbonat 18
3.3.2 Sintesis Monogliserida dari PFAD 19
3.4 Bagan Penelitian
3.4.1 Pembuatan Gliserol Karbonat 20
Bab 4 Hasil dan Pembahasan
4.1 Hasil Penelitian 22
4.2 Pembahasan 23
Bab 5 Kesimpulan dan Saran
5.1 Kesimpulan 32
5.2 Saran 32
Daftar Pustaka 33
DAFTAR TABEL
Halaman
Tabel 2.1 Diagram Alur Oleokimia 7
Tabel 4.1 Komposisi Asam Lemak pada PFAD 23
DAFTAR GAMBAR
Halaman Gambar 4.1. Spektrum FT-IR Senyawa Gliserol Karbonat 24
Gambar 4.2. Spektrum 1H-NMR Senyawa Karbonat 25
Gambar 4.3. Kromatogram GC Komposisi Asam Lemak PFAD 27
Gambar 4.4. Spektrum FT-IR Senyawa Monogliserida 30
Gambar 4.5. Kromatogram GC Monogliserida Hasil Sintesis 31
DAFTAR LAMPIRAN
Halaman Lampiran 1. Spektrum FT–IR Senyawa Gliserol Sebagai Pembanding 34 Lampiran 2. Kromatogram GC Komposisi Asam Lemak PFAD 35 Lampiran 3. Kromatogram GC Monogliserida Hasil Sintesis 37
ABSTRAK
Sintesis monogliserida dilakukan melalui reaksi antara gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2-on) dengan Palm Fatty Acid Distillate (PFAD) menggunakan katalis trietilamin (TEA). Gliserol karbonat (4-hidroksimetil-1,3dioksolan-2-on) disintesis melalui reaksi antara gliserol dengan dimetil karbonat menggunakan katalis K2CO3 pada
suhu 73 – 750C selama 3 jam. Hasil yang diperoleh berupa cairan kental berwarna kuning pucat sebanyak 12,012 gram (93,65%) dan dianalisis dengan spektrofotometer FT-IR dan
1
THE STUDY OF MONOGLYCERIDE SYNTHESIS BY REACTION BETWEEN GLYCEROL CARBONATE (4-HYDROXYMETHYL-1,3-DIOXOLAN-2-ON) WITH PALM FATTY ACID DISTILLATE (PFAD) USING TRIETHYLAMINE
(TEA) AS A CATALYST
ABSTRACT
The synthesis of monoglyceride by reaction of glycerol carbonate (4-hydroxymethyl-1 ,3-dioxolan-2-on) with Palm Fatty Acid Distillate (PFAD) using triethylamine (TEA) as a catalyst. Glycerol carbonate (4-hydroxymethyl-1,3-dioxolan-2-on) is synthesized by reaction of glycerol with dimethyl carbonate using K2CO3 as a catalyst at a temperature of
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Monogliserida dan digliserida telah diproduksi sejak tahun 1980-an untuk skala
industri dengan metode gliserolisis trigliserida. Akhir - akhir ini, monogliserida dan
digliserida telah diproduksi dengan mereaksikan suatu substrat dengan gliserol, dimana
substratnya dapat berupa asam lemak, trigliserida, ataupun metil ester asam lemak.
Monogliserida dan digliserida diperoleh melalui reaksi esterifikasi langsung asam lemak
dengan gliserol, transesterifikasi trigliserida atau metil ester asam lemak dengan gliserol,
dan kondensasi asam lemak dengan glisidol atau turunannya ( Awang, 2004 ).
Bila dibuat dengan cara reaksi gliserolisis secara transesterifikasi maka proses
yang berlangsung harus pada suhu yang tinggi ( 2100 – 2600 C) dan menggunakan katalis anorganik seperti natrium, kalium, atau kalsium hidroksida ( Noureddini, 1997 ). Hal ini
disebabkan karena sifat dari gliserol yang pada suhu kamar sulit larut pada lemak atau
minyak (hanya sekitar 4%). Dengan menggunakan suhu tinggi maka akan meningkatkan
kelarutan gliserol hingga mencapai 40 – 45% ( Sonntag, 1982 ).
Esterifikasi secara langsung dari gliserol dengan asam lemak menggunakan katalis
homogen maupun heterogen akan menghasilkan produk yang berupa campuran dari
mono-, di-, dan trigliserida. Senyawa ester gliserol merupakan kelompok terbanyak dari
ester asam lemak yang sangat komersil. Dikarenakan adanya spesifikasi bagian yang
berupa hidrofilik dan hidrofobik pada strukturnya, maka dapat berperan sebagai surfaktan
non-ionik dengan harga HLB yang rendah sehingga sangat bermanfaat sebagai zat
Gliserol karbonat dapat digunakan sebagai zat antara dalam proses sintesis
monogliserida.Telah banyak jenis metode yang telah dilaporkan untuk pembuatan gliserol
karbonat seperti reaksi antara gliserol dan phosgen, siklisasi dari 1,2-dihidroksipropil
karbamat, gliserol dan CO2, transesterifikasi antara gliserol dan etilen karbonat atau
dimetil karbonat dan penggunaan urea untuk konversi gliserol menjadi turunan karbonat.
Hanya proses dua terakhir yang memiliki teknikal dan harga ekonomis yang dapat dikerjakan dengan mudah untuk skala industri dan laboratorium. Bila menggunakan
dimetil karbonat, maka hasil gliserol karbonat yang terbentuk dapat mencapai 97 % dan
memiliki sifat yang ramah lingkungan (Ghandi, 2007).
Untuk mensintesis monogliserida dari asam lemak dapat juga dilakukan melalui
reaksi antara gliserol karbonat dan asam lemak tunggal. Dimana pada kondisi ini
temperatur yang digunakan lebih rendah yakni 1430 – 1450C sehingga reaksi dapat berlangsung secara regiospesifik ( Ghandi, 2007 ).
Selain dengan cara tersebut ada pula cara lain untuk mensintesis monogliserida
yaitu dengan mereaksikan asam lemak dengan glisidol serta asam lemak dengan gliserol
asetonida. Bila mereaksikan dengan glisidol, hasil monogliserida yang diperoleh sangat
murni. Hanya saja glisidol merupakan suatu prekursor yang tidak stabil dan dapat
menimbulkan penyakit kanker pada manusia serta harganya mahal, sehingga cara ini
tidak efektif untuk dilakukan. Bila dilakukan dengan mereaksikan asam lemak dan
gliserol asetonida maka hasil monogliserida yang diperoleh cukup besar yaitu 66,8%.
Namun cara ini sulit dilakukan karena harus melibatkan proses hidrolitik pada zat antara
ester-ketal ( Ghandi, 2007 ).
Palm Fatty Acid Distillate (PFAD) memiliki tingkat kandungan FFA (Free Fatty Acid) yang sangat tinggi yaitu 93% (45,6% asam palmitat; 33,3% asam oleat; 7,7% asam linoleat; 3,8% asam stearat; 1,0% asam miristat; 0,6% tetrakosenoat; 0,3% asam
linolenat; 0,3% ekosanoat; 0,2% ekosenoat; dan 0,2% asam palmitoleat). PFAD sangat
Dalam pemanfaatannya, PFAD hanya digunakan sebagai sabun batangan saja sehingga
perlu ditingkatkan lagi nilai ekonomisnya.
Berdasarkan hal tersebut maka ingin disintesis monogliserida campuran melalui
reaksi antara gliserol karbonat dengan Palm Fatty Acid Distillate ( PFAD ) menggunakan
katalis trietilamin ( TEA ). Gliserol karbonat diperoleh melalui reaksi antara gliserol dengan dimetil karbonat menggunakan katalis K2CO3. Hasil yang diperoleh dianalisis
dengan spektrofometer FT – IR, 1H-NMR, dan kromatografi gas (GC).
1.2 Permasalahan
Apakah senyawa gliserol karbonat dapat disintesis melalui reaksi antara gliserol
dengan dimetil karbonat menggunakan katalis K2CO3.
Apakah senyawa monogliserida dapat disintesis secara regiospesifik melalui
reaksi antara Palm Fatty Acid Distillate (PFAD) dengan gliserol karbonat menggunakan
katalis trietilamin ( TEA ) dalam kondisi nitrogen.
1.3 Tujuan Penelitian
Untuk mensintesis senyawa gliserol karbonat melalui reaksi antara gliserol dengan
dimetil karbonat menggunakan katalis K2CO3.
Untuk mensintesis senyawa monogliserida secara regiospesifik melalui reaksi antara Palm Fatty Acid Distillate (PFAD) dengan gliserol karbonat menggunakan katalis
1.4 Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi ilmiah terhadap perkembangan
ilmu kimia khususnya dalam bidang oleokimia dan sintesis kimia organik. Demikian juga
dalam hal pemanfaatan asam lemak bebas yang merupakan produk samping pada
pengolahan minyak kelapa sawit
1.5 Lokasi Penelitian
Penelitian ini dilakukan di laboratorium kimia organik F-MIPA USU. Analisis secara
spektrofotometer FT-IR di laboratorium UGM, 1H-NMR di laboratorium Farmasi UNAIR, dan GC di perusahaan swasta yang bergerak dalam industri minyak nabati di
Medan.
1.6 Metodologi Penelitian
Penelitian ini dilakukan untuk mensintesis monogliserida melalui reaksi antara gliserol
karbonat (4-hidroksimetil-1,3-dioksolan-2-om) dengan Palm Fatty Acid Distillate
(PFAD) menggunakan katalis trietilamin (TEA). Gliserol karbonat disintesis melalui
reaksi antara gliserol dengan dimetil karbonat menggunakan katalis K2CO3. Direfluks
pada suhu 73 – 750C selama 3 jam, dimana dilakukan uji KLT setiap 1 jam. Hasil reaksi
didestilasi dengan tekanan 0,5 cmHg pada suhu 400C. Residu yang diperoleh disaring dengan menggunakan resin penukar kation Amberlit IR-120 dan filtrat yang diperoleh
dianalisis dengan spektrofotometer FT-IR dan 1H-NMR. Sintesis monogliserida melalui reaksi antara gliserol karbonat dengan PFAD menggunakan katalis trietilamin (TEA)
yang direfluks pada suhu 115 – 1200C selama 10 jam, dimana dilakukan uji KLT setiap 1 jam. Ditambahkan petroleum eter hingga terbentuk 2 lapisan dan lapisan atas didekantasi.
pada temperatur kamar. Hasil yang diperoleh dianalisis dengan spektrofotometer FT-IR
BAB 2
TINJAUAN PUSTAKA
2.1 Oleokimia
Oleokimia merupakan suatu bagian ilmu kimia yang mempelajari tentang proses
pengolahan asam lemak dan gliserol serta turunannya, baik yang diperoleh dari minyak
atau lemak maupun hasil sintesis dari produksi etilena dan propilena secara industri
petrokimia.
Bahan dasar oleokimia diproduksi dari reaksi pemecahan atau pemisahan dan
reaksi lebih lanjut dari minyak atau lemak yaitu: asam lemak, gliserol, metil ester asam
lemak, alkohol asam lemak, dan amina. Dua bahan dasar terakhir merupakan bahan dasar
yang utama karena memegang peranan penting dalam pembuatan turunannya lebih lanjut
(Richtler, 1984).
Oleokimia alami merupakan senyawa kimia yang berasal dari minyak atau lemak
tumbuh – tumbuhan yang diperoleh dengan cara saponifikasi dan diikuti dengan reaksi
hidrolisis sehingga menghasilkan asam lemak bebas dan gliserol. Dari asam lemak ini
dapat dibuat lebih lanjut turunan asam lemak seperti alkohol asam lemak, amina asam
lemak dan turunan lainnya. Sedangkan oleokimia sintesis berasal dari petrokimia
misalnya pembuatan alkohol asam lemak dari etilena serta gliserol dari propilena (Austin,
1985).
Bahan oleokimia yang dihasilkan dari produk petrokimia yang diolah dari hasil
minyak bumi dan gas alam merupakan bahan yang tidak dapat terbaharui, sehingga
diperkirakan tidak dapat bersaing dengan bahan yang berasal dari hasil pertanian yang
sebagai surfaktan pada produk – produk kosmetik, obat – obatan, makanan serta produk
pencuci dan pembersih.
Secara skematis perubahan minyak atau lemak dan olefin menjadi produk oleokimia
dapat dilihat pada tabel 2.1 (Richtler, 1984).
Tabel 2.1 Diagram Alur Oleokimia
Bahan Baku Oleokimia dasar Derivat
2.2 Palm Fatty Acid Distillate ( PFAD )
Palm Fatty Acid Disillate ( PFAD ) merupakan hasil samping dari pemurnian CPO setelah melalui tahapan – tahapan proses degumming, deasidifikasi dan pengeringan
sistem vakum . PFAD tersedia dalam bentuk padatan berwarna putih dan kuning pada
temperatur kamar dan akan mencair bila dipanaskan. PFAD memiliki tingkat kandungan FFA ( Free Fatty Acid ) yang sangat tinggi yaitu 93% ( 45,6% asam palmitat; 33,3%
asam oleat; 7,7% asam linoleat; 3,8% asam stearat; 1,0% asam miristat; 0,6%
tetrakosenoat; 0,3% asam linolenat; 0,3% ekosanoat; 0,2% ekosenoat; dan 0,2% asam
palmitoleat).
Palm Fatty Acid Distillate (PFAD) dapat digunakan dalam industri sabun, industri pakan ternak, dan sebagai bahan mentah untuk industri petrokimia (Chongkong, 2007).
2.3 Gliserida
Gliserida disebut juga dengan asilgliserol yang merupakan senyawa ester antara
gliserol dan asam lemak. Gliserida yang bersifat padat pada suhu kamar disebut dengan
lemak sedangkan yang bersifat cair disebut dengan minyak. Gliserida dengan 1,2, dan 3
rantai asam lemak maka masing – masing disebut dengan mono-, di-, dan triasilgliserol
H2C O C
Gliserida secara alami dapat ditemui disemua lemak hewan, minyak nabati dan
minyak ikan sebagai ester gliserol dari asam lemak. Gliserida ini dapat dihidrolisis
menjadi gliserol dan asam lemak, sehingga gliserida merupakan suatu sumber yang
berpotensi untuk membuat gliserol yang kemudian pada industri oleokimia digunakan
sebagai bahan komersil untuk berbagai keperluan. Disamping dapat diperoleh dari
sumber alami, gliserol juga dapat disintesis dari produk petrokimia seperti propilena melalui tahap reaksi adisi dengan Cl2 membentuk alil klorida yang diikuti reaksi adisi
HOCl membentuk epiklorhidrin serta reaksi substitusi dengan NaOH membentuk gliserol
( Austin,1985 ).
2.4 Monogliserida dan Digliserida
Pada saat ini monogliserida atau campuran mono dan digliserida merupakan
bahan komersil yang cukup penting dan banyak digunakan dalam industri kimia untuk
aditif makanan, surfaktan, cat, plastik, dan polimer. Bentuk dan fasa monogliserida sangat
bervariasi dapat berupa cair, plastis atau padat yang tergantung pada proses dan bahan
baku yang digunakan ( Sadi,1994 ).
Mono- dan diasilgliserol (digliserida) dalam industri pangan digunakan sebagai
dapat memperbaiki reologi adonan dan memperpanjang masa simpan tekstur tortilla
jagung. Monogliserida dalam adonan bereaksi dengan amilopektin membentuk senyawa
kompleks yang berperan memperbaiki adonan, volume, dan tekstur roti serta
memperpanjang masa simpan produk roti tersebut. Lemak dengan rendah kalori, dapat
mensubstitusi 35% lemak dalam adonan dengan adanya emulsifier mono- dan digliserida
pada tingkat kepekatan 0,5%. Mono- digliserida terbentuk dari reaksi antara gliserol dan trigliserida. Reaksi tersebut dikenal dengan reaksi gliserolisis. Reaksi ini dapat
berlangsung dengan katalis alkali ( gliserolisis cara kimia ) maupun dengan biokatalis
lipase ( gliserolisis cara enzimatik) (Hasanuddin, 2001).
Mono- dan digliserida dapat disintesis dari asam lemak dengan cara esterifikasi
langsung ataupun dengan gliserolisis sebagian dari lemak alami. Mono- dan digliserida
asam lemak bermanfaat sebagai emulsifier non-ionik, zat penstabil, dan antioksidan serta
dapat juga digunakan sebagai surfaktan ( Gavrila, 2000 ).
2.5 Trigliserida
Trigliserida yang tersusun dari asam lemak tidak jenuh akan berwujud cair dan
mempunyai titik cair yang rendah. Umumnya trigliserida ini terdapat pada minyak nabati.
Trigliserida yang tersusun dari asam lemak jenuh akan berwujud padat dan mempunyai
titik didih cair yang tinggi. Umumnya trigliserida ini terdapat pada minyak hewani.
Giserida dalam minyak atau lemak bukan merupakan gliserida sederhana (tiga gugus
hidroksinya berikatan dengan tiga asam dari jenis yang sama pada gliserol), tetapi
merupakan gliserida campuran (Christie,1982). Trigliserida secara alami terdapat pada
2.6 Gliserol
Secara industri, gliserol merupakan suatu produk minyak dan lemak yang
diperoleh dari saponifikasi, hidrolisa ataupun transesterifikasi.
Gliserol berupa komponen kimia yang memiliki struktur 1,2,3-propanatriol, CH2OHCHOHCH2OH. Sifat – sifat dari gliserol antara lain :
- berupa cairan kental dan berasa manis
- tidak berwarna
- dapat larut dalam air dan alkohol
- tidak dapat larut dalam benzene, kloroform, karbon tetraklorida, karbon disulfida dan
petroleum eter
- tekanan uap 0,0025mmHg (500) - titik didih 2900C (760 mmHg) - titik lebur 18,170C
- viskositas 1,499
- titik beku ( gliserol 66,7% ) 46,50C (Bonnardeaux, 2006)
2.7 Organik Karbonat
Organik karbonat merupakan suatu zat intermediet dalam kimia. Contohnya saja
dimetil karbonat. Selain sebagai zat karbonilasi dan metilasi untuk pembuatan urea,
urethan, isosianat, garam kuartener ammonium, fenol ester, dan polikarbonat seperti yang
dikatakan di atas, dimetil karbonat dapat juga digunakan sebagai minyak pelumas
sintetik, monomer untuk reaksi polimerisasi, zat pemlastis. Senyawa organik karbonat yang paling umum yaitu : dimetil karbonat, dietil karbonat, n-propil karbonat,
Ada berbagai metode untuk pembuatan organik karbonat dari alkohol, yaitu
(Bhattacharya,1991)
I. Oksidatif Karbonilasi Langsung
2 ROH + CO + ½ O2→ R2CO3 + H2O
II. Oksidatif Karbonilasi secara Tak Langsung
(i) dengan phosgen
(i) dengan etilen karbonat
C2H4O + CO2 → C2H4CO3
C2H4CO3 + 2 ROH → R2CO3 + HOCH2CH2OH
(ii) dengan Di-tert-butil proxide ( DTBP)
2 C4H10 + 3/2 O2 → C4H9OOC4H9 + H2O
2.8 Metode Pembuatan Dimetil Karbonat
Dimetil karbonat merupakan suatu prekursor yang penting dari resin polikarbonat dan juga dapat digunakan sebagai zat karbonilasi dan metilasi. Karena tingkat keracunan
dari dimetil karbonat dapat diabaikan, maka sangat menjanjikan sebagai suatu zat yang
dapat direaksikan dengan phosgen, dimetil sulfat, n-etil iodida, dan juga dapat
Dimetil karbonat dapat disintesis dari propilen atau glikol etilen dengan adanya
ester fase cair untuk menggantikan reaksi antara propilen atau etilen karbonat dan
metanol (Morrel, 2003)
Dimetil karbonat dapat disintesis melalui :
1. reaksi karbonilasi oksidatif senyawa alkohol atau fenol
2. reaksi senyawa aromatis dan phosgene
Reaksi karbonilasi oksidatif dari metanol
Pembuatan dimetil karbonat dengan reaksi metanol dengan karbon monoksida dan
oksigen dengan adanya tembaga (I) klorida atau tembaga (II) metoksiklorida terjadi
dalam 2 tahap atau 1 tahap proses katalitik, yaitu :
2 CuCl + 2 MeOH + ½ O2→ 2 Cu(OMe)Cl + H2O
2 Cu(OMe)Cl + CO → (MeO)2CO + 2 CuCl
2 MeOH + CO + ½ O2 CuCl/Cu(MeO)Cl→ (MeO)2CO + H2O
Pembuatan dimetil karbonat dengan cara ini terjadi secara eksotermik. Oksidasi
langsung dari karbon monoksida menjadi karbon dioksida akan lebih meningkat karena
pembentukan air yang dapat larut dalam sistem katalitik. Pada konsentrasi air yang tinggi,
maka kemungkinan terjadi dekomposisi senyawa dimetil karbonat akibat hidrolisis akan
Metode phosgen (COCl2)
Pada metode ini senyawa hidroksi dilarutkan dalam pelarut campuran atau tunggal
yang bersifat inert dan bebas air (diklorometan, kloroform, benzene, toluen) dengan
adanya piridin dan phosgen berlebih pada atau di bawah suhu kamar.
Piridin bertindak sebagai aseptor asam dan bereaksi dengan phosgen yang merupakan satu – satunya aseptor asam yang dapat digunakan.
Senyawa hidroksi aromatis lebih lambat bereaksi dengan phosgen daripada
senyawa hidroksi alifatik. Pengubahan senyawa hidroksi menjadi karbonat dapat terjadi
dengan cepat, untuk itu reaksi dapat berlangsung secara kontinu tanpa ada kesulitan
sehingga dihasilkan karbonat dengan hasil yang tinggi.
Salah satu kelemahan dari metode ini adalah proses reaksi yang melibatkan
penggunaan zat – zat kimia yang beracun dan berbahaya seperti phosgen dan piridin.
Kelebihan piridin harus dinetralisasi serta terbentuknya produk samping yang harus
dipisahkan sehingga membutuhkan langkah – langkah pemurnian tambahan
(Shaikh,1996).
2.9 Gliserol Karbonat
Gliserol karbonat bersifat stabil, cairan agak berwarna yang dapat digunakan
sebagai pelarut, aditif dan merupakan zat antara kimia. Sebagai zat antara, gliserol
karbonat dapat bereaksi dengan cepat dengan alkohol, fenol, dan asam karboksilat dengan
kehilangan CO2 maupun amin alifatik dengan diperolehnya kembali karbon dioksida.
Gliserol karbonat dapat diperoleh dengan berbagai macam metode yaitu dengan
menggunakan komponen epoksi maupun gliserol sebagai bahan dasar.
Telah dilaporkan bahwa telah banyak cara untuk membuat gliserol karbonat.
pemunian dengan destilasi vakum yang umumnya dilakukan pada suhu yang relatif tinggi
( 125 – 1500C ).
Pembuatan gliserol karbonat yang paling baik yaitu dengan cara mereaksikan
gliserol dan dimetil karbonat karena sifat gliserol karbonat yang dihasilkan ramah
lingkungan dan reagen yang digunakan dapat diperbaharui (Rokicki, 2005).
Metode Sintesis Gliserol Karbonat
Senyawa gliserol karbonat dapat disintesis melalui beberapa metode, yaitu :
1. melalui reaksi gliserol dan dimetil karbonat
2. melalui reaksi gliserol dan etilen karbonat
3. melalui reaksi trans-esterifikasi gliserol dan etilen karbonat atau propena karbonat
4. melalui reaksi gliserol dan urea
Sintesis senyawa gliserol karbonat melalui reaksi gliserol dan dimetil karbonat
harus dilakukan dalam kondisi yang sesuai. Dimetil karbonat yang digunakan yaitu dalam
jumlah molar yang berlebih 3:1 untuk dimetil karbonat : gliserol untuk menyetarakan
kesetimbangan reaksi sehingga diperoleh hasil yang diinginkan. Sedangkan untuk gliserol
yang digunakan harus mengandung paling sedikitnya 2% air dan berlangsung pada suhu
60-700C dengan adanya K2CO3 sebagai katalis sehingga menghasilkan gliserol karbonat
dalam jumlah yang cukup banyak. Untuk mendorong terjadinya pembentukan produk
samping maka reaksi dilakukan dengan cara pengadukan selama 3 jam. Sehingga
diperoleh metanol dan dimetil karbonat yang tidak habis bereaksi sebagai produk
samping. Pemisahan antara gliserol karbonat yang diperoleh dengan produk samping
Reaksi yang terjadi adalah sebagai berikut ( Rokicki, 2005 ) :
HO
OH
OH
+ O
O O
K2CO3
70OC HO O
O
O
+ CH
3OH
gliserol dimetil karbonat
BAB 2
TINJAUAN PUSTAKA
2.1 Oleokimia
Oleokimia merupakan suatu bagian ilmu kimia yang mempelajari tentang proses
pengolahan asam lemak dan gliserol serta turunannya, baik yang diperoleh dari minyak
atau lemak maupun hasil sintesis dari produksi etilena dan propilena secara industri
petrokimia.
Bahan dasar oleokimia diproduksi dari reaksi pemecahan atau pemisahan dan
reaksi lebih lanjut dari minyak atau lemak yaitu: asam lemak, gliserol, metil ester asam
lemak, alkohol asam lemak, dan amina. Dua bahan dasar terakhir merupakan bahan dasar
yang utama karena memegang peranan penting dalam pembuatan turunannya lebih lanjut
(Richtler, 1984).
Oleokimia alami merupakan senyawa kimia yang berasal dari minyak atau lemak
tumbuh – tumbuhan yang diperoleh dengan cara saponifikasi dan diikuti dengan reaksi
hidrolisis sehingga menghasilkan asam lemak bebas dan gliserol. Dari asam lemak ini
dapat dibuat lebih lanjut turunan asam lemak seperti alkohol asam lemak, amina asam
lemak dan turunan lainnya. Sedangkan oleokimia sintesis berasal dari petrokimia
misalnya pembuatan alkohol asam lemak dari etilena serta gliserol dari propilena (Austin,
1985).
Bahan oleokimia yang dihasilkan dari produk petrokimia yang diolah dari hasil
minyak bumi dan gas alam merupakan bahan yang tidak dapat terbaharui, sehingga
sebagai surfaktan pada produk – produk kosmetik, obat – obatan, makanan serta produk
pencuci dan pembersih.
Secara skematis perubahan minyak atau lemak dan olefin menjadi produk oleokimia
dapat dilihat pada tabel 2.1 (Richtler, 1984).
Tabel 2.1 Diagram Alur Oleokimia
Bahan Baku Oleokimia dasar Derivat
2.2 Palm Fatty Acid Distillate ( PFAD )
Palm Fatty Acid Disillate ( PFAD ) merupakan hasil samping dari pemurnian CPO setelah melalui tahapan – tahapan proses degumming, deasidifikasi dan pengeringan
sistem vakum . PFAD tersedia dalam bentuk padatan berwarna putih dan kuning pada
temperatur kamar dan akan mencair bila dipanaskan. PFAD memiliki tingkat kandungan FFA ( Free Fatty Acid ) yang sangat tinggi yaitu 93% ( 45,6% asam palmitat; 33,3%
asam oleat; 7,7% asam linoleat; 3,8% asam stearat; 1,0% asam miristat; 0,6%
tetrakosenoat; 0,3% asam linolenat; 0,3% ekosanoat; 0,2% ekosenoat; dan 0,2% asam
palmitoleat).
Palm Fatty Acid Distillate (PFAD) dapat digunakan dalam industri sabun, industri pakan ternak, dan sebagai bahan mentah untuk industri petrokimia (Chongkong, 2007).
2.3 Gliserida
Gliserida disebut juga dengan asilgliserol yang merupakan senyawa ester antara
gliserol dan asam lemak. Gliserida yang bersifat padat pada suhu kamar disebut dengan
lemak sedangkan yang bersifat cair disebut dengan minyak. Gliserida dengan 1,2, dan 3
rantai asam lemak maka masing – masing disebut dengan mono-, di-, dan triasilgliserol
H2C O C
Gliserida secara alami dapat ditemui disemua lemak hewan, minyak nabati dan
minyak ikan sebagai ester gliserol dari asam lemak. Gliserida ini dapat dihidrolisis
menjadi gliserol dan asam lemak, sehingga gliserida merupakan suatu sumber yang
berpotensi untuk membuat gliserol yang kemudian pada industri oleokimia digunakan
sebagai bahan komersil untuk berbagai keperluan. Disamping dapat diperoleh dari
sumber alami, gliserol juga dapat disintesis dari produk petrokimia seperti propilena melalui tahap reaksi adisi dengan Cl2 membentuk alil klorida yang diikuti reaksi adisi
HOCl membentuk epiklorhidrin serta reaksi substitusi dengan NaOH membentuk gliserol
( Austin,1985 ).
2.4 Monogliserida dan Digliserida
Pada saat ini monogliserida atau campuran mono dan digliserida merupakan
bahan komersil yang cukup penting dan banyak digunakan dalam industri kimia untuk
aditif makanan, surfaktan, cat, plastik, dan polimer. Bentuk dan fasa monogliserida sangat
bervariasi dapat berupa cair, plastis atau padat yang tergantung pada proses dan bahan
baku yang digunakan ( Sadi,1994 ).
Mono- dan diasilgliserol (digliserida) dalam industri pangan digunakan sebagai
emulsifier pada pengolahan margarin, mentega, kacang, pemutih, puding, roti, biskuit dan
dapat memperbaiki reologi adonan dan memperpanjang masa simpan tekstur tortilla
jagung. Monogliserida dalam adonan bereaksi dengan amilopektin membentuk senyawa
kompleks yang berperan memperbaiki adonan, volume, dan tekstur roti serta
memperpanjang masa simpan produk roti tersebut. Lemak dengan rendah kalori, dapat
mensubstitusi 35% lemak dalam adonan dengan adanya emulsifier mono- dan digliserida
pada tingkat kepekatan 0,5%. Mono- digliserida terbentuk dari reaksi antara gliserol dan trigliserida. Reaksi tersebut dikenal dengan reaksi gliserolisis. Reaksi ini dapat
berlangsung dengan katalis alkali ( gliserolisis cara kimia ) maupun dengan biokatalis
lipase ( gliserolisis cara enzimatik) (Hasanuddin, 2001).
Mono- dan digliserida dapat disintesis dari asam lemak dengan cara esterifikasi
langsung ataupun dengan gliserolisis sebagian dari lemak alami. Mono- dan digliserida
asam lemak bermanfaat sebagai emulsifier non-ionik, zat penstabil, dan antioksidan serta
dapat juga digunakan sebagai surfaktan ( Gavrila, 2000 ).
2.5 Trigliserida
Trigliserida yang tersusun dari asam lemak tidak jenuh akan berwujud cair dan
mempunyai titik cair yang rendah. Umumnya trigliserida ini terdapat pada minyak nabati.
Trigliserida yang tersusun dari asam lemak jenuh akan berwujud padat dan mempunyai
titik didih cair yang tinggi. Umumnya trigliserida ini terdapat pada minyak hewani.
Giserida dalam minyak atau lemak bukan merupakan gliserida sederhana (tiga gugus
hidroksinya berikatan dengan tiga asam dari jenis yang sama pada gliserol), tetapi
merupakan gliserida campuran (Christie,1982). Trigliserida secara alami terdapat pada
2.6 Gliserol
Secara industri, gliserol merupakan suatu produk minyak dan lemak yang
diperoleh dari saponifikasi, hidrolisa ataupun transesterifikasi.
Gliserol berupa komponen kimia yang memiliki struktur 1,2,3-propanatriol, CH2OHCHOHCH2OH. Sifat – sifat dari gliserol antara lain :
- berupa cairan kental dan berasa manis
- tidak berwarna
- dapat larut dalam air dan alkohol
- tidak dapat larut dalam benzene, kloroform, karbon tetraklorida, karbon disulfida dan
petroleum eter
- tekanan uap 0,0025mmHg (500) - titik didih 2900C (760 mmHg) - titik lebur 18,170C
- viskositas 1,499
- titik beku ( gliserol 66,7% ) 46,50C (Bonnardeaux, 2006)
2.7 Organik Karbonat
Organik karbonat merupakan suatu zat intermediet dalam kimia. Contohnya saja
dimetil karbonat. Selain sebagai zat karbonilasi dan metilasi untuk pembuatan urea,
urethan, isosianat, garam kuartener ammonium, fenol ester, dan polikarbonat seperti yang
dikatakan di atas, dimetil karbonat dapat juga digunakan sebagai minyak pelumas
sintetik, monomer untuk reaksi polimerisasi, zat pemlastis. Senyawa organik karbonat yang paling umum yaitu : dimetil karbonat, dietil karbonat, n-propil karbonat,
Ada berbagai metode untuk pembuatan organik karbonat dari alkohol, yaitu
(Bhattacharya,1991)
I. Oksidatif Karbonilasi Langsung
2 ROH + CO + ½ O2→ R2CO3 + H2O
II. Oksidatif Karbonilasi secara Tak Langsung
(i) dengan phosgen
(i) dengan etilen karbonat
C2H4O + CO2 → C2H4CO3
C2H4CO3 + 2 ROH → R2CO3 + HOCH2CH2OH
(ii) dengan Di-tert-butil proxide ( DTBP)
2 C4H10 + 3/2 O2 → C4H9OOC4H9 + H2O
2.8 Metode Pembuatan Dimetil Karbonat
Dimetil karbonat merupakan suatu prekursor yang penting dari resin polikarbonat dan juga dapat digunakan sebagai zat karbonilasi dan metilasi. Karena tingkat keracunan
dari dimetil karbonat dapat diabaikan, maka sangat menjanjikan sebagai suatu zat yang
dapat direaksikan dengan phosgen, dimetil sulfat, n-etil iodida, dan juga dapat
Dimetil karbonat dapat disintesis dari propilen atau glikol etilen dengan adanya
ester fase cair untuk menggantikan reaksi antara propilen atau etilen karbonat dan
metanol (Morrel, 2003)
Dimetil karbonat dapat disintesis melalui :
1. reaksi karbonilasi oksidatif senyawa alkohol atau fenol
2. reaksi senyawa aromatis dan phosgene
Reaksi karbonilasi oksidatif dari metanol
Pembuatan dimetil karbonat dengan reaksi metanol dengan karbon monoksida dan
oksigen dengan adanya tembaga (I) klorida atau tembaga (II) metoksiklorida terjadi
dalam 2 tahap atau 1 tahap proses katalitik, yaitu :
2 CuCl + 2 MeOH + ½ O2→ 2 Cu(OMe)Cl + H2O
2 Cu(OMe)Cl + CO → (MeO)2CO + 2 CuCl
2 MeOH + CO + ½ O2 CuCl/Cu(MeO)Cl→ (MeO)2CO + H2O
Pembuatan dimetil karbonat dengan cara ini terjadi secara eksotermik. Oksidasi
langsung dari karbon monoksida menjadi karbon dioksida akan lebih meningkat karena
pembentukan air yang dapat larut dalam sistem katalitik. Pada konsentrasi air yang tinggi,
maka kemungkinan terjadi dekomposisi senyawa dimetil karbonat akibat hidrolisis akan
Metode phosgen (COCl2)
Pada metode ini senyawa hidroksi dilarutkan dalam pelarut campuran atau tunggal
yang bersifat inert dan bebas air (diklorometan, kloroform, benzene, toluen) dengan
adanya piridin dan phosgen berlebih pada atau di bawah suhu kamar.
Piridin bertindak sebagai aseptor asam dan bereaksi dengan phosgen yang merupakan satu – satunya aseptor asam yang dapat digunakan.
Senyawa hidroksi aromatis lebih lambat bereaksi dengan phosgen daripada
senyawa hidroksi alifatik. Pengubahan senyawa hidroksi menjadi karbonat dapat terjadi
dengan cepat, untuk itu reaksi dapat berlangsung secara kontinu tanpa ada kesulitan
sehingga dihasilkan karbonat dengan hasil yang tinggi.
Salah satu kelemahan dari metode ini adalah proses reaksi yang melibatkan
penggunaan zat – zat kimia yang beracun dan berbahaya seperti phosgen dan piridin.
Kelebihan piridin harus dinetralisasi serta terbentuknya produk samping yang harus
dipisahkan sehingga membutuhkan langkah – langkah pemurnian tambahan
(Shaikh,1996).
2.9 Gliserol Karbonat
Gliserol karbonat bersifat stabil, cairan agak berwarna yang dapat digunakan
sebagai pelarut, aditif dan merupakan zat antara kimia. Sebagai zat antara, gliserol
karbonat dapat bereaksi dengan cepat dengan alkohol, fenol, dan asam karboksilat dengan
kehilangan CO2 maupun amin alifatik dengan diperolehnya kembali karbon dioksida.
Gliserol karbonat dapat diperoleh dengan berbagai macam metode yaitu dengan
menggunakan komponen epoksi maupun gliserol sebagai bahan dasar.
pemunian dengan destilasi vakum yang umumnya dilakukan pada suhu yang relatif tinggi
( 125 – 1500C ).
Pembuatan gliserol karbonat yang paling baik yaitu dengan cara mereaksikan
gliserol dan dimetil karbonat karena sifat gliserol karbonat yang dihasilkan ramah
lingkungan dan reagen yang digunakan dapat diperbaharui (Rokicki, 2005).
Metode Sintesis Gliserol Karbonat
Senyawa gliserol karbonat dapat disintesis melalui beberapa metode, yaitu :
1. melalui reaksi gliserol dan dimetil karbonat
2. melalui reaksi gliserol dan etilen karbonat
3. melalui reaksi trans-esterifikasi gliserol dan etilen karbonat atau propena karbonat
4. melalui reaksi gliserol dan urea
Sintesis senyawa gliserol karbonat melalui reaksi gliserol dan dimetil karbonat
harus dilakukan dalam kondisi yang sesuai. Dimetil karbonat yang digunakan yaitu dalam
jumlah molar yang berlebih 3:1 untuk dimetil karbonat : gliserol untuk menyetarakan
kesetimbangan reaksi sehingga diperoleh hasil yang diinginkan. Sedangkan untuk gliserol
yang digunakan harus mengandung paling sedikitnya 2% air dan berlangsung pada suhu
60-700C dengan adanya K2CO3 sebagai katalis sehingga menghasilkan gliserol karbonat
dalam jumlah yang cukup banyak. Untuk mendorong terjadinya pembentukan produk
samping maka reaksi dilakukan dengan cara pengadukan selama 3 jam. Sehingga
diperoleh metanol dan dimetil karbonat yang tidak habis bereaksi sebagai produk
samping. Pemisahan antara gliserol karbonat yang diperoleh dengan produk samping
Reaksi yang terjadi adalah sebagai berikut ( Rokicki, 2005 ) :
HO
OH
OH
+ O
O O
K2CO3
70OC HO O
O
O
+ CH
3OH
gliserol dimetil karbonat
BAB 3
BAHAN DAN METODE PENELITIAN
3.1 Alat – alat
Alat – alat yang digunakan dalam penelitian ini adalah :
- Labu leher tiga Pyrex
- Serangkaian alat FT-IR FT-IR Shimadzu 8201-DC
- Serangkaian alat 1H-NMR Hitachi FT – NMR R-1900 - Serangkaian alat Kromatografi Gas (GC)
3.2 Bahan – Bahan
Bahan – bahan yang digunakan dalam penelitian ini adalah :
- Palm Fatty Acid Distillate ( PFAD)
3.3 Prosedur Penelitian
3.3.1 Pembuatan Gliserol Karbonat
Sebanyak 20 gram gliserol 99,5% (0,2174 mol) dimasukkan ke dalam labu leher
tiga dan ditambahkan moleculer shieves sebanyak 2 gram. Kemudian ditambahkan 60
gram dimetil karbonat (0,6667 mol) dan 0,9 gram K2CO3 (6,52 mmol) sebagai katalis.
Selanjutnya labu dihubungkan dengan pendingin bola dan direfluks pada suhu 73 – 750C selama 3 jam, dimana untuk mengetahui terjadinya reaksi maka dilakukan uji KLT setiap 1 jam. Hasil reaksi di destilasi dengan tekanan 0,5cmHg pada suhu 400C. Residu yang
diperoleh disaring dengan resin penukar kation Amberlit IR-120 sebanyak 24,4 gram.
3.3.2. Sintesis Monogliserida dari PFAD
Sebanyak 9 gram PFAD (0,0352 mol berdasarkan berat molekul asam palmitat)
dimasukkan ke dalam labu leher tiga kemudian ditambahkan moleculer shieves sebanyak
2 gram dan 0,37 ml trietilamin (0,2.66 mmol) sebagai katalis. Selanjutnya dirangkai alat
refluks dengan pendingin bola dan penampung gelembung gas yang dialiri dengan gas Nitrogen secara perlahan. Dipanaskan hingga suhu 800C sambil diaduk. Kemudian
ditambahkan 4,2086 gram gliserol karbonat (0,0357 mol) setetes demi setetes selama 1
jam. Dipanaskan hingga suhu 115 – 1200C dan diaduk selama 10 jam, dimana untuk mengetahui terjadinya reaksi maka dilakukan uji KLT setiap 1 jam. Selanjutnya suhu
diturunkan hingga mencapai 600C dan ditambahkan 34 ml petroleum eter kemudian diaduk selama 15 – 20 menit. Kemudian suhu diturunkan hingga mencapai 40 – 450C dan dibiarkan selama 15 – 20 menit hingga terbentuk 2 lapisan kemudian didekantasi. Lapisan
atas didinginkan hingga terbentuk kristal putih. Kemudian dipisahkan dan kristal tersebut
dibiarkan pada temperatur kamar sehingga berubah menjadi larutan. Larutan tersebut
3.4 Bagan Penelitian
3.4.1 Pembuatan Gliserol Karbonat
← dimasukkan ke dalam labu leher tiga
← ditambahkan moleculer shieve sebanyak 2 gram
← ditambahkan 60 gram dimetil karbonat (0,6667 mol)
← ditambahkan 0,9 gram K2CO3 (6,52 mmol)
← direfluks selama 3 jam pada suhu 73 – 750C
← diuji dengan KLT setiap 1 jam
←didestilasi dengan tekanan 0,5cmHg pada suhu 400C
← disaring dengan resin Amberlit IR-120 sebanyak 24 ,4 gram
← ditimbang
20 gram gliserol 99,5% (0,2174mol)
campuran
destilat residu
filtrat residu
Gliserol Karbonat
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
Monogliserida dapat disintesis melalui reaksi antara gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2-on) dengan Palm Fatty Acid Distillate (PFAD)
menggunakan katalis trietilamin (TEA). Namun sebelumnya gliserol karbonat disintesis
melalui reaksi antara gliserol dengan dimetil karbonat menggunakan katalis K2CO3 pada
suhu 73–750C selama 3 jam kemudian didestilasi vakum. Gliserol karbonat yang diperoleh berupa cairan kental berwarna kuning pucat sebanyak 12,012 gram (93,65%).
Kemudian dianalisis dengan spektrofotometer FT–IR dan 1H–NMR.
Hasil analisis dengan spektrofotometer FT – IR memberikan spektrum dengan
puncak – puncak serapan vibrasi pada daerah bilangan gelombang 3371 cm-1, 2939 cm-1, 2885 cm-1, 1782 cm-1, 1651 cm-1,1404 cm-1,1303 cm-1,1195 cm-1, dan 1049 cm-1.
Hasil analisis secara 1H–NMR memberikan spektrum dengan puncak – puncak pergeseran kimia masing – masing pada daerah δ = 1,6 ppm (s); δ = 2,2-2,3 ppm (t); δ =
3,7-3,9 ppm (m); dan δ = 4,4-4,8 ppm (m).
Hasil analisis komposisi asam lemak pada PFAD dapat dilihat pada tabel berikut:
Tabel 4.1 Komposisi Asam Lemak pada PFAD
Asam Lemak Persentase (%)
Asam Palmitat 45,6376
Asam Oleat 37,4339
Asam Linoleat 8,8285
Asam Stearat 4,2281
Monogliserida yang diperoleh melalui reaksi antara gliserol karbonat
(4-hidroksimetil-1,3dioksolan-2-on) dan PFAD dianalisis dengan spektrofotometer FT-IR
dan kromatografi gas (GC).
Hasil analisis monogliserida dengan spektrofotometer FT – IR memberikan
spektrum dengan puncak – puncak serapan vibrasi pada daerah bilangan gelombang 3397 cm-1, 3006 cm-1, 2925 cm-1, 2854 cm-1, 1743 cm-1, 1638 cm-1, 1465 cm-1, 1376 cm-1, 1245
cm-1, 995 cm-1, dan 722 cm-1.
Berdasarkan analisis kromatografi gas diketahui bahwa persentase untuk
monogliserida, digliserida, dan trigliserida dapat dilihat pada tabel berikut :
Tabel 4.2 Komposisi Hasil Sintesis
Senyawa Persentase (%)
Monogliserida 15,83
Digliserida 9,320
Trigliserida 1,096
4.2 Pembahasan
Senyawa gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2on) diperoleh melalui
reaksi antara gliserol dengan dimetil karbonat dengan perbandingan 1:3 menggunakan
menggunakan kromatografi lapis tipis (KLT) setiap 1 jam dengan membandingkan jarak
noda antara reaktan dan produk. Adsorben yang digunakan yaitu silika 60 GF dengan
pelarut n-heksana:dietileter v/v (70:30). Hasil yang diperoleh berupa cairan kental
berwarna kuning pucat dan dianalisis dengan spektrofotometer FT– IR dan 1H-NMR.
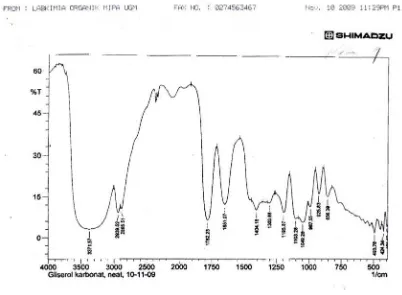
Hasil analisis FT-IR memberikan spektrum dengan puncak – puncak serapan seperti pada Gambar 4.1.
Gambar 4.1. Spektrum FT-IR Senyawa Gliserol Karbonat
Puncak serapan pada daerah bilangan gelombang 3371 cm-1 menunjukkan vibrasi stretching gugus hidroksi (-OH) yang berbeda dengan gugus –OH pada gliserol
(Lampiran 1) yang didukung oleh vibrasi bending gugus –OH pada bilangan gelombang
Berdasarkan literatur, gugus C=O pada senyawa cincin 5 berada pada daerah bilangan
gelombang 1789 cm-1 dan untuk karbonat linear 1745 cm-1 (Rokicki,2005). Selanjutnya puncak serapan pada daerah bilangan gelombang 1404 cm-1 menunjukkan adanya vibrasi
bending untuk gugus CH-sp3 asimetris sedangkan 1303 cm-1 menunjukkan adanya vibrasi bending untuk gugus CH-sp3 simetris. Puncak serapan pada daerah bilangan gelombang 1195 cm-1 dan 1049 cm-1 menunjukkan adanya vibrasi stretching gugus C-O-C pada senyawa cincin 5.
Senyawa gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2-on) juga dianalisis
dengan spektrofotometer 1H-NMR dengan pelarut CDCl3 menggunakan standar TMS dan
spektrum yang diperoleh seperti pada Gambar 4.2.
Gambar 4.2. Spektrum 1H-NMR Senyawa Karbonat
Pergeseran kimia pada daerah δ = 1,6 ppm (s) kemungkinan proton dari H2O. Pergeseran
kimia pada daerah δ = 2,2-2,3 ppm (t) menunjukkan pergeseran kimia proton dari gugus – OH yang secara teori daerah pergeseran kimia proton berada pada daerah 0-4 ppm
gugus –OH. Kemu dian p erg eseran kimia p ada d aerah δ = 4 ,4-4,8 ppm (m) yang
menunjukkan pergeseran kimia proton dari gugus –CH dan –CH2 yang berada pada cincin
5.
Adapun mekanisme reaksi pembentukan senyawa gliserol karbonat
(4-hidroksimetil-1,3-dioksolan-2-on) diperkirakan sebagai berikut :
CH2
Pada tahap pertama atom O dari gliserol yang bersifat nukleofil akan berinteraksi
dengan atom K yang berasal dari katalis K2CO3, sehingga terjadi pemutusan ikatan antara
atom K dan O. Atom O yang berasal dari katalis yang bersifat asam akan mengabstraksi
proton yang terikat pada atom O posisi C-1 dari gliserol. Selanjutnya atom O pada C-1
yang telah terikat dengan atom K akan lebih bersifat nukleofil sehingga menyerang atom
Karbon karbonil yang bersifat elektrofil dari dimetil karbonat sehingga membentuk atom
O yang bermuatan (+). Kemudian atom O karbonil yang bermuatan (-) akan menyerang
Pada tahap berikutnya atom O yang berasal dari katalis, HKCO3 akan menyerang
atom K yang berikatan dengan atom O yang bermuatan (+). Kemudian gugus –OH yang
bermuatan (-) yang telah dilepaskan akan menyerang atom C dari -CH3 yang terikat
dengan atom O pada cincin 5 dan akan stabil bila kemudian atom O membentuk ikatan
rangkap. Kemudian atom –OCH3 akan terlepas dan menyerang proton yang berasal dari
katalis HKCO3. Dan terbentuklah 2 molekul metanol dan senyawa karbonat siklik yaitu
gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2-on).
Hasil dari analisis kromatografi gas untuk PFAD diketahui bahwa 4 komposisi
asam lemak terbanyak yaitu Asam Palmitat (45,636%), Asam Oleat (37,4339%), Asam
Linoleat (8,8285%), dan Asam Stearat (4,2281) dan kromatogram yang diperoleh seperti
pada Gambar 4.3.
Gambar 4.3. Kromatogram GC Komposisi ASam Lemak PFAD
Senyawa gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2-on) yang terbentuk
direaksikan dengan PFAD menggunakan trietilamin sebagai katalis. Adapun mekanisme
reaksi pembentukan monogliserida diperkirakan adalah sebagai berikut :
R C
Pada tahap pertama atom N yang memiliki pasangan elektron bebas yang bersifat
basa akan menyerang proton pada asam lemak sehingga atom O akan bermuatan (-),
sedangkan atom N menjadi bermuatan (+). Selanjutnya atom O yang bermuatan (-) yang
berasal dari asam lemak akan menyerang atom C-1 pada gliserol karbonat sehingga atom
O akan terlepas dan terbukanya posisi cincin 5. Atom O yang bermuatan (-) pada posisi
atom C-2 yang berasal dari cincin 5 akan mengabstraksi proton yang berikatan pada atom
Pada keadaan transisi ini terdapat interaksi antara atom O dari atom C-2 dengan
atom H dari –OH pada atom C-3, dimana atom O dari C-2 akan mengabstraksi proton
yang terdapat pada gugus karbonat sehingga akan melepaskan karbon dioksida (CO2) dan
terbentuklah α-monogliserida.
Dengan cara yang sama kemungkinan juga dapat terjadi pada posisi atom C-2 atau
isomer β, dimana pada jalur reaksi ini tidak terdapat jembatan hidrogen. Adapun
mekanisme reaksi pembentukan monogliserida untuk isomer β diperkirakan sebagai
Berdasakan literatur bahwa monogliserida yang terbentuk akan lebih cenderung
membentuk isomer α (regiospesifik) karena pada keadaan transisi adanya interaksi antara
gugus OH pada atom C-3 dan atom O pada posisi C-2 akan bersifat menstabilkan keadaan
transisi dan dapat memperkecil energi aktivasi (Ghandi,2007).
Monogliserida yang diperoleh dianalisis dengan spektofotometer FT – IR dan
memberikan puncak – puncak serapan seperti pada Gambar 4.4.
Gambar 4.4. Spektrum FT-IR Senyawa Monogliserida
Puncak serapan pada daerah bilangan gelombang 3397 cm-1 menunjukkan vibrasi stretching gugus hidroksi (-OH). Puncak serapan pada daerah bilangan gelombang 3006
gelombang 1638 cm-1 menunjukkan adanya vibrasi stretching C=C. Pada daerah bilangan gelombang 1465 cm-1 menunjukkan adanya vibrasi bending CH-sp3 asimetris dan pada daerah bilangan gelombang 1376 cm-1 menunjukkan adanya vibrasi bending CH-sp3
simetris.
Monogliserida yang diperoleh dianalisis dengan kromatografi gas dan memberikan kromatogram seperti pada Gambar 4.5.
Gambar 4.5. Kromatogram GC Monogliserida Hasil Sintesis
Dari data kromatografi gas tersebut diketahui bahwa monogliserida,digliserida, dan
trigliserida yang diperoleh sebanyak 15,83% ; 9,320% dan 1,096%.
Sedangkan pada PFAD (Lampiran 5) diketahui bahwa sudah adanya kandungan
monogliserida, digliserida dan trigliserida sebanyak 0,1836%; 0,0141% dan 0,8209%.
Dengan demikian maka monogliserida, digliserida dan trigliserida hasil reaksi adalah
15,6464%; 9,3059%; dan 0,2751%. Berdasarkan hasil kromatografi gas, monogliserida
yang diperoleh masih sedikit dan berupa campuran (monogliserida, digliserida, dan
trigliserida). Ini menunjukkan bahwa reaksi belum berlangsung secara regiospesifik. Hal
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Senyawa gliserol karbonat (4-hidroksimetil-1,3-dioksolan-2-on) dapat disintesis melalui reaksi antara gliserol dengan dimetil karbonat menggunakan katalis K2CO3 dan
diperoleh sebanyak 12,012 gram (93,65%).
Monogliserida campuran dapat disintesis melalui reaksi antara gliserol karbonat
(4-hidroksimetil-1,3-dioksolan-2on) dengan Palm Fatty Acid Distillate (PFAD)
menggunakan katalis trietilamin (TEA). Hasil yang diperoleh sebesar 15,83% dan reaksi
belum berlangsung secara regiospesifik.
5.2 Saran
Disarankan untuk meneliti kondisi reaksi yang tepat sehingga reaksi dapat berlangsung secara regiospesifik untuk menghasilkan monogliserida dalam bentuk isomer
DAFTAR PUSTAKA
Austin,G. 1985. Shreve’s Chemical Process Industries. New York : Mc.Graw Hill,Inc
Awang,R., Ahmad,S., Ibrahim,M.F.W.,Yunus,W.M.Z. 2004. Synthesis of Monoglycerides from Dihidroxystearic Acid : Effect of Reaction Parameters. Malaysia : Journal
of Chemistry vol.6 no 1
Bhattacharya,A.K. 1991. Fuel Oxygenates : Organic Carbonate Synthesis. US Patent. 5001252
Bonnardeaux. 2006. Glycerin Overview. Australia : State of Western
Carl,H.S. 2003. The Extraordinary Chemistry of Ordinary Things. Fourth Edition. Miami: John Willey and Sons
Chongkong,S., Tonguraia,C., Chetpattananondha,P. 2007. Biodiesel Production by Esterification of Palm Fatty Acid Distillate (PFAD). Thailand : Elsevier
Christie,W. 1982. Lipid Analysis. New York : Permangor Press Oxford
Delledone, D., Dreoni,D., Rivetti,F. 1995. Catalytic Procedure for The Preparation of Organic Carbonate.US Patent. 5322958
Deman, J. 1980. Principles of Food Chemistry. New York : Van Nostrand Reinhold Company
Gavrila, A.I., Avram,R., Chipurici,P. 2000. Mono and Diglycerides-Synthesis and Uses. Romania : Faculty of Industrial Chemistry Politehnica University of Bucharest
Ghandi, M., Mostashari,A., Karegar,M., Barzegar,M. 2007. Efficient Synthesis of α -Monoglycerides Via Solventless Condensation of Fatty Acids with Glycerol Carbonate. Iran : J.Am.Oil.Soc vol 84 : 681 – 685
Hasanuddin, A. 2001. Kajian Teknologi Pengolahan Minyak Kelapa Sawit Mentah untuk Produksi Emulsifier Mono- diasilgliserol dan Konsentrat Karotenoid. Makalah Falsafah Sains ( PPs 702 ). Institut Pertanian Bogor
Morrell, D.G. 2003. Catalysis of Organic Reactions. New York : Marcel Dekker,Inc
Richtler, H., Knaut,J. 1984. Challenges To A Nature Industry : Marketing and Economics of Oleochemicals in Western Europe. Germany : J.Am.Oil.Chem.Soc vol 61
Rokicki, G., Rakoczy,P., Parzuchowski,P., Sobiecki,M. 2005. Hyperbranched Aliphatic Polyethers Obtained from Environmentally Benign Monomer : Glycerol Carbonate. Poland : Green Chem 7
Sadi, S. 1994. Gliserolisis Minyak Kelapa Sawit dan Inti Sawit dengan Piridin. Buletin PPKS vol 2
Shaikh, A.S., Sivaram,G., Swaminathan.1996. Organic Carbonate. Chemical Review 61
Sonntag,T., Norman,O.V. 1982. Glycerolysis of Fats and Methyl Esters- Status, Review, and Critique. New Orleans : J.Am.Oil.Chem.Soc vol 59 no 10
Lampiran 1. Spektrum FT–IR Senyawa Gliserol Sebagai Pembanding
HO
OH
OH