SINTESIS NANOSELULOSA DARI TONGKOL JAGUNG
DENGAN PERLAKUAN HIDROLISIS KIMIA DAN
HOMOGENISASI
SKRIPSI
NICHE EVANDANI
F24080050
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
SYNTHESIS NANOCELLULOSE FROM CORN COBS WITH
CHEMICAL HYDROLYSIS AND HOMOGENIZATION TREATMENT
Niche Evandani1, Hanifah Nuryani Lioe1, Sri Yuliani2. 1
Department of Food Science and Technology, Faculty of Agricultural Technology, Bogor Agricultural University, IPB Darmaga Campus, PO BOX 220, Bogor, West Java, Indonesia.
2
Balai Besar Penelitian dan Pengembangan Pascapanen Pertanian, Cimanggu, PO BOX 16114, Bogor, West Java Indonesia.
Phone: +62 856 2453 5081, E-mail: nicheevan@yahoo.com
ABSTRACT
Corn cobs has a high potency to be used as a source of raw materials for
nanocellulose synthesis.The objective of this research is to synthesize
nanocellulose from corn cobs with chemical hydrolysis and homogenization
treatment. Alkali treatment,bleaching treatment, acid treatment and
homogenization treatment on the corn cobs are effective in the depolymerization
and defibrillation of the fibre to produce nanocellulose. This research consists of
four main steps those are pre-elliminary research, chemical analysis, synthesize
nanocellulose, and final product characterization.Parameters thatwillbe tested
aretheconcentration ofNaOH(2%, 4%, and 8%), and the time ofhomogenization
(2 hours, 3 hours, and 4 hours). The results show that the concentration of NaOH
affect the level of cellulose and lignin final product.The bestconcentration
ofNaOH needed to isolatecelluloseis 2%. Futhermore, the concentration of NaOH
also affected the color and suspension of the final product. Final product with 8%
NaOH treatment had the brightest color and the most stable suspension, while the
homogenization time did not affect the colorand can not be seen the effect to the
suspension formation of the final product . ScanningElectronMicrocope(SEM)
results showed thatthechemical hydrolysis and mechanical treatmenthad
successfully isolated thecelluloseandits sizehad reachedbelow 100nm, but stillin
small amounts. Cellulose that was observed withSEM had an averagesize
of80-270nmdiameter.
NICHE EVANDANI. F24080050. Sintesis Nanoselulosa dari Tongkol Jagung dengan Perlakuan Hidrolisis Kimia dan Homogenisasi. Di bawah bimbingan Hanifah Nuryani Lioe dan Sri Yuliani. 2012.
RINGKASAN
Selulosa merupakan salah satu polimer alam yang paling banyak dimanfatkan dalam industri. Selulosa dengan bantuan nanoteknologi dapat ditingkatkan kualitasnya menjadi produk yang bernilai ekonomi tinggi, yaitu nanoselulosa. Nanoselulosa memiliki sifat-sifat yang khas seperti sangat kuat, rasio permukaan terhadap volume yang besar, kemampuan mengikat air yang tinggi, kekuatan tarik yang tinggi, jaringan yang halus, dan sangat porous. Sifat-sifat tersebut membuat nanoselulosa merupakan bahan yang sangat menjanjikan untuk industri komposit, kemasan pangan, bahan otomotif, pulp dan kertas, dsb (Subyakto et al. 2009)
Tujuan utama dari penelitian ini adalah sintesis nanoselulosa dari tongkol jagung dengan menggunakan metode hidrolisis kimia dan homogenisasi. Adapun tujuan khusus dari penelitian ini adalah menentukan konsentrasi NaOH dan proses homogenisasi yang terbaik untuk sintesis nanoselulosa dari tongkol jagung dengan perlakuan hidrolisis kimia dan homogenisasi.Manfaat yang diharapkan dalam penelitian ini adalah dapat memanfaatkan limbah pertanian (tongkol jagung) menjadi produk yang bernilai ekonomi tinggi, yaitu nanoselulosa.
Metode penelitian yang digunakan merupakan campuran perlakuan kimia dan mekanik. Secara garis besar terdapat 4 tahapan perlakuan dalam medote sintesis nanoselulosa yang digunakan yaitu, hidrolisis basa, bleaching, hidrolisis asam dan homogenisasi. Rancangan percobaan yang digunakan adalah rancangan acak lengkap faktorial dan 2 ulangan. Faktor yang akan diuji pengaruhnya yaitu konsentrasi NaOH dengan 3 taraf: 2%, 4%, dan 8%, serta waktu homogenisasi dengan 3 taraf: 2 jam, 3 jam, dan 4 jam.
Pada penelitian pendahuluan telah dilakukan dua kali trial and error. Berdasarkan penelitian pendahuluan diketahui bahwa metode hidrolisis kimia dan homogenisasi telah mampu mengisolasi selulosa dengan diameter dibawah 500 nm. Selain itu, diketahui juga bahwa waktu dan kecepatan homogenisasi mempengaruhi proses sintesis nanoselulosa.
Bahan baku penelitian ini adalah tepung tongkol jagung yang telah lolos saringan 100 mesh. Komposisi kimia tepung tongkol jagung berdasarkan hasil analisis proksimat adalah kadar air 8,94% (bk), kadar abu 2,42% (bk), kadar lemak 4,86% (bk), kadar protein 0,57% (bk), kadar karbohidrat (by differene) 83,21% (bk), dan kadar selulosa 57,38 % (bk), dan kadar lignin 9,88 % (bk). Kadar selulosa yang tinggi pada tongkol jagung menunjukkan bahwa tongkol jagung berpotensial tinggi untuk dijadikan sumber bahan baku sintesis nanoselulosa.
Parameter produk akhir yang diukur pada penelitian ini mencakup karakteristik kimia, fisik, dan mikrostruktural produk akhir sintesis nanoselulosa. Karakteristik kimia yang diukur adalah kadar selulosa dan lignin produk akhir. Karakteristik fisik yang diukur adalah parameter warna dan pembentukan suspensi produk akhir. Karakteristik mikrostruktural yang diukur adalah pengamatan mikrostruktural produk akhir dengan menggunakan mikroskop cahaya dan Scanning Electron Microscope (SEM).
Hasil penelitian menunjukkan bahwa konsentrasi NaOH pada tahapan hidrolisis basa mempengaruhi kadar selulosa dan lignin produk akhir. Konsentrasi NaOH yang terbaik untuk mengisolasi selulosa tanpa mendegradasinya adalah 2% . Produk akhir dengan perlakuan NaOH 2% kadar selulosanya mencapai 77,17% dan kadar lignin yang tersisa tinggal 6,32%.
terhadap warna produk akhir. Waktu homogenisasi juga tidak dapat dilihat pengaruhnya pada proses pembentukan suspensi jika hanya fisiknya yang diamati secara langsung.
SINTESIS NANOSELULOSA DARI TONGKOL JAGUNG
DENGAN PERLAKUAN HIDROLISIS KIMIA DAN
HOMOGENISASI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
NICHE EVANDANI
F24080050
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Sintesis Nanoselulosa dari Tongkol Jagung dengan Perlakuan Hidrolisis Kimia dan Homogenisasi
Nama : Niche Evandani
NIM : F24080050
Menyetujui, Pembimbing I,
(Dr. Ir. Hanifah Nuryani Lioe, M.Si) NIP 19680809 199702 2 001
Pembimbing II,
(Dr. Sri Yuliani, MT) NIP 19690701 199403 2 003
Mengetahui:
Ketua Departemen (Dr. Ir. Feri Kusnandar, M.Sc)
NIP 19680526 199309 2 004
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul Sintesis Nanoselulosa dari Tongkol Jagung dengan Perlakuan Hidrolisis Kimia dan Homogenisasi
adalah hasil karya saya sendiri dengan arahan Dosen Pembimbing Akademik, dan belum diajukan dalam bentuk apapun pada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, 25 September 2012 Yang membuat pernyataan
©Hak cipta milik Niche Evandani, tahun 2012 Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari Institut Pertanian Bogor dan Balai Besar Pengembangan dan Penelitian Pascapanen Pertanian Bogor, sebagian atau seluruhnya
RIWAYAT HIDUP
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Kuasa atas berkat dan rahmat-Nya sehingga penulis berhasil menyelesaikan skripsi ini. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar sarjana Teknologi Pangan pada Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor. Skripsi yang berjudul “Sintesis Nanoselulosa dari Tongkol Jagung dengan Perlakuan Hidrolisis Kimia dan Homogenisasi” ini disusun berdasarkan magang penelitian yang dilakukan di Balai Besar Penelitian dan Pengembangan Pascapanen Bogor.
Selama kegiatan perkuliahan, magang penelitian, penulisan dan penyusunan skripsi ini tidak terlepas dari bantuan berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih yang mendalam kepada :
1. Keluarga terkasih : Yohanes Sugandi dan Erlianna Purba selaku orang tua, Nicho Afiandi dan Nichi Firani yang selalu memberikan doa, kasih sayang dan dukungan moril maupun materi kepada penulis.
2. Ibu Dr.Ir Hanifah Nuryani Lioe, M.Si selaku dosen pembimbing akademik yang selalu bersedia meluangkan waktunya untuk membimbing dengan sabar, memberikan saran dan motivasi kepada penulis.
3. Ibu Sri Yuliani, MT selaku dosen pembimbing akademik kedua yang telah memberikan dana dan kesempatan kepada penulis untuk melakukan magang penelitian di Balai Besar Penelitian dan Pengembangan Pascapanen Bogor, juga atas kesediaan dan kesabarannya untuk membimbing, memberikan saran dan motivasi kepada penulis.
4. Bapak Dr. Ir. Feri Kusnandar, M.Sc selaku dosen penguji yang telah memberikan banyak saran dan masukan demi perbaikan skripsi ini.
5. Segenap dosen pengajar Departemen Ilmu dan Teknologi Pangan yang tidak bisa penulis sebutkan satu-persatu atas seluruh ilmu, masukan, dan bimbingan yang diberikan kepada penulis
6. Pak Tri, Pak Danu, Pak Marman, Bu citra dan segenap staff serta teknisi Balai Besar Penelitian dan Pengembagan Pascapanen Pertanian Bogor atas bantuan, saran dan motivasi yang diberikan selama penulis melakukan kegiatan magang penelitian.
7. Keluarga besar Yayasan Goodwill Internasional yang telah memberikan bantuan dana, ilmu, motivasi, dan pengalaman berharga selama penulis mengikuti kegiatan Goodwill Leadership Training.
8. Sahabat satu bimbingan Fitrina dan Kornelia atas kesediannya berbagi pikiran, semangat dan motivasi yang diberikan kepada penulis.
9. Ferdi, Mumun,Uni, Tiur, Yuli, Dea, Stefani dan Jessyln yang selalu membuat hari-hari penuh dengan canda tawa dan semangat.
10. Keluarga besar ITP 45 atas kebersamaan dan kekeluargaan, serta berbagai pengalaman berharga yang membuat saat-saat perkuliahan menjadi begitu berkesan.
11. Para Staf UPT ITP : Bu Novi, Mbak Anie, Mbak Darsi. Terima kasih atas bantuan dan kesabarannya dalam mengurus masalah administrasi penulis.
Penulis meyakini bahwa masih banyak pihak-pihak yang belum disebutkan. Oleh karena itu, penulis mengucapkan terima kasih banyak kepada semua pihak yang telah banyak membantu. Penulis juga menyadari bahwa skripsi ini masih banyak kekurangan, sehingga penulis sangat mengharapkan kritik dan saran yang membangun dari berbagai pihak demi memperbaiki penulisan skripsi ini. Akhir kata, semoga skripsi ini bisa bermanfaat dan berguna bagi semua pihak. Terima kasih.
Bogor, September 2012
DAFTAR ISI
Halaman
RINGKASAN ... iii
RIWAYAT HIDUP ... ix
KATA PENGANTAR ... x
DAFTAR ISI ... xii
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
I. PENDAHULUAN A. Latar Belakang ... 1
B. Tujuan Penelitian ... 2
C. Manfaat Penelitian ... 2
II. TINJAUAN PUSTAKA ... 3
A. Nanoteknologi ... 3
B. Limbah Lignoselulosa... 4
C. Selulosa ... 5
D. Hemiselulosa... 6
E. Lignin ... 7
F. Nanoselulosa ... 8
G. Metode Sintesis Nanoselulosa ... 9
III. BAHAN DAN METODOLOGI PENELITIAN A. Bahan dan Alat ... 11
B. Metodologi Penelitian ... 11
1. Persiapan Bahan Baku ... 11
2. Penelitian Pendahuluan ... 11
3. Penelitian Utama... 14
a. Sintesis Nanoselulosa ... 14
b. Analisis Kimia ... 16
1. Analisis Kadar Air ... 16
2. Analisis Kadar Abu ... 16
3. Analisis Kadar Protein ... 16
4. Analisis Kadar Lemak ... 17
5. Analisis Kadar Karbohidrat (by difference) ... 17
6. Analisis Kadar ADF ... 17
7. Analisis Kadar Selulosa ... 18
8. Analisis Kadar Lignin ... 18
c. Karakterisasi Produk Akhir Sintesis Nanoselulosa ... 19
1. Karakterisasi Kimia Produk ... 19
2. Karakterisasi Fisik Produk ... 19
3. Karakterisasi Mikrostruktural Produk Akhir Sintesis Nanoselulosa ... 20
3.1 Karakterisasi Mikrostruktural dengan Mikroskop Cahaya ... 20
3.2 Karaktererisasi Mikrostruktural dengan Scanning Electron Microscope (SEM) ... 20
d. Analisis Statistik ... 21
IV. HASIL DAN PEMBAHASAN ... 22
A. Penelitian Pendahuluan ... 22
B. Penelitian Utama ... 25
1. Komposisi Kimia Tepung Tongkol Jagung ... 25
2. Karakterisasi Kimia Produk Akhir Sintesis Nanoselulosa ... 26
3. Karakterisasi Fisik Produk Akhir Sintesis Nanoselulosa ... 28
a. Parameter Warna ... 28
b. Parameter Pembentukan Suspensi ... 29
4. Karakterisasi Mikrostruktural Produk Akhir Sintesis Nanoselulosa ... 31
a. Karakterisasi Mikrostruktural dengan Mikroskop Cahaya ... 31
b. Karakterisasi Mikrostruktural dengan Scanning Electron Microscope ... 32
V. SIMPULAN DAN SARAN ... 36
VI. DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Tabel 1. Aplikasi nanoteknologi dalam pengemasan ... 3
Tabel 2. Aplikasi nanoteknologi dalam bidang pangan ... 4
Tabel 3. Komposisi kimia limbah jagung ... 5
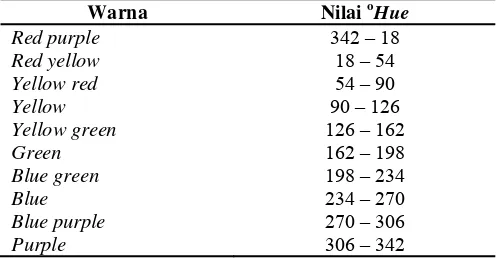
Tabel 4. Warna sampel berdasarkan nilai Hue ... 19
Tabel 5. Komposisi kimia tepung tongkol jagung ... 25
DAFTAR GAMBAR
Gambar 1. Ilustrasi susunan komponen dinding sel tanaman ... 6
Gambar 2.Struktur hemiselulosa ... 7
Gambar 3. Struktur lignin... 7
Gambar 4. Nanoselulosa dari ampas tebu ... 8
Gambar 5. Nanoselulosa dari daun nanas ... 9
Gambar 6. Diagram alir metode trial-error I ... 12
Gambar 7. Diagram alir metode trial-error II ... 13
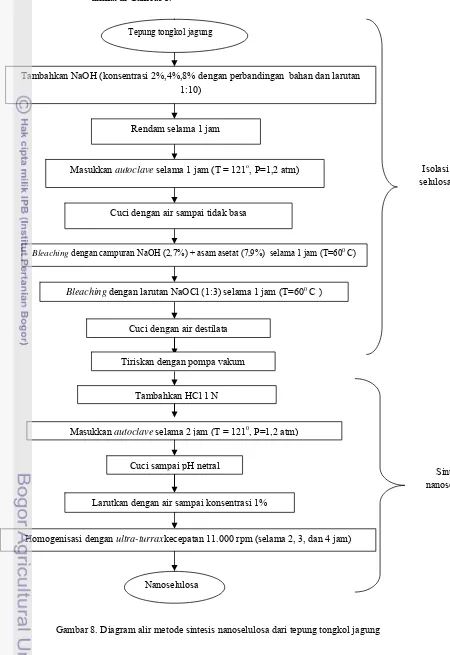
Gambar 8. Diagram alir merode sintesis nanoselulosa dari tepung tongkol jagung ... 15
Gambar 9. Bahan baku dan bahan setengah jadi dalam proses sintesis nanoselulosa dari tepung tongkol jagung ... 22
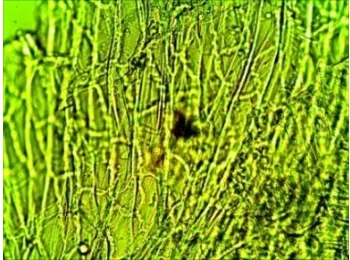
Gambar 10. Tepung tongkol jagung pada perbesaran 400 kali dengan menggunakan mikroskop cahaya ... 23
Gambar 11. Selulosa pada produk akhir trial-error I sintesis nanoselulosa pada perbesaran 400 kali dengan mikroskop cahaya ... 23
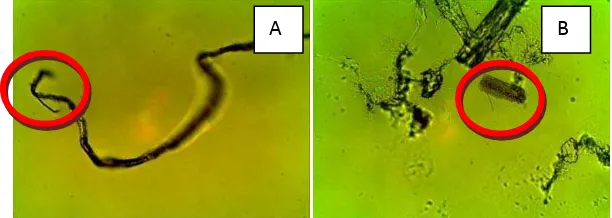
Gambar 12. Selulosa pada produk akhir trial-error II sintesis nanoselulosa pada perbesaran 400 kali dengan menggunakan mikroskop cahaya ... 24
Gambar 13. Selulosa pada produk akhir trial-error II sintesis nanoselulosa pada perbesaran 100 kali dengan menggunakan mikroskop cahaya ... 24
Gambar 14. Grafik batang perbandingan kadar selulosa dan lignin antar produk akhir dengan berbagai perlakuan konsentrasi NaOH ... 26
Gambar 15. Perbandingan warna produk akhir sintesis nanoselulosa ... 28
Gambar 16. Perbandingan pembentukan suspensi pada produk akhir sintesis nanoselulosa ... 29
Gambar 17. Selulosa pada produk akhir sintesis nanoselulosa pada perbesaran 400 kali dengan menggunakan mikroskop cahaya ... 31
Gambar 18. Selulosa pada produk akhir sintesis nanoselulosa dengan konsentrasi NaOH 2% dan waktu homogenisasi 4 jam ... 32
Gambar 19. Selulosa pada produk akhir sintesis nanoselulosa dengan konsentrasi NaOH 4% dan waktu homogenisasi 4 jam ... 33
DAFTAR LAMPIRAN
Lampiran 1. Hasil analisis kimia tepung tongkol jagung ... 42
Lampiran 2. Hasil pengukuran warna produk akhir dengan Chromatometer Minolta 300 ... 43
Lampiran 3. Hasil analisis ragam dan uji Duncan atribut warna produk akhir sintesis nanoselulosa . 46 Lampiran 4. Hasil analisis ADF, selulosa dan lignin produk akhir sintesis nanoselulosa ... 48
Lampiran 5. Hasil analisis ragam selulosa produk akhir sintesis nanoselulosa ... 49
Lampiran 6. Hasil analisis ragam lignin produk akhir sintesis nanoselulosa ... 50
Lampiran 7. Gambar instrumen Scanning Electron Microscope ... 51
Lampiran 8. Gambar Ion Coater ... 51
Lampiran 9. Gambar sampel yang telah dipreparasi dan dilapis dengan emas sebelum diamati dengan Scanning Electron Microscope (SEM) ... 52
I. PENDAHULUAN
A.
Latar Belakang
Nanoteknologi dianggap sebagai sebuah evolusi dari ilmu pengetahuan karena memberikan banyak keuntungan dan kemudahan. Menurut Sekhon (2010), nanoteknologi adalah teknologi yang melibatkan atom dan molekul dengan ukuran lebih kecil dari 100 nanometer, namun beberapa pakar mengusulkan pelebaran skala dari 100 nm menjadi 300 nm sehingga yang disebut nanoteknologi adalah benda yang ukuran materialnya kurang dari 300 nm (Winarno dan Fernandez 2010). Nanoteknologi telah banyak dikembangkan dalam berbagai macam industri termasuk industri pangan. Dalam bidang pangan nanoteknologi bisa digunakan untuk pengembangan kemasan pangan, nanoenkapsulasi, nanoemulsi, nanopartikel dan sebagainya (Sekhon 2010).
Nanoteknologi memiliki potensial besar untuk menghasilkan kemasan baru. Salah satu aplikasinya adalah nanokomposit pada kemasan. Nanokomposit dapat dilakukan dengan cara menyisipkan partikel nano (nanofiller) ke dalam matriks. Nanopartikel yang biasa digunakan untuk nanokomposit diantaranya adalah carbon nanotube, selulosa, silika, dan kitin (Azeredo 2009). Nanokomposit umumnya digunakan untuk memperbaiki sifat mekanik dan kemampuan perlindungan (barrier properties) kemasan (Azeredo 2009).
Selulosa merupakan salah satu polimer alam yang paling banyak dimanfatkan dalam industri, dengan bantuan teknologi nano selulosa dapat ditingkatkan kualitasnya menjadi produk yang bernilai ekonomi tinggi, yaitu nanoselulosa. Nanoselulosa merupakan selulosa berukuran nano yang memiliki sifat-sifat khas seperti sangat kuat, rasio permukaan terhadap volume yang besar, kemampuan mengikat air yang tinggi, kekuatan tarik yang tinggi, jaringan yang halus, dan sangat porous. Sifat-sifat tersebut membuat nanoselulosa menjadi bahan yang sangat menjanjikan untuk industri komposit, kemasan pangan, bahan otomotif, pulp dan kertas dan sebagainya (Subyakto et al. 2009). Nanoselulosa tersebut biasa disintesis dari tanaman yang banyak mengandung serat.
Terdapat banyak bahan baku di alam yang memiliki potensi tinggi sebagai sumber serat dari tumbuhan non-kayu, misalnya sisal, kapas dan flax (Akin 2011). Selain tumbuhan non-kayu, limbah pertanian juga memiliki potensi yang tinggi sebagai sumber serat. Tongkol jagung, jerami, sekam, dedaunan, dan kulit kacang-kacangan merupakan limbah pertanian yang memiliki potensi tinggi untuk dimanfatkan kembali menjadi produk baru bernilai ekonomi tinggi. Limbah-limbah pertanian tersebut tergolong ke dalam limbah lignoselulosa. Limbah lignoselulosa adalah limbah yang mengandung selulosa, hemiselulola dan lignin (Richana dan Suarni 2004).
pada tahun 2011 mencapai 17,39 ton pipilan kering (BPS 2011). Seiring dengan kebutuhan jagung yang cukup tinggi, maka akan bertambah pula limbah yang dihasilkan dari industri pangan dan pakan berbahan baku jagung. Pemanfaatan limbah merupakan salah satu alternatif untuk menaikkan nilai ekonomi dari limbah tersebut,untuk itulah dalam penelitian ini limbah pertanian tongkol jagung akan dimanfaatkan menjadi bahan sumber sintesis nanoselulosa sehingga dapat bermanfaat bagi peningkatan nilai tambah limbah pertanian.
Terdapat beberapa penelitian sebelumnya yang telah dilakukan untuk mengisolasi selulosa dan sintesis nanoselulosa dari limbah pertanian dengan berbagai macam metode. Limbah pertanian yang banyak digunakan adalah jerami (Khaushik dan Sigh 2011 ), daun pisang (Cherian et al. 2008), dan daun nanas (Cherian et al. 2010). Dari beberapa penelitian tersebut diketahui bahwa metode kimia-mekanik terbukti efektif untuk mengisolasi selulosa dan mereduksi ukurannya menjadi nanoselulosa. Prinsip dari proses sintesis nanoselulosa adalah isolasi selulosa dengan cara menghidrolisis hemiselulosa dan mendelignifikasi lignin dengan larutan basa (NaOH atau KOH), proses bleaching, menguraikan fibril-fibril selulosa yang masih menyatu dalam bentuk mikrofibril selulosa dengan hidrolisis asam (HCl atau H2SO4), dan bantuan perlakuan
mekanik, contohnya homogenisasi (Cherian et al. 2010) . Konsentrasi NaOH yang digunakan termasuk faktor penting karena sangat berpengaruh terhadap jumlah selulosa yang berhasil diisolasi, begitu juga dengan proses homogenisasi yang mempengaruhi proses reduksi ukuran selulosa menjadi nanoselulosa. Oleh karena itu, tujuan dari penelitian ini adalah menentukan konsentrasi NaOH dan proses homogenisasi yang terbaik untuk sintesis nanoselulosa dari tongkol jagung dengan perlakuan hidrolisis kimia dan homogenisasi.
B.
Tujuan Penelitian
Tujuan umum dari penelitian ini adalah sintesis nanoselulosa dari tongkol jagung dengan menggunakan perlakuan hidrolisis kimia dan homogenisasi. Adapun tujuan khusus dari penelitian ini antara lain :
1. Menentukan konsentrasi bahan penghidrolisis yang terbaik untuk proses sintesis nanoselulosa.
2. Menentukan perlakuan mekanik yang terbaik untuk proses sintesis nanoselulosa 3. Karakterisasi kimia, fisik, dan mikrostruktural produk akhir sintesis nanoselulosa.
C.
Manfaat Penelitian
II. TINJAUAN PUSTAKA
A.
Nanoteknologi
Kata nano berarti benda-benda yang berukuran sangat kecil dengan ukuran sepermiliar meter (10-9 m) (Winarno dan Fernandez 2010). Menurut Sekhon (2010), nanoteknologi adalah teknologi yang melibatkan atom dan molekul dengan ukuran lebih kecil dari 100 nanometer, namun beberapa pakar mengusulkan pelebaran skala dari 100 nm menjadi 300 nm sehingga yang disebut nanoteknologi adalah benda yang ukuran materialnya kurang dari 300 nm (Winarno dan Fernandez 2010). Adapun Winarno dan Fernandez (2010) mendefinisikan nanoteknologi sebagai kegiatan yang meliputidesign, produksi dan pemanfaatan struktur, peralatan sistem dan material dengan cara pengendalian ukuran dan bentuk material pada skala atom dan molekul.
Nanoteknologi dianggap sebagai sebuah evolusi dari ilmu pengetahuan karena memberikan banyak keuntungan dan kemudahan. Wacana nanoteknologi telah masuk ke Indonesia pada awal tahun 2000 dan telah banyak dikembangkan sejak 3 tahun ke belakang. Nanoteknologi telah banyak dikembangkan dalam berbagai macam industri termasuk industri pangan, dalam bidang pangan nanoteknologi bisa digunakan untuk pengembangan kemasan pangan, nanoenkapsulasi, nanoemulsi, nanopartikel dan sebagainya. Nanoteknologi yang diterapkan dalam proses pengolahan pangan disebut dengan nanofood (Winarno dan Fernandez 2010).Adapun aplikasi nanoteknologi dalam kemasan pangan dapat dilihat pada Tabel 1, sedangkan aplikasi nanoteknologi pada bidang pangan lainnya dapat dilihat pada Tabel 2.
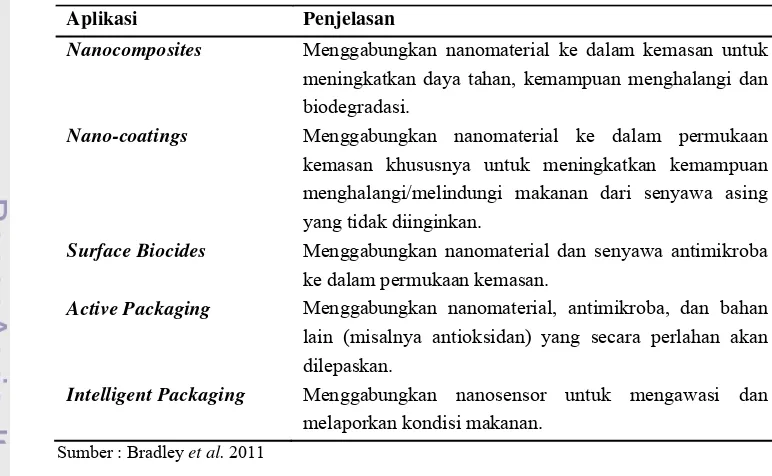
Tabel 1. Aplikasi nanoteknologi dalam pengemasan
Aplikasi Penjelasan
Nanocomposites Menggabungkan nanomaterial ke dalam kemasan untuk meningkatkan daya tahan, kemampuan menghalangi dan biodegradasi.
Nano-coatings Menggabungkan nanomaterial ke dalam permukaan kemasan khususnya untuk meningkatkan kemampuan menghalangi/melindungi makanan dari senyawa asing yang tidak diinginkan.
Surface Biocides Menggabungkan nanomaterial dan senyawa antimikroba ke dalam permukaan kemasan.
Active Packaging Menggabungkan nanomaterial, antimikroba, dan bahan lain (misalnya antioksidan) yang secara perlahan akan dilepaskan.
Intelligent Packaging Menggabungkan nanosensor untuk mengawasi dan melaporkan kondisi makanan.
Tabel 2. Aplikasi nanoteknologi dalam bidang pangan
No Sub-bidang Aplikasi
1 Pertanian • Molekul tunggal pendeteksi untuk menentukan interaksi enzim dan substrat
• Nanokapsul untuk mengirimkan pestisida, pupuk, dan bahan lainnya agar lebih efisien • Nanochips untuk identitas pelestarian
• Nanosensor untuk deteksi hewan dan tanaman patogen
• Nanokapsul untuk mengirimkan vaksin
• Nanopartikel untuk mengirimkan DNA ke tanaman (target rekayasa genetika)
2 Pengolahan pangan
• Nanoenkapsulasi flavor
• Nanotube dan nanopartikel sebagai penggumpal dan agen viskositas
• Nanoemulsi dan partikel untuk ketersediaan dan penyerapan nutrisi yang lebih baik
3 Suplemen • Tepung berukuran nano untuk meningkatkan absors dari nutrisi
• Nanokristal selulosa sebagai pengangkut obat • Vitamin dalam bentuk spary yang
menyebarluaskan molekul dalam nanodroplet untuk penyerapan lebih baik.
Sumber : Winarno dan Fernandez (2010)
B.
Limbah Lignoselulosa
Limbah pada dasarnya adalah suatu bahan yang tidak dipergunakan kembali dan merupakan hasil dari aktivitas manusia atau proses-proses alam yang mempunyai nilai ekonomi sangat rendah. Tongkol jagung, jerami, dedaunan, dan kulit kacang-kacangan merupakan limbah pertanian yang memiliki potensi tinggi untuk dimanfatkan kembali menjadi produk baru bernilai ekonomi tinggi karena keberadaannya yang melimpah di Indonesia. Limbah-limbah pertanian tersebut tergolong ke dalam limbah lignoselulosa. Limbah lignoselulosa adalah limbah yang mengandung selulosa, hemiselulola dan lignin (Richana dan Suarni 2004).
sangat prospektif untuk dikembangkan. Di luar negeri telah dilakukan beberapa penelitian yang mencoba memanfaatkan jerami (Kaushik dan Sigh 2011), sekam (Johar et al.2012), dan kulit kacang kedelai(Alemdar dan Sain 2008) sebagai bahan baku untuk pembuatan nanoselulosa.
Jagung merupakan salah satu bahan makanan pokok yang paling banyak dikonsumsi oleh masyarakat Indonesia . Banyak daerah di Indonesia yang berbudaya mengkonsumsi jagung, antara lain Madura, Yogyakarta, Sulawesi Selatan, Maluku Utara, Nusa Tenggara Timur, dll. Produksi jagung di Indonesia pada tahun 2011 mencapai 17,39 ton pipilan kering (BPS 2011). Seiring dengan kebutuhan jagung yang cukup tinggi, maka akan bertambah pula limbah yang dihasilkan dari industri pangan dan pakan berbahan baku jagung.Tanaman jagung termasuk jenis tanaman pangan yang diketahui banyak mengandung serat kasar yang terdiri dari senyawa kompleks selulosa, hemiselulosa dan lignin. Komposisi kimia limbah jagung dapat dilihat pada Tabel 3.
Tabel 3. Komposisi Kimia Limbah Jagung
Komponen Tongkol Jagung
Air (%) 7.68
Serat (%) 38.99 (crude fiber)
Selulosa (%) 19.49
Xilan (%) 12.4
Lignin (%) 9.1
Sumber : Richana dan Suarni (2004)
C.
Selulosa
Selulosa merupakan polisakarida yang kandungannya paling tinggi dalam dinding sel tanaman. Struktur kimia selulosa berupa rantai yang tidak bercabang dan tersusun atas satuan -D-gluko-piranosa dengan ikatan glikosida 1,4. Analisis sinar-X membuktikan bahwa selulosa berupa rantai-rantai panjang sejajar yang terikat menjadi satu oleh ikatan hidrogen. Hal ini yang menyebabkan selulosa berbentuk serat-serat panjang (Sumardjo 2009). Struktur kimia selulosa terdiri dari unsur C, O, H yang membentuk rumus molekul (C6H10O5)n.
Selulosa terbagi ke dalam tiga jenis, yaitu α-selulosa, -selulosa, dan -selulosa berdasarkan derajat polimerisasi dan kelarutannya dalam larutan NaOH. α-selulosa adalah bagian selulosa yang tidak larut dalam larutan alkali kuat (NaOH). -selulosa adalah bagian selulosa yang larut dalam media alkali dan mengendap jika dinetralkan, sedangkan
-selulosa adalah bagian selulosa yang larut dalam alkali dan tetap larut jika larutan dinetralkan. α-selulosa tersebut biasa digunakan sebagai penentu atau penduga dari tingkat kemurnian selulosa(Sumada dkk 2011).
Gambar 1. Ilustrasi susunan komponen dinding sel tanaman
D.
Hemiselulosa
Hemiselulosa adalah polisakarida kedua terbanyak setelah selulosa. Selama ini hemiselulosa sudah dimanfaatkan oleh industri untuk memproduksi etanol, xylitol, dan 2,3-butanadiol. Hemiselulosa merupakan polimer karbohidrat yang heterogen dengan tulang punggung xylose yang menghubungkan glukosa, asam galaktosa dan manosa (Singh dan Harvey 2010). Polisakarida yang tergolong ke dalam hemiselulosa yaitu glukan (polimer dari monomer D-glukosa—C6H12O6), mannan (polimer dari manosa--
C6H12O6), galaktan (polimer dari galaktosa-- C6H12O6), arabinan (polmer dari arabinosa—
Pada dinding sel tanaman, hemiselulosa terdapat pada matriks di middle lamela dan berfungsi sebagai perekat antar serat/mikrofibril selulosa (seperti pada gambar 1). Hemiselulosa memiliki bobot molekul yang lebih rendah dibandingkan selulosa dan bersifat tidak tahan terhadap perlakuan panas. Tidak seperti selulosa, polisakarida hemiselulosa bersifat amorf dan strukturnya kurang bercabang, sehingga potensi kelarutannya sangat berbeda. Hemiselulosa tersebut dapat dipisahkan dari selulosa dengan alkali karena ikatannya lemah sehingga mudah dihidrolisis (Placket 2011). Struktur molekul hemiselulosa dan penyusunnya dapat dilihat pada Gambar 2.
Gambar 2. Struktur hemiselulosa
E.
Lignin
Lignin merupakan sebuah polimer yang tersusun atas unit-unit fenilpropana. Dalam dinding sel tanaman, lignin berfungsi sebagai perekat dan melapisiselulosa dan hemiselulosa (seperti pada gambar 1) . Lignin yang melindungi selulosadah hemiselulosa tersebut bersifat tahan terhadap hidrolisis karena adanya ikatan arialkil dan ikatan ester (Soeprijanto 2010). Menurut Akin (2010) lignin merupakan komponen pada dinding sel yang sangat mempengaruhi kekuatan dan kekerasan dinding sel, serta daya tahan terhadap serangan mikroba patogen.
Gambar 3. Struktur lignin
F.
Nanoselulosa
Nanoselulosa merupakan selulosa yang diameternya berukuran nano. Nanoselulosa berbeda dengan selulosa alami karena nanoselulosa memiliki sifat-sifat yang khas seperti sangat kuat, rasio permukaan terhadap volume yang besar, kemampuan mengikat air yang tinggi, kekuatan tarik yang tinggi, jaringan yang halus, dan sangat porous. Berdasarkan metode sintesisnya nanoselulosa digolongkan menjadi tiga yaitu, Microfibrillated Cellulose (MFC)/Nanofibrillated Cellulose (NFC), Nanocristalline Cellulose (NCC), dan Bacterial Nanocellulose (BNC) (Klemn et al. 2011). MFC atau NFC disintesis dari pulp kayu yang kemudian mengalami proses pre-treatment (enzimatik, kimia, atau mekanik) dan proses homogenisasi, NCC disintesis dari pulp kayu yang kemudian mengalami proses grinding, hidrolisis asam dan separasi, sedangkan BNC disintesis dari gula atau alkohol dengan menggunakan bantuan mikroba, contohnya Gluconacetobacter (Bouchard 2012). Ukuran diameter MFC atau NFC biasanya berkisar antara 5-60 nm dengan panjang beberapa mikrometer, ukuran diameter NCC biasanya berkisar 5-70 nm dengan panjang 100-250 nm, sedangkan ukuran diameter BNC biasanya berkisar 20-100 nm (Klemn 2011).
Gambar 4. Nanoselulosa dari ampas tebu (hasil pengamatan dengan Scanning Electron Microscope)
Sumber : Mandal dan Chakrabarty (2011)
Gambar 5.Nanoselulosa dari daun nanas (hasil pengamatan dengan Transimission Electron Microscope)
Sumber: Cherian et al.. (2010)
Nanoselulosa bisa dimanfaatkan di berbagai bidang seperti pada industri kertas, industri kemasan, industri pangan dan industri farmasi. Pada industri kertas nanoselulosa bisa dimanfatkan sebagai bahan penguat kertas. Pada industri kemasan nanoselulosa bisa dimanfaatkan sebagai bahan penguat kemasan. Pada industri pangan nanoselulosa bisa dimanfaatkan bahan pengental dan penstabil suspensi pangan, sedangkan pada industri farmasi nanoselulosa bisa dimanfaatkan sebagai bahan perban dan komponen pembentuk tablet obat (Klemn et al. 2011).
G.
Metode Sintesis Nanoselulosa
Bacterial nanocellulose ukuran diameternya sekitar 20-100 nm (Klemn et al. 2011). BNC biasanya diproduksi oleh Gluconacetobacteryang telah dikultivasi pada media fruktosa dengan suhu 30o C (Ghosh et al. 2010). Pada metode ini residu bakteri dan komponen lain pada media pertumbuhan dapat dihilangkan dengan dipanaskan kemudian dicuci dengan air.Adapun pada metode electro spinning, nanoselulosa diproduksi dengan menggunakan energi listrik yang memberikan tekanan tinggi ke larutan polimer yang dilewatkan pada sebuh lubang kecil sehingga terbentuk serabut-serabut tipis berukuran nano (Ghost et al. 2010).
Metode sintesis nanoselulosa dengan perlakuan mekanik biasanya membutuhkan energi yang tinggi. Prinsip dari metode ini adalah fibrilasi selulosa karena adanya gaya gesek dan tekanan yang sangat tinggi. Contoh perlakuan dari metode ini adalah fibrilasi dengan high shear homogenization, fibrilisasi dengan stone atau disc refiner maupun cryocrushing, sedangkan metode pada metode kimia nanoselulosa diproduksi dari Microcrystalline cellulose (MCC) yang diberi perlakuan asam dengan H2SO4 pada
konsentrasi sekitar 65%(Ghost 2010).
Metode bio-mekanik menggabungkan prinsip biologi dan mekanik untuk memproduksi nanoselulosa. Produksi nanoselulosa dengan perlakuan mekanik membutuhkan energi yang tinggi. Oleh karena itu, menurut Ghost (2010) sebagai alternatif untuk mengurangi energi dapat digunakan enzim unuk membantu proses degradasi hemiselulosa, lignin dan pektin yang terkandung dalam bahan baku . Enzim yang digunakan biasanya diisolasi dari fungi kelompok jamur busuk putih (white rot fungi) yang tergolong Basidiomicetes. Fungi tersebut menghasilkan enzim lignolitik yang dapat mendegradasi lignin. Enzim yang dapat mendegradasi lignin terdiri dari tiga jenis enzim, yaitu lignin peroksidase, mangan peroksidase dan lakase (Hattaka 2001). Serat yang telah diberi perlakuan dengan enzim selanjutnya akan diberi perlakuan kimia sepeti shear refining dan cryocrushing.
Metode kimia-mekanik menggabungkan prinsip kimia dan mekanik untuk memproduksi nanoselulosa. Perlakuan kimia yang dilakukan adalah hidrolisis dengan larutan basa (NaOH) yang diikuti hidrolisis dengan larutan asam (HCl) pada suhu diatas 80oC. Perlakuan kimia tersebut bertujuan untuk menghilangkan hemiselulosa, lignin dan pektin yang terkadung dalam bahan baku. Perlakuan mekanik yang dilakukan seperti homogenisasi atau cryocrushing pada serat yang telah mengalami perlakuan kimia sebelumnya. Adapun perlakuan mekanik ini bertujuan untuk memisahkan fibril-fibril selulosa yang masih saling berikatan sehingga dihasilkan nanoselulosa dengan diameter yang berukuran nano (Ghost et al. 2010).
III. METODOLOGI PENELITIAN
A.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah tongkol jagung hasil limbah pertanian. Bahan yang digunakan untuk sintesis nanoselulosa adalah natrium hidroksida (NaOH), asam asetat (CH3COOH), sodium hipoklorit, asam klorida (HCl) dan air
destilata. Bahan yang digunakan untuk analisis proksimat dan analisis kimia lainnya adalah asam sulfat (H2SO4), asam borat (H2BO3), asam klorida (HCl), K2SO4, heksana,
alkohol dan aseton.
Alat yang digunakan dalam penelitian ini adalah oven, timbangan analitik, autoclave, kertas saring, pH meter, pompa vakum, Scanning Electron Microscope (SEM) type JSM-5000 Japan, ultraturrax, mikroskop cahaya, ChromatometerMinolta 300 dan alat-alat laboratorium lainnya (gelas piala, gelas ukur, erlenmeyer, pipet,labu lemak dan sebagainya).
B.
Metode Penelitian
1. Persiapan Bahan Baku
Bahan baku yang digunakan dalam penelitian ini adalah tongkol jagung. Pada tahap persiapan bahan, tongkol jagung dikeringkan terlebih dahulu dengan oven bersuhu 720C selama 48 jam. Setelah mengalami proses pengeringan, tongkol jagung tersebut digiling dan diayak dengan saringan 100 mesh. Tepung tongkol jagung inilah yang nantinya akan digunakan sebagai bahan baku untuk sintesis nanoselulosa dari tongkol jagung dengan perlakuan hidrolisis kimia dan homogenisasi.
2.
Penelitian PendahuluanTepung tongkol jagung
Tambahkan 2% NaOH (perbandingan serat larutan 1:10)
Masukkan ke dalam autoclave selama 1 jam (T = 121oC, P=1,2 atm)
Gambar 6. Diagram alir metode trial-error I Tambahkan HCl 1 N
Tiriskan dengan pompa vakum Cuci dengan air destilata
Bleaching dengan campuran (NaOH 2,7 %+as.asetat 7,9%) kemudian NaOCl (1:3) (masing-masing selama 1 jam)
Cuci dengan air sampai tidak basa
Homogenisasi dengan ultra-turrax kecepatan 11.000 rpm selama 1 jam
Larutkan dengan air destilata Cuci sampai pH netral
Masukkan ke dalam autoclave selama 2 jam (T = 1210C, P=1,2 atm)
Isolasi selulosa
Sintesis nanoselulosa
Tepung tongkol jagung
Tambahkan 2% NaOH (perbandingan bahan dan larutan 1:10)
Masukkan ke dalam autoclave selama 1 jam (T = 121o C, P=1,2 atm)
Cuci dengan air sampai tidak basa
Bleaching dengan campuran (NaOH 2,7 %+as.asetat 7,9%) kemudian NaOCl (1:3) (masing-masing selama 1 jam)
Cuci dengan air destilata
Tiriskan dengan pompa vakum
Tambahkan HCl 1 N
Masukkan ke dalamautoclave selama 15 menit, lepaskan tekanannya tiba-tiba
Gambar 7. Diagram alir metode trial-error II
Homogenisasi dengan ultra-turrax kecepatan 16.000 rpm selama 3 jam
Larutkan dengan air destilata Cuci sampai pH netral
(T = 1210C, P=1,2 atm), ulangi 8 kali
Sintesis nanoselulosa
Isolasi selulosa
3.
Penelitian Utama
a. Sintesis Nanoselulosa
Metode yang digunakan untuk sintesis nanoselulosa adalah metode campuran perlakuan kimia dan mekanik (hidrolisis kimia dan homogenisasi). Metode ini merupakan modifikasi dari metode sebelumnya yang dilakukan pada proses trial and error I. Modifikasi yang dilakukan adalah menambah proses perendaman selama 1 jam dengan larutan penghidrolisis sebelum dimasukkan ke autoclave dan meningkatkan suhu proses bleaching (dari suhu ruang menjadi 60o C). Kedua hal tersebut dilakukan untuk mengoptimalkan proses hidrolisis hemiselulosa dan lignin dari bahan baku.
Secara garis besar terdapat empat tahapan perlakuan dalam sintesis nanoselulosa. Tahap pertama adalah perlakuan basa dengan menggunakan NaOH disertai pemanasan. Tahapan tersebut bertujuan untuk menghidrolisis hemiselulosa dan depolimerisasi lignin pada tepung tongkol jagung menjadi komponen gula dan fenolik yang larut air (Cherian et al. 2010). Pada penelitian ini digunakan 3 taraf konsentrasi NaOH, yaitu NaOH 2%, NaOH 4% dan NaOH 8%. Hal tersebut dilakukan untuk mengetahui konsentrasi larutan NaOH yang terbaik untuk mengisolasi selulosa tanpa mendegradasinya.
Tahap kedua adalah perlakuan bleachingdengan menggunakan campuran NaOH 2,7% dan asam asetat 7,9% kemudian dilanjutkan dengan NaOCl (1:3). Tahapan tersebut bertujuan untuk menghilangkan lignin yang masih tersisa. Lignin perlu dihilangkan dalam proses sintesis nanoselulosa karena lignin jika teroksidasi struktur aromatiknya akan menghasilkan senyawa kuinon berwarna coklat yang tidak diinginkan (Hattaka 2001). Selain itu, lignin juga perlu dihilangkan agar selulosa pada bahan baku lebih mudah diisolasi karena menghilangkan lignin yang menyelubungi selulosa. Tahap ketiga adalah perlakuan asam dengan menggunakan HCl 1 N disertai pemanasan. Tahapan tersebut bertujuan untuk membantu menguraikan fibril-fibril selulosa yang masih saling berikatan dalam bentuk mikrofibril selulosa. Sampel yang telah mengalami 3 tahapan tersebut akan diuji kadar selulosa dan lignin
Tahap keempat adalah homogenisasi, tahapan ini bertujuan untuk mereduksi ukuran lebih lanjut karena dengan adanya gaya gesek dan tekanan diharapkan mampu memutuskan ikatan hidrogen intramolekular antar fibril selulosa. Pada penelitian ini proses homogenisasi dilakukan dengan menggunakan alat ultraturrax pada kecepatan 11.000 rpm . Proses homogenisasi dilakukan dengan 3 taraf waktu homogenisasi, yaitu 2 jam, 3 jam dan 4 jam. Hal tersebut dilakukan untuk mengetahui waktu homogenisasi yang paling optimal untuk mereduksi ukuran fibril selulosa. Metode yang digunakan pada penelitian ini merupakan metode yang telah diadaptasi dari penelitian yang telah dilakukan Cherian et al. (2010) .
diagram alir metode sintesis nanoselulosa dari tepung tongkol jagung dapat dilihat di Gambar 8.
Tambahkan NaOH (konsentrasi 2%,4%,8% dengan perbandingan bahan dan larutan 1:10)
Masukkan autoclave selama 1 jam (T = 121o, P=1,2 atm)
Cuci dengan air sampai tidak basa
Bleaching dengan campuran NaOH (2,7%) + asam asetat (7,9%) selama 1 jam (T=600 C)
Tiriskan dengan pompa vakum Cuci dengan air destilata Tepung tongkol jagung
Rendam selama 1 jam
Isolasi selulosa
Bleaching dengan larutan NaOCl (1:3) selama 1 jam (T=600C )
Nanoselulosa
Homogenisasi dengan ultra-turraxkecepatan 11.000 rpm (selama 2, 3, dan 4 jam) Tambahkan HCl 1 N
Masukkan autoclaveselama 2 jam (T = 1210, P=1,2 atm)
Cuci sampai pH netral
Sintesis nanoselulosa
[image:31.595.94.544.108.763.2]Larutkan dengan air sampai konsentrasi 1%
b. Analisis Kimia
1. Analisis Kadar Air Metode Oven (SNI 01-2891-1992)
Kadar air ditentukan secara langsung dengan menggunakan metode oven pada suhu 105oC. Sampel sejumlah 1-2 gram ditimbang dan dimasukkan dalam cawan yang telah dikeringkan dan diketahui bobotnya. Kemudian contoh dan cawan dikeringkan dalam oven bersuhu 105oC selama 3 jam, lalu didinginkan dalam desikator dan ditimbang sampai diperoleh bobot tetap. Kadar air sampel dapat dihitung dengan menggunakan rumu sebagai berikut : s
% Keterangan :
a = bobot sampel sebelum dikeringkan (g) b = kehilangan bobot setelah dikeringkan (g)
2. Analisis Kadar Abu Metode Pengabuan Kering (SNI 01-2891-1992)
Cawan porselin kosong dikeringkan dalam oven bersuhu 105oC selama 15 menit, kemudian didinginkan dalam desikator dan ditimbang. Sampel sebanyak 2-3 gram dimasukkan dalam cawan dan ditimbang. Cawan berisi sampel dibakar sampai asapnya habis, kemudian dimasukkan ke dalam tanur listrik dengan suhu 550o C sampai pengabuan sempurna. Cawan berisi sampel dikeluarkan dari tanur, kemudian didingankan dalam desikator dan ditimbang sampai diperoleh bobot tetap. Kadar abu sampel dapat di dengan menggunakan rumus sebagai berikut :
hitung
% Keterangan :
a = bobot sampel sebelum diabukan (g)
b = bobot sampel + cawan sesudah diabukan (g) c = bobot cawan (g)
3. Analisis Kadar Protein Metode Kjeldahl (SNI 01-2891-1992)
Sampel sebanyak 0,51 gram dimasukkan ke dalam labu kjeldahl 100ml, kemudian tambahkan 2 gram campuran Selenium dan 25 ml H2SO4 pekat. Labu
, 4
Keterangan: w = bobot sampel
V1 = volume HCl 0,001 N yang digunakan untuk penitaran sampel
V2 = volume HCl yang digunakan untuk penitaran blanko
N = normalitas HCl
fk = faktor konversi untuk protein dan makanan secara umum (6,25) fp = faktor pengenceran
4. Analisis Kadar Lemak Metode Soxhlet (SNI 01-2891-1992)
Labu lemak yang akan digunakan dikeringkan dalam oven kemudian didinginkan dalam desikator dan ditimbang. Sebanyak 1-2 gram sampel dimasukkan ke dalam selongsong kertas saring yang dialasi dengan kapas. Sumbat selongsong kertas yang berisi sampel dikeringkan dalam oven pada suhu tidak lebih dari 80oC selama kurang lebih 1 jam, kemudian dimasukkan pada labu ekstraksi Soxhlet. Alat kondensor diletakkan di atasnya dan labu lemak diletakkan di bawahnya. Pelarut heksana dimasukkan dalam labu lemak secukupnya, selanjutnya dilakukan ekstraksi selama 6 jam sampai pelarut yang turun kembali ke labu berwarna jernih. Pelarut yang ada dalam labu lemak didestilasi dan pelarut ditampung kembali. Labu lemak yang berisi lemak hasil ekstraksi dipanaskan dalam oven suhu 105oC hingga mencapai berat tetap, kemudian didinginkan dalam desikator dan timbang. Kadar lemak sampel dapat dihitung dengan menggunakan rumus sebagai berikut;
% Keterangan:
a = bobot sampel (g)
b = bobot labu lemak + lemak hasil ekstraksi (g) c = bobot labu lemak kosong (g)
5. Analisis Kadar Karbohidrat By Difference
Kadar karbohidrat sampel dianalisis dengan menggunakan metode by difference. Kadar karbohidrat dihitung sebagai sisa dari kadar air, abu, protein dan lemak sampel. Kadar karbohidrat sampel dapat dihitung dengan rumus sebagai berikut :
Kadar Karbohidrat = 100-(kadar air + kadar abu +kadar protein +kadar lemak)
6. Analisis Kadar Acid Detergent Fiber (ADF)(AOAC 973.18 1990)
residu menggunakan air panas dan aceton. Keringkan pada oven 105° C selama ± 4 jam sampai beratnya stabil, angkat dan dinginkan dalam desikator. Setelah dingin, keluarkan cawan dari desikator dan timbang (c). Kadar ADF sampel dapat dihitung dengan menggunakan rumus sebagai berikut:
% ADF = x 100%
% Hemiselullosa = % NDF - % ADF
Keterangan : a = bobot sampel(g)
b = bobot cawan kaca masir (g)
c = bobot cawan+residu setelah dikeringkan (g)
7. Analisis Kadar Selulosa(AOAC 973.18 1990)
Analisa selulosa merupakan lanjutan dari analisa ADF. Sampel analisa ADF yang sudah ditimbang (c) ditambah larutan asam sulfat (H2SO4) 72% sampai
terendam selama 3 jam. Setelah 3 jam, residu dibilas menggunakan air panas dan aceton. Keringkan pada oven 105° C selama ± 4 jam sampai beratnya stabil, angkat dan dinginkan dalam desikator. Setelah dingin, keluarkan cawan dari desikator dan timbang (d). Kadar selulosa sampel dapat dihitung dengan menggunakan rumus sebagai berikut:
% Selulosa = x 100%
Keterangan: a = bobot sampel (g)
c = bobot cawan+sampel hasil analisis ADF (g) d = bobot cawan+residu akhir setelah dikeringkan (g)
8. Analisis Kadar Lignin((AOAC 973.18 1990)
Analisa lignin merupakan kelanjutan dari analisa ADF dan selulosa. Sampel yang sudah dikeringkan (d), selanjutnya dibakar dalam tanur dengan tempratur ± 600°C. Angkat dan dinginkan cawan dalam eksikator dan timbang (e). Besarnya kandungan lignin dihitung menggunakan persamaan sebagai berikut :
% Lignin =
x 100%
Keterangan : a = bobot sampel (g)
c. Karakterisasi Produk Akhir Sintesis Nanoselulosa
1. Karakterisasi Kimia Produk Akhir
Karakterisasi kimia dilakukan pada sampel yang telah mengalami proses hidrolisis basa, bleaching dan hidrolisis asam namun belum dilarutkan dalam air dan mengalami proses homogenisasi. Karakterisasi kimia yang dilakukan mencakup analisis kadar Acid Detergent Fiber (ADF), selulosa, dan lignin dengan metode Van Soest (untuk metode lengkapnya dapat dilihat pada sub bab analisis kimia).
2. Karakterisasi Fisik Produk Akhir
2.1 Parameter Warna
[image:35.595.184.432.507.636.2]Karakteristik warna produk akhir akan diukur dengan Chromatometer Minolta 300. Chromatometer adalah suatu alat analisis warna secara trimulus untuk mengukur warna yang dipantulkan oleh suatu permukaan. Sistem notasi warna yang digunakan pada penelitian ini adalah sistem notasi warna Hunter (L a b). Ilustrasi sistem notasi warna Hunter (L a b). Notasi L pada sistem hunter menyatakan cahaya pantul yang menghasilkan warna akromatik putih, abu-abu dan hitam Notasi L* : 0 menyatakan warna hitam dan L* : 100 menyatakan warna putih. Notasi a pada sistem hunter menyatakan warna kromatik campuran merah-hijau dengan nilai +a* (positif) dari 0 sampai +80 untuk warna merah, dan nilai –a* (negatif) dari 0 sampai -80 untuk warna hijau. Notasi b pada sistem Hunter menyatakan warna kromatik campuran biru-kuning dengan nilai +b* (positif) dari 0 sampai +70 untuk warna kuning, dan nilai –b*(negatif) dari 0 sampai -70 untuk warna biru (Hunter Lab 2008). Sementara itu nilai oHue menunjukkan warna dari sampel. Nilai oHue diperoleh dari perhitungan arc tan (b/a). Warna sampel berdasarkan nilai oHueditunjukkan pada Tabel 4.
Tabel 4. Warna sampel berdasarkan nilai oHue
Warna Nilai oHue
Red purple 342 – 18
Red yellow 18 – 54
Yellow red 54 – 90
Yellow 90 – 126
Yellow green 126 – 162
Green 162 – 198
Blue green 198 – 234
Blue 234 – 270
Blue purple 270 – 306
Purple 306 – 342
2.2Parameter Pembentukan Suspensi
Produk akhir yang telah mengalami keseluran proses kemudian akan diamati penampakan suspensinya secara kasat mata, apakah terdispersi sempurna atau terdapat fase lain yang mengendap. Penampakan suspensi produk akhir sintesis nanoselulosa merupakan sebuah sifat fisik yang cukup penting karena produk nanoselulosa dengan kualitas baik memiliki suspensi yang terdispersi sempurna.
3. Karakterisasi Mikrostruktural
3.1 Karakterisasi Mikrostruktural dengan Mikroskop Cahaya
Nanoselulosa yang dihasilkan diukur diameternya dengan menggunakan skala garis yang terdapat pada mikroskop cahaya. Skala pengukuran pada mikroskop terdapat 2 skala yaitu skala okuler dan skala objektif. Pada perbesaran 1000 kali, jarak antara dua garis terkecil memiliki nilai 0,1 μm dan pada perbesaran 400 kali, jarak antara dua garis terkecil memiliki nilai 0,25 μm.
3.2 Karakterisasi Mikrostruktural dengan Scanning Electron Microscope (SEM) Nanoselulosa yang dihasilkan diamati dengan SEM untuk dianalisis karakteristik mikrostrukturalnya dan untuk mengukur diameter nanoselulosa yang dihasilkan. Pada penelitian ini instrumen SEM yang digunakan adalah SEM tipe JSM-5000.
3.3 Preparasi Sampel
Preparasi sampel perlu dilakukan agar sampel dapat diamati dengan baik. Sampel yang akan diamati merupakan sampel cair, dan untuk mengamatinya diperlukan preparasi khusus. Preparasi sampel yang digunakan untuk sampel produk akhir sintesis nanoselulosa yaitu, teteskan saru droplet suspensi nanoselulosa ke atas stub yang telah dilapisi dengan cover glass, kemudian keringkan dalam oven vakum bersuhu 75o C selama kurang lebih 15 menit (Zhou 2012)
3.4 Pelapisan Sampel
Pelapisan (coating) sampel perlu dilakukan untuk memperbesar kontras antara preparat yang akan diamati dengan lingkungan sekitarnya. Pelapisan sampel dapat menggunakan logam mulia seperti emas. Proses coating dilakukan oleh alat yang bernama ion coater. Proses coating in dilakukan dalam keadaan vakum selama 20 menit.
3.5 Pengamatan Sampel
maka sampel akan mengeluarkan elektron baru yang akan diterima oleh detektor dan dikirim ke monitor (CRT). Diamater gambar pada sampel diukur dengan menggunakan software image type J version 3.7
d. Analisis Statistik
IV.HASIL DAN PEMBAHASAN
A.
Penelitian Pendahuluan
Pada penelitian pendahuluan dilakukan dua kali proses trial and error sintesis nanoselulosa dengan menggunakan metode hidrolisis kimia dan homogenisasi Secara garis besar terdapat empat tahapan perlakuan dalam medote sintesis nanoselulosa yang digunakan yaitu, hidrolisis basa, bleaching, hidrolisis asam dan homogenisasi.Melalui proses trial dan error akan dilihat faktor yang mempengaruhi sintesis nanoselulosa. Terdapat dua faktor yang telah diuji pengaruhnya, yaitu banyaknya siklus steam explosion serta waktu dan kecepatan homogenisasi. Alat yang digunakan untuk proses steam explosion adalah autoclave, sedangkan alat yang digunakan untuk proses homogenisasi adalah ultra-turrax.. Adapun penampakan bahan baku dan setengah jadi dalam proses sintesis nanoselulosa dapat dilihat pada Gambar 9.
A B C D
Gambar 9. Bahan baku dan bahan setengah jadi dalam proses sintesis nanoselulosa dari tepung tongkol jagung
Keterangan:
A: Tepung tongkol jagung
B: Tepung tongkol jagung setelah perlakuan basa C : Tepung tongkol jagung setelah bleaching D : Tepung tongkol jagung setelah perlakuan asam
Sampel yang telah mengalami proses hidrolisis kimia, bleaching, hidrolisis asam, dan homogenisasi kemudian diamati karakteristik mikrostrukturalnya dengan menggunakan mikroskop cahaya. Pengamatan dengan mikroskop cahaya dilakukan pada perbesaran 400 kali dan 1000 kali. Penampakan mikrostruktural tepung tongkol jagung dapat dilihat pada Gambar 10, penampakan mikrostruktural produk akhir trial and error I dapat dilihat pada Gambar 11, sedangkan penampakan mikrostruktural produk akhir trial and error II dapat dilihat pada Gambar 12 dan 13.
Gambar 10. Tepung tongkol jagung pada perbesaran 400 kali dengan menggunakan mikroskop cahaya
Gambar 11. Produk akhir trial and error I sintesis nanoselulosa pada perbesaran 400 kali dengan menggunakan mikroskop cahaya
B A
Gambar 12. Selulosa pada produk akhir trial and error II sintesis nanoselulosa pada perbesaran 400 kali dengan menggunakan mikroskop cahaya
Gambar 13. Selulosa pada produk akhir trial and error II sintesis nanoselulosa pada perbesaran 1000 kali dengan menggunakan mikroskop cahaya
B A
A B
Gambar 12 merupakan penampakan produk akhir trial-error II sintesis nanoselulosa pada perbesaran 400 kali dengan menggunakan mikroskop cahaya. Gambar 12A menunjukkan nanofibril selulosa dengan ukuran diameter yang sudah cukup kecil sekitar 300nm. Gambar 12B menujukkan campuran antara selulosa yang berdiameter kecil dan besar, lingkaran merah pada kedua gambar tersebut menunjukkan proses defibrillation mikrofibril selulosa menjadi nanofibril selulosa. Gambar 13 menunjukkan penampakan produk akhir trialerror II sintesis nanoselulosa pada perbesaran 1.000 kali dengan menggunakan mikroskop cahaya, gambar 13A menunjukkan nanoselulosa dengan diamater sekitar 200-250 nm, sedangkan gambar 13B menunjukkan nanofibril selulosa dengan diameter 250-350 nm. Produk akhir yang diinginkan dari penelitian ini adalah nanofibril selulosa dengan diameter sekitar 100-300 nm sehingga dapat disebut nanoselulosa (Winarno dan Fernandez 2010) . Oleh karena itu, dapat ditarik kesimpulan bahwa metode trial-error II lebih baik daripada metode trial-error I untuk mensintesis nanoselulosa.
B.
Penelitian Utama
Berdasarkan penelitian pendahuluan, dapat diambil kesimpulan bahwa metode hidrolisis kimia dan homogenisasi telah mampu mengisolasi selulosa dengan diameter dibawah 500 nm, namun masih dalam jumlah yang relatif sedikit. Selain itu, diketahui juga bahwa waktu dan kecepatan homogenisasi mempengaruhi proses sintesis nanoselulosa, semakin tinggi kecepatan dan semakin lama waktu homogenisasi maka akan semakin baik proses reduksi ukuran selulosa. Oleh karena itu, pada penelitian utama akan digunakan metode hidrolisis kimia dan homogenisasi dengan proses homogenisasi pada kecepatan 11000 rpm pada tiga taraf waktu (2 jam, 3 jam dan 4 jam). Pada penelitian utama ini tidak dilalukan homogenisasi pada kecepatan 16000 rpm karena kemampuan alat yang digunakan (ultra-turrax) tidak mencukupi.
Pada penelitian utama juga akan dilakukan beberapa modifikasi pada metode hidrolisis kimia dan homogenisasi, yaitu adanya proses perendaman selama 1 jam sebelum hidrolisis basa pada suhu tinggi dan peningkatan suhu pada proses bleaching (dari suhu ruang menjadi 60o C), tahapan jelasnya dapat dilihat pada Gambar 6. Modifikasi tersebut dilakukan untuk mengoptimalkan proses sintesis nanoselulosa.
1.
Komposisi Kimia Tepung Tongkol Jagung
Parameter bahan baku (tepung tongkol jagung) yang diukur pada penelitian ini adalah kadar air, kadar abu, kadar lemak, kadar protein, kadar karbohidrat (by difference), kadar selulosa, dan kadar lignin. Kadar selulosa dan lignin bahan baku merupakan salah satu parameter penting untuk proses sintesis nanoselulosa. Bahan baku yang baik untuk proses sintesis nanoselulosa memiliki kandungan selulosa yang tinggi dan lignin yang rendah. Rata-rata limbah pertanian yang digunakan untuk sebagai bahan baku sintesis nanoselulosa memliki kadar selulosa diatas 30% dan lignin dibawah 25%, misalnya sekam dengan kadar selulosa 35% dan kadar lignin 23% (Johar et al. 2012), jerami dengan kadar selulosa 43,2 % dan kadar lignin 22%, serta kulit kedelai dengan kadar selulosa 56,4% dan kadar lignin 18% (Alemdar dan Sain 2008).Komposisi kimia tepung tongkol jagung yang digunakan pada penelitian ini dapat dilihat pada Tabel 5.
Tabel 5. Komposisi kimia tepung tongkol jagung
No Parameter % bb % bk
1 Kadar Air 8,19 8,94
2 Kadar Abu 2,22 2,42
3 Kadar Lemak 4,46 4,86
4 Kadar Protein 0,52 0,57
5 Kadar Karbohidrat (by difference) 84,61 83,21
• Kadar Selulosa 52,73 57,38
Tongkol jagung yang digunakan sebagai bahan baku cenderung memiliki kadar air yang rendah, sehingga tidak mudah ditumbuhi oleh jamur. Selain itu karakteristik tongkol jagung yang digunakan cenderung memiliki kadar lemak yang tinggi (4,46 % bb) dan kadar protein yang rendah (0,52%bb), bila dibandingkan dengan penelitian yang dilakukan Venty (2009). Pada penelitian yang dilakukan Venty (2009) tongkol jagung yang digunakan memiliki kadar lemak sebesar 0,7 % bb dan kadar protein sebesar 3,2 %BB.
Tongkol jagung yang digunakan sebagai bahan baku karakteristiknya cenderung memilki kadar selulosa yang tinggi (52,73 %bb) bila dibandingkan dengan tongkol jagung yang digunakan pada penelitian Shofiyanto (2008). Tongkol jagung yang digunakan pada penelitian Shofiyanto (2008) kadar selulosanya hanya 41 %bb. Kadar selulosa yang tinggi pada tongkol jagung menunjukkan bahwa tongkol jagung memiliki potensial yang tinggi sebagai bahan baku untuk sintesis nanoselulosa.
2.
Karakterisasi Kimia Produk Akhir Sintesis Nanoselulosa
Karakterisasi kimia dilakukan pada sampel yang telah mengalami proses hidrolisis basa,bleaching, dan hidrolisis asam, namun belum dilarutkan dalam air dan mengalami proses homogenisasi. Dari total 18 sampel yang ada, masing-masing diambil secara acak 2 sampel dengan 3 perlakuan yang berbeda (konsentrasi NaOH 2%, konsentrasi NaOH 4%, dan konsentrasi NaOH 8%) untuk dianalisis kadar selulosa dan lignin. Kadar selulosa dan lignin merupakan salah satu parameter yang penting untuk mengetahui kualitas nanoselulosa yang dihasilkan. Produk akhir sintesis nanoselulosa yang baik memiliki kadar selulosa yang tinggi dan kadar lignin yang rendah. Adapun grafik batang perbandingan kadar selulosa dan lignin antar produk akhir dengan berbagai perlakuan konsentrasi NaOH dapat dilihat pada Gambar 14.
0.00 10.00 20.00 30.00 40.00 50.00 60.00 70.00 80.00
0 2 4 8
57.38 77.17 59.96 54.75 9.88 6.32 19.21 3.72 Kadar sel u lo sa dan li gni n
Konsentrasi NaOH (%)
%Selulosa(BK) %Lignin(BK) (b) (b) (a) (a) (b) (b)
Keterangan :
• Konsentrasi NaOH 0% = bahan baku
• Angka yang diikuti oleh huruf yang berbeda menunjukkan berbeda nyata berdasarkan uji DMRT 5%
Berdasarkan analisis statistik pada taraf signifikasi 95% diketahui bahwa perlakuan hidrolisis basa dengan NaOH 4% dan NaOH 8% tidak memberikan pengaruh yang berbeda nyata terhadap kadar selulosa pada produk akhir, sedangkan perlakuan hidrolisis basa dengan NaOH 2% memberikan pengaruh yang berbeda nyata dengan perlakuan NaOH 4% dan 8% terhadap kadar selulosa pada produk akhir. Hasil penelitian menunjukkan bahwa produk akhir dengan perlakuan NaOH 2% memiliki kadar selulosa yang paling tinggi, yaitu 77,17%, produk akhir dengan perlakuan NaOH 4% memiliki kadar selulosa 59,96%, dan sampel dengan perlakuan NaOH 8 % memiliki kadar selulosa yang paling rendah , yaitu 54, 75%. Data tersebut menunjukkan bahwa dengan metode yang digunakan konsentrasi NaOH yang terbaik untuk mengisolasi selulosa adalah 2%.
Cherian et al. (2010) menyatakan bahwa konsentrasi larutan alkali sebagai bahan penghidrolisis harus sangat terkontrol agar tidak mendegradasi senyawa selulosa. Berdasarkan penelitian yang dilakukan Cherian et al. (2010) untuk mengisolasi selulosa dari daun nanas juga didapatkan hasil bahwa konsentrasi NaOH yang terbaik untuk mengisolasi selulosa tanpa mendegradasinya adalah 2 %. Hal ini terjadi karena hidrolisis basa dengan NaOH pada suhu dan tekanan tinggi dapat memutuskan ikatan hidrogen intramolekular selulosa pada posisi C-3 dan C-6 glucopyranosesehingga selulosa terpecah menjadi komponen gula yang lebih sederhana (Cherian et al. 2010).
Kadar selulosa yang berhasil diisolasi pada penelitian ini hampir sama dengan kadar selulosa yang berhasil diisolasi pada penelitian yang dilakukan oleh Kaushik dan Singh (2010). Pada penelitian yang dilakukan Kaushik dan Singh (2010) selulosa diisolasi dari jerami gandum dengan menggunakan metode steam explosion dan high shear homogenization. Kaushik dan Sigh menggunakan NaOH 2% (untuk perendamanan bahan baku selama satu malam) dilanjutkan NaOH 10%dalam proses hidrolisis basa. Dari penelitian tersebut berhasil diisolasi selulosa sebanyak 75,28%.
3.
Karakterisasi Fisik Produk Akhir Sintesis Nanoselulosa
a. Parameter Warna
Mutu suatu produk sering kali dapat dinilai melalui karakteristik warna yang dimilikinya.Produk nanoselulosa yang baik memiliki warna yang cerah (mendekati putih). Penampakan produk akhir sintesis nanoselulosa antar perlakuan dapat dilihat pada gambar 15. Produk akhir tersebut akan dianalisis parameter warnanya dengan menggunakan sistem notasi Hunter (L a b).
[image:44.595.267.430.232.354.2]A B C
Gambar 15. Perbandingan warna produk akhir sintesis nanoselulosa dengan berbagai
Keterangan:
A = produk akhir dengan perlakuan NaOH 2% B = produk akhir dengan perlakuan NaOH 4% C = produk akhir dengan perlakuan NaOH 8%
Hasil pengukuran parameter warna dengan ChromameterMinolta 300 akan dianalisis statistik dengan menggunakan software The SAS System for Windows 9.0. Selain nilai L a b, nilai Hue sampel juga akan dihitung untuk menunjukkan kategori warna sampel. Hasil pengukuran parameter warna produk akhir sintesis nanoselulosa dapat dilihat pada Tabel 6.
Tabel 6. Hasil pengukuran atribut warna produk akhir sintesis nanoselulosa
Parameter
Faktor
Konsentrasi NaOH 2% Konsentrasi NaOH 4% Konsentrasi NaOH 8% WH 2 WH 3 WH 4 WH 2 WH 3 WH 4 WH 2 WH 3 WH 4 L 32,35de 33,12de 31,73e 33,58cd 33,71cd 34,01bc 37,81a 35,27b 37,17a a 2,98ab 3.04ab 2,88bc 3,19a 3,05ab 2,73cd 2,88bc 2,73cd 2,59d b 0,19a 0,71a -0,51a -1,72b -1,83b -1,75b -4,15c -4,64c -3,95c Hue 84,37a 79,90a 76,89a 61,93b 59,10b 57,42b 33,24c 32,40c 30,23c Angka yang diikuti oleh huruf yang berbeda menunjukkan berbeda nyata berdasarkan uji DMRT 5%
Keterangan :
Melalui analisis statistik dengan Uji Duncan dapat dilihat bahwa perlakuan homogenisasi selama 2, 3, dan 4 jam pada konsentrasi NaOH 2% dan 4% tidak memberikan pengaruh yang berbeda nyata terhadap nilai L produk akhir. Berdasarkan tabel 5 dapat dilihat bahwa perlakuan dengan konsentrasi NaOH 8% pada waktu homogenisasi 2 jam memiliki nilai L yang paling tinggi, sedangkan perlakuan dengan NaOH 2% pada waktu homogenisasi 4 jam memiliki nilai L yang paling rendah.
Hasil penelitian menunjukkan semakin tinggi konsentrasi NaOH yang digunakan maka akan semakin cerah warna produk akhir yang dihasilkan. Jika dilihat pada gambar 15, produk akhir yang diberi perlakuan NaOH 8% berwarna putih kekuningan, sedangkan produk akhir yang diberi perlakuan NaOH 2% dan 4% berwarna kecoklatan. Menurut Hattaka (2001) warna coklat tersebut mengindikasikan kadar lignin yang masih cukup tinggi pada produk akhir karena lignin jika teroksidasi struktur aromatiknya akan menghasilkan senyawa kuinon berwarna coklat yang tidak diinginkan.
Berdasarkan hasil analisis statistik pada dengan uji Duncan dapat dilihat bahwa perlakuan homogenisasi tidak berpengaruh nyata terhadap nilai hue produk akhir, sedangkan perlakuan dengan konsentrasi NaOH yang berbeda berpengaruh nyata terhadap nilai hue produk akhir. Hasil penelitian menunjukkan bahwa produk akhir dengan perlakuan NaOH 2% dan 4% warnanya tergolong ke dalam yellow-red karena memiliki nilai hue dengan kisaran 54-90, sedangkan produk akhir dengan perlakuan NaOH 8% warnanya tergolong ke dalam red-yellow karena memiliki nilai hue dengan kisaran 18-54 (Hutching 1999).
b. Parameter Pembentukan Suspensi
Suspensi didefinisikan sebagaisistem dua fase dengan partikel padat yang terdispersi dalam fase kontinyu yang bisa berupa fase padat, cair, ataupun gas (Wasan 2008).Terbentuknya suspensi yang partikelnya terdispersi sempurna merupakan salah satu parameter yang penting dalam proses sintesis nanoselulosa. Produk nanoselulosa yang baik pada suspensi dibawah 5% akan membentuk suspensi yang terdispersi sempurna dan pada suspensi diatas 10 % akan membentuk gel (Cranston 2011). Gambar perbandingan pembentukkan suspensi pada produk akhir dengan perlakuan yang berbeda dapat dilihat pada Gambar 16.
[image:45.595.220.409.573.715.2]A B C
Keterangan :
A = produk akhir dengan perlakuan NaOH 2% B = produk akhir dengan perlakuan NaOH 4% C = produk akhir dengan perlakuan NaOH 8%
Hasil penelitian menunjukkan bahwa konsentrasi NaOH berpengaruh terhadap pembentukan suspensi produk akhir.Pada Gambar 16 dapat dilihat bahwa terdapat endapan pada suspensi produk akhir dengan perlakuan NaOH 2% dan 4%, sedangkan pada suspensi produk akhir dengan perlakuan NaOH 8% memiliki suspensi yang baik (fase padatnya terdispersi sempurna dalam fase cair). Hal ini terjadi karena stabilitas suspensi dipengaruhi oleh beberapa faktor seperti ukuran partikel, jumlah partikel dan sifat/muatan partikel (Pakki E 2007) .
Semakin kecil ukuran partikel maka akan semakin sulit partikel tersebut mengendap, hal ini berhubungan dengan luas penampang partikel terhadap daya tekan ke atas cairan dari suspensi tersebut. Hubungan antara ukuran partikel merupakan perbandingan terbalik dengan luas penampangnya, sehingga semakin kecil ukuran pastikel akan semakin besar luas penampangnya sehingga akan semakin memperlambat gerakan partikel untuk mengendap(Particles Science Inc, 2009).
Stabilitas suspensi juga dipengaruhi oleh jumlah partikel karena semakin banyak partikel dalam sebuah suspensi maka partikel tersebut akan susah melakukan gerakan yang bebas sehingga sering terjadi benturan antar partikel yang menyebabkan terbentukknya endapan(Particles Science Inc, 2009). Produk akhir dengan perlakuan NaOH 2% dan 4% memiliki kadar selulosa dan lignin yang lebih tinggi dibandingkan produk akhir dengan perlakuan NaOH 8% sehingga jumlah partikelnya otomatis lebih banyak dan menyebabkan terbentuknya endapan, sedangkan produk akhir dengan perlakuan NaOH 8% kandungan selulosa dan ligninnya paling sedikit sehingga jumlah partikelnya pun jauh lebih sedikit dibandingkan produk akhir dengan perlakuan NaOH 2% dan 4%.Kadar lignin pada produk akhir juga mempengaruhi stabilitas suspensi karena lignin bersifat hidrofobiksedangkan fase cair yang digunakan untuk pembentukan suspensi adalah air destilata. Oleh karena itu, semakin tinggi kadar ligninnya maka akan semakin sulit terbentuk suspensi yang terdispersi sempurna.
4.
Karakterisasi Mikrostruktural Produk Akhir Sintesis
Nanoselulosa
a. Karakterisasi Mikrostruktural dengan Mikroskop Cahaya
Pengamatan dengan menggunakan mikroskop cahaya dilakukan pada produk akhir . Pengamatan perlu dilakukan untuk mengetahui struktur selulosa yang dihasilkan pada produk akhir. Adapun hasil pengamatan produk akhir sintesis nanoselulosa dengan mikroskop cahaya dapat dilihat pada Gambar 17.
A B C
D E F
H I
G
Gambar17.Selulosa pada produk akhir sintesis nanoselulosa pada perbesaran 400 kali dengan menggunakan mikroskop cahaya
Keterangan gambar :
Berdasarkan hasil pengamatan terlihat bahwa setiap perlakuan telah berhasil memisahkan selulosa dari hemiselulosa dan lignin. Pada gambar 17F-I terlihat proses defibrillation mikrofibril selulosa menjadi nanofibril selulosa. Dari sembilan perlakuan jika diamati dengan mikroskop cahaya perbesaran 400 kali, ukuran diameter selulosanya tidak menunjukkan hasil yang terlalu berbeda, rata-rata diameter selulosa yang ada sekitar 500-1.000 nm. Selulosa yang teramati adalah selulosa yang berukuran besar karena keterbatasan alat yang digunakan, sehingga untuk mengetahui ukuran pastinya perlu dilakukan pengamatan mikrostruktural lebih lanjut dengan menggunakan Scanning Electron Microscope (SEM) pada perbesaran 10.000 kali.
b. Karakterisasi Mikrostruktural dengan Scanning Electron Microscope (SEM)
[image:48.595.159.533.399.667.2]Pengamatan dengan SEM dilakukan pada produk akhir yang telah mengalami proses preparasi dan coating dengan emas. Dari total 18 sampel yang ada masing-masing diamati dua sampel dengan perlakuan NaOH 2% waktu homogenisasi 4 jam, NaOH 4% waktu homogenisasi 4 jam dan NaOH 8% waktu homogenisasi 4 jam. Sampel dengan perlakuan homogenisasi 4 jam yang dianalisis dengan SEM karena diasumsikan semakin lama waktu homogenisasi maka semakin baik proses reduksi ukuran. Adapun hasil pengamatan produk akhir dengan menggunakan SEM dapat dilihat pada Gambar 18, Gambar 19, dan Gambar 20.
J K
L M
1μm 1μm
1μm 1μm
Gambar 18. Selulosa pada produk akhir sintesis nanoselulosa dengan perlakuan konsentrasi NaOH 2% dan waktu homogenisasi 4 jam
Keterangan gambar:
Diameter selulosa pada produk akhir diukur dengan menggunakan software image J ver 3.7. Berdasarkan hasil pengukuran didapatkan selulosa dengan diameter 186 nm dan 103 nm (dapat dilihat pada gambar 18 K) dan selulosa dengan diameter 88 nm dan 179 nm (dapat dilihat pada gambar 18 M). Pada gambar 18 J dan18 L terlihat masih banyak serat-serat yang berukuran besar. Pada gambar 18 K dan 18 M terlihat proses defibrillation mikrofibril selulosa menjadi nanofibril selulosa.
N O
1μm
P Q
[image:49.595.142.516.210.476.2]1μm 1μm 1μm
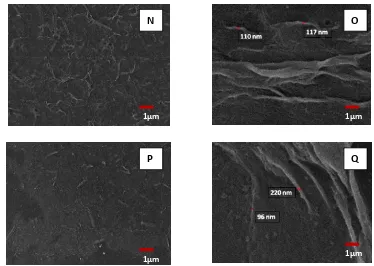
Gambar 19. Selulosa pada produk akhir sintesis nanoselulosa dengan perlakuan konsentrasi NaOH 4% dan waktu homogenisasi 4 jam
Keterangan gambar:
N dan P = perbesaran gambar 100 kali O dan Q = perbesaran gambar 10.000 kali
R S
T U
1μm 1μm
[image:50.595.134.523.82.354.2]1μm 1μm
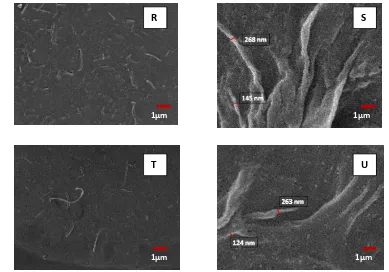
Gambar 20. Selulosa pada produk akhir sintesis nanoselulosa dengan perlakuan konsentrasi NaOH 8% dan waktu homogenisasi 4 jam
Keterangan gambar:
R dan T = perbesaran gambar 100 kali S dan U = perbesaran gambar 10.000 kali
Berdasarkan hasil pengukuran didapatkan selulosa dengan diameter 145 nm dan 268 nm (dapat dilihat pada gambar 20 S) dan selulosa dengan diameter 124 nm dan 263 nm (dapat dilihat pada gambar 20 U). Pada gambar 20 R dan 20 T terlihat masih banyak serat-serat yang berukuran besar. Pada gambar 20 S juga terlihat defibrillation mikrofibril selulosa menjadi nanofibril selulosa.
Secara keseluruhan berdasarkan hasil pengamatan dengan SEM dapat dilihat bahwa dengan metode hidrolisis kimia dan homogenisasi yang digunakan telah berhasil mensintesis selulosa dalam ukuran nano (di bawah 100 nm), namun masih dalam jumlah yang sedikit. Berdasarkan pengamatan dengan menggunakan SEM, dari keseluruhan sampel pada penelitian ini didapatkan nanoselulosa yang diameternya kisaran 80-270 nm.Hal ini terjadi karena perlakuan mekanik yang belum optimal untuk mereduksi ukuran (memisahkan fibril-fibril tunggal selulosa yang masih menyatu dalam mikrofibril selulosa), sehingga pada penelitian ke