PENINGKATAN PEROLEHAN LOGAM EMAS
MELALUI TEKNIK BIOOKSIDASI BAHAN TAMBANG
DENGAN MENGGUNAKAN
Acidithiobacillus
sp.
AZARIA INDRAWARDHANA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Peningkatan Perolehan Logam Emas Melalui Teknik Biooksidasi Bahan Tambang dengan Menggunakan Acidithiobacullus sp. adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
RINGKASAN
AZARIA INDRAWARDHANA. Peningkatan Perolehan Logam Emas Melalui Teknik Biooksidasi Bahan Tambang dengan Menggunakan Acidithiobacullus sp. Dibimbing oleh DWI ANDREAS SANTOSA dan SYAIFUL ANWAR.
Optimalisasi perolehan pada proses pengolahan mineral menjadi tantangan bagi seluruh Stakeholders. Dalam mengolah bijih, nilai perolehan emas yang dapat dilakukan oleh pabrik pengolahan di lokasi tambang rata-rata di bawah 80%. Rendahnya nilai perolehan pada pengolahan mineral berharga salah satunya disebabkan oleh karakteristik cadangan yang mengandung banyak ikatan sulfida (pirit). Alternatif solusi yang dapat dilakukan untuk menaikkan nilai perolehan adalah dengan cara menguraikan ikatan sulfida (pirit) melalui proses oksidasi dengan memanfaatkan bakteri pengoksidasi pirit yaitu Acidithiobacillus sp. Tujuan dari penelitian ini adalah: (i) mengkarakterisasi bijih tipe-D, (ii) menguji kemampuan bakteri Acidithiobacillus sp. untuk menurunkan kadar pirit di dalam bijih tipe-D, (iii) menguji kemampuan bakteri Acidithiobacillus sp.dalam meningkatkan perolehan emas dari bijih tipe-D.
Percobaan ini menggunakan Acidithiobacillus sp. yang diisolasi dari air asam tambang di wilayah penambangan emas terbesar di Indonesia yang berada di Kabupaten Mimika, Provinsi Papua dan Acidithiobacillus ferooxidans koleksi kultur Indonesian Center for Biodiversity and Biotechnology (ICBB-CC) yang diuji pada 2 jenis bijih Tipe-D 3445 dan 3625. Penelitian ini dilakukan dalam 3 bagian yaitu: (i) karakterisasi bijih tipe-D dengan menggunakan metode Analisa Butir Mineral, X-ray diffraction test, Fire assay dan Flotation test, (ii) menguji kemampuan Acidithiobacillus sp. dan Acidithiobacillus ferrooxidans mengurangi kandungan pirit yang terdapat dalam bijih Tipe-D 3445 dan 3625, dan (iii) menguji kemampuan Acidithiobacillus sp. dan Acidithiobacillus ferooxidans meningkatkan perolehan emas dengan metode flotasi.
Hasil penelitian menunjukkan bahwa pada bijih tipe-D 3445 kandungan pirit berkurang dari 92% menjadi 72.56% - 74.37% oleh Acidithiobacillus sp. 8N1.8 dan 8N1.9 dari air asam tambang dalam waktu 2-3 hari dan berkurang menjadi 76.5% - 76.66 % oleh Acidithiobacillus ferooxidans ICBB 8793 dan ICBB 8795 dalam waktu 6-7 hari. Pada bijih tipe-D 3625, kandungan pirit berkurang dari 15,7% menjadi 3,65% - 4,62% oleh keempat Acidithiobacillus sp. dari air asam tambang dan Acidithiobacillus ferooxidans koleksi ICBB-CC dalam waktu 1 hari. Kandungan emas pada bijih tipe-D 3445 meningkat dari 0,179 g/ton menjadi 0,190
– 0,241 g/ton pada minggu pertama dan 0,199 – 0,253 g/ton pada minggu ke-3. Pada bijih tipe-D 3625 kandungan emas meningkat dari 0.077 g/ton menjadi 0.110 - 0.133 g/ton pada minggu pertama dan 0.150 - 0.160 g/ton pada minggu ke-3. Nilai perolehan (recovery) kumulatif pada bijih tipe-D 3445 meningkat setiap minggunya dari 8-11% pada minggu ke-0 menjadi 26-35% pada minggu ke-1, menjadi 35-60% pada minggu ke-3 dan menjadi 44-86% pada minggu ke-8. Nilai perolehan (recovery) kumulatif pada bijih tipe-D 3625 meningkat setiap minggunya dari 7% pada minggu ke-0 menjadi 16-24% pada minggu ke-1, menjadi 42-47% pada minggu ke-3 dan menjadi 67-72% pada minggu ke-8.
SUMMARY
AZARIA INDRAWARDHANA. Increasing Gold Recovery Through Biooxidation Ore Materials by Using Acidithiobacullus sp. Supervised by DWI ANDREAS SANTOSA and SYAIFUL ANWAR.
Recovery optimalization in mineral processing (flotation) is a challenge for all stakeholders. In the flotation process, recovery can be performed on average below 80%. The low recovery in processing of valuable mineral reserves are defined by large amount of sulfides material (pyrite). Alternative solutions that can be done to increase the recovery is to separate the chemical bonds of sulfides material (pyrite) through oxidation process using pyrite-oxidizing bacteria known as Acidithiobacillus sp. This research was aimed to: (i) to characterized D-Type ores, (ii) to test the ability of Acidithiobacillus sp. to decrease pyrite content in D-Type ores, and (iii) to test the ability of Acidithiobacillus sp. to increase gold recovery from D-Type ores.
This experiment uses Acidithiobacillus sp. isolated from acid mine drainage which located in the biggest mining area in Indonesia, Mimika District, Papua Province and Acidithiobacillus ferooxidans culture collection from Indonesian Center for Biodiversity and Biotechnology (ICBB-CC) which tested to two D-Type ores 3445 and 3625. This research was done in three phase: (i) characterizing D-Type ore by mineral grain analysis, x-ray diffraction test, fire assay and flotation tests, (ii) testing the ability of Acidithiobacillus sp. and Acidithiobacillus ferrooxidans reducing the pyrite contain in the type-D ore 3445 and 3625 and (iii) testing the ability Acidithiobacillus sp. and selected Acidithiobacillus ferooxidans to increasw recovery of gold in flotation process.
The result showed that at 3445 D-type ore, pyrite content was reduced from 92% to 72.56% - 74.37% by Acidithiobacillus sp. 8N1.8 and 8N1.9 from acid mine water within 2-3 days and reduced to 76.5% - 76.66% by Acidithiobacillus ferooxidans ICBB 8793 and 8795 ICBB within 6-7 days. At the 3625 D-type ore, pyrite content was reduced from 15.7% to 3.65% - 4.62% by all Acidithiobacillus sp. either from acid mine drainage and Acidithiobacillus ferooxidans from ICBB-CC within 1 day. Gold content in the 3445 type-D ore increased from 0.179 g/ton to 0.190 to 0.241 g/tonne in the 1st week and 0.199 to 0.253 g/ton on the 3rd week while in the 3625 type-D ore increased from 0.077 g/ton to 0110-0133 g/tonne in the 1st week and 0,150-0,160 g/ton on the 3rd week. The cumulative recovery value at 3445 type-D ore increased from 8-11% to 26-35% at 1st week, 35-60% in the 3rd week and to 44-86% at 8th week while at 3625 type-D ore increased from 7% to 16-24% at 1st week, to 42-47% in 3rd week and to 67-72% in 8th week.
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Bioteknologi Tanah dan Lingkungan
PENINGKATAN PEROLEHAN LOGAM EMAS MELALUI
TEKNIK BIOOKSIDASI BAHAN TAMBANG DENGAN
MENGGUNAKAN
Acidithiobacillus
sp
.
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga tesis ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan November 2013 ini adalah biooksidasi, dengan judul Peningkatan Perolehan Logam Emas Melalui Teknik Biooksidasi Bahan Tambang dengan Menggunakan Acidithiobacullus ferooxidans.
Terima kasih penulis ucapkan kepada Bapak Prof Dr Ir Dwi Andreas Santosa, MS dan Bapak Dr Syaiful Anwar, MSc selaku pembimbing, serta Bapak Dr Ir Iskandar selaku penguji yang telah banyak memberi saran. Di samping itu, terima kasih juga penulis sampaikan kepada Kementerian Energi dan Sumberdaya Mineral, Direksi dan staf PT Freeport Indonesia, Direksi dan staf PT Eksplorasi Nusa Jaya dan seluruh rekan kerja yang tidak dapat disebutkan satu persatu, yang telah membantu selama pengumpulan data.
Ungkapan terima kasih juga disampaikan kepada almarhum papa tercinta, mama, Okky dan Winny, Andra, mami Nurul Herwindyah dan Callista Almahyra Indrawardhana serta seluruh keluarga, atas segala doa dan kasih sayangnya. Semoga tesis ini bermanfaat.
i
DAFTAR ISI
DAFTAR ISI DAFTAR TABEL DAFTAR GAMBAR
DAFTAR LAMPIRAN
1. PENDAHULUAN 1
Latar Belakang 1
Tujuan Penelitian 2
Ruang Lingkup Penelitian 3
2. TINJAUAN PUSTAKA 4
Emas dan Pirit 4
Biomining dan Biooksidasi 5
Bakteri Pengoksidasi Pirit 5
Mekanisme Oksidasi Mineral 7
Karakteristik Bijih di Wilayah Pertambangan 8
Bijih Sulfida (Tipe-D) sebagai Problematic Ores 9
Pengolahan Bijih 9
Kominusi 9
Flotasi 11
3. BAHAN DAN METODE 13
Bahan dan Alat 13
Waktu dan Tempat Penelitian 13
Metode 13
Pengambilan Sampel Bijih Tipe-D dan Air Asam Tambang 13
Karakterisasi Bijih Tipe-D 14
Analisa Butir 14
X-Ray Diffraction Test 14
Fire Assay Test 15
Flotasi 15
Isolasi Acidithiobacillus sp. dari Air Asam Tambang 17
Seleksi Acidithiobacillus sp. dari Air Asam Tambang dan Acidithiobacillus
ferooxidans ICBB-CC 17
Pengujian Bakteri dengan Biooksidasi untuk Penurunan Kandungan Pirit dan
Peningkatan Perolehan Emas 17
4. HASIL DAN PEMBAHASAN 19
Karakterisasi Bijih Tipe-D 19
Isolasi Acidithiobacillus sp. dari Air Asam Tambang 20
Seleksi Acidithiobacillus sp. dari Air Asam Tambang dan Acidithiobacillus
ferooxidans Koleksi ICBB-CC 21
Seleksi Acidithiobacillus sp. dari Air Asam Tambang 21
Seleksi Acidithiobacillus ferooxidans Koleksi ICBB-CC 22
Biooksidasi Bijih Tipe-D dengan Acidithiobacillus sp. dan Acidithiobacillus
ferooxidans 23
Hasil Uji Biooksidasi pada Bijih Tipe-D 3445 dan 3625 25
Pengukuran Kandungan Pirit dengan Metode X-ray Diffraction Test 25
Metode Fire Assay
Peningkatan Nilai Perolehan pada Bijih Tipe-D 3445 dan 3625 dengan Metode
Flotasi 28
5. SIMPULAN DAN SARAN 31
Simpulan 31
Saran 31
DAFTAR PUSTAKA 32
LAMPIRAN 34
RIWAYAT HIDUP 45
DAFTAR TABEL
1. Komposisi media Acidithiobacillus ferooxidans cair 17
2. Kandungan total di dalam umpan bijih tipe-D 19
3. Kandungan total di dalam konsentrat bijih tipe-D 19
4. Penurunan kandungan pirit pada bijih tipe-D 3445 selama proses biooksidasi dengan menggunakan Acidithiobacillus
26
5. Penurunan kandungan pirit pada bijih tipe-D 3625 selama proses biooksidasi dengan menggunakan Acidithiobacillus
27
6. Perhitungan recovery kumulatif pada bijih tipe-D 3445 29 7. Perhitungan recovery kumulatif pada bijih tipe-D 3625 29
DAFTAR GAMBAR
1. Kandungan emas yang terkunci oleh pirit (kiri) dan kandungan calcopyrit
(CuFeS2) yang terkunci oleh pirit (kanan) 2
2. Butiran emas (nugget) dari lokasi penambangan 4
3. Bijih pirit murni (kiri) dan bijih pirit yang berasosiasi dengan emas (kanan) 5
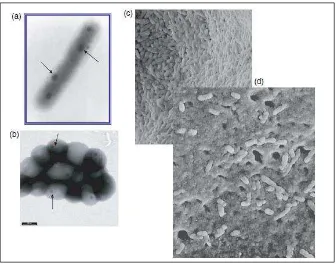
4. Mikroorganisme acidophilic yang berpartisipasi dalam ekstraksi logam melalui biomining. (a) sel Acidithiobacillus ferrooxidans. (b) sekelompok sel Metallicus sulfolobus. (c) biofilm, monolayer sel Acidithiobacillus ferrooxidans yang tumbuh di permukaan dari butiran sulfur. (d) biofilm Acidithiobacillus ferrooxidans yang terlihat pada (c) telah dihilangkan dari partikel padat. 6
5. Skema interaksi bakteri – mineral pirit 7
6. Cadangan bijih di wilayah pertambangan PTFI 8
7. Mineral berharga yang berasosiasi dengan pengotornya 10
8. X-section partikel bijih 10
9. Skema kominusi 2 tahap 11
10. Kurva perbandingan recovery-grade 11
11. Skema pengolahan emas dengan cara flotasi 12
12. Mikroskop stereo binokuler 14
13. Mesin X-ray diffraction endeavour D4 15
14. Proses pengujian dengan api (fire assay) pada bijih 15
15. Proses flotasi mineral berharga dengan denver flotation machine 16
16. Skema proses flotasi 16
17. Analisa butir dan proses flotasi bijih tipe-D 3445 (kiri) dan bijih tipe-D 3625
(kanan) sebelum biooksidasi 19
pertama
19. Hasil isolasi Acidithiobacillus sp. dari sampel air asam tambang PTFI tahap
kedua 20
20. Hasil iolasi Acidithiobacillus sp. dari sampel air asam tambang PTFI tahap
ketiga 21
21. Seleksi Acidithiobacillus sp. dari air asam tambang di dalam media tumbuh
yang mengandung bijih pirit 21
22. Grafik penurunan pH media Acidithiobacillus sp. yang diisolasi dari air asam
tambang PTFI 22
23. Seleksi Acidithiobacillus ferooxidans ICBB-CC di dalam media tumbuh yang
mengandung bijih pirit 22
24. Grafik penurunan pH media Acidithiobacillus ferooxidans koleksi ICBB-CC 23
25. Proses biooksidasi dengan menggunakan botol plastik dan aerator. 23
26. Perubahan bijih tipe-D 3445 yang belum di oksidasi (kiri) dan sudah teroksidasi
(kanan) 24
27. a. Bijih tipe-D belum teroksidasi; b. Teroksidasi oleh Acidithiobacillus sp. 8N1.8; c. Teroksidasi oleh Acidithiobacillus sp. 8N1.9; d. Teroksidasi oleh A.ferooxidans ICBB 8793 dan e. Teroksidasi oleh A.ferooxidans ICBB 8793. 24
28. Perubahan bijih tipe-D 3625 yang belum teroksidasi (kiri) dan yang sudah
teroksidasi (kanan) 25
29. a. Bijih tipe-D 3625 belum teroksidasi; b. Teroksidasi oleh Acidithiobacillus sp. 8N1.8; c. Teroksidasi oleh Acidithiobacillus sp. 8N1.9; d. Teroksidasi oleh A.ferooxidans ICBB 8793 dan e. Teroksidasi oleh A.ferooxidans ICBB 8793. 25
30. Penurunan kandungan pirit pada bijih Tipe-D 3445 selama proses biooksidasi
dengan menggunakan Acidithiobacillus 25
31. Penurunan kandungan pirit pada bijih tipe-D 3625 selama proses biooksidasi
dengan menggunakan Acidithiobacillus 26
32. Kandungan mineral teroksidasi pada bijih tipe-D 3445 (a) dan 3625 (b) 27
33. Kandungan emas bijih tipe-D 3445 (a) dan 3625 (b) 28
34. Nilai perolehan (recovery) emas dengan metode flotasi pada bijih tipe-D
3445(a) dan 3625(b) 30
LAMPIRAN
1. Hasil pengujian x-ray diffraction (XRD) awal pada bijih tipe-D 3445 dan 3625 34 2. Hasil pengujian flotasi awal pada bijih tipe-D 3445 dan 3625 35 3. Hasil isolasi pertama sampel air asam tambang di lokasi tambang terbuka
grasberg 36
4. Hasil isolasi sampel air asam tambang di lokasi tambang bawah tanah 37 5. Hasil isolasi Acidithiobacillus sp. dari air asam tambang dengan media tumbuh
padat 38
6. Penurunan pH media isolat Acidithiobacillus sp. dari air asam tambang 39 7. Penurunan pH media isolat Acidithiobacillus ferooxidans koleksi ICBB 39
8. Jumlah sel masing-masing isolat yang diukur dengan metode most probable
number 39
9. Kandungan pirit pada bijih tipe-D 3445 dan 3625setelah bioksidasi 39
10. Kandungan mineral teroksidasi dan emas pada bijih tipe-D 3445 dan 3625
dengan metode fire assay 40
1
PENDAHULUAN
Latar Belakang
Indonesia terkenal sebagai salah satu negara yang kaya dengan bahan tambang. Bahan tambang tersebut tersebar di seluruh wilayah kepulauan Indonesia yang terdiri dari berbagai komoditi seperti emas, tembaga, perak dan lainnya. Berdasarkan data Badan Geologi Kementerian Energi dan Sumber Daya Mineral (ESDM) tahun 2013, cadangan emas di Indonesia mencapai 3,4 milyar ton, terdiri dari cadangan emas primer sebesar 3,3 milyar ton dan cadangan emas aluvial sebesar 17 juta ton. Pelaksanaan kegiatan pertambangan mineral dan batubara yang profesional ditandai dengan meningkatnya jumlah produksi mineral dan batubara, meningkatnya kualitas kegiatan pertambangan umum, meningkatnya investasi, meningkatnya nilai tambah bahan tambang dan lainnya. Indikator keberhasilan dan target yang ingin dicapai oleh Kementerian Energi dan Sumberdaya Mineral dalam 5 tahun ke depan tercantum di dalam Rencana Strategis (Renstra) ESDM yang salah satunya adalah peningkatan nilai perolehan pada pengolahan mineral logam sebesar 95% pada tahun 2015. Berdasarkan data Rencana Kerja Tahunan Teknis dan Lingkungan (RKTTL) Perusahaan Kontrak Karya Tahun 2014, tingkat perolehan pengolahan di beberapa perusahaan pertambangan mineral masih belum optimal. Salah satu contoh perusahaan Kontrak Karya generasi pertama, dalam mengolah mineral sebesar 65 juta ton per tahun dengan kadar 0,8–1 g/ton, nilai perolehan maksimal yang dapat dilakukan oleh pabrik pengolahan di lokasi tambang rata - rata sebesar 80%. Kondisi ini menunjukkan bahwa masih terdapat lebih dari 20% mineral berharga yang terbuang. Selain mengurangi potensi pendapatan, tersisanya mineral berharga berpotensi menimbulkan masalah sosial yang berkepanjangan. Salah satu penyebab rendahnya perolehan mineral berharga adalah karakteristik cadangan yang dikategorikan sebagai bijih tipe-D yang mengandung banyak mineral sulfida (pengotor) sehingga sulit dipisahkan dengan cara flotasi biasa.
2
Gambar 1 Kandungan emas yang terkunci oleh pirit (kiri) dan kandungan calcopyrit (CuFeS2) yang terkunci oleh pirit (kanan) (PTFI 2013)
Dengan kondisi tersebut, penulis melihat bahwa harus ada alternatif teknologi lain yang dapat mengakomodasi kelemahan metode pengolahan yang konvensional agar dapat meningkatkan perolehan mineral berharga pada proses pengolahan bijih sulfida dan mengurangi mineral berharga yang terbuang. Berbagai teknologi diuji coba dan diterapkan, salah satu alternatif teknologi yang digunakan adalah bioteknologi (Schippers et al. 2013). Bioteknologi memiliki potensi untuk membantu dan memecahkan berbagai persoalan di dunia pertambangan baik minyak, gas, batubara dan bijih (Nagaoka et al. 1999). Bioteknologi telah mulai diterapkan pada pertambangan batubara dan mineral (Zammit 2012). Microbial desulfurization dapat dimanfaatkan untuk menurunkan kandungan sulfur pada batubara dan kandungan pirit pada logam. Dengan menggunakan bakteri, kandungan sulfur dalam batubara dapat diturunkan sebanyak 63% hanya dalam waktu 24 jam (Santosa 2010). Melalui bioteknologi ERM (enhanced recovery of metals) bahan tambang logam dapat ditingkatkan perolehannya terutama dari deposit yang kandungan bijihnya rendah. Salah satu teknologi dalam katagori tersebut yang dapat digunakan adalah biohydrometallurgy atau bioleaching. Bioleaching menggunakan bakteri untuk mengubah sifat fisik dan kimia bahan tambang sehingga logam dapat diekstraksi dengan cara yang lebih ekonomis. Dalam percobaan laboratorium, 97% tembaga asal bahan tambang kualitas rendah dapat diekstrak (Santosa 2010). Selain dari bioleaching, biooksidasi dapat digunakan untuk meningkatkan perolehan logam mulia. Dengan biooksidasi, konsentrasi pirit pada mineral berharga dapat dikurangi antara 77% hingga 95% (Nagaoka et al. 1999). Pada proses bioleaching dan biooksidasi, beberapa mikroorganisme termasuk Acidithiobacillus ferooxidans mampu mengakumulasi logam dalam selnya dengan konsentrasi yang jauh lebih tinggi dibanding di lingkungan sekitarnya. Salah satu percobaan menunjukkan bahwa 2 tahap biooksidasi, konsentrat emas meningkat perolehannya menjadi 94,7% dibandingkan dengan metode konvensional yang hanya menghasilkan perolehan di bawah 70% (Amankwah et al. 2004).
Tujuan Penelitian
Berdasarkan latar belakang yang telah diuraikan di atas, bijih sulfida (Tipe-D) yang mengandung pirit tinggi menjadi permasalahan utama pengolahan emas dengan metode flotasi di perusahaan pertambangan khususnya PTFI. Untuk
Emas
Pirit
Pirit
3 mengatasi permasalahan tersebut, alternatif solusi yang dilakukan adalah mengoksida bijih sulfida dengan menggunakan bakteri Acidithiobacillus sp. dari air asam tambang dan Acidithiobacillus ferooxidans koleksi ICBB agar ikatan sulfida dapat terurai dan bijih emas dapat terbebaskan. Secara garis besar penelitian ini bertujuan untuk:
1. Mengkarakterisasi bijih sulfida (Tipe-D).
2. Mengisolasi Acidithiobacillus sp. dari air asam tambang yang berasal dari wilayah pertambangan PTFI.
3. Menseleksi Acidithiobacillus sp. dari air asam tambang dan Acidithiobacillus ferooxidans koleksi ICBB-CC.
4. Menguji kemampuan Acidithiobacillus sp. dan Acidithiobacillus ferrooxidans mengurangi kandungan pirit yang terdapat dalam bijih tipe-D 3445 dan 3625. 5. Menguji kemampuan Acidithiobacillus sp. dan Acidithiobacillus ferooxidans
terseleksimeningkatkan perolehan recovery emas. Ruang Lingkup Penelitian
Penelitian ini dilakukan dalam beberapa tahap dengan ruang lingkup kegiatan penelitian sebagai berikut :
1. Menyeleksi bakteri yang berpotensi sebagai pendegradasi pirit yang berasal dari air asam tambang dari wilayah penambangan PTFI.
2. Menguji efektivitas bakteri terseleksi dalam mendegradasi pirit pada bijih tipe-D.
2
TINJAUAN PUSTAKA
Emas dan Pirit
Emas adalah unsur kimia dengan simbol Au (dari bahasa Latin: aurum) dengan nomor atom 79 dan titik lebur berada pada 1064,18C. Emas merupakan logam yang bersifat lunak dan mudah ditempa, kekerasannya berkisar antara 2,5 – 3 (skala Mohs), serta berat jenisnya tergantung pada jenis dan kandungan logam lain yang berpadu dengannya. Mineral pembawa emas biasanya berasosiasi dengan mineral ikutan (gangue minerals). Mineral ikutan tersebut umumnya kuarsa, karbonat, turmalin, flourpar, dan sejumlah kecil mineral non logam. Mineral pembawa emas juga berasosiasi dengan endapan sulfida. Emas terbentuk dari proses magmatisme atau pengkonsentrasian di permukaan. Beberapa endapan terbentuk karena proses metasomatisme kontak dan larutan hidrotermal, sedangkan pengkonsentrasian secara mekanis menghasilkan endapan letakan (placer).
Kelenturan emas yang tinggi, ketahanan terhadap korosi dan sebagian besar reaksi kimia lainnya serta konduktivitas listrik yang bagus menyebabkan emas terus digunakan dalam konektor listrik tahan korosi di semua jenis perangkat komputerisasi.
Gambar 2 Butiran emas (nugget) dari lokasi penambangan (www.akhmadarqom.com)
Pirit merupakan sulfida besi dengan rumus kimia FeS2 dengan titik lebur pada
1194C. Nama pirit berasal dari Yunani yang berarti api. Pirit biasanya ditemukan berasosiasi di dalam urat kuarsa, batuan sedimen, batuan metamorf, serta batuan dasar pada cadangan batubara dan mineral sebagai pengganti fosil. Meskipun dijuluki emas tiruan, pirit kadang-kadang ditemukan dalam ikatan emas karena bentuk dan warnanya menyerupai emas dan kuningan.
2
Gambar 3 Bijih pirit murni (kiri) dan bijih pirit yang berasosiasi dengan emas (kanan) (www.tankonyvtar.hu)
Biomining dan Biooksidasi
Biomining merupakan pendekatan baru untuk ekstraksi mineral yang diinginkan dari bijih yang sudah dieksplorasi oleh industri pertambangan dalam beberapa tahun terakhir. Pada metode biomining, tidak menggunakan bahan kimia beracun dan suhu yang ekstrim yang dapat merusak tetapi menggunakan bakteri untuk mengekstraksi mineral (Jerez 2011). Pengembangan industri biomining telah diterapkan di beberapa negara termasuk Afrika Selatan, Brasil dan Australia (Wang & Mujumnar 2007). Bakteri akan mengoksidsi besi dan sulfur pada bijih sulfida kemudian melepaskan tembaga, emas dan uranium yang terikat. Teknologi ini disebut sebagai teknologi biooksidasi. Industri pabrik pengolahan yang menggunakan metode biooksidasi pada umumnya menggunakan kultur campuran bakteri mesofilik dari genus Acidithiobacillus ferooxidans atau Leptospirillum ferrooxidans (Larsson et al. 1990).
Pada beberapa penelitian, Acidithiobacillus ferrooxidans dapat digunakan untuk melarutkan pirit dari bijih yang mengandung sulfida tinggi dan dapat meningkatkan perolehan mineral berharga pada proses pengolahan (Konishi et al. 1990). Selain itu, dimungkinkan juga untuk melakukan ekstraksi dari bijih kadar rendah. Aplikasi bioteknologi untuk penambangan dan pengolahan sudah tak terhitung jumlahnya, beberapa contoh yaitu penambangan in-situ, metode biodegradasi, bioremediasi pasif drainase air asam tambang dan bioleaching dari bijih dan konsentrat dengan menggunakan bioreaktor (Fernando 2000). Penelitian ini menghasilkan beberapa penerapan teknologi yang efisien dan solusi terhadap masalah yang kompleks seperti bioleaching logam dari mineral oksida, biooksidasi dari bijih sulfida, bioprocessing bijih fosfat, dan lainnya. Semua teknologi mulai dari penambangan in-situ sampai pengolahan mineral dan teknologi pengolahan, bioteknologi memberikan alternatif solusi pada industri pengolahan mineral yang inovatif dan hemat biaya.
Bakteri Pengoksidasi Pirit
3 hidupnya memerlukan keberadaan senyawa sulfur anorganik. Bakteri ini bernafas secara istimewa dengan memanfaatkan oksigen sebagai terminal akseptor elektron. Acidithiobacillus ferrooxidans adalah bakteri Gram negatif yang memerlukan suasana autotrophic dan aerob. Bakteri ini motil, dan memiliki flagela polar. Acidithiobacillus ferrooxidans adalah suatu acidophil, hidup di lingkungan dengan kisaran pH optimal 1,5 sampai 2,5. Acidithiobacillus ferrooxidans juga termofilik, dalam suhu 45° - 50°C. Toleransi suhu tinggi dari bakteri mungkin karena kandungan GC bakteri tersebut tinggi yaitu 55% - 65% (Rawlings & Tomonobu 1994). Energi Acidithiobacillus ferrooxidans berasal dari oksidasi besi ferro ke besi ferri, dan reduksi sulfur menjadi senyawa asam sulfat. Kandungan sulfur dapat terkonsentrasi di dinding sel bakteri. Acidithiobacillus ferrooxidans adalah bakteri yang paling aktif di limbah tambang ketika dalam kondisi asam dan indikasi pencemaran logam. Drainase air asam tambang yang ekstrim juga dapat mengekspos kandungan pirit tingkat tinggi, unsur yang mudah teroksidasi oleh Acidithiobacillus ferrooxidans.
Hal ini diketahui bahwa leaching bacteria kebanyakan tumbuh melekat pada permukaan substrat padat seperti sulfur dan logam sulfida (Gambar 4). Lampiran ini terutama dimediasi oleh zat polimer ekstraseluler (extracellular polymeric substances) yang mengelilingi sel dan dengan komposisi yang disesuaikan dengan substrat pertumbuhan.
Gambar 4 Mikroorganisme acidophilic yang berpartisipasi dalam ekstraksi logam melalui biomining. (a) sel Acidithiobacillus ferrooxidans. (b) sekelompok sel Metallicus sulfolobus. (c) Biofilm, monolayer sel Acidithiobacillus ferrooxidans yang tumbuh di permukaan dari butiran sulfur. (d) Biofilm Acidithiobacillus ferrooxidans yang terlihat pada (c) telah dihilangkan dari partikel padat. (Jerez 2009)
4
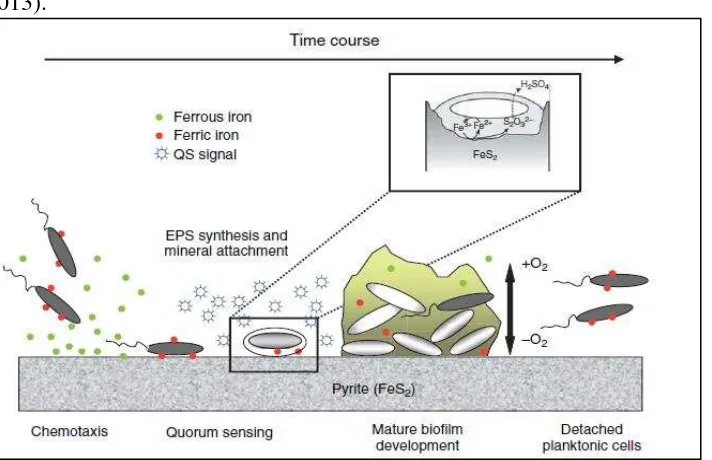
logam sulfida secara kimiawi seperti pirit dioxidasi menjadi Fe+3 dan tiosulfat yang dapat menjadi asam sulfat. Kontak yang dekat antara bakteri dengan mineral membuat oksidasi sulfida menjadi lebih efisien dan spesifik (Jerez 2013).
Gambar 5 Skema Interaksi Bakteri – Mineral Pirit (Jerez 2013) Mekanisme Oksidasi Mineral
Oksidasi ion besi (Fe2+) ke ion ferri (Fe3+) merupakan reaksi yang memproduksi energi untuk beberapa mikroorganisme. Karena hanya sejumlah kecil energi yang diperoleh, Fe2+ dalam jumlah besar harus teroksidasi. Selanjutnya, Fe3+ akan membentuk larutan Fe(OH)3 yang mengendap dalam H2O. Banyak
mikroorganisme pengoksidasi Fe2+ juga mengoksidasi sulfur. Pada kondisi demikian, acidophiles lebih mengasamkan lingkungannya dengan memproduksi H2SO4. Hal ini dibuktikan dengan sebagian fakta bahwa pada pH netral Fe2+ cepat
teroksidasi secara kimia jika terjadi kontak dengan udara. Dalam kondisi ini tidak ada Fe2+ untuk memungkinkan pertumbuhan yang signifikan. Pada pH rendah, bagaimanapun, Fe2+ jauh lebih stabil. Hal ini menjelaskan mengapa sebagian besar mikroorganisme pengoksidasi Fe2+ hanya ditemukan di lingkungan asam dan obligat acidophiles(Fowler et al. 1999).
Bakteri terbaik pengoksidasi Fe2+ adalah Acidithiobacillus ferrooxidans (Jerez 2009). Mikrobiologi pengoksidasi Fe2+ merupakan aspek penting dari peningkatan konsentrasi asam dalam proses biooksidasi pada pengolahan mineral sebuah tambang tetapi juga menjadi masalah ekologi yang serius karena meningkatkan konsentrasi air asam tambang yang bermasalah bagi lingkungan itu sendiri. Namun, kondisi ini dapat berguna jika dieksploitasi dengan benar dan dikontrol. Pemisahan Sulfur yang terkandung di dalam pirit (FeS2) adalah langkah awal pada proses ini.
Pirit adalah struktur cristalline larut yang melimpah pada mineral bijih. Hal ini dihasilkan oleh reaksi:
S + FeS → FeS2
5 Dua akseptor elektron dapat mempengaruhi pada proses ini adalah ion O2 dan Fe3+.
Fe3+ hanya akan hadir dalam jumlah yang signifikan dalam kondisi asam (pH < 2,5). Pertama proses kimia lambat dengan O2 sebagai akseptor elektron akan memulai
oksidasi pirit:
FeS2 + 7/2 O2 + H2O → Fe2+ + 2 SO42- + 2 H+
Reaksi ini mengasamkan lingkungan dan Fe2+ akan terbentuk agak stabil. Dalam lingkungan seperti ini, Acidithiobacillus ferrooxidans akan dapat tumbuh dengan cepat. Setelah pengasaman lanjut, ferroplasma akan meningkatkan tingkat keasaman. Sebagai konsekuensi dari aktivitas mikrob, energi reaksi menghasilkan:
Fe2+→ Fe3+
Fe3+ ini yang tetap larut pada pH rendah dan bereaksi secara spontan dengan pirit menjadi:
FeS2 + 14 Fe3+ + 8 H2O → 15 Fe2+ + 2 SO42- + 16 H+
Fe2+ dapat diproduksi lagi dan digunakan oleh mikroorganisme lalu dengan demikian reaksi selanjutnya akan dimulai.
Suhu di dalam dump leach sering meningkat secara spontan sebagai akibat dari aktivitas mikrob. Dengan demikian, kemolitotrof termofil pengoksidasi besi seperti spesies Acidithiobacillus dan Leptospirillum pada temperatur yang lebih tinggi di atas 40°C dapat menjadi hal yang sangat penting dalam proses leaching (Rawlings 2003).
Karakteristik Bijih di Wilayah Pertambangan
Secara garis besar, kandungan bijih di dalam wilayah pertambangan emas PTFI adalah sistem mineralisasi porfiri. Distribusi mineral berharga seperti kalkopirit, bornit dan digenit terkonsentrasi dengan bentuk seperti tapal kuda menutupi inti (core). Inti ini adalah intrusi terakhir diorite south kali. Dengan kondisi litologi tersebut, semua material didefinisikan menjadi Stockwork, Dalam Coarse, Dalam Fine, Hard Zone, Heavy Sulfide Zone, Kali, Pokerchip dan Sediment (Gambar 6). Berdasarkan perencanaan penambangan ke depannya, akan diterapkan metode penambangan bawah tanah (underground). Cadangan akan didominasi oleh material dengan sulfida tinggi (Heavy Sulfide Zone) dengan kadar pirit tinggi. Pirit akan menjadi masalah pada proses pengolahan karena dapat menurunkan perolehan (recovery) pada proses pengolahan dengan metode flotasi.
6
Bijih Sulfida (Tipe-D) Sebagai Problematic Ores
Pabrik pengolahan (mill) memiliki beberapa parameter metalurgi yang perlu dicapai ketika melakukan pengolahan bijih yang berasal dari tambang permukaan dan tambang bawah tanah. Beberapa parameter itu antara lain: ukuran penggerusan, grade umpan, grade konsentrat, grade pada tailing dan lainnya. Jika area tambang mengirim banyak bijih sulfida dengan kadar pirit lebih dari 40%, akan berdampak pada penurunan perolehan emas maupun tembaganya. Mineral pengotor yang memberikan dampak penurunan perolehan bijih antara lain pirit, oksida-hidrosulfat (hematit, jarosit, limonit, cuprit), tanah liat dan serisit. Persentase mineral pengotor tersebut dalam bijih tercermin dalam parameter metalurgi selama tes flotasi yang dianalia dengan X-Ray Diffraction Test.
Bijih dengan kandungan pirit tinggi (problematic ores) pertama kali ditemukan pada bulan September 2006 ketika penambangan masuk pada wilayah Grasberg Igneous Complex (GIC) yang dapat dilihat pada Gambar 6. Dalam dokumentasi Intermediate Planning Model (IPM) ada dua jenis problematic ores dan keduanya diklasifikasikan sebagai bijih tipe-D untuk membedakan jenis bijih bersih tipe A, B, B tinggi dan C. Bijih bermasalah pertama disebut sebagai tipe-D asli dan yang kedua disebut sebagai tipe-D serisit. Tipe-D asli memiliki kandungan pirit > 10%, oksida > 5%, tanah liat > 5%, Pb > 0,08% dan Zn > 0,08% dan untuk tipe-D serisit memiliki kandungan Serisit > 10% (Perdana & Wiwoho 2012).
Pengolahan Bijih Kominusi
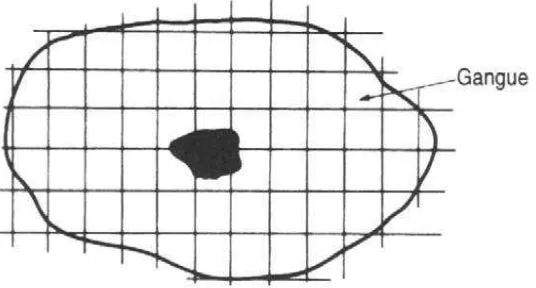
Proses pengolahan bijih emas dimulai dengan tahap operasi kominusi yang terdiri dari crushing (peremukan) dan grinding (penggilingan). Salah satu tujuan utama dari kominusi adalah pembebasan (liberasi) atau melepaskan mineral berharga yang berasosiasi dari pengotornya pada ukuran partikel terkasar yang memungkinkan. Jika proses ini tercapai, maka tidak hanya menghemat energi karena pengurangan jumlah partikel halus yang dihasilkan, tetapi setiap tahapan selanjutnya menjadi lebih mudah dan lebih murah. Jika produk yang dibutuhkan adalah dengan kadar tinggi, maka pembebasan (liberasi) yang baik menjadi sangat penting. Dalam prakteknya, pembebasan (liberasi) yang sempurna jarang dicapai, bahkan sampai dengan ukuran bijih yang diinginkan. Gambar 7 menunjukkan bongkah bijih yang telah direduksi menjadi sejumlah kubus yang mempresentasikan volume dan ukuran yang lebih kecil dari sampel bijih aslinya. Hal ini memperlihatkan bahwa setiap partikel yang dihasilkan mengandung mineral berharga dan mengandung sebagian pengotor atau dengan kata lain pembebasan (liberasi) belum tercapai sempurna.
7
Gambar 7 Mineral berharga yang berasosiasi dengan pengotornya (Wills & Napier-Munn 2005).
Proses kominusi menciptakan berbagai fragmen, mulai dari kaya mineral berharga sampai dengan pengotornya. Partikel tipe 1 yang kaya mineral diklasifikasikan sebagai konsentrat karena memiliki derajat penguncian dengan mineral pengotor yang masih dalam batas toleransi. Partikel tipe 4 akan juga digolongkan sebagai tailing karena hanya sejumlah kecil mineral yang muncul dan akan mengurangi nilai perolehan dalam konsentrat. Partikel jenis 2 dan 3 digolongkan sebagai middlings, karena diperlukan proses penghancuran tahap kedua untuk membebasan mineral berharga dari pengotornya (Gambar 9).
Gambar 8 X-section partikel bijih (Wills & Napier-Munn 2005).
Pada proses kominusi, terbatas pada mineralogi bijihnya, sebagai contoh dalam bijih yang mengandung tembaga asli secara teoritis mungkin menghasilkan konsentrat yang mengandung 100% Cu, tetapi jika mineral bijihnya adalah kalkopirit (CuFeS2), konsentrat terbaik akan hanya berisi 34,5% Cu (Wills &
8
Gambar 9 Skema kominusi 2 tahap (Wills & Napier-Munn 2005)
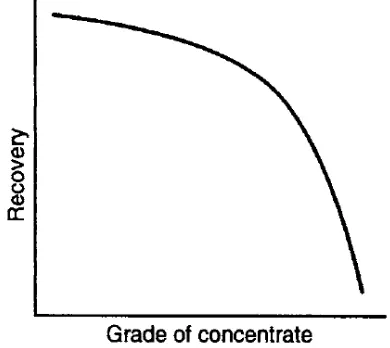
Rasio konsentrat adalah rasio berat umpan dibandingkan dengan berat konsentrat tersebut yang merupakan ukuran efisiensi proses konsentrasi dan terkait dengan grade konsentrat. Nilai dari rasio konsentrasi umumnya akan meningkat bersamaan dengan grade konsentrat. Rasio konsentrat dan recovery pada dasarnya independen satu sama lain. Sebagai contoh, untuk mendapatkan konsentrat berkadar tinggi dengan rasio yang tinggi, caranya dengan mengambil bijih galena murni dari bijih timah, tetapi kondisi ini mengakibatkan recoverynya akan sangat rendah karena ada kemungkinan terdapat 60% mineral pengotor dalam konsentrat tersebut. Ada hubungan terbalik antara nilai perolehan (recovery) dengan grade konsentrat pada semua proses konsentrasi. Jika tujuannya untuk mencapai konsentrat grade tinggi, nilai perolehannya (recovery) nya rendah. Jika tujuannya untuk recovery mineral tinggi, akan lebih banyak mineral pengotor dalam konsentrat dan grade konsentrat akan turun.
9 Grade konsentrat dan nilai perolehan (recovery) merupakan faktor metalurgi, yaitu efisiensi dari setiap operasi konsentrasi dapat dinyatakan dengan kurva pada Gambar 10. Kurva menunjukkan karakteristik hubungan kebalikan antara recovery dan grade konsentrat, proses pengolahan mineral umumnya bergerak sepanjang kurva tersebut. Tantangan pada pengolahan mineral adalah untuk mengoptimalkan pergerakan titik tertinggi pada kedua faktor baik recovery maupun grade konsentrat (optimalisasi).
Flotasi
Pada umumnya emas diekstraksi melalui proses sianidasi, amalgamasi atau flotasi. Namun, karena masalah lingkungan dan bahaya terhadap kesehatan, maka proses amalgamasi dan sianidasi menjadi semakin jarang digunakan. Secara umum pengolahan bijih emas untuk menjadi bullion meliputi operasi pengecilan ukuran atau kominusi, pelindian (leaching), pemisahan padatan-larutan atau solid-liquid separation, vacuum deaeration, cementation, filtration, dan smelting. Flotasi adalah suatu proses pemisahan mineral berharga dari pengotornya menggunakan perbedaan sifat permukaan partikel dari beragam mineral. Dalam proses flotasi biasanya sifat permukaan mineral berharga dirubah sehingga mineral berharga dapat menempel pada gelembung udara dan naik ke permukaan tangki flotasi sebagai lumpur konsentrat, sedangkan mineral tidak berharga akan tenggelam ke dasar tangki flotasi menjadi tailing (Lloyd 1981). Ketika buih telah memenuhi permukaan tangki flotasi, buih dialirkan ke saluran penampung lumpur konsentrat (concentrate launder) kemudian dialirkan ke tangki penyimpanan konsentrat. Proses flotasi pemurnian dibagi menjadi 3 tahapan yaitu flotasi cleaner pertama, cleaner kedua dan flotasi scavanger. Flotasi pertama dan kedua dilakukan dalam tangki yang berbentuk kolom setinggi 20 – 25 meter yang dilengkapi dengan air pembilas (wash water) untuk membilas mineral tidak berharga yang masih terperangkap diantara buih yang mengapung di permukaan tangki. Saluran udara dipasang lebih banyak di dasar tangki agar gelembung udara mampu membawa mineral berharga lebih banyak. Kolom setinggi 20 – 25 meter berfungsi untuk menambah waktu tinggal (resident time) mineral berharga di dalam tangki agar mendapatkan cukup kesempatan untuk menempel pada gelembung udara. Tangki kolom flotasi cleaner diisi oleh lumpur konsentrat produk produk dari flotasi rougher dengan kadar padatan 10% - 16%, sedangkan tangki kolom flotasi cleaner scavenger diisi oleh lumpur pasir sisa tambang produk dari flotasi cleaner.
3
BAHAN DAN METODE
Bahan dan Alat
Percobaan ini menggunakan bijih pirit dan bijih tipe-D dengan kandungan pirit masing-masing 94,5%, 92% dan 15,7% sebanyak 30kg. Bijih tersebut dihancurkan hingga ukuran 80% lolos 60µm (sesuai dengan ukuran pada pabrik pengolahan / mill); Air asam tambang sebanyak 108 sampel yang tersebar di wilayah penambangan terbuka dan penambangan bawah tanah; Isolat ICBB nomor ICBB 8789, ICBB 8790, ICBB 8793, ICBB 8795, ICBB 8796 dan ICBB 8797; Media tumbuh Acidithiobacillus ferooxidans padat dan cair.
Peralatan yang digunakan pada penelitian ini antara lain: Mikroskop Stereo Binokuler yang digunakan untuk mengetahui kandungan dalam setiap bijih dan melihat perubahan struktur bijih akibat dari proses oksidasi; Mesin XRD (X-ray diffraction) Test Endeavor D4 yang digunakan untuk menganalisis bahan serbuk polikristalin melalui difraksi sinar-X dan digunakan untuk mengetahui kadar pirit yang terkandung di dalam bijih; Mesin Flotasi Denver D-12 yang digunakan untuk memisahkan berbagai macam sulfida, karbonat dan oksida dengan alat alat pendukungnya seperti flotation cell, filter press, aeration control, flotation reagent, pH meter, scrapper, botol air, nampan, oven, kertas dan spidol; Tungku Kupelasi, Atomic Adsorbtion Spectrophotometer dan alat lainnya untuk pengujian dengan api (Fire Assay Test). Fire Assay Test digunakan untuk mengetahui kandungan emas dan kandungan mineral teroksidasi di dalam bijih. Botol plastik untuk biooksidasi, volume 6,75liter dengan diameter 25cm dan tinggi 30cm, aerator (mesin udara), selang udara, keran udara, pipa aerator dan peralatan yang digunakan untuk peremajaan isolat bakteri, laminar flow cabinet, pipet mikro, bunsen, timbangan, pH meter, erlenmeyer, autoklaf, shaker, stirrer, dan botol.
-Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan September 2013 - Juni 2015 di beberapa tempat antara lain: bijih pirit yang diambil pada ketinggian 3445m dpl, bijih tipe-D pada ketinggian 3445 dpl dan 3625m dpl; sampel air asam tambang sebanyak 108 titik diambil pada ketinggian 3235m dpl, 4150m dpl dan 4255m dpl serta pada area penambangan bawah tanah AB Tunnel pada ketinggian 2510m dpl, Big Gossan pada ketinggian 3046m dpl, Deep Mine Level Zone (DMLZ) pada ketinggian 2550m dpl dan Wanagon Drainage Drift di ketinggian 3580m dpl (koordinat pada Lampiran 3 dan 4); Isolasi dan seleksi Acidithiobacillus sp. dilakukan di Laboratorium Bioteknologi Tanah, Departemen Ilmu Tanah dan Sumberdaya Lahan, Institut Pertanian Bogor; Analisa butir dilakukan di Laboratorium Pengolahan Mineral, Pusat Sumberdaya Geologi, Kementerian Energi dan Sumberdaya Mineral, Bandung; X-Ray Diffraction Test, Fire Assay dan Flotasi dilakukan di Laboratorium Metalurgi PTFI, Mile 74, Papua.
Metode
Pengambilan Sampel Bijih Tipe-D dan Air Asam Tambang
2
kandungan mineral di dalamnya. Pengujian sampel setiap bijih meliputi pengujian fire assay, flotation test dan XRD-test untuk mengetahui kandungan pirit awal, kandungan emas awal dan nilai perolehan awal pada saat sebelum diperlakukan dengan Acidithiobacillus sp. yang diperoleh dari air asam tambang.
Air asam tambang diambil dari berbagai sumber di area penambangan terbuka pada ketinggian 3235 mdpl, ketinggian 4150 mdpl dan pada ketinggian 4255 mdpl serta pada area penambangan bawah tanah AB Tunnel pada ketinggian 2510 mdpl, Big Gossan pada ketinggian 3046 mdpl, Deep Mine Level Zone (DMLZ) pada ketinggian 2550 mdpl dan Wanagon Drainage Drift di ketinggian 3580 mdpl (koordinat pada Lampiran 3 dan 4).
Karakterisasi Bijih Tipe-D
Karakterisasi bijih dilakukan dengan beberapa metode antara lain : analisa butir, XRD test, fire assay test dan flotation test. Karakterisasi ini digunakan untuk mengukur kondisi awal 2 jenis bijih sulfida yang digunakan di dalam percobaan yang meliputi kandungan pirit, emas, mineral oksida dan nilai perolehan pada proses pengolahan dengan flotasi. Karakterisasi bijih meliputi pengujian:
Analisa Butir
Pada proses analisa butir, bijih dianalisa dengan mikroskop stereo binokuler (Gambar 12) dan diidentifikasi mineral yang terdapat di dalam setiap bijih sebelum dan sesudah dioksidasi. Pada analisa ini akan terlihat perubahan butir mineral di bawah pemantauan mikroskop dan memantau apakah proses biooksidasi dengan menggunakan mikrob dapat berjalan atau tidak.
Gambar 12 Mikroskop stereo binokuler X-Ray Diffraction Test (XRD)
3 pada goniometer dan secara bertahap diputar saat dibombardir dengan sinar-X, aktivitas ini menghasilkan pola difraksi bintik-bintik jarak teratur yang dikenal sebagai refleksi (Dinnebier & Friese 2003). Gambar dua dimensi yang diambil pada rotasi yang berbeda yang diubah menjadi model tiga dimensi. Hasil yang diharapkan dari pengujian ini adalah untuk mengetahui kandungan mineral sulfida yang terdapat di dalam bijih.
Gambar 13 Mesin x-ray diffraction endeavour D4 Fire Assay Test
Fire Assay adalah pengujian untuk mengetahui seberapa besar kandungan emas pada suatu bijih dengan menggunakan tungku kupelasi dan Atomic Adsorbtion Spectrophotometri (AAS) (Gambar 14). Jika dilakukan pada bullion dengan standar internasional, metode ini dapat mengukur secara akurat pada logam emas untuk 1 bagian dalam 10.000. Akurasi pada bahan bijih biasanya terbatas pada 3-5% dari nilai yang dilaporkan (Clark et al. 1999). Dalam kasus fire assay emas, lamanya waktu untuk melaksanakan tes diimbangi dengan melakukan sejumlah besar tes secara bersamaan di laboratorium khusus yang dilengkapi dengan beberapa tungku fusi dan kupelasi. Keuntungan utama dari fire assay adalah dapat menggunakan sampel besar dan dapat meningkatkan akurasi dalam menganalisis bijih kadar rendah pada kisaran ≤ 1 g/ton.
4
Flotasi adalah suatu proses pemisahan mineral berharga (emas) dari mineral tidak berharga menggunakan perbedaan sifat permukaan partikel dari beragam mineral. Proses ini menggunakan alat Denver Flotation Machine (Gambar 15). Rougher Flotation Test adalah pengujian untuk mengetahui seberapa besar mineral dapat diperoleh dengan sedikit penekanan pada kualitas konsentrat yang dihasilkan.
Gambar 15 Proses flotasi mineral berharga dengan denver flotation machine Proses flotasi secara umum dideskripsikan pada grafik Gambar 16. Proses ini dimulai dari umpan masuk yang di-flotasi hingga menghasilkan 2 produk yaitu concentrate dan tail (sisa). Pada proses flotasi, semakin banyak konsentrat yang terambil tentunya semakin baik, dengan kata lain nilai perolehan (recovery) nya tinggi. Perbandingan antara umpan masuk dengan konsentrat ditambah tailing dikenal dengan istilah Material Balance.
Gambar 16 Skema proses flotasi (Wills 2005)
Untuk mengetahui seberapa besar nilai perolehan (recovery) pada setiap pengolahan bijih yang dilakukan, digunakan persamaan Material Balance dan Metalurgical Balance sebagai berikut:
Material Balance : F = C + T (1) Metalurgical Balance : Ff = Cc + Tt (2) Mass Yield : �
� (3)
Recovery : ��
��
(4)
5 C = Concentrate ; c = Kadar di dalam Concentrate,
T = Tailing (Sisa) ; t = Kadar di dalam Tailing. Isolasi Acidithiobacillus sp. dari Air Asam Tambang
Isolasi Acidithiobacillus sp. yang terdapat dalam air asam tambang dilakukan dalam 3 tahapan dengan media cair dan padat (Priramadani 2008). Sampel air asam tambang diambil dari lokasi tambang terbuka dan tambang bawah tanah sebanyak 108 sampel. Masing-masing sampel diambil sebanyak 1 ml dan dicampur dengan 10 ml media pertumbuhan Acidithiobacillus ferooxidans Leathen (Widyati & Hazra 2007) untuk diisolasi. Tahap pertama pada proses ini adalah memanaskan media agar semua bahan terlarut dengan sempurna dan disterilisasi dengan otoklaf pada suhu 121ºC tekanan 1 ATM selama 15 menit. Setelah selesai, media dimasukkan ke dalam tabung reaksi steril. Setelah media siap selanjutnya diambil masing-masing 1 ml sampel air asam tambang dan dimasukkan ke dalam masing-masing tabung diatas. Kultur tersebut kemudian diinkubasi pada shaker dengan kecepatan 250 rpm pada suhu kamar. Pertumbuhan Acidithiobacillus sp. ditandai dengan berubahnya warna medium menjadi kuning karat (Bramantyo 2008).
Setelah mendapatkan 5 isolat terbaik dari air asam tambang, percobaan dilanjutkan pada proses seleksi. Pada proses ini isolat dicampur dengan media tumbuh Acidithiobacillus ferooxidans pada Tabel 1 tanpa FeSO4. Sebagai pengganti
sulfur yang terdapat pada FeSO4, digunakan bijih pirit dengan kandungan 95,4%.
[image:30.595.129.510.444.550.2]Seleksi dilakukan dalam waktu 15 hari dengan parameter penurunan nilai pH terendah dan perubahan warna menjadi kuning karat. Proses seleksi memilih 2 isolat terbaik, kemudian populasi dihitung dengan metode Most Probable Number (Sutton 2010).
Tabel 1 Komposisi media Acidithiobacillus ferooxidans cair
No. Bahan Unsur Kimia g.l-1
1. Dipotassium phosphate K2HPO4 0,50
2. Ammonium sulphate (NH4)2SO4 3,00
3. Calcium Nitrate Ca(NO3)2 0,01
4. Ferrous sulphate FeSO4.7H2O 30,00
5. Magnesium sulphate MgSO4.7H2O 0,50
6. Potassium chloride KCl 5,00
Seleksi Acidithiobacillus sp. dari Air Asam Tambang dan Acidithiobacillus
ferooxidans ICBB-CC
Selain Acidithiobacillus sp. dari lokasi penambangan, penelitian ini juga menggunakan Acidithiobacillus ferooxidans koleksi ICBB. Acidithiobacillus ferooxidans ICBB yang digunakan adalah ICBB 8789, ICBB 8790, ICBB 8793, ICBB 8795, ICBB 8796 dan ICBB 8797. Proses seleksi dilakukan dengan metode yang sama pada saat seleksi Acidithiobacillus sp. dari lokasi penambangan, Acidithiobacillus ferooxidans ICBB ini diuji kemampuannya dalam menurunkan kadar pirit yang terdapat pada bijih tipe-D. Acidithiobacillus ferooxidans paling efektif dalam mengurangi kandungan pirit pada bijih tipe-D akan dipilih untuk proses biooksidasi (Rawlings 2005).
6
Penurunan kadar pirit di dalam bijih tipe-D dilakukan dengan proses biooksidasi. Proses ini dilakukan dengan mencampurkan bijih sulfida sebanyak masing-masing 2 kg dengan media Leathen tanpa FeSO4 sebanyak 2 liter.
Acidithiobacillus sp. 8N1.8 dan 8N1.9 yang berasal dari air asam tambang dan Acidithiobacillus ferooxidans ICBB 8793 dan ICBB 8795 masing masing sebanyak 100 ml kemudian diinokulasikan ke dalam campuran media tumbuh. Percobaan ini dilakukan di dalam botol/akuarium kaca yang dialiri udara oleh aerator serta disirkulasikan dengan menggunakan pompa sirkulator supaya media selalu mengalir dan berputar dari atas ke bawah sehingga seluruh permukaan konsentrat dapat teraliri media (Syed 2011). Perlakuan pada bijih tipe-D terhadap isolat Acidithiobacillus sp. dan Acidithiobacillusferooxidans dijabarkan sebagai berikut :
a. Faktor pertama adalah bijih yang terdiri dari:
- Bijih tipe-D 3445 dengan kandungan pirit 92% dari tambang terbuka - Bijih tipe-D 3625 dengan kandungan pirit 15,7% dari tambang terbuka b. Faktor kedua adalah Isolat A. ferooxidansyang terdiri dari:
- Acidithiobacillus sp. 8N1.8 - Acidithiobacillus sp. 8N1.9
- Acidithiobacillus ferooxidans ICBB 8793 - Acidithiobacillus ferooxidans ICBB 8795
4
HASIL DAN PEMBAHASAN
Karakterisasi Bijih Tipe-D
[image:32.595.134.511.254.298.2]Pengujian awal terhadap kedua tipe bijih yang diambil dari lokasi penambangan dilakukan melalui 3 proses pengujian. Pengujian pertama adalah untuk mengetahui seberapa banyak kandungan pirit, mineral teroksidasi dan kandungan emas dengan menggunakan metode fire assay dan x-ray diffraction test (Lampiran 1). Hasil dari 3 proses pengujian menunjukkan kandungan mineral emas, pirit dan mineral teroksidasi yang terdapat di dalam bijih tipe-D 3445 dan 3625 yang dapat dilihat pada Tabel 2.
Tabel 2 Kandungan total di dalam umpan bijih tipe-D
Sampel ID Py (%) CuOx(%) Au (g/t)
Bijih Tipe-D 3445 92 0,005 0,179
Bijih Tipe-D 3625 15,7 0,029 0,132
[image:32.595.168.475.439.668.2]Pengujian kedua terhadap bijih tipe-D adalah untuk mengetahui nilai perolehan pada proses pengolahan. Flotation Test dilakukan dengan menggunakan mesin Denver Flotation Machine dan hasil pada kedua bijih tipe-D digambarkan pada Gambar 17 dan Tabel 3. Pada Tabel 3 menjelaskan bahwa dengan kandungan pirit yang tinggi akan menurunkan nilai perolehan (recovery) pada proses flotasi (Lampiran 2). Pada bijih tipe-D 3445 memiliki kandungan pirit sebesar 92%, saat proses flotasi, nilai perolehan (recovery) hanya sebesar 23,33%. Begitu juga dengan bijih tipe-D 3625 yang memiliki kandungan pirit sebesar 15,7%, saat proses flotasi nilai perolehan (recovery) nya sebesar 74,12%.
Gambar 17 Analisa butir dan proses flotasi bijih tipe-D 3445 (kiri) dan bijih tipe-D 3625 (kanan) sebelum biooksidasi
Tabel 3. Kandungan total di dalam konsentrat bijih tipe-D
Sampel ID Mass Yield Ro Con Assay Rougher Recovery (%) Cu(%) Au (g/t) Cu (%) Au(%)
[image:32.595.134.534.725.771.2]2
Bijih Tipe-D 3625 28,13 2,83 0,35 92,10 74,12 Isolasi Acidithiobacillus sp. dari Air Asam Tambang
[image:33.595.152.394.208.386.2]Air asam tambang diambil dari lokasi penambangan terbuka Grasberg di Bottom Pit, 8 North dan PAD 0,1 4, 5, 8, C dan tambang bawah tanah di wilayah Big Gossan, DMLZ, Amole Portal dan Wanagon Drainage Drift. Proses isolasi pertama terdapat 28 sampel yang mengalami perubahan dari warna bening menjadi kuning karat (Gambar 18). Total 28 sampel yang tumbuh tersebut berasal dari lokasi penambangan terbuka di lokasi 8 North (14 sampel), Bottom Pit (4 sampel), PAD 0 (4 sampel), PAD 1 (1 sampel) dan PAD8 (5 sampel).
Gambar 18 Hasil isolasi Acidithiobacillus sp. dari sampel air asam tambang PTFI tahap pertama
Pada tahap kedua, dari 28 sampel yang diisolasi, terdapat 12 isolat yang tumbuh dan berubah warna. 10 isolat yang tumbuh sebelum hari ke-3 dan 2 isolat tumbuh di hari ke-6 yang dapat dilihat pada Gambar 19.
Gambar 19 Hasil isolasi Acidithiobacillus sp. dari sampel air asam tambang PTFI tahap kedua
[image:33.595.150.397.477.661.2]3
Gambar 20 Hasil isolasi Acidithiobacillus sp. dari sampel air asam tambang PTFI tahap ketiga
Kelima isolat ini kemudian diseleksi dengan cara diuji kemampuannya untuk mengurangi kadar pirit pada bijih tipe-D. Pengujian ini bertujuan untuk mencari dua isolat terbaik yang mampu mengurangi kadar pirit dengan parameter perubahan warna dari bening menjadi kuning karat dan penurunan pH paling cepat.
Seleksi Acidithiobacillus sp. dari Air Asam Tambang dan Acidithiobacillus
ferooxidans Koleksi ICBB-CC
Seleksi Acidithiobacillus sp. dari Air Asam Tambang
Seleksi Acidithiobacillus sp. dari air asam tambang dilakukan dengan mencampurkan masing-masing 5 isolat yang didapat dari isolasi pada tahap sebelumnya dengan bijih pirit 95,4%. Percobaan ini dilakukan selama 15 hari dan diamati perubahannya. Dua parameter yang menjadi acuan adalah penurunan nilai pH terendah dan perubahan warna media dari bening menjadi kuning karat (Gambar 21). Setelah 15 hari perlakuan, didapatkan isolat Acidithiobacillus sp. 8N1.8 dan 8N1.9 menurunkan nilai pH paling rendah pada hari ke 2 dan 3 menjadi 2,38 dan 2,20 (Gambar 22). Dua isolat Acidithiobacillus sp. inilah yang kemudian digunakan untuk percobaan berikutnya (Lampiran 6)
[image:34.595.148.496.579.719.2]4
Gambar 22 Grafik penurunan pH media Acidithiobacillus sp. yang diisolasi dari air asam tambang PTFI
Seleksi Acidithiobacillus ferooxidans Koleksi ICBB-CC
Percobaan ini juga menggunakan Acidithiobacillus ferooxidans koleksi ICBB sebanyak 6 isolat selain dari Acidithiobacillus sp. yang diisolasi dari air asam tambang. Acidithiobacillus ferooxidans koleksi ICBB yang akan digunakan adalah nomor ICBB 8789, ICBB 8790, ICBB 8793, ICBB 8795, ICBB 8796, dan ICBB 8797. Sebelum di uji, Acidithiobacillus ferooxidans asal ICBB tersebut diremajakan terlebih dahulu dengan media cair (media Leathen). Proses peremajaan dilakukan selama 8 minggu karena Acidithiobacillus ferooxidans tersebut sudah lama tidak aktif dan disimpan di dalam lemari pendingin.
Gambar 23 Seleksi Acidithiobacillus ferooxidans ICBB-CC di dalam media tumbuh yang mengandung bijih pirit
Setelah peremajaan, kemudian dilakukan seleksi pada keenam isolat ICBB selama 14 hari. Parameter seleksi Acidithiobacillus ferooxidans terbaik adalah penurunan pH tercepat (Gambar 24) dan perubahan media dari bening menjadi kuning karat (Gambar 23). Hasil seleksi pada 6 isolat tersebut dipilih 2 isolat terbaik berdasarkan nilai pH terendah yaitu ICBB 8793 dan ICBB 8795 (Lampiran 7).
Kedua Acidithiobacillus ferooxidans koleksi ICBB-CC ini yang akan digunakan untuk pengujian lebih lanjut untuk percobaan biooksidasi. Sebelum dilakukan uji biooksidasi, keempat Acidithiobacillus terbaik asal penambangan dan koleksi ICBB dianalisa terlebih dahulu populasinya dengan metode MPN (Most Probable Number) pada Lampiran 8.
2.15 2.35 2.55 2.75 2.95
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
pH
Hari ke-
Acidithiobacillus sp. 8N1.8 Acidithiobacillus sp. 8N1.9 Acidithiobacillus sp. 8N1.12 Acidithiobacillus sp. 8N3.19 Acidithiobacillus sp. BP3.23
[image:35.595.82.473.381.531.2]5
Gambar 24 Grafik penurunan pH media Acidithiobacillus ferooxidans ICBB-CC Biooksidasi Bijih Tipe-D dengan Acidithiobacillus sp. dan Acidithiobacillus
ferooxidans
Bijih tipe-D 3445 dioksidasi dengan 4 Acidithiobacillus terbaik (Gambar 25). Hasil dari oksidasi tersebut dianalisa dan diamati perubahannya mulai dari bentuk fisik, warna, perubahan kandungan mineral yang terdapat di dalamnya dan peningkatan perolehan pada proses pengolahan dengan cara flotasi. Hasil yang cukup signifikan dapat terlihat pada bijih tipe-D 3445 yang menunjukkan perubahan fisik dari warna hitam menjadi kuning karat (Gambar 26). Selain perubahan warna, bijih diamati bentuk fisiknya di bawah mikroskop binokuler dengan perbesaran 64x (Gambar 27). Hasil pengamatan di bawah mikroskop ini, terlihat jelas perubahan yang dialami oleh bijih tipe-D yang sebelumnya tidak ada mineral yang teroksidasi menjadi terdapat mineral yang teroksidasi oleh aktivitas baik Acidithiobacillus sp. dari air asam tambang maupun Acidithiobacillus ferooxidans koleksi ICBB-CC. Pada proses oksidasi, aktivitas bakteri Acidithiobacillus membentuk biofilm yang dapat dilihat pada Gambar 26.
Gambar 25 Proses biooksidasi dengan menggunakan botol plastik dan aerator
1.20 1.70 2.20 2.70
0 1 2 3 4 5 6 7 8 9 1011121314
pH
Hari ke-
A.ferooxidans ICBB 8789 A.ferooxidans ICBB 8790 A.feroosidans ICBB 8793 A.ferooxidans ICBB 8795 A.ferooxidans ICBB 8796 A.ferooxidans ICBB 8797
[image:36.595.222.422.440.584.2]6
Gambar 26 Perubahan bijih tipe-D 3445 yang belum di oksidasi (kiri) dan sudah teroksidasi (kanan)
Gambar 27 a. Bijih tipe-D belum teroksidasi; b. Teroksidasi oleh Acidithiobacillus sp. 8N1.8; c. Teroksidasi oleh Acidithiobacillus sp. 8N1.9; d. Teroksidasi oleh A.ferooxidans ICBB 8793 dan e. Teroksidasi oleh A.ferooxidans ICBB 8793.
Selain mengoksidasi bijih tipe-D 3445 yang memiliki kandungan pirit sebesar 92%, percobaan juga dilakukan dengan bijih tipe-D 3625yang memiki kandungan pirit sebesar 15,7%. Bijih tipe-D 3625 tersebut dioksidasi dengan 4 isolat asal lokasi penambangan dan koleksi ICBB. Hasil dari proses oksidasi pada bijih tipe-D 3625 pada Gambar 28 menunjukkan perubahan fisik dari warna putih menjadi kuning karat (Jerez 2013).
7 oleh Acidithiobacillus ferooxidans koleksi ICBB-CC dan Acidithiobacillus sp. yang berasal dari air asam tambang.
Gambar 28 Perubahan bijih tipe-D 3625 yang belum teroksidasi (kiri) dan yang sudah teroksidasi (kanan)
Gambar 29 a. Bijih tipe-D 3625 belum teroksidasi; b. Teroksidasi oleh Acidithiobacillus sp. 8N1.8; c. Teroksidasi oleh Acidithiobacillus sp. 8N1.9; d. Teroksidasi oleh A.ferooxidans ICBB 8793 dan e. Teroksidasi oleh A.ferooxidans ICBB 8793.
Hasil Uji Biooksidasi pada Bijih Tipe-D 3445 dan 3625 Pengukuran Kandungan Pirit dengan Metode X-ray Diffraction Test
Analisa X-ray Diffraction Test (XRD) dilakukan untuk mengukur kandungan pirit pada bijih Tipe-D yang sudah dioksidasi. Hasil pengukuran terhadap bijih tipe-D 3445 setelah dilakukan proses biooksidasi oleh 4 Acidithiobacillus asal penambangan dan ICBB, kandungan pirit yang terdapat pada bijih menurun secara signifikan (Gambar 30).
Gambar 30 Penurunan kandungan pirit pada bijih tipe-D 3445 selama proses biooksidasi dengan menggunakan Acidithiobacillus
70.00 75.00 80.00 85.00 90.00 95.00
0 1 2 3 4 5 6 7
K
an
d
u
n
g
an
Pi
ri
t
(%
)
Hari ke-
Acidithiobacillus sp 8N1.8
Acidithiobacillus sp 8N1.9
A.ferooxidans ICBB 8793
A.ferooxidans ICBB 8795
[image:38.595.152.516.587.724.2]8
[image:39.595.95.456.264.347.2]Tabel 4 dan Gambar 30 menjelaskan bahwa semua bakteri dapat menurunkan kandungan pirit pada bijih tipe-D 3445. Penurunan kandungan pirit paling besar terjadi pada hari ke-2 oleh Acidithiobacillus sp. 8N1.8 dari 92% menjadi 74,37% atau penurunan sebesar 19,16% dan Acidithiobacillus sp. 8N1.9 dari 92% menjadi 72,56% pada hari ke-3 atau penurunan sebesar 21,13%. A.ferooxidans ICBB 8793 menurunkan kandungan pirit dari 92% menjadi 76,66% dalam waktu 7 hari atau penurunan sebesar 16,67% sedangkan A.ferooxidans ICBB 8795 menurunkan kandungan pirit dari 92% menjadi 76,50% dalam waktu 6 hari atau penurunan sebesar 16,84%. Hal ini membuktikan bahwa isolat yang berasal dari lokasi yang sama dengan bijih akan lebih efektif dalam proses biooksidasi untuk menurunkan kadar pirit (Larsson et al. 2007).
Tabel 4 Penurunan kandungan pirit pada bijih tipe-D 3445 selama proses biooksidasi dengan menggunakan Acidithiobacillus
Isolat kandungan pirit setelah oksidasi (%) hari ke- Penurunan Pirit (awal - terendah)
% penurunan
pirit
Acidithiobacillus sp.8N1.8 74,37 2 17,63 19,16
Acidithiobacillus sp.8N1.9 72,56 3 19,44 21,13
A.ferooxidans ICBB 8793 76,66 7 15,34 16,67
A.ferooxidans ICBB 8795 76,50 6 15,50 16,84
[image:39.595.103.471.423.536.2]Pada bijih tipe-D 3625 dengan kandungan pirit 15,7%, rata-rata isolat memiliki kemampuan menurunkan kandungan pirit menjadi antara 3-4% (penurunan sebesar 77-79%) dalam waktu yang bervariasi antara 2 hingga 6 hari (Gambar 31).
Gambar 31 Penurunan kandungan pirit pada bijih tipe-D 3625 selama proses biooksidasi dengan menggunakan Acidithiobacillus
Penurunan kandungan pirit paling besar didapatkan pada hari ke-2 oleh A.ferooxidans ICBB 8795 dari 15,7% menjadi 3,20% (penurunan 79,61%) dan Acidithiobacillus sp. 8N1.9 dari 15,7% menjadi 3,23% pada hari ke-5 (penurunan 79,42%). A.ferooxidans ICBB 8793 menurunkan kandungan pirit dari 15,7% menjadi 3,35% dalam waktu 6 hari (penurunan 78,66%) dan Acidithiobacillus sp. 8N1.8 menurunkan kadar pirit dari 15,7% menjadi 3,48% dalam waktu 4 hari (penurunan 77,83%) (Tabel 5).
2.00 4.00 6.00 8.00 10.00 12.00 14.00 16.00
0 1 2 3 4 5 6 7
K an d u n g an Pi ri t (% ) Hari ke-
Acidithiobacillus sp 8N1.8
Acidithiobacillus sp 8N1.9
A.ferooxidans ICBB 8793
A.ferooxidans ICBB 8795
9 Tabel 5 Penurunan kandungan pirit pada bijih tipe-D 3625 selama proses
biooksidasi dengan menggunakan Acidithiobacillus
Isolat Kandungan Pirit terendah (%) Hari ke- Penurunan Pirit (awal - terendah)
% Penurunan
Pirit
Acidithiobacillus sp.8N1.8 3,48 4 12,22 77,83
Acidithiobacillus sp.8N1.9 3,23 5 12,47 79,42
A.ferooxidans ICBB 8793 3,35 6 12,35 78,66
A.ferooxidans ICBB 8795 3,20 2 12,50 79,61
Hal ini tidak jauh berbeda dengan yang dilakukan oleh Nagaoka pada tahun 1999 bahwa penurunan kadar pirit dengan biooksidasi menggunakan bakteri dapat menurunkan kandungan pirit menjadi antara 77% - 95%.
Pengukuran Kandungan Mineral Teroksidasi dan Kandungan Emas dengan Metode Fire Assay
Biooksidasi pada kedua bijih tipe-D menyebabkan kandungan mineral teroksidasi meningkat. Kandungan mineral teroksidasi pada bijih tipe-D 3445 meningkat dari 0,005% menjadi 0,011% - 0,070% pada minggu pertama dan menjadi 0,039% - 0,120% pada minggu ketiga (Gambar 32a) tetapi menurun pada minggu ke-8. Sementara pada bijih tipe-D 3625, kandungan mineral teroksidasi meningkat dari 0,029% menjadi 0,060% - 0,083% pada minggu pertama dan menjadi 0,064% - 0,124% pada minggu ketiga dan menurun pada minggu ke-8 (Gambar 32b). Penurunan kandungan mineral teroksidasi pada minggu kedelapan terjadi karena terdapat kemungkinan bahwa proses oksidasi yang terjadi sebelumnya kembali tereduksi dan menyebabkan turunnya kandungan mineral teroksidasi, namun perlu dilakukan penelitian lebih lanjut untuk membuktikan analisa ini.
Gambar 32 Kandungan mineral teroksidasi pada bijih tipe-D 3445 (a) dan 3625 (b) Selain dari pengukuran terhadap kandungan mineral teroksidasi, pengujian terhadap kenaikan kandungan emas setelah mengalami oksidasi juga dilakukan terhadap kedua jenis bijih tipe-D. Kandungan emas dalam bijih tipe-D 3445 meningkat dari 0,179 g/ton menjadi 0,190 - 0,241 g/ton (6% - 35%) pada minggu
0 0.05 0.1 0.15
0 1 3 8
Cu
Ox(%
)
Minggu ke-
Acidithiobacillus sp 8N1.8
Acidithiobacillus sp 8N1.9
A.ferooxidans ICBB 8793
A.ferooxidans ICBB 8795
0 0.05 0.1 0.15
0 1 3 8
[image:40.595.139.518.476.684.2]10
pertama dan menjadi 0,199 - 0,253 g/ton (6% - 41%) pada minggu ketiga (Gambar 33a). Pada bijih tipe-D 3625, oksidasi dengan menggunakan Acidithiobacillus baik yang berasal dari air asam tambang dan koleksi ICBB-CC dapat meningkatkan kandungan emas dari 0,077 g/ton menjadi 0,110 - 0,133 g/ton (43% - 73%) pada minggu pertama dan menjadi 0,150 - 0,160g/ton (95% - 107%) pada minggu ketiga (Gambar 33b).
Peningkatan kandungan emas yang terdapat di dalam bijih tipe-D pada pengukuran minggu ke-1, ke-3 dan ke-8 ini disebabkan oleh terurainya ikatan sulfida yang menutup bijih emas secara keseluruhan maupun sebagian (Wills 2005) oleh karena proses biooksidasi. Dengan terbebaskannya bijih emas yang terperangkap dari ikatan sulfida (pirit), bijih emas dapat terbaca oleh Atomic Adsorbtion Spectrophotometer (AAS). Selain itu, peningkatan kandungan emas yang terbaca juga akibat dari titik lebur emas (1064,18C) lebih rendah dari pirit (1164C), jadi pada saat proses kupelasi (Fire Assay) mencapai suhu lebur emas, emas yang terekspose akan melebur sementara pirit masih belum melebur. Kondisi inilah yang menyebabkan mengapa pembacaan kandungan emas tiap minggunya meningkat.
Gambar 33 Kandungan emas bijih tipe-D 3445 (a) dan 3625 (b) Peningkatan Nilai Perolehan (Recovery) pada Bijih Tipe-D 3445 dan 3625
dengan Metode Flotasi
Pada percobaan sebelumnya, telah teruji bahwa dengan biooksidasi dapat menurunkan kadar mineral sulfida (pirit) dan menguraikan bijih emas yang terperangkap. Dengan terurainya ikatan sulfida (pirit), nilai perolehan (recovery) emas pada proses pengolahan dengan metode flotasi akan meningkat (Fernando 2000). Untuk membuktikan hal ini, dilakukan uji flotasi pada kedua bijih tipe-D yang sudah teroksidasi pada percobaan sebelumnya.
Pengujian awal flotasi pada bijih tipe-D 3445, nilai perolehan (recovery) emas individu adalah 23,33% dan bijih tipe-D 3625 adalah 74,12%, untuk mengetahui apakah bijih yang telah teroksidasi, dilaku