RIWAYAT HIDUP
Penulis dilahirkan di Bumi Jaya, pada tanggal 11 Maret 1990, sebagai anak keempat dari lima bersaudara, putri dari Bambang Trinarwanto S.Pd dan Rohiyati.
Jenjang pendidikan diawali dari Sekolah Dasar (SD) di SD Negeri 1 Bumi Jaya, diselesaikan pada tahun 2002. Sekolah Menengah Pertama (SMP) di SMP Negeri 2 Negara Batin diselesaikan pada tahun 2005, dan Sekolah Menengah Atas (SMA) di MAN 1 Metro diselesaikan pada tahun 2008. Tahun 2008, penulis terdaftar sebagai Mahasiswa Jurusan Kimia FMIPA Unila melalui jalur SNMPTN (Seleksi Nasional Masuk Perguruan Tinggi Negeri).
Motto
“
Wattaqullaah wa yu’allimukumullaah,wallaahu bikulli
syai-
in ‘aliim”
Bertakwalah pada Allah maka Allah akan mengajarimu.
Sesungguhnya Allah Maha Mengetahui segala sesuatu.
(Al-Baqorah : 282)
Berusaha dan berdo’a serta rasa syukur merupakan
kunci
dari kebahagian dan kesuksesan.
(Dewi Kartika Sari)
Kebanyakan dari kita tidak mensyukuri apa yang sudah
kita miliki, tetapi kita selalu menyesali apa yang belum kita
capai.
(Schopenhauer)
Apa yang anda lakukan saat ini, itulah yang menentukan masa
depan anda.
ABSTRACT
IDENTIFICATION OF ACTIVE COMPOUNDS FROM THE SHELL OF KERANJI TREE (Dalium indum) AS CORROSION
INHIBITOR OF MILD STEEL
By
Dewi Kartika sari
In this study, the efficacy of active compounds isolated from the shell of keranji tree (Dalium indum) was tested as corrosion inhibitor of mild steel in corrosion media of brine solution concentrated with carbondioxide gas. Isolation of the active compounds was carried our by maseration method using methanol, followed by fractination using chloroform and ethylacetate. Both fractions were found to active as corrosion inhibitor, however the ethylacetate fraction was found to work much better. Corrosion inhibition was determinded using two methods of weight loss measurement and potentiodynamic polarization. The extract sample is characterized by FT-IR and sufface of mild steal is caracterized by SEM-EDS. Experiment without corrosion inhibitor resulted in corrosion rate of 1.179 mmpy. Measurement of corrosion rate using the weight loss method indicated that the optimum concentration of the ethylacetate fraction was 200 ppm, resulted in corrosion rate reduction to 0.534 mmpy which correspond to 54.7% corrosion protection. Using the potentiodynamic polarization method, it was found that the optimum concentration was 250 ppm with Icorr of -6.91448 mA, which correspond to corrosion rate of 0.427 mmpy or 63.84% corrosion protection.
ABSTRAK
IDENTIFIKASI SENYAWA AKTIF DARI KULIT BUAH ASAM KERANJI (Dalium indum) SEBAGAI INHIBITOR KOROSI BAJA LUNAK
Oleh
Dewi Kartika Sari
Telah dilakukan penelitian tentang identifikasi senyawa yang aktif sebagai inhibitor korosi dari kulit buah asam keranji (Dalium indum). Isolasi dilakukan dengan metode maserasi menggunakan metanol dilanjutkan dengan fraksinasi menggunakan dua pelarut yaitu kloroform dan etilasetat. Filtrat hasil fraksinasi selanjutnya diuji terhadap korosi baja lunak dalam medium korosi berupa air laut buatan yang dijenuhi dengan gas karbondioksida. Daya hambat korosi ditentukan dengan dua cara, yakni metode kehilangan berat dan metode potensiodinamik polarisasi. Ekstrak buah asam keranji dianalisis dengan FT-IR untuk melihat gugus fungsinya dan permukaan baja lunak dianalisis dengan SEM-EDS. Hasil penelitian menunjukkan senyawa aktif dalam fasa kloroform dan etilasetat mempunyai kemampuan untuk menghambat korosi, namun senyawa aktif dalam etilasetat bekerja jauh lebih efektif. Hasil percobaan tanpa inhibitor menunjukkan laju korosi sebesar 1,179 mmpy. Hasil percobaan menggunakan fraksi etilasetat dengan metode kehilangan berat menunjukkan bahwa konsentrasi optimum ekstrak etilasetat adalah 200 ppm, dan mampu menurunkan laju korosi hingga menjadi 0,534 mmpy setara dengan persen proteksi sebesar 54,7%. Dengan metode potensiodinamik polarisasi didapatkan konsentrasi optimum adalah 250 ppm dengan nilai Icorr sebesar -6,91448 mA. Nilai Icorr ini menunjukkan laju korosi sebesar 0,427 mmpy dan setara dengan persen proteksi sebesar 63,84%.
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini telah dilaksanakan dari bulan Juli sampai Oktober 2012 di
Laboratorium Biomassa FMIPA Unila.
B. Alat dan Bahan
Alat yang digunakan dalam penelitian ini adalah alat-alat gelas yang digunakan
dalam laboratorium; timbangan analitik, autoklaf, orbital shaker, rotary evaporator,
alat pengukuran potensiostat, Scanning Electron Microscope (SEM), dan
Spectrophotometri Fourier Transform Infrared (FT-IR)(varian 2000 scimitar series).
Bahan yang digunakan adalah buah asam keranji yang telah dikeringkan dan
dihaluskan, yang diperoleh dari Banten. Mild steel (2x1) cm2 tebal 0,1 cm, kertas
abrasif dengan grit 240,400, 600, dan 800. Bahan kimia yang dipakai meliputi
etilasetat, metanol, aseton, akuades, kloroform, dan silika gel Merck kiesegal 60 F254
21
C. Prosedur Penelitian
1. Pengumpulan dan persiapan sampel
Sampel berupa buah asam keranji diambil dari daerah Banten, kemudian buah asam
keranji tersebut dipisahkan antara kulit, daging buah dan bijinya. lalu dikeringkan
dan dihaluskan hingga menjadi serbuk halus.
1.1. Persiapan spesimen baja lunak (mild steel)
Spesimen baja lunak dipotong-potong dengan lebar 1 cm dan panjang 2 cm kemudian
diamplas dengan kertas abrasif mulai dari grit 240, 400, 600 dan terakhir dengan grit
800. Setelah permukaan mild steel rata atau homogen selanjutnya dibersihkan
dengan akuades, dan larutan aseton kemudian disimpan dalam desikator. Permukaan
logam tersebut diukur dimensinya lalu ditimbang massanya.
1.2. Pembuatan larutan inhibitor
Ekstrak kasar buah asam keranji yang diperoleh kemudian dibuat larutan induk
sebesar 10.000 ppm dengan melarutkan 0,5 kg ekstrak kasar buah asam kranji dalam
50 mL akuades.
1.3. Larutan medium korosif
Air laut buatan (brine solution) dibuat dengan melarutkan NaCl 3% (w/v) dan
NaHCO3 100 mg/L dengan akuades dalam labu ukur. Larutan ini dijenuhkan dengan
22
2. Ekstraksi buah asam keranji
Sebanyak 0,5 kg buah asam keranji yang telah dihaluskan, dimaserasi dengan
menggunakan 1,5 L metanol selama 3 hari. Ekstrak metanol yang diperoleh disaring
kemudian dipekatkan dengan rotary evaporator pada suhu 45-50˚C dengan laju
putaran 120-150 rpm. Sehingga diperoleh fitrat pekat, kemudian filtrat pekat tersebut
diekstraksi dengan kloroform dan etilasetat.
3. Pengujian sampel
3.1. Uji korosi dengan metode kehilangan berat (weight loss)
Larutan korosi yang digunakan telah disiapkan ke dalam botol gelas sebanyak
masing-masing 100 mL dengan suhu 250C. Larutan induk inhibitor yang telah
dibuat ditambahkan ke dalam medium korosif sebanyak 0,5 mL agar konsentrasi
larutan menjadi 50 ppm, sedangkan untuk konsetrasi 100, 150, 200, dan 250 ppm
dibuat dengan cara yang sama. Kemudian gas karbondioksida dialirkan ke dalam
masing-masing botol selama 45 menit. Sampel mild steel yang telah ditimbang
massanya, dimasukkan ke dalam larutan medium korosif tanpa atau dengan adanya
inhibitor yang telah jenuh dengan gas karbondioksida. Selanjutnya dikocok (shaker)
selama 24 jam. Sampel kemudian dikeluarkan dan dibersihkan dengan HCl encer dan
akuades serta dibilas dengan aseton, setelah kering sampel tersebut ditimbang
23
3.2. Potensiodinamik polarisasi
Pertama-tama elektroda pembanding, elektroda bantu platina dan elektroda kerja baja
dicuci dengan menggunakan larutan medium korosif dan dibilas dengan akuades.
Setelah itu elektroda kerja, elektroda pembanding dan elektroda bantu dirangkai pada
suatu sel korosi yang disebut sebagai sel tiga elektroda dengan larutan medium
korosif sebagai elektrolitnya, kemudian dialiri gas CO2 dan selama pengukuran,
dipastikan tidak ada kontaminasi oleh oksigen. Lalu dihubungkan dengan alat
potensiostat dan komputer.
Elektroda kerja dibiarkan selama 10 menit di dalam elektrolit. Setelah itu dilakukan
polarisasi dengan menggunakan metode potensiodinamik. Potensial diatur dengan
rentang pengukuran -2 V sampai 1,5 V terhadap potensial pembanding dengan
kecepatan scan 20 mV/s. Perubahan arus yang terjadi, diukur dengan potensiostat.
Kemudian data yang didapatkan diolah untuk menentukan grafik potensiodinamik
(E terhadap log I). Sehingga dapat dihitung persen proteksi dengan Persamaan (3).
4. Analisis sampel
4.1. Analisis permukaan sampel
Morfologi sampel mild steel diamati menggunakan Scanning Electron Microscopy
(SEM) menggunakan larutan medium korosif dengan dan tanpa inhibitor setelah
24
4.2. Analisis gugus fungsi
Untuk mengidentifikasi gugus fungsi pada sampel kulit buah asam keranji diamati
menggunakan Spektrofotometer Fourier Transform Infrared (FTIR) dilakukan di
I. PENDAHULUAN
A. Latar Belakang
Korosi adalah perusakan material, terutama logam, sebagai konsekuesi dari reaksi
kimia yang terjadi dengan lingkungan. Korosi menjadi masalah ekonomi karena
menyangkut umur, penyusutan dan efisiensi pemakaian suatu bahan maupun
peralatan terutama dalam kegiatan industri. Korosi menyebabkan kerugian yang
sangat besar, Groysman and Brodsky, (2006) menyatakan biaya korosi sampai
5% dari GNP berbagai negara.
Banyak cara yang telah dilakukan untuk menghambat proses korosi, diantaranya
adalah pemilihan material, pelapisan pada permukaan logam, perlindungan
katodik, penambahan inhibitor korosi dan lain-lain (Nathan, 1977). Penggunaan
inhibitor korosi merupakan cara yang paling efektif untuk menghambat korosi,
karena dalam penggunaannya memerlukan biaya yang relatif murah dan
prosesnya sederhana.
Inhibitor korosi adalah suatu senyawa kimia dengan jumlah sedikit dapat
menurunkan laju korosi dalam media korosif dengan merubah kondisi logam.
Proses yang terjadi pada permukaan bisa sebagai adsorpsi inhibitor atau
pembentukan lapisan tipis permukaan yang tidak larut. Lapisan yang terbentuk
bahkan lebih tipis dari lapisan proteksi secara coating. Inhibitor korosi yang
2
mengandung gugus-gugus yang memiliki pasangan elektron bebas, seperti
nitrogen, sulfur, pospor, dan oksigen. Beberapa contoh senyawa yang
mengandung nitrogen yang digunakan sebagai inhibitor korosi yaitu; polimer
vinil piridina (Annand et al., 1965), imidazolina (Clewlow et al.,1993, Durnie
2000, Ilim et al.,2004), nitrit, kromat, dan fosfat (Hartati, 2003), ekstrak
tumbuhan lada, pinang, daun teh (Ilim dkk., 2008).
Berdasarkan penelitian (Ilim dkk., 2008), bahwa ekstrak buah lada, buah pinang
dan daun teh dapat digunakan sebagai inhibitor korosi baja lunak pada medium air
laut buatan yang jenuh dengan gas CO2. Inhibitor ekstrak buah pinang
mempunyai proteksi yang paling tinggi di antara inhibitor lainnya. Pada
penelitian ini difokuskan penggunaan inhibitor korosi senyawa organik yang
berasal dari bahan alam yaitu buah asam keranji (Dalium indum) karena senyawa
bahan alam lebih bersifat ramah lingkungan. Secara tradisional air rebusan dari
daun asam keranji ini telah digunakan untuk mencuci besi yang berkarat. Pada
penelitian ini dapat diketahui bahwa ekstrak buah asam keranji dapat berfungsi
sebagai inhibitor korosi.
Metode yang digunakan untuk mengektraksi buah asam keranji yaitu dengan cara
maserasi menggunakan pelarut metanol, kemudian dilakukan fraksinasi dengan
kloroform dan dilanjutkan dengan etilasetat. Medium korosi yang digunakan
adalah air laut buatan yang jenuh dengan gas CO2. Pengujian laju korosi untuk
setiap fraksi dilakukan dengan metode kehilangan berat dan potensiostat.
Identifikasi struktur dilakukan dengan menggunakan Spektrofotometri Fourier
3
terkorosi dengan atau tanpa larutan inhibitor menggunakan mikroskop pemindai
elektron-spektroskopi dispersi energi(SEM-EDS).
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengekstrak buah asam keranji dengan pelarut metanol.
2. Uji ekstrak kasar dan fraksi-fraksi sebagai inhibitor korosi dengan metode
kehilangan berat dan potensiostat.
C. Manfaat Penelitian
Penelitian ini diharapkan memberikan manfaat yaitu:
1. Dapat memberikan informasi ilmiah tentang aktifitas buah asam keranji
sebagai inhibitor korosi.
Puji syukur kepada Allah SWT
Kupersembahkan karya sederhana ini kepada :
Kedua orang tuaku,
Ayah dan Ibunda yang telah memberikan kasih sayang
serta doa untukku. Terima Kasih,
kalianlah inspirasi tuk masa depanku.
Kakak-kakak dan Adikku terkasih atas kasih sayang
kalian yang tulus padaku
Keluarga besar “
Dewi
” di J
awa dan Way Kanan yang
telah mendukungku
Seluruh sahabat terbaikku
Seseorang yang akan mendampingiku kelak
SANWACANA
Assalamualaikum Wr.Wb.
Alhamdulillahi robbil’alamin, puji syukur penulis ucapkan ke hadirat Allah SWT,
karena atas segala rahmat dan karunia-Nya skripsi ini dapat diselesaikan.
Skripsi dengan judul "Identifikasi Senyawa Aktif Dari Kulit Buah Asam
Keranji (Dalium indum) Sebagai Inhibitor Korosi Baja Lunak" adalah salah
satu syarat untuk memperoleh gelar Sarjana Sains pada Jurusan Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
Dalam pelaksanaan dan penulisan skripsi ini tidak lepas dari kesulitan dan
rintangan, namun itu semua dapat penulis lalui karena rahmat dan ridha Allah
SWT serta bantuan dan dorongan semangat dari orang-orang yang hadir
dikehidupan penulis. Dalam kesempatan ini, penulis menyampaikan terima kasih
setulus-tulusnya kepada :
1. Ayah dan ibundaku tercinta, yang selalu memberikan kasih sayang, do’a,
motivasi dan pengorbanan, yang diberikan demi kelancaran penulis dalam
menuntut ilmu.
2. Ibu Dra. Ilim, M.S., selaku pembimbing I penelitian yang telah banyak
memberikan nasihat, saran, ilmu, motivasi, perhatian, serta kesabaran dalam
membimbing penulis dalam menyelesaikan skripsi ini dan selama menjadi
3. Bapak Wasinton Simanjuntak, Ph.D., selaku pembimbing II penelitian yang
telah memberikan kritik, saran, dan arahan yang diberikan kepada penulis
sehingga skripsi ini terselesaikan dengan baik.
4. Ibu Prof.Dr.Tati Suhartati,M.S., selaku penguji penelitian yang telah
memberikan semangat, kritik, saran, dan arahan kepada penulis sehingga
skripsi ini terselesaikan dengan baik.
5. Ibu Dr. Buhani, M.Si., selaku Pembimbing Akademik atas kesediaannya untuk memberikan bimbingan, bantuan, nasehat, dan informasi yang
bermanfaat kepada penulis.
6. Bapak Andi Setiawan, Ph.D., selaku Ketua Jurusan Kimia FMIPA Unila.
7. Bapak Prof. Suharso, Ph.D., selaku Dekan Fakultas Matematika dan Ilmu
Pengetahuan Alam.
8. Seluruh dosen FMIPA Unila yang telah mendidik dan memberikan ilmu
pengetahuan yang sangat berguna kepada penulis selama kuliah.
9. Kedua orang tuaku yang sangat kucintai. Bapak tercinta Bambang Tn S.Pd
yang selalu menjadi inspirasi dan semangat dalam segala hal. Terima kasih
bapak atas do’amu yang tak putus dan segala bentuk pengorbananmu.
Mimiku tersayang ibunda Rohiyati yang selalu memberikan kasih sayang,
sabar mengahadapi aku dan selalu mendoakanku setiap waktu. Terima kasih
ibunda atas nasehat dan do’a yang tak henti kau panjatkan untukku. Dengan
tulus dan rendah hati kuucapkan terima kasih banyak atas segala hal terbaik
dan semua yang telah diberikan kepadaku serta bentuk pengorbananmu.
10. Kakak dan adikku yang sangat kusayangi Aa’ Ade Supriyatna, teteh Sri
ya atas do’a, dukungan dan selalu jadi penyemangatku. Kalian adalah
saudara terbaik bagiku. Semangat terus ya kakak dan adikku, aku sayang
kalian.
11. Keluarga besar “ abah Warga dan nenek Sutijah serta keluarga besar kakek
Sunarso dan nenek Sri Suarni”.
12. Mas Choirul Setiyo Budi yang senantiasa memberikan nasehat dan dukungan.
13. Sahabat-sahabat terbaikku (Eny Heriyani S.Si, Evi S.Si, Wanti S.Si, Albert
Ferdinan S.Si, Lenny Warlina S.Si, Raffel S.Si, Riki Fauzi S.Si dan Musrifatu
S.Si) yang setia mememani penelitianku sampai malam dan membantuku
baik dalam doa, nasehat dan upaya. Terima Kasih teman atas segala
dukungan, motivasi dan bantuan yang telah kalian berikan. Untuk
teman-temanku di laboratorium elektrokimia (Juju, Meta, Gege, Nunk, Retno, Arif
Ashari, Vinin, dan Reza) yang tidak bosan-bosannya mendengar segala keluh
kesahku, menasehati dan mendoakanku selama di kampus. Semangat dan
sukses buat penelitianya. Terima kasih teman-temanku.
14. Teman-teman satu angkatanku : Siti Oktavia Rumapea S.Si, Ayu, M.Amin,
M. Ramdan S.Si, Puji Mugianto S.Si, TB. Didi Supriadi, Eko, Majid, Sobari,
Idrus, Ruzky, Mychel, Miftahudin Ramli S.Si, Sundari Riawati S.Si, Ni Putu
Yuliastiani S.Si, Harnita, Kiki, Sofa Nurfauziah S.Si, Ricardo Novia, Nuro,
Adek Purnawati S.Si, Vivi, Ani Sulistiani S.Si, Eliana S.Si, Rudi, Putri,
Mifta, Musrifatun S.Si, Dewa, Robby, Nanda, terima kasih teman atas
dukungan, kebersamaan selama ini, keceriaan kalian disetiap hari-hariku, aku
15. Kakak-kakak Kimia 2005, 2006, 2007, dan adik-adik kimia 2009, 2010, 2011
dan 2012 FMIPA Unila terima kasih atas segala dukungannya.
16. Teman-teman kosan Elya Artika, Rega Renfilia, Ani, Ni Wayan Hermayanti,
Yunida dan Isna,. Terima kasih atas kebersamaan dan keceriaan yang sudah
kita lewati.
17. Kelompok kecil Liqo’ yang selalu mengasihi dan mendo’akanku (ani,eli, sri,
mifta, mute’) dan untuk kak Idra tutor kami. Terima kasih banyak ya ukhti,
aku sayang kalian semua.
18. Semua pihak yang telah membantu dan mendukung penulis dalam
penyusunan skripsi ini. Terima kasih.
Akhir kata, Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan.
Penulis berharap semoga skripsi yang sederhana ini dapat berguna bagi kita
semua. Amin
Bandar Lampung, 27 Febuari 2013 Penulis
II. TINJAUAN PUSTAKA
A. Pengertian Korosi
Korosi secara umum didefinisikan sebagai suatu peristiwa kerusakan atau
penurunan kualitas suatu bahan yang disebabkan oleh terjadinya reaksi antara
bahan dengan lingkungannya. Korosi pada logam (perkaratan) yaitu peristiwa
perusakan pada logam yang disebabkan oleh reaksi oksidasi. Kerusakan terhadap
logam-logam tersebut dipengaruhi oleh adanya gas oksigen, amoniak, klorida, air,
larutan garam, basa, asam, dan juga akibat arus listrik. Pada umumnya korosi
yang paling banyak terjadi adalah korosi oleh udara dan air (Fontana, 1986).
Korosi menjadi masalah ekonomi karena menyangkut umur, penyusutan dan
efisiensi pemakaian suatu bahan maupun peralatan terutama dalam kegiatan
industri. Banyak sekali kerugian yang diakibatkan oleh korosi. Kerusakan pada
pipa gas, pipa minyak, kapal, dan alat-alat lain yang terbuat dari besi atau baja.
Milyaran dollar AS telah dikeluarkan setiap tahunnya untuk merawat jembatan,
peralatan perkantoran, kendaraan bermotor, mesin-mesin industri, serta peralatan
elektronik lainnya agar konstruksinya dapat bertahan lama (Akhadi, 1991).
Keberadaan gas CO2 di dalam air dapat mempercepat reaksi korosi logam. Hal ini
disebabkan karena adanya pengaruh keasaman dari gas CO2 sehingga dapat
membentuk ion karbonat. Ion karbonat ini bertindak sebagai ligan dan
mengkatalisis reaksi pelarutan logam sehingga akan terjadi proses korosi.
5
terbentuk adalah besi karbonat (FeCO3) yang dapat mengendap pada permukaan
logam membentuk lapisan tipis (Yuliani, 2005).
Proses pencegahan korosi dapat dilakukan, diantaranya dengan pelapisan pada
permukaan logam, perlindungan katodik maupun anodik dan penambahan
inhibitor korosi (Haryono dkk, 2010). Penambahan inhibitor korosi merupakan
cara yang paling efektif untuk menghambat korosi, karena dalam penggunaanya
memerlukan biaya yang relatif murah dan prosesnya sederhana (Ilim, 2007).
B. Inhibitor Korosi
Inhibitor korosi adalah zat yang ketika ditambahkan dalam konsentrasi kecil pada
lingkungan, efektif mengurangi laju korosi logam pada lingkungan tersebut
(Rahim and Kassim, 2008). Sejumlah inhibitor menghambat korosi melalui cara
adsorpsi untuk membentuk suatu lapisan tipis dan melalui pengaruh lingkungan
(misalnya pH) menyebabkan inhibitor dapat mengendap dan selanjutnya
teradsopsi pada permukaan logam serta melindunginya terhadap korosi
(Dalimunthe, 2004). Pada umumnya inhibitor korosi berasal dari
senyawa-senyawa organik dan anorganik yang mengandung gugus-gugus yang memiliki
pasangan elektron bebas, seperti nitrit, kromat, fosfat dan senyawa-senyawa
amina (Haryono dkk., 2010).
1. Inhibitor organik
Pada umumnya senyawa-senyawa organik yang dapat digunakan sebagai inhibitor
adalah senyawa-senyawa yang mampu membentuk senyawa kompleks baik
kompleks yang terlarut maupun kompleks yang mengendap. Untuk itu diperlukan
6
membentuk ikatan kovalen terkoordinasi, yaitu atom nitrogen, belerang dan
oksigen pada suatu senyawa tertentu (Dalimunthe, 2004). Atom O, N, dan S
ditemukan memiliki kebasaan yang lebih tinggi dan kepadatan elektron dan
dengan demikian bertindak sebagai inhibitor korosi. Atom O, N, dan S adalah
pusat aktif untuk proses adsorpsi pada permukaan logam. Efisiensi inhibisi
mengikuti urutan O < N < S < P. Ketersediaan elektron tak berikatan (pasangan
elektron bebas) dalam molekul inhibitor memfasilitasi transfer elektron dari
inhibitor dengan logam. Ikatan kovalen koordinat yang melibatkan transfer
elektron dari inhibitor pada permukaan logam dapat terbentuk. Dengan demikian
terjadi adsorpsi antara permukaan logam dan inhibitor yang membentuk lapisan
pelindung pada logam (Rani and Basu, 2011).
Inhibitor organik diklasifikasikan dalam dua jenis, yaitu sintetik dan alami.
Inhibitor sintetik seringkali digunakan dalam menghambat laju korosi logam,
namun inhibitor ini selain mahal juga ternyata berbahaya bagi manusia dan
lingkungan karena bersifat toksik. Oleh karena itu saat ini sedang dikembangkan
green inhibitor (inhibitor yang ramah lingkungan) yang bersifat non-toksik,
murah, sudah tersedia di alam, mudah diperbaharui dan tidak merusak lingkungan
(El-Etre and Abdallah, 2000).
Green inhibitor ini berasal dari tumbuh-tumbuhan atau biji-bijian.
Tumbuh-tumbuhan yang digunakan biasanya yang mengandung tanin, asam-asam organik
maupun asam-asam amino, dan alkaloid yang diketahui mempunyai kemampuan
menghambat korosi (Oguzie, 2007). Green inhibitor dari tumbuhan, yang sering
7
catappa L.), sifat inhibisi dan adsorpsinya disebabkan karena adanya saponin,
tanin, flavanoid, terpen dan alkaloid (Rani and Basu, 2011).
2. Inhibitor anorganik
Inhibitor anorganik dapat menginhibisi material logam baik secara anodik atau
katodik karena memiliki gugus aktif (Wiston, 2000). Inhibitor ini terdiri dari
beberapa senyawa anorganik antara lain : fosfat, kromat, dikromat, silikat, borat,
molibdat dan arsenat. Senyawa-senyawa tersebut sangat berguna dalam aplikasi
pelapisan korosi, namun inhibitor ini memiliki kelemahan yaitu bersifa toksik
(Ameer et al., 2000).
3. Mekanisme proteksi
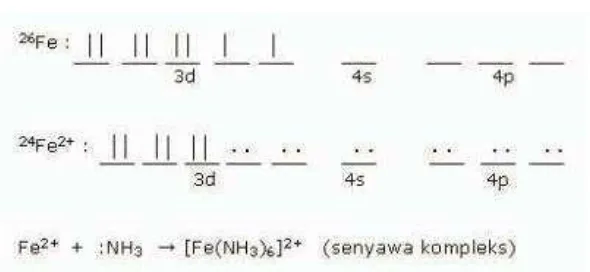
Reaksi yang terjadi antara logam Fe2+ dengan medium korosif diperkirakan
menghasilkan Fe(HCO3)2, dan oksidasi lebih lanjut menghasilkan FeCO3 yang
merupakan produk korosi yang tidak diinginkan karena mempercepat laju korosi.
Reaksi yang terjadi:
Fe (s) + 2H2CO3 Fe(HCO3)2(S) + H2 (g)
Fe(HCO3)2(s) FeCO3(s) + H2CO3
Sedangkan reaksi antara Fe2+ dengan inhibitor ekstrak etilasetat menghasilkan
senyawa kompleks sebagai produk korosi yang diharapkan dapat menghambat
laju korosi. Pada inhibitor ekstrak etilasetat diduga adanya senyawa tanin yang
mengandung gugus O-H yang diharapkan mendonorkan sepasang elektronnya
8
korosif sehingga diharapkan produk-produk korosi yang terbentuk memiliki
kestabilan yang lebih baik dibanding dengan Fe2+ saja (Haryono dkk., 2010)
Reaksi antara Fe2+ dengan inhibitor ekstrak bahan alam menghasilkan senyawa
kompleks. Inhibitor ekstrak bahan alam, misalnya yang mengandung nitrogen,
mendonorkan sepasang elektronnya pada permukaan logam mild steel ketika ion
Fe2+ terdifusi ke dalam larutan elektrolit, reaksinya adalah:
Fe → Fe2+
+ 2e- (melepaskan elektron)
Fe2+ + 2e-→ Fe (menerima elektron)
Gambar 2.1. Mekanisme proteksi (Haryono dkk. 2010).
Produk yang terbentuk di atas mempunyai kestabilan yang tinggi dibanding
dengan Fe saja, sehingga sampel besi atau baja yang diberikan inhibitor ekstrak
bahan alam akan lebih tahan (terproteksi) terhadap korosi. Contoh lainnya, dapat
juga dilihat dari struktur senyawa nikotin dan kafein yang terdapat dalam ekstrak
daun tembakau, teh, dan kopi, pada senyawa kafein dan nikotin yang mengandung
gugus atom nitrogen akan menyumbangkan pasangan elektron bebasnya untuk
mendonorkan elektron pada logam Fe2+ sehingga terbentuk senyawa kompleks
9
Banyak tanaman di Indonesia yang memiliki kandungan senyawa nitrogen atau
alkaloid, di antaranya adalah daun teh, pepaya, daun lada, lidah buaya, buah
pinang dan sebagainya. Sehingga pada penelitian ini akan digunakan tanaman
buah asam keranji sebagai inhibitor korosi baja lunak.
.
C.Asam Kranji
Asam kranji ( Dialium indum) adalah tanaman yang ditemukan di Thailand
Selatan, Malaysia, dan Indonesia. Ini termasuk dalam keluarga Leguminosae,
buah asam keranji ini biasa untuk dikonsumsi, bentuknya seperti buah anggur
berukuran kecil dengan warna ungu ketika muda dan kecokelatan bila sudah
dikeringkan. Karena dinilai kayunya yang keras dan kuat, maka spesies ini
terancam, dengan adanya penebangan liar dan pemukiman manusia. Rasa buah
ini mirip dengan asam. Di Thailand, buah asam keranji disebut dengan "Luk Yee"
atau "Yee", sedangkan di Malaysia dan Indonesia orang biasa menyebutnya
dengan nama "Keranji". Buah asam keranji ini digunakan sebagai makanan
ringan seperti permen di Thailand. Buah asam keranji juga dapat ditemukan di
negara-negara Afrika Barat seperti Sierra Leone, Senegal, Nigeria dimana dikenal
sebagai awin dalam bahasa Yoruba, icheku dalam bahasa Igbo dan kurm Tsamiyar
di Hausa (Wang, 1992).
Nama umum buah asam keranji yaitu:
Indonesia : Asam keranji, kranji, asam cina, kuranji, ki pranji (Sunda), parangi
10
(a) (b)
Gambar 2.2.Tumbuhan buah asam keranji (a). Segar (b). Kering
1. Klasifikasi
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh) Super Divisi : Spermatophyta (Menghasilkan biji)
Divisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (Berkeping dua / dikotil)
Sub Kelas : Rosidae
Ordo : Fabales
Famili : Fabaceae (Suku polong-polongan)
Genus : Dialium
Spesies : Dialium indum
2. Kandungan kimia asam kranji
Tabel 2.1 Komposisi buah asam dalam persen (%) :
11
3. Manfaat asam keranji
Buah asam ini banyak digunakan sebagai pengasam makanan di daerah
Kalimantan. Di Jakarta asam ini dulu sering dijajakan di sekolah-sekolah sebagai
jajanan anak. Bentuk buahnya sebesar kelereng, warna kulitnya jika sudah
diperam berwarna kehitaman dengan daging buah kecoklatan. Rasanya asam
namun tidak seasam asam jawa. Tapi juga ada yang manis, masyarakat
Kalimantan Barat biasa menyebutnya buah asam kranji madu. Rasanya seperti
coklat dan madu, sangat lezat.
Dilihat dari kandungan kimia dari buah asam keranji yaitu daun dan buah Dialium
indum mengandung saponin, flavonoida dan polifenol,daging buah berkhasiat
sebagai obat sariawan, gusi berdarah dan sakit diare, sedangkan rebusan daunnya
untuk mencuci besi yang berkarat. Dari kandungan kimia yang ada dalam buah
asam keranji, maka buah ini mempunyai kemampuan sebagai inhibitor
korosi(Wang, 1992).
D. Metode Pemisahan
Ekstraksi merupakan salah satu proses penarikan komponen/zat aktif dengan
menggunakan pelarut tertentu. Prinsip ekstraksi didasarkan pada distribusi zat
terlarut dengan perbandingan tertentu antara dua pelarut yang tidak saling
bercampur (Khopkar, 2002). Ekstraksi digolongkan ke dalam dua bagian besar
berdasarkan bentuk fasa yang diekstraksi yaitu ekstraksi cair-cair dan ekstraksi
cair-padat. Untuk ekstraksi cair-cair dapat menggunakan corong pisah, sedangkan
ekstraksi cair-padat terdiri dari beberapa cara yaitu maserasi, perkolasi dan
12
Maserasi merupakan proses ekstraksi dengan cara perendaman sampel
menggunakan pelarut organik pada suhu ruang. Proses ini sangat menguntungkan
dalam proses isolasi senyawa organik bahan alam karena dengan perendaman
sampel akan terjadi pemecahan dinding dan membran sel akibat perbedaan
tekanan di dalam dan di luar sel, sehingga metabolit sekunder yang ada dalam
sitoplasma akan terlarut dalam pelarut organik serta struktur senyawa tidak akan
mudah rusak (Harborne, 1984).
H. Metode Analisis Korosi
1. Polarisasi potensiodinamik
Polarisasi potensiodinamik adalah metode untuk menentukan perilaku korosi
logam berdasarkan hubungan potenial dan arus anodik atau katodik. Korosi
logam terjadi jika terdapat arus anodik yang besarnya sama dengan arus katodik,
walaupun tidak ada arus yang diberikan di luar sistem. Hal ini disebabkan
ada perbedaan potensial antara logam dan larutan sebagai lingkungannya
(Sunarya, 2008). Laju korosi dapat ditentukan dengan metode ini dengan
menggunakan potensiostat dengan tiga elektroda, yaitu elektroda acuan tipe
kalomel (SCE), elektroda bantu berupa platina dan elektroda kerja berupa
spesimen baja. Data yang didapat dari metode ini adalah kurva polarisasi
anodik/katodik yang menyatakan hubungan antara arus (µA/cm2) sebagai fungsi
potensial (mV). Menurut Kandias (2009) selanjutnya kurva tersebut
diekstraposisi untuk dapat menentukan laju korosi dan arus korosi melalui
Persamaan (1).
13
Rp = hambatan polarisasi
Vcorr = laju korosi Faraday
Ae = massa ekivalen logam (g/mol.ekivalen)
ρ = massa jenis logam (g/cm3)
1.1. Metode Tafel
Kecepatan atau laju korosi yang terjadi pada logam dalam lingkungan elektrolit
baik tanpa atau dengan adanya inhibitor korosi dapat dilakukan dengan
menggunakan metode Tafel. Pengukuran dengan metode Tafel untuk kinerja
inhibisi dilakukan dalam sel elektrokimia dengan sistem tiga elektroda, yaitu
sampel baja karbon sebagai elektroda kerja, elektroda Pt sebagai elektroda bantu,
dan elektroda kalomel sebagai elektroda pembanding.
Kinetika elektrokimia untuk korosi pada logam dapat dikarakterisasi dengan
menentukan tiga parameter yaitu densitas hantaran (Icorr), potensial korosi (Ecorr),
dan slop Tafel katodik (β a dan β c ). Hasil pengolahan data ketiga parameter di
atas dapat menentukan harga hambatan polarisasi (Rp) serta densitas hantaran
(Icorr) dan dari hasil kedua olahan ini dapat dinyatakan sebagai laju korosi Faraday
( Vcorr atau CF ) dalam satuan milimeter pertahun (Kandias, 2009).
Hambatan polarisasi, Rp (ohm, cm2) adalah suatu besaran yang menentukan laju
14
kurva potensial sebagai fungsi rapat arus disekitar potensial korosinya. Rp
diasosiasikan dengan hukum Stren Geary, pada Persamaan(1).
Nilai Rp ini menunjukkan laju korosi, jika nilai Rp sangat kecil maka sistem
sangat korosif. Sedangkan β a dan β c merupakan kemiringan Tafel anodik dan
Tafel katodik. β merupakan nilai terapan Stern Greary ( Fahrurrozie, 2009).
Prinsip polarisasi Tafel adalah antaraksi antarmuka antara larutan uji dengan
elektroda. Interaksi ini menimbulkan polarisasi logam dan arus tertentu.
Berdasarkan ektrapolasi Tafel ini dapat diketahui dominasi reaksi yang terjadi
antara anodik dan katodik. Jika potensial anodik dapat bergeser kearah negatif
maka polarisasi atau reaksi anodik yang berperan ditandai dengan terjadinya
oksidasi pada baja karbon. Namun jika potensial korosi bergeser kearah positif
maka reaksi katodik berperan ditandai dengan terjadinya reduksi ion-ion H+ yang
banyak.
1.2. Laju korosi
Dalam suatu sistem reaksi terdapat suatu reaksi antara komponen-komponen
didalamnya, yang secara mikro melibatkan elektron-elektron. Begitu juga dalam
proses korosi, transfer elektron menuju ke permukaan logam berlangsung secara
kesinambungan hingga secara kesetimbangan. Untuk mencapainya, biasanya
dilakukan OCP (open circuit potensial) dengan cara menstabilkan interaksi antara
larutan dengan logam (arus korosi) selama beberapa saat. Transfer elektron
tersebut merupakan parameter menentukan laju korosi logam (Sunarya, 2008).
Laju korosi dapat dilakukan dengan metode polarisasi potensiodinamik. Data
15
menyatakan hubungan arus antara arus ( ) sebagai fungsi potensial (mV).
Selanjutnya kurva tersebut diektrapoasi untuk menentukan laju korosi dan arus
melalui Persamaan (1) dan (2). Untuk menghitung persentase proteksi dari
inhibitor yang digunakan dengan menggunakan pada Persamaan (3).
% proteksi = (Icorr0 - Icorri)x 1/ Icorr0 x 100% ... (3)
Keterangan: Icorr0 = laju korosi tanpa inhibitor Icorri = laju korosi dengan inhibitor.
2. Metode kehilangan berat (weight loss)
Metode weight loss menunjukkan plot antara laju korosi terhadap waktu
perendaman merupakan persentasi inhibisi inhibitor yang dapat disusun
berdasarkan indikasi dari hambatan polarisasinya yang dapat disusun berdasarkan
indikasi dari hambatan polarisasinya serta urutan kemampuan masing-masing
inhibitor ketika terserang pada permukaan logam. Kemudian data yang diperoleh
selanjutnya digunakan untuk menghitung weight loss dengan menggunakan pada
Persamaan (4).
CR(mmpy)=10x(Wt/A)(I/D)X(365/t)………...(4)
CR = laju korosi (mmpy)
Wt = berat (gram) yaitu antara berat awal dikurang dengan berat akhir A = luas sampel (cm2)
D = density (gram/cm2)
Untuk menghitung persentase proteksi dari inhibitor yang digunakan dengan
16
% proteksi = (Cr0 - Cri)x 1/ Cr0 x 100 %...(5)
Keterangan: Cr0 = laju korosi tanpa inhibitor CRi = laju korosi dengan inhibitor.
I. Analisis Spektrofotometri
1. Spektrophotometri fourier transform infrared (FTIR)
Spektrofotometri FT-IR merupakan suatu metode yang mengamati interaksi
molekul dengan radiasi elektromagnetik yang berada pada daerah panjang
gelombang 0,75 – 1.000 µm atau pada bilangan gelombang 13.000 – 10 cm-1.
Radiasi elektromagnetik dikemukakan pertama kali oleh James Clark Maxwell,
yang menyatakan bahwa cahaya secara fisis merupakan gelombang
elektromagnetik, artinya mempunyai vektor listrik dan vektor magnetik yang
keduanya saling tegak lurus dengan arah rambatan (Hsu, 1994).
Pada dasarnya Spektrofotometer FTIR (Fourier Trasform Infra Red) adalah
hampir sama dengan Spektrofotometer IR dispersi, yang membedakannya adalah
pengembangan pada sistem optiknya sebelum berkas sinar infra merah melewati
contoh. Dasar pemikiran dari Spektrofotometer FTIR adalah dari persamaan
gelombang yang dirumuskan oleh Jean Baptiste Joseph Fourier (1768-1830)
seorang ahli matematika dari Perancis.
Pada sistem optik FTIR digunakan radiasi LASER (light amplification by
stimulated emmission of radiation) yang berfungsi sebagai radiasi yang
diinterferensikan dengan radiasi infra merah agar sinyal radiasi infra merah yang
17
Detektor yang digunakan dalam Spektrofotometer FTIR adalah TGS (tetra
glycerine sulphate) atau MCT (mercury cadmium telluride). Detektor MCT lebih
banyak digunakan karena memiliki beberapa kelebihan dibandingkan detektor
TGS, yaitu memberikan respon yang lebih baik pada frekwensi modulasi tinggi,
lebih sensitif, lebih cepat, tidak dipengaruhi oleh temperatur, sangat selektif
terhadap energi vibrasi yang diterima dari radiasi infra merah.
Vibrasi yang digunakan untuk identifikasi adalah vibrasi tekuk, khususnya vibrasi
rocking (goyangan), yaitu yang berada di daerah bilangan gelombang 2000 – 400
cm-1. Karena di daerah antara 4000 – 2000 cm-1 merupakan daerah yang khusus
yang berguna untuk identifkasi gugus fungsional. Daerah 4000 – 2000 cm-1 ini
menunjukkan absorbsi yang disebabkan oleh vibrasi regangan. Sedangkan daerah
antara 2000 – 400 cm-1 seringkali sangat rumit, karena vibrasi regangan maupun
bengkokan mengakibatkan absorbsi pada daerah tersebut. Dalam daerah 2000 –
400 cm-1 tiap senyawa organik mempunyai absorbsi yang unik, sehingga daerah
tersebut sering juga disebut sebagai daerah sidik jari (fingerprint region).
Meskipun pada daerah 4000 – 2000 cm-1 menunjukkan absorbsi yang sama, pada
daerah 2000 – 400 cm-1 juga harus menunjukkan pola yang sama sehingga dapat
disimpulkan bahwa dua senyawa adalah sama.
Pada analisis dengan spektrofotometer FTIR diharapkan gugus fungsi terlihat pita
serapan pada daerah 3500-3000 cm-1 yang menunjukkan karakteristik vibrasi ulur
OH, pita serapan diatas 3300 cm-1 yang menunjukkan karakteristik vibrasi ulur
NH amina. Pita serapan lainnya yang menunjukkan adanya vibrasi NH amina
18
primer), diharapkan muncul pita serapan pada daerah 1250-1000 cm-1 yang
menunjukkan vibrasi ulur CN, pita serapan daerah 3000-2850 cm-1 menunjukkan
karakteristik vibrasi ulur CH, pita serapan lainnya pada daerah 1470-1350 cm-1
yang menunjukkan vibrasi tekuk CH, dan pita serapan pada daerah 1250-970 cm-1
yang menunjukkan vibrasi tekuk C-O (Hsu, 1994).
Secara keseluruhan, analisis menggunakan Spektrofotometer FTIR memiliki dua
kelebihan utama dibandingkan metoda konvensional lainnya, yaitu:
1. Dapat digunakan pada semua frekuensi dari sumber cahaya secara simultan
sehingga analisis dapat dilakukan lebih cepat daripada menggunakan cara
sekuensial atau scanning.
2. Sensitifitas dari metode Spektrofotometri FTIR lebih besar daripada cara
dispersi, sebab radiasi yang masuk ke sistem detektor lebih banyak karena
tanpa harus melalui celah (slitless) (Hsu, 1994).
2. Scanning electron microscope (SEM)
Scanning Electron Microscope (SEM) adalah jenis mikroskop elektron untuk
memindai gambar permukaan suatu sampel padat dengan menggunakan sinar
elektron berenergi tinggi dalam pola pemindai pixel (Fansuri dan Martianingsih,
2011). SEM merupakan alat yang dapat digunakan untuk mempelajari atau
mengamati rincian bentuk maupun struktur mikro, topografi, morfologi
permukaan dari suatu obyek, seperti bahan logam dan polimer keramik yang tidak
dapat dilihat dengan mata atau dengan mikroskop optik.
19
dikumpulkan dengan tegangan tinggi dan berkas elektron difokuskan dengan sederetan lensa elektromagnetik. Ketika berkas elektron mengenai target,
informasi dikumpulkan melalui tabung sinar katoda yang mengatur intensitasnya. Setiap jumlah sinar yang dihasilkan dari tabung sinar katoda dihubungkan dengan jumlah target, jika terkena berkas elektron berenergi tinggi dan menembus
permukaaan target, elektron kehilangan energi, karena terjadi ionisasi atom dari cuplikan padatan. Elektron bebas ini tersebar keluar dari aliran sinar utama, sehingga tercipta lebih banyak elektron bebas, dengan demikian energinya habis lalu melepaskan diri dari target. Elektron ini kemudian dialirkan ke unit