CONTOH PERHITUNGAN
A. PadaPercobaan Ekstraksi
Asam oleat = 0.887 gr/ml
Volume sampel = 3 ml
Massa sampel = ρ x V
= 0.887 gr/ml x 3 ml
= 2.661 gr
Volume NaOH = 2,4 ml
% ��� =������������ 28.2
�����������
% ��� =2.4 � 0.1 � 28.2 2.661
% FFA = 2.543405
B. Pada Percobaan Esterifikasi
1. Perhitungan untuk katalis H2SO4 Pada Suhu 55 oC
• 15 menit
Volume NaOH 0.5 ml
% ��� =0.6 � 0.1 � 28.2 2.661
% FFA = 0,635851
%
���
=
��
����������
28.2
2. Perhitungan
untuk katalis H2SO4 Pada Suhu
60 oC
• 15 menit
Volume NaOH 0.4 ml
% ��� =0.55 � 0.1 � 28.2 2.661
% FFA = 0,582863
3. Perhitungan untuk katalis H2SO4 Pada Suhu 65 oC
• 15 menit Menit
(Waktu)
% FFA (H2SO4 0,5 %)
55 oC 60oC 65oC
15 0,635851 0,582863 0,529876
30 0,582863 0,529876 0,423901
45 0,529876 0,423901 0,370913
60 0,423901 0,370913 0,317926
75 0,317926 0,317926 0,317926
90 0,264937 0,264937 0,264937
105 0,264937 0,264937 0,21195
120 0,21195 0,21195 0,105975
Waktu
(menit)
% FFA (H2SO4 1 %)
55 oC 60oC 65oC
15 0,582863 0,529876 0,423901
30 0,529876 0,423901 0,370913
45 0,423901 0,317926 0,317926
60 0,317926 0,264937 0,264937
75 0,317926 0,264937 0,21195
90 0,21195 0,21195 0,105975
105 0,21195 0,105975 0,095377
Volume NaOH 0.8
ml
% ��� = 0.85 � 0.1 � 28.2 2.661
% FFA = 0,900789
4. Persentase Penurunan Kadar FFA Selama Proses Esterifikasi
% FFA awal = 2,5 %
% FFA pada kondisi terbaik
(waktu 120 menit, katalis H2SO4 1 % , Suhu 60 oC) = 0,095377 %
% Penurunan FFA =2,5−0,095377
2.5 � 100 %
= 96,18 % Waktu
(Menit)
% FFA (H2SO4 1,5 %)
55 oC 60oC 65oC
15 0,900789 0,900789 0,900789
30 0,847802 0,847802 0,847802
45 0,794813 0,741826 0,794813
60 0,741826 0,688838 0,741826
75 0,741826 0,63581 0,63581
90 0,741826 0,529876 0,582863
105 0,688838 0,423901 0,529876
5. Perhitungan untuk katalis C6H8O7 Pada Suhu 55 oC
• 15 menit
Volume NaOH 0.6 ml
% ��� = 0.9 � 0.1 � 28.2 2.661
% FFA = 0,953777
Waktu
(Menit)
% FFA (C6H8O7) 0,1 % w/v
55 oC 60oC 65oC
15 0,953777 0,95777 0,847802
30 0,953777 0,847802 0,741826
45 0,900789 0,847802 0,635851
60 0,847802 0,741826 0,529876
75 0,847802 0,635851 0,529876
90 0,635851 0,635851 0,529876
105 0,529876 0,529876 0,423901
120 0,423901 0,423901 0,423901
6. Perhitungan untuk katalis C6H8O7 Pada Suhu 55 oC
• 15 menit
Volume NaOH 0.8 ml
% ��� =0.85 � 0.1 � 28.2 2.661
% FFA = 0,900789
Waktu
(Menit)
% FFA (C6H8O7)0,2% w/v
15 0,900789 0,847802 0,847802
30 0,847802 0,794813 0,794813
45 0,794813 0,741826 0,741826
60 0,741826 0,741826 0,688838
75 0,741826 0,63581 0,63581
90 0,63581 0,63581 0,529876
105 0,63581 0,529876 0,423901
120 0,529876 0,423901 0,370913
7. Perhitungan untuk katalis C6H8O7 Pada Suhu 55 oC
• 15 menit
Volume NaOH 0.8 ml
% ��� =0.82 � 0.1 � 28.2 2.661
% FFA = 0,866899
Waktu
(menit)
% FFA (C6H8O7)0,3%w/v
55 oC 60oC 65oC
15 0,866899 0,847802 0,847802
30 0,741826 0,763021 0,847802
45 0,741826 0,741826 0,763021
60 0,63581 0,63581 0,741826
75 0,63581 0,63581 0,63581
90 0,529876 0,529876 0,529876
8. Persentase Penurunan Kadar FFA Selama Proses Esterifikasi
% FFA awal = 2,5 %
% FFA pada kondisi terbaik
(waktu 120 menit, katalis C6H8O7 0,2 % , Suhu 65 oC) = 0,370913%
% Penurunan FFA =2,5 −0,370913
2.5 � 100 %
= 85,16 %
LAMPIRAN II
GAMBAR GRAFIK HASIL PERCOBAAN
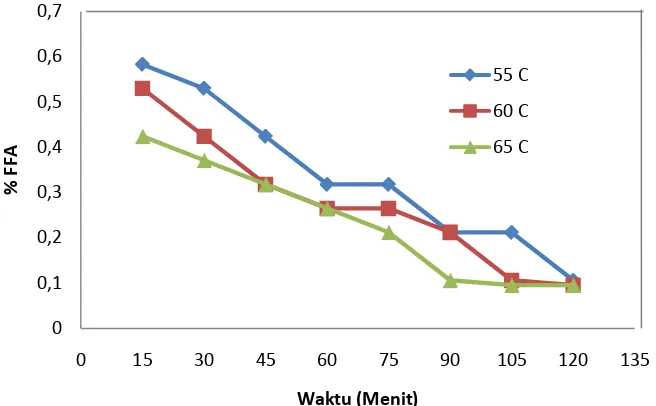
Gambar L2.1 Pengaruh waktu dan penambahan Katalis H2SO4 0,5 % v/v terhadap %
FFA pada berbagai suhu
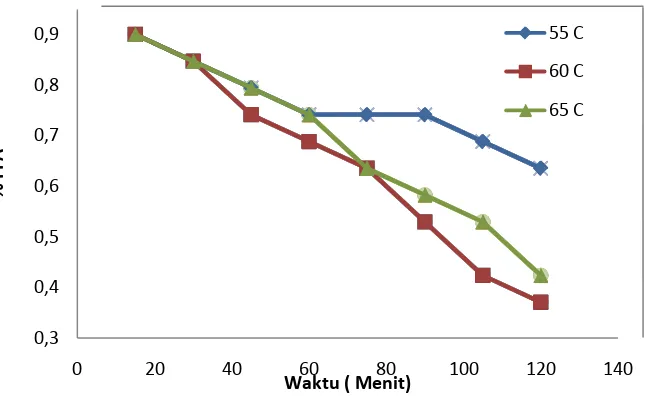
Gambar L2.2 Pengaruh Pengaruh waktu dan penambahan Katalis H2SO4 1,5 %
v/v terhadap % FFA pada berbagai suhu 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7
0 20 40 60 80 100 120 140
% FFA waktu (Menit) 55 C 60 C 65 C 0,3 0,4 0,5 0,6 0,7 0,8 0,9
0 20 40 60 80 100 120 140
%
FFA
Waktu ( Menit)
55 C
60 C
Gambar L2.3 Pengaruh waktu dan penambahan Katalis C6H8O7 0,1 % terhadap % FFA
pada berbagai suhu
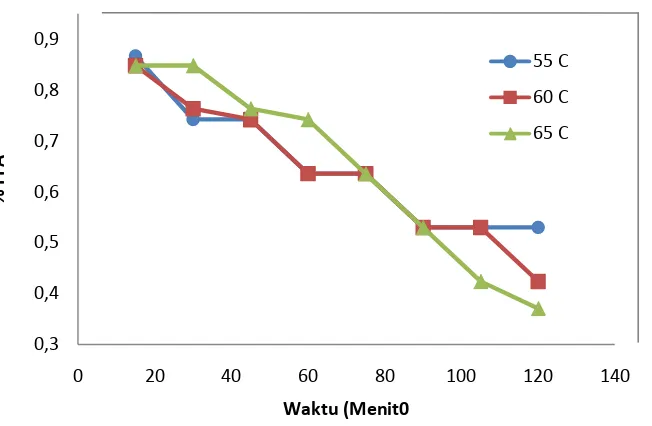
Gambar L2.4 Pengaruh waktu dan penambahan Katalis C6H8O7 0,3 % terhadap % FFA
pada berbagai suhu 0,3
0,4 0,5 0,6 0,7 0,8 0,9 1
0 20 40 60 80 100 120 140
%
FFA
Waktu (Menit)
55 C
60 C
65 C
0,3 0,4 0,5 0,6 0,7 0,8 0,9
0 20 40 60 80 100 120 140
%
FFA
Waktu (Menit0
55 C
60 C
LAMPIRAN III
FOTO PENELITIAN
GambarL3.1 Dedak padi sebagai bahan bakuGambarL3.2 PeralatanEktraksi
GambarL3.5 HasilEsktraksi GambarL3.6 ProsesTitrasi GambarL3.7
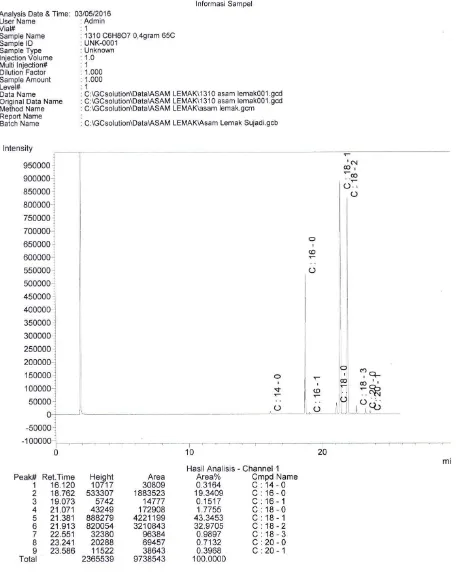
LAMPIRAN IV HASIL ANALISA GC
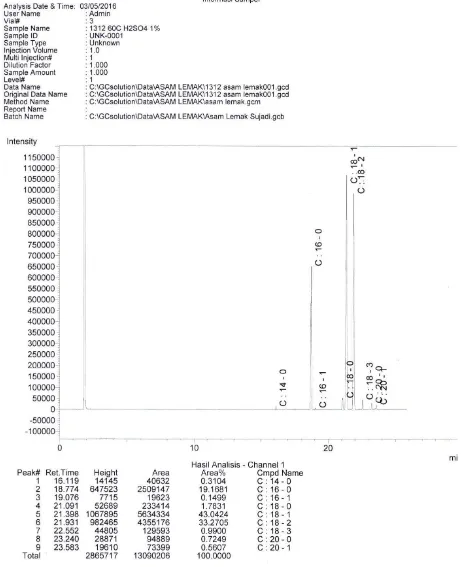
Gambar L4.2 Kromatogram Komposisi Asam Lemak Minyak Dedak Padi Dengan Penambahan Katalis H2SO4 1% v/v Pada Suhu 60 oC dengan Waktu
Gambar L4.3 Kromatogram Komposisi Asam Lemak Minyak Dedak Padi Dengan Penambahan Katalis C6H8O7 0,2% w/v Pada Suhu 60 oC dengan
DAFTAR PUSTAKA
SBP Board Of Consultants & Engineers, 1998, SBP Handbook Oil Seeds, Oils, Fats & Derivatives, SBP Publication Division New Delhi.
Perry, R.H. and Green, D.W. 1984, Perry’s Chemical Engineering Handbook 6thed, McGraw Hill Book Company, Ich,New York
SitiZullaikah et al, 2005, Two-step process to produce biodiesel acid catalyst from rice bran oil. Depertment of chemical engineering Universitas of Science and technology 96
Yue Zhang et a, 2013 1, One step production of biodiesel from rice bran oil catalyzed by chlorosulfonic acid modified zirconia via simultaneous esterification and trasnesterification, Bioresource technology 147 (59-64)
Aprilinapurbasari and Silviana, 2008, kajianawalpembuatan biodiesel dariminyakdedakdengan proses esterifikasi, Teknik Kimia UNDIP, Semarang.
Pei-jingShui et al, 2013, Biodiesel production from rice bran by a two step in situ proess, Bioresource technology 101 (984-989)
ArsidaPertama sari and Indah Marita, 2010, Modifikasi proses in-situ esterifikasiuntuk proses pembuatan biodiesel daridedakpadi, Teknikkimia UNDIP, Semarang.
NdaruCandraSukmana and EndangPurwanti, 2011. Kalor biodiesel HasilEsterifikasidengankatalisasamsitratdantrasesterifikasidengankatalisKaliumhi droksidaminyakbijiNyamplung,
FakultasMatematikadanilmupengetahuanAlamITS, Surabaya.
Adi, N., 2003, Ekstraksi Minyak dari Dedak Padi dengan Pelarut n-Hexane, ProsidingSeminar Nasional Teknik Kimia Indonesia, Yogyakarta.
Putrawan ,I.D.G.A., Shobih, Soerawidjaja ,T.H., 2006, Stabilisasi Dedak Padi sebagaiSumber Minyak Pangan, Seminar Nasional Teknik Kimia Indonesia, Palembang
Nurul Maharani, 2010 Pembuatan Metil Ester (Biodiesel) Dari Minyak Dedak Dan Metanol Dengan Proses Esterifikasi Dan Transesterifikasi,Fakultas Teknik Uvinersitas Diponegoro, Semarang.
BAB III
METODOLOGI PENELITIAN
3.1 PENETAPAN VARIABEL
1. Ekstraksiminyakdedak
Perbadingandedakdengan N-Hexane : 10 gr : 150 ml
Suhu : 65 oC
WaktuEsktraksi : 5 jam
2. Esterifikasi
Waktu : 2 jam
Suhu : 55oC, 60 oC, 65 oC
Katalis - H2SO40,5%, 1%, 1,5% v/v
- C6H8O70,1%, 0,2%, 0,3% v/v
3.2 BAHAN DAN ALAT YANG DIGUNAKAN
3.2.1 Bahan
1. Dedak
2. Metanol
3. Etanol 96 %
4. N-Hexane
5. Indikator PP
6. H2SO4
7. Aquadest
8. NaOH
3.2.2 Alat
1. Labulehertiga
2. Buret
3. Condensor
4. Corongpemisah
5. Erlenmeyer
6. Water Bath
7. GelasUkur
9. Statifdanklem
10. Termometer
11. Beaker glass
12. Hot Plate
3.3 LANGKAH PERCOBAAN
3.3.1 Langkah PercobaanEkstraksi
1. Kedalamlabudimasukkan10 gr dedakpadikemudianditambahkan 150 ml
N-Hexane dandipanaskansampaisuhu 65 oCdandilakukanselama 5 jam.
2. Kemudianhasilesktaksididestilasi, yang
bertujuanuntukmemisahkanhasilekstraksi dari pelarut.
3. Laludilakukananalisakadar FFA minyakdedakpadi.
(Sumber :Arsida dkk.2010)
3.3.2 Langkah PercobaanEsterifikasi
1. Kedalamlabulehertigadimasukkanmiyakdedakpadi, metanol, katalis
H2SO4, kemudiandipanaskan.
2. Suhureaksi dipertahankan 55oCselama 2 jam.
3. Kemudiansampeldiambildan dilakukantitrasisetiapselangwaktu 15
menitselamawaktureaksiuntukanalisaasamlemakbebassesuaiprosedur SNI
01-3555-1998 yaitudengancara sebagai berikut:
a. Diambil 3 ml sampel
b. Kemudianditambahkan 9 ml ethanol 96 %
c. Laludipanaskansampai 45oC
d. Kemudianditambahkan 2-3 tetesindikator PP dan
dititrasidenganlarutanstandart NaOH 1 N hinggawarnamerahmuda.
4. Dan percobaandilakukankembalidengansuhu60oCdan65oC
5. Danpercobaandilakukankembalidenganmengguankankatalis C6H8O7
(Sumber :Arsida dkk.2010)
3.5 FLOWCHAT PERCOBAAN
3.5.1 Proses Ekstraksi
Gambar 3.2 Flowchart Ekstraksi Dedak Padi MULAI
10 gr dedakpadimasukkankedalamlabu
Kemudiandipanaskanpadasuhu 65 oC Kemudianditambahkan N-Hexane sebanyak
150 ml
Hasil ekstraksi kemudian di destilasi
Kemudiandilakukananalisa FFA darihasilekstraksi
3.5.2 Proses Esterifikasi
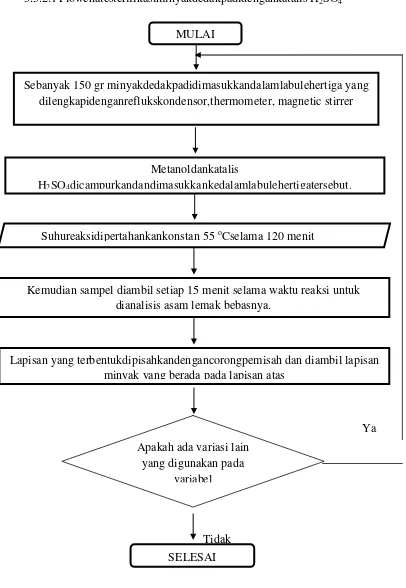
3.5.2.1Flowchatesterifikasiminyakdedakpadidengankatalis H2SO4
Ya
Tidak
Gambar 3.3 Flowchart Esterifikasi Minyak Dedak Padi Dengan Katalis H2SO4
MULAI
Sebanyak 150 gr minyakdedakpadidimasukkandalamlabulehertiga yang dilengkapidenganreflukskondensor,thermometer, magnetic stirrer
Metanoldankatalis
H2SO4dicampurkandandimasukkankedalamlabulehertigatersebut.
Suhureaksidipertahankankonstan 55 oCselama 120 menit
Kemudian sampel diambil setiap 15 menit selama waktu reaksi untuk dianalisis asam lemak bebasnya.
Lapisan yang terbentukdipisahkandengancorongpemisah dan diambil lapisan minyak yang berada pada lapisan atas
SELESAI Apakah ada variasi lain
3.5.2.2 FlowchatEsterifikasiminyakdedakpadidengankatalis C6H8O7
Ya
Tidak
Gambar 3.4 Flowchart Esterifikasi Minyak Dedak Padi Dengan Katalis C6H8O7
3.5.3 Proses Analisis FFA
Sebanyak 150 grminyakdedakpadidimasukkandalamlabulehertiga yang dilengkapidenganreflukskondensor,thermometer, magnetic
stirrer
MetanoldankatalisC6H8O7dicampurkandandimasukkankedalamlabule
hertigatersebut.
Suhureaksidipertahankankonstan 55 oCselama 120 menit
Kemudian sampel diambil setiap 15 menit selama waktu reaksi untuk dianalisa asam lemak bebasnya.
Lapisan yang terbentukdipisahkandengancorongpemisah dan diambil lapisan minyak yang berada pada lapisan atas
SELESAI MULAI
Apakah ada variasi lain yang digunakan pada
Gambar 3.5 Flowchart analisis FFA
BAB IV
MULAISebanyak 3 ml minyak dedak padi dimasukkan kedalam erlenmeyer kemudian ditambahkan methanol
Dicatat Volume NaOH yang terpakai
SELESAI
HASIL DAN PEMBAHASAN
4.1 Pengaruh waktu dan Penambahan katalis Asam Sulfat (H2SO4) terhadap %
FFA pada berbagai suhu.
Bahan baku yang digunakan pada penelitian ini adalah dedak padi. Dedak padi ini
di ekstraksi untuk mendapatkan minyak dedak padi dan kemudian di esterifikasi
menurunkan asam lemak bebas yang terkandung dalam minyak tersebut. Berdasarkan
penelitian yang dilakukan, pada berbagai variasi diperoleh hasil seperti yang
ditunjukkan pada tabel4.1.
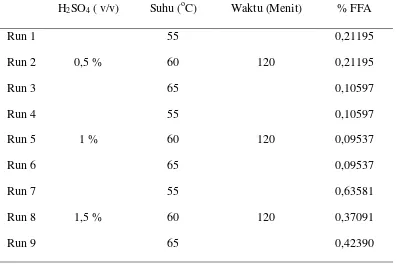
Tabel 4.1 Hasil-Hasil Percobaan Yang Diperoleh Pada Berbagai Keadaan Dengan Penambahan Katalis H2SO4 Terhadap % FFA
H2SO4 ( v/v) Suhu (oC) Waktu (Menit) % FFA
Run 1
0,5 %
55
120
0,21195
Run 2 60 0,21195
Run 3 65 0,10597
Run 4
1 %
55
120
0,10597
Run 5 60 0,09537
Run 6 65 0,09537
Run 7
1,5 %
55
120
0,63581
Run 8 60 0,37091
Run 9 65 0,42390
Pada Percobaan esterifikasi ini dilakukan dengan mengubah suhu untuk setiap
percobaan (55oC, 60oC, 65oC) sedangkan untuk waktu esterifikasi dilakukan selama 2
jam dengan jumlah katalis H2SO4 (0,5%, 1%,1,5% v/v). Kondisi terbaik yang diperoleh
pada percobaan tersebut adalah pada suhu 60oC dengan katalis H2SO41% Seperti yang
antar partikel semakin besar, sehingga reaksi berjalan semakincepat dan konstanta reaksi
semakin besar (Maharani, 2010).
Gambar 4.1 menunjukkan pengaruh penambahan katalis H2SO4 1% v/v terhadap %
FFA. Hasil-hasil percobaan yang lain ditunjukkan pada lampiran II.
Gambar 4.1 Pengaruh waktu dan penambahan Katalis H2SO4 1 % v/v terhadap % FFA pada
berbagai suhu
Dari Gambar 4.1 dapat dilihat bahwa pada suhu tetap dengan peningkatan waktu
menyebabkan kadar FFA menurun. Kondisi terbaikdiperoleh pada waktu 120
menit dengan suhu 60oC dan katalis H2SO41% v/v dimana kadar FFA 0,09537%, dan
apabila waktu esterifikasi dilanjutkan kemungkinan tidak akan mengalami penurunan
karena kadar setimbang telah tercapai pada waktu 120 menit.
Pada penelitian ini, kadar FFA awal minyak dedak padi adalah sebesar 2,5 %.
Setelah proses esterifikasi menggunakan katalis H2SO4pada kondisi suhu 60oC dengan
katalis H2SO41% v/v dan waktu 120 menit kadar FFAnya turun menjadi 0,09537%
seperti yang ditunjukkan oleh tabel 4.1. Dengan demikian selama proses esterifikasi
terjadi penurunan FFA sebesar 96,18 %.
Semakin lama waktu reaksi, maka kemungkinan kontak antar zatsemakin besar
sehingga akan menghasilkan konversi yang besar. Jika kesetimbangan reaksi sudah
tercapai maka dengan bertambahnya waktu reaksi tidak akan menguntungkan
karenatidak memperbesar hasil. Dalam penelitian yang telah dilakukan, diperoleh data
bahwa selama waktu 15sampai dengan 120 menit diperoleh % FFA yang menurun. 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7
0 15 30 45 60 75 90 105 120 135
Pada waktu tetap kenaikan suhu menyebabkan kadar FFA menurun. Secara umum
kenaikan suhu menyebabkan kecepatan reaksi bertambah besar.
4.2 Pengaruh waktu dan penambahan katalis Asam Sitrat (C6H8O7) terhadap %
FFA pada berbagai suhu
Hasil-hasil penelitian yang diperoleh pada berbagai variasi ditunjukkan pada tabel
4.2.
Tabel 4.2 Hasil-hasil percobaan yang diperoleh pada berbagai keadaan dengan Penambahan Katalis C6H8O7 Terhadap % FFA
C6H8O7 ( %) Suhu (oC) Waktu (Menit) % FFA
Run 1
0,1
55
120
0,42390
Run 2 60 0,42390
Run 3 65 0,42390
Run 4
0,2
55
120
0,52987
Run 5 60 0,42391
Run 6 65 0,37091
Run 7
0,3
55
120
0,52987
Run 8 60 0,42390
Run 9 65 0,37091
Pada percobaan esterifikasi ini dilakukan dengan mengubah suhu untuk setiap
percobaan (55oC, 60oC, 65oC) sedangkan untuk waktu esterifikasi dilakukan selama 2
jam dengan jumlah katalis C6H8O7(0,1%, 0,2% , 0,3% w/v). Seperti yang ditunjukkan
pada tabel 4.2 didapat % FFA yang terbaik pada suhu 65 oC dengan katalis C6H8O70,2%
w/v. Kenaikan suhu menyebabkan tumbukan antar partikel semakin besar, sehingga
reaksi berjalan semakincepat dan konstanta reaksi semakin besar.
Pada penelitian ini, kadar FFA awal minyak dedak padi adalah sebesar 2,5 %.
Setelah proses esterifikasi menggunakan katalis C6H8O7pada kondisi suhu 65oC dengan
katalis C6H8O70,2% w/v dan waktu 120 menit kadar FFAnya turun menjadi 0,37091%
seperti yang ditunjukkan oleh tabel 4.2. Dengan demikian selama proses esterifikasi
Gambar 4.2 Pengaruh waktu dan penambahan Katalis C6H8O7 0,2 %w/v terhadap %
FFA pada berbagai suhu
Dari Gambar 4.2 dapat dilihat pada suhu tetap dengan peningkatan waktu
menyebabkan kadar FFA menurundan pada waktu tetap dengan kenaikan suhu
menyebabkan kadar FFA menurun. Secara umum kenaikan suhu menyebabkan
kecepatan reaksi bertambah besar.
Semakin lama waktu esterifikasi maka % FFA yang dihasilkan semakin kecil. Dari
titik waktu 15 menit sampai 60 menit mengalami penurunan % FFA yang signifikan
yaitu 0,2% dan dari titik waktu 75 menit sampai 90 menit mengalami penurunan yang
hanya sebesar 0,1% demikian juga pada waktu 105 menit dan 120 menit dan kondisi
yang terbaik untuk reaksi tersebut adalah pada suhu 65oC dengan katalis 0,2%, dan
apabila waktu esterifikasi dilanjutkan kemungkinan akan mengalami penurunan.
Dari gambar 4.2 menunjukkan bahwa semakin tinggi suhu reaksi yang maka %
FFA akan semakin rendah. Jika suhu dinaikkan maka tumbukan antar partikel semakin
besar, sehingga reaksi berjalan semakincepat dan konstanta reaksi semakin
besar.Semakin tinggi temperaturnya, maka semakin besar konstanta laju reaksinya. Hal
ini sesuai dengan persamaan Archenius :
k = A exp(-Ea/RT)
k = konstanta laju reaksi
A = frekuensi tumbukan
R = konstanta gas
T = temperatur 0,3 0,4 0,5 0,6 0,7 0,8 0,9
0 15 30 45 60 75 90 105 120 135
Ea = energi aktivasi
4.3 Hasil GC Minyak Dedak Padi
Komposisi asam lemak hasil analisa GC (Gas Chromatography) yang dianalisa di
Laboratorium Pusat Penelitian Kelapa Sawit (PPKS) Jl. Brigjen Katamso 51, Medan
pada lampiran IV. Dari kromatogram lampiran IV komposisi asam lemak minyak dedak
padi tersebut dapat dilihat pada tabel 4.3, tabel 4.4 dan tabel 4.5.
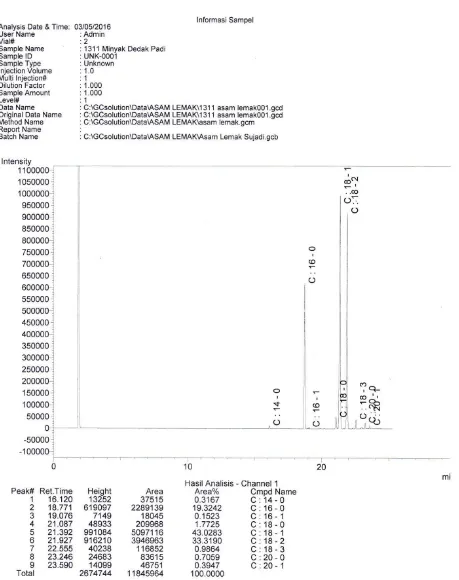
Tabel 4.3 KomposisiAsam Lemak Minyak dedak padi Berdasarkan Analisa GC Sebelum Proses Esterifikasi
Komponen Jumlah (%b)
Asam Miristat (C14:0) 0,3167
Asam Palmitat (C16:0) 19,3242
Asam Palmitat (C16:1) 0,1523
Asam Stearat (C18:0) 1,7725
Asam Oleat (C18:1) 43,0283
Asam Linoleat (C18:2) 33,3190
Asam Linoleat (C18:3) 0,9864
Asam Palmitoleat (C20:0) 0,7059
Asam Eikosenoat (C20:1) 0,3947
Jumlah 100,0000
Tabel 4.4 Komposisi Asam Lemak minyak dedak padi dengan penambahan katalis H2SO4 1 % v/v pada suhu 60 oC dengan waktu 120 menit berdasarkan
Analisa GC
Komponen Jumlah (%b)
Asam Miristat (C14:0) 0,3104
Asam Palmitat (C16:0) 19,1681
Asam Palmitat (C16:1) 0,1499
Asam Stearat (C18:0) 1,7831
Asam Linoleat (C18:2) 33,2705
Asam Linoleat (C18:3) 0,9900
Asam Palmitoleat (C20:0) 0,7249
Asam Eikosenoat (C20:1) 0,5607
Jumlah 100,0000
Tabel 4.5 Komposisi Asam Lemak minyak dedak padi dengan penambahan katalis C6H8O7 0,3 % w/v pada suhu 65oC dengan waktu 120 menit berdasarkan
Analisa GC
Komponen Jumlah (%b)
Asam Miristat (C14:0) 0,3167
Asam Palmitat (C16:0) 19,3242
Asam Palmitat (C16:1) 0,1523
Asam Stearat (C18:0) 1,7725
Asam Oleat (C18:1) 43,0283
Asam Linoleat (C18:2) 33,3190
Asam Linoleat (C18:3) 0,9864
Asam Palmitoleat (C20:0) 0,7059
Asam Eikosenoat (C20:1) 0,3947
Jumlah 100,0000
Dari Hasil analis GC (Gas Chromatography)(terlampir) yang dilakukan, proses
ekstraksi dan proses esterifikasi sebagai upaya untuk memanfaatkan dedak padi sebagai
bahan baku pembuatan metil ester. Komponen yang terbesar minyak dedak padi ini
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
1. Pelarut N-Heksana cocok digunakan untuk esktraksi minyak dari dedak padi.
2. Selama proses esterifikasi dengan menggunakan katalis H2SO4terjadi penurunan
FFA sebesar 96,18 %.
3. Selama proses esterifikasi dengan menggunakan C6H8O7terjadi penurunan FFA
sebesar 85,16 %.
4. Komponen yang terbesar minyak dedak padi ini didominasi oleh asam oleat.
5.2 SARAN
Perlu adanya kajian lebih lanjut dalam rangka meningkatkan dan membandingkan
BAB II
TINJAUAN PUSTAKA
2.1 BIODIESEL
Biodiesel bersifat ramah lingkungan, dapat terurai, memiliki sifat pelumasan
terhadap piston mesin, dan kesinambungan ketersediaan bahan bakunya terjamin jika
dibandingkan dengan bahan bakar solar yang berasal dari minyak dari minyak bumi,
karena itu peggunaan biodiesel baik sebagai pengganti ataupun campuran pada solar
dapat menjawab kebutuhan terhadap semakin menipisnya sumber minyak bumi di
Indonesia. Biodiesel yang memiliki sifat menyerupai minyak solar dapat digunakan baik
secara murni maupun dicampur dengan petrodisel, tanpa menyebabkan terjadinya
perubahan yang berarti pada mesin kendaraan yang ada ( Zullaikah,2005).
Biodiesel adalah energi terbarukan yang tidak menimbulkan polusi bahan bakar
karbon netral dan biodegradabel terbarukan yang dapat dicampurkan dengan minyak
solar atau digunakan langsung dalam mesin diesel dengan sedikit modifikasi. Umumnya
biodiesel dianggap sebagai alternatif yang menjanjikan untuk diesel berbasis bbm yang
digunakan untuk aplikasi transportasi (Zullaikah, 2005).
Bahan bakar biodiesel menjadi lebih menarik karena manfaatnya terhadap
lingkungan. Tanaman dan minyak nabati serta lemak hewani adalah sumber biomassa
yang dapat diperbaharui. Saat ini, sebagian besar biodiesel muncul dari trasesterifikasi
sumber daya yang dapat dimakan, seperti lemak hewan, minyak sayur, dan bahan
limbah minyak goring dengan proses katalis kondisi basa. Namun, konsumsi tinggi
katalis, pembentukan sabun and redahnya hasil panen membuat biodiesel saat ini lebih
mahal daripada bahan bakar yang diturunkan dari minyak bumi (Shui dkk,2010).
Dedak merupakan produk samping penggilingan gabah menjadi beras. Selama ini,
dedak hanya dimanfaatkan sebagai makanan ternak dan uggas selebihnya dipakai untuk
bahan abu gosok atau dibiarkan begitu saja
(Arsida dkk,2010).
Melihat besarnya jumlah produksi dedak padi dan belum maksimalnya
pemanfaatan dedakpadi di Indonesia maka dilakukan penelitian mengenai dedak padi
untuk meningkatkan nilai ekonomi dedak itu sendiri. Minyak dedak yang diperoleh dari
ekstaksi dedak dengan pelarut volatile, umumnya N-Hexane. Peningkatan kandungan
asam lemak bebas secara cepat pada minyak karena adanya lipase aktif setelah proses
penggilingan menyebabkan minyak dedak padi tidak dapat digunakan sebagai edible-oil.
Salah satu pemanfaatan minyak dedak padi yang sedang dikembangkan saat ini adalah
sebagai bahan baku pembuatan biodiesel.
Dedak padi adalah bahan yang cocok untuk produksi biodiesel. Pertama, produksi
biodiesel dari minyak dedak padi memiliki kinerja yang baik dalam tes mesin dan uji
emisi. Hasil penelitian menunjukkan bahwa produksi biodiesel dari minyak dedak padi
mentah yag berkualitas baik dan dapat digunakan sebagai bahan bakar alternative dalam
mesin diesel saat ini tanpa modifikasi mahal. Kedua, stabil pasokan sumber bahan
tersedia bila dedak padi digunakan untuk memproduksi biodieselterutama di cina. Cina
memproduksi lebih dari sepuluh juta ton per tahun dedak padi. Sebagai produk
sampingan dari penggilingan padi, dedak padi mengandung 15- 23 lipid. Karena adanya
digunakan sebagai pakan ternak atau bahan bakar boiler dan minyak dedak yang
dihasilkan bukan untuk dimakan(Arsida, 2010).
2.3 MINYAK DEDAK PADI
Minyak dedak padi adalah minyak berkandungan gizi tinggi karena asam lemak,
komponen-komponen aktif biologis dan antioksidan (oryzanol, tocopherol,
phytosterol,polyphenol dan squalene) (Arsida, 2010).
Minyak mentah dedak padi sulit dimurnikan karena tingginya kandungan asam
lemak bebas dan senyawa tak tersaponifikasi berwarna gelap. Kandungan asam lemak
bebas 4-8 % tetap diperoleh walaupun dedak padi diekstrak sesegera mungkin.
Peningkatan asam lemak bebas secara cepat terjadi karena adanya lipase aktif dalam
dedak, karena alasan tersebut minyak dedak padi tidak dapat digunakan sebagai edible
oil. Pengaruh waktu penyimpanan dedak terhadap kandungan FFA dalam minyak dedak
dapat dilihat pada tabel 2.1, sedangkan karakteristik dan komposisi asam lemak dalam
[image:32.595.247.450.239.394.2]minyak dedak padi ditunjukkan pada tabel 2.2 dan tabel 2.3.
Tabel 2.1 Pengaruh Waktu Penyimpanan Dedak Terhadap Kandungan FFA DalamMinyak Dedak Padi
Waktu Penyimpanan FFA (%)
3 jam 3,0
30 hari 18,2
49 hari 27,0
72 hari 34,3
100 hari 62,6
[image:33.595.109.510.86.189.2]Sumber : SBP Board of Consulttants and Engineers 1998
Tabel 2.2 Karakteristik Minyak Dedak Padi
Karakteristik Rentang Nilai
Specific gravity pada 20 oC/ 30 oC 0,916-0,921
Refractive index pada 25 oC 1,47-1,473
Bilangan iodine 99-108
Bilangan Penyabunan 181-189
Material tak tersabunkan (%) 3-5
Titer (oC) 24-25
Asam Lemak bebas (%) 3-60
Sumber : SBP Board of Consultants and Engineers 1998
Tabel 2.3 Komposisi Asam Lemak dalam Minyak Dedak
Jenis Asam Lemak Konsentrasi (%b)
Asam Miristat (C14 : 0) 0,1
Asam Palmitat (C16 : 0) 12-18
Asam stearate ( C18:0) 1-3
Asam Oleat (C18 : 1) 40-50
Asam linoleat (C18 :2) 29-42
Asam Linolenat (C18:3) 1
Asam Palmitoleat (C20 : 0) 0,2-0,4
Sumber : SBP Board of Consultants and Engineers 1998
[image:33.595.131.513.230.446.2]Asam sulfat (H2SO4) merupakan cairan yag bersifat korosif, tidak berwarna,
tidak berbau, sangat reaktif dan mampu melarutkan berbagai logam. Bahan kimia ini
dapat larut dengan air dengan segala perbandingan, mempunyai titik leleh 10,49 oC dan
titik didih pada 340 oC tergantung kepekatan serta pada temperature 300 oC atau lebih
terdekomposisi menghasilkan sulfur trioksida.Sifat-sifat asam sulfat ditunjukkan Tabel
2.4
Tabel 2.4 Sifat Fisika dan Kimia Asam Sulfat
Berat molekul 98,08 g/gmol
Titik leleh 10,49 oC
Titik didih 340 oC
Specific gravity 1,834
Warna Tidak berwarna
Wujud Cair
Sumber : Aprilina, 2008
2.5 EKSTRAKSI
Ekstraksi merupakan salah satu cara pmisahan campuran dimana terdapat zat
terlarut dan pelarut. Biasa ekstraksi ini dilakukan untuk mengambil zat terlarut dalam
pelarut.
Faktor-faktor yang mempengaruhi proses ekstraksi yaitu :
1. Ukuran bahan
Pengecilan ukuran bertujuan untuk memperluas permukaan bahan sehingga
mempercepat penetrasi pelarut ke dalam bahan yag akan diekstrak dan
mempercepat waktu ekstaksi. Sebenarnya semakin kecil ukuran bahan semakin
luas pula permukaan bahan sehingga semakin banyak oleoresin yang dapat
diekstrak. Tetapi ukuran bahan yang terlalu kecil juga menyebabkan banyak
minyak volatile yang menguap selama penghancuran.
Secara umum, kenaikan temperature akan meningkat jumlah zat terlarut ke
dalam pelarut. Temperautr pada proses ekstraksi memang terbatas hingga suhu
titik didih pelarut yang digunakan.
3. Pelarut
Pelarut harus yang baik maka tidak akan merusak solute atau residu pelarut,
viskositasnya tidak tinggi (kental) agar sirkulasi bebas dapat terjadi.
Dalam pemilihan pelarut harus memperhatikan beberapa factor diantaranya adalah
pemilihan pelarut pada umumnya dipengaruhi oleh factor-faktor berikut ini
1. Seleksi pelarut hanya boleh melarutkan ekstraksi yang diinginkan, bukan
komponen-komponen lain dari bahan ekstraksi.
2. Kelarutan pelarut sedapat mungkin memiliki kemampuan melarutkan ekstrak yang
besar (kebutuhan pelarut lebih sedikit).
3. Kemampuan untuk tidak saling bercampur pada ekstraksi cair-cair, pelarut tidak
boleh atau hanya secara terbatas larut dalam bahan ekstraksi.
4. Kerapatan terutama pada ekstraksi cair-cair, sedapat mungkin terdapat perbedaan
kerapatan yang besar antara pelarut dan bahan ekstraksi.
5. Reaktifitas pada umumnya pelarut tidak boleh menyebabkan perubahan secara
kimia pada komponen-komponen bahan ekstraksi.
6. Titik didih karena ekstrak dan pelarut biasanya harus dipisahkan dengan cara
penguapan, destilasi atau reaktifikasi, maka titik didih kedua bahan ini tidak boleh
terlalu dekat (Aprilina, 2008).
2.6 ESTERIFIKASI
Esterifikasi adalah tahap konversi dari asam lemak bebas menjadi ester.
Esterifikasi mereaksikan minyak lemak dengan alkohol. Katalis-katalis yang cocok
adalah zat berkarakter asam kuat, dankarena ini asam sulfat, asam sulfonat organic atau
resin penukar kation asam kuat merupakan katalis-katalis yag biasa terpilih dalam
praktek industrial. Untuk mendorong agar reaksi bias berlangsung ke konversi yang
sempurna pada temperature rendah (misalnya paling tinggi 120 oC), reaktan metanol
harus ditambahkan dalam jumlah yang sangat berlebih (biasanya lebih besar dari 10 kali
nisbah stoikhiometrik) dan air produk ikutan harus disingkirkan dari fasa reaksi, yaitu
fasa minyak. Melalui kombinasi-kombinasi yang tepat dari kondisi-kondisi reaksi dan
dituntaskan dalam waktu 1 sampai beberapa jam. Reaksi esterifikasi dari asam lemak
menjadi metil ester adalah :
RCOOH + CH3OH RCOOH3 + H2O
Asam Lemak Metanol Metil Ester Air
Esterifikasi biasanya dilakukan untuk membuat biodiesel dari minyak berkadar
asam lemak bebas tinggi. Pada tahap ini, asam lemak bebas akan dikonversi menjadi
metil ester. Tahap esterifikasi biasanya diikuti dengan tahap trasesterifikasi. Namun
sebelum produk esterifikasi diumpankan ke tahap transesterifikasi, air dan bagian
tersbesar katalis asam yang dikandungnya harus disingkirkan terlebih dahulu (Shui
dkk,2010).
2.6.1 Hal-Hal Yang Mempengaruhi Reaksi Esterifikasi
Factor-faktor yang berpengaruh pada reaksi esterifikasi antara lain :
a. Waktu reaksi
Semakin lama waktu reaksi maka kemungkinan kontak antar zat semakin
besar sehingga akan menghasilkan konversi yang besar. Jika kesetimbangan
reaksi sudah tercapai maka dengan bertambahnya waktu reaksi tidak akan
menguntungkan karena tidak memperbesar hasil.
b. Pengadukan
Pengadukan akan menambah frekuensi tumbukan antara molekul zat
pereksi dengan zat yang bereaksi sehingga mempercepat reaksi dan reaksi terjadi
sempurna. Sesuai dengan persamaan Archenius :
K = A e(-Ea/RT)
Dimana : T = suhu absolut (oC)
R = Konstanta gas umum ( cal/gmol oK)
E = Tenaga aktifasi (cal/gmol)
A = Faktor tumbukan (t-1)
K = Konstata kecepatan reaksi (t-1)
Semakin besar tumbukan maka semakin besar harga konstanta kecepatan reaksi.
Sehingga dalam hal ini pengadukan sangat penting mengingat larutan
minyak-katalis methanol merupakan larutan immiscible.
Katalisator berfungsi untuk mengurangi tenaga aktifasi pada suatu reaksi
sehingga pada suhu tertentu harga konstanta kecepatan reaksi semakin besar.
Pada reaksi esterifikasi yang suah dilakukan biasanya menggunakan konsentrasi
katalis antara 1-4 % berat sampai 10 % berat campuran pereaksi.
d. Suhu Reaksi
Semakin tinggi suhu yang dioperasikan maka semakin banyak konversi
yang dihasilkan hal ini sesuai dengan persamaan Archenius. Bila suhu naik maka
harga k semakin besar sehigga reaksi berjala cepat dan hasil konfersi semakin
besar ( Aprillina, 2008).
Reaksi esterifikasi merupakan reaksi pembentukan ester dengan reaksi langsung
antara suhu asam karboksilat dengan suatu alcohol. Suatu reaksi pemadatan untuk
membentuk suatu ester disebut esterifikasi. Eserifikasi dapat dikatalis oleh kehadiran
ion H+. asam belerang sering digunakan sebagai suatu katalisator untuk reaksi ini.
Pada skala industry etil asetat di produksi dari reaksi esterifikasi antara sam asetat
(CH3COOH) dan etanol (C2H5OH) dengan bantuan katalis berupa asam sulfat (H2SO4)
(Aprillina, 2008).
Ester adalah subuah asam karboksilat mengandung gugus COOH, dan pada
sebuah ester hindrogen pada gugus ini digantikan dengan sebuah gugus hidrokarbon
dari berbagai jenis. Gugus ini bias berupa gugus alkil seperti metil atau etil, atau gugus
yang megandung sebuah cincin benzene seperti fenil.
Ester dapat terhidrolisis dengan pengaruh asam membentuk alcohol dan asam
karboksilat. Reaksi hidrolisis tersebut merupakan kebalikan dari pengesteran. Disini
senyawa karbon mengikat gugus fungsi-COOR adalah alkilalkanoat. Ester diturunkan
dari alcohol dan asam karboksilat. Untuk ester turunan dari asam karboksilat paling
sederhana, nama-nama tradisional digunakan, seperti formate, asetat dan propionate.
Proses esterifikasi adalah suatu reaksi refersibel antara suatu asam karboksilat
dengan suatu alcohol. Produk esterifikasi disebut ester yang mempunyai sifat yang khas
yaitu baunya yang harum sehingga pada umumnya digunakan sebagai pengaharum
(Essence) sintesis. Reaksi esterifikasi merupakan reaksi refersibel yang sangat lambat.
akan tercapai dalam beberapa jam. Esterifikasi dipengaruhi oleh beberapa faktor
diantara nya adalah : struktur molekul dari alkohol, suhu proses dan konsentrasi katalis
maupun reaktan.
Ester diturunkan dari asam karboksilat dengan mengganti gugus OH dengan gugus
OR ( R adalah gugus alkil atau aril). Ester merupakan senyawa organik yang bersifat
netral, tidak beeraksi dengan logam NA dan PCL3.Ester termasuk salah satu turunan
asam karboksilat yang diperoleh dengan mereaksikan suatu asam (karboksilat dengan
alkohol atau phenol.Rumus nya RCOOR dimana R dan R adalah gugus organic
(Aprillina, 2008).
2.7 Transesterifikasi
Transesterifikasi (biasa disebut dengan alkoholisis) adalah tahap konversi
daritrigliserida (minyak nabati) menjadi alkil ester, melalui reaksi dengan alkohol,
danmenghasilkan produk samping yaitu gliserol. Di antara alkohol-alkohol monohidrik
yangmenjadi kandidat sumber/pemasok gugus alkil, metanol adalah yang paling umum
digunakan,karena harganya murah dan reaktifitasnya paling tinggi (sehingga reaksi
disebut metanolisis).Jadi, di sebagian besar dunia ini, biodiesel praktis identik dengan
ester metil asam-asamlemak (Fatty Acids Metil Ester). Reaksi transesterifikasi
trigliserida menjadi metilester adalah :
O O
H2C - O - C - R1 R1 - C - OCH3 H2COH
O Katalis O
HC - O - C - R2 + 3CH3OH R2 - C - OCH3 + HCOH
O O
H2C - O - C - R3 R3 - C - OCH3 H2COH
Trigliserida Metanol Metil Ester Gliserol
Transesterifikasi juga menggunakan katalis dalam reaksinya. Tanpa adanya
katalis, konversiyang dihasilkan maksimum namun reaksi berjalan dengan lambat.
Katalisyang biasa digunakan pada reaksi transesterifikasi adalah katalis basa, karena
Reaksi transesterifikasi sebenarnya berlangsung dalam 3 tahap yaitu sebagai berikut:
1. Trigliserida (TG) + ROH Katalis Digliserida (DG) + R’COOR
2. Digliserida (DG) + ROH Katalis Monogliserida (MG) + R’’COOR
3. Monogliserida (MG) + ROHKatalisGliserol (GL) + R’’’COOR
Produk yang diinginkan dari reaksi transesterifikasi adalah ester metil asam-asam
lemak.Terdapat beberapa cara agar kesetimbangan lebih ke arah produk, yaitu:
a. Menambahkan metanol berlebih ke dalam reaksi.
b. Memisahkan gliserol.
c. Menurunkan temperatur reaksi (transesterifikasi merupakan reaksi eksoterm).
2.7.1 Hal-hal yang Mempengaruhi Reaksi Transesterifikasi
Tahapan reaksi transesterifikasi pembuatan biodiesel selalu menginginkan
agardidapatkan produk biodiesel dengan jumlah yang maksimum. Beberapa kondisi
reaksi yangmempengaruhi konversi serta perolehan biodiesel melalui transesterifikasi
adalah sebagai berikut :
a. Pengaruh air dan asam lemak bebas
Minyak nabati yang akan ditransesterifikasi harus memiliki angka asam yang
lebih kecildari 1. Banyak peneliti yang menyarankan agar kandungan asam lemak
bebas lebih kecildari 0.5% (<0.5%). Selain itu, semua bahan yang akan digunakan
harus bebas dari air.Karena air akan bereaksi dengan katalis, sehingga jumlah
katalis menjadi berkurang. Katalis harus terhindar dari kontak dengan udara agar
tidak mengalami reaksi dengan uapair dan karbon dioksida.
b. Pengaruh perbandingan molar alkohol dengan bahan mentah
Secara stoikiometri, jumlah alkohol yang dibutuhkan untuk reaksi adalah 3
mol untuksetiap 1 mol trigliserida untuk memperoleh 3 mol alkil ester dan 1 mol
gliserol.Perbandingan alkohol dengan minyak nabati 4,8:1 dapat menghasilkan
konversi 98%. Secara umum ditunjukkan bahwa semakin banyak jumlahalkohol
yang digunakan, maka konversi yang diperoleh juga akan semakin bertambah.Pada
rasio molar 6:1, setelah 1 jam konversi yang dihasilkan adalah 98-99%,
sedangkanpada 3:1 adalah 74-89%. Nilai perbandingan yang terbaik adalah 6:1
karena dapatmemberikan konversi yang maksimum.
Pada rasio 6:1, metanol akan memberikan perolehan ester yang tertinggi
dibandingkan dengan menggunakan etanol atau butanol.
d. Pengaruh Jenis Katalis
Alkali katalis (katalis basa) akan mempercepat reaksi transesterifikasi bila
dibandingkandengan katalis asam. Katalis basa yang paling populer untuk reaksi
transesterifikasi adalahnatrium hidroksida (NaOH), kalium hidroksida (KOH),
natrium metoksida (NaOCH3),dan kalium metoksida (KOCH3). Katalis sejati bagi
reaksi sebenarnya adalah ion metilat(metoksida). Reaksi transesterifikasi akan
menghasilkan konversi yang maksimum denganjumlah katalis 0,5-1,5%-b minyak
nabati. Jumlah katalis yang efektif untuk reaksi adalah0,5%-b minyak nabati untuk
natrium metoksida dan 1%-b minyak nabati untuk natriumhidroksida.
e. Metanolisis Crude dan Refined Minyak Nabati
Perolehan metil ester akan lebih tinggi jika menggunakan minyak nabati
refined. Namunapabila produk metil ester akan digunakan sebagai bahan bakar
mesin diesel, cukup digunakan bahan baku berupa minyak yang telah dihilangkan
getahnya dan disaring.
f. Pengaruh temperatur
Reaksi transesterifikasi dapat dilakukan pada temperatur 30 - 65° C (titik
didih methanolsekitar 65° C). Semakin tinggi temperatur, konversi yang diperoleh
akan semakin tinggiuntuk waktu yang lebih singkat.
Ester yang terdiri dari asam-asam yag berat molekul rendah dan alkohol
merupakan senyawa-senyawa cair yang tidak berwarna, sedikit larut dalam air dengan
bau semerbak, dan mudah menguap. Ester dari beberapa asam karboksilat dengan rantai
panjang terdapat secara alamiah di dalam lemak, lilin dan minyak.
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Bahanbakarminyakmerupakansalahsatukebutuhanutama yang banyakdigunakan
di berbagai
Negara.Saatinikebutuhanakanbahanbakarsemakinmeningkatseiringsemakinmeningkatny
apopulasi dan semakinberkembangnyateknologi,
akantetapicadangansumberdayaminyakbumi yang
berasaldarifosilsemakinmenipiskarenasifatnya yang tidakdapatdiperbaharui. Salah satu
alternative sumber energi adalah Fatty Acid Metil Ester (Biodiesel)
sebagaiprodukuntukmenggantikansumber energi darifosil.
Biodiesel merupakanmonoalkil ester
dariasam-asamlemakrantaipanjangyangterkandungdalamminyaknabatiataulemakhewaniutukdigun
akansebagai alternatif yang paling tepatuntukmenggantikanbahanbakarmesin diesel.
Biodiesel bersifat biodegradable, dan hampir tidakmengandung sulfur.Alternatif
bahanbakarterdiridarimetalatauetil ester, hasiltransesterifikasibaikdaritriakilgliserida
(TG) atauesterifikasidariasamlemakbebas (FFA) (Aprilina, 2008).
Pembuatan biodiesel dariminyaktanamanmemilikikasus yang
berbeda-bedasesuaidengankandugan
FFA.Padakasusminyaktanamandengankandunganasamlemakbebastinggidilakukanduaje
nis proses, yaituesterifikasidantrasesterifikasi, sedangkanuntukminyaktanaman yang
kadunganasamlemakrendahdilakukan proses transesterifikasi.Proses
esterifikasidantrasesterifikasibertujuanuntukmengubahasamlemakbebasdantrigliseridada
lamminyakmenjadimetil ester (biodiesel) dangliserol.
Biodiesel merupakansolusi yang paling
tepatuntukmenggantikanbahanbakarfosilsebagaisumber energi transportasiutamadunia,
karena biodiesel merupakanbahanbakarterbaharui yang dapatmenggantikan diesel petrol
padamesindandapatdiangkutsertadijualdenganmenggunakaninfrastruktursekarangini.
Dedakmerupakanproduksampingpeggilingangabahmenjadiberas.Penggilingansatu
Bergantungpadavarietasberasdanderajatpeggilingannya, dedakpadimegandung 16-32 %
minyak. Sekitar 60-70 % minyakdedakpaditidakdapatdigunakansebagaibahanmakanan
(non-edible oil) disebabkankestabilandanperbedaancarapenyimpanandedakpadi (Yue
hang, 2013).
Dengankadarlemakkurangdari 25 %,
caraterbaikuntukmengambilminyakdedakadalahmelaluiekstraksimenggunakanpelarutmu
dahmenguap, sepertimetanol dan heksan. Minyaknabati yang
mengandungtrigliseridadan FFA biasanyadiekstrakdengan hexane atau
methanol.Minyakdedakhasilekstraksi (minyakdedakmentah)
dipisahkandaripelarutmelalui proses penguapandanselanjutnyadilakukan proses
esterifikasi. Reaksiesterifikasimerupakanreaksipembentukan ester
denganreaksilangsungantarasuatuasamkarboksilatdengansuatu
alkohol.Suatureaksipemadatanuntukmembentuksuatu ester disebutesterifikasi (Siti
zullaikah, 2005).
Biodiesel merupakanbahanbakar alternatif yang menjanjikan yang
dapatdibuatdariminyaknabati, baikminyakbarumaupunbekaspenggorengan, melalui
proses trasesterifikasi, esterifikasiatauesterifikasi-trasesterifikasidengan alkohol.
Biodiesel ramahterhadaplingkungankarena biodegradable, nontoxic danrendahemisi
[image:42.595.118.536.496.784.2](Arsida dkk.2010).
Tabel 1.1 Penelitian-Penelitian Terdahulu Berkenaan Dengan Ekstraksi Dedak Padi
No JudulPenelitian Variabel Hasil
1 Kajianawalpembuatan biodiesel dariminyakdedakpadidengan
prosesesterifikasi
(AprilinaPurbasari, dkk. 2008)
T= 70oC
t =2 jam
Pelarut : metanol
Kandungan FFA
minyakdeda kpadi 62,21 %
2 Two-step process to produce biodiesel acid catalyst from rice bran oil (Zullaikahsiti, dkk. 2005)
t= 3 jam
T= 60 oC
Pelarut : N-Hexane
FFA
dalamminya kdedakpadi 82 %
3 In situ production of fatty acid methyl ester from low quality rice bran : An economical route for
Pelarut: Metanol
t= 5 jam
Kandugan FFA
biodiesel production.
(Hong Lei,dkk.2009)
T= 65oC
Metanol : dedak = 200 ml : 50 gr
kpadi 83 %
4 Modifikasi proses in-situ esterifikasiuntuk proses pembuatan biodiesel daridedakpadi (Arsida dkk,2010).
T= 65 oC
N-Hexane: dedak = 150 : 10
[image:43.595.115.516.277.733.2]Minyakdeda kpadiFFA= 39,27 %
Tabel 1.2 Penelitian-Penelitian Terdahulu Berkenaan Dengan Esterifikasi Minyak Dedak Padi
No JudulPenelitian Variabel Hasil
1 Kajianawalpembuatan biodiesel dariminyakdedakpadidengan proses esterifikasi
(AprilinaPurbasari, dkk.2008)
Katalis HCL 2,5 %
T= 1 jam
t = 50 oC
V=100 rpm
Kandungan FFA
dalamminyak 0,85 %
2 In situ production of fatty acid methyl ester from low quality rice bran : An economical route for biodiesel production (Hong Lei,dkk.2009)
t = 2jam
T= 60 oC
H2SO4 1 % v/v
FFA 0,61 %
3 Modifikasi proses in-situ
esterifikasiuntuk proses pembuatan biodiesel daridedakpadi
(Arsida dkk,2010).
t= 2 jam
T= 60oC
H2SO41 % v/v
FFA 0,56 %
4 Kalor Biodiesel Hasil esterifikasi dengan katalis asam sitrat dan trasesterifikasi dengan katalis kalium hidroksida minyak biji nyamplung.
(Ndaru Candra,2011)
Katalis
C6H8O70,4626 gr
T= 60oC
t=3 jam
methanol : minyak= 20 : 1
Padapenetianini proses ekstraksiminyakdedakpadimenggunakanpelarut n-hexane
selama 5 jam padasuhu 65 oC, sedangkan proses
esterifikasdilakukandenganmengguakankatalisasamsulfat (H2SO4) danasamsitrat
(C6H8O7) padasuhu 60 oCselama 2 jam.
1.1PERUMUSAN MASALAH
Permasalahan yang seringdihadapiadalahmahalnyahargaminyaknabati yang
digunakandalampembuatan
biodiesel.Olehkarenaitudicobauntukmenggunakanminyakdedakpadi yang
dapatdigunakansebagai alternatif bahanbakupembuatan biodiesel.
Namundemikianminyakdedakpadimengandungasamlemakbebastetapi dapat diturunkan
dengan proses esterifikasi. Padapenelitianiniminyakdedakpadidiperolehmelalui proses
ekstraksidengan N-Hexane, kemudiandilanjutkandenganprosesesterifikasi yang
bertujuanuntukmengurangikandunganasamlemakbebasnyadenganmenggunakanasamsulf
at (H2SO4)danasamsitrat (C6H8O7).
1.2TUJUAN PENELITIAN
Adapuntujuandaripenelitianiniadalah:
1. Mempelajaripengaruh variabel proses dalam proses esterifikasi
2. Mengujikualitasminyakdedakpadi yang dihasilkan.
1.3MANFAAT PENELITIAN
Adapunmanfaatdaripenelitianiniadalahuntukmemberikanpengetahuantentangb
agaimanapengaruhvariabel proses esterifikasiterhadap % FFA
minyakdedakpadisertamengetahuikualitasminyakdedakpadi yang dihasilkan.
1.4RUANG LINGKUP PENELITIAN
Penelitiandilakukan di Laboratorium Proses Industri Kimia Universitas
Sumareta Utara. Bahanbaku yang digunakanadalahdedakpadi yang
diperolehdariekstraksidedakpadi. Penelitianinidilaksanakandenganduatahapan proses
yaitu proses ekstraksidedakpadi dan proses esterifikasi.
Perbandingandedakdengan n-Hexane : 30 gr : 450 ml
Suhu : 65 oC
WaktuEkstraksi : 5 jam
2. Proses Esterifikasi
Waktu : 2 jam
Suhu : 60 oC
Katalis : -H2SO40,5%, 1%, 1,5%dariberatminyakdedakpadi (Arsidadkk, 2010).
- C6H8O70,1%, 0,2%,
0,3%dariminyakdedakpadi(Ndaruchandra, 2011).
(Sumber :Arsidadkk, 2010)
Analisis yang dilakukandalampenelitianiniadalah :
1. Analisis FFA dalamminyakdedakpadi dilakukan dengan titrasi menggunakan
NaOH.
ABSTRAK
Indonesia sebagai penghasil gabah terbesar ketiga di dunia, memproduksi dedak dalam jumlah besar. Kandungan asam lemak bebas (Free Fatty Acid
(FFA)) yang tinggi menyebabkan minyak dedak padi dapat dikonversi menjadi
Fatty Acid Methyl Ester (biodiesel) dengan esterifikasi. Tujuan dari penelitian ini adalah memanfaatkan dedak sebagai bahan baku pembuatan metil esterserta mempelajari pengaruh variabel dalam proses esterifikasi serta menguji minyak dedak padi yang dihasilkan. Minyak dedak padi merupakan turunan penting dari dedak padi. Kandungan asam lemak bebas dalam dedak padi dapat meningkat cepat karena adanya enzim lipase aktif dalam dedak padi setelah proses penggilingan. Di dalam penelitian ini, digunakan 2 jenis katalis asam yaitu H2SO4
dan C6H8O7. Pada proses ini dedak padi diekstraksi untuk mendapatkan minyak
dedak padi nya dan selanjutnya dilakukan proses esterifikasi untuk menurunkan asam lemak bebasnya dan dilakukan pengujian kadar FFA terhadap minyak dedak padi, analisa produk yang meliputi Analisis % FFA dan komposisi minyak dedak padi dengan GC. Dari analisa gas kromatografi yang kami lakukan, komponen terbesar minyak dedak padi didominasi metil oleat. Selama proses esterifikasi dengan menggunakan katalis H2SO4terjadi penurunan FFA sebesar 96,18 % dan
selama proses esterifikasi dengan menggunakan katalisC6H8O7 terjadi penurunan
PEMANFAATAN DEDAK PADI SEBAGAI BAHAN BAKU
PEMBUATAN METIL ESTER DENGAN PROSES
EKSTRAKSI DAN ESTERIFIKASI DENGAN
KATALIS ASAM SULFAT (H
2SO
4) DAN
ASAM SITRAT (C
6H
8O
7)
SKRIPSI
Oleh
130425008
ATIKA VIVI YANTI SARUMPAET
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PEMANFAATAN DEDAK PADI SEBAGAI BAHAN BAKU
PEMBUATAN METIL ESTER DENGAN PROSES
EKSTRAKSI DAN ESTERIFIKASI DENGAN
KATALIS ASAM SULFAT (H
2SO
4) DAN
ASAM SITRAT (C
6H
8O
7)
SKRIPSI
Oleh
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
ATIKA VIVI YANTI SARUMPAET
130425008
PERNYATAAN KEASLIAN SKRIPSI
saya menyatakan dengan sesungguhnya bahwa skripsi dengan judul:
PEMANFAATAN DEDAK PADI SEBAGAI BAHAN BAKU PEMBUATAN METIL ESTER DENGAN PROSES EKSTRAKSI DAN ESTERIFIKASI
DENGAN KATALIS ASAM SULFAT DAN ASAM SITRAT
dibuat untuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada
Departemen Teknik Kimia Fakultas Teknik Universitas sumatera Utara. Skripsi
ini adalah hasil karya saya kecuali kutipan-kutipan yang telah saya sebutkan
sumbernya.
Demikian pernyataan ini diperbuat, apabila dikemudian hari terbukti bahwa karya
ini bukan karya saya atau merupakan hasil jiplakan maka saya bersedia menerima
sanksi sesuai dengan aturan yang berlaku.
Medan, April 2016
NIM 130425008
PENGESAHAN
Skripsi dengan judul :
PEMANFAATAN DEDAK PADI SEBAGAI BAHAN BAKU
PEMBUATAN METIL ESTER DENGAN PROSES
EKSTRAKSI DAN ESTERIFIKASI DENGAN
KATALIS ASAM SULFAT (H
2SO
4) DAN
ASAM SITRAT (C
6H
8O
7)
dibuat untuk melengkapi persyaratan menjadi Sarjana Teknik pada Departemen
Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini telah
diujikan pada sidang ujian skripsi pada 20 April 2016 dan dinyatakan memenuhi
syarat/sah sebagai skripsi pada Departemen Teknik Kimia Fakultas Teknik
Universitas Sumatera Utara.
Mengetahui, Medan, April 2016
Dosen Penguji I Dosen Penguji II
Dr.Ir.Rondang Tambun, ST, MT
Koordinator Penelitian Dosen Pembimbing
Mersi Suriani Sinaga ST,MT NIP. 19720612 200012 2 001 NIP. 19680820 199802 2 001
PRAKATA
PujidansyukurpenulispanjatkankehadiratTuhan Yang
MahaEsaataslimpahanrahmatdankarunia-Nya
sehinggaSkripsiinidapatdiselesaikan.TulisaninimerupakanSkripsidenganjudul“PE
MANFAATAN DEDAK PADI SEBAGAI BAHANBAKU PEMBUATAN
METIL ESTER DENGAN PROSES EKSTRAKSI DAN ESTERIFIKASI
DENGAN KATALIS ASAM SULFAT (H2SO4) DAN ASAM
SITRAT(C6H8O7)”, berdasarkanhasilpenelitian yang penulislakukan di
DepartemenTeknik Kimia FakultasteknikUniversitas Sumatera Utara.
Skripsiinimerupakansalahsatusyaratuntukmendapatkangelarsarjanateknik.
Hasilpenelitianinisangatbaikuntuk
dipublikasikanataupenelitianinidapatdimanfaatkan di masa yang akandatang,
karena dedak padi yang dapat dikatakan limbah dari penggilingan padi dapat
dimanfaatkan menjadi sesuatu yang ,lebih bermanfaat dan dapat mengurangi
penggunaan bahan bakar yang berasal dari fosil.
Selama
melakukanpenelitiansampaipenulisanskripsiinipenulisbanyakmendapatbantuandar
iberbagaipihak ,untukitupenulismengucapkanterimakasihdanpenghargaan yang
sebesar-besarnyakepadaDr. Ir. Taslim M.Si selakupembimbing.
Penulismenyadaribahwaskripsiinimasihjauhdarisempurnaolehkarenaitupen
ulismengharapkan saran danmasukan demi
kesempurnaanskripsiini.Semogaskripsiinimemberikanmanfaatbagipengembangani
lmupengetahuan.
Penulis
Atika Vivi Yanti Sarumpaet
DEDIKASI
Penulismendedikasikanlaporanhasilpenelitianinikepada:
1. Kedua orang tuapenulis, Pahot Sarumpaet STh dan Tiarmin Malau
2. Saudarapenulis (Devia Rosinta Uli Sarumpaet SKp, Josafat Arahon
Sarumpaet, Josua Saut Hasiholan Sarumpaet)
3. BapakdanibudosenDepartemenTeknik Kimia, FakultasTeknik, Universitas
Sumatera Utara.
4. PegawaiadministrasiDepartemenTeknik Kimia, FakultasTeknik,
Universitas Sumatera Utara.
5. Sahabat-sahabatterbaik di teknik Kimia Ekstensi,
khususnyasemuamahasiswastambuk 2013 yang
memberikanbanyakdukungandansemangatkepadapenulis
6. Seluruhteman-teman, danabang/kakak yang
turutmemberikanbantuankepadapenulisdalammenyelesaikanlaporanhasilpe
RIWAYAT HIDUP PENULIS
Nama : Atika Vivi Yanti Sarumapet
NIM : 130425008
Tempat/tgllahir : Tarutung, 30 Juni 1992
Nama orang tua: Pahot Sarumpaet S.Th
Alamat Orang tua:
Jln. Bahagia No.6 Pematang Siantar
AsalSekolah
• SD HKBP Pearaja Tarutungtahun1998-2004 • SMP Negri 2Tarutung tahun 2004-2007
• SMA Negri 1 Pematang Siantar tahun 2007-2010 • D3 PTKI Medan tahun 2010-2013
Artikel yang telahdipublikasidalamJurnal:
Atikasarumpaet,”Pemanfaatan Dedak Padi sebagai bahan baku Pembuatan Metil
Ester dengan Proses ekstraksi dan Esterifikasi dengan katalis asam Sulfat
ABSTRAK
Indonesia sebagai penghasil gabah terbesar ketiga di dunia, memproduksi dedak dalam jumlah besar. Kandungan asam lemak bebas (Free Fatty Acid
(FFA)) yang tinggi menyebabkan minyak dedak padi dapat dikonversi menjadi
Fatty Acid Methyl Ester (biodiesel) dengan esterifikasi. Tujuan dari penelitian ini adalah memanfaatkan dedak sebagai bahan baku pembuatan metil esterserta mempelajari pengaruh variabel dalam proses esterifikasi serta menguji minyak dedak padi yang dihasilkan. Minyak dedak padi merupakan turunan penting dari dedak padi. Kandungan asam lemak bebas dalam dedak padi dapat meningkat cepat karena adanya enzim lipase aktif dalam dedak padi setelah proses penggilingan. Di dalam penelitian ini, digunakan 2 jenis katalis asam yaitu H2SO4
dan C6H8O7. Pada proses ini dedak padi diekstraksi untuk mendapatkan minyak
dedak padi nya dan selanjutnya dilakukan proses esterifikasi untuk menurunkan asam lemak bebasnya dan dilakukan pengujian kadar FFA terhadap minyak dedak padi, analisa produk yang meliputi Analisis % FFA dan komposisi minyak dedak padi dengan GC. Dari analisa gas kromatografi yang kami lakukan, komponen terbesar minyak dedak padi didominasi metil oleat. Selama proses esterifikasi dengan menggunakan katalis H2SO4terjadi penurunan FFA sebesar 96,18 % dan
selama proses esterifikasi dengan menggunakan katalisC6H8O7 terjadi penurunan
DAFTAR ISI
KATA PENGANTAR i
DAFTAR ISI ii
DAFTAR GAMBAR iv
DAFTAR TABEL v
BAB I PENDAHULUAN 1
1.1 LATAR BELAKANG 1
1.2 PERUMUSAN MASALAH 3
1.3 TUJUAN PENELITIAN 4
1.4 MANFAAT PENELITIAN 4
1.5 RUANG LINGKUP PENELITIAN 4
BAB II TINJAUAN PUSTAKA 6
2.1 BIODIESEL 6
2.2 DEDAK PADI 7
2.3 MINYAK DEDAK PADI 8
2.4 ASAM SULFAT 9
2.5 EKSTRAKSI 10
2.6 ESTERIFIKASI 11
2.6.1 Hal-hal Yang Mempengaruhi Ekstraksi 12
2.7 TRANSESTERIFIKASI 14
2.7.1 Hal-hal yang mempengaruhi transesterifikasi 15
BAB III METODOLOGI PENELITIAN 17
3.1 PENETAPAN VARIABEL 17
3.2 BAHAN DAN PERALATAN 17
3.2.1 Bahan 17
3.3 LANGKAH PERCOBAAN 18
3.3.1 LangkahPercobaan Ekstraksi 18
3.3.2 LangkahPercobaanEsterifikasi 18
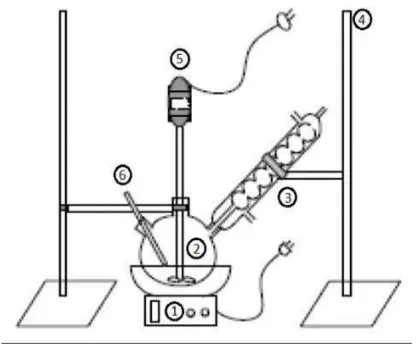
3.4 GAMBAR RANGKAIAN ALAT 19
3.5 FLOWCHART PERCOBAAN 19
3.5.1 Flowchart Proses Ekstraksi 19
3.5.2 Flowchart Proses Estrifikasi 20
3.5.2.1 Flowchartuntukpenambahankatalis H2SO4 20
3.5.2.2 Flowchart untukpenambahankatalis C6H8O721
3.5.3 Flowchart Analisa FFA 22
BAB IV HASIL DAN PEMBAHASAN
4.1 Pengaruh waktu dan Penambahan katalis Asam Sulfat (H2SO4)
terhadap % FFA pada berbagai suhu. 23
4.2 Pengaruh waktu dan penambahan katalis Asam Sitrat
(C6H8O7)terhadap % FFA pada berbagai suhu
25
4.3 Hasil GC produk Metil ester 27
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan 29
5.2 Saran 29
DAFTAR PUSTAKA 30
LAMPIRAN I 31
LAMPIRAN II 36
LAMPIRAN III 38
DAFTAR TABEL
Tabel 1.1 Penelitianterdahuluberkenaandenganekstraksiminyakdedakpadi3
Tabel 1.2 penelitianterdahuluberkenaandenganesterifikasiminyakdedakpadi 3
Tabel 2.1 Pengaruhwaktupenyimpanandedakterhadapkandungan FFA minyak
9
Tabel 2.3 Komposisiasamlemakbebasdalamminyakdedakpadi 9
Tabel 2.4 Sifatfisikadankimiaasamsulfat 10
Tabel 4.1Hasil-Hasil Percobaan Yang Diperoleh Pada Berbagai Keadaan
DenganPenambahanKatalis H2SO4 Terhadap % FFA23
Tabel 4.2 Hasil-hasil percobaan yang diperoleh pada berbagai keadaan dengan
PenambahanKatalis C6H8O7 Terhadap % FFA25
Tabel 4.3 KomposisiAsam Lemak Minyak dedak padi Berdasarkan AnalisaGC
SebelumProses Esterifikasi 27
Tabel 4.3 Komposisi Asam Lemak minyak dedak padi dengan penambahankatalis
H2SO41 % v/v pada suhu 60 oC berdasarkan Analisa GC 27
Tabel 4.3 Komposisi Asam Lemak minyak dedak padi dengan penambahankatalis