LAMPIRAN A
DATA BAHAN BAKU
A.1 KOMPOSISI ASAM LEMAK MINYAK DEDAK PADI
Tabel A.1 Komposisi Asam Lemak Bahan Baku Minyak Dedak Padi
Asam Lemak Komposisi
(%)
Berat Molekul (gram/mol)
% x BM (gram/mol)
Asam Laurat (C12:0) 0,0114 200 0,0228
Asam Miristat (C14:0) 0,3912 228 0,8919
Asam Palmitat (C16:0) 20,8620 256 53,4067
Asam Palmitoleinat (C16:1) 0,2638 254 0,6701
Asam Stearat (C18:0) 2,0197 284 5,7359
Asam Oleat (C18:1) 42,4643 282 119,7493
Asam Linoleat (C18:2) 32,2081 280 90,1827
Asam Linolenat (C18:3) 1,2199 278 3,3913
Asam Arakidat (C20:0) 0,0522 312 0,1629
Asam Eikosenoat (C20:1) 0,5074 310 1,5729
Jumlah 100 275,7866
Dari perhitungan maka diperoleh berat molekul rata-rata FFA minyak dedak padi sebesar 275,7866 gram/mol.
A.2 KOMPOSISI TRIGLISERIDA MINYAK DEDAK PADI Tabel A.2 Komposisi Trigliserida Bahan Baku Minyak Dedak Padi
Asam Lemak Komposisi
(%)
Berat Molekul (gram/mol)
% x BM (gram/mol)
Asam Laurat (C12:0) 0,0114 638 0,0727
Asam Miristat (C14:0) 0,3912 722 2,8245
Asam Palmitat (C16:0) 20,8620 806 168,1477
Asam Palmitoleinat (C16:1) 0,2638 800 2,1104
Asam Stearat (C18:0) 2,0197 890 17,9753
Asam Oleat (C18:1) 42,4643 884 375,3844
Asam Linoleat (C18:2) 32,2081 878 282,7871
Asam Linolenat (C18:3) 1,2199 872 10,6375
Asam Arakidat (C20:0) 0,0522 974 0,5084
Asam Eikosenoat (C20:1) 0,5074 968 4,9116
Dari perhitungan maka diperoleh berat molekul rata-rata trigliserida minyak dedak padi sebesar 865,3598 gram/mol.
A.3 KADARFREE FATTY ACID(FFA) MINYAK DEDAK PADI % Kadar FFA =
10 m BM V N sampel RBO Lemak Asam titran NaOH = 10 05 , 7 7866 , 275 25 , 1 25 , 0
LAMPIRAN B
DATA PENELITIAN
B.1 DATA LOGAM KALIUM PADA KOH/ZEOLIT ALAM Tabel B.1 Hasil Analisis Kandungan Logam Kalium pada
Variasi Konsentrasi KOH
No.
Konsentrasi Larutan KOH (gram dalam
100 mlaquadest)
Kandungan Logam Kalium (%)
1 0 1,2758
2 75 36,0473
3 100 33,9951
4 125 16,3029
5 150 12,8272
6 175 7,7375
B.2 DATA DENSITAS BIODIESEL
Tabel B.2 Hasil Analisis Densitas Biodiesel Rasio Mol Alkohol / Minyak Waktu (jam) Suhu (oC)
Jumlah Katalis (% berat)
Densitas (kg/m3)
8:1 2,0 60 2,0 866,6872
8:1 2,0 60 3,0 868,3065
8:1 2,0 60 4,0 866,2824
10:1 2,0 60 2,0 867,4969
10:1 2,0 60 2,5 867,0920
10:1 2,0 60 3,0 866,6872
10:1 2,0 60 3,5 866,2824
10:1 2,0 60 4,0 867,0920
10:1 1,5 60 2,0 867,0920
10:1 2,5 60 2,0 865,4728
10:1 3,0 60 2,0 866,6872
10:1 3,5 60 2,0 864,6505
12:1 2,0 60 2,0 867,4969
12:1 2,0 60 2,0 866,6872
B.3 DATA VISKOSITAS KINEMATIK BIODIESEL
Tabel B.3 Hasil Analisis Viskositas Kinematik Biodiesel
Rasio Mol Alkohol /
Minyak
Waktu (jam)
Suhu (oC)
Jumlah Katalis (% berat)
trata-rata (detik)
Viskositas Kinematik
(cSt)
8:1 2,0 60 2,0 358,3333 4,4171
8:1 2,0 60 3,0 348,6667 4,2979
8:1 2,0 60 4,0 350,6667 4,3226
10:1 2,0 60 2,0 369,0000 4,5486
10:1 2,0 60 2,5 367,3333 4,5280
10:1 2,0 60 3,0 372,0000 4,5855
10:1 2,0 60 3,5 359,6667 4,4335
10:1 2,0 60 4,0 356,0000 4,3883
10:1 1,5 60 2,0 368,3333 4,5403
10:1 2,5 60 2,0 357,6667 4,4089
10:1 3,0 60 2,0 354,3333 4,3678
10:1 3,5 60 2,0 378,3333 4,6636
12:1 2,0 60 2,0 349,3333 4,3061
12:1 2,0 60 2,0 349,0000 4,3020
B.4 DATAYIELDMETIL ESTER
Tabel B.4 Hasil AnalisisYieldMetil Ester Rasio Mol
Alkohol / Minyak
Waktu (jam)
Suhu (oC)
Jumlah Katalis (% berat)
Kemurnian (%)
Yield (%)
8:1 2,0 60 2,0 97,5325 92,78
8:1 2,0 60 3,0 96,7020 95,31
8:1 2,0 60 4,0 96,3792 95,20
10:1 2,0 60 2,0 98,7673 98,71
10:1 2,0 60 2,5 96,2321 97,05
10:1 2,0 60 3,0 98,6635 96,95
10:1 2,0 60 3,5 98,5918 95,11
10:1 2,0 60 4,0 99,0741 96,86
10:1 1,5 60 2,0 96,5299 95,82
10:1 2,5 60 2,0 96,4410 92,12
10:1 3,0 60 2,0 97,0280 90,55
10:1 3,5 60 2,0 93,8454 88,30
12:1 2,0 60 2,0 96,9003 96,53
12:1 2,0 60 2,0 96,2426 94,01
LAMPIRAN C
CONTOH PERHITUNGAN
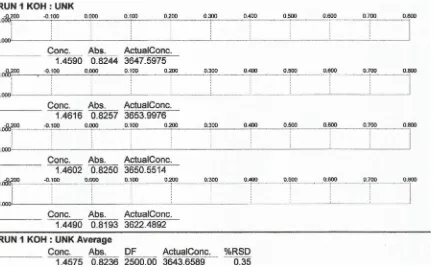
C.1 PERHITUNGAN KADAR LOGAM K (KALIUM) PADA KATALIS KOH/ZEOLIT ALAM
Kadar Logam K =
Sampel Massa
V . ActualConc
Keterangan : ActualConc. = Hasil pembacaan pada AAS
V = Volume pengenceran (ml)
Massa sampel = Berat sampel yang diuji (gram)
ActualConc. = 3643,6589
V = 100 ml
Massa sampel = 1,0108 gram
Kadar Logam K =
Sampel Massa V . ActualConc = 1,0108 100 3643,6589
= 360472,7839 ppm
= 1.000.000 % 100 9 360472,783
= 36,0473 %
Untuk konsentrasi larutan KOH yang lainnya sama dengan perhitungan di
atas.
C.2 PERHITUNGAN KADAR FFA MINYAK DEDAK PADI (RICE BRAN OIL)
Kadar FFA = x100%
000 1 Sampel Massa M V N
Keterangan : N = Normalitas larutan NaOH (mol/l)
M = Berat molekul FFA minyak dedak padi (BM = 275,7866
gram/mol)
Normalitas larutan NaOH = 0,25 N
Volume larutan NaOH terpakai = 1,25 ml
BM FFA = 275,7866 gram/mol
Berat minyak dedak padi = 7,05 gram
Kadar FFA = x100%
000 1 Sampel Massa M V N
= x100%
000 1 7,05 275,7866 1,25 0,25
= 1,225 %
C.3 PERHITUNGAN KEBUTUHAN METANOL
O O
H2C-O-C-R1 R1-C-OCH3 H2C-OH
O O
HC-O-C-R2 + 3CH3OH KOH/Zeolit Alam R2-C-OCH3 + HC-OH
O O
H2C-O-C-R3 R3-C-OCH3 H2C-OH
Trigliserida Metanol Biodiesel Gliserol
Massa Minyak Dedak Padi = 50 gram
Metanol : Minyak Dedak Padi = 8 : 1 (mol/mol)
BM Trigliserida = 865,3598 gram/mol
Mol Minyak Dedak Padi =
da Trigliseri BM Massa = gram/mol 865,3598 gram 50
= 0,0578 mol
Mol metanol = 1 8
Maka massa metanol = mol metanol x BM metanol
= 0,4622 mol x 32 gram/mol
= 14,7915 gram
Volume metanol =
m = gram/ml 0,7918 gram 14,7915= 18,6809 ml
Untuk kebutuhan metanol yang lainnya sama dengan perhitungan di atas.
C.4 PERHITUNGANYIELDBIODIESEL
Yield = x Kemurnian
Baku Bahan Massa Praktik Biodiesel Massa
= x 98,7673%
gram 50
gram 49,97
= 98,71 %
Untuk data yang lainnya sama dengan perhitungan di atas.
C.5 PERHITUNGAN DENSITAS BIODIESEL
Volume piknometer =
air Densitas
air Massa
= 24,7033 ml
Densitas sampel =
piknometer Volume
sampel Massa
Massa piknometer kosong = 21,46 gram = 0,02146 kg
Massa piknometer + biodiesel = 42,89 gram = 0,04289 kg
Massa biodiesel = 21,43 gram = 0,02143 kg
Densitas biodiesel =
3 6 -m 10 x 24,7033 kg
0,02143 = 867,4969 kg/m3
Untuk data yang lainnya sama dengan perhitungan di atas.
C.6 PERHITUNGAN VISKOSITAS BIODIESEL
sg =
air Densitas
Viskositas sampel = k x sg x t
Keterangan : k = konstanta viskosimeter (kg/m.s2)
t = waktu alir (s)
Kalibrasi air :
air(40oC) = 992,25 kg/m3
Viskositas air (40oC) = 0,6560 x 10-3kg/m.s
tair= 53,63 detik
sgair= 1
Viskositas air = k x sg x t
0,6560 x 10-3kg/m.s = k x 1 x 53,63 s
k = 1,22 x 10-5kg/m.s2
Viskositas biodiesel : trata-rata biodiesel= 369 detik
sgbiodiesel= 3 3
kg/m 992,25
kg/m 867,4969
= 0,8743
Viskositas biodiesel = k x sg x t
= 1,22 x 10-5x 0,8743 x 369
= 3,9459 x 10-3kg/m.s
Viskositas kinematik = 3
-3
kg/m 867,4969
kg/m.s 10
x 3,9459
= 4,5486 x 10-6m2/s
= 4,5486 mm2/s
= 4,5486 cSt
LAMPIRAN D
HASIL ANALISIS KOMPOSISI BAHAN BAKU
MINYAK DEDAK PADI, KATALIS KOH/ZEOLIT
ALAM, DAN BIODIESEL
D.1 HASIL ANALISIS KOMPOSISI BAHAN BAKU MINYAK DEDAK PADI
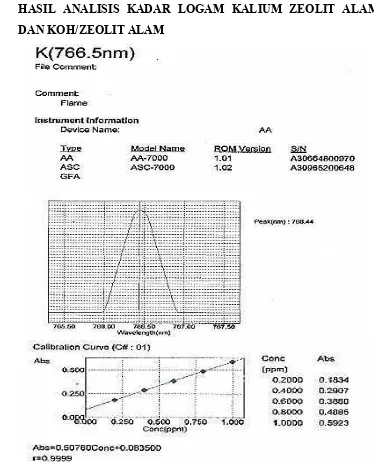
D.2 HASIL ANALISIS KADAR LOGAM KALIUM ZEOLIT ALAM DAN KOH/ZEOLIT ALAM
Gambar D.3 Hasil Analisis untuk Sampel Zeolit Alam Tanpa Modifikasi Senyawa KOH
D.3 HASIL ANALISIS GUGUS ZEOLIT ALAM DAN KOH/ZEOLIT ALAM
Gambar D.5 Hasil Analisis FTIR untuk Sampel Zeolit Alam Tanpa Modifikasi Senyawa KOH
D.4 HASIL ANALISIS KOMPOSISI BIODIESEL
Gambar D.7 Hasil Analisis GC Komposisi Biodiesel pada Kondisi Suhu Reaksi 60oC, Perbandingan Mol Alkohol terhadap Minyak 10:1, Waktu Reaksi 2 Jam,
LAMPIRAN E
DOKUMENTASI PENELITIAN
E.1 FOTO PREPARASI ZEOLIT ALAM
Gambar E.1 Foto Zeolit Alam
Gambar E.2 Foto Perendaman dengan H2O2
Gambar E.4 Foto Zeolit Alam Hasil Pemanasan dengan Penangas Air
Gambar E.5 Foto Perendaman denganAquadest
Gambar E.7 Foto Pemanasan dengan Oven
Gambar E.8 Foto Hasil Pemanasan dengan Oven
Gambar E.10 Foto Pengayakan Serbuk Zeolit Alam
Gambar E.11 Foto Serbuk Zeolit Alam
E.2 FOTO PROSES IMPREGNASI ZEOLIT ALAM
Gambar E.13 Foto Hasil Impregnasi Zeolit Alam
Gambar E.14 Foto Pemanasan dengan Oven
Gambar E.16 Foto Hasil Penyaringan dengan Pompa Vakum
Gambar E.17 Foto Proses Kalsinasi denganFurnace
Gambar E.19 Foto Penggilingan dengan Mortar
Gambar E.20 Foto Katalis KOH/Zeolit Alam
E.3 FOTO PENGUJIAN KADAR ASAM LEMAK BEBAS
E.4 FOTO PROSES TRANSESTERIFIKASI
Gambar E.22 Foto Minyak Dedak Padi
Gambar E.23 Foto Rangkaian Alat Proses Transesterifikasi
Gambar E.25 Foto Penyaringan Katalis dengan Pompa Vakum
Gambar E.26 Foto Pemisahan Hasil Transesterifikasi dengan Corong Pemisah
Gambar E.28 Foto Biodiesel Hasil Pencucian
E.5 FOTO ANALISIS BIODIESEL
Gambar E.29 Foto Analisis Densitas
DAFTAR PUSTAKA
[1] Widayat, Agam Duma Kalista Wibowo dan Hadiyanto, “Study on Production Process of Biodiesel from Rubber Seed (Hevea Brasiliensis) by In Situ (Trans)Esterification Method with Acid Catalyst” Journal Energy Procedia,32 (2013), hal. 64 – 73.
[2] Ali Shemsedin Reshad, Pankaj Tiwari dan Vaibhav V. Goud, “Extraction of Oil from Rubber Seeds for Biodiesel Application: Optimization of Parameters” Elsevier, Fuel150 (2015), hal. 636–644.
[3] Ru Yang, Mengxing Su, Jianchun Zhang, Fuqiang Jin, Chunhong Zha, Min Li, dan Xinmin Hao, “Biodiesel Production from Rubber Seed Oil Using Poly (Sodium Acrylate) Supporting NaOH as a Water-Resistant Catalyst” Elsevier,Bioresource Technology,102 (2011), hal. 2665–2671.
[4] Huei Ruey Ong, Maksudur R. Khan, M.N.K. Chowdhury, Abu Yousuf dan Chin Kui Cheng, “Synthesis and Characterization of Cuo/C Catalyst for the Esterification of Free Fatty Acid in Rubber Seed Oil” Elsevier,Journal Fuel,120 (2014), hal. 195–201.
[5] Yanna Syamsuddin dan Husni Husin, “Pembuatan Katalis Padat ZrO2/Al2O3untuk Produksi Biodiesel dari Minyak Jarak”Jurnal Rekayasa Kimia dan Lingkungan,Vol. 7, No. 3, (2010), hal. 112-117.
[6] Chanatip Samart, Surachai Karnjanakom, Chaiyan Chaiya, Prasert Reubroycharoen, Ruengwit Sawangkeaw, dan Metta Charoenpanich, “Statistical Optimization of Biodiesel Production from Para Rubber Seed Oil by SO3H-MCM-41 Catalyst” Elsevier, Arabian Journal Of Chemistry (2015) (In Press).
[7] Ricky Indra Kusuma, Johan Prabowo Hadinoto, Aning Ayucitra, Felycia Edi Soetaredjo, dan Suryadi Ismadji, “Natural Zelite from Pacitan Indonesia, as Catalysts Support for Transesterification of Palm Oil” Elsevier,Applied Clay Science,74 (2013), hal. 121-126.
[8] K. Noiroj, P. Intarapong, A. Luengnaruemitchai, S. Jai-In, “A Comparative Study of KOH/Al2O3 and KOH/Nay Catalysts for Biodiesel Production via Transesterification from Palm Oil” Renewable Energy, 34 (2009), hal. 1145–1150.
[9] W. Widayat dan S. Suherman, “Biodiesel Production from Rubber Seed Oil via Esterification Process” Int. Journal of Renewable Energy Development1 (2) (2012), hal. 57-60.
[11] S.Senthil Kumar dan K.Purushothaman, “High FFA Rubber Seed Oil as an Alternative Fuel for Diesel Engine – An Overview” Research Inventy, International Journal of Engineering and Science, Vol. 1, Issue 10 ISBN: 2319-6483, ISSN: 2278-4721 (December 2012), hal. 16-24.
[12] BPS. 2015. “Padi”. www.bps.go.id. Diakses pada tanggal 26 Juni 2015.
[13] M. Hadipernata, W. Supartono, dan M. A. F. Falah, “Proses Stabilisasi Dedak Padi (Oryza sativa L) Menggunakan Radiasi Far Infra Red (FIR) sebagai Bahan Baku Minyak Pangan” Jurnal Aplikasi Teknologi Pangan Vol. 1 No. 4. (2012) hal. 103-107.
[14] Sh. K. Amin dan H.A. M. Abdallah, “Enhancement of Free Fatty Acid in Rice Bran Oil for Acid Catalysis Biodiesel Production”Australian Journal of Basic and Applied Sciences, 6, ISSN 1991-8178 (2012), hal. 795-806.
[15] Emmanuel I. Bello dan Oluwole O. Oluboba, “Rice Bran Oil Biodiesel” European Journal of Engineering and Technology, Vol. 2 No. 2 ISSN 2056-586 (2014), hal. 59-69.
[16] Luluk Amnah Fitriyana, Soeprodjo dan Sri Kadarwati, “Produksi Biodiesel dari Dedak Padi (Rice Bran) Melalui Dua Tahap Reaksi In-Situ” Indonesian Journal of Chemical Science,1 (2) ISSN NO 2252-6951 (2012), hal. 140-146.
[17] Man Kee Lam, Keat Teong Lee dan Abdul Rahman Mohamed, “Homogenous, Heterogeneous and Enzymatic Catalysts for Transesterification of High Free Fatty Acid Oil (Waste Cooking Oil) to Biodiesel : A Review” Elsevier, Biotechnology Advances, 28 (2010), hal. 500-518.
[18] Mopelola Abeke Omotoso dan Olakunle Alex Akinsanoye, “A Review of Biodiesel Generation From Non Edible Oil Seed Oils Crop Using Conventional Heterogeneous Catalysts” Journal of Petroleum Technology and Alternative Fuels, Vol. 6 (1) ISSN 2360-8560 (Februari, 2015), hal. 1-12.
[19] M. E Borges dan L Diaz, “Recent Development on Heterogeneous Caralysts for Biodiesel Production by Oil Esterification and Transesterification Reactions : A review” Elsevier, Renewable and Sustainable Energy Reviews, 16 (2012), hal. 2839-2849.
[20] Yi-Hsu Ju dan Shaik Ramjan Vali, “Rice Bran Oil as a Potential Resource for Biodiesel : A Review. National Taiwan University of Science and Technology, Taipei” Journal of Scientific & Industrial Research, Vol. 64 (November 2005), hal. 866-882.
[22] Xuebing Zhao, Feng Qi, Chongli Yuan, Wei Du, dan Dehua Liu, “Lipase-Catalyzed Process for Biodiesel Production: Enzyme Immobilization, Process Simulation and Optimization”,Renewable and Sustainable Energy Reviews,44 (2015), hal. 182 – 197.
[23] Science Lab. 2015. “Material Safety Data Sheet Methanol MSDS”. www.sciencelab.com. Diakses pada tanggal 30 Juni.
[24] L.M. Atadashi, M.K. Aroua, A.R. Abdul Aziz dan N.M.N. Sulaiman, “The Effect of Catalysts in Biodiesel Production : A Review” Elsevier,Journal of Industrial and Engineering Chemistry,19 (2013), hal. 14-26.
[25] Kyong-Hwan Chung, Duck-Rye Chang dan Byung–Geon Park, “Removal of Free Fatty Acid in Waste Frying Oil by Esterification with Methanol on Zeolite Catalysts”Bioresource Technology,99 (2008), hal 7438-7443.
[26] Abebe K. Endalew, Yohannes Kiros dan Rolando Zanzi, “Inorganic Heterogeneous Catalysts for Biodiesel Production from Vegetable Oils”. Elsevier,Biomass and Bioenergy,35 (2011), hal. 3787-3809.
[27] Rahmiyati Kasim. “Desain Esterifikasi Menggunakan Katalis Zeolit pada Proses Pembuatan Biodiesel Dari Crude Palm Oil (CPO) melalui Metode Dua Tahap Esterifikasi-Transesterifikasi”. Tesis, Pasca Sarjana Institut Pertanian Bogor, Bogor, 2010.
[28] Anthony Satriyo Utomo. “Preparasi NaOH/Zeolit sebagai Katalis Heterogen untuk Sintesis Biodiesel dari Minyak Goreng Secara Transesterifikasi”. Skripsi Program Studi Teknik Kimia Universitas Indonesia, Depok, 2011.
[29] Dimitar Georgiev, Bogdan Bogdanov, Krasimira Angelova, Irena Markovska dan Yancho Hristov, “Synthetic Zeolites - Structure, Clasification, Current Trends in Zeolite Synthesis Review”Economics and Society development on the Base of Knowledge, Vol. 7 (2009), hal. 6-11.
[30] Hector Valdes, Serguei Alejandro, dan Claudio A. Zaror, “Natural Zeolite Reactivity Towards Ozone: The Role of Compensating Cations” Journal of Hazardous Materials, Volume: 227– 228 (2012), hal: 34– 40.
[31] A.P. Singh Chouhan dan A.K. Sarma, “Modern Heterogeneous Catalysts for Biodiesel Production : A Comprehensive Review” Elsevier,Renewable and Sustainable Energy Reviews,15 (2011), hal. 4378-4399.
[32] Shaobin Wang dan Yuelian Peng, “Review : Natural Zeolites as Effective Adsorbents in Water and Wastewater Treatment” Chemical Engineering Journal,156 (2010), hal. 11-24.
Some Industrial Zeolite Rich Rocks” Elsevier, Microporous and Mesoporous Materials(2015) (In Press).
[34] Faheem H. Akhtar, Yasir A. Elsheikh, M. Bassyouni, Monazza Kaukab, Ayyaz Muhammad dan Nadeem Feroze, “An Alkali Catalyzed Transesterification of Rice Bran, Cottonseed and Waste Cooking Oil” Scientific Paper. Hem. Ind. 68 (3) (2014), hal. 347-355.
[35] M. Mathiyazhagan dan A. Ganapathi, “Review Article Factors Affecting Biodiesel Production” Research in Plant Biology, 1(2) ISSN: 2231-5101 (2011), hal. 1-5.
[36] Aminul Islam, Yun Hin Taufiq-Yap, Chi-Ming Chu, Eng-Seng Chan dan Pogaku Ravindra, “Studies Design of Heterogeneous Catalysts for Biodiesel Production.” Elsevier, Process and Environmental Protection, Vol. 91(2013), hal. 131-144.
[37] Haitang Wu, Junhua Zhang, Qin Wei, Jilu Zheng dan Jianan Zhang, “Transesterification of Soybean Oil to Biodiesel Using Zeolite Supported CaO as Strong Base Catalysts” Elsevier, Fuel Processing Technology,109 (2013), hal. 13-18.
[38] Kian Heed Kay dan Suhaimi Md Yasir, “Biodiesel Production From Low Quality Crude Jatropha Oil Using Heterogeneous Catalysts” Elsevier, APCBEE Procedia3 (2012), hal. 23-27.
[39] Joana M. Dias, Maria C. M. Alvim-Ferraz, Manuel F. Almeida, Jose D. Mendez Diaz, Manuel Sanchez Polo, dan Jose Rivera Utrilla, “Selection of Heterogeneous Catalysts for Biodiesel Production from Animal Fat” Elsevier,Fuel, 94 (2012), hal. 418-425.
[40] Dae-Won Lee, Young-Moo Park dan Kwan-Young Lee, “Heterogeneous Base Catalysts for Transesterification in Biodiesel Synthesis”. Springer, Catal Surv Asia, 13 (2009), hal. 63-77.
[41] Kornkanok Watcharathamrongkul, Bunjerd Jongsomjit dan Muenduen Phisalaphong, “Calcium Oxide Based Catalysts for Ethanolisis of Soybean Oil”Songklanakarin J. Sci. Technology,32 (6) (2010), hal. 627-634.
[42] A.S. Ramadhas, S. Jayaraj, dan C. Muraleedharan, “Biodiesel Production From High FFA Rubber Seed Oil”, Elsevier, Fuel, 84 (2005), hal. 335– 340.
[43] Evangelista, Joao Paulo da Costa, Manda Duarte Gondim, Luiz Di Souza dan Antonio Souza Araujo, “Alumina Suported Potassium Compounds as Heterogenous Catalysts for Biodiesel Production : A Review” Elsevier, Renewable and Sustainable Energy Reviews,59 (2016), hal. 887-894.
[45] Robert H. Perry, Dow W. Green, Chemical Engineering HandBook. 7th
Edition(New York: McGraw-Hill Book Company, 1997), hal. 16-4.
[46] Ates, Ayten dan Gokcen Akgul, “Modification of Natural Zeolite with NaOH for Removal of Manganese in Drinking Water” Elsevier, Powder Technology, 287 (2016), hal. 285-291.
[47] Mohammad Almjadleh, Sameer Alasheh dan Ibrahim Raheb, “Use of Natural and Modified Jordanian Zeolitic Tuff for Removal of Cadmium(II) from Aqueous Solutions”Jordan Journal of Civil Engineering, Vol. 8, No. 3. (2014), hal. 332-343.
[48] Donald L. Pavia, Gary M. Lampman, George S. Kriz. Introduction to Spectroscopy : A Guide for Students of Organic Chemistry (United State of America : Thomson Learning, 2001), hal. 26.
[49] Evangelos P. Favvas, Constantinos G. Tsanaktsidis, Andreas A. Sapalidis, George T. Tzilantonis, Sergios K. Papageorgiou dan Athanasios Ch, Mitropoulos, “Clinoptilolite, a Natural Zeolite Material : Structural Characterization and Performance Evaluation on its Dehydration Properties of Hydrocarbon-Based Fuels” Elsevier, Microporous and Mesoporous Materials,225 (2016), hal. 385-391.
[50] K. Barczyk, W. Mozgawa, dan M. Krol. “Studies of Anions Sorption on Natural Zeolite” Elsevier, Spectrohimica Acta Part A : Molecular and Biomolecular Spectroscopy,133 (2014), hal. 876-882.
[51] Andika Munandar, Didik Krisdiyanto, Khamidinal dan Pedy Artsanti, “Adsorpsi Logam Pb dan Fe dengan Zeolit Alam Teraktivasi Asam Sulfat”. UIN Sunan Kalijaga, Yogyakarta. Seminar Nasional Kimia dan Pendidikan Kimia VI ISBN : 979363174-0. 2014.
[52] Wuttichai Roschat, Theeranum Siritanon, Boonyawan Yoosuk dan Vinich Promarak, “Risk Husk Derived Sodium Silicate as a Highly Efficient and Low Cost Basic Heterogenous Catalyst for Biodiesel Production” Elsevier, Energy Conversion and Management,119 (2016), hal. 453-462.
[53] Guan Yi Chen, Rui Shan, Bei Bei Yan, Jia Fu Shi, Shang Yao Li dan Chang Ye Liu, “Remarkably Enchancing the Biodiesel Yield from Palm Oil Upon Abalone Shell Derived CaO Catalysts Treated by Ethanol” Elsevier,Fuel Processing Technology,143 (2016), hal. 110-117.
[54] Gashaw, Alemayehu dan Abile Teshita, “Production of Biodiesel from Waste Cooking Oil and Factors Affecting Its Formation: A Review” International Journal of Renewable and Sustainable Energy, Volume: 3, (2014), hal: 92-98.
Oil : Catalyst Characterization and Biodiesel Yield Performance” Elsevier, Applied Energy,160 (2015), hal. 58-70.
[56] I. Boumesbah, Z. Hachaichi-Sadouk dan A. Tazerouti, “Biodiesel Production from Waste Frying Oil and Determination of Fuel Properties” Revue des Energies Renouvelables SIENR’14 Ghardaïa(2014), hal. 109 – 113.
[57] Barabaas, Istvan dan Ioan-Adrian Todorut. “Biodiesel Quality, Standards and Properties, Biodiesel- Quality, Emissions and By-Products”. Technical University of Cluj-Napoca, Romania. 2011.
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilakukan di Laboratorium Penelitian, Departemen Teknik Kimia
Fakultas Teknik, Universitas Sumatera Utara, Medan. Penelitian ini dilakukan
selama lebih kurang 6 bulan.
3.2 BAHAN DAN PERALATAN
3.2.1 Bahan Penelitian
Pada penelitian ini bahan yang digunakan antara lain:
1. Minyak Dedak Padi (RBO)
2. Zeolit Alam
3. Aquadest(H2O)
4. Potassium Hidroksida (KOH)
5. Metanol (CH3OH)
6. Phenolftalein (C20H14O4)
7. Natrium Hidroksida (NaOH)
8. Hidrogen Peroksida (H2O2) 30%
9. N-Heksana
3.2.2 Peralatan Penelitian
Pada penelitian ini peralatan yang digunakan antara lain :
1. Erlenmeyer
2. Magnetic Stirrer
3. Hot Plate
4. Muffle furnace
5. Oven
6. Refluks Kondensor
7. Corong Pemisah
9. Gelas Ukur
10. Neraca Digital
11. Batang Pengaduk
12. Spatula
13. Termometer
14. Corong Gelas
15. Pipet Tetes
16. Statif dan Klem
17. Stopwatch
18. Piknometer
19. Viskosimeter Ostwald
20. Karet Penghisap
21. Buret
22. Vacuum filter
23. Water bath
24. Kertas saring Whatman no. 42
3.3 RANCANGAN PERCOBAAN
3.3.1 Modifikasi Katalis
Modifikasi katalis zeolit alam dengan KOH dilakukan dengan variabel
tetap berupa kecepatan pengadukan, suhu reaksi, dan rasio massa zeolit/ larutan
KOH serta variabel bebas berupa konsentrasi larutan KOH. Adapun kombinasi
[image:33.595.120.513.592.708.2]perlakuan penelitian dapat dilihat pada tabel 3.1 berikut :
Tabel 3.1 Rancangan Percobaan Modifikasi Katalis
Run Kecepatan Pengadukan (rpm) Suhu (ºC) Rasio Massa Zeolit/Larutan KOH Konsentrasi Larutan KOH
(gram/mLaquadest)
1
500 60 1:4
75/100
2 100/100
3 125/100
4 150/100
3.3.2 Sintesis Biodiesel
Sintesis biodiesel dilakukan dengan reaksi transesterifikasi dengan
variabel bebas jumlah katalis KOH/zeolit alam, waktu reaksi dan rasio mol
metanol/minyak. Sedangkan variabel tetap berupa suhu reaksi transesterifikasi 60
ºC dan kecepatan pengadukan 500 rpm. Adapun rancangan percobaan yang akan
[image:34.595.131.530.231.510.2]dilakukan dapat dilihat pada Tabel 3.2 berikut
Tabel 3.2 Rancangan Percobaan Sintesis Biodiesel
Run Rasio metanol/minyak (mol/mol) Suhu Reaksi (ᵒC) Waktu Reaksi (Jam) Katalis (% berat)
1 10 : 1 60 2,0 2,0
2 10 : 1 60 2,0 2,5
3 10 : 1 60 2,0 3,0
4 10 : 1 60 2,0 3,5
5 10 : 1 60 2,0 4,0
6 10 : 1 60 1,5 2,0
7 10 : 1 60 2,5 2,0
8 10 : 1 60 3,0 2,0
9 10 : 1 60 3,5 2,0
10 8 : 1 60 2,0 2,0
11 8 : 1 60 2,0 3,0
12 8 : 1 60 2,0 4,0
13 12 : 1 60 2,0 2,0
14 12 : 1 60 2,0 3,0
15 12 : 1 60 2,0 4,0
3.4 PROSEDUR PENELITIAN
3.4.1 PretreatmentBahan Baku
Zeolit alam yang digunakan berasal dari PT. Rudang Jaya, yang terlebih
dahulu dibersihkan dari impuritis yang berupa senyawa – senyawa organik yang
terdapat di dalam zeolit. Serta dipersiapkan ukuran partikelnya sebagai katalis
heterogen basa. Beberapa tahapannya sebagai berikut [7] :
1. Zeolit alam dicuci dengan 30% hidrogen peroksida untuk menghilangkan
impuritisnya, larutan sambil diaduk sampai beberapa menit.
2. Setelah selesai, dihilangkan sisa larutan hidrogen peroksida (H2O2) pada
campuran zeolit alam dan dipanaskan dalamwater bathhingga kering.
4. Dipisahkan kembali sisa aquadest dan zeolit alam dikeringkan dalam oven
selama 24 jam dengan suhu 110oC.
5. Zeolit alam yang telah kering digiling dengan mortar agar menghasilkan
bubuk zeolit alam dengan ukuran 140 mesh.
3.4.2 Pembuatan Modifikasi Katalis Heterogen KOH/Zeolit Alam sebagai Katalis Basa Kuat
Katalis yang akan digunakan dalam penelitian adalah modifikasi dari
katalis zeolit alam dengan didukung oleh senyawa KOH sebagai katalis basa
kuat prosedurnya sebagai berikut [7] :
1. Dilakukan perendaman katalis zeolit dengan KOH dengan variasi konsentrasi
larutan KOH yang telah ditentukkan. Variasi pertama dibuat larutan KOH
dengan 75 gram padatan KOH yang dilarutkan dengan 100 mL aquadest.
Perbandingan massa antara zeolit dengan larutan KOH adalah 1:4.
2. Proses modifikasi katalis dilakukan dalam labu leher tiga. Dimasukkan
campuran KOH/zeolit alam ke dalam labu leher tiga dengan rangkaian
peralatan refluks kondensor, termometer danmagnetic stirrer.
3. Proses impregnasi katalis dilakukan pada suhu 60oC selama 2 jam .
4. Kemudian campuran larutan KOH/zeolit alam diletakkan dalam oven dengan
suhu 60oC selama 24 jam.
5. Setelah proses impregnasi selesai, katalis termodifikasi dipisahkan dengan
larutan KOH denganvacuum filter.
6. Katalis termodifikasi yang tertahan di kertas saring, selanjutnya akan
dikeringkan dengan oven pada suhu 110oC selama 24 jam untuk
menghilangkan kandungan air.
7. Kemudian katalis dikalsinasi padafurnacepada suhu 450oC selama 4 jam.
8. Setelah selesai dikalsinasi, katalis KOH/zeolit alam dihaluskan dengan mortar
9. Kemudian katalis KOH/zeolit siap untuk dianalisis dengan menggunakan
3.4.3 Proses Transesterifikasi RBO Menggunakan Katalis Heterogen KOH/Zeolit Alam
Adapun proses reaksi transesterifikasi yang akan dilakukan adalah sebagai
berikut [7,42] :
1. RBO, metanol dan katalis KOH/zeolit alam yang telah disiapkan ditimbang
dengan variasi rasio mol RBO/metanol yang telah ditentukan.
2. Metanol dan katalis termodifikasi dengan jumlah variasi tertentu
dimasukkan ke dalam labu kemudian dipanaskan hingga 60°C sambil
diaduk dengan kecepatan pengadukan 500 rpm.
3. Secara perlahan – lahan minyak 50 gram dimasukkan ke dalam labu dan
reaksi dilangsungkan sesuai variasi waktu yang dilakukan.
4. Setelah reaksi selesai, reaktor didinginkan pada suhu ruangan. Katalis
dipisahkan dari campuran denganvacuum filter.
5. Campuran hasil reaksi dimasukkan ke dalam corong pemisah dan dibiarkan
selama 24 jam hingga terbentuk 2 lapisan.
6. Lapisan bawah yang merupakan metanol dan gliserol dipisahkan dari lapisan
atas.
7. Produk biodiesel lapisan atas kemudian dicuci dengan air panas (60oC)
hingga air cucian bersih.
8. Produk biodiesel lapisan atas dipanaskan pada suhu 100oC untuk
menghilangkan sisa air.
9. Metil ester yang telah kering ditimbang dan dianalisis.
10. Prosedur di atas diulangi untuk variabel proses lainnya seperti yang telah
3.4.4 Sketsa Percobaan
Gambar 3.1 Rangkaian Peralatan Pembuatan Biodiesel dariRice Brand Oil (RBO) Secara Transesterifikasi Menggunakan Katalis KOH/Zeolit Alam
Keterangan gambar :
1. Statif dan klem
2.Stirrer
3. Termometer
4. Labu leher tiga
5.Heater
6. Refluks kondensor
7. Air dingin masuk
8. Air dingin keluar
3.4.5 Prosedur Analisis Modifikasi Katalis
3.4.5.1 Analisis Kadar Logam Kalium pada Katalis Heterogen Zeolit Alam yang Dimodifikasi dengan KOH menggunakan AAS
Untuk analisis jumlah kadar logam kalium pada modifikasi katalis ini
menggunakan instrumen AAS pada Laboratorium Badan Riset dan Standarisasi
(Baristand).
1
2
3 4
5
7 8
3.4.5.2 Analisis Gugus K–O pada Katalis Heterogen Zeolit Alam yang Dimodifikasi dengan KOH menggunakan FTIR
Untuk analisis gugus K–O pada modifikasi katalis ini menggunakan
instrumen FTIR pada Laboratorium Penelitian, Fakultas Farmasi, Universitas
Sumatera Utara.
3.4.6 Prosedur Analisis Minyak Dedak Padi (RBO) dan Biodiesel
3.4.6.1 Analisis Kadar Free Fatty Acid (FFA) Bahan Baku RBO dengan Metode Tes AOCS Official Method Ca 5a-40
Untuk analisis kadar FFA bahan baku RBO sesuai dengan AOCSOfficial
MethodCa 5a-40 dengan prosedur sebagai berikut
1. Bahan baku RBO sebanyak 7,05 ± 0,05 gram dimasukkan ke dalam
erlenmeyer.
2. Etanol 95% ditambahkan sebanyak 75 ml.
3. Campuran dikocok kuat dan dilakukan titrasi dengan NaOH 0,25 N dengan
indikator fenolftalein 3-5 tetes. Titik akhir tercapai jika warna larutan berwarna
merah rosa dan warna ini bertahan selama 10 detik.
Dimana: T = normalitas larutan NaOH
V = volum larutan NaOH terpakai
M = berat molekul FFA
3.4.6.2 Analisis Komposisi Bahan Baku RBO dan Biodiesel yang dihasilkan menggunakan GCMS
Komposisi bahan baku RBO serta biodiesel yang dihasilkan akan
dianalisis menggunakan instrumen GCMS pada Laboratorium Pusat Penelitian
Kelapa Sawit (PPKS).
3.4.6.3 Analisis Viskositas Biodiesel yang Dihasilkan dengan Metode Tes ASTM D 445
Viskositas adalah ukuran hambatan cairan untuk mengalir secara gravitasi,
untuk aliran gravitasi dibawah tekanan hidrostatis, tekanan cairan sebanding
(Stokes). Satuan SI untuk viskositas m2per detik (104 St). Lebih sering digunakan
centistokes (cSt) (1cSt =10-2 St = 1 mm2/s). Untuk analisis viskositas
menggunakan metode tes ASTM D-445. Untuk pengukuran viskositas ini
menggunakan peralatan utama yaitu viskosimeter Ostwald tube tipe kapiler,
viscosimeter holder dan pemanas pada 37,8oC. Termometer yang digunakan
dengan ketelitian 0,02oC dan menggunakan stop watch dengan ketelitian 0,2 detik.
3.4.6.4 Analisis Densitas Biodiesel yang Dihasilkan dengan Metode Tes OECD 109
Untuk analisis densitas menggunakan metode tes OECD 109. Untuk
pengukuran densitas ini menggunakan peralatan utama yaitu piknometer.
Perbedaan berat kosong dan penuh dihitung pada suhu 40oC.
3.4.6.5 Analisis Titik Nyala Biodiesel
Uji titik nyala untuk biodiesel yang dihasilkan akan dianalisis
menggunakan instrumen pada Laboratorium Politeknik Teknologi Kimia Industri
3.5 FLOWCHART PENELITIAN
[image:40.595.156.459.106.538.2]3.5.1 FlowchartPretreatmentKatalis Heterogen Zeolit Alam
Gambar 3.2 Diagram AlirPretreatmentKatalis Heterogen Zeolit Alam Campuran diaduk dalam beberapa menit
Dimasukkan zeolit alam ke dalambeaker glassdan ditambahkan 30% larutan hidrogen peroksida (H2O2)
Zeolit alam digiling dengan mortar dan diayak dengan ayakan 140 mesh
Mulai
Selesai
Sisa larutan H2O2dalam campuran dibuang dan zeolit
alam dipanaskan dalamwater bathhingga kering
Zeolit alam dicuci dengan aquadesthingga bersih
3.5.2 Flowchart Pembuatan Katalis Modifikasi KOH/Zeolit Alam sebagai Katalis Basa Kuat
Gambar 3.3 Flowchart Pembuatan Modifikasi Katalis Heterogen KOH/Zeolit Alam sebagai Katalis Basa Kuat
Dibuat larutan KOH sesuai dengan variasi yang ada. Pada variasi pertama 75 gram KOH dengan 100 mLaquadest
Dimasukkan campuran KOH/zeolit alam dan larutan KOH dengan perbandingan massa 1:4 ke dalam labu leher tiga
Campuran larutan KOH/zeolit alam diletakkan dalam oven pada suhu 60oC selama 24 jam
Dipisahkan dari larutan KOH denganvacuum filter
Katalis termodifikasi yang tertahan di kertas saring, selanjutnya akan dikeringkan dengan oven pada suhu 110oC selama 24 jam
menghilangkan kandungan air
Dikalsinasi katalis padafurnacepada suhu 450oC selama 4 jam. Mulai
Selesai Apakah masih ada variasi lain ?
Dilakukan impregnasi katalis pada suhu 60oC selama 2 jam
Dilakukan analisis FTIR dan AAS pada katalis KOH/zeolit alam
Tidak
3.5.3 Flowchart Proses Transesterifikasi RBO Menggunakan Modifikasi Katalis Heterogen KOH/Zeolit Alam Sebagai Katalis Basa Kuat
Metanol dan katalis KOH/zeolit alam dengan variasi berat tertentu dimasukkan ke labu dan dipanaskan
pada suhu 60oC dengan pengadukan 500 rpm
Campuran hasil reaksi dimasukkan ke dalam corong pemisah dan dibiarkan selama 24 jam hingga terbentuk 2 lapisan
Lapisan atas dicuci dengan air panas (60oC) hingga air cucian bersih
Lapisan atas yang merupakan metil ester dipanaskan pada suhu 100°C RBO,metanol dan katalis KOH/zeolit alam yang disiapkan ditimbang
dengan rasio RBO/metanol yang diinginkan
Minyak sebanyak 50 gram dimasukkan ke dalam labu secara perlahan - lahan
Metil ester yang telah kering ditimbang dan dilakukan analisis
Mulai
Lapisan bawah yang merupakan metanol dan gliserol dipisahkan dari lapisan atas
Katalis dipisahkan denganvacuum filter
A
Reaksi berlangsung dengan variasi waktu tertentu
Gambar 3.4 Flowchart Proses Transesterifikasi RBO Menggunakan Modifikasi Katalis Heterogen KOH/Zeolit Alam Sebagai Katalis Basa Kuat
Selesai Apakah masih ada
variasi lain ?
Ya
Tidak
BAB IV
HASIL DAN PEMBAHASAN
4.1 HASIL ANALISIS BAHAN BAKU
Pada penelitian ini dilakukan dengan menggunakan bahan baku berupa
minyak dedak padi (rice bran oil) yang digunakan dalam proses pembuatan
biodiesel. Berikut ini merupakan komposisi asam-asam lemak yang terkandung
dalam minyak dedak padi (rice bran oil) yang ditampilkan dalam hasil analisis
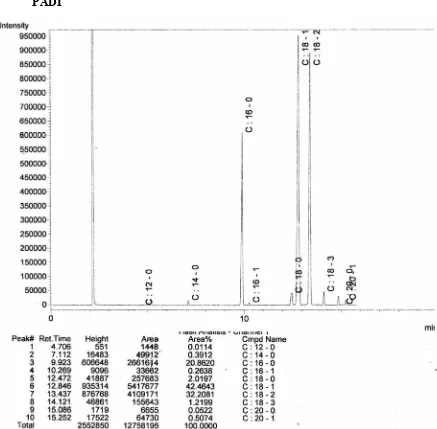
[image:44.595.116.512.317.485.2]dengan GC (Gas Chromatography) pada Tabel 4.1 berikut.
Tabel 4.1 Komposisi Asam Lemak dari Minyak Dedak Padi
No. Puncak Retention
Time(menit) Komponen Penyusun
Komposisi % berat
1 4,706 Asam Laurat (C12:0) 0,0114
2 7,112 Asam Miristat (C14:0) 0,3912
3 9,923 Asam Palmitat (C16:0) 20,8620
4 10,269 Asam Palmitoleiat (C16:1) 0,2638
5 12,472 Asam Stearat (C18:0) 2,0197
6 12,846 Asam Oleat (C18:1) 42,4643
7 13,437 Asam Linoleat (C18:2) 32,2081
8 14,121 Asam Linolenat (C18:3) 1,2199
9 15,086 Asam Arakidat (C20:0) 0,0522
10 15,252 Asam Eikosenoat (C20:1) 0,5074
Berdasarkan data hasil analisis GC (Gas Chromatography) yang berupa
komposisi asam lemak dari minyak dedak padi (rice bran oil) dapat diperoleh
berat molekul minyak dedak padi (dalam bentuk trigliserida) yaitu 865,3598
gram/mol, sedangkan berat molekul FFA dari minyak dedak padi adalah 275,7866
gram/mol. Berdasarkan kromatogram tersebut dapat dilihat bahwa komponen
asam lemak yang dominan pada sampel minyak dedak padi (rice bran oil) yaitu
pada puncak 6 yang termasuk asam lemak tidak jenuh berupa asam oleat (C18:1)
sebesar 42,4643 %, puncak 7 yang termasuk asam lemak tidak jenuh berupa asam
linoleat (C18:2) sebesar 32,2081 % dan puncak 3 yang termasuk asam lemak
jenuh berupa asam palmitat (C16:0) sebesar 20,8620 %.
Selain mengidentifikasi komponen asam lemak dalam minyak dedak padi
(rice bran oil) seperti densitas, viskositas dan kadar FFA. Data-data yang telah
diperoleh disajikan dalam Tabel 4.2.
Tabel 4.2 Sifat Fisika dari Minyak Dedak Padi
Sifat Fisika Jumlah
Densitas, kg/m3 0,90858 Viskositas, mm2/s 43,0162
FFA, % 1,2225
4.2 PEMBUATAN KATALIS HETEROGEN MODIFIKASI
KOH/ZEOLIT ALAM
Pada penelitian ini menggunakan katalis heterogen yang berupa
KOH/zeolit alam. KOH/zeolit alam merupakan hasil impregnasi zeolit alam
dalam larutan KOH dengan kondisi operasi tertentu. Perlakukan basa kuat dalam
impregnasi dengan pertukaran ion dapat mengubah karakteristik hidrofobik atau
hidrofilik menjadi beberapa ion atau senyawa organik dalam proses adsorpsi [32].
Larutan KOH memiliki sifat basa yang lebih tinggi dibandingkan dengan garam
kalium lainnya, sehingga dapat membentuk ikatan Al-O-K yang lebih stabil pada
permukaan zeolit alam dalam proses impregnasi. Pembentukan kebasaan juga
terjadi pada proses kalsinasi yaitu terbentuknya senyawa K2O. Sehingga dengan
adanya senyawa K2O yang terbentuk maka akan meningkatkan kebasaan dari
katalis yang memberikan konversi yang tinggi pada metil ester. Hal ini juga
dijelaskan oleh Evangelista, dkk (2016) tentang review katalis alumina dengan
senyawa kalium pada pembuatan biodiesel [43]. Dalam pembuatan biodiesel
dengan menggunakan katalis zeolit alam tanpa modifikasi hanya menghasilkan
yield metil ester sebesar 6,25%. Oleh karena itu, modifikasi zeolit alam dengan
proses impregnasi, dimana akan terbentuk senyawa K2O, dapat meningkatkan
kemurnian danyieldbiodiesel yang dihasilkan.
4.2.1 Analisis Kandungan Logam K(Kalium) dengan AAS (Atomic Absorption Spectrophotometry) pada Zeolit Alam dan Modifikasi KOH/Zeolit Alam
Pada proses pembuatan katalis heterogen KOH/zeolit alam ini telah
dilakukan dengan 5 variasi konsentrasi larutan KOH. Hal ini dilakukan agar
KOH/zeolit alam. Analisis AAS (Atomic Absorption Spectrophotometry)
bertujuan mengetahui kandungan logam kalium pada katalis heterogen
KOH/zeolit alam. Berikut ini merupakan hasil analisis dengan AAS (Atomic
Absorption Spectrophotometry) pada katalis heterogen KOH/zeolit alam dalam
[image:46.595.166.468.197.436.2]proses impregnasi dapat dilihat pada Gambar 4.1.
Gambar 4.1 Hasil Analisis Modifikasi Zeolit Alam dengan AAS (Atomic Absorption Spectrophotometry)
Gambar 4.1 di atas menunjukkan bahwa kandungan logam kalium yang
paling tinggi terdapat pada konsentrasi larutan KOH 75/100 ml aquadest yaitu
sebesar 36,0473%. Pada modifikasi katalis ini dilakukan dengan proses
impregnasi sehingga menghasilkan ikatan Al-O-K atau Si-O-K pada struktur
[image:46.595.191.445.604.722.2]zeolit alam yang dihasilkan, struktur zeolit dapat dilihat pada Gambar 4.2 berikut.
Gambar 4.2 Struktur Zeolit Alam Hasil Proses Impregnasi dengan terbentuknya ikatan Si-O-K
Pada konsentrasi 100/100 ml aquadest terlihat pada grafik kandungan
logam kalium semakin menurun hingga konsentrasi larutan KOH 175/100 ml
aquadest. Penurunan kandungan logam kalium ini dapat disebabkan oleh
beberapa hal, diantaranya karena semakin tingginya konsentrasi larutan KOH,
maka akan membuat larutan KOH menjadi jenuh atau lewat jenuh. Dalam hal ini
KOH tidak larut sempurna dalam aquadest. Oleh karena itu, mengurangi ion K+
yang terurai dari larutan KOH, sehingga mengurangi pula penyerapan ion K+pada
permukaan zeolit alam dalam proses impregnasi [44]. Dalam proses impregnasi
adsorpsi logam kalium dan terjadi pertukaran ion antara K+dari larutan KOH dan
Al ataupun Si pada zeolit alam yang akan membentuk ikatan Al-O-K seperti yang
telihat pada struktur zeolit alam . Dalam pertukaran ion ini, dapat terjadi reaksi
balik jika telah tercapai jumlah kation yang setara [45]. Oleh karena itu, pada
proses pertukaran ion dalam zeolit alam dengan K+ dapat terjadi reaksi balik
dengan konsentrasi KOH yang semakin tinggi dimana menyebabkan penurunan
kandungan logam kalium. Selain itu, persaingan ion – ion antara ion K+ dan ion
logam pada zeolit alam yang semakin banyak dengan bertambahnya konsentrasi
juga menyebabkan keterbatasan dalam penyerapan K+. Oleh karena itu, terjadi
penurunan kandungan logam kalium pada KOH/zeolit alam dengan semakin
tingginya konsentrasi larutan KOH.
Kandungan logam kalium tertinggi yang diperoleh sebesar 36,0473% pada
konsentrasi 75 gram/100 mLaquadest, kandungan logam ini lebih kecil dari yang
telah dilaporkan Kusuma, dkk [7]. Hal ini disebabkan oleh ukuran ayakan yang
digunakan dalam penelitian lebih kecil dibandingkan dengan ukuran ayakan yang
digunakan oleh Kusuma, sehingga ukuran partikel zeolit menjadi lebih besar dan
luas permukaan pori akan semakin kecil.
4.2.2 Analisis FTIR (Fourier Transform Infra Red) Zeolit Alam dan Modifikasi KOH/Zeolit Alam
Berdasarkan hasil analisis dengan AAS diatas, dengan hasil terbaiknya
pada konsentrasi larutan KOH sebesar 75/100 ml aquadest yang didapatkan
kandungan logam kalium (K) tertinggi sebesar 36,0473 %. Pada hasil terbaik
mengetahui keberadaan gugus K–O pada katalis heterogen zeolit alam yang telah
dimodifikasi dengan KOH serta membandingkan dengan gugus zeolit alam tanpa
modifikasi. Hal ini disajikan dalam Gambar 4.3.
Keterangan analisis gugus fungsi [46, 47, 48, 49, 50]:
[image:48.595.124.526.152.441.2]- 3433,29 cm-1: gugus hidroksil O–H - 3371,57cm-1: gugus hidroksil O–H - 1631,78 cm-1: ikatan molekul H2O - 1647,21cm-1: ikatan molekul H2O - 1384,89cm-1: internal asimetris Si-O(Si) - 1053,13 cm-1: regang simetris ikatan Si (T–O–T) - 1010,70cm-1: regang simetris ikatan Si (T–O–T) - 790,81 cm-1 : vibrasi ulur simetris oksida logam (MO) - 887,26cm-1 : vibrasi ulur simetris oksida logam (MO) - 462,92 cm-1 : vibrasi tekuk T–O (T = Si atau Al) - 459,06cm-1 : vibrasi tekuk T–O (T = Si atau Al)
Gambar 4.3 Hasil Analisis Modifikasi Zeolit Alam dengan FTIR (Fourier Transform Infra Red)
Pada Gambar 4.3 menunjukkan hasil karakterisasi FTIR dari zeolit alam
dan modifikasinya yaitu KOH/zeolit alam. Hasil FTIR menunjukkan bahwa pada
zeolit alam terlihat puncak 3433,29 cm-1yang merupakan serapan dari gugus O–H
sedangkan pada modifikasi KOH/zeolit alam gugus hidroksi O-H terlihat pada
yang merupakan ikatan molekul H2O yang teradsorbsi terlihat memiliki
penurunan persentasi transmitan pada KOH/zeolit alam dengan puncak 1647,21
cm-1. Hal ini disebabkan pada proses impregnasi dan proses kalsinasi dimana
molekulH2O terlepas dari struktur zeolit alam dan digantikan dengan ion K. Oleh sebab itu, terjadi penurunan pada ikatan molekul H2O yang teradsorbsi pada zeolit
alam.
Pada zeolit alam terlihat puncak 1053,13 cm-1 yang menunjukkan adanya
regang simetris ikatan Si dalam bentuk T–O–T. Sedangkan pada KOH/zeolit
regang simetris ikatan Si terlihat pada puncak 1010,70 cm-1. Serapan vibrasi tekuk
T–O berada pada kisaran 420-500 cm-1. Puncak 462,92 cm-1dan 459,06 cm-1pada
pada zeolit alam dan KOH/zeolit alam menunjukkan adanya vibrasi tekuk dari
ikatan T–O (Si–O atau Al–O). Puncak ini merupakan interpretasi dari jalinan
internal pada kerangka zeolit alam. Pada dasarnya struktur zeolit alam dan
struktur zeolit alam yang telah dimodifikasi tidak jauh berbeda. Pada beberapa
puncak gugus serapan KOH/zeolit alam mengalami sedikit perubahan yaitu
penurunan intensitas gelombang. Hal ini disebabkan karena dalam proses
impregnasi terjadi dekationisasi sebagai desilikasi dan hilangnya sifat
mengkristal, seperti yang dinyatakan oleh Ates dan Gokcen (2016) [46].
Pada puncak 790,81 cm-1 pada zeolit alam merupakan vibrasi ulur simetri
oksida logam. Sedangkan pada KOH/zeolit alam terlihat pada puncak yang
berbeda yaitu 887,26 cm-1. Logam tersebut dapat diidentifikasikan sebagai
kalium, karena terjadinya impregnasi zeolit alam dengan larutan KOH yang
mengandung logam kalium. Dengan demikian, pada zeolit alam dan KOH/zeolit
alam terdapat oksida kalium (KO). Munandar, dkk (2014) menyatakan bahwa
interval spektra 770-803 cm-1 merupakan interpretasi gugus fungsi K-O [51].
Selain itu, Almjadleh, dkk (2014) melaporkan bahwa pada puncak 750,31 cm-1
terdapat vibrasi ulur simetris oksida logam (MO) serta Ates dan Gokcen (2016)
melaporkan bahwa pada kisaran puncak 600-800 cm-1 merupakan ikatan dari
pertukaran kation [46, 47]. Oleh karena itu, dapat diindifikasikan bahwa pada
puncak serapan ini terdapat gugus dari kation K+yang berikatan dengan kerangka
utama zeolit alam, baik itu Si–O–K atau Al–O–K. Keberadaan puncak ini pada
katalis dalam reaksi. Selain itu, dapat dilihat bahwa pada KOH/zeolit alam
memiliki puncak yang lebih kuat pada gugus serapan 887,26 cm-1 yang
mengindifikasikan gugus kalium dibandingkan pada zeolit alam yang memiliki
puncak yang lebih lemah. Hal ini membuktikan bahwa kandungan kalium pada
KOH/zeolit alam lebih besar dari zeolit alam tanpa modifikasi.
4.3 PENGARUH VARIABEL PERCOBAAN TERHADAP YIELD
BIODIESEL PADA PROSES TRANSESTERIFIKASI
4.3.1 Pengaruh Jumlah Katalis KOH/Zeolit Alam terhadapYieldBiodiesel
Dari hasil pembuatan katalis heterogen modifikasi KOH/zeolit alam
(konsentrasi 75 gram/100 ml aquadest) yang memiliki logam kalium yang
tertinggi dilanjutkan pada pembuatan biodiesel dari minyak dedak padi (rice bran
oil). Adapun hasil pembuatan biodiesel yang telah dilakukan dengan variasi
[image:50.595.163.468.381.580.2]jumlah katalis dapat dilihat pada Gambar 4.4.
Gambar 4.4 Hubungan antara Jumlah Katalis KOH/Zeolit Alam denganYield Biodiesel pada Kondisi Suhu Reaksi 60 ºC, Waktu 2 Jam,
dan Perbandingan Mol Alkohol/Minyak 10:1
Gambar 4.4 menunjukkan hubungan jumlah katalis KOH/zeolit alam
terhadap yield biodiesel, dimana semakin besar jumlah katalis KOH/zeolit alam
maka yield yang dihasilkan akan semakin kecil. Yield biodiesel mengalami
Pada reaksi transesterifikasi minyak dan metanol dengan katalis
KOH/zeolit alam sebesar 2% memiliki laju yang tinggi. Hal ini dibuktikan dengan
lapisan metil ester telah banyak terbentuk pada jumlah katalis 2% dan besarnya
massa metil ester yang dihasilkan. Akan tetapi, pada reaksi transesterifikasi
dengan penambahan jumlah katalis KOH/zeolit alam setelah 2% tidak
meningkatkan yield biodiesel. Penambahan jumlah katalis ini tidak dapat
meningkatkan yieldbiodiesel disebabkan adanya keterbatasan perpindahan massa
dan tingginya viskositas pada campuran reaksi. Oleh karena itu, akan
menimbulkan masalah pada lemahnya proses pencampuran komponen reaktan
sehingga terjadinya penurunan yield FAME. Proses perpindahan massa ini terjadi
pada proses pembentukan metoksida. Pada reaksi dengan katalis heterogen,
metoksida dibentuk pada permukaan katalis, dimana pada proses ini bergantung
pada perpindahan massa dari metanol terhadap katalis. [52, 53]. Keterbatasan
perpindahan massa yang terjadi inilah akan mempersulit pencampuran dari
reaktan dan menurunkan yield biodiesel. Hal ini ditunjukkan pada penambahan
katalis KOH/zeolit alam setelah 2% (2,5; 3; 3,5) mengalami penurunan yield
biodiesel. Tetapi pada penambahan jumlah katalis 4% yield biodiesel mengalami
kenaikan kembali, hal ini dapat disebabkan ketidakhomogenan kandungan logam
kalium pada katalis KOH/zeolit alam. Ketidakhomogenan logam kalium pada
zeolit alam akan berdampak pula pada ketidakhomogenan logam kalium pada
KOH/zeolit alam. Selain itu, sifat higroskopis KOH terhadap udara menjadikan
katalis KOH/zeolit alam menggumpal dan basah dalam waktu singkat. Oleh
karena itu, dapat menyebabkan dengan penambahan jumlah katalis 4%
memberikanyieldbiodiesel yang lebih tinggi.
Kondisi terbaik yang dihasilkan adalah pada suhu reaksi 60 ºC, waktu
reaksi 2 jam, perbandingan mol alkohol/minyak 10:1, dan jumlah katalis
KOH/zeolit alam 2 %. Pada kondisi tersebut memberikan yield biodiesel sebesar
98,71 %. Roschat, dkk (2016) juga melaporkan bahwa dengan menggunakan
katalis natrium silikat pada CPO dengan jumlah katalis 2,5% menghasilkan yield
biodiesel yang terbaik dan mengalami penurunan dengan penambahan katalis
4.3.2 Pengaruh Waktu Reaksi terhadapYieldBiodiesel
Dari hasil pembahasan sebelumnya yang menghasilkan kondisi terbaik,
dimana jumlah katalis KOH/zeolit alam sebesar 2% dijadikan sebagai variabel
tetap pada variasi waktu reaksi dalam pembuatan biodiesel. Adapun hasil
pembuatan biodiesel yang telah dilakukan dengan variasi waktu reaksi dapat
[image:52.595.165.469.216.412.2]dilihat pada Gambar 4.5 berikut.
Gambar 4.5 Hubungan antara Waktu Reaksi denganYieldBiodiesel pada Kondisi Suhu Reaksi 60 ºC, Jumlah Katalis 2 %,
dan Perbandingan Mol Alkohol/Minyak 10:1
Gambar 4.5 menunjukkan hubungan waktu reaksi terhadapyieldbiodiesel,
dimana semakin lama waktu reaksi maka yield yang dihasilkan akan semakin
besar, dan yield terbaik diperoleh pada waktu reaksi 2 jam. Tetapi setelah waktu
reaksi 2 jamyieldbiodiesel mengalami penurunan.
Pada reaksi awal transesterifikasi minyak dedak padi dan metanol dengan
katalis KOH/zeolit alam akan berjalan secara perlahan untuk mendispersikan
minyak dan alkohol [54]. Selanjutnya reaksi transesterifikasi akan berjalan cepat
hingga menghasilkanyieldbiodiesel yang terbaik [55]. Hal ini dapat dilihat terjadi
peningkatan yield biodiesel dari 95,82% hingga 98,71% yang dihasilkan dari
waktu reaksi 1,5 jam hingga 2 jam. Pada reaksi transesterifikasi dengan waktu
reaksi 2 jam inilah menghasilkan yield biodiesel yang terbaik. Setelah waktu
reaksi 2 jam yield biodiesel mengalami penurunan. Hal ini disebabkan reaksi
mengakibatkan reaksi balik [53]. Reaksi balik pada transesterifikasi akan
menghasilkan asam lemak dan akan mengurangi yield FAME yang dihasilkan
[56]. Hal ini dapat ditunjukkan bahwa pada waktu reaksi setelah 2 jam (2,5 ; 3 ;
3,5 jam) mengalami penurunanyieldbiodiesel dari 98,71% hingga 88,30%.
Kondisi terbaik yang dihasilkan adalah pada suhu reaksi 60 ºC, jumlah
katalis KOH/zeolit alam 2 %, perbandingan mol alkohol/minyak 10:1 dan waktu
reaksi 2 jam. Pada kondisi tersebut memberikan yield biodiesel sebesar 98,71 %.
Tan, dkk (2015) juga melaporkan bahwa pada minyak goreng bekas dengan
katalis cangkang telur menghasilkan yield tertinggi pada waktu reaksi 2 jam dan
mengalami penurunan setelah waktu reaksi lebih dari 2 jam [55].
4.3.3 Pengaruh Perbandingan Mol Alkohol/Minyak terhadap Yield
Biodiesel
Dari hasil pembahasan sebelumnya yang menghasilkan kondisi terbaik,
dimana waktu reaksi sebesar 2 jam dijadikan sebagai variabel tetap pada variasi
perbandingan mol alkohol/minyak dalam pembuatan biodiesel. Adapun hasil
pembuatan biodiesel yang telah dilakukan dengan variasi perbandingan mol
[image:53.595.141.467.463.661.2]alkohol/minyak dapat dilihat pada Gambar 4.6 berikut.
Gambar 4.6 Hubungan antara Perbandingan Mol,Alkohol/Minyak denganYield Biodiesel pada Kondisi Suhu Reaksi 60 ºC, Waktu Reaksi 2 jam, serta
Gambar 4.6 menunjukkan hubungan waktu reaksi terhadap yieldbiodiesel
pada variasi katalis 2 %, 3%, dan 4%, dimana semakin besar perbandingan mol
alkohol/minyak maka yield yang dihasilkan akan semakin meningkat dan yield
terbaik diperoleh pada perbandingan mol alkohol/minyak 12:1. Akan tetapi,
setelah perbandingan mol alkohol/minyak 12:1 terjadi penurunanyieldbiodiesel.
Pada reaksi transesterifikasi penggunaan rasio mol alkohol/minyak sangat
mempengaruhi yield biodiesel. Pada dasarnya penggunaan rasio molar
metanol/minyak yang berlebih akan mengeser reaksi ke arah equilibrium reaksi
dan membantu mencapai yield biodiesel yang terbaik [55]. Hal ini ditunjukkan
terjadinya peningkatanyieldbiodiesel pada perbandingan mol alkohol/minyak 8:1
hingga perbandingan mol alkohol/minyak 10:1 dari masing-masing variasi katalis
2, 3, dan 4%. Dan pada perbandingan mol alkohol/minyak 10:1, reaksi
transesterifikasi telah bergeser pada kesetimbangan reaksi dan mencapai yield
terbaik pada masing-masing variasi katalis. Penggunaan rasio molar
metanol/minyak yang terlalu tinggi akan melarutkan gliserol sebagai reaksi
samping dengan kelebihan metanol, sehingga dapat menghalangi reaksi metanol,
minyak dan katalis. Selain itu, gugus polar hidroksil metanol akan menjadi
emulsifier yang akan mengakibatkan semakin sulit proses pemisahan biodiesel
dari campuran hasil reaksi sehingga akan menggurangi % yield FAME [52]. Hal
ini ditunjukkan terjadinya penurunan yield biodiesel dari perbandingan mol
alkohol/minyak 10:1 hingga perbandingan mol alkohol/minyak 12:1 pada
masing-masing variasi katalis 2, 3, dan 4%.
Kondisi terbaik yang dihasilkan adalah pada waktu reaksi 2 jam, suhu
reaksi 60 ºC, perbandingan mol alkohol/minyak 10:1, dan jumlah katalis
KOH/zeolit alam 2%. Pada kondisi tersebut memberikan yield biodiesel sebesar
98,71 %. Tan, dkk (2015) juga melaporkan bahwa pada minyak goreng bekas
dengan katalis cangkang telur semakin besar rasio mol metanol/minyak akan
semakin tinggiyieldbiodiesel hingga rasio mol 10:1. Setelah rasio mol lebih besar
4.4 KARAKTERISTIK BIODIESEL
Karakteritik biodiesel merupakan sifat fisik dan atau sifat kimia yang
dimiliki oleh biodiesel. Standar karakteritik biodiesel dapat dilihat berdasarkan
standar ASTM D6751 dan SNI yang dapat dilihat pada Tabel 4.3. Karakteristik
biodiesel meliputi densitas, viskositas kinematik, kandungan ester, dan titik nyala.
Kontaminasi dari biodiesel dapat mempengaruhi densitasnya, oleh karena itu
densitas dapat dijadikan indikator dari kontaminan. Biodiesel memiliki sifat lebih
polar dari bahan bakar diesel sehingga viskositas biodiesel lebih tinggi dari bahan
bakar diesel. Titik nyala berbanding terbalik dengan volatilitas bahan bakar. Titik
nyala biodiesel semakin rendah dengan adanya sisa alkohol yang tidak bereaksi
[57]. Titik nyala biodiesel berbanding terbalik dengan densitasnya, semakin
[image:55.595.111.515.368.466.2]rendah densitas biodiesel maka titik nyala biodiesel akan semakin rendah [58].
Tabel 4.3 Karakteristik Biodiesel [18]
Parameter Unit Nilai Standar ASTM
D6751
Standar SNI
Ester Content Densitas pada 40 ̊C Viskositas kinematik pada 40 ̊C
Flash Point % (m/m) kg/m3 mm/s2 ̊C 98,7673 867,4969 4,5486 152 -3,5-5 > 130 > 96,5 850-900 2,3 - 6
>100
Dari hasil uji beberapa karakteristik biodiesel yang dihasilkan, dapat
dilihat bahwa biodiesel telah memenuhi standar SNI dan ASTM. Hal ini
menunjukkan penggunaan katalis modifikasi zeolit alam dengan KOH dalam
proses transesterifikasi dapat menghasilkan karakteristik biodiesel yang sesuai
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang dapat diambil dari penelitian ini adalah :
1. Zeolit alam yang dimodifikasi dengan KOH sebagai katalis heterogen pada pembuatan biodiesel menggunakan minyak dedak padi (rice bran oil) dapat memberikan yieldbiodiesel yang tinggi dibandingkan dengan zeolit alam tanpa modifikasi.
2. Yield terbaik diperoleh sebesar 98,71% pada jumlah katalis 2%, waktu reaksi 2 jam, perbandingan alkohol/minyak 10:1, suhu 60 ºC, dan kecepatan pengadukan 500 rpm.
3. Dari hasil pengujian sifat fisik biodiesel yang meliputi : kemurnian, densitas, viskositas kinematik dan titik nyala telah sesuai dengan Standar Nasional Indonesia (SNI) dan ASTM.
5.2 SARAN
Adapun saran yang dapat diberikan dari penelitian ini adalah:
1. Penelitian berikutnya disarankan untuk mengkaji lebih lanjut penyebab penurunan kandungan logam kalium pada katalis KOH/zeolit alam sebelum tercapainya larutan jenuh KOH.
2. Penelitian berikutnya disarankan untuk mengkaji pengunaan reuse katalis modifikasi KOH/zeolit alam yang digunakan terhadap yield metil ester yang dihasilkan.
BAB II
TINJAUAN PUSTAKA
2.1 BIODIESEL
Biodiesel adalah bahan bakar diesel alternatif yang berasal dari minyak
nabati ataupun lemak hewan. Komponen utama dalam minyak nabati dan lemak
hewan adalah trigliserida atau yang dikenal sebagai ester dari asam lemak yang
bereaksi membentuk gliserol. Biasanya, trigliserida dari minyak nabati dan lemak
hewan mengandung beberapa asam lemak yang berbeda [17]. Ketersediaan dari
bahan baku biodiesel saat ini dapat diperoleh dari minyak bahan pangan (kedelai,
cottonsed, kelapa, kacang, canola/rapeseed, biji bunga matahari), minyak bahan
non pangan, lemak hewan, alga, dan minyak limbah dari bahan pangan [1,11,18].
Produksi biodiesel dari minyak bahan pangan akan menaikkan harga dari
beberapa komoditas di pasar serta akan menciptakan beberapa masalah. Harga
dari minyak bahan pangan yang tinggi akan menyebabkan harga keseluruhan
produksi dari biodiesel juga akan tinggi. Produksi biodiesel dari minyak bahan
non pangan akan memberikan ketersediaan yang baik serta memberikan harga
yang lebih murah contohnya jatropha, pongamia, karanji, linseed, rice bran,
rubber seed dan castor. Asam lemak yang terkandung dalam suatu minyak akan
mendeskripsikan nomor karbon serta akan mempengaruhi dalam proses
transesterifikasi yang juga akan mempengaruhi kandungan dari hasil biodiesel
yang dihasilkan [11,18].
Proses produksi biodiesel dapat dilakukan menggunakan katalis homogen
asam, proses superkritikal, proses enzim, katalis heterogen asam dan
sonochemical [1]. Sedangkan metode yang digunakan dalam produksi biodiesel
diantaranya : langsung menggunakan minyak nabati, mikroemulsi, pirolisis, dan
transesterifikasi. Dalam pembuatan biodiesel dengan pirolisis dan mikroemulsi
akan menghasilkan biodiesel yang memiliki angka setana yang rendah.
Transesterifikasi merupakan metode yang sering digunakan dalam pembuatan
biodiesel. Dalam proses transesterifikasi direaksikan trigliserida yang berupa
katalis, yang akan menghasilkan metil ester atau biodiesel [19]. Beberapa standar
[image:58.595.112.514.156.513.2]pembentukkan biodiesel dapat dilihat pada tabel berikut :
Tabel 2.1Standart American Society for Testing and Materials(ASTM) yang Diizinkan untuk Biodiesel dan Diesel [18]
Property Diesel Biodiesel
Standard ASTM D975 ASTM D6751
Composition HCa(C10-C21) FAMEb(C12-C22)
Kin.viscosity(mm2/s) at 40oC
1.9-4.1 1.9-6.0
Boiling Point(oC) 188-343 182-338
Flash Point(oC) 60-80 100-170
Cloud Point(oC) -50 to 5 -3 to 12
Pour Point(oC) -35 to -15 -15 to 16
Water(vol%) 0.05 0.05
Carbon(wt%) 87 77
Hydrogen(wt%) 13 12
Oxygen(wt%) 0 11
Sulfur(wt%) 0.05 0.05
Cetane number (ignition quality)
40-55 48-60
Stoichiometric air/fuel ratio(AFR)
15 13.8
HFRRc (Dm) 685 314
BOCLEd scuff (g) 3600 >7000
Life-cycle energy balance
(energy units produced per unit energy
consumed)
0.83/1 3.2/1
Metil ester content - min 96,5% (EN 14103)
2.2 BAHAN BAKU
2.2.1 Minyak Dedak Padi (Rice Bran Oil)
Minyak dedak padi (rice bran oil) berasal dari dedak padi yang dihasilkan
dari penggilingan padi. Potensi minyak dedak padi (rice bran oil) bergantung
pada potensi tanaman padi. Indonesia merupakan negara agraris dan termasuk
negara penghasil padi terbesar di dunia. Indonesia yang juga terletak pada garis
khatulistiwa yang memiliki dua musim, yaitu musim hujan dan musim kemarau,
sehingga berbagai jenis tanaman mudah dibudidayakan di Indonesia, termasuk
tanaman padi. Oleh karena itu, tanaman padi sangat berpotensi besar di Indonesia
[12]. Selain itu, produksi padi di Indonesia semakin meningkat dari tahun ke
Tabel 2.2 Data Statistik Tanaman Padi di Indonesia [12]
Keterangan Tahun Pertumbuhan
(%)
2011 2012 2013 2014 2015
Produksi
(juta ton) 65,757 69,056 71,280 70,846 74,992 5,85 Luas Panen
(juta Ha) 13,204 13,446 13,835 13,797 14,178 2,76 Produktivitas
(Ku/Ha) 49,80 51,36 51,52 51,35 52,89 3,00
Dedak padi (Oryza Sativa Linn) adalah hasil samping yang didapat dari
kulit lapisan luar yang berwarna cokelat pada kernel padi dari penggilingan padi.
Kandungan pada padi (dalam basis kering) yaitu endosperm 70-72, hull 20, bran
7,0-8,5, dan embrio 2-3%. Dedak padi mengandung minyak (15-23%).
Gambar 2.1 Kompisisi Padi [20]
Crude RBO (Rice Bran Oil) mempunyai kesulitan dalam pemurniannya,
hal ini dikarenakan kandungan FFA yang tinggi, dan warna gelap. RBO memiliki
kandungan trigliserol yang lebih rendah dibandingkan dengan minyak nabati
lainnya dan memiliki kandungan gliserida, glikolipid, wax ester yang tinggi.
Dedak padi mengandung beberapa tipe lipase. Selain lipase, dedak padi juga
mengandung amilase, katalase, ascorbic acid oxidase, cytochrome oxidase, dan
lain lain [20].
Kandungan asam lemak bebas pada minyak dedak padi (rice bran oil)
tergantung pada kualitas dedak padi dalam proses ekstraksinya. Kandungan asam
lemak bebas pada refined oil bervariasi antara 2 – 5% sedangkan crude oils
memiliki kandungan asam lemak bebas (FFA) 15 – 40%. Jika disimpan dalam
waktu sebulan maka FFA minyak dedak padi (rice bran oil) akan meningkat
[image:59.595.234.387.306.470.2]padi harus dinonaktifkan [7]. Berikut ini merupakan komposisi asam lemak
[image:60.595.173.453.157.290.2]minyak dedak padi (rice bran oil) :
Tabel 2.3 Komposisi Minyak Dedak Padi [15]
Jenis Asam Lemak Konsentrasi (%b) Asam Miristat (C14:0) 0,112 Asam Palmitat (C16:0) 14,991 Asam Palmitoleat (C16:0) 0,146 Asam Stearat (C18:0) 1,275 Asam Oleat (C18:1) 41,513 Asam Linoleat (C18:2) 38,652 Asam Linolenat (C18:3) 1,416 Asam Arasidat (C20:0) 0,765 Asam Arasidonik (C20:4) 0,243
Tabel 2.4 Karakteristik Minyak Dedak Padi [21]
Jenis Asam Lemak Konsentrasi (%b) Viskositas (38oC) 42,2 cSt Densitas (21oC) 0,923 g/mL
Cloud point 11oC
Pour point -1oC
Flash point 258oC
Gross heat value 42,3 MJ/kg
Rice bran oil bukan merupakan minyak yang biasa digunakan dalam
pembuatan biodiesel dibandingkan dengan sumber tanaman atau biji lainnya
seperti jagung, cotton, biji bunga matahari atau soybean. Minyak dedak padi
sangat berpotensi dalam pembuatan biodiesel karena dapat dilihat dari potensi
dedaknya yang banyak sehingga menjadikan biaya bahan baku yang murah
dibandingkan bahan baku minyak yang lain [20].
2.2.2 Metanol
Metanol yang juga sering disebut metil alkohol adalah senyawa kimia
yang tersusun dari tiga unsur kimia yaitu karbon, hidrogen dan oksigen. Rumus
kimia dari metanol yaitu CH3OH. Pada reaksi transesterifikasi menggunakan
alkohol sebagai reaktannya, yang juga disebut sebagai reaksi alkoholisis.
Beberapa alkohol yang digunakan dalam reaksi transesterifikasi yaitu metanol,
butanol, etanol, dan propanol. Tetapi metanol merupakan jenis alkohol yang
menghasilkan konversi biodiesel yang tinggi dibandingkan dengan jenis alkohol
lain [19]. Penggunaan metanol dalam pembuatan biodiesel dapat meningkatkan
[image:61.595.108.518.175.363.2]laju reaksi dibandingkan dengan penggunaan alkohol lainnya [22].
Tabel 2.5 Sifat-Sifat Fisika dan Kimia Metanol [23]
No. Sifat Fisika Sifat Kimia
1 Wujud berupa cairan tidak berwarna
Berat molekul: 32 g/mol
2 Merupakan produk yang stabil Titik didih: 64,5oC (148,1oF) 3 Larut dalam air, metanol, dan
dietil eter
Titik leleh: -97,8oC (144oF)
4 Bereaksi tinggi dengan agen pengoksida
Specific gravity: 0,796 pada 20oC
5 Tidak korosif pada kaca pH: 7 (netral)
6 Beracun Tekanan uap: 97,68 mmHg pada 20oC 7 Berbahaya apabila terkena kulit
tangan, mata
Densitas uap: 1,11
8 Mudah terbakar Nilai ambang bau: 160 ppm
2.2.3 Zeolit
Dalam pembuatan biodiesel masih terdapat masalah pada segi ekonomi
dan kecepatan reaksi. Pada beberapa literatur menyebutkan bahwa katalis
heterogen merupakan solusinya. Jika