PENGUKAIAN PENTAKLOROFENOL
DALAM
AIR
DENGAN
IRADIASI
GAMMA
AGUSTIN SUMARTONO
PROGRAM PASCASARJANA
INSTITUT PERTANIAN BOGOR
AGUSTIN SUMAK~I'ONO. Penguraian Pentaklorofenol dalam Air dengan lradiasi Gamma. Dibimbiny olch ZAINAL ALIM dan M.ANWAR NUR
Surat pernyataan
Bersania ini saya menyatakan bahwa tesis yang berjudul "l'enguraian pentaklorofenol dalam air dengan iradiasi gamma" adalah benar merupakan hasil karya saya sendiri dan belurn pernah dipublikasikan. Semua surnber dan inforrnasi telah diupayakan dan jelas dapat diperiksa kebenarannya.
Jakarta 17 Oktober- 2002
I'ENGtJKAIAN YENTAKLOROFENOL DALAM AIR
DENGAN IRADIASI G A M M A
AGllSTlN SLJRIAKTONO
Tesi s
sebagai salah satu syarat untuk mernperoleh gelar Magister Sains pada
Progl-an1 Studi Kirnia
I'KOGRAR4 PASCASAK,IANA
INS'I'I'T~IT PEKrI'ANI.AN ROGOR
Judul Tesis : Penguraian Pentaklorofenol dalam Air dengan Iradiasi Gamma Nama : Agustin Sumartono
NIM : P34500005
Program Studi : Kimia
Menyetujui
1 . Komisi Pembimbing
Dr. Zainal Alim Mas'ud. DEA
Ketua Anggota
Mengetahui,
2. Ketua Program Studi Kimia
Penulis dilahirkan di Brebes pada tanggal 18 Agustus 195 1 sebagai anak ke empat dari enam bersaudara pasangan R. Soemartono dan Kamaroekmi. Pendidikan sarjana di tempuh di Jurusan Kimia, Fakultas MIPA, Universitas Nusa Bangsa, Bogor. lulus tahun 1999.
Penulis bekerja di Puslitbang Teknologi Isotop dan Radiasi, Batan Jakarta, sejak tahun 1971. Pekerjaan yang dilakukan selama ini antara lain isolasi dan struhur elusidasi dari ekstrak tanaman Sembung (Hl~mtea Hal.samifira), penelitian penguraian zat organik talian-urai seperti zat warna tekstil, senyawa-senyawa fenol, surfaktan, dan endosulfan dengan iradiasi gamma. Penulis mendapatkan kesempatan mengikuti pel at i lian I?adioi.so/ope.s ('ow-se for notl-Gt.nd~ra/es dan ,S/rrdy o f /~adioi.so/o~)r.s t 11 ILI
lJ~.s/icide Atmlysis tahun 1976 di Australia, dan pelatihan di Jepang mengenai S/rrdic..s otl 111c ('otl.s/i/~ret~/.s o f 111dotwsicr11 Med~ci~ml /'lat~/.s pada tahun 1985. Pada tahun
1993 penulis mendapatkan kesempatan pelatihan mengenai /?adiafiorl rlrea/nletl~ of
I'KA K A T A
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Adapun judul penelitian yang dilaksanakan sejak bulan Juni 2001 irii ialah Penguraian Pentaklorofenol dalam Air- dengan Iradiasi Gamma. Penelitian dilakukan di Laboratorium Lingkungan Bidang Sumber Daya Alam dan Lingkungan Puslitbang Teknologi lsotop dan Radiasi, Hatan Jakarta.
Terima kasih penulis ucapkan kepada Bapak Dr. Zainal Alim Mas'ud. DEA dan Bapak Prof. Dr.lr. M . Anwar Nur, MSG selaku pembimbing. Penghal-gaan penul is sampaikan kepada Bapak Dr. Wuryanto, APU selaku Kepala P3TIR Batan vang telah rnemberikan kesempatan kepada penulis untuk menyelesaikan tugas penelitian
Penghargaan serupa penulis sampaikan kepada Bapak Drs. Zainal Abidin, Dipl.Geo yang telah men~berikan kesempatan melakukan penelitian. Juga kepada rekarl se.ja\i-at Dra.Winarti Andayani MSi, Nur Hidayati S.Si, Christina Tri Suharni, H.hl.Puri. Arrnanu, Bonang, Edy Muljana, Saiman, Udin, Maryoto yang telah menibantu dalani menyelesaikan penelitian. Juga kepada rekan-rekan seangkatan Irma, Rudi, dan Arvo yanz rnemberikan dukungan moril Ungkapan terima kasih juga disampaikan kepada suami dan anak-anak, serta Ratih dan seluruh keluarga besar DAT 48 atas serrala bantuan moril dan materiil serta doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
Jakarta, Oktober 2002
D A F T A K IS1
f{alaman
I)!If'TAR G A M B A R
I'f I Y IjAHULUAN I'INJAUAN PUSTAKA
I'entaklorofenol SitBt fisiha dan kimia Kegunaan PCI' I'enyuraian PCP 'l'eori Kirnia Radiasi Sumber Kadiasi
lnteraksi Sinar Gamma dengan Materi Satuan Dosis Radiasi
Kilai G Kadiolisis Air
Keaksi I'roduk Primer dengan Zat Organik dalarn Larutan Air OLsidasi Senya\va Organik dalam Larutan Air
BAHAN DAN METODE Bahan
Peralat a11
Metode Penelitian
tlASlL DAN PEMBAHASAN
I'enentuan Dosis optimum pada Penyuraian l'('1' Pengaruh pH pada Penguraian PCP
l'etigaruli Laju Dosis pada Penguraian I'CP Pengaruh Konsentrasi pada penguraian PCI' Penlbahan pH setelah Radiasi
I'ensukuran Asam-asam Organik yang terbentuk Penguhuran Daya hantar Listrik (Dtil,)
DAFTAR TAREI,
1 . Perubahan serapan PCP setelah diiradiasi dengan dosis 0- 10 h( i\
1 . Struhtul rnolekul pentaklorofenol (PCP)
3. I<lkL h;irilburan Cornpton
4 . I'roduhsi pasangan ion
5. Spehtruni I'CI' setelah diiradiasi dengan dosis 0-10 kGy, pl4 awal 7 dan laju dosis I kGy/jarn
6 . ~ p e h t r u m PCP setelah diiradiasi dengan dosis 0-5 kGy. pH awal 7 dan laji~ dosis 1 kGy1-jam
7. ~ ; , c h ~ r u m PCP setelah diiradiasi dengan dosis 0-2 kGy. pll awal 7 dan laju dosis 1 kGy1-jaiii
8 . ~ p e k t r u n l PCP setelah diiradiasi dengan dosis 0-2 kGy. pH awal 5 dan 1 a . i ~ dosis 1 kGyIjarn
9 ~ p e k t r u m PCP setelah diiradiasi dengan dosis 0-2 kGy, pH awal 6 dan laju dosis 1 kGv1jam
I 0 ~ ~ c k t r u m
PCP
setelah diiradiasi dengan dosis 0-2 kGy, pH awal 8 dan laju dosis I kGy/jam1 1 . f'ensaruh laju dosis pada penguraian PC/' dengan konsentrasi 10 pprn dan pl~l awal 7
12. Pengaruh konsentrasi terhzdap penurunan intensitas serapan pada 220 nm, 250 11111 dan 320 nm
13 .Perubahan pH PCP setelah diiradiasi 14 a Spektruiil standar asam oksalat
b Spektrum PCP yang diiradiasi dengari dosis 2 L(;v 15 I'engukuran asam oksalat yang terbentuk setelah diiradiasi
16. I'en~ukuran daya hantar lsitrik PCP setelah diiradiasi 1 7. l'en~ukuran klor yang terbentuk setelah diiradiasi
18. Pengukuran PCP setelah diiradiasi
19. Spektn~m PCP setelah diiradiasi dengan dosis 2 kGy. pl-l awal 7 dan laju
D A F T A R L A M P I R A N
Halaman
1 . Absorban PCP 10 ppm setelah diiradiasi pada pH 5, laju dosis 1 kGy1jam 4 1 2. Absorban PCP 10 ppm setelah diiradiasi pada pH 6, laju dosis 1 kGy1jam 4 1 3. Absorban PCP 10 ppni setelah diiradiasi pada pH 7 laju dosis I kGyIjam 42 4. Absorban PCP I0 ppni setelah diiradiasi pada pH 8, laju dosis 1 kGy1jam 4 2 5. Data persentase periguraian pada variasi laju dosis 4 3 6. Absorban PCP dengan konsentrasi 2 ppm, pH 7 laju dosis 0,5 kGy1jam 43 7. Absorbari I T I ' dengan konsentrasi 4 ppm, pH 7 laju dosis 0,5 kGy1-jam 44 8. Absorban PCI' dengan konsentrasi 8 ppm, pH 7 laju dosis 0,SkGyIjam 44 9. Absorban PCP densan konsentrasi 10 ppm, pH 7 laju dosis 0,SkGyIjam 45 10. I'engukuran perubahan pH larutan PCP dengan pH awal 7, 10 ppm laju dosis 45
1 kGy/-jam
1 I . Kurva kalibrasi standar asarn oksalat 46
12. Kromatoy-am standar asani oksalat
13. Jumlah asam oksalat yang terbentuk setelah radiasi
14. Kroniatograni asam oksalat yang terbentuk dari sampel yang diiradiasi 4 8 15 Nilai daya hantar listrik PCP setelah diiradiasi 49
I6 Kur-va kalibrasi staridar klor 4 9
17. Penentuan ion klor vans terbentuk 5 0
18 Kurva kalibrasi standar IY'P 50
19. Penentuan PCP setelah diiradiasi 5 1
PENDAHULUAN
I'eningkatan pengggunaan pupuk, pestisida, hngisida, Dan sebagainya dalam pertanian modern memberi dampak terhadap pencemaran sumber air permukaan maupun sumber daya air (Getoff and Solar 1986 dan Getoff 1993). Di Indonesia beberapa jenis pestisida diproduksi dan dibuat fonnulasinya, ha1 ini akan memberikan dampak negatif karena limbah yang dihasilkan dari bahan aktif pestisida tersebut uniumnya bersifat racun (Meister 1985). Limbah yang mengandung senyawa aroniatik pada umumnya agak sulit diuraikan baik dengan cara fisika, kimia maupun biologi. Selain memerlukan waktu yang lama, hasil yang diperoleh tidak memuaskan. Pentaklorofenol banyak digunakan sebagai pembasmi rayap, mencegah pembusukan yang disebabkan oleh jamur atau cendawan, dan serangga penyerang kayu. Pada proses pengawetan kayu, limbah yang dibuang ke lingkungan ternyata mengandung PCP sebanyak 0,05-2760 p a , sedangkan di industri kimia, PCP yang ditemukan dalam limbah sebanyak 5400 pg/L (James and Ramamoorthy 1984). Senyawa ini sangat beracun, karsinogenik, dan termasuk senyawa yang tahan urai oleh karena itu limbah yang mengandung pentaklorofenol harus diolah terlebih dahulu sebelum dibuang ke lingkungan. Berdasarkan sifat racunnya perlakuan dan pemusnahan PCP tidak hanya pada proses biodegradasi saja namun diperlukan alternatif lain. Senyawa ini sulit diuraikan dengan cara konvensional baik cara fisika, kimia maupun biologi. Beberapa cara dengan menggunakan tawas dan karbon aktif digunakan untuk mengeliminasi senyawa ini, namun proses ini hanya akan menimbulkan masalah baru karena pada proses ini dihasilkan sludge yang masih rnengandung pentaklorofenol pada fasa padat. Pengolahan dengan proses biologi memerlukan waktu yang lama, sedangkan proses kimia sangat sulit dilakukan karena senyawa ini sulit diuraikan dengan proses kimia. Oleh karena itu perlu dilakukan alternatif lain untuk menguraikan senyawa tersebut menjadi senyawa sederhana yang tidak beracun (He el a/. 2001 dan Sawai 1995).
Nickelsen et a/. (1994) telah mempelajari penguraian beberapa senyawa aromatis diantaranya benzen, toluen, m-silen, dan o-silen dengan berkas elektron dan menunjukkan senyawa-senyawa tersebut terurai >99%. Kurucz ef a / . (1992) mempelajari penguraian benzen, toluen, fenol, PCE, TCE, dan kloroform dengan variasi pH dan dosis. Hal ini dilakukan untuk melihat keefektifan berkas elektron dalam menguraikan senyawa-senyawa tersebut. Radiasi gamma terhadap fenol dengan konsentrasi 50 ppm dengan penambahan oksidator Hz02 dan dosis 5 kGy dapat menguraikan fenol tersebut sebanyak 92% (Andayani et a/. 1993). Penggunaan radiasi gamma untuk menguraikan senyawa pencemar lain seperti senyawa alifatis dan aromatis terklorinasi anisol, bifenil dapat menguraikan senyawa tersebut menjadi asam-asam organik (Quint et a/. 1996).
Interaksi radiasi sinar gamma dengan air akan menghasilkan spesi-spesi sebagai berikut : radikal hidrogen (He), radikal hidroksil (.OH), elektron tersolvasi (e,,-), molekul Hz02, Hz dan ion hidrogen. Radikal hidrogen dan elektron tersolvasi merupakan spesi reduktor, sedangkan radikal hidroksil dan molekul H202 merupakan spesi oksidator. Jika selama iradiasi dialiri oksigen, maka radikal hidrogen akan bereaksi cepat dengan 0 2 membentuk radikal perhidroksil (H02e) yang juga mempunyai sifat oksidator. Diantara spesi-spesi tersebut radikal OH merupakan spesi yang paling reaktif sebagai oksidator untuk mengubah pencemar organik menjadi COz dan Hz0 pada tahap akhir. Dari hasil beberapa penelitian tersebut menunjukkan bahwa teknik radiasi merupakan salah satu teknologi alternatif dalam pengolahan limbah terutama untuk limbah yang mengandung senyawa tahan urai (Miyata 1993, Donne1 and Sangster 1969, Spinks and Woods 1976).
TINJAUAN
PUSTAKA
PentaklorofenolPentaklorofenol atau (PCP) mulai dikenal dan digunakan sebagai pengawet kayu
sejak tahun 1936 dan dipakai sebagai herbisida oleh C.Chabrolin mulai tahun 1930 Selain itu PCP juga digunakan untuk mencegah rayap dan melindungi pembusukan kayu dari jamur dan kerusakan kayu oleh serangga. Pentaklorofenol mempunyai
nama dagang DOWICIDE 7", DOWICIDE EC-7"dan SINTOPHEN 20 (Hayes and
Caws 199 1 ).
Pentaklorofenol, terutama dalam bentuk garam natrium dapat diaplikasikan dalam skala luas baik di industri pengawetan kayu maupun dalam bidang pertanian sebagai fungisida, dan bakterisida. Pada tahun 70-an PCP di China digunakan sebagai pembasmi siput dan sebagai herbisida. Penggunaan PCP secara luas dan pembuangan
limbahnya yang tidak tepat menyebabkan pencemaran lingkungan. Penguraian secara biologi sangat lambat oleh karena itu tidak mengejutkan bila ditemukan PCP dalam banyak sumber air minum (He el a/. 2001, Fang el nl. 1998).
Sifat fisika dan kimia
PCP atau pentaklorofenol mempunyai rumus empiris C6HCI50, bobot molekul 266,35 dan struktur molekul seperti pada Gambar 1 . Pentaklorofenol berbentuk kristal tidak benvarna dan mempunyai bau seperti fenol, titik leleh 191°c, dan pada suhu 1 0 0 ' ~ tekanannya 0,12 torr. PCP teknis berbentuk hablur atau serpih berwarna abu-abu dengan titik didih 1 5 8 ' ~ . PCP teknis ini merupakan campuran penta dan
Gambar I . Strrlktrlr rnolekr~l Pentaklorofenol (PCP)
PCP mempunyai sifat racun pada tanaman, hewan, dan manusia. Walaupi~n pada dosis yang sangat rendah 0,l - 1 pg/L PCP dapat mempengaruhi organisme dan menyebabkan perubahan ekosistim. Berdasarkan pada sifat racurlriya perlakuan dari pengolahan PCP tidak hanya berdasarkan pada penguraian cara bioloris sa-la. Berdasarkan sifat racunnya perlakuan dan pemusnahan PCP tidak hanya pada proses biodegradasi saja namun diperlukan alternatif lain. PCP dikenal sebagai nt~c.or~/~lc. oxicla/ivc. pho.v/~horylntiow, merusak daya hantar listrik membran dan menghambat enzim selular seperti ATP-ase, 0-galaktosidase dan sebagainya, namun kegiatan rrttcorrplit~~ ini belum jelas ( H o and Bolton 1998).
Kegunaan PCP
deklorinasi pada posisi orlo, nte~u dan para. Proses deklorinasi PCP dilakukan bertahap dengan reaksi deklorinasi pada posisi o, n1 dan p dari proses ini dihasilkan senyawa intermediet dengan berbagai variasi klor (Magar el at. 1999).
PCP di Amerika banyak digunakan sebagai pengawet kayu, oleh karena itu daerah sekitar pengawetan kayu tercemar oleh PCP tersebut. Salah satu penanggulansan untuk menghilangkan pencemar tersebut dilakukan dengan pembersihan dengan pelarut. Pemilihan pelarut hams disesuaikan dengan keefektifan pelarut dalam mengekstrak pencemar. Kelarutan pencemar organik dalam pelarut dan kekeruhan
pelarut dengan air merupakan faktor yang penting (Khodadoust el a/. 1999). Pembentukan PCDD dan PCDF dapat dihasilkan dari PCP yang digunakan sebayai
pengawet kayu dan pestisida, ha1 ini terjadi karena adanya proses pemanasan. Kontaminasi telur, ayam, dan daging sapi dilaporkan pada tahun 1989 dari daerah yang berada dekat dengan areal proses pengawetan kayu. Fasilitas pengolahan kayu yang menggunakan PCP ternyata mencemari hasil peternakan mereka (Harnly el a / .
2000).
Penguraian PCP
Beberapa penguraian cara biologi antara lain penguraian cara abiotik, penguraian oleh mikrob, penguraian dalam sistem perairan, dan penguraian dalam tanah.
1 . Penguraian cara abiotik
Baik PCP maupun Na-PCP dapat terurai secara abiotik dalam air, pelarut organik, dan permukaan tanah. Menurut Wong dan Crisby dalam Anonim 1987 ada 3 tipe hasil penguraian yang te jadi yaitu :
a). Fenol terklorinasi rendah biasanya 2,3,4,6 dan 2,3,5.6-tetraklorofenol bersama dengan triklorofenol.
b). Dihidroksibenzena terklorinasi biasanya tetraklororesorsinol dan tetra klorokatekol.
c). Fragmen non aromatik biasanya dikloroasam maleat. lradiasi terhadap senyawa ini akan dihasilkan COz dan ion klor.
3,3. PCP dalam bentuk ion mudah terurai dalam waktu 20 jam dengan waktu paruh 3,5 jam, sedangkan waktu paruh PCP non ionik 100 jam pcnguraian ini terjadi karena adanya pemindahan gugus klor oleh gugus hidroksil.
2. Penguraian oleh mikroba
Penguraian PCP oleh mikroba telah dipelajari dengan nlcnggunakan media asli maupun buatan dengan biakan tunggal maupun canipuran Iliperoleh hasil bahwa jamur dapat menyerang PCP dengan enzim fenol oksidase. Penguraian PCP
dilakukan oleh jamur genus Ykichoderma. Beberapa kernungkinan mekanisme penguraian PCP dilaporkan oleh beberapa peneliti antara lain :
- metilasi, dihasilkan metil eter PCP, penta kloro anisol
- asilasi dari gugus hidroksil menghasilkan pentaklorofenol asetat
- deklorinasi tetraklorofenol dan hidrolisis tetraklorodihidroksi benzena
Jadi senyawa yang terbentuk dalam jumlah banyak dan akan terakuniulasi ke berbagai tempat, tahap akhir adalah pecahnya cincin rnenjadi senyawa alifatik terklorinasi seperti tetrakloro dan mukonat. Deklorinasi iebih lanjut akan menjadi senyawa alifatik dengan berat molekul rendah misalnya asani asetat atau suksinat yang akan masuk dalam lingkar asam trikarboksilat.
3 . Penguraian dalam sistem perairan
Penguraian PCP dalam sistim perairan lebih mudah terjadi karena adanya cahaya, pH basa, dan jumlah oksigen yang tinggi. PCP akan terurai dari sistini tersebut pada laju yang berbeda dengan waktu paruh antara 12,s sampai 18,6 hari kecuaii untuk sistim anaerobik tanpa hydrosoil (79,8 hari). Bila dalam sistim tidak ada cahaya clan lumpur, kondisi anaerobik dan pH rendah akan terjadi persistensi PCP. Hal ini menunjukkan bahwa bentuk fenol PCP lebih persisten dari bentuk fenat, proses oksidasi merupakan mekanisme utama pada penguraian PCP dalam lingkungan air.
4. Penguraian dalam tanah
spesies l~setrcl'omot~as, sehinsga aktivitas PCP terpecah. Pada suhu 20°C PCP dengan konsentrasi 50 m d L terurai scbanyak 50% dalam waktu 8 hari. Pengaruh oksigen pada proses biodegradasi bcrvariasi pada banyak hal, kondisi tanah anaerobik meningkatkan laju penguraian. sejauh ini menurunnya kondisi ini menghasilkan proses reduksi deklorinasi I l i sisi lain biodegradasi dalam tahap pembentukan senyawa intermediet pentakloroanisol lebih cepat dalam kondisi aerobik
dibandingkan dengan kondisi anaerobik. Penguraian PCP dalam tanah rata-rata 88% dari 100 m g k g tanah liat pada kondisi aerobik (160 hari pada suhu 23°C) sedang pada kondisi anaerobik hanya terurai sebanyak 7%. Penguraian PCP juga dihambat oleh beberapa fungisida dan kondisi dibawah permukaan air (Anonim 1987).
Teori Kimia Radiasi
Kimia Radiasi mempelajari perubahan kimia dalam suatu materi yang ditimbulkan oleh radiasi pengion dengan energi tinggi (40 keV - 4 MeV). Radiasi dengan energi rendah (< 40 keV) hanya dapat mengakibatkan eksitasi. Sifat utama radiasi yang
berenergi tinggi ialah dapat menyebabkan proses ionisasi dan eksitasi. lonisasi, yaitu pelepasan elektron dari orbitalnya akibat adanya energi dari luar (Miyata 1993, Donnel and Sangster 1969, Spinks and Woods 1976).
AB
+
AB' + e-Eksitasi, yaitu perpindahan elektron k e tingkat energi yang lebih tinggi jika diberi
energi dari luar. A B
+
AB*Interaksi ionisasi dan eksitasi akan nienyebabkan pemutusan ikatan kiniia dan
pembentukan ikatan kimia yang baru sehingga akan diperoleh hasil akhir yang dapat dimanfaatkan dalam berbagai bidang antara lain polimerisasi karet alam. pcrubahan permanen struktur molekul biologi (mutan), sterilisasi alat-alat kedoktcran. dan pengolahan limbah.
Radiasi ialah pancaran energi atau partikel energilfoton oieh suatu surnber. adapun jenis-jenis radiasi terbagi atas :
Radiasi pengion, menirnbulkan ionisasi dan eksitasi jika berinteraksi dengan materi, energinya Icbih tinggi dari potensial ionisasi atom atau molekul yang terdiri dari :
partikel bermuatan a (inti ~ e ~ ' ) , (pancaran elektron dari inti), berkas elektron dipercepat. berkas ion antara lain : netron (bermasa 1 tetapi tidak bermuatan), gelombany clektromagnetik (tidak bermasa dan tidak bermuatan), misalnya : sinar x
diperoleh dcngan menernbakkan berkas elektron pada target logam berat dan sinar y dilepaskan pada peluruhan inti unsur radioaktif.
Sumber Kadiasi
Sumber radiasi terdiri atas sumber radiasi alam (yang termasuk dalam sumber radiasi alam antara lain : radium, radon, cobalt-60, cesium- 137, dan strontium-90) dan surnber radiasi buatan (yang termasuk dalam sumber radiasi buatan antara lain, sinar x. akselerator Van de Graaf, betatron, siklotron, berkas elektron, dan reaktor nuklir)
interaksi Sinar Gamma dengan Materi
Sinar gamma merupakan radiasi elektromagnetik yang dipancarkan dalam bentuk
partikel-partikel berenergi atau disebut foton. lnteraksinya dengan materi tergantung pada energi dan materinya sendiri. Mekanisme interaksi sinar gamma dengan materi dibagi menjadi tiga macam (Donne1 and Sangster 1969, Spinks and Woods 1976) :
a. Efek fotolistrik
Dalam peristiwa ini seluruh energi foton digunakan untuk mengeksitasi elektron
yang terdapat pada orbital dalam. Peristiwa ini hanya terjadi pada energi foton < 0,l
MeV dengan nomer atom target (Z) rendah.
Ion posbf
b. Efek hamburan Compton
Pada proses ini hanya sebagian energi foton diberikan kepada materi untuk ionisasi, sisanya dilepaskan sebagai sinar gamma berenergi lebih rendah. Hal ini terjadi pada foton yang mempunyai energi 0,IMeV < Eo < 1 MeV, dan tidak bergantung pada nomer atom target
,/*-Be-
I #-. \I \
1 -
1
+ o e .
I
.
@
- - -
.
,;
\ /ion
;i~ii'\
Gar~lbar 3. Efek hamburan Compton
c. Produksi pasangan ion
Proses ini terjadi bila seluruh energi foton diberikan dan menghasilkan pasangan elektron-positron. Kedua spesi ini saling menghapuskan dan membentuk sinar gamma dengan energi 0,s MeV. Proses ini dapat t e j a d i pada foton yang mempunyai energi > 1,02 M e V dengan nomer atom target tinggi. Elektron yang terbentuk dari interaksi sinar gamma disebut elektron sekunder yang dibekali energi, sehingga menjadi sangat reaktif Elektron sekunder ini akan mengionisasi materi yang dilaluinya.
/-.
I \
Oe-
l o ;
+
\ /
\
.
//
-
--
0
e+
ion positif positron
Satria11 Ilosis Hadiasi
Satuan radiasi ialah Gray, yang didefinisikan sebagai energi sebesar 1 joule yang diserap oleh setiap kilogram materi yang diiradiasi.
1 Gray (Gy) = 100 rad = I joulelkg
Satuan radiasi ini juga disebut satuan radiasi terserap karena yang diukur bukan radiasi yang datang ataupun radiasi yang ditransmisikan melainkan yang diserap oleh materi. Sati~an selain Gray, yang juga dipakai dalam radiasi ialah rad dengan 1 rad (r)
= 100 erglg = 0,Ol joulelg. Nilai C ((;-~*crllfe)
Satuan lain yang biasa digunakan dalam kimia radiasi ialah nilai G, dimana nilai G ini digunakan untuk membandingkan jumlah produk yang terbentuk. Nilai G yaitu banyak nya atom, molekul, ion yang berubah atau yang terbentuk akibat penyerapan energi radiasi sebesar 100 ev oleh materi yang diiradiasi.
ftadiolisis Air
Kadiolisis ialah suatu proses penguraian oleh radiasi pengion yang tejadi pada suliu ruang. Radiolisis air oleh radiasi pengion akan menyebabkan efek langsung dan tidak langsung. Efek langsung yaitu interaksi radiasi dengan materi, sedangkan efek tidak langsung yaitu interaksi radiasi produk radiolisis air dengan molekul zat terlarut (Miyata 1993, Donnel and Sangster 1969, Spinks and Woods 1976). Adapun proses radiolisis air dapat digambarkan sebagai berikut:
11:O 1-1~0 ' + e- (ionisasi) ( 1 )
[H20]* 4 H + OH (eksitasi) (2)
karena kepolaran H;O niaka akan terjadi :
t o
+ 1 - 1 2 0----+
HTO' + .OH ( 3 )c- + H:O d He- + OH- (4)
EleLtron juga mengalami perlambatan karena pemindahan energinya, keniudian akan rnencapai enersi minimum (elektron thermal) dan akan dikelilingi oleh H 2 0 karena Lepolarannya yang disebut elektron terhidrasi (e.,,, ) ( 5 )
Produk ( 1 - 6) disebut bentuk antara yang terdistribusi tidak hon~ogen di dalain . Y / ) ~ I I . Adapun di dalam sjmr sendiri akan terjadi reaksi sesama radikal yaitu radikal-radikal H dan O H yang akan membentuk produk molekul Hz dan H 2 0 2 .
H e + H e + Hz (k=1 x1 0'('dm3 mol-Is-') ( 7 )
.OH + *OH
+
H 2 0 2 (k=6x 1 ~ ~ d m % o l - ' s - ' ) (8) H + O H---+
Hz0 (k=2,5x 1 0"dm3 mol-'s-')H + e,;
--+
H Z + OH,; (k=2x 10" dm3mol-Is-') OH + e,,;+
OH,, (k=2,5x10"' drn.'mol-Is-') e,,- + e+
H + 2 O H (k=3x 10' d m h m o l " ~ ~ ' ) eCiq- + Haq+--+
H (k=2,3x10l0 dm"nol-'s-' )H + OH,,-
---+
e,,,- +H20 (k=2,5x 10' d ~ n ~ m o l - ' s - ~ )__+
OH 1 H a '
+aq@-
(pK = 11,9)H202
---+
Hay' + HOzaq- (pK = 1 1,65)Jadi H e, *OH, H 3 0 . , e,,-, Hz dan H 2 0 2 merupakan produk primer radiolisis yaitu
bentuk intermediate yang tidak bereaksi dan akan keluar dari sprrr dan terdishsi nierata dalam sistim H20. Produk primer ini akan bereaksi dengan zat-zat terlarut di dalam air misalnya 0 2 (dari udara terlarut):
He
+
O2+
H O p (radikal perhidroksil) (k=2,1 ~ 1 0 " ' d m h o l - I s - ' ) eoq + 0 2-
4 0 2 . - (ion superoksida) (k=1,9x 10'" drn'mol-'4')
H02. H +02- (PK = 4 3 )
Reaksi Produk Primer dengan Zat Organik dalam Larutan Air
Telah dijelaskan bahwa masing-masing spesi H, OH, H 0 2 dan e,, mempunvai sifat niengoksidasikan dan rnengubah molekul zat organik, (RH) dan menghasilkan radikal bebas R (Re), niolekul H2 atau H 2 0 . Sebagai ilustrasi, oksidasi anilin sebasai berikut :
2. Adisi
3. Kombinasi
4. Pemindahan elektron
M (Z')
+
He---+
M (Z+1)'+
He-M (2')
+
@ OH+
M (Z+l)'+
OH.-Radikal-radikal R , HRH dan KROH yang terbentuk tergantung pada reaktifitas dan konsentrasi radikal tersebut sedang reaksi selanjutnya dapat terjadi dengan radikal bebas lain atau molekul-molekul terlarut. Reaksi yang mungkin te rjadi ialah
Reaksi rekombinasi Re + He ---- R H
Reaksi kombinasi 2 radikal organik Re + Re
-+
RR Re+
R'e j RR'e Reaksi oksidasi satu tahapRe
+
*OH---+
ROH (12)Reaksi oksidasi oleh molekul oksigen terlarut
Re + 02----+ RO2e (13)
bertambahnya bobot molekul maka akan menurunkan kelarutan senyawa organik dalam air. Hal ini juga membuktikan bahwa tehnik radiasi mempunyai kemampuan mengubah pencemar organik sehingga dapat diproses dengan cara koagulasi maupun pengendapan (Miyata 1993).
Oksidasi Senyawa Organik dalam Larutan Air
Radiasi pengion menghasilkan spesi pengoksidasi yang mempunyai kemampuan dapat menguraikan senyawa organik dalam larutan limbah. Penguraian tersebut dapat melalui proses langsung maupun tidak langsung. Adapun mekanisme reaksi
sederhana dapat digambarkan sebagai berikut: a. Reaksi inisiasi
RH + *OH
---+
R* + H20 b. Reaksi propagasiR* + 0 2
+
ROO*ROO* + RH
+
ROOH+
ReROOH
+
RO*+
*OH RO* + RH---+
ROH + R*c. Pembentukan COz (pemecahan ikatan C-C)
ROH + .OH
--+
R'C*(OH)H + H20R'C*'(OH)H + 0 2
--+
R'C(OH)(OO*)HR'C(OH)(OO*)H
+
R'* + C 0 2 + H 2 0BA1I.AN
DAN hl~'1'0I)I-
Bahar~
Bahan yang dipakai pada penelitian ini PCP dengan hc.mi~rnian 96%. etanol absolut, metanol, HJPOI, asam oksalat, NaOH, Hs(S('N):. \n('l. NHIFe(S04)2 13, HzO, larutan bufer standar pH 7 dan pH 4, akuades dan ahua t ~ d c s
Peralatan
Peralatan yans dipakai antara lain iradiator sanlrnr-1 IKI'ASENA (Iradiator
60
Panorama Serbaguna) dengan sumber C o pada bulari Juni 2001 rnempunyai aktivitas 22000 Ci, aerator, spektrofotometer uv-vis 1-11' 8-153, pH meter Methrom tipe 620, HPLC LC 9A Shimadzu, dilengkapi dengan detektor SPD 6 A. pompa Shirnadzu LC 5A, rekorder Chromatopac CR3A, koloni I'henomeneu C-18 dan Shodex RS Pax, alat pengukur DHL, dan peralatan kaca lainnya
Metode Penelitian
PCP dapat diuraikan pada dosis dan laju dosis rendah. oleh karena itu pada awal percobaan dilakukan penentuan dosis optimum agar rentang dosis yang diinginkan dapat lebih terfokus Laju dosis yang digunakan pada penelitian ini dilakukan variasi laju dosis 0,5 kGy/jam dan 1 kGy/jam Penguraian PCP juga dipenzaruhi oleh pH, oleh karena itu variasi pH juga dilakukan dalam penelitian ini
Diagram penelitian dapat digambarkan sebagai berikut
I'enentuan dosis optimum:
pH awal 7, laju dosis 1 kGy/jan~ dosis : 0-10 kGy, 0-5 kCv dan 0-2 kGv
1 Pengaruh pH (pH 5,6, 7, dan 8)
PCP 10 ppm dosis 0-2 kGy, laju dosis 1 kGy/jam
2 Pengamh laju dosis (laju dosis 0,5 kGy/jam dan 1 kGy1jam)
PCP 10 ppm pH 7 dosis 0-2 kGy
3 Pengamh konsentrasi (2, 4, 8, dan 10 ppm) pH 7 dosis 0-2 kGy laju dosis 0,5 kGy1jam 4 Pengukuran asam-asam organik
PCP 10 ppm, pH 7 dosis 0-2 kGy, laju dosis 0,5 kGy/jam 5 Pengukuran klor
PCP 10 ppm, pH 7, dosis 0-2 kGy, laju dosis 0,5 kGy/jam 6 Pengukuran sisa PCP
PCP 10 ppm, pH 7, dosis 0-2 kGy, laju dosis 0,5 kGy1jam 7 Pengkuran daya hantar listrik
PCP 10 ppm, pH 7, dosis 0-2 kGy, laju dosis 0,5 kGyIjam
1 Penentuan dosis optimum pada penguraian PCP
Penentuan dosis optimum pada penguraian PCP dilakukan menggunakan lamtan PCP dengan konsentrasi 10 ppm.
a. Mula-mula dilakukan radiasi dengan pH awal 7, laju dosis 1 kGyIjam dan dosis O- 10 kGy. Sebanyak 250 ml PCP dengan konsentrasi 10 ppm dimasukkan dalam botol
khusus dengan (t=16 cm, 0 5 cm). Selama iradiasi dialirkan udara dari bagian bawah
larutan. Pengambilan sampel dilakukan setelah 0, 2, 4, 6, 8, dan 10 jam. Sampel kemudian diukur serapannya dengan menggunakan spektrofotometer uv-vis.
b. Radiasi dilanjutkan dengan menurunkan dosis radiasi menjadi 0-5 kGy dengan kondisi yang sama dengan sebelumnya. Pengambilan sampel dilakukan setelah 0, 1, 2, 3, 4, dan 5 jam. Sampel diukur serapannya dengan menggunakan spektrofotometer uv-vis.
c. Kadiasi dilanjutkan dengan merubah dosis menjadi 0-2 kGy dengan kondisi sama dengan sebelumnya. Pengambilan sampel dilakukan setelah 0, 30, 45, 60, 90, dan 120
2 Pengaruh 1111 pada penguraian PCP
PCP dengari konsentrasi 10 ppm diiradiasi dengan variasi pH awal yaitu pH 5, 6, 7, dan 8 . Kadiasi dilakukan dengan dosis 0-2 kGy, laju dosis 1 kGy/jam. Sebanyak 250 rnl sampel dimasukkan ke dalam botol khusus untuk meradiasi dengan (t=16 cm, 0 5 cm). Sclama iradiasi udara dialirkan melalui bagian bawah larutan. Pengambilan
sampel dilakukan setelah 0, 30, 45, 60, 90, dan 120 menit. Larutan kemudian diukur serapannya dcngan menggunakan spektrofotometer uv-vis. Pekerjaan ini dilakukan
dua kali.
3 Pengaruh laju dosis terhadap penguraian PCP
Sebanyak 5 ml PCP dengan pH awal 7 dan konsentrasi 10 ppm dimasukkan ke dalam ampul. dialiri udara kemudian ditutup. Sampel diiradiasi dengan dosis 0-2 kGy dan variasi laju dosis 0,5 kGy/jam dan 1 kGy/jam. Setelah diiradiasi sampel diukur serapannya dengan menggunakan spektrofotometer uv-vis. Pengamatan dilakukan dengan n~elihat penurunan intensitas serapan pada panjang gelombang 220, 250, dan
320 nm. Dilakukan juga perhitungan persentase penguraian PCP dari masing-masing konsentrasi tersebut. Peke j a a n dilakukan dua kali.
4 Pengaruh konsentrasi pada penguraian PCP
Sebanyak 5 ml PCP dengan pH awal 7 dan variasi konsentrasi 2 , 4 , 8, dan 10 ppm
dimasukkan ke dalam ampul, kemudian dialiri udara dan ditutup. Larutan ini diiradiasi dengan dosis 0-2 kGy dan laju dosis 0,5 kGy/jam. Setelah diiradiasi sampel diukur serapannya dengan spektrofotometer uv-vis. Pekerjaan ini dilakukan dua kali.
5 Pengukuran asam-asam organik hasil pengi~raian PCP
Sebanyak 5 ml PCP dengan pH awal 7 dan konsentrasi 10 ppm dimasukkan ke dalam ampul, dialiri udara dan ditutup. Larutan diiradiasi dengan dosis 0, 0,5,0,75, 1, 1,5, dan 2 kGy dengan laju dosis 0,5 kGy/jam. Setelah diiradiasi dilakukan
pengukuran asam-asam organik yang terbentuk. Pengukuran asam-asam organik yang terbentuk dilakukan dengan menggunakan alat HPLC, kolom Shodek Pax, pelarut HJPOJ 0,005% dengan laju alir 1 mllmenit dan detektor uv pada panjang
6 Pengukuran klor
Sebanyak 5 rnl PCP dengan pH awal 7 dan konsentrasi 10 ppm dimasukkan ke dalarn anipul, dialiri udara dan ditutup. Larutan diiradiasi dengan dosis 0, 0,5, 0,75, 1,
1,5, dan 2 kGy dengan laju dosis 0,5 kGyIjam. Setelah diiradiasi dilakukan pengukur-an klor yang terbentuk. Pengukuran klor dilakukari dengan penambahan pereaksi Hg(SCN)2 dan NH4Fe(S04)?, kemudian larutan diukur dengan menggunakan spektroiotonieter pada panjang gelombang 460 nm.
7 Pengukuran sisa I'CP
Sebanyak 5 ml PCP dengan pH awal 7 dan konsentrasi 10 ppm dimasukkan ke dalam ampul, dialiri udara. dan ditutup. Larutan diiradiasi dengan dosis 0,0,5, 0,75, 1, 1.5, dan 2 kGy dengan laju dosis 0.5 kGy/jam. Setelah diiradiasi dilakukan pengukuran sisa PCP. Pengukuran sisa I'CP dilakukan dengan alat HPLC dengan koloni Phenomenec C-18 dengan detektor UV 215 nm, pelarut metanol : air (7:3)
dengan pH 3 . Peke rjaan ini dilakukan dua kali.
8. P e r ~ g u k u r a n d a y a h a n t a r listrik (DHL) d a n pH
HASlL DAN I'EMBAlMSAh
Penentuan dosis optimum pada pengul-aian PCP
Dosis optimum pada penguraian PCP adalah dosis terendah yarig dapat digunakan untuk menguraikan PCP. Pada awal penelitian diketahui bahwa penguraian PCP tidak memerlukan dosis yang tinggi, namun berapa dosis yang tepat perlu dikaji lebih lanjut. Tahap pertama dilakukan radiasi dengan rentang dosis 0-10 kGy, namun karena penurunan intensitas serapan hanya terlihat sarnpai dosis 2 kGy, niaka radiasi dilanjutkan dengan memperkecil rentang dosis. Tahap kedua dilakukan radiasi dengan dosis 0-5 kGy, penurunan intensitas serapan terlihat sampai dosis 2 kGy, liemudian intensitas naik. Tahap ketiga dilakukan radiasi dengan rentang dosis 0-2 kGy, pada tahap ini penurunan intensitas serapari terlihat dengan nyata.
PCP mernpunyai serapan pada daerah ultraviolet dengan panjang gelombang 220, 250, dan 320 nm seperti terlihat pada Gainbar 5. Serapan pada panjang gelombang 220 nm nienunjukkan adanya senyawa aromatik tersubstitusi, sedangkan panjang gelombang 250 dan 320 nm menunjukkan adanya ikatan rangkap dan elektron bebas pada atom oksiyen atau klor.
:7 f i 250 :iX) .XD .1X' -to
- - - -. . . - -- - - - - - - -- - Panjang gelombang (nni)
Canibar 5. Spektrum PCP setelah diiradiasi dengan dosis 0-10 kGy, p H awal 7 dan Iaju dosis I kCy/jam
'1'abt.l 1. Perubahan serapan PCP setelah diiradiasi dengari dosis 0-10 kGy
- -
-Ilosis radiasi (kGy) G a p a n (nm)
Ilari Tabel 1 terlihat bahwa dosis optinial vary dikehendaki tidak terlihat den2an
jclas Oleh karena itu radiasi dilanjutkan denyan rentang dosis 0-5 kGy dengan Londisi sania dengan di atas. Perubahan spektrum I'CP setelah diiradiasi dengan dosis
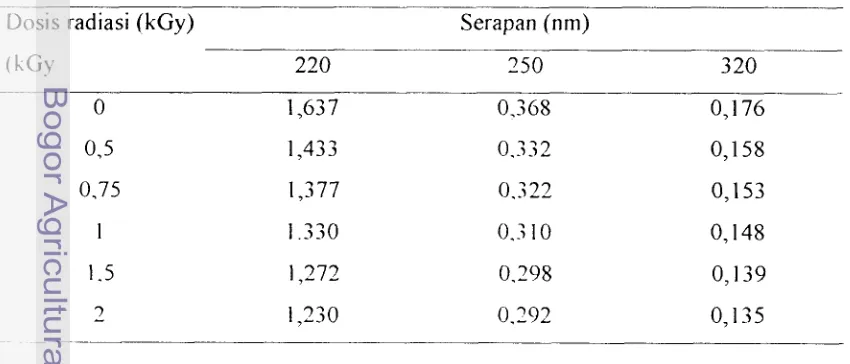
Tabel 2. Perubahan serapan PCP setelah diiradiasi derlgan dosis 0-5 k e y
-
Dosis radiasi (kGy) Serapan (nm)
(kGy 220 250 3 20
0 1,678 0,388 0,198
1 1,412 0,328 0,160
2 1.233 - 0,105
-7
3 1418 - -
4 1,392 - -
5 1,420 -
Dari data tersebut terliliat bahwa perubahan spektrum PCP setelah diiradiasi dengan dosis 0-10 k<;y dan 0-5 kGy niemiliki pola spektrum yang hampir sama, diniana pada dosis 2 kGy intensitas serapan mengalami penurunan. Naniun dengan naiknya dosis di alas 2 kGy intensitas serapan pada panjang gelombang 220 nm mengalami kenaikan dan adanya pergeseran panjang gelombang Pada panjang gelombang 250 dan 320 nm intensitas serapan mengalami penurunan dengan nai knya dosis. Oleh karena itu radiasi dilanjutkan dengan rentang dosis 0-2 kGy den2an kondisi sama derigan di atas
1 I 1
200 250 3x1 350 400 450 Panjang gelombar~g(nm)
[image:104.543.24.474.47.748.2]I'erubahan spektrum PCP yang diiradiasi dengan dosis 0-2 kGy dapat dilihat pada Gambar 7, sedangkan perubahan nilai serapan dapat dilihat pada Tabel 3. Dari data tersebut dapat dilihat bahwa intensitas serapan pada tiga panjang gelombang 220. 250, dan 320 nm mengalami penurunan dengan naiknya dosis radiasi. Penurunan pada panjang gelomban_g 220 nm masih belum optimum, oleh karena itu perlu dilakukan variasi parameter lainnya sehingga akan diperoleh penurunan serapan yang oi)filnurn.
.
, , 1 T 77---. . . .
1 1 1 - . 7-
- 7 7-' 7 - 7 - 7 - - y 7 -' -.
-200 2 5 0 - 300 _ 350 400 450 Panjang gelombang (nm)
Gambar 7. Spektrurn PCP setelah diiradiasi dengan dosis 0-2 kGy, pH awal
7 dan Iaju dosis 1 kGy/jam
Tabel 3. Perubahan serapan PCP setelah diiradiasi dengan dosis 0-2 kGy
[image:105.543.51.476.488.670.2]Peagaruh pH pada penguraiarl PCP
Penyaruh pH pada penguraian PCP dilakukan dengan variasi pH 5 , 6, 7, dan 8 . Radiasi dilakukan pada dosis 0-2 kGy dengan laju dosis 1 kGyIjam. Spektruni PCP yang diiradiasi pada pH 5, 6, 7, dan 8 dapat dilihat pada Gambar 8, 9, 7, dan 10. Dari spektrum pada Gambar 8, 9, dan 10 dapat dilihat bahwa panjang gelombang 220 nm mengalami pergeseran ke arah pergeseran biru (efek hipsokromik), sedangkan panjang gelombany 250 dan 320 nm mengalami penurunan intensitas serapan. Berkurangnya intensitas pada 250 dan 320 nm menunjukkan ikatan rangkap maupun elektron bebas pada atom oksigen maupun klor semakin nienurun.
I 7 7 T -7T
-
-7---
, 7 -7200 2% - 300 - - 350 Panjang gelombang (nm)
--
--X -X ) m 303 350 P a i ~ j a i ~ g gelombirng (om)
,
Gainbar 9. Spektrum P C P setelah diiradiasi dengan dosis 0-2 kGy, p l i awal 6 dan Iaju dosis I kGy/janl
Ganlbar 10. Spektrum P C P setelah diiradiasi dengan dosis 0-2 k C y , p H awal 8 dan Iaju dosis 1 kGy/jam
Seperti diketahui panjang gelombang 250 menunjukkan ikatan rangkap tereksitasi n
+
x*, sedangkan panjang gelombang 320 nm menun-jukkan pasangan elektron bebas dari atom oksigen atau klor yang tereksitasi n+
n*. Panjany gelombang 220 nnlpengaruh pemindahan konjugasi. Kemungkinan yang dapat terjadi ialah karena adanya perubahan medium. Seperti diketahui larutan hasil radiasi biasanya mengalami penurunan pH, artinya suasana larutan berubah nicnjadi asam. Meningkatnya keasaman mengindikasikan H radikal (He) semakin ban>.ak. sehingsa diasumsikan di dalam larutan radikal [I akan menggantikan iori kloi- diilam scnyawa
PCP.
Karena ion klor mempunyai keelektronegatifan tinggi dan adanva elektron bebas maka ia dapat menggeser panjang gelombang spektrum I'CI' ke arah perseseran merah atau panjang gelombans yang lebih besar. Sebaliknya, ion ti tidak rnenipunyai pasangan elektron bebas sehingga adanya atom H dalam senyawa PCi' nlenyebabkan terjadinya efek hipsokromik (Silverstein 198 1 ).
Serapan pada panjang selombang 220 nm mengalarni penurunan sarnpai dosis
0,75 kGy, kemudian meningkat kembali sampai dosis 2 kGy. Peninskatan ini dipengaruhi banyak ha1 antara lain koefisien molar ekstingsi (E). konsentrasi senyawa
dan tebal kuvet. Pengaruh yang mungkin terjadi ialah dari nilai E, karena konsentrasi
larutan dan tebal kuvet sarna. Nilai E ini dipengaruhi probabilitas transisi elektron dan
sistim penyerapan. Salah satu faktor yang berperan dalam nilai E ini ialah timpan3
Molekul PCP Pentaklorof'enolat (ion PCP)
Adanya kelebihan elektron pada oksigen akan terdislokasi ke atom karbon dalani cincin benzena ha1 ini mengakibatkan pentaklorofenolat rnempunyai probabilitas transisi yang kecil. Hal ini akan mengakibatkan senyawa pentaklorofenolat sulit tereksitasi pada saat diiradiasi .
C I C I C I C I
Dalaln suasana larutan yang bersifat asam, senyawa pentaklorofenolat akan menibentuk molekul PCP, makin tinggi dosis niolekul PCP yang terbentuk niakin bertambah. Pentaklorofenol memiliki probabilitas transisi yang besar karena PCP niemilki orbital
x
yang tumpangsuh. Ikatan rangkap pada benzena yang berjumlah tiga menghasilkan enam orbital x yang terdiri dari tiga orbital x bonding dan ti9a orbitalx
anti bonding. Eksitasi x3 x *
berlanssung dari orbital 7t tingkat energibonding tertinggi ke orbital anti bonding terendah. Transisi
x
+ x * ini melibatkan orbital yang sangat overlap dan menghasilkan eksitasi niaksi mum 1 ,O. Molekul PCP mempunyai probabilitas eksitasi yang tinggi. maka nilai E akan tinggi. Bila dikaitkanKenlungkinan lair1 !.ang dapat meningkatkan nilai serapan pada panjany gelonibang 220 nnl ialall heberadaan 02. Molekul O2 memiliki dua elektron bebas yang tidak berpasangan Jika O 2 dialirkan ke dalam larutan PCP yang diiradisi dengan sinar gamma, maka molckul tersebut dapat bereaksi dengan elektron tersolvasi menibentuk 02.- denyan rnckanisnie sebagai berikut:
0 0 2 . +e-;,,, +O:. h l . c > s 10"'
Menurut Fang rl ctl. ( IOOX) 02.- hereaksi lambat dengan PCP dan dapat mereduksi beberapa radi kal perit ak lorofenoksil umtuk meregenerasi PCP, ha1 ini yang nienyebabkan pan-jany !elombang 220 nm meningkat kembali. Spektrum PCP yang diiradiasi pada pH a u a l 7 dapat dilihat pada Gambar 4, diniana serapari pada panjans gelombang 220, 250. dan 320 nm mengalami penurunan dengan naiknva dosis radiasi. Pergeserari panjang gelonibang 220 nm dan penurunan intensitas serapan tidak terlalu besar. Menurut He ri a/. (2001) penguraian PCP sangat tergantung pada dosis y a n s diberikan, bila dosis yang diberikan lebih tinggi. maka senyawa intermediet akan bersaing dengan PCP dalam menangkap spesi pengoksidasi .OH atau e-,,. Keberadaan spesi pengoksidasi seperti O H radikal (*OH) dari molekul Hz02 harus dijaga agar junilahnya cukup untuk mengoksidasi senyawa PCP. Usaha yang dilakukan oleh He adalah dengan menggunakan dosis radiasi yang lebih rendah dengan laju dosis yang disesuaikan agar penurunan pH dapat ditekan sehingga keberadaan radikal O H dapat dijaga.
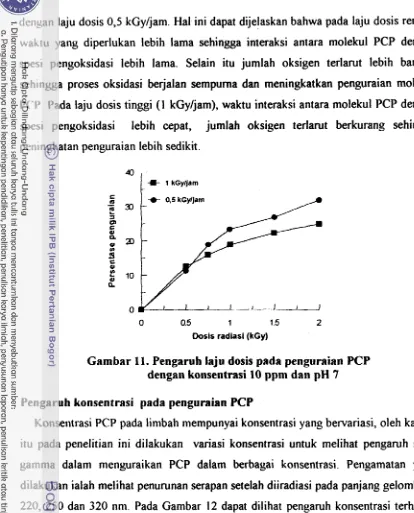
Per~garuh laju dosis pada penguraian PCP
dengan laju dosis 0,s kGy/jam. Hal ini dapat dijelaskan bahwa pada laju dosis rendah waktu yang diperlukan lebih lama sehingga interaksi antara molekul PCP dengan spesi pengoksidasi lebih lama. Selain itu jumlah oksigen terlarut lebih banyak sehingga proses oksidasi berjalan sempurna dan meningkatkan penguraian molekul
P<'lD Pada laju dosis tinggi (1 kGyIjam), waktu interaksi antara molekul PCP dengan spesi pensoksidasi lebih cepat, jumlah oksigen terlarut berkurang sehingga peningkatan penguraian lebih sedikit .
0 0.5 1 1.5 2
[image:111.505.25.439.38.551.2]Dosis radiasi (kGy)
Gambar 11. Pengaruh laju dosis pada penguraian PCP
dengan konsentrasi 10 ppm dan pH 7 Pengaruh konsentrasi pada penguraian PCP
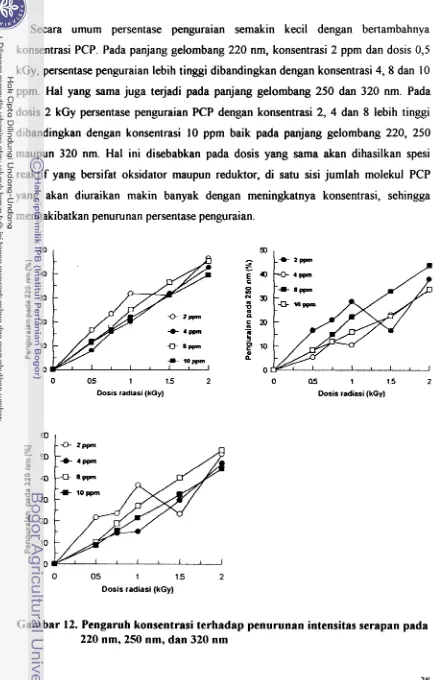
Konsentrasi PCP pada limbah mempunyai konsentrasi yang bervariasi, oleh karena itu pada penelitian ini dilakukan variasi konsentrasi untuk meli hat pengaruh sinar gamma dalam menguraikan PCP dalam berbagai konsentrasi. Pengamatan yang dilakukan ialah melihat penurunan serapan setelah diiradiasi pada panjang gelombang 220, 250 dan 320 nm. Pada Gambar 12 dapat dilihat pengaruh konsentrasi terhadap persentase penguraian pada panjang gelombang 220 nm, 250 nm dan 320 nm. Persentase penguraian dapat dihitung dari persamaan
Penguraian % = Ag
-
A, x 100 AoSecara umum persentase penguraian semakin kecil dengan bertambahnya konsentrasi PCP. Pada panjang gelombang 220 nm, konsentrasi 2 ppm dan dosis 0,5 kGy, persentase penguraian lebih tinggi dibandingkan dengan konsentrasi 4, 8 dan 10 ppm. Hal yang sama juga terjadi pada panjang gelombang 250 dan 320 nm. Pada dosis 2 kGy persentase penguraian PCP dengan konsentrasi 2, 4 dan 8 lebih tinggi dibandingkan dengan konsentrasi 10 ppm baik pada panjang gelombang 220, 250 maupun 320 nm. Hal ini disebabkan pada dosis yang sama akan dihasilkan spesi reaktif yang bersifat oksidator maupun reduktor, di satu sisi jumlah molekul PCP yang akan diuraikan makin banyak dengan meningkatnya konsentrasi, sehingga mengakibatkan penurunan persentase penguraian.
0 05 1 1.5 2 0 05 1 1.5 2
Dosis radiasi ( f f i y ) Dosis radiasi (kGy)
[image:112.527.39.473.23.703.2]0 05 1 15 2 Dosis radiasi (kGy)
Gambar 12. Pengaruh konsentrasi terhadap penurunan intensitas serapan pada
Perubahan pH setelah radiasi
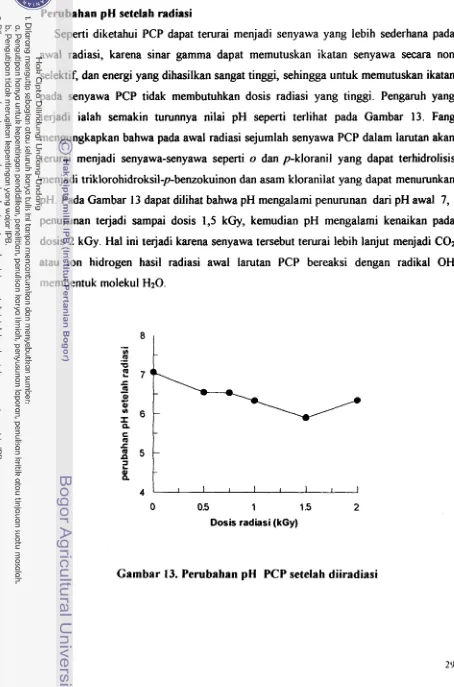
Seperti diketahui PCP dapat terurai menjadi senyawa yang lebih sederhana pada awal radiasi, karena sinar gamma dapat memutuskan ikatan senyawa secara non selektif, dan energi yang dihasilkan sangat tinggi, sehingga untuk memutuskan ikatan pada senyawa PCP tidak membutuhkan dosis radiasi yang tinggi. Pengaruh yang terjadi ialah semakin turunnya nilai pH seperti terlihat pada Gambar 13. Fang
mengungkapkan bahwa pada awal radiasi sejumlah senyawa PCP dalam larutan akan terurai menjadi senyawa-senyawa seperti o dan p-kloranil yang dapat terhidrolisis menjadi triklorohidroksil-p-bemokuinon dan asam kloranilat yang dapat menurunkan pH. Pada Garnbar 13 dapat dilihat bahwa pH mengalami penurunan dari pH awal 7, penurunan terjadi sampai dosis 1,5 kGy, kemudian pH mengalami kenaikan pada dosis 2 kGy. Hal ini terjadi karena senyawa tersebut tewrai lebih lanjut menjadi COz
atau ion hidrogen hasil radiasi awal larutan PCP bereaksi dengan radikal OH
membentuk molekul
HzO.
4 1 I I 1 I I 1 i 1
0 0.5 1 1.5 2
[image:113.534.11.465.43.730.2]Dosis radiasi (kGy)
Menurut He (2001)mekanisme reaksi yang terjadi sebagai berikut
c
l
*
;
*- +H+L
N;
-
ti+
CI
-
N; (PK~*,S)C I
C
I
C
ic+cl
C I
53% ran eleMr0n 'OH 47% penarnbahan radilel
-
OH-7+
Pada tahap awal, PCP bereaksi dengan radikal OH melalui dua tahap reaksi yang saling bersaing, yaitu pertukaran elektron dan penambahan radikal (He rr cr/. 2001). He menemukan bahwa sekitar 53% radikal OH berada pada perlukaran elektron dan sisanya terjadi penambahan radikal. Kedua mekanisme tersebut hanva memerlukan sebagian PCP yang diuraikan dan lebih dari satu ion klor yanp terlepas, jadi dapat dijelaskan bila dosis yang digunakan tidak tepat, maka dalam larutan akan terbentuk senyawa-senyawa seperti kloranil yang toksisitasnya perlu diketahui Oleh karena itu perlu dikaji untuk mendapatkan dosis yang tepat dalam penguraian PCP ini supaya hasil akhir tidak meracuni lingkungan.
Adanya OH pada cincin benzena akan terjadi reaksi substitusi nukleofilik pada posisi
orto
dan para. Reaksi selanjutnya akan melepas satu persatu atom klor, sehingga reaksi lebih lanjut dihasilkan asam oksalat yang akan terurai lebih lanjut menjadi C02, ion klor dan H20.Pengukuran asam-asam organik yang terbentuk
satu sama lain. Jadi diasumsikan bahwa hasil penguraian PCP berupa senyawa bersifat asam yaitu asam oksalat. Pada dosis 0,5 kGy asam oksalat meningkat dengan tajam, kemudian menurun pada dosis 2 kGy disajikan pada Gambar 15. Penurunan ini diduga karena asam oksalat yang terbentuk terurai menjadi COz dan H20. Mekanisme reaksi pada proses fotolisis menurut Wong dan Crosby dalam Anonim 1987 digambarkan sebagai berikut:
CI
HO CJ sederhana
C1 OH 0 0
PCP
0 H C I 0 0
Pada proses fotolisis tersebut yang terjadi ialah putusnya atom klor yang digantikan oleh gugus hidroksil. Ada tiga tipe penguraian PCP, yaitu
a. PCP terurai menjadi fenol terklorinasi rendah biasanya 2,3.4.6- dan 2,3,5,6- tetraklorofenol bercampur dengan triklorofenol.
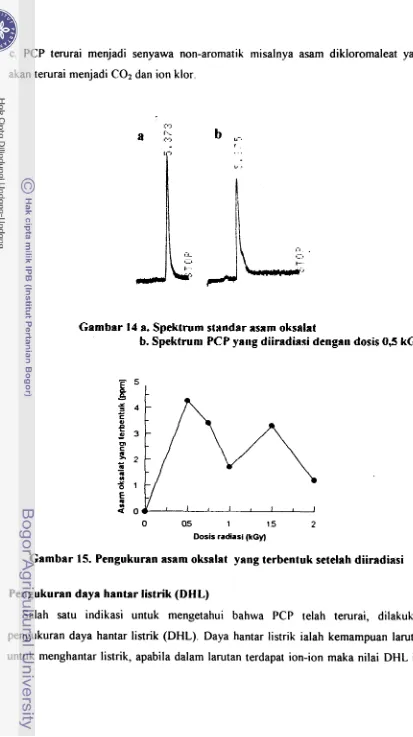
c. PCP terurai menjadi senyawa non-aromatik misalnya asam dikloromaleat yang akan terurai menjadi COz dan ion klor.
Gambar 14 a. Spektrum standar asam oksalat
b. Spektrum PCP yang diiradiasi dengan dosis 0,5 kGy
0 Cl5 1 15 2 Dosis radiasi (kGy)
Gambar 15. Pengukuran asam oksalat yrng terbentuk setelah diiradirsi
Pengukuran daya hantar listrik (DH L)
akan naik. Hasil pengukuran daya hantar listrik dapat dilihat pada Gambar 16, pada awal radiasi (0 kGy) terlihat bahwa nilai DHL sebesar 15 pS/cm. Setelah diiradiasi nilai DHL meningkat dengan tajam pada dosis 0,75 kGy sebesar 29 pS/cm, kemudian menurun dan naik kembali pada dosis 2 kGy menjadi 21 pS/cm. Peningkatan nilai DHL pada dosis 0,75 dan 1 kGy membuktikan adanya spesi selain asam oksalat yang mampu menghantar Iistrik. Data ini menunjukkan bahwa molekul PCP telah terurai.
: I , , , ,
0
0 a5 1 1.5 2
Dosis radiasi (kGy)
Gambar 16. Pengukuran daya hantar listrik PCP setelah diiradiasi
Pengukuran klor yang terbentuk
Pengukuran klor setelah radiasi dilakukan dengan menggunakan spektrofotometer uv-vis pada panjang gelombang 460 nm. Larutan PCP hasil radiasi direaksikan dengan Hg(SCN)z dan ~ e j ' . Pengukuran klor dilakukan dengan cara tidak langsung karena yang diukur bukan serapan klor melainkan serapan Fe(SCN), Adapun reaksi yang te jadi adalah
Hg(SCN)z + 2 CI-
---+
HgClz+
2 S C N 3 S C N+
~ e "---+
FFe(CN)lProses deklorinasi PCP menunjukkan putusnya satu atau dua atom klor yang
digambarkan oleh Wu* ( 1 999) sebagai berikut :
$
'OHcQ;
CI
'
P-H+
-
H
J
$
CIc
'
ICI + H+
c
ICI
c@ ct
&I@
CIC
CI
/ CI 0 .
CI CI C I C I
c@l
*Wu J, Yongke He, Xingwang F. 1999. Komunikasi pribadi. Remediation of drinking
Pengukuran PCP setelah radiasi
PCP sebelum dan sesudah diiradiasi dianalisis dengan menggunakan HPLC, hasil pengukuran dapat dilihat pada Gambar 18. Konsentrasi PCP dalam larutan makin menurun dengan meningkatnya dosis radiasi. Proses penguraian PCP 'dapat te rjadi karena putusnya atom klor, ha1 ini terjadi karena adanya pertukaran klor dengan gums hidroksil. Bila penurunan konsentrasi PCP dalam larutan dihubungkan dengan intensitas serapan seperti terlihat dalam Gambar 19 maka turunnya serapan pada panjang gelombang 220, 250, dan 320 nm menunjukkan konsentrasi PCP makin
tunm. Penurunan intensitas pada panjang gelombang 220, 250, dan 320 nm
menunjukkan bahwa molekul PCP telah terurai. Konsentrasi PCP dalam larutan setelah diiradiasi pada dosis 2 kGy sebesar 1,7 ppm dari PCP awal 10 ppm artinya sebanyak 83% PCP telah terurai.
t-
I
am:l&'
' '2;o' 'A '
.' 4
'.+'
'%!!iie-'-i.'
' ' ' '-
[image:121.520.28.490.23.713.2]Panjang gelombang (nm)
Gambar 18. Pengukuran konsentrasi Gambar 19. Spektrum PCP setelah
KESIMPULAN
Dari hasil penelitian dapat disimpulkan bahwa PCP dapat diuraikan dengan sinar gamma, pada dosis dan laju dosis yang rendah. Pada penelitian ini dosis optimum yang dapat dipakai adalah 2 kGy dan laju dosis 0,s kGyIjam dengan persentase penguraian yang dapat dicapai sebesar 83%. Penguraian PCP sangat tergantung pada pH larutan. Dari berbagai variasi pH yang diteliti menunjukkan bahwa proses penguraian optimum pada pH 7. Berdasarkan data daya hantar listrik (DHL) dan pH menggambarkan hasil penguraian PCP merupakan senyawa ion yang bersifat asam. Selanjutnya kromatograrn HPLC menunjukkan adanya asam oksalat dalam hasil penguraian tersebut.
SARAN
DAFTAR PUSTAKA
Andayani W, Sumartono A, Armanu. 1993. Pengaruh Iradiasi Gamma pada Penguraian Fen01 dalam air. Risalah Pertemuan Ilmiah Aplikasi Isotop dan Radiasi dalam Bidang Industri, Pertanian dan Lingkungan Badan Tenaga Atom Nasional Jakarta 14- 1 5 Desember.
Anonim. 1987. Environmental Health Criteria 71: Pentachlorophenol World Health Organization (WHO) Geneva.
Fang Xingwang, Yongke He, Jun Liu, Jilan Wu. 1998. Oxidative decomposition of pentachlorophenol in aqueous solution. Radiat Phys aitd Chem 53:4 1 1-4 1 5.
Getoff N, Solar S. 1986. Radiolysis and pulse radiolysis of chlorinated phenols in aqueous solution. Radial Phys Chem 28:443-450.
Getoff N. 1993.Purification of drinking water by irradiation. A Review. Proc Indian Acad Sci 105:373-391.
Harnly ME, Petreas MX, Flattery J, Goldman LR. 2000. Polichlorinated dibenzo-p- dioxin and polychlorinated dibenzofbran contamination in soil and home produced chicken eggs near pentachlorophenol sources. Environ. Sci Tech 34: 1 143-1 149.
Hayes WJ Jr, Caws ER Jr. 1991. Haildbook of I'esticide Toxicololy Tokyo: Academic.
He Yongke, Jun Liu, Jilan Wu. 2001. Gamma radiation treatment of pentachlorophenol, 2,4-dichlorophenol and 2-chlorophenol in water. Wina: International Atomic Energy Agency Tecdoc.
Ho Te-Fu L, Bolton JR. 1998. Toxicity changes during the UV treatment of pentachlrophenol in dilute aqueous solution. Wat Res. 32:489-497.
James WM, Ramamoorthy S. 1984. Orgattic (Ihemicals in Nafrrral Waters Applied
Monitoring and Impact Assessment Tokyo.
Khodadoust AP, Suidan MT, Sorial GA, Dionysiou DD, Brenner RC. 1999 Desorption of pentachlorophenol from soils using mixed solvents. ICnviroi~ , . I
Ikch. 33:4483-4491.
Magar VS, Stensel HD, Puhakka JA, Fergusson J F 1999. Sequential anaerobic dechlorination of pentachlorphenol: Competitive inhibition effects and a kinetic model. litn~iroti Sci 'ltchtlol. 33: 1604- 16 1 1 .
Meister RT. 1985. Farm Chemicals Handbook. Meister Publishing Co C48.
Mills G and Hoffmann R. 1993. Photocatalytic degradation of pentachlorophenol on Ti02 particles: Identification of intermediates and mechanism of reaction. Ltlvirott Sci Techrtol. 27: 168 1
-
1689.Miyata T. 1993. Liquid wastes-chemistry, Department of Environment and Resources. UNDPtIAEAIRCA, Regional Training on Radiation Technology for Environment Conservation. Takasaki Radiation Chemistry Research Establishment J AERI Japan.
Nickelsen MG, Cooper WJ. 1992. Removal of benzene and selected alkyl-substituted benzenes fiom aqueous solution utilizing continous high-energy electron irradiation. Etwirot~ ,Sct Tech. 26: 144- 1 5 1.
Nickelsen MG, Cooper WJ, Lin K, Kurucz CN,Waite TD. 1994. High energy electron beam generation of oxidants for the treatment of benzene and toluene in the presence of radical scavengers. Wat Nes. 28: 1227- 1237.
O'Donnel JH, Sangster DF. 1969. Pritncipfe.~ of l<adtatiotn CXemislry. London Edward Arnold (Publishers) Ltd.
Quint RM, Park HR, Krajnik P, Solar S, Getoff N, Sehested K. 1996, Gamma radiolysis and pulse radiolysis of aqueous 4-chloroanisole. Kadiat.Phys.Chem.
471835-845.
Sawai T. 1995. Decomposition of organic wastes in UNDP/lAEA/RCA Regional Training Course on Application of Radiation Processing for Decontamination of Liquid Wastes Takasaki Radiation Chemistry Research Establishment JAERl Japan.
Silverstein RM, Bassler
GC,
Morriel TC. 198 1. ,S/)ectrome/ric Jdetntlficatiotn cfOrgatnic ('omptrrlds .Singapore John Wi ley Sons.
S pinks J
WT,
WoodsRJ.
1 976. Atn It~trodttctiot~ to I<~~diutiotr ( 'hrmi.stry. John Wi ley& Sons. 2nd edition.
Weavers. LK, Malmstadt N, Hofmann MR. 2000. Kinetics and mechanism of pentachlorphenol degradation by sonification, ozonation, and sonolytic ozonation,
LAMPIRAN 1
Absorban PCP 10 ppm setelah diiradiasi pada pH
5,
laju dosis 1 kGy/jamDosis radiasi (kGy) Absorban
Dosis radiasi (kGy) 220 nm 250 nm 320 nm
0 1,650 0,3 64 0,178
0,s 1,515 0,329 0,153
0,75 1,522 0,338 0,152
1
,o
1,52 1 0,289 0,1241,5 1,650 0,25 1 0,097
2,o 1,867 0,244 0,086
Absorban PCP 10 ppm setelah diiradiasi pada pH 6, laju dosis 1 kGy/jam
Dosis radiasi (kGy) Absorban
Absorban PCP 10 ppm setelah diiradiasi pada pH 7, laju dosis 1 kGyIjam
Dosis radiasi ( k ~ ~ ) Absorban
Dosis radiasi (kGy) 220 nm 250 nm 320 nm
LAMPIRAN 4
Absorban PCP 10 ppm setelah diiradiasi pada pH 8, laju dosis 1 kGy/jam
Dosis radiasi (kGy) Absorban
Dosis radiasi (kGy) 220 nm 250 nm 320 nm
0 1,750 0,389 0,193
0-5 1,682 0,362 0,170
0,75 1,589 0,349 0,16 1
I,o 1,558 0,342 0,157
1,5 1,476 0,302 0,132
LAMPIRAN 5
Data persentase penguraian pada variasi laju dosis
Dosis radiasi (kGy) Persentase penguraian (%)
Laju dosis 0,s kGy1jam Laju dosis 1 kGyIjam
LAMPIRAN 6
Absorban
PCP
dengan konsentrasi 2 ppm, pH 7 iaju dosis 0,5 kGy/jamDosis radiasi (kGy) Absorban
Dosis radiasi (kGy) 220 nm 250 nm 320 nm
0 0,430 0,112 0,053
075 0,359 0,093 0,04 1
0,75 0,330 0,088 0,040
I
,o
0,294 0,080 0,0341,5 0,295 0,094 0,04 1
LAMPIRAN 7
Absorban
PCP
dengan konsentrasi 4 ppm, pH 7 laju dosis 0,5 kGy/jamDosis radiasi (kGy) Absorban
Dosis radiasi (kGy) 220 nm 250 nm 320 nm
Absorban PCP dengan konsentrasi 8 ppm, pH 7 laju dosis 0,5 k(iy/jam
Dosis radiasi ( k e y ) Absorban
LAMPIRAN 9
Absorban PCP dengan konsentrasi 10 ppm, pH 7 laju dosis 0,5 kGy/jam
Dosis radiasi (kGy) Absorban
Dosis radiasi
(kGy)
220 nm 250 nm 320nm
LAMPIRAN 10
Pengukuran perubahan pH larutan PCP dengan pH awal 7, 10 ppm laju dosis I
kGyIjam
Dosis (kGy) Perubahan pH <