SINTESIS ZEOLIT P1 DAN NANOKOMPOSIT ZEOLIT P1/TiO
2DARI ABU TERBANG BATU BARA DAN SEKAM PADI SERTA
UJI KEMAMPUAN ADSORPSI DAN FOTODEGRADASINYA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUANALAM INSTITUT PERTANIAN BOGOR
2013
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Sintesis Zeolit P1 dan Nanokomposit Zeolit P1/TiO2 dari Abu Terbang Batu bara dan Sekam Padi serta
Uji Kemampuan Adsorpsi dan Fotodegradasinya adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Februari 2013
Ade Irawan
ABSTRAK
ADE IRAWAN. Sintesis Zeolit P1 dan Nanokomposit Zeolit P1/TiO2 dari Abu
Terbang Batu Bara dan Sekam Padi serta Uji Kemampuan Adsorpsi dan Fotodegradasinya. Dibimbing oleh SRI SUGIARTI dan ETI ROHAETI.
Abu terbang merupakan limbah dari pembangkit listrik tenaga uap (PLTU) batu bara yang memiliki kandungan silika dan alumina yang cukup tinggi. Sekam merupakan limbah dari penggilingan padi yang mengandung kandungan silika yang tinggi. Campuran keduanya berpotensi membentuk zeolit. Pada penelitian ini zeolit berhasil disintesis menggunakan metode hidrotermal. Zeolit yang dihasilkan merupakan zeolit tipe P1. Selain itu, untuk meningkatkan karakternya, zeolit sintetis dibuat menjadi nanokomposit Zeolit-TiO2 sehingga dihasilkan material baru yang
memilki sifat adsorpsi-fotodegradasi. Nanokomposit yang telah disintesis memiliki kemampuan adsorpsi-fotodegradasi karena mampu mendegradasi biru metilena di bawah sinar ultraviolet. Optimisasi adsorpsi biru metilena oleh zeolit dan nanokompositnya menghasilkan konsentrasi optimum adsorbat sebesar 300 ppm dan waktu agitasi optimum selama 3 jam untuk kedua adsorben, serta bobot optimum adsorben pada 80 dan 10 mg masing-masing untuk zeolit dan nanokompositnya. Pola isoterm adsorpsi kedua adsorben mengikuti pola Langmuir sehingga dapat diasumsikan bahwa adsorben memiliki permukaan yang homogen sehingga proses adsorpsi membentuk satu lapisan tunggal saat adsorpsi maksimum.
Kata kunci: abu terbang, fotodegradasi, nanokomposit zeolit-TiO2, sekam padi, zeolit
sintesis.
ABSTRACT
ADE IRAWAN. Synthesis of Zeolite P1-type and Nanocomposite Zeolie P1/TiO2
from Rice Husk and Coal Fly Ash and Their Adsorption and Photodegradation Tests Capabilities. Supervised by SRI SUGIARTI and ETI ROHAETI.
Fly ash is a waste of coal power plant with high content of silica and alumina. Husk is a waste of rice mill containing a high amount of silica. Mixture of both materials is potential to form zeolites. In this study, zeolites have been synthesized using hydrothermal method. The resulting zeolite is a P1-type zeolite. In addition, to improve their chemical characteristic, the synthetic zeolite was mixed with TiO2 to
give nanocomposite zeolite-TiO2 new materials that have
adsorption-photodegradation properties. The synthesized-nanocomposites showed to adsorptive-photocatalytic properties due to their capabilities in degrading methylene blue under ultraviolet light radiation. Optimization adsorption of methylene blue by the zeolites and nanocomposites resulted in optimum adsorbate concentration of 300 ppm, and optimum agitation time of 3 hours for both adsorbents, and the optimum adsorbent weight at 80 and 10 mg for zeolites and zeolite nanocomposite respectively. The adsorptions system followed Langmuir pattern isotherm for both adsorbents, therefore it can be assumed that both adsorbents have homogeneous surface and that the process of adsorption occurs as a single layer at the maximum adsorption.
Keywords: fly ash, nanocomposite zeolite-TiO2, photodegradation, rice huks,
ADE IRAWAN
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
2013
SINTESIS ZEOLIT P1 DAN NANOKOMPOSIT ZEOLIT P1/TiO
2Judul Skripsi : Sintesis Zeolit P1 dan Nanokomposit Zeolit P1/TiO2 dari Abu
Terbang Batu Bara dan Sekam Padi serta Uji Kemampuan Adsorpsi dan Fotodegradasinya
Nama : Ade Irawan NIM : G44080071
Disetujui,
Dr Sri Sugiarti, PhD Dr Eti Rohaeti, MS Pembimbing I Pembimbing II
Diketahui,
Prof Dr Ir Tun Tedja Irawadi, MS Ketua Departemen
PRAKATA
Segala puji dan syukur penulis panjatkan kepada Allah SWT sehingga penulis bisa menyelesaikan karya ilmiah ini. Penelitian ini dimulai dari bulan Maret sampai September 2012 bertempat di Laboratorium Kimia Anorganik, Laboratorium Kimia Analitik, dan Laboratorium Bersama, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Penulis mengucapkan terima kasih kepada Ibu Dr Sri Sugiarti, PhD selaku pembimbing satu dan Ibu Dr Eti Rohaeti, MS selaku pembimbing dua atas dukungan dan masukan yang senantiasa diberikan kepada penulis selama penelitian dan penyusunan karya ilmiah ini. Ucapan terima kasih disampaikan kepada Pak Syawal, Nurul, Pak Mulyadi, Pak Sunarsa dan Pak Eman selaku laboran yang telah banyak membantu penulis dalam pengerjaan penelitian.
Ucapan terima kasih kepada Linda Trivana, Evan, dan teman teman kimia 45 yang telah meluangkan waktunya untuk menemani penulis ketika harus mengerjakan penelitian di malam hari. Ucapan terima kasih kepada Pak Dikdik, dan Pak Ahmad atas kerja samanya untuk analisis XRD dan mikroskop elektron payar(SEM) di Balitbang kehutanan, Bogor.
Bogor, Februari 2013
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
METODE 3
Bahan dan Alat 3
Lingkup Kerja 3
HASIL DAN PEMBAHASAN 6
Sintesis dan Pencirian Natrium Silikat 6 Aktivasi dan Pencirian Abu Terbang Batu Bara 7 Sintesis dan Pencirian Zeolit Sintesis 10 Sintesis dan Pencirian Nanokomposit 12
Optimisasi Adsorpsi 14
Isoterm Adsorpsi 16
Uji Fotodegradasi 16
SIMPULAN DAN SARAN 18
Simpulan 18
Saran 18
DAFTAR PUSTAKA 18
LAMPIRAN 21
DAFTAR TABEL
1 Kode sampel pembuatan zeolit 5
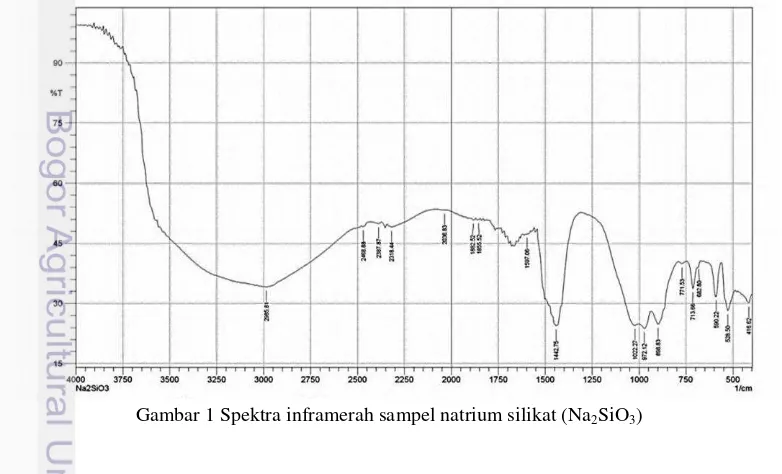
2 Interpretasi spektra inframerah sampel natrium silikat (Na2SiO3) 7
3 Puncak-puncak utama 2θ pada abu terbang dan Interpretasi fase 8
4 Puncak-puncak utama 2θ pada zeolit sintetis dan tipe produk 13
5 Nilai linearitas isoterm adsorpsi 16
6 Nilai konstanta Xm 16
DAFTAR GAMBAR
1 Spektra inframerah sampel natrium silikat (Na2SiO3) 6
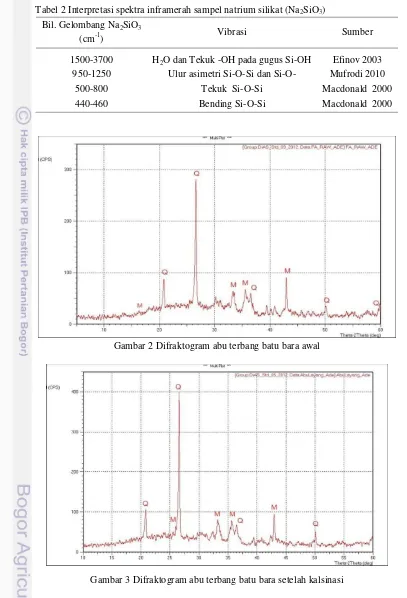
2 Difraktogram abu terbang batu bara awal 7
3 Difraktogram abu terbang batu bara setelah kalsinasi 7
4 Difraktogram abu terbang batu bara setelah kalsinasi dan refluks 8
5 Morfologi permukaan abu terbang perbesaran 1000x 9
6 Morfologi abu terbang setelah kalsinasi perbesaran 1000x 9
7 Morfologi abu terbang setelah kalsinasi dan refluks HCl perbesaran 1000x 9
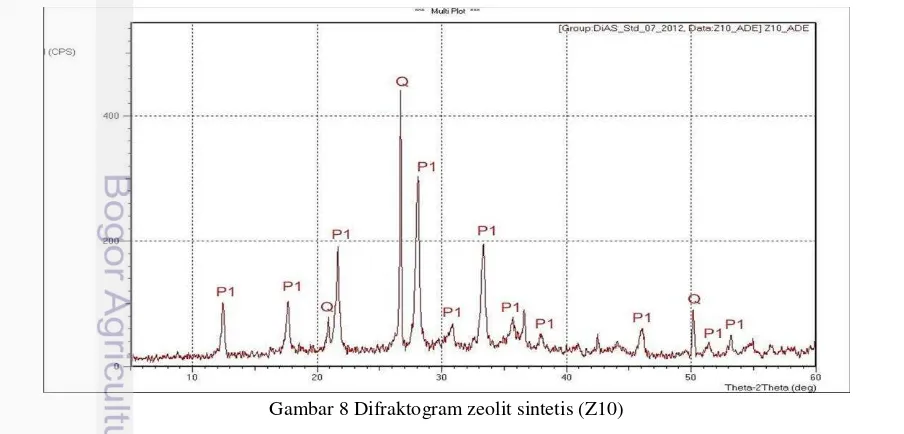
8 Difraktogram zeolit sintetis (Z10) 10
9 Difraktogram zeolit sintetis (Z9) 11
10 Morfologi permukaan Z9 perbesaran 7500x 11
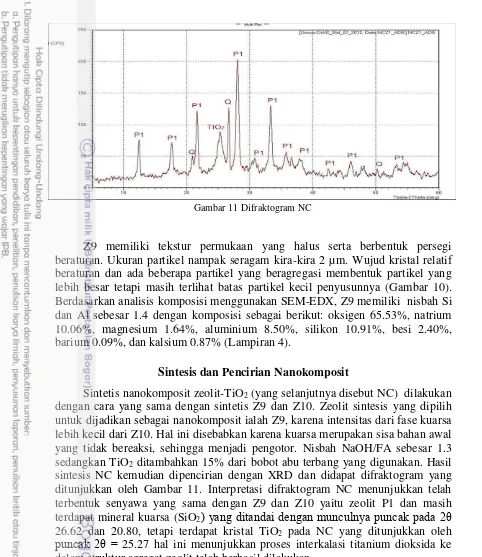
11 Difraktogram NC 12
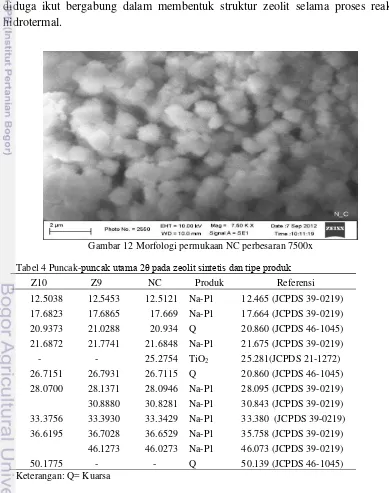
12 Morfologi permukaan NC perbesaran 7500x 13
14 Optimisasi waktu agitasi adsorpsi oleh Z9 dan nanokomposit (NC) 15
15 Optimisasi bobot adsorben adsorpsi oleh Z9 dan nanokomposit (NC) 15
16 Filtrat hasil uji fotokatalisis tanpa radiasi UV 17
17 Filtrat hasil uji fotokatalisis dengan radiasi UV 17
DAFTAR LAMPIRAN
1 Diagram alir penelitian 21
2 Komposisi Natrium silikat 22
3 Komposisi abu terbang batu bara 23
4 Komposisi Z9 24
5 Komposisi NC 25
6 Optimisasi konsentrasi adsorpsi biru metilena 26
7 Optimisasi waktu agitasi adsorpsi biru metilena 28
8 Optimisasi bobot adsorben terhadap adsorpsi biru metilena 30
9 Isoterm adsorpsi biru metilena oleh Z9 dan nanokomposit (NC) 31
10 Hasil uji fotokatalisis 34
PENDAHULUAN
Abu Terbang merupakan salah satu hasil samping pembakaran batu bara yang dihasilkan dari pembangkit listrik tenaga uap (PLTU), yang terutama tersusun atas oksida-oksida dari senyawa anorganik. Jumlah dan karakteristik abu yang dihasilkan sangat ditentukan oleh jenis batu bara dan sistem pembakaran yang digunakan. Abu batu bara merupakan materi sisa yang ada setelah semua materi yang dapat bakar pada batu bara telah habis terbakar. Oleh karena itu, abu batu bara merupakan campuran yang kompleks sebagai hasil perubahan kimia komponen batu bara yang berlangsung selama pembakaran. Berdasarkan ukuran partikelnya abu batu bara dapat dibedakan menjadi dua macam, yaitu abu terbang (fly ash) dan abu dasar (bottom ash) (Jumaeri 2007).
Hasil analisis kandungan mineral menunjukkan abu terbang mengandung oksida-oksida logam termasuk logam-logam berat dalam jumlah kecil. Oksida utama dari abu terbang batu bara adalah silika (SiO2), alumina (Al2O3) dan besi
(Fe2O3). Keberadaan komponen silika dan alumina memungkinkan abu terbang
dimanfaatkan sebagai sumber silika dan alumina dalam sintesis zeolit (Mufrodi 2010).
Zeolit merupakan senyawa aluminosilikat terhidrasi yang memiliki kerangka struktur tiga dimensi dan merupakan padatan kristalin dengan kandungan utama silikon, aluminium, dan oksigen serta dapat mengikat sejumlah molekul air di dalam porinya. Zeolit ada dua macam, yaitu zeolit alam dan zeolit sintetik. Zeolit alam semakin banyak dimanfaatkan sehingga jumlahnya semakin berkurang dan sifat-sifat zeolit alam sangat terbatas maka dilakukan sintesis zeolit untuk mensubstitusi zeolit yang berasal dari alam. Umumnya, zeolit alam seperti mordenite memiliki diameter pori 3.0-6.2 Å (Breck 1974) sehingga kemampuan sebagai penyaring atau pemisah terhadap molekul-molekul yang berukuran besar sangat terbatas, oleh karena itu dilakukan sintesis zeolit. Zeolit sintetik merupakan zeolit yang dibuat untuk mendapatkan sifat tertentu. Zeolit sintesis dikembangkan untuk mengatasi kelemahan dari zeolit alam, antara lain dengan mengatur pori-porinya sehingga lebih spesifik pemanfaatannya. Zeolit mempunyai muatan parsial negatif, ukuram pori yang seragam, dan memiliki luas permukaan yang besar sehingga telah dimanfaatkan sebagai adsorben, penyaring molekul, katalis, dan bahan baku detergen(Thammavong 2003, Das 2011).
Zeolit P1 merupakan salah satu tipe zeolit sintetik. Umumnya, sintesis zeolit P1 dari abu terbang menggunakan metode alkali hidrotermal, akan tetapi zeolit yang dihasilkan merupakan campuran dari berbagai jenis zeolit sintetik seperti zeolit A, P1, faujasit, Y, sodalit, dan hidroksi sodalit, Sedangkan dengan metode leburan alkali-hidrotermal menghasilkan zeolit A, faujasit, atau zeolit X secara selektif. Disebabkan oleh nisbah Si/Al pada zeolit P1 sebesar 1.7, dengan demikian untuk mendapatkan zeolit P1 secara selektif diperlukan penambahan silika dari sumber lain. Sumber silika lain yang memiliki potensi adalah sekam padi (Zhang et al. 2007; Sutarno et al.2010).
2
sekam padi yang kurang tepat akan menimbulkan pencemaran terhadap lingkungan. Sekam padi mengandung 78-80% bahan organik yang mudah menguap (lignin, selulosa, gula) jika sekam dibakar dan dihasilkan sisa pembakaran berupa abu sekitar 20-22% (Warsito et al. 2006). Kandungan silika
(SiO2) dalam abu sekam padi berkisar antara 90-99%, selain itu terdapat sejumlah
kecil alkali dan logam pengotor. Kandungan silika yang tinggi pada abu hasil pembakaran sekam padi menjadi alasan utama pemanfaatannya menggantikan sumber silika lain yang lebih mahal, selain itu mudah didapat (Aina 2007 ; Putro & Prasetyoko 2007).
Modifikasi dengan mengonversi abu terbang dan abu sekam padi menjadi zeolit P1, diharapkan dapat menambah potensinya sebagai adsorben zat warna, karena rangka aluminosilikat pada zeolit menjadi lebih bermuatan positif dan akan menambah kapasitas adsorpsi adsorben tersebut. Konversi abu terbang batu bara dan abu sekam padi menjadi zeolit dapat diperoleh melalui reaksi hidrotermal dalam suasana basa (Musyoka et al. 2009).
Dalam penelitian yang dilakukan sebelumnya, pengolahan limbah zat warna dilakukan dengan metode adsorpsi. Kelemahan metode ini adalah selektivitasnya yang rendah terutama untuk limbah yang berbentuk cair. Kelemahan metode ini dapat diperbaiki melalui gabungan metode adsorpsi-fotodegradasi. Dalam metode ini, senyawa organik diadsorpsi oleh permukaan padatan yang sekaligus mampu mendegradasi senyawa organik. Degradasi sempurna menghasilkan CO2 dan H2O
yang aman bagi lingkungan sehingga mengurangi faktor regenerasi (Fatimah &
Wijaya 2005).
Penelitian sebelumnya, Hediana (2011) berhasil mensintesis nanokomposit sodalit-TiO2 dan terbukti memiliki kemampuan adsorpsi dan fotodegradasi
terhadap zat warna biru metilena. Selain itu, nanokomposit yang dihasilkan tersebut memiliki daya jerap yang lebih besar daripada sodalit.
Pada penelitian ini telah dilakukan sintesis, pencirian, dan optimisasi adsorpsi zeolit sintetis maupun nanokomposit zeolit sintetis-TiO2. Optimisasi
adsorpsi dilakukan terhadap parameter konsentrasi adsorbat, waktu agitasi, dan bobot adsorben. Adanya aktivitas fotokatalisis pada sampel nanokomposit diketahui melalui uji fotodegradasi. Zeolit yang terbentuk merupakan tipe P1 sehingga memiliki kemampuan adsorpsi lebih tinggi dari penelitian Hediana (2011).
Perumusan Masalah
Tujuan Penelitian
Penelitian ini bertujuan mensintesis zeolit dan nanokomposit zeolit-TiO2
menggunakan sekam padi sebagai sumber silika dan abu terbang batu bara sebagai sumber silika dan alumina, melakukan pencirian zeolit hasil sintesis dengan spektroskopi XRD dan SEM-EDX, serta uji adsorpsi terhadap zat warna biru metilena dan fotodegradasinya.
Manfaat Penelitian
Penelitian ini bermanfaat untuk meningkatkan nilai tambah pada abu terbang batu bara dan sekam padi melalui pembentukan zeolit dan nanokomposit zeolit/TiO2 yang bermanfaat sebagai adsorben serta bahan yang bersifat
fotokatalis.
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Maret sampai September 2012 di Laboratorium Anorganik Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Hipotesis
Zeolit P1 dapat disintesis dari bahan dasar sekam padi dan abu terbang batu bara melalui metode peleburan alkali dilanjutkan dengan reaksi hidrotermal. Modifikasi zeolit P1 menjadi nanokomposit zeolit P1/TiO2 mampu mengadsorpsi
dan mendegradasi zat warna biru metilena.
METODE
Bahan dan Alat
Bahan-bahan yang digunakan antara lain sekam padi dari desa Setu gede Bogor, abu terbang dari PLTU Suralaya, NaOH dari merk. Hasil-hasil dalam pekerjaan ini dianalisis menggunakan , fourier transform infra red (FTIR) merek
Bruker, spektrofotometer UV-Vis merek Shimazu, XRD merek Shimazu dan SEM-EDX meek Bruker.
Lingkup Kerja
Penelitian ini terdiri atas 4 tahap (Lampiran 1). Tahap pertama mencakup sintesis silika dari abu sekam padi. Tahap kedua sintesis zeolit dan sintesis nanokomposit zeolit-TiO2. Tahap ketiga Pencirian zeolit hasil sintesis dan tahap
4
Sintesis Natrium Silikat dari Abu Sekam Padi (Mujiyanti et al. 2010)
Sintesis natrium silikat dari abu sekam padi meliputi tahapan penyiapan abu dan tahapan reaksi dengan NaOH. Abu sekam padi disiapkan dengan cara sekam padi dicuci bersih kemudian dikeringkan dibawah sinar matahari. Setelah sekam kering, kemudian dilakukan proses pengarangan dan pengabuan dengan cara sekam padi dibakar dalam keadaan menumpuk. Abu sekam padi yang dihasilkan kemudian diabukan kembali dengan menggunakan tanur pada suhu 600ºC selama 1 jam. Abu sekam padi digerus dan diayak sehingga diperoleh serbuk abu sekam padi yang lolos pada ayakan 200 mesh. Abu sekam padi yang diperoleh kemudian dicuci dengan HCl 3%. Abu sekam padi dimasukkan ke dalam gelas piala. lalu dicampur dengan HCl 3% (hasil pengenceran HCl 37%), yaitu 10 ml untuk 1 g abu sekam, kemudian dipanaskan di atas penangas pada suhu 200ºC, disaring dan dinetralkan dengan akuades. Hasil pencucian dikeringkan dalam oven.
Tahapan terakhir sintesis natrium silikat ialah mereaksikan abu sekam padi dan larutan NaOH. Abu sekam padi bersih kemudian ditambahkan 82,5 ml NaOH 4 M, lalu dididihkan sambil diaduk dengan pengaduk magnet. Setelah agak kering, larutan dituangkan ke dalam cawan porselin dan dileburkan pada suhu 500ºC selama 30 menit. Padatan yang dihasilkan merupakan natrium silikat (Na2SiO3) dan didinginkan. Natrium silikat (Na2SiO3) berbentuk padatan
berwarna putih kehijauan. Natrium silikat yang dihasilkan dilalukan pencirian menggunakan FTIR dan SEM-EDX untuk mengetahui hasil sintesis.
Sintesis Zeolit
Sintesis zeolit dilakukan berdasarkan prosedur Ojha(2004) dengan beberapa modifikasi. Sampel abu terbang ditimbang sebanyak 5 gram lalu dimasukkan ke dalam cawan kemudian dikalsinasi untuk menghilangkan karbon yang tidak terbakar pada 800ºC selama 2 jam. Setelah dikalsinasi, sampel abu terbang direfluks dengan HCl untuk meminimalkan pengotor dan meningkatkan aktivitas zeolit.
Selanjutnya abu terbang dicampur dengan NaOH. Nisbah NaOH terhadap abu terbang (berdasarkan bobot) ialah sebesar 1 dan 1.3 (Ojha 2004). Setiap campuran tersebut kemudian dimasukkan ke dalam tanur pada suhu 550ºC selama 1 jam. Campuran leburan yang dihasilkan kemudian didinginkan sampai suhu kamar, dan ditambahkan 0.9 g natrium silikat (Na2SiO3) kemudian ditambahkan
50 mL air suling lalu diaduk menggunakan pengaduk magnet selama beberapa jam. Tahap ini disebut proses ageing. Setelah proses ageing selesai, dilanjutkan
dengan proses hidrotermal dengan menempatkan campuran ke dalam botol PP di dalam oven pada suhu 90 ºC selama 24 jam. Setelah itu sampel dibilas dengan air suling hingga filtratnya memiliki pH 9-10 dan selanjutnya sampel dikeringkan. Produk padat yang diperoleh dilakukan pencirian dengan XRD dan SEM-EDX.
Sintesis Nanokomposit Zeolit/TiO2
Sintesis nanokomposit zeolit/TiO2 dilakukan dengan cara yang sama dengan
sintesis zeolit. Komposisi NaOH/Abu terbang dipilih dari hasil sintesis terbaik. TiO2 ditambahkan sebelum dilakukan ageing sebanyak 15% dari bobot abu
5
Tabel 1 Kode sampel pembuatan zeolit Kode
Penentuan Konsentrasi Optimum untuk Uji Adsorpsi
Larutan biru metilena (MB) dibuat dengan konsentrasi yang bervariasi, yaitu 100, 150, 200, 250, 300, dan 350 mg/l. Zeolit atau nanokomposit ditimbang sebanyak 50 mg, kemudian ditambahkan 15 ml larutan MB dari setiap konsentrasi dalam tabung reaksi yang berbeda dan dikocok selama 2 jam. Setelah itu, campuran dipisahkan dengan sentrifuga dan filtratnya dilakukan pengukuran konsentrasi MB dengan spektrofotometer UV-Vis. Kapasitas adsorpsi dihitung dengan menggunakan persamaan berikut:
Q = o- a
Keterangan:
Q = Kapasitas adsorpsi V = Volume larutan (L) Co = Konsentrasi awal (ppm) Ca = Konsentrasi akhir (ppm) M = Massa adsorben (g)
Penentuan konsentrasi optimum juga dilakukan pada sampel nanokomposit zeolit-TiO2 dengan perlakuan yang sama seperti zeolit.
Penentuan Waktu Agitasi Optimum untuk Adsorpsi
Sebanyak 50 mg sampel zeolit atau nanokomposit ditambahkan larutan biru metilena berdasarkan konsentrasi optimum yang diperoleh sebanyak 15 mL. Setelah itu, larutan kocok dengan variasi waktu 0.5, 1.0, 1.5, 2.0, 3.0, dan 4 jam. Setelah itu, larutan disentrifugasi selama 15 menit dengan kecepatan 3000 rpm untuk memisahkan endapan. Campuran kemudian diukur absorbannya menggunakan spektrofotometer UV-tampak pada panjang gelombang 664 nm.
Penentuan Bobot Adsorben Optimum untuk Adsorpsi
Uji Fotodegradasi Senyawa Biru Metilena
Sebanyak 100 mg nanokomposit Zeolit-TiO2 ditambahkan 15 mL larutan
biru metilena dengan konsentrasi 12.5 ppm. Larutan kemudian disinari dengan sinar UV pada panjang gelombang 365 nm selam 6 jam. Setelah itu, diambil filtratnya dan dilakukan analisis menggunakan spektrofotometer UV-tampak pada panjang gelombang 200–700 nm. Uji fotodegradasi juga dilakukan pada sampel Zeolit, dan TiO2 sebagai pembanding. Setelah itu, hasilnya dibandingkan dengan
perlakuan tanpa sinar UV.
HASIL DAN PEMBAHASAN
Sintesis dan Pencirian Natrium Silikat
Natrium silikat disintesis dari bahan awal berupa abu sekam padi yang direaksikan dengan NaOH. Natrium silikat yang dihasilkan dilakukan pencirian menggunakan SEM-EDX dan FTIR. Interpretasi FTIR (Gambar 1, Tabel 2)
menunjukkan gugus -OH pada natrium silikat hasil sintesis. Selain itu, terdapat serapan yang menunjukkan gugus Si-O seperti ditunjukkan pada Tabel 2. Komposisi natrium silikat dianalisis menggunakan SEM-EDX menunjukkan komposisi unsur yang terdapat dalam natrium silikat sintetis berdasarkan % atom terdiri atas oksigen 71.98 %, natrium 22.63%, dan silikon 5.39% (Lampiran 2). Berdasarkan data di atas, diperkirakan masih terdapat kelebihan NaOH yang tidak bereaksi dengan abu sekam padi dan Na2SiO3 yang dihasilkan menjerap H2O.
Berdasarkan SEM-EDX juga dapat disimpulkan proses pengabuan dan pencucian berhasil ditandai dengan tidak terdeteksinya unsur karbon dan oksida logam pengotor dari natrium silikat hasil sintesis.
7
Tabel 2 Interpretasi spektra inframerah sampel natrium silikat (Na2SiO3)
Bil. Gelombang Na2SiO3
(cm-1) Vibrasi Sumber
1500-3700 H2O dan Tekuk -OH pada gugus Si-OH Efinov 2003
950-1250 Ulur asimetri Si-O-Si dan Si-O- Mufrodi 2010
500-800 Tekuk Si-O-Si Macdonald 2000
440-460 Bending Si-O-Si Macdonald 2000
Gambar 2 Difraktogram abu terbang batu bara awal
8
Aktivasi dan Pencirian Abu Terbang Batu Bara
Proses pencirian menggunakan XRD dilakukan pada rentang sudut 2θ antara 5-60. Berdasarkan data difaktogram tersebut dapat dilihat komposisi abu terbang batu bara didominasi oleh senyawaan silikon dan aluminium yaitu terdeteksinya senyawa mullit, kuarsa, dan senyawa lain yang bersifat amorf. Keberadaan mineral silika dalam abu terbang diketahui dengan terbentuknya puncak pada 2θ sekitar 26.62 dan 20.80, sedangkan mineral mullit ditandai dengan munculnya puncak pada sudut sekitar 26.30 (Tabel 3). Hal ini memperkuat penelitian yang telah dilakukan sebelumnya tentang adanya senyawa silika dan mullit pada abu terbang batu bara (Jumaeri et al. 2007, Zakaria 2010).
Pengaruh kalsinasi dan refluks dengan HCl 3% terhadap abu terbang dapat dilihat pada difraktogram pada Gambar 3, 4, dan 5. Berdasarkan difraktogram, telah terjadi peningkatan kristalinitas dari abu terbang yang diberi perlakuan dibandingkan abu terbang awal. Abu terbang awal memiliki kristalinitas sebesar 57.69%, sedangkan yang telah diberi perlakuan memiliki kristalinitas 62.14% (kalsinasi) dan 73.57% (kalsinasi dan refluks). Kalsinasi menyebabkan fasa kristalin dari sampel meningkat, sedangkan refluks menyebabkan terlarutnya fasa amorf sehingga meningkatkan proposi fasa kristalin.
Gambar 4 Difraktogram abu terbang batu bara setelah kalsinasi dan refluks Tabel 3 Puncak-puncak utama 2θ pada abu terbang dan Interpretasi fase
Abu terbang
9
Gambar 5 Morfologi permukaan abu terbang perbesaran 1000x
Gambar 6 Morfologi abu terbang setelah kalsinasi perbesaran 1000x
10
Selain itu, abu terbang batu bara juga dipencirian dengan SEM. Berdasarkan hasil pencirian SEM abu terbang batu bara memiliki tekstur permukaan yang halus dan bentuk kristal bulat, dan kisaran diameter partikel berukuran 0,1µm-20.0µm (Gambar 5). Dari citraan SEM pada abu terbang yang kalsinasi dan abu terbang refluks (Gambar 6 dan 7) dapat dilihat bahwa telah terjadi penurunan sejumlah pengotor. Hal ini sejalan dengan hasil analisis XRD sebelumnya. Komposisi abu terbang dianalisis menggunakan SEM-EDX dengan hasil didominasi oleh atom oksigen 64.79%, natrium 0.22%, magnesium 0.85%, aluminium 14.66%, silikon 16.32%, besi 1.43%, barium 0.36%, dan kalium 1.36% (Lampiran 3). Dengan ada kandungan aluminium dan silikon menunjukkan abu terbang dapat digunakan sebagai bahan sintesis zeolit.
Sintesis dan Pencirian Zeolit Sintesis
Hasil pencirian zeolit sintetis menggunakan XRD dapat dilihat pada Gambar 8 dan 9. Berdasarkan difraktogram tersebut dapat dilihat bahwa telah terjadi perubahan signifikan dari difraktogram abu terbang. Hal ini dapat ditinjau dari jumlah puncak dan intensitas puncak yang dihasilkan. Z10 disintesis dengan nisbah NaOH/Abu Terbang sebesar 1 dan penambahan 0.9 g natrium silikat. Z10 dipencirian menggunakan XRD, menghasilkan difraktogram yang dapat dilihat pada Gambar 8. Berdasarkan data difraktogram menunjukkan Z10 merupakan zeolit tipe P1. Hal ini ditunjukkan dengan pola difraksi Z10 yang mirip dengan pola standar Zeolit P1 JCPDS nomor arsip 39-0219. Selain itu terdeteksi pula mineral kuarsa (SiO2) dengan masih adanya puncak disekitar 2θ 26,62 dan 20,80.
11
Z9 disintesis dengan nisbah NaOH/Abu terbang sebesar 1.3 dan penambahan 0.9 g natrium silikat. Z9 dipencirian menggunakan XRD dan SEM. Difraktogram Z9 dapat dilihat pada Gambar 9. Berdasarkan data difraktogram menunjukkan Z9 merupakan zeolit tipe P1. Hal ini ditunjukkan dengan pola difraksi Z9 yang mirip dengan pola standar Zeolit P1 JCPDS nomor arsip 39-0219. Selain itu terdeteksi pula mineral kuarsa (SIO2) dengan masih adanya
puncak disekitar 2θ 26.62 dan 20.80 . Z9 dan Z10 memiliki perbedaan pada intensitas puncak difraktogram yang dihasilkan. Intensitas puncak mineral kuarsa pada Z10 lebih tinggi dari Z9, hal ini disebabkan karena penambahan NaOH pada Z9 lebih banyak dari Z10, Sehingga dapat disimpulkan bahwa NaOH berperan penting untuk mendekomposisi mineral kuarsa agar ikut bergabung membentuk struktur zeolit. Pernyataan ini sesuai dengan hasil penelitian Fukui et al. (2006)
bahwa semakin banyak NaOH yang ditambahkan semakin kecil proposi abu terbang yang tidak bereaksi.
Gambar 9 Difraktogram zeolit sintetis (Z9)
12
Z9 memiliki tekstur permukaan yang halus serta berbentuk persegi beraturan. Ukuran partikel nampak seragam kira-kira 2 µm. Wujud kristal relatif beraturan dan ada beberapa partikel yang beragregasi membentuk partikel yang lebih besar tetapi masih terlihat batas partikel kecil penyusunnya (Gambar 10). Berdasarkan analisis komposisi menggunakan SEM-EDX, Z9 memiliki nisbah Si dan Al sebesar 1.4 dengan komposisi sebagai berikut: oksigen 65.53%, natrium 10.06%, magnesium 1.64%, aluminium 8.50%, silikon 10.91%, besi 2.40%, barium 0.09%, dan kalsium 0.87% (Lampiran 4).
Sintesis dan Pencirian Nanokomposit
Sintetis nanokomposit zeolit-TiO2 (yang selanjutnya disebut NC) dilakukan
dengan cara yang sama dengan sintetis Z9 dan Z10. Zeolit sintesis yang dipilih untuk dijadikan sebagai nanokomposit ialah Z9, karena intensitas dari fase kuarsa lebih kecil dari Z10. Hal ini disebabkan karena kuarsa merupakan sisa bahan awal yang tidak bereaksi, sehingga menjadi pengotor. Nisbah NaOH/FA sebesar 1.3 sedangkan TiO2 ditambahkan 15% dari bobot abu terbang yang digunakan. Hasil
sintesis NC kemudian dipencirian dengan XRD dan didapat difraktogram yang ditunjukkan oleh Gambar 11. Interpretasi difraktogram NC menunjukkan telah terbentuk senyawa yang sama dengan Z9 dan Z10 yaitu zeolit P1 dan masih terdapat mineral kuarsa (SiO2 yang ditandai dengan munculnya puncak pada 2θ
26.62 dan 20.80, tetapi terdapat kristal TiO2 pada NC yang ditunjukkan oleh
puncak 2θ = 25.27 hal ini menunjukkan proses interkalasi titanium dioksida ke dalam struktur agregat zeolit telah berhasil dilakukan.
Pembentukkan material baru dari abu terbang batu bara tidak selalu disertai dengan peningkatan kristalinitas. Kristalinitas abu terbang awal, abu terbang kalsinasi, abu terbang kalsinasi HCl, Z10, Z9, dan NC berturut-turut didapat sebesar 57.68%, 62.14%, 73.54%, 84.25%, 57.75%, dan 52.68%. Intensitas kristal kuarsa yang tinggi pada Z10 diduga menyumbang tingginya kristalinitas tersebut. Menurut West (1984), refleksi intensitas difraksi sinar-X mengindikasikan kesempurnaan kristal dan kerapatan atom dalam kristal. Semakin ramping refleksi intensitas suatu material maka kristalinitasnya semakin baik dengan susunan atom semakin rapat.
13
Hasil SEM kristal NC memiliki tekstur yang mirip seperti Z9. Ukuran kristal NC berkisar antara 1 µm lebih kecil dari Z9 yang berkisar antara 2 µm. Akan tetapi kristal NC lebih cenderung membentuk agregasi membentuk partikel yang lebih besar dari Z9 (Gambar 12). Hal ini mungkin disebabkan oleh TiO2
yang terdapat dalam NC.
Berdasarkan analisis komposisi menggunakan SEM-EDX, NC memiliki nisbah Si/Al mendekati 1 dengan komposisi sebagai berikut: oksigen 62.86%, natrium 7.31%, magnesium 0.97%, aluminium 10.47%, silikon 10.35%, besi 1.93%, titanium 4.03%, barium 1.11%, dan kalsium 0.97% (Lampiran 5). kandungan natrium dalam zeolit sintetis meningkat lebih dari 30 kali lipat dibandingkan abu terbang, sedangkan kalium tidak terdeteksi sehingga dapat disimpulkan bahwa ion Na menjadi penyeimbang muatan kerangka zeolit. Bentuk kristal Z9 dan NC relatif homogen namun tidak sempurna kemungkinan disebabkan oleh adanya ion logam pengotor yang cukup besar. Unsur tersebut diduga ikut bergabung dalam membentuk struktur zeolit selama proses reaksi hidrotermal.
Gambar 12 Morfologi permukaan NC perbesaran 7500x Tabel 4 Puncak-puncak utama 2θ pada zeolit sintetis dan tipe produk
Z10 Z9 NC Produk Referensi
12.5038 12.5453 12.5121 Na-P1 12.465 (JCPDS 39-0219) 17.6823 17.6865 17.669 Na-P1 17.664 (JCPDS 39-0219) 20.9373 21.0288 20.934 Q 20.860 (JCPDS 46-1045) 21.6872 21.7741 21.6848 Na-P1 21.675 (JCPDS 39-0219) - - 25.2754 TiO2 25.281(JCPDS 21-1272)
26.7151 26.7931 26.7115 Q 20.860 (JCPDS 46-1045) 28.0700 28.1371 28.0946 Na-P1 28.095 (JCPDS 39-0219) 30.8880 30.8281 Na-P1 30.843 (JCPDS 39-0219) 33.3756 33.3930 33.3429 Na-P1 33.380 (JCPDS 39-0219) 36.6195 36.7028 36.6529 Na-P1 35.758 (JCPDS 39-0219)
46.1273 46.0273 Na-P1 46.073 (JCPDS 39-0219)
50.1775 - - Q 50.139 (JCPDS 46-1045)
14
Tabel 4 merupakan ringkasan dari data difraktogram Zeolit sintetis. Berdasarkan data diatas, tipe zeolit yang terbentuk merupakan zeolit tipe Na-P1. Selain itu, mineral kuarsa masih ditemukan dalam zeolit dan nanokompositnya. Penurunan intensitas mineral kuarsa dengan penambahan NaOH dapat diamati hilangnya puncak 2θ pada 50.1775 (Gambar 8 dan Gambar 9).
Optimisasi Adsorpsi
Pada penelitian ini dilakukan optimisasi terhadap tiga parameter adsorpsi, yaitu konsentrasi, waktu agitasi, dan bobot adsorben terhadap biru metilena sebagai adsorbat. Prosedur pengujian mengacu pada penelitian yang telah dilakukan oleh Suswono (2012), Widiyanti (2011), dan Hediana (2011) dengan beberapa modifikasi.Uji adsoprsi dilakukan untuk membandingkan kapasitas adsorpsi antara zeolit dan nanokompositnya, sehingga Uji adsorpsi hanya dilakukan pada Z9 dan nanokompositnya karena Z10 tidak dibuat nanokomposit.
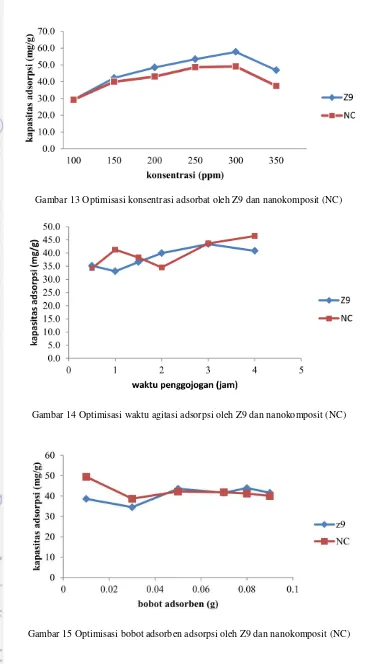
Hasil adsorpsi biru metilena oleh Z9 dan nanokomposit menunjukkan kondisi optimum pada konsentasi biru metilena 300 ppm. Konsentrasi ini dianggap optimum karena pada konsentrasi biru metilena sebesar 350 ppm, kurva mengalami penurunan (Gambar 13, Lampiran 6). Hal ini berarti pada saat konsentrasi biru metilena kurang dari 300 ppm, permukaan tapak aktif Z9 dan NC belum semua terisi oleh adsorbat yaitu biru metilena. Hal ini ditandai dengan semakin besarnya nilai kapasitas adsorpsi (Q).
Konsentrasi adsorbat optimun yang diperoleh digunakan sebagai konsentrasi absorbat dalam penentuan waktu agitasi optimum absorben dalam menjerap biru metilena. Hasil pengukuran sampel Z9 dan NC menunjukkan waktu optimum untuk kedua adsorben ialah 3 jam (Gambar 14, Lampiran 7). Ini terlihat dari waktu agitasi yang lebih lama dari 3 jam, nilai kapasitas adsorpsi NC cenderung naik sedangkan Z9 cenderung turun. NC memiliki kecendrungan tersebut karena mampu melakukan fotodegradasi, sedangkan Z9 tidak. Waktu agitasi yang lebih lama tidak selalu diikuti dengan kenaikan kapasitas adsorpsi. Hal ini disebabkan agitasi yang berlebih dapat menyebabkan molekul adsorbat yang terikat pada adsorben terlepas kembali sehingga bisa menurunkan efektivitas adsorpsi. Fenomena ini biasa terjadi pada jenis adsorpsi fisik (fisisorpsi).
Konsentrasi absorbat optimum dan waktu agitasi optimum yang diperoleh digunakan sebagai Konsentrasi absorbat dan waktu agitasi dalam penentuan bobot optimum absorben dalam menjerap biru metilena. Hasil pengukuran sampel Z9 dan nanokomposit menunjukkan adsorpsi mencapai optimum dengan bobot masing-masing sebesar 80 mg dan 10 mg (Gambar 15, Lampiran 8). Kenaikan bobot setelah 80 mg untuk Z9 dan 60 mg untuk nanokomposit sudah tidak diikuti dengan kenaikan persentase adsorpsi.
15
Gambar 13 Optimisasi konsentrasi adsorbat oleh Z9 dan nanokomposit (NC)
Gambar 14 Optimisasi waktu agitasi adsorpsi oleh Z9 dan nanokomposit (NC)
16
Isoterm Adsorpsi
Isoterm adsorpsi adalah hubungan yang menunjukkan distribusi adsorben antara fase teradsorpsi pada permukaan adsorben dengan fase ruah saat kesetimbangan pada temperatur tertentu. Pada penelitian ini, adsorpsi biru metilena oleh Z9 dan nanokomposit diuji dengan dua persamaan, yaitu persamaan Freundlich dan Langmuir. Berdasarkan nilai linearitas tertinggi, adsorpsi biru metilena oleh Z9 dan nanokomposit mengikuti persamaan Langmuir (Tabel 5, Lampiran 9). Dengan demikian, dapat diasumsikan bahwa adsorben memiliki permukaan yang homogen sehingga proses adsorbsi terjadi melalui mekanisme yang sama dan membentuk satu lapisan tunggal saat adsorpsi maksimum.
Berdasarkan tipe adsorpsi yang diperoleh yaitu Langmuir, maka dapat ditentukan nilai Xm dan k dari persamaan regresi Langmuir (Tabel 6). Nilai Xm menggambarkan jumlah adsorbat yang dijerap oleh permukaan adsorben. Nilai Xm Z9 lebih besar dari nanokomposit (NC). Hal ini menunjukkan jumlah biru metilena yang dijerap oleh Z9 lebih banyak dari pada nanokomposit (NC). Nilai k merupakan konstanta yang bertambah dengan kenaikan ukuran molekuler yang menunjukkan kekuatan ikatan molekul adsorbat pada permukaan adsorben. Molekul biru metilena lebih kuat terikat pada Z9 dibandingkan dengan NC.
Uji Fotodegradasi
Fotodegradasi merupakan proses penguraian senyawa organik dengan bantuan energi cahaya (foton) melalui reaksi fotokatalisis. Oksida logam TiO2
dapat dijadikan katalis dalam reaksi fotokatalisis. TiO2 dapat digunakan sebagai
fotokatalis karena merupakan semikonduktor yang mampu mengadsorpsi radiasi elektromagnetik pada daerah ultraviolet.
Pengujian fotodegradasi nanokomposit Zeolit-TiO2 dilakukan untuk melihat
kemampuan nanokomposit dalam menjerap sekaligus mendegradasi zat warna dengan bantuan radiasi sinar UV. Nanokomposit Zeolit-TiO2 hasil sintesis
digunakan untuk uji fotodegradasi zat warna biru metilena. Reaksi yang terjadi pada katalisis degradasi biru metilena adalah reaksi redoks yaitu terjadi pelepasan
Tabel 5 Nilai linearitas isoterm adsorpsi birumetilena oleh Z9 dan nanokomposit.
Adsorben Isoterm % linearitas
Z9 Freundlich 77.44
Langmuir 98.66 Nanokomposit Freundlich 55.56 Langmuir 97.37
Tabel 6 Nilai konstanta Xm dan k dari persamaan regresi langmuir
Sampel Xm k
Z9 48.309 0.378
17
Gambar 16 Filtrat hasil uji fotokatalisis tanpa radiasi UV (A)TiO2 + biru metilena (B) Z9 + biru metilena
(C) NC tanpa radiasi UV
Gambar 17 Filtrat hasil uji fotokatalisis dengan radiasi UV (D) TiO2 + biru metilena (E) Z9 + biru metilena
(F) NC tanpa radiasi UV
dan penangkapan elektron yang diakibatkan oleh energi foton hv (Sumerta et al.
2002). Proses fotodegradasi menggunakan sinar UV. Sinar UV berperan sebagai sumber foton. Berikut adalah proses fotodegradasi zat warna :
TiO2 + hν→ TiO2 (e- + H+)
TiO2 (H+) + H2O → TiO2 + HO* + H+
TiO2 (e-) + O2→ TiO2 + O2-
Zat warna + hν→ Zat warna*
Zat warna* + O2-→ produk degradasi
SIMPULAN DAN SARAN
Simpulan
Zeolit tipe P1 telah berhasil disintesis dari abu terbang batu bara dan abu sekam padi dengan nisbah NaOH/abu terbang batu bara sebesar 1 dan 1.3 serta terbukti mampu menjerap zat warna biru metilena. Selain itu nanokomposit Zeolit-TiO2 juga telah berhasil disintesis dan terbukti mampu menjerap dan
mendegradasi zat warna biru metilena. Adsorpsi biru metilena oleh zeolit dan nanokompositnya optimum terjadi pada konsentrasi 300 ppm, waktu agitasi optimum selama 3 jam untuk kedua adsorben. Bobot optimum masing-masing adsorbat adalah 80 dan 10 mg. Adsorpsi oleh kedua adsorben mengikuti isoterm Langmuir.
Saran
Perlu dilakukan optimisasi komposisi dalam pembuatan nanokomposit Zeolit-TiO2 sehingga diperoleh material dengan daya jerap dan aktivitas
fotokatalisis yang lebih baik. Selain itu, perlu juga dilakukan uji kemampuan regenerasinya sebagai adsorben. Optimisasi konsentrasi fotokalisis juga disarankan untuk mengetahui konsentrasi optimum limbah yang dapat difotodegradasi.
DAFTAR PUSTAKA
Aina H. 2007. Sintesis aditif β-Ca2SiO4 dari abu sekam padi dengan variasi temperatur pengabuan [skripsi]. Yogyakarta (ID): Universitas Gadjah Mada. Breck DW. 1974. Zeolite Molecular Sieve: Structure Chemistry and Use. New
York (US): Wiley.
Das SN. 2011. Zeolite synthesis and its aplication as adsorbent [Tesis]. Punjab(IN): Departemen of Chemical Engineering Thapar University. Efinov AM, Pogareva VG, Shashkin. 2003. Water-related bands in absorption
spectra of silicate glasses. J of Non Cryst Sol 332:93-114.DOI:
10.1016/j.jnoncrysol.2003.09.020
Fatimah I, Wijaya K. 2005. Sintesis TiO2-zeolit sebagai fotokatalis pada
pengolahan limbah cair industri tapioka secara adsorpsi-fotodegradasi.
TEKNOIN 10:4.
Fukui K, Nishimoto T, Takiguchi M, Yoshida H. 2006. Effects of NaOH
concentration on zeolite synthesis from fly ash with a hydrotermal treatment method. KONA 24: 183-191.
Hediana N. 2011. Sintesis, pencirian, dan uji fotodegradasi nanokomposit sodalit/TiO2 terhadap zat warna biru metilena [skripsi]. Bogor (ID): Institut
Pertanian Bogor.
Johan E, Ogami K, Abidin Z, Matsue N, Henmi T. 2011.Synthesis of zeolite MFI
19
Jumaeri, Astuti W, Lestari. 2007. Preparasi dan pencirian zeolit dari abu terbang batu bara secara alkali hidrotermal. Reaktor 1(11):38-44.
Chareonpanich M, Namto T, Kongkachuichay P, Limtrakul J . 2003. Synthesis of
ZSM-5 zeolite from lignite fly ash and rice husk ash. Bangkok(TH): Universitas Kasetsart.
MacDonald SA, Schardt CR, Masiello DJ, Simmons JH. 2000. Dispersion analysis of FTIR feflection measurements in silicate glasses. J Of Non-Crys mat 275:72-83.DOI: 10.1016/j.fuproc.2003.10.026
Mufrodi Z, Sutrisno B, Hidayat A. 2010. Modifikasi limbah abu layang sebagai material baru adsorben, di dalam Prosiding Seminar Nasional Teknik Kimia Yogyakarta, 26 januari 2010. Hlm 1-6.
Mujiyanti DR, Nuryono, Kunarti ES. 2010. Sintesis dan karakterisasi silika gel dari abu sekam padi yang diimobilisasi dengan 3-(Trimetoksisilil)-1-Propantiol. J Sains dan Kim Ter 2:150-167.
Musyoka NM, Petrik LF, Balfour G, Natasha M, Gitari W, Mabovu B. 2009. Removal of toxic elements from brine using zeolit Na-P1 made from A South African coal fly ash, di dalam prosiding International Mine Water Conference Pretoria(ZA) 19-23 Oktober 2009. hal 680-687.
Ojha K, Narayan CP, Amar NS. 2004. Zeolite from fly Ash: synthesis and characterization. Bull Master Sci, 6:555-564.DOI:10.1007/BF02707285
Putro AL, Prasetyoko D. 2007. Abu sekam padi sebagai sumber silika pada sintesis zeolit ZSM-5 tanpa menggunakan templat organik. Akta Kimindo 3: 33-36.
Sumerta IK, Karna W, Iqmal T. 2002. Fotodegradasi metilen biru menggunakan katalis TiO2-Monmorilonit dan Sinar UV. Makalah pada Seminar Nasional
Pendidikan Kimia. Yogyakarta (ID): Jurusan Kimia FMIPA.
Suswono EJ. 2012. Optimisasi adsorpsi biru metilena oleh alofan dan nanokomposit alofan-TiO2 serta uji fotokatalisisnya [Skripsi]. Bogor (ID):
Institut Pertanian Bogor.
Sutarno, Aryanto Y, Budyantoro A. 2010. Kajian pengaruh berat NaOH/abu layang terhadap kristalinitas dalam sintesis faujasit. J Ilm Das 10:1-5.
Thammavong S. 2003. Studies of synthesis, kinetics, and particle size of zeolite X from Narathiwat kaolin [tesis]. Suranaree (TH): Degree of Master of Science in Chemistry Suranaree University of Technology.
Warsito S, Sriatun, Taslimah. 2006. Pengaruh penambahan surfaktan
cetyltrimethylammonium bromide (n-CTMABr) pada sintesis zeolit Y.
Semarang (ID): Fakultas MIPA Universitas Diponegoro.
Querol X, Moreno N, Umana JC, Alstuey A, Hernandez, Lopez-Soler A, Plana F.
2002. Synthesis of zeolites from coal fly ash: an overview. In J of Coal Geo 50: 413-423.DOI:10.1016/S0166-5162(02)00124-6
Zakaria A. 2011. Adsorpsi Cu(II) menggunakan zeolit sintetis dari abu terbang batu bara [Tesis]. Bogor (ID): Sekolah Pascasarjana IPB.
Zhang B, WU D, Wang C, HE S, Zhang ZJ , Kong H. 2007. Simultaneous removal of ammonium and phosphate by zeolite synthesized from coal fly ash as influenced by acid treatment. J of Envir Sci 19:540-545.DOI: 10.1016/S1001-0742(07)60090-4.
Widiyanti E. 2011. Sintesis nanokomposit alofan/TiO2 dan uji fotodegradasi pada
20
West AR. 1984. Solid State Chemistry and Its Applications. New York (US): John
21
Lampiran 1 Diagram alir penelitian
22
23
24
25
26
Lampiran 6 Optimisasi konsentrasi adsorpsi biru metilena
a. Z9
Konsentrasi Massa Absorban Fp konsentrasi akhir
(ppm) kosentrasi terjerap
Konsentrasi Massa Absorban Fp
konsentrasi
27
Contoh perhitungan: Kapasitas adsorpsi (Q)
Q =
=
ml 00- 0
0.0 09g
mg 000
ppm
Keterangan:
28
Lampiran 7 Optimisasi waktu agitasi adsorpsi biru metilena
a. Z9
29
Contoh perhitungan: Kapasitas adsorpsi (Q)
Q = om- a mg 000ppm = ml 000.0 02 g- . mg 000ppm
Keterangan:
30
Lampiran 8 Optimisasi bobot adsorben terhadap adsorpsi biru metilena
a. Z9
Persamaan garis kurva standar biru metilena: y = 0.18015 x - 0.02099 R2 = 0.98842
31
Lampiran 9 Isoterm adsorpsi biru metilena oleh Z9 dan nanokomposit (NC) a. Z9
0.0000 0.5000 1.0000 1.5000 2.0000 2.5000
lo
g
x
/m
32
Isoterm Langmuir
Persamaan garis isotherm Langmuir yang dihasilkan y = 0.0207x - 0.0547 dengan r2 = 98.66%
Maka dari persamaan
, diperoleh nilai Xm = 48.309 dan k = 0.378
b. Nanokomposit Zeolit-TiO2 (NC)
C awal
(mg/L) C akhir (mg/L) C teradsorpsi (mg/L) Massa (g)
33
Isoterm Freunluich
Isoterm Langmuir
Persamaan garis isotherm Langmuir yang dihasilkan y = 0.0257x - 0.1802 dengan R2 = 97.37%
0.0000 0.5000 1.0000 1.5000 2.0000 2.5000
34
Lampiran 10 Hasil uji fotokatalisis
A. Tanpa Penyinaran UV
Z9 TiO2 Nanokomposit
B. Dengan Penyinaran UV
35
Lampiran 11 Spektrum UV filtrat sampel
A) Tanpa Penyinaran UV
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 8 Desember 1989 dari pasangan Bapak Agus dan Ibu Idah. Penulis merupakan anak pertama dari dua bersaudara. Pada tahun 2008, penulis lulus dari MA Negeri 1 Bogor dan diterima menjadi mahasiswa Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI) di Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA).