SINTESIS TURUNAN ARILAMIDA-3 DAN UJI AKTIVITAS IN VITRO TERHADAP ENZIM MATRIX METALLOPROTEINASE-9 (MMP-9)
SEBAGAI KANDIDAT ANTI-KANKER PAYUDARA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh :
Kevin Cahaya Putra
NIM : 158114111
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
SINTESIS TURUNAN ARILAMIDA-3 DAN UJI AKTIVITAS IN VITRO TERHADAP ENZIM MATRIX METALLOPROTEINASE-9 (MMP-9)
SEBAGAI KANDIDAT ANTI-KANKER PAYUDARA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh :
Kevin Cahaya Putra
NIM : 158114111
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
HALAMAN PERSEMBAHAN
“Segala perkara dapat kutanggung di dalam Dia yang
memberi kekuatan kepadaku”
(Filipi 4:13)
“
Diberkatilah orang yang mengandalkan Tuhan, yang
menaruh harapannya pada Tuhan!”
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa karena
berkat anugerah-Nya penulis dapat melewati tiga setengah tahun untuk
menjalankan studi di almamaternya dan sampai pada skripsi yang berjudul “Sintesis
Turunan Arilamida-3 dan Uji Aktivitas In Vitro Terhadap Enzim Matrix
Metalloproteinase-9 (MMP-9) Sebagai Kandidat Anti-Kanker Payudara”. Penelitian ini merupakan bagian dari penelitian Maywan Hariono, Ph.D., Apt. yang
didanai oleh Indonesia Toray Science Foundation periode 2017/2018 dengan judul
“Synthesis, Enzymatic Assay, and Molecular Modelling of Purin Derivatives Targeting Hemopexin Domain of Matrix Metalloproteinase-9 (PEX-9) in the
Discovery of Novel Anti-Breast Cancer”. Perjalanan studi yang penulis tempuh penuh suka dan duka, namun skripsi ini dapat ditempuh dengan baik dan tepat
waktu. Skripsi ini disusun sebagai syarat untuk memperoleh gelar sarjana Farmasi
(S.Farm.) di Universitas Sanata Dharma Yogyakarta.
Banyak pihak yang turut serta membantu, mendukung, dan membimbing
penulis dalam penyusunan naskah skripsi ini. Tanpa bantuan mereka, penulis tidak
mungkin sampai pada tahap penyelesaian skripsi ini. Oleh karena itu, penulis
hendak mengucapkan terima kasih yang sedalam-dalamnya kepada:
1. Ibu Dr. Yustina Sri Hartini, Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
2. Bapak Maywan Hariono, Ph.D., Apt. selaku dosen pembimbing skripsi
yang dengan sabar dan tulus membimbing tim penelitian sampai detik ini
serta selalu memberikan dukungan, kritik dan saran kepada penulis dari
awal penyusunan skripsi hingga selesai.
3. Ibu Phebe Hendra, M.Si., Ph.D., Apt. dan ibu Dr. Erna Tri Wulandari, M.Si.,
Apt., selaku dosen penguji skripsi yang menyemangati dan memberi
masukan dalam menyelesaikan penelitian ini.
4. Almarhumah mama yang sampai detik terakhir menghembuskan nafas
terakhir selalu mendukung dan menyemangati penulis dalam studinya
5. Papa yang selalu setia, memotivasi, mendukung, dan membantu penulis
dalam mengerjakan skripsi sampai pada tahap akhir hingga selesainya
skripsi ini.
6. Adik-adik yang selalu mengerti dan menyemangati penulis ketika
mengerjakan skripsi dan semoga adik-adik segera menyusul penulis dalam
mengerjakan skripsi mereka kelak.
7. Mak yang selalu sabar dan mendukung penulis dalam mengerjakan skripsi,
penulis berharap agar mak sehat selalu.
8. Ndut yang selalu mengerti, mendukung, dan membantu penulis dari awal
hingga penulis dapat menyelesaikan skripsi ini dan bersama-sama
merasakan suka-duka selama dua tahun ini.
9. “Skripsi Analog” yang terdiri dari teman-teman penelitian Ervan, Krisna, Sangga, Wisnu, dan Aldo yang selalu bekerja bersama-sama hingga larut
malam dan merasakan suka-duka bersama selama mengerjakan penelitian
ini terutama saat mengerjakan “kurva baku” bersama.
10.Sahabat-sahabat yang tidak sengaja ditemukan di Farmasi “Pethodon” Sangga, Ricky, Ervan, Aris, Willy, dan Kemara yang selalu mengerti satu
sama lain dan menempuh suka-duka bersama selama tiga setengah tahun
ini.
11.Sahabat-sahabat pejuang nonton bioskop “Survivor” Sangga, Cicik, Ricky, Yansen, Gumi, Momon, dan Vivi yang telah berjuang bersama dalam satu
kelas selama tiga setengah tahun ini.
12.Sahabat-sahabat penikmat sus coklat “Sus Coklat” Sangga, Ricky, Felis, Glenys, dan Trisna yang selalu berbagi dan menikmati sus coklat bersama.
13.Sahabat-sahabat yang satu dalam iman dan tidak pernah melupakan salah
satu sahabatnya “Cross” yang ada untuk menyemangati penulis.
14.Sahabat-sahabat yang tidak pernah pudar “Crossworshipper” selalu memberikan semangat dan dukungan satu sama lain serta tidak pernah lupa
ABSTRAK
Pada kanker payudara, diketahui bahwa enzim matrix metalloproteinase
(MMP) dan khususnya MMP-9 diekspresikan dalam jumlah yang tinggi sehingga banyak penelitian tentang penemuan MMP inhibitor (MMPI). Kebanyakan MMPI diketahui gagal pada uji klinis karena menimbulkan efek samping yang merugikan seperti inflamasi dan sindroma muskuloskeletal. Penelitian ini bertujuan untuk mensintesis senyawa arilamida-3 yang dirancang aktif menghambat MMP-9 pada
hemopexin domain (PEX-9) dengan mereaksikan 3,4,5-trimetoksianilin dan 3-bromopropionil klorida dengan katalisator piridin pada suhu kamar. Produk hasil sintesis berupa serbuk berwarna putih dan larut dalam kloroform dengan titik lebur 115,7-120,1°C. Uji DAB-HCl menunjukkan hasil negatif yang berarti gugus amina primer telah tersubstitusi. Uji KLT menunjukkan senyawa hasil sintesis berbeda dengan bahan baku dan murni secara KLT. Hasil elusidasi struktur menunjukkan proton etilen terletak pada geseran kimia 2-4 ppm berdasarkan 1H-NMR dan 15-55 ppm pada 13C-NMR, C=O dan -NH- amida pada 1658,78 dan 3448,72 cm-1 berdasarkan FTIR, serta m/z 317 berdasarkan GC-MS. Senyawa hasil sintesis diuji aktivitasnya dalam menghambat enzim MMP-9 in vitro dengan fluorogenic assay. Hasil uji in vitro menunjukkan persen penghambatan senyawa arilamida-3 sebesar 5% pada konsentrasi 200 µg/mL mengindikasikan bahwa senyawa tersebut mempunyai aktivitas rendah dalam menghambat MMP-9.
Kata kunci: hemopexin, in vitro, kanker payudara, matrix metalloproteinase-9
ABSTRACT
In breast cancer, it is known that Matrix Metalloproteinase-9 enzyme (MMP-9) and especially MMP-9 are highly expressed by the cancer cells so that many studies have been done to discover MMP inhibitor. Most of these inhibitors fail in clinical trials due to the adverse side effects such an inflammation and musculoskeletal syndrome. This study aims to synthesize arylamide derivative-3 which is selectively targeting hemopexin domain (PEX-9) by reacting 3,4,5-trimethoxyaniline and 3-bromopropionyl chloride with pyridine as catalysator at room temperature. The product was determined its physical appearance as a white powder which is soluble in chloroform with 115,7-120,1°C melting point. DAB-HCl test showed negative result which is confirming substitution of primary amine group at 3,4,5-trimethoxyaniline. Arylamide-3 is pure by KLT and has different Rf with 3,4,5-trimethoxyaniline. Structure elucidation showed ethylene proton appears at 2-4 ppm using 1H-NMR and its carbon appears at 15-55 ppm using 13C-NMR, carbonyl group and secondary amine appears at 1658,78 and 3448,72 cm-1 using FTIR, and m/z 317 using GC-MS. Arylamide derivative-3 was then tested for its activity in inhibiting MMP-9 in vitro with fluorogenic assay. The results showed a percent inhibition of arylamide-3 of 5% at 200 µg/mL associated with its low activity to inhibit MMP-9.
DAFTAR ISI
Halaman
HALAMAN SAMPUL……… i
HALAMAN PERSETUJUAN PEMBIMBING……….. ii
HALAMAN PENGESAHAN………. iii
HALAMAN PERSEMBAHAN……….. iv
PERNYATAAN KEASLIAN KARYA……….. v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI……….. vi
PRAKATA………... vii
ABSTRAK………... x
ABSTRACT………... xi
DAFTAR ISI……… xii
DAFTAR TABEL……… xiii
DAFTAR GAMBAR………... xiv
DAFTAR LAMPIRAN……… xv
PENDAHULUAN……… 1
METODE PENELITIAN………. 4
HASIL DAN PEMBAHASAN……… 7
KESIMPULAN……… 16
SARAN……… 16
UCAPAN TERIMA KASIH……… 17
DAFTAR PUSTAKA……….. 18
LAMPIRAN………. 20
DAFTAR TABEL
Halaman Tabel 1. Perhitungan persen penghambatan senyawa arilamida-3
DAFTAR GAMBAR
Halaman Gambar 1. Struktur Senyawa 2 dengan gugus fungsi yang diduga
farmakofor (Dufour et al., 2011)………. 1 Gambar 2. Struktur arilamida-3 dengan gugus fungsi yang mirip
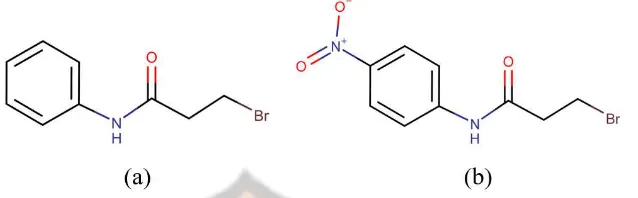
dengan Senyawa 2………... 3 Gambar 3. (a) Struktur senyawa milik Adhipandito, (b) Struktur
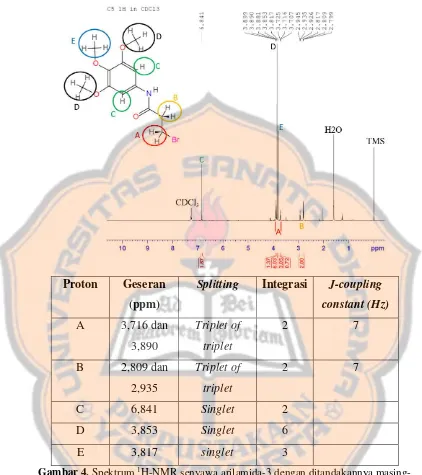
senyawa milik Ludji……… 4 Gambar 4. Spektrum 1H-NMR senyawa arilamida-3 dengan
ditandakannya masing-masing sinyal A, B, C, D, dan E
beserta karakteristik masing-masing sinyal……….. 11 Gambar 5. Spektrum 13C-NMR senyawa arilamida-3 dengan
ditandakannya masing-masing sinyal A, B, C, D, E, F,
G, I, dan J beserta karakteristik masing-masing sinyal…. 12 Gambar 6. Spektrum inframerah senyawa arilamida-3………. 13 Gambar 7. Kromatogram GC arilamida-3 dengan ditandakannya
masing-masing puncak A, B, C, D, dan E……… 14 Gambar 8. Spektrum MS senyawa arilamida-3………. 14 Gambar 9. Struktur 3D kristalografi sinar X senyawa
DAFTAR LAMPIRAN
Halaman Lampiran 1. Representasi tata letak 96-microwell plate dengan B:
bufer, Sp: sampel senyawa arilamida-3, E: enzim MMP-9, dan Sb: substrat disertai dengan volume
dalam µL………. 20 Lampiran 2. Mekanisme reaksi SNA antara 3,4,5-trimetoksianilin
dan 3-bromopropionil klorida………. 20 Lampiran 3 (a) Sintesis senyawa arilamida-3 pada awal
pengadukan, (b) Crude product setelah dibilas dengan
aquadest dan dibiarkan mengering…………. 21 Lampiran 4. (a) Serbuk 3,4,5-trimetoksianilin yang berwarna
sedikit kekuningan (b) Serbuk arilamida-3 yang
berwarna putih………. 21 Lampiran 5. Hasil Uji Kelarutan Senyawa Arilamida-3………….. 22 Lampiran 6. Mekanisme reaksi antara DAB-HCl dan
3,4,5-trimetoksianilin………... 22 Lampiran 7. Hasil uji pendahuluan DAB-HCl antara bahan baku
dan arilamida-3………... 23 Lampiran 8. Profil KLT arilamida-3 (Rf = 0,55) dibandingkan
dengan bahan baku (Rf = 0,38).………... 23 Lampiran 9. Perhitungan bahan sintesis dan hasil rendemen
senyawa arilamida-3………... 24 Lampiran 10. Perbesaran spektrum 1H-NMR pada geseran 2,6-4,1
ppm………. 25 Lampiran 11. Perbesaran spektrum 1H-NMR pada geseran 6,1-7,9
ppm……….. 25 Lampiran 12. Spektrum inframerah senyawa
PENDAHULUAN
Pada tahun 2011, Dufour et al., menemukan suatu obat yang secara selektif
menghambat enzim matrix metalloproteinase-9 (MMP-9) pada kanker payudara.
Pada penelitian tersebut dilakukan penapisan virtual dan uji in vitro terhadap 5
senyawa yang diduga aktif menghambat aktivitas MMP-9. Senyawa yang paling
aktif adalah senyawa dari database ZINC dengan kode 135415473
(~{N}-[4-(difluoromethoxy)phenyl]-2-[(6-oxo-4-propyl-1~{H}-pyrimidin-2-yl)sulfanyl]
acetamide) yang kemudian disebut Senyawa 2 dengan struktur seperti pada Gambar
1. Senyawa 2 ditemukan aktif in silico dan in vitro diduga karena memiliki cincin
planar dan gugus aril amida yang berinteraksi secara selektif dengan kantung aktif
MMP-9 pada domain non-katalitik (Dufour et al., 2011).
Gambar 1. Struktur Senyawa 2 dengan gugus fungsi yang diduga farmakofor (Dufour et al., 2011)
Pada awal tahun 1990-an, MMP mulai diketahui memiliki peranan besar
dalam perkembangan kanker. Oleh karena itu, banyak ditemukan MMP inhibitor
(MMPI) sebagai strategi untuk terapi kanker dengan mentarget domain katalitik
dari MMP. Namun, beberapa dari obat-obat tersebut gagal dalam berbagai fase uji
klinis karena tidak selektifnya domain katalitik pada semua MMP terhadap MMPI.
Semua MMP (MMP-1 sampai MMP-26) akan dihambat padahal MMP lain juga
diperlukan tubuh untuk metabolisme normal yang salah satunya untuk
penyembuhan luka. Salah satu MMPI yaitu marimastat dapat menyebabkan efek
samping sindroma muskuloskeletal dan inflamasi. Selain itu, senyawa ini diketahui
secara statistik tidak meningkatkan kualitas hidup pasien secara signifikan pada uji
klinis. Ketidakselektifan MMPI tersebut disebabkan domain katalitik memiliki Cincin planar
Rantai alkil
kemiripan sekuens asam amino sejumlah 43-65% dengan semua MMP (Dufour et
al., 2011, Cathcart et al., 2015).
Semua kelompok MMP memiliki bagian struktur yang terdiri dari signal
peptide, propeptide domain, domain katalitik, dan hemopexin domain (PEX)
(Bauvois, 2012). Uniknya, hemopexin MMP-9 (PEX-9) hanya mempunyai
kemiripan kurang lebih 25-35% dengan PEX domain pada MMP lain (Dufour et
al., 2011, Ugarte-Berzal et al., 2016). Hal ini menjadikan PEX-9 lebih selektif
ditargetkan dalam penemuan obat kanker melalui mekanisme penghambatan MMP
(Dufour et al., 2011).
Pada tahun 2018, kanker memiliki jumlah kasus baru sebanyak 18,1 juta
dan jumlah kematian sebanyak 9,6 juta. Kanker payudara merupakan jenis kanker
dengan penyebab kematian terbanyak kelima di dunia dengan angka 6,6%. Pada
wanita, kanker payudara merupakan kanker yang sangat umum terdiagnosis
diantara kanker yang lain dengan angka kejadian kasus sebanyak 24,2% (IARC,
2018). Kanker payudara paling banyak dialami oleh wanita di Indonesia setelah
kanker serviks (Wahidin et al., 2012). Kasus kanker payudara di Indonesia terdapat
sebanyak 0,5% dan DI Yogyakarta merupakan provinsi dengan kasus kanker
payudara terbanyak yaitu sebanyak 2,4% (Kemenkes, 2015).
Kebanyakan penyebab kematian pada penderita kanker bukan karena tumor
primer, melainkan karena metastasis yang biasanya dialami oleh penderita kanker
stadium akhir. Metastasis merupakan proses menyebarnya sel tumor ke organ lain
melalui pembuluh darah, dan 90% penderita kanker yang telah mencapai tahap
metastasis mengalami kematian (Welch et al., 2000, Chaffer and Weinberg, 2011).
Sel tumor yang mengalami metastasis akan melewati extracellular matrix
(ECM) yang mengontrol sel untuk bermigrasi dari satu organ ke organ yang lain
melalui pembuluh darah. Hal ini karena sel tumor memproduksi MMP yang
merupakan enzim untuk mendegradasi ECM (Gialeli et al., 2011). Pada kanker
payudara, ditemukan ekspresi MMP-9 yang tinggi dibandingkan dengan payudara
normal dan ini merupakan ciri khas dari kanker payudara jenis triple-negative dan
ada obatnya. Studi menunjukan adanya hubungan ekspresi berlebihan MMP-9
dengan tingginya insiden metastasis (Yousef et al., 2014).
Pada penelitian ini telah disintesis turunan dari Senyawa 2 yang akan diberi
nama arilamida-3 yang strukturnya disajikan pada Gambar 2. Senyawa ini
merupakan turunan arilamida yang disintesis dari 3,4,5-trimetoksianilin dan
3-bromopropionil klorida. Pada bagian meta dan para dari cincin arilamida terdapat
gugus metoksi.
Gambar 2. Struktur arilamida-3 dengan gugus fungsi yang mirip dengan Senyawa 2
Senyawa yang akan disintesis oleh peneliti tidak mengadaptasi seluruh
farmakofor dari penelitian Dufour, melainkan hanya mengadaptasi gugus arilamida
dan rantai alkil. Adhipandito (2017) dan Ludji (2017) telah mensintesis 2 senyawa
yang merupakan fragmen dari Senyawa 2 milik Dufour dan telah di uji aktivitasnya
terhadap enzim MMP-9 in vitro. Tahap sintesis dalam penelitian mereka telah
dipublikasikan, namun tahap uji in vitro belum sampai pada tahap publikasi.
Senyawa Adhipandito dan Ludji disajikan pada Gambar 3. Persen penghambatan
terhadap enzim MMP-9 senyawa Adhipandito sebesar 11% dan Ludji sebesar 69%.
Pada senyawa Dufour, tidak dijelaskan fungsi gugus fungsional -OCHF2 yang
berkarakter Electron Withdrawing Group (EWG) dan Electron Donating Group
(EDG). Maka dari itu tujuan Ludji memodifikasi bagian tersebut dengan
memasukkan gugus nitro yang bersifat EWG dan ternyata meningkatkan aktivitas
penghambatan MMP-9 dibandingkan milik Adhipandito yang tidak mengalami
modifikasi. Oleh karena itu, menarik untuk dilakukan modifikasi dengan EDG pada
posisi 3, 4, dan 5 dari cincin arilamida dengan harapan meningkatkan aktivitas
penghambatan terhadap MMP-9.
Rantai alkil
Gambar 3. (a) Struktur senyawa milik Adhipandito, (b) Struktur senyawa milik Ludji Keuntungan yang lain adalah metode sintesis senyawa arilamida-3 hanya
melalui satu tahap dibandingkan dengan Senyawa 2 yang harus melalui dua sampai
tiga tahap reaksi kimia. Hal ini menyebabkan senyawa arilamida-3 lebih efisien dari
segi biaya dan waktu. Senyawa arilamida-3 dilihat kebenaran strukturnya dengan
spektroskopi resonansi magnetik inti, inframerah, massa, dan kristalografi x-ray.
Kemudian senyawa arilamida-3 di uji aktivitas penghambatannya terhadap enzim
MMP-9 in vitro dengan metode fluorogenic assay.
METODE PENELITIAN Bahan
Kecuali dinyatakan lain, semua bahan kimia yang dipakai bermutu analisis
yang disuplai oleh Sigma Aldrich dan Merck. Bahan utama yang digunakan untuk
sintesis adalah: 3,4,5-trimetoksianilin, 3-bromopropionil klorida, piridin, plat silika
gel GF254, etil asetat, n-heksana, kloroform, dan 4-dimetilamino benzaldehida HCl
(DAB-HCl). Bahan yang digunakan untuk elusidasi struktur adalah: pellet kalium
bromida (KBr) dan kloroform-D (CDCl3). Bahan yang digunakan untuk uji in vitro
adalah: kit enzim MMP-9 yang terdiri dari enzim MMP-9 dari manusia yang
terliofilisasi, substrat peptida, buffer, peptida NNGH, gliserol, dan
dimetilsulfoksida (DMSO).
Alat
Alat yang digunakan untuk sintesis adalah: Labu alas bulat (Pyrex), alat-alat
gelas pada umumnya, timbangan analitik (Mettler Toledo®), melting point system
(Mettler Toledo®), pompa vakum (GAST model DOA-P504-BN), oven (Memmert
GmbH + Co.KG), dan lampu UV254. Alat yang digunakan untuk elusidasi struktur
Resonance (Bruker 176 dan 700 MHz), dan spektrometer massa (Waters® Xevo®).
Pengujian dengan spektrometer inframerah dan massa dilakukan di Fakultas MIPA
Kimia UGM, sedangkan pengujian dengan spektrometer NMR dilakukan di Institut
Farmasetikal dan Nutrasetikal Malaysia. Alat yang digunakan untuk uji in vitro
adalah: pipet mikro (Eppendorf), micro well plate 96, pipet tips, inkubator, vortex,
Tecan Microplate Reader (Infinite 200Pro).
Tata Cara Penelitian
Sintesis Senyawa Turunan Arilamida-3 (Diadaptasi dari metode Arifiyanto, 2001)
3,4,5-trimetoksianilin sebanyak 3,59 mmol (0,66 g) dimasukkan ke dalam
labu alas bulat dan ditambahkan piridin sebagai katalis sebanyak 3,59 mmol (0,28
g; 0,29 mL). 3-bromopropionil klorida kemudian ditambahkan tetes demi tetes
sebanyak 4,00 mmol (0,69 g; 0,40 mL) sambil diaduk hingga terbentuk padatan
(reaksi dimonitor dengan KLT dalam fase gerak n-heksana:etil asetat 2:2 dan fase
diam silika gel GF254). Padatan disaring dan dicuci dengan aquadest untuk
menghilangkan sisa piridin dan HCl sebagai produk samping reaksi (dicuci hingga
pH netral). Kemudian dilakukan rekristalisasi dengan menggunakan pelarut
kloroform. Produk diuji organoleptis, titik lebur, kelarutan, KLT dan elusidasi
struktur dengan 1H-NMR, 13C-NMR, FTIR, GC-MS, dan kristalografi x-ray.
Uji Organoleptis
Bentuk dan warna dari produk hasil sintesis diamati dan diidentifikasi.
Uji Kelarutan
Senyawa hasil sintesis ditimbang sebanyak 5 mg dan dilarutkan dalam
sejumlah pelarut dari polar hingga non-polar tetes demi tetes hingga tepat larut.
Pelarut yang di uji adalah air, etanol, DMSO, aseton, kloroform, etil asetat, dan n
-heksana. Kategori kelarutan senyawa hasil sintesis ditentukan berdasarkan
Farmakope Indonesia V.
Uji DAB-HCl
3,4,5-trimetoksianilin dan senyawa hasil sintesis masing-masing ditimbang
sebanyak 1 mg kemudian dimasukkan ke dalam drupple plate. Masing-masing
Uji KLT
3,4,5-trimetoksianilin dan senyawa hasil sintesis masing-masing ditimbang
sebanyak 1 mg kemudian dilarutkan dalam kloroform. Masing-masing senyawa
ditotolkan pada plat silika gel GF254 yang telah diaktifkan pada suhu 100°C. Totolan
berjarak 1 cm dari bawah. Plat yang disiapkan sejumlah dengan 3 sistem fase gerak
yang telah disiapkan dan dijenuhkan dengan kertas saring yaitu fase gerak n
-heksana:etil asetat dengan perbandingan 1:3, 2:2, dan 3:1 (Adhipandito, 2017).
Kemudian plat dimasukkan ke dalam gelas beker yang berisi fase gerak dan dieluasi
hingga 1 cm dari atas. Kemudian plat dikeluarkan, dikeringkan, dan dilihat
bercaknya di bawah lampu UV 254 nm serta dihitung nilai Rf.
Uji Titik Lebur
Senyawa hasil sintesis ditimbang sebanyak 1 mg dan dihaluskan. Kemudian
senyawa dimasukkan ke dalam pipa kapiler untuk dimasukkan ke dalam melting
point system. Suhu diatur dalam rentang 100-200°C dan didapatkan hasil berupa
jarak lebur.
Uji Aktivitas In Vitro
Enzim MMP-9 yang terliofilisasi direkonsitusi dengan 110 µL gliserol 30%
dalam air deionisasi. Enzim yang telah terekonstitusi dilarutkan dalam 550 µL bufer
dan siap digunakan. Sampel (200 µg/mL) sebanyak 1 µL dipipet dan dimasukkan
ke setiap sumuran 96-microwell plate dan ditambahkan 5 µL enzim MMP-9 dan 44
µL bufer. Kemudian kontrol positif dibuat dalam sumuran yang lain dengan
mencampurkan 2 µL inhibitor NNGH (Asparagin-Asparagin-Glisin-Histidin)
(2mM), 5 µL enzim MMP-9, dan 43 µL bufer. Kemudian kontrol negatif dibuat
dalam sumuran yang lain dengan mencampurkan 5 µL enzim MMP-9 dan 45 µL
bufer sebagai kontrol negatif. Bufer dipipet sebanyak 100 µL dan dimasukkan ke
dalam sumuran yang lain sebagai blanko. Kemudian diinkubasi pada suhu 37°C
selama 30 menit. Setelah inkubasi selesai, masing-masing sumuran ditambahkan 50
µL larutan substrat kemudian diinkubasi kembali pada suhu 37°C selama 60 menit.
Tata letak 96-microwell plate disajikan pada Lampiran 1.
Fluorosensi kemudian dibaca menggunakan Tecan Microplate Reader pada
sampel, kontrol negatif, dan kontrol positif dikurangkan blanko kemudian
didapatkan persen aktivitas enzim dengan rumus: 𝑓𝑙𝑢𝑜𝑟𝑜𝑠𝑒𝑛𝑠𝑖 𝑠𝑎𝑚𝑝𝑒𝑙
𝑓𝑙𝑢𝑜𝑟𝑜𝑠𝑒𝑛𝑠𝑖 𝑘𝑜𝑛𝑡𝑟𝑜𝑙 𝑛𝑒𝑔𝑎𝑡𝑖𝑓 𝑥 100%. Persen penghambatan MMP-9 didapatkan
dengan rumus: 100% - persen aktivitas enzim (%).
HASIL DAN PEMBAHASAN Sintesis Senyawa
Substitusi Nukleofilik Asil (SNA) merupakan reaksi yang terjadi pada
pembentukan arilamida-3 antara 3,4,5-trimetoksianilin dan 3-bromopropionil
klorida dengan piridin sebagai katalisator. Reaksi substitusi merupakan reaksi
kimia yang melibatkan penggantian gugus pergi dari suatu senyawa dengan gugus
fungsi yang lain (Smith and March 2007). Pada reaksi SNA ini, yang berperan
sebagai gugus pergi adalah gugus klorida (-Cl) dari 3-bromopropionil klorida,
sedangkan gugus pengganti adalah NH dari 3,4,5-trimetoksianilin (Koltunov et al.,
2016). Gugus klorida (-Cl) pada 3-bromopropionil klorida merupakan gugus pergi
yang baik tetapi Cl yang berkarakter elektronegatif relatif masih terikat kuat dengan
-CO- karbonil apabila tidak dipercepat dengan katalisator (Zhang et al., 2009).
Nukleofil yang akan menyerang 3-bromopropionil klorida adalah
3,4,5-trimetoksianilin yang merupakan suatu nukleofil yang baik karena memiliki amina
primer yang pada atom N memiliki pasangan elektron bebas dan dapat bereaksi
dengan turunan asam karboksilat untuk membentuk suatu amida (Kahl et al., 2012).
Mekanisme reaksi disajikan pada Lampiran 2.
Produk awal hasil reaksi (crude product) berupa serbuk berwarna putih,
kemudian produk dibilas dengan aquadest dan dibiarkan mengering seperti terlihat
pada Lampiran 3. Pencucian dengan aquadest bertujuan untuk menghilangkan sisa
piridin dan HCl yang terbentuk sebagai produk sampingan karena dikhawatirkan
HCl akan menghidrolisis produk yang berupa amida.
Uji pendahuluan hasil sintesis arilamida-3 ditegakkan dengan uji
organoleptis, kelarutan, DAB-HCl, KLT, dan titik lebur. Pada uji organoleptis
terlihat senyawa hasil sintesis berupa serbuk berwarna putih. Warna senyawa hasil
seperti terlihat pada Lampiran 4. Perbedaan warna antara senyawa awal dan
senyawa hasil sintesis menunjukkan bahwa senyawa hasil sintesis berbeda dengan
senyawa awal. Pada uji kelarutan, senyawa arilamida-3 larut dalam kloroform,
aseton, etil asetat, dan DMSO sehingga arilamida-3 bersifat semi polar. Hasil uji
kelarutan disajikan pada Lampiran 5.
Pada uji DAB-HCl, senyawa yang memiliki gugus amina primer akan
bereaksi dengan DAB-HCl dan membentuk basa Schiff yang berwarna jingga,
sedangkan senyawa yang tidak memiliki amina primer tidak akan bereaksi dengan
DAB-HCl dan tidak menghasilkan warna jingga (Adegoke, 2011). Arilamida-3
tidak bereaksi dengan DAB-HCl dan tidak membentuk warna jingga karena pada
arilamida-3 gugus amina primer sudah mengalami substitusi dengan
3-bromopropionil klorida. Mekanisme reaksi DAB-HCl dengan
3,4,5-trimetoksianilin disajikan pada Lampiran 6, sedangkan hasil uji pendahuluan yang
membedakan antara bahan baku dengan hasil sintesis disajikan pada Lampiran 7.
Pada uji KLT, sistem fase gerak yang dipilih adalah n-heksana:etil asetat 2:2 karena
perbedaan Rf antara bahan baku dan arilamida-3 lebih besar dibandingkan dengan
n-heksana:etil asetat 1:3 dan 3:1. Pada fase gerak n-heksana:etil asetat 2:2,
arilamida-3 memiliki faktor retensi (Rf) sebesar 0,55 dan bahan baku
(3,4,5-trimetoksianilin) sebesar 0,38. Perbedaan Rf ini menunjukkan bahwa produk hasil
sintesis merupakan senyawa yang berbeda dengan bahan baku atau dengan kata lain
telah berhasil disintesis. Profil KLT arilamida-3 dibandingkan dengan bahan baku
disajikan pada Lampiran 8.
Produk hasil sintesis dinyatakan murni secara KLT sehingga tidak
diperlukan pemurnian dengan kromatografi kolom. Uji yang dilakukan selanjutnya
yaitu uji titik lebur untuk mengetahui perbedaan jarak lebur antara senyawa hasil
sintesis dengan bahan baku. Apabila terjadi perbedaan yang signifikan antara bahan
baku dengan senyawa hasil sintesis maka prediksi bahwa arilamida-3 sudah
terbentuk semakin kuat. Selain itu, jarak lebur mengindikasikan kemurnian suatu
senyawa yang apabila berjarak kurang dari ≤1,5°C maka dinyatakan murni secara titik lebur. Hasil percobaan menunjukkan bahwa senyawa hasil sintesis memiliki
3,4,5-trimetoksianilin yang memiliki jarak lebur 111-114°C (Oakwood Products, 2018).
Jarak lebur yang lebih dari 1,5°C berarti mengindikasikan senyawa belum murni
100% karena jarak lebur yang lebar menunjukkan masih terdapat pelarut atau
reagen yang masih belum terbilas atau teruapkan. Pemurnian senyawa dapat
dilakukan dengan rekristalisasi atau kromatografi kolom agar mendapatkan jarak
lebur yang sesuai dengan syarat kemurnian.
Rendemen produk yang didapatkan sebanyak 23,5%. Rendemen ini masih
jauh dari kriteria ideal (100%) sehingga masih memerlukan optimasi terkait mol
bahan, suhu, katalisator, atau lama pengadukan pada prosedur sintesis dan
pemurniannya. Perhitungan rendemen disajikan pada Lampiran 9.
Elusidasi Struktur
Kerangka hidrokarbon senyawa hasil sintesis ditentukan dengan
spektroskopi NMR yang terdiri dari proton-1 (1H) dan karbon-13 (13C). Spektrum 1H-NMR disajikan pada Gambar 4 yang menunjukkan sinyal-sinyal sebagai
berikut: sinyal pada pergeseran 2,809 ppm dan 2,935 ppm adalah proton etilen (B)
sedangkan sinyal pada pergeseran 3,716 ppm dan 3,890 ppm adalah proton etilen
(A). Kedua set proton ini menegaskan bahwa senyawa hasil sintesis sudah
terbentuk. Pola splitting sinyal kedua set tersebut adalah triplet. Hal ini karena
kedua set proton saling bertetangga dengan jumlah proton tetangga yang tidak
ekivalen sebanyak 2. Normalnya kedua set proton ini muncul sebagai 2 sinyal
triplet, namun hasil percobaan menunjukkan munculnya 4 sinyal triplet pada jarak
yang saling berdekatan. Hal ini mungkin disebabkan 2 proton pada C yang sama
bisa merasakan 2 kali lingkungan magnetik dari proton tetangganya. Hal ini
ditegaskan dengan jumlah integrasi sebanyak 2 untuk 2 sinyal triplet yang saling
berdekatan. J-coupling constant untuk kedua sinyal triplet = 7 Hz yang
mengindikasikan bahwa kedua set proton bertetangga secara langsung. Proton
etilen (A) berada pada geseran kimia yang lebih deshielded dibandingkan dengan
proton etilen (B) karena proton (A) terikat langsung dengan atom Br yang memiliki
elektronegatifitas tinggi (Fessenden, 1986, Pavia et al., 2015).
Proton selanjutnya adalah metoksi yang muncul pada geseran 3,853 ppm
sinyal pada geseran 3,817 ppm adalah metoksi (E). Hal ini karena metoksi (D) lebih
dekat dengan gugus amida yang merupakan Electron Withdrawing Group (EWG)
sehingga kurang terlindungi dibandingkan dengan metoksi (E) yang berada pada
posisi para (Pavia et al., 2015). Selain itu, berdasarkan integrasinya proton (D)
dihitung sejumlah 6 sedangkan proton (E) dihitung sejumlah 3 sehingga sesuai
dengan prediksi strukturnya. Penegasan selanjutnya kedua sinyal bentuknya singlet.
Hal ini juga sesuai karena ketiga proton tidak mempunya tetangga yang tidak
ekivalen. Perbesaran spektrum 1H-NMR pada geseran 2,6-4,1 ppm disajikan pada
Lampiran 10.
Proton selanjutnya adalah proton pada benzena (C) yang muncul pada
geseran 6,841 ppm. Integrasi proton (C) dihitung sejumlah 2. Hal ini sesuai dengan
prediksi karena proton pada benzena (C) berada pada lingkungan yang sama atau
Proton Geseran (ppm)
Splitting Integrasi J-coupling constant (Hz)
Gambar 4. Spektrum 1H-NMR senyawa arilamida-3 dengan ditandakannya
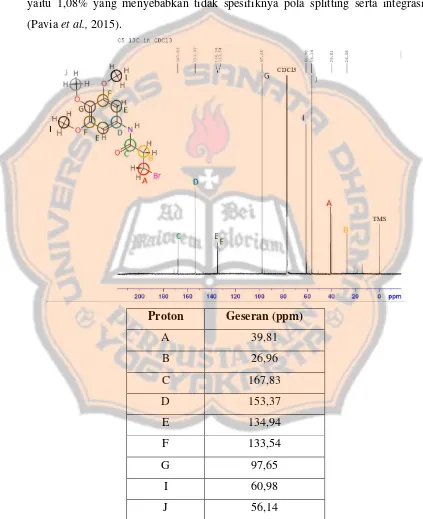
masing-masing sinyal A, B, C, D, dan E beserta karakteristik masing-masing-masing-masing sinyal Pada spektrum 13C-NMR, terdapat 9 sinyal yang diindikasi sebagai karbon
pada senyawa hasil sintesis. Karbon etilen (A) dan (B) muncul pada geseran 39,81
ppm dan 26,96 ppm. Karbon metoksi (I) dan (J) muncul pada geseran 60,98 ppm
dan 56,14 ppm. Karbon pada benzena (G), (F), (E), dan (D) muncul pada geseran
97,65 ppm, 133,54 ppm, 134,94 ppm, dan 153,37 ppm. Karbon karbonil (C) muncul
pada geseran 167,83 ppm. Hal ini sesuai dengan prediksi geseran kimia 13C-NMR
diindikasi lewat geseran kimia dengan mengabaikan pola splitting, integrasi, serta
J-coupling constant. Hal ini karena 13C mempunyai momen magnetik yang rendah
sebesar 67,28 radians/Tesla dibandingkan dengan 1H yang mempunyai momen
magnetik sebesar 267,53 radians/Tesla. Selain itu, kelimpahan 13C di alam kecil
yaitu 1,08% yang menyebabkan tidak spesifiknya pola splitting serta integrasi
(Pavia et al., 2015).
Proton Geseran (ppm)
A 39,81
B 26,96
C 167,83
D 153,37
E 134,94
F 133,54
G 97,65
I 60,98
J 56,14
masing-Metode elusidasi selanjutnya adalah FTIR yang bertujuan untuk mengetahui
gugus fungsional yang terdapat pada arilamida-3. Suatu molekul akan menyerap
radiasi inframerah yang menyebabkan molekul tersebut berada dalam keadaan
vibrasi tereksitasi kemudian energi yang terserap akan dibuang dalam bentuk panas
apabila molekul kembali ke keadaan dasar. Energi yang terserap akan menyebabkan
ikatan bervibrasi ulur (stretching vibration) atau tekuk (bending vibration).
Molekul yang dapat menyerap radiasi inframerah secara baik adalah molekul yang
memiliki momen dipol yang tinggi (Fessenden, 1986, Pavia et al., 2015).
Berdasarkan spektrum inframerah, terdapat pita pada daerah sekitar
bilangan gelombang (ῡ) 1658,78 cm-1 yang menunjukkan adanya gugus C karbonil (C=O) dan pita yang melebar pada daerah sekitar bilangan gelombang 3448,72 cm -1 yang menunjukkan adanya gugus NH (-NH-). Adanya gugus C karbonil dan NH
ini menandakan pada arilamida-3 terdapat gugus amida (-CONH-). Pada daerah
500-1500 cm-1 atau daerah sidik jari dapat dilihat pita-pita yang berbeda polanya
dengan senyawa awal. Spektrum inframerah senyawa awal disajikan pada
Lampiran 12 (Pubchem, 2019). Spektrium inframerah arilamida-3 disajikan pada
Gambar 6.
Gambar 6. Spektrum inframerah senyawa arilamida-3
Metode elusidasi selanjutnya adalah dengan GC-MS yang bertujuan untuk
mengetahui bobot molekul dari arilamida-3. Senyawa dipisahkan terlebih dahulu
molekulnya. Puncak F merupakan puncak tertinggi yang menunjukkan puncak
tersebut adalah senyawa arilamida-3 karena terdapat dalam konsentrasi yang paling
tinggi. Kromatogram GC arilamida-3 disajikan pada Gambar 7.
Gambar 7. Kromatogram GC arilamida-3 dengan ditandakannya masing-masing puncak A, B, C, D, dan E
Puncak tertinggi pada kromatogram memiliki m/z sebesar 317 yang terbaca
pada spektrum MS. Hal ini mendukung kebenaran hasil sintesis arilamida-3 yang
memiliki bobot molekul sebesar 317,03 g/mol. Selain itu, senyawa arilamida-3
memiliki atom brom (Br) yang pada spektra MS memiliki ciri khas bentuk spektra
kembar dengan nilai m/z M+2 (ion molekul plus 2 satuan massa) dan intensitas
kedua peak sama. Hal ini dikarenakan Br yang terdapat pada alam terdiri dari
campuran 50,5% 79Br dan 49,5% 81Br (Zhai and Zhang, 2009, Pavia et al., 2015).
Pada spektrum MS senyawa arilamida-3 yang disajikan pada Gambar 8, terdapat
peak kembar pada 317 m/z yang menunjukkan adanya atom Br pada senyawa
arilamida-3.
Gambar 8. Spektrum MS senyawa arilamida-3
Kristalografi x-ray merupakan metode penentuan struktur yang paling sahih
merefleksikan inti dari struktur senyawa tersebut seperti yang disajikan pada
Gambar 9. Secara keseluruhan, struktur arilamida-3 dipastikan kebenarannya mulai
dari 1H-NMR, 13C-NMR, FTIR, MS, dan kristalografi sinar X sehingga
disimpulkan bahwa senyawa hasil sintesis terbentuk sesuai dengan hipotesisnya.
Gambar 9. Struktur 3D kristalografi sinar X senyawa arilamida-3 Uji Aktivitas In Vitro
Senyawa arilamida-3 kemudian dilakukan uji aktivitas penghambatan
enzim MMP-9 in vitro. MMP-9 yang merupakan enzim protease dan memiliki
aktivitas proteolitik akan memotong ikatan peptida pada substratnya. Substrat
dalam pengujian ini mengikat gugus fluorofor sehingga ketika terpotong oleh
MMP-9, gugus fluorofor terlepas dan terbaca fluoresensinya oleh
spektrofluorometri pada panjang gelombang (λ) eksitasi325 nm dan emisi 393 nm. Fluoresensi yang tinggi menunjukkan aktivitas enzim sebanyak 100%, sedangkan
fluoresensi yang rendah menunjukkan adanya penghambatan pada aktivitas enzim.
Senyawa arilamida-3 memiliki persen penghambatan sebesar 5% pada konsentrasi
200 µg/mL yang disajikan pada Tabel 1. Perhitungan IC50 tidak dapat dilakukan
karena persen penghambatan yang didapat dibawah 50%. Berdasarkan persen
penghambatan, senyawa arilamida-3 termasuk dalam kategori low active
(Aderogba, 2013). Penambahan gugus metoksi sebagai EDG pada bagian para dan
meta gugus arilamida pada senyawa arilamida-3 ternyata menurunkan nilai persen
penghambatan dibandingkan dengan senyawa milik Adhipandito dan Ludji yang
penambahan gugus EWG dalam senyawa penghambat aktivitas enzim MMP-9
lebih baik dibandingkan dengan gugus EDG.
Tabel 1. Perhitungan persen penghambatan senyawa arilamida-3 terhadap MMP-9 Fluoresens
Rata-Aktivitas inhibitor = rata-rata/32332 x 100%; Penghambatan enzim = 100% - aktivitas inhibitor
KESIMPULAN
Hasil penelitian menunjukkan bahwa senyawa arilamida-3 dapat disintesis
dari 3,4,5-trimetoksianilin dan 3-bromopropionil klorida dengan katalisator piridin
melalui mekanisme reaksi SNA dengan produk hasil sintesis berupa serbuk
berwarna putih yang larut dalam kloroform dan memiliki titik lebur 115,7-120,1°C.
Senyawa arilamida-3 dapat menghambat aktivitas MMP-9 sebesar 5% pada
konsentrasi 200 µg/mL yang berasosiasi pada aktivitas yang rendah.
SARAN
Berdasarkan nilai persen penghambatan senyawa arilamida-3 terhadap
aktivitas enzim MMP-9 in vitro yang didapatkan sebesar 5% pada konsentrasi 200
gugus EDG akan mengurangi nilai persen penghambatan aktivitas enzim MMP-9
sehingga disarankan untuk penelitian selanjutnya tidak mempertimbangkan gugus
EDG dalam modifikasi struktur suatu senyawa yang bertujuan untuk menghambat
enzim MMP-9.
UCAPAN TERIMA KASIH
Penulis berterima kasih kepada Indonesia Toray Science Foundation
periode 2017/2018 dan Divisi Penelitian dan Pengembangan BEM Fakultas
DAFTAR PUSTAKA
Adegoke, O.A., 2011. Analytical, biochemical and synthetic applications of para-dimethylaminobenzaldehyde. International Journal of Pharmaceutical Sciences Review and Research, 11 (2), 17–29.
Aderogba, M.A., 2013. Antimicrobial and Selected In Vitro Enzyme Inhibitory Effects of Leaf Extracts, Flavonols and Indole Alkaloids Isolated from Croton menyharthii. Molecule, 18, 12633-12644.
Adhipandito, C.F., 2017. Sintesis Analog Purin (FFUSD-001) dan Studi In Silico Terhadap Matrix Metalloproteinase-9 (MMP-() Hemopexin Domain sebagai Kandidat Anti-Kanker Payudara. Skripsi. Universitas Sanata Dharma.
Arifiyanto, A., 2001. Pengaruh Penambahan Basa Natrium Hidroksida dan Piridin dalam Sintesis Benzoilanilida.
Bauvois, B., 2012. New facets of matrix metalloproteinases MMP-2 and MMP-9 as cell surface transducers: Outside-in signaling and relationship to tumor progression. Biochimica et Biophysica Acta - Reviews on Cancer, 1825 (1), 29–36.
Cathcart, J., Pulkoski-Gross, A., and Cao, J., 2015. Targeting matrix metalloproteinases in cancer: Bringing new life to old ideas. Genes and Diseases, 2 (1), 26–34.
Chaffer, C.L. and Weinberg, R.A., 2011. A perspective on cancer cell metastasis.
Science (New York, N.Y.), 331 (6024), 1559–1564.
Dufour, A., Sampson, N.S., Li, J., Kuscu, C., Rizzo, R.C., DeLeon, J.L., Zhi, J., Jaber, N., Liu, E., Zucker, S., and Cao, J., 2011. Small-molecule anticancer compounds selectively target the hemopexin domain of matrix metalloproteinase-9. Cancer Research, 71 (14), 4977–4988.
Fessenden, R.J., Fessenden, J.S., 1986. Kimia Organik Edisi Ketiga. Jakarta: Penerbit Erlangga.
Gialeli, C., Theocharis, A.D., and Karamanos, N.K., 2011. Roles of matrix metalloproteinases in cancer progression and their pharmacological targeting.
FEBS Journal, 278 (1), 16–27.
IARC, 2018. Latest Global Cancer Data [Press Release]. Available from:
https://www.iarc.fr/wp-content/uploads/2018/09/pr263_E.pdf (Accessed: 5 November 2018).
Kahl, T., Schroder, K.-W., Lawrence, F.R., Marshall, W.J., Hoke, H., and Jackh, R., 2012. Aniline. Ullmann’s Encyclopedia of Industrial Chemistry, 2, 108– 137.
Koltunov, K.Y., Sobolev, V.I., and Bondareva, V.M., 2016. Oxidation, oxidative esterification and ammoxidation of acrolein over metal oxides: Do these reactions include nucleophilic acyl substitution? Catalysis Today, 1–5.
Ludji, D.P.K.S., 2017. Sintesis Analog Purin (FUSD-002) dan Studi In Silico Terhadap Matrix Metalloproteinase-9 (MMP-9) Hemopexin Domain sebagai Kandidat Anti-Kanker Payudara. Skripsi. Universitas Sanata Dharma.
Oakwood Products, 2018. Safety Data Sheet: 3,4,5-Trimethoxyaniline [online]. Available from: https://ehslegacy.unr.edu/msdsfiles/31329.pdf (Accessed: 19 Januari 2019).
Pavia, D.L., Lampman, G.M., Kriz, G.S., and Vyvyan, J.R., 2015. Introduction to Spectroscopy Fifth Edition. Cengange Learning.
Pubchem, 2019. 3,4,5-Trimethoxyaniline | C9H13NO3 - PubChem [online]. Available from: https://pubchem.ncbi.nlm.nih.gov/compound/3_4_5-trimethoxyaniline#section=Infrared-Spectra (Accessed: 24 Januari 2019).
Smith, M.B. and March, J., 2007. March’s Advanced Organic Chemistry. New Jersey: John Wiley & Sons, Inc.
Ugarte-Berzal, E., Vandooren, J., Bailón, E., Opdenakker, G., and García-Pardo, A., 2016. Inhibition of MMP-9-dependent degradation of gelatin, but not other MMP-9 substrates, by the MMP-9 hemopexin domain blades 1 and 4. Journal of Biological Chemistry, 291 (22), 1–13.
Wahidin, M., Noviani, R., Hermawan, S., Andriani, V., Ardian, A., and Djarir, H., 2012. Population-Based Cancer Registration in Indonesia. Asian Pacific Journal of Cancer Prevention, 13 (4), 1709–1710.
Welch, D.R., Steeg, P.S., and Rinker-schaeffer, C.W., 2000. Molecular biology of breast cancer metastasis Genetic regulation of human breast carcinoma metastasis. Breast Cancer Research, 2 (6), 1–6.
Yousef, E.M., Tahir, M.R., St-Pierre, Y., and Gaboury, L.A., 2014. MMP-9 expression varies according to molecular subtypes of breast cancer. BMC Cancer, 14, 1–12.
Zhai, H. and Zhang, X., 2009. A new method for differentiating adducts of common drinking water DBPs from higher molecular weight DBPs in electrospray ionization-mass spectrometry analysis. Water Research, 43 (8), 2093–2100. Zhang, L., Wang, X. jun, Wang, J., Grinberg, N., Krishnamurthy, D.K., and
LAMPIRAN
Lampiran 1. Representasi tata letak 96-microwell plate dengan B: buffer, Sp: sampel senyawa arilamida-3, E: enzim MMP-9, dan Sb: substrat disertai dengan
volume dalam µL.
Lampiran 3. (a) Sintesis senyawa arilamida-3 pada awal pengadukan, (b) Crude product setelah dibilas dengan aquadest dan dibiarkan mengering.
Lampiran 4. (a) Serbuk 3,4,5-trimetoksianilin yang berwarna sedikit kekuningan (b) Serbuk arilamida-3 yang berwarna putih
Lampiran 5. Hasil Uji Kelarutan Senyawa Arilamida-3
Pelarut Kelarutan Perbandingan
Kloroform Larut 1:20
Air Tidak larut 1:1000
Aseton Larut 1:30
Etil asetat Larut 1:20
n-heksana Tidak larut 1:1000
DMSO Larut 1:30
Etanol Agak sukar larut 1:80
Lampiran 7. Hasil uji pendahuluan DAB-HCl antara bahan baku dan arilamida-3.
Lampiran 8. Profil KLT arilamida-3 (Rf = 0,55) dibandingkan dengan bahan baku (Rf = 0,38).
1
2 1 = Bahan baku (Rf 0,38)
Lampiran 9. Perhitungan bahan sintesis dan hasil rendemen senyawa arilamida-3. Perhitungan bahan:
1. 3,4,5-trimetoksianilin (BM: 183,2 g/mol) sebanyak 3,59 mmol
3,59 mmol x 183,2 g/mol = 657,69 mg = 0,66 g
2. Piridin (BM: 79,1 g/mol, massa jenis: 0,98 g/mL) sebanyak 3,59 mmol
3,59 mmol x 79,1 g/mol = 283,97 mg = 0,28 g
Massa arilamida-3 teoritis (BM: 317 g/mol)= 3,59 mmol x 317 g/mol = 1138,03 mg
Massa arilamida-3 yang didapat = 268 mg
Rendemen intermediet = 𝑚𝑎𝑠𝑠𝑎 𝑦𝑎𝑛𝑔 𝑑𝑖𝑑𝑎𝑝𝑎𝑡
𝑚𝑎𝑠𝑠𝑎 𝑡𝑒𝑜𝑟𝑖𝑡𝑖𝑠 𝑥 100% =
268 𝑚𝑔
Lampiran 10. Perbesaran spektrum 1H-NMR pada geseran 2,6-4,1 ppm.
BIOGRAFI PENULIS
Penulis skripsi berjudul “Sintesis Turunan
Arilamida-3 dan Uji Aktivitas In Vitro Terhadap
Enzim Matrix Metalloproteinase-9 (MMP-9)
Sebagai Kandidat Anti-Kanker Payudara” memiliki nama lengkap Kevin Cahaya Putra. Penulis lahir di
Yogyakarta pada tanggal 6 Maret 1997 sebagai anak
pertama dari tiga bersaudara dari pasangan Iwan
Binanto dan Alm. Carla Santoso. Pendidikan formal
yang pernah ditempuh penulis diselesaikan di TK
Mutiara Persada (2001-2003), SD Tarakanita (2003-2009), SMP Stella Duce 1
(2009-2012), dan SMA Negeri 2 Yogyakarta (2012-2015). Penulis kemudian
melanjutkan Pendidikan Sarjana 1 di Fakultas Farmasi Universitas Sanata Dharma
pada tahun 2015. Selama menempuh kuliah, penulis pernah mendapatkan prestasi
berupa Juara II pada lomba Pharmaceutical Industry Case Study (PICS) 2017 di
ITB dan terlibat sebagai anggota tim dalam Program Kreativitas Mahasiswa
Pengabdian Masyarakat (PKM-M) yang didanai oleh Direktorat Jendral Pendidikan
Tinggi (Dikti). Selain itu, penulis pernah menjadi Ketua dari grup penelitian Drug
Discovery Research Group (DDRG) (2018), Ketua I inisiasi fakultas TITRASI
(2017), Koordinator Divisi Perlengkapan dan Table Pharmacy Performance (2016)
dan Lomba Cerdas Cermat Kimia (2016), anggota Divisi Perlengkapan inisiasi
fakultas TITRASI (2016), anggota Divisi Perlengkapan Pharmacy Performance
(2015) dan Road to School (2015). Penulis juga berperan aktif sebagai asisten