UJI TOKSISITAS DAN ANALISIS KANDUNGAN SENYAWA MINYAK ATSIRI
RIMPANG TEMU PUTIH (Curcuma zedoaria (Berg.) Rosc.)
Wiwik Susanah Rita
1, I Made Dira Swantara
1, I Made Sughita
2, Ni Made Puspawati
1,
Lestari Mamik Setiani
11
Jurusan Kimia FMIPA,
2Jurusan Ilmu dan Teknologi Pangan Fakultas Teknologi Pertanian,
Universitas Udayana
E-mail: wiwiksr@yahoo.com; wiwiksr@kimia.unud.ac.id
ABSTRACT
Analysis compounds and toxicity test of Curcuma zedoaria (Berg.) Rosc. essential oil has been done. The
essential oil was extracted by steam distillation, while the toxicity test, as a prescreening for compounds suspected to have antitumor activity, was done by
Brine Shrimp Lethality Test (BSLT) against Artemia salina
Leach larvae. The toxic fraction was analyzed by Gas Chromatography and Mass Spectroscopy (GC-MS). Twenty Kg of temu putih was freshly steam distilled which gave 15.30 mL (13.49 g) gold oil. The oil was then subjected towards BSLT and the result showed the oil was active with LC50 of 19.96 ppm. The composition of essential oil was analyzed using MS. The GC-MS spectra showed that the essential oil of temu putih was composed of eight major components including camphen, β-pinen, 1,3,3-trimetil-sineol, camphor, 1-ethenyl-1-methyl-2,4-bis(1-methylethenyl) cyclohexane, curzerene, germacron, and velleral. Keywords: Curcuma zedoaria (Berg.) Rosc., essential oils, toxicity, Artemia salina Leach.
PENDAHULUAN
Semakin banyaknya kasus kematian akibat penyakit kanker menyebabkan terus dikembangkannya obat yang dapat menghambat pertumbuhan dan penyebaran sel kanker dalam tubuh. Keragaman tumbuhan Indonesia memberikan potensi untuk dikembangkannya suatu obat tradisional yang dapat menghambat atau menghentikan pertumbuhan sel-sel kanker. Salah satu tumbuhan yang dipercaya dapat mengatasi perkembangan sel kanker tersebut adalah temu putih (Curcuma zedoaria Rosc.). Bagian yang biasanya
digunakan untuk pengobatan adalah rimpangnya. Beberapa penelitian menunjukkan bahwa rimpang temu putih (Curcuma zedoaria) mempunyai banyak
manfaat diantaranya mempunyai aktivitas antimikroba, yaitu antibakteri dan antijamur (Bugno et al., 2007;
Wilson et al., 2005; Ficker, et al., 2003). Seo et al., (2005)
melaporkan bahwa ekstrak air rimpang temu putih berperanan dalam menghambat penyebaran sel kanker melanoma B16, sementara Kim et al., (2005) menyatakan
bahwa ekstrak air rimpang temu putih tersebut dapat digunakan untuk terapi penyakit liver kronis. Menurut Mau et al., (2003), minyak atsiri epikurzerenon,
kurzerena, and azulenon juga berpotensi sebagai antioksidan.
Rimpang segar temu putih pada konsentrasi 50, 100, 150, dan 200 mikrogram/mL mempunyai potensi kematian sel kanker di atas 50 persen. Sedangkan untuk sediaan jadi temu putih (ZF kapsul) mempunyai potensi kematian sel kanker di bawah 50 persen pada dosis yang sama (Gklinis, 2004). Sukmana (2006) melaporkan bahwa pemberian ekstrak Curcuma zedoaria
pada mencit jantan dapat meningkatkan jumlah sel mukosa kolon mencit yang mengalami apoptosis setelah dipapar 9,10-Dimethyl-1,2-benz-(a)anthracene (DMBA).
Rimpang temu putih mengandung 1-2,5% minyak menguap dengan komposisi utama seskuiterpen. Minyak menguap tersebut mengandung lebih dari 20 komponen seperti kurzerenon (zedoarin) yang merupakan komponen terbesar, kurzerena, pirokurkuzerenon, kurkumin, kurkumenon, epikurkumenol, kurkumol (kurkumenol), isokurkumenol, prokurkumenol, dehidrokurdon, furanodienon, isofuranodienon, furanodiena, zederon, dan kurdion. Selain itu mengandung fl avonoid, sulfur, gum, resin, tepung, dan sedikit lemak (Pdpersi, 2006). Sedangkan minyak atsiri yang terdapat pada temu putih asli India ditemukan juga 1,8-sineol (15.9%) and germakron (9.0%) (Purkayastha et al., 2006).
Sementara itu minyak atsiri dalam rimpang temu putih yang diperoleh di sekitar Bali memiliki aktivitas antioksidan dengan % peredaman sebesar 64,63% pada 5 menit pertama dan 73,63% pada menit ke-60, serta dapat menghambat pertumbuhan jamur Candida albicans
(Rita et al., 2008).
Uji toksisitas terhadap larva udang Artemia salina
L digunakan sebagai skrining awal untuk senyawa-senyawa yang diduga mempunyai aktivitas antitumor dan antikanker. Toksisitas yang tinggi dari senyawa uji sangat berkorelasi dengan aktivitas senyawa sebagai antitumor (Colegate, 1993). Uji toksisitas ekstrak n-heksana, kloroform, dan etilasetat rimpang temu putih terhadap larva udang Artemia salina L. menunjukkan bahwa ekstrak n-heksana, koroform, dan etilasetat bersifat toksik dengan LC50 berturut-turut
sebesar 125,9; 28,2; dan 302,0 ppm. (Rita, 2009). Suatu bahan dikatakan bersifat toksik jika nilai LC50nya di bawah 1000 ppm (Meyer et al., 1982).
Oleh karena rimpang temu putih berpotensi sebagai obat yang dapat digunakan untuk menyembuhkan kanker, dan memiliki kandungan utama minyak atsiri, maka perlu dilakukan penelitian tentang uji toksisitas dan analisis kandungan senyawa minyak atsiri rimpang temu putih yang diperoleh di sekitar Bali.
METODOLOGI PENELITIAN Alat dan Bahan
Bahan yang dipergunakan dalam penelitian ini adalah rimpang temu putih yang diperoleh di Denpasar pada bulan Oktober 2009. Penyiapan bahan meliputi determinasi tanaman yang dilakukan di UPT Balai Konversi Tumbuhan Kebun Raya Eka Karya Bali, pengumpulan bahan, pembersihan, dan pemotongan bahan. Bahan uji yang digunakan yaitu Larva udang
Artemia salina L. Bahan kimia yang digunakan dalam
penelitian ini adalah akuades, dimetil sulfoksida (DMSO) Merck, kalsium klorida anhidrat (CaCl2) Merck,
dan ragi.
Alat yang digunakan dalam penelitian ini adalah pisau, timbangan, seperangkat alat destilasi uap (destilasi stahl), botol tempat minyak atsiri, aluminium foil, neraca analitik, pipet mikro, pipet volume, pipet tetes, tabung reaksi, dan seperangkat alat GC-MS QP2010S SHIMADZU.
Tempat penelitian
Penelitian ini dikerjakan di Laboratorium Penelitian Jurusan Kimia FMIPA Universitas Udayana dan Laboratorium Biologi Kelautan Universitas Udayana. Identifi kasi dengan GC-MS dilakukan di Laboratorium Kimia Organik Universitas Gadjah Mada, Yogyakarta. Isolasi minyak atsiri dengan destilasi uap
Metode yang digunakan adalah destilasi uap (destilasi stahl). Rimpang temu putih sebanyak ± 20 kg didestilasi secara bertahap sebanyak 4 kali, dengan setiap kali destilasi menggunakan ± 5 kg rimpang temu putih. Rimpang temu putih dipotong kecil-kecil kemudian dimasukkan ke dalam dandang yang telah berisi air. Dandang yang digunakan dilengkapi dengan kondensor, kemudian dipanaskan dengan api kecil. Destilat yang diperoleh merupakan campuran minyak dan air. Dimana, dengan menggunakan destilasi stahl, minyak dapat langsung terpisah dari air. Namun, minyak perlu dibebaskan lagi dari sisa-sisa air dengan menambahkan CaCl2 anhidrat untuk mengikat air. Minyak atsiri yang diperoleh dapat digunakan untuk uji toksisitas terhadap larva udang Artemia salina L dan
dianalisis menggunakan GC-MS.
Uji toksisitas terhadap larva udang Artemia salina L. Minyak atsiri yang telah diperoleh kemudian diuji
toksisitasnya menggunakan larva udang Artemia salina
L. Pada uji toksisitas, terlebih dahulu dibuat media pertumbuhan larva udang dengan cara menyaring air laut secukupnya. Air laut tersebut dimasukkan ke dalam akuarium yang memiliki sekat berlubang dengan satu bagian dari akuarium dibuat terang sedangkan satu bagian lagi dibuat gelap. Telur Artemia salina L
dimasukkan pada bagian gelap, selanjutnya akuarium disimpan pada tempat yang memiliki penerangan dan diberi oksigen selama 48 jam.
Uji toksisitas dilakukan dengan menyiapkan 10 tabung reaksi, dimana 9 tabung digunakan untuk tempat bahan uji dan 1 tabung untuk kontrol. Sebanyak 20 mg minyak atsiri rimpang temu putih ditimbang, kemudian dilarutkan dalam 2 mL etanol. Selanjutnya, larutan yang diperoleh dipipet masing-masing sebanyak 5 µL, 50 µL dan 500 µL ke dalam tabung reaksi dan pelarutnya diuapkan selama 24 jam. Selanjutnya, dimasukkan 1 mL air laut, 50 µL dimetil sulfoksida, 10 ekor larva udang Artemia salina L, dan setetes ragi roti, kemudian ditambahkan air laut sampai volumenya 5 mL, sehingga konsentrasi masing-masing larutan sebesar 10, 100, dan 1000 ppm.
Sedangkan untuk kontrol, ke dalam tabung reaksi dimasukkan 2 mL air laut, 50 µL dimetil sulfoksida, 10 ekor larva udang Artemia salina L, dan setetes ragi roti, kemudian ditambahkan air laut sampai volumenya 5 mL. Pengamatan dilakukan selama 24 jam. Selanjutnya, dilakukan perhitungan terhadap larva udang Artemia salina L yang mati dan dihitung nilai LC50.
Analisis kualitatif dengan kromatografi gas– spektroskopi massa (GC-MS)
Minyak atsiri yang diperoleh kemudian dianalisis dengan GC–MS untuk mengetahui komponen penyusun minyak atsiri rimpang temu putih. Spektrum massa yang diperoleh dibandingkan dengan spektrum senyawa standar yang telah diketahui dalam database yang telah terprogram pada alat GC–MS.
HASIL DAN PEMBAHASAN Ekstraksi Minyak Atsiri
Sampel yang digunakan dalam penelitian ini adalah 20 kg temu putih yang diekstraksi dengan destilasi uap. Destilasi dilakukan secara bertahap sebanyak 4 kali, dimana setiap destilasi digunakan ± 5 kg sampel temu putih yang telah dibersihkan dan dipotong kecil-kecil. Minyak atsiri yang diperoleh berwarna kuning kental sebanyak 15,30 mL (13,49 g). Minyak atsiri yang diperoleh memiliki densitas sebesar 0,88 g/mL, dengan kadar minyak sebesar 0,067 % b/b, Selanjutnya, minyak atsiri yang diperoleh digunakan untuk uji toksisitas antitumor terhadap larva udang Artemia salina Leach.
Uji Toksisitas Minyak Atsiri
Hasil uji toksisitas minyak atsiri rimpang temu putih terhadap larva udang Artemia salina L. disajikan
dalam Tabel 1 dan Gambar 1. Hasil uji toksisitas ini
Konsentrasi ppm
Jumlah larva yang
mati Jumlah larva yang hidup Akumulasimati Akumulasi hidup % kematian
1 2 3 1 2 3
10 7 6 8 3 4 2 3,7 16,6 24,18
100 10 10 10 0 0 0 8,4 5,3 61,13
1000 10 10 10 0 0 0 18,4 0 100.00
menunjukkan bahwa minyak atsiri rimpang temu putih mempunyai nilai LC50 sebesar 19,96 ppm, sehingga dapat dikatakan bahwa minyak atsiri rimpang temu putih berpotensi sebagai antitumor.
Tabel 1. Hasil uji toksisitas minyak atsiri rimpang temu putih terhadap larva udang Artemia salina L.
Keterangan: Jumlah larva tiap konsentrasi 10 ekor (total larva pada tiga konsentrasi adalah 30 ekor).
Gambar 1. Grafi k log konsentrasi Vs % kematian minyak atsiri temu putih Analisis Minyak Atsiri Rimpang Temu Putih dengan
GC-MS
Minyak atsiri rimpang temu putih yang diperoleh dari proses destilasi uap dianalisis komponen senyawa yang terkandung di dalamnya dengan menggunakan GC-MS. Kromatogram hasil analisis minyak atsiri
Gambar 2. Kromatogram hasil analisis minyak atsiri rimpang temu putih
rimpang temu putih dengan GC memperlihatkan 19 puncak seperti yang ditunjukkan dalam Gambar 2.
Masing-masing puncak diidentifi kasi lebih lanjut dengan spektrometer massa, dimana setiap senyawa memiliki pola fragmentasi massa yang spesifi k. Identifi kasi dilakukan dengan membandingkan spektrum massa masing-masing puncak dengan senyawa-senyawa yang sudah diketahui dan terprogram dalam database GC-MS (WILEY 7), sehingga dapat diduga senyawa-senyawa penyusun minyak atsiri rimpang temu putih.
Hasil analisis spektrum massa dari kromatogram minyak atsiri rimpang temu putih dan perkiraan senyawa berdasarkan database WILEY 7 dapat dilihat pada Tabel 2.
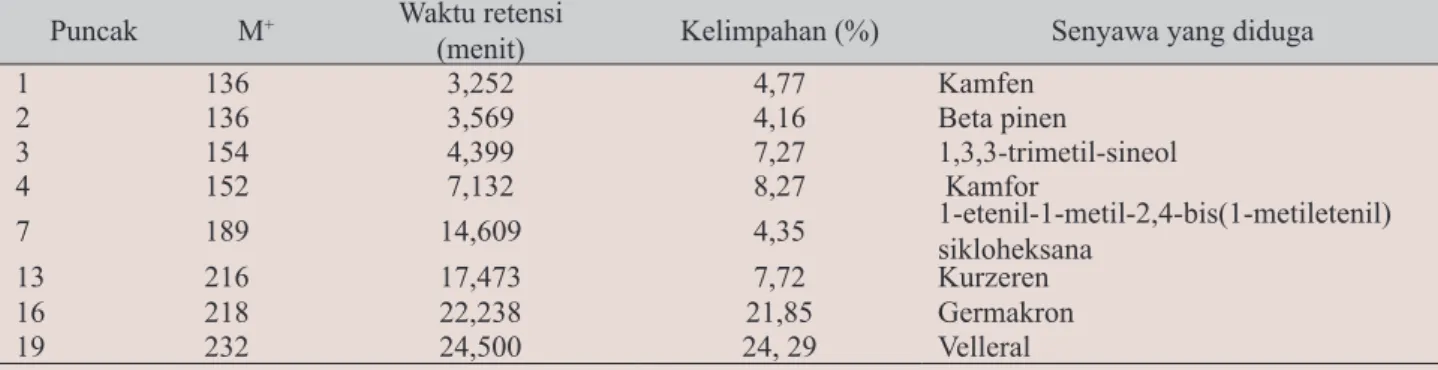
Tabel 2. Senyawa-senyawa yang diduga dari masing-masing puncak pada kromatogram minyak atsiri rimpang temu putih berdasarkan database WILEY 7.
Spektrum massa dari senyawa kamfen (4,77%) dapat dilihat pada Gambar 3.
Gambar 3 (a) Spektrum massa puncak 1; (b) Spektrum massa database standar senyawa kamfen
Tabel 3. Kemungkinan fragmen yang hilang dari senyawa kamfen a.
b.
Puncak M+ Waktu retensi
(menit) Kelimpahan (%) Senyawa yang diduga
1 136 3,252 4,77 Kamfen 2 136 3,569 4,16 Beta pinen 3 154 4,399 7,27 1,3,3-trimetil-sineol 4 152 7,132 8,27 Kamfor 7 189 14,609 4,35 1-etenil-1-metil-2,4-bis(1-metiletenil) sikloheksana 13 216 17,473 7,72 Kurzeren 16 218 22,238 21,85 Germakron 19 232 24,500 24, 29 Velleral
Berdasarkan data dari library WILEY 7 berat molekul senyawa kamfen adalah 136. Oleh karena itu ion molekul (M+) senyawa pada puncak 1 adalah m/z 136 dengan puncak dasar pada m/z 93. Dengan melihat berat molekul dan pola fragmentasi berdasarkan
pendekatan WILEY 7, maka diduga senyawa puncak 1 adalah kamfen (2,2-dimetil-3-metilenbisiklo-heptana).
Spektrum massa senyawa kamfen menunjukkan hilangnya fragmen-fragmen seperti terlihat pada Tabel 3.
No m/z Kemungkinan fragmen yang hilang
1 136 M+ 2 121 M+ - 15 - .CH 3 3 107 M+ - 29 - .CH 2 CH3 4 93 M+ - 43 - .C 3H7 5 79 (M+ - 15)-28-14 - CH 2 6 67 (M+ - 43)-26 - C 2H2 7 53 (M+ - 15)-28-14-26 - C 2H2
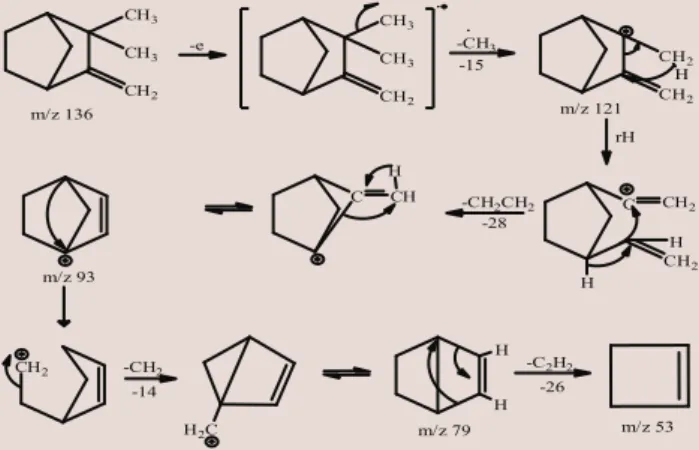
Senyawa kamfen memiliki struktur sebagai berikut:
Fragmentasi yang terjadi pada senyawa kamfen sesuai dengan spektrum massa di atas dapat diperkirakan sebagai berikut.
CH3
CH3
CH2
Berdasarkan data dari GC-MS, maka senyawa-senyawa mayor yang terdeteksi selain kamfen adalah beta pinen, 1,3,3-trimetil-sineol, kamfor, 1-etenil-1-metil-2,4-bis(1-metiletenil) sikloheksana, kurzeren, germakron, dan velleral. Struktur senyawa-senyawa tersebut dapat dilihat pada Gambar 4.
CH3 CH3 CH2 H3C H3C CH2 O CH3 CH3 CH3 CH3 H3C H3C O
kamfen β-pinen Sineol Kamfor
CH CH2 CH3 C CH3 CH2 H2C C CH3 O Me CH2=C-Me Me CH2=C-Me CMe O Me Me CH3 CH3 CH3 HC HC O O 1-etenil- 1-metil- 2,4-bis(1-metiletenil) sikloheksana
Kurzerena Germakron Velleral
Gambar 4. struktur senyawa-senyawa mayor yang terdapat dalam minyak atsiri rimpang temu putih Curcuma zedoaria (Berg) Rosc.)
Senyawa velleral muncul dengan persentase kelimpahan terbesar yaitu 24,29%, dimana senyawa ini termasuk dalam golongan azulen. Menurut Rita
et al., 2008, velleral dalam minyak atsiri menyebabkan
minyak atsiri aktif sebagai antijamur terhadap jamur
Candida albicans dan antioksidan. Senyawa β-pinen juga muncul dengan persentase kelimpahan 4,16% dimana senyawa ini termasuk dalam golongan
monoterpen hidrokarbon yang banyak terkandung dalam minyak atsiri. Senyawa terpena lainnya yang muncul adalah kamfen (4,77%), 1,3,3-trimetil-sineol (7,27%), kamfor (8,27%), dan germakron (21,85%). Dengan adanya senyawa terpena dan kesinergisan komponen-komponen senyawa lain dalam minyak atsiri sehingga dapat mengoptimalkan toksisitas minyak atsiri.
KESIMPULAN DAN SARAN Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan bahwa minyak atsiri rimpang
temu putih (Curcuma zedoaria (Berg.) Rosc.) memiliki
densitas sebesar 0,88 g/mL, kadar minyak sebesar 0,067 % b/b, dan bersifat toksik terhadap larva udang
Artemia salina Leach dengan nilai LC50 sebesar 19,96 ppm. Senyawa yang terdapat dalam minyak atsiri yaitu terdiri dari 19 senyawa dengan 8 senyawa mayor antara lain kamfen (4,77%), beta pinen (4,16%), 1,3,3-trimetil-sineol (7,27%), kamfor (8,27%), 1-etenil-1-metil-2,4-bis(1-metiletenil) sikloheksana (4,35%), kurzeren (7,72%), germakron (21,85%), dan velleral (24,29%).
Saran
Saran yang dapat dikemukakan adalah perlu dilakukannya penelitian antitumor minyak atsiri
rimpang temu putih (Curcuma zedoaria (Berg.) Roscoe)
terhadap sel tumor.
UCAPAN TERIMA KASIH
Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada DP2M Ditjen Dikti sebagai penyedia dana dan Lembaga Penelitian Universitas Udayana yang telah memfasilitasi dalam penyaluran dana sehingga penelitian ini dapat berlangsung. Serta Semua pihak yang telah membantu penulis dalam menyelesaikan penelitian ini.
DAFTAR PUSTAKA
Bugno, A., Nicoletti, M.A., Almodovar, A.A.B, Pereira, T.C., and Auricchio, M.T. 2007. Antimicrobial
effi cacy of Curcuma zedoaria extract as assessed
by linear regression compared with commercial
CH3 CH3 CH2 m/z 136 -e CH3 CH3 CH2 -CH3 -15 CH2 CH2 Η rH C CH2 CH2 H H -CH2CH2 -28 C CH H CH2 -CH2 -14 m/z 93 m/z 121 H2C H H m/z 79 -C2H2 -26 m/z 53
mouthrinses, Braz. J. Microbiol. Vol.38 no.3.\
Colegate, S.M., and Molyneux, R.J., 1993, Bioactive
Natural Product, CRC Press, London.
Ficker, C.E., Smith, M.L., Susiarti, S., Leaman, D.J., Irawati, C., and Arnason, J.T. 2003. Inhibition of human pathogenic fungi by members of Zingiberaceae used by the Kenyah (Indonesian
Borneo), Journal of Ethnopharmacology, Vol. 85, Issue
2-3, p. 289-293.
Kim, D-I, Lee, T-K; Jang T-H, and Kim, C-H. 200., The inhibitory effect of a Korean herbal medicine,
Zedoariae rhizoma, on growth of cultured human
hepatic myofi broblast cells, Life Sciences, Vol. 77,
Issue 8, pp. 890-906.
Mau, J.L, Lai, E.Y.C., Wang, N-P, Chen, C-C; Chang, C-H, and Chyau, C-C. 2003. Composition and antioxidant activity of the essential oil from
Curcuma zedoaria, Food Chemistry, Volume 82,
Issue 4, Pages 583-591.
Meyer, B.N, Ferrigni, N.R, and McLaughlin. 1982. Brine Shrimp: A Convenient General Bioassay for
Active plant Constituents, Journal of Planta Medical
Research, Volume 45, pp. 31-34.
Pdpersi, 2006, Temu Putih (Curcuma zedoria [Berg.]
Rosc.), http//www.pdpersi.co.id./temu putih. Akses 12/02/2008.
Purkayastha, J., Nath, S. C. and Klinkby, N. 2006,
Essential Oil of the Rhizome of Curcuma zedoaria
(Christm.) Rosc. Native to Northeast India,
Journal of Essential Oil Research: JEOR, Mar/Apr
2006.
Rita, W. S., Puspawati, N. M, Marlin Wijayanti, N. P, 2008, Aktivitas Antijamur dan Antioksidan
Minyak Atsiri Rimpang Temu Putih (Curcuma
zedoaria Rosc.), Proceeding SNHKI, ISBN
978-979-8286-83-4.
Rita, W.S., 2009, Penapisan Fitokimia dan Uji Toksisitas Ekstrak Rimpang Temu Putih
(Curcuma zedoaria Rosc.), Medicina, Jurnal Ilmiah
Kedokteran, 40(2): 104-108.
Seo, W-G, Hwang J-C, Kang, S-K; Jin, U-H, Suh, S-J, Moon, S-K, and Kim, C-H. 2005. Suppressive effect of Zedoariae rhizoma on pulmonary
metastasis of B16 melanoma cells, Journal of
Ethnopharmacology, Vol. 101, Issue 1-3, p.249-257.
Sukmana, J. (2006), Efek Curcuma zedoaria terhadap
Peningkatan Apotosis Sel Mukosa Kolon Mencit Jantan yang Terpapar 9,10-dimethyl-1, 2- benz(a)
anthracene, Master Theses dari JIPTUNAIR,
Copyright © 2006 by Airlangga University Library,
Surabaya,
http://adln.lib.unair.ac.id/go.php?id=jiptunair-gdl-s2-2007-sukmanajud-6312&PHPSESSID=5a6769 dff38e0f3f4b3b91df43575469, akses 11/02/2008.
Wilson, B., Abraham, G., Manju, V.S., Mathew, M., Vimala, B., Sundaresan, S., and Nambisan,
B. 2005. Antimicrobial Activity of Curcuma
zedoaria and Curcuma malabarica tubers, Journal of Ethnopharmacology, Vol. 99, Issue 1, 147-151.