commit to user
BAB 2TINJAUAN PUSTAKA DAN LANDASAN TEORI
2.1 Tinjauan Pustaka
2.1.1 Pengertian Air Limbah
Limbah adalah buangan yang kehadirannya pada suatu saat dan tempat tertentu tidak dikehendaki lingkungan karena tidak memiliki nilai ekonomi. Limbah yang memiliki sifat racun dan berbahaya dikenal dengan limbah B3, yang dinyatakan sebagai bahan yang dalam jumlah relatif sedikit tetapi berpotensi untuk merusak lingkungan hidup dan sumber daya. Bila ditinjau secara kimiawi, bahan- bahan ini terdiri dari bahan kimia organik dan anorganik. (Kristanto, Philip. 2002)
Air limbah adalah kotoran dari masyarakat dan rumah tangga dan juga yang berasal dari industri, air tanah, air permukaan serta buangan lainnya. (Sugiharto,
1987)
Sumber Air Limbah
Menurut (Sugiharto, 1987), data mengenai sumber air limbah dapat di pergunakan untuk memperkirakan jumlah rata-rata aliran air limbah dari berbagai jenis perumahan, dan industri. Semuanya ini harus di hitung perkembangannya atau pertumbuhannya sebelum membuat suatu bangunan pengolah air limbah serta merencanakan pemasangan saluran pembawanya.
1. Air limbah rumah tangga (domestic wastes water) adalah air limbah yang berasal dari permukiman penduduk. Pada umumnya air limbah berupa tinja, air seni, air bekas cucian dapur, dan kamar mandi seperti sabun/ detergen. Sumber lain berasal dari air hujan yang tercampur air comberan, dan sebagainya.
2. Air limbah industri (industrial wastes water) berasal dari berbagai jenis industri akibat proses produksi. Zat-zat yang terkandung di dalamnya sangat bervariasi sesuai dengan bahan baku yang dipakai oleh masing-masing industri.
commit to user
2.1.2 Karakteristik Air LimbahKarakteristik air limbah perlu diketahui untuk menentukan cara pengolahan yang tepat. Karakteristik air limbah dibagi menjadi 3 yaitu fisika, kimia dan biologi sebagai berikut: (Siregar, Sakti A. 2005)
1. Karakteristik fisika
Karakteristik fisika air limbah meliputi temperatur, bau, warna dan padatan adalah sebagai berikut :
a. Padatan
Pada limbah cair terdapat padatan organik dan anorganik yang mengendap dan tersuspensi sehingga dapat menyebabkan pendangkalan.
b. Warna
Kekeruhan menunjukkan sifat optis di dalam air karena terganggunya cahaya matahari saat masuk ke dalam air akibat adanya koloid dan suspensi.
c. Bau
Bau merupakan parameter yang subjektif. Pengukuran bau tergantung pada sensitivitas indera penciuman seseorang. Bau disebabkan karena adanya mikroorganisme yang menguraikan bahan organik.
d. Temperatur
Temperatur merupakan parameter yang penting dalam pengoperasian unit pengolahan limbah karena berpengaruh terhadap proses biologis dan fisika. Limbah cair biasanya suhunya lebih tinggi karena adanya proses pembusukan.
2. Karakteristik kimia
Karakter kimia air limbah meliputi senyawa organik dan senyawa anorganik. Senyawa organik adalah karbon yang dikombinasi dengan satu atau lebih elemen-elemen lain (O, N, P, H). Senyawa anorganik terdiri atas semua kombinasi elemen yang bukan tersusun dari karbon organik. Karbon anorganik dalam air limbah terdiri atas sand, grit dan mineral-mineral, baik
suspended maupun dissolved. Elemen-elemen yang terdapat dalam jumlah
commit to user
yang terdapat dalam air limbah biasanya terdiri atas oksigen, nitrogen, karbondioksida, hidrogen sulfida, amonia dan metana.
3. Karakteristik Biologi
Karakteristik biologi digunakan untuk mengukur kualitas air terutama air yang dikonsumsi sebagai air minum dan air bersih. Parameter yang biasa digunakan adalah banyaknya mikroorganisme yang terkandung dalam air limbah. Keberadaan bakteri dalam unit pengolahan limbah merupakan kunci efisiensi proses biologis. Bakteri juga berperan penting untuk mengevaluasi kualitas air.
2.1.3 Air Limbah Industri Batik
Jumlah aliran air limbah yang berasal dari industri sangat bervariasi tergantung dari jenis dan besar-kecilnya industri, pengawasan pada proses industri, derajat penggunaan air, derajat pengolahan air limbah yang ada. Puncak tertinggi aliran tidak akan dilewati, apabila menggunakan tangki penahan dan bak pengaman. Jumlah air limbah yang dihasilkan oleh industri yang tidak menggunakan proses basah diperkirakan sekitar 50 m3/ha/hari. 85-95% dari jumlah air yang dipergunakan adalah berupa air limbah, apabila tidak diolah dan dimanfaatkan kembali. (Sugiharto,1987)
Kualitas limbah cair industri batik sangat tergantung jenis proses yang dilakukan, pada umumnya limbah cair bersifat basa dan kadar organik yang tinggi yang disebabkan oleh sisa-sisa pembatikan.
Proses pencelupan atau pewarnaan pada umumnya merupakan penyumbang sebagian kecil limbah organik, dan warna yang pekat. Apabila langsung dibuang ke badan air dapat mencemari dan mengurangi keindahan sungai atau badan air lainnya.
Pada proses persiapan, yaitu proses nganji , menyumbang zat organik yang banyak mengandung zat padat tersuspensi, apabila tidak segera diolah akan menimbulkan bau yang tidak sedap.
commit to user
2.2 Landasan Teori
2.2.1 Teori Elektrokimia
Secara umum sel elektrokimia dibagi menjadi sel galvani atau sel elektrokimia dan sel elektrolisis. Proses yang terjadi pada sel galvani adalah reaksi kimia berubah menjadi energi listrik, sedangkan di dalam sel elektrolisis sebaliknya, dari energi listrik menjadi energi kimia. Pada sel galvani elektroda positif menjadi katoda, dan elektroda negatif sebagai anoda, sedangkan pada sel elektrolisis sebaliknya, yaitu elektroda negatif sebagai katoda, dan elektroda positif sebagai anoda. (Daryoko, Mulyono. 2009)
Ketika terjadi proses di dalam sel elektrolisis, maka akan ada pelucutan ion-ion bermuatan. Selama proses berlangsung, arus listrik mengalir melalui elektrolit, memberikan energi yang cukup untuk menjalankan reaksi oksidasi dan reduksi. Ion-ion yang bermuatan bergerak, setelah arus listrik mengalir dalam elektrolit. Ion positif bergerak ke elektroda negatif (katoda) dan ion negatif bergerak ke elektroda positif (anoda). Saat ion-ion bermuatan saling bersinggungan dengan elektroda akan terjadi reaksi elektrokimia. Pada elektroda positif (anoda), ion negatif melepaskan elektron dan teroksidasi. Pada elektroda negatif (katoda), ion positif menerima elektron dan tereduksi.
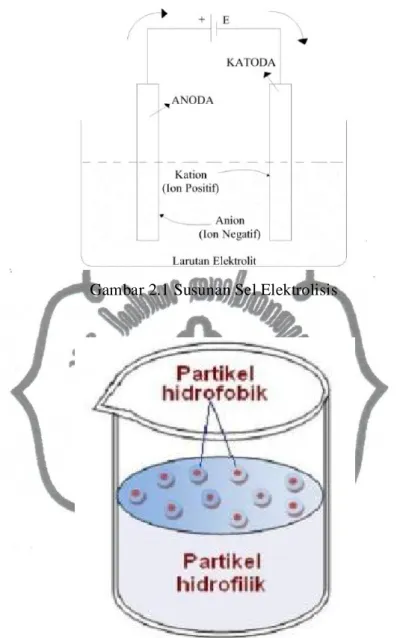
Dalam proses itu maka akan muncul gelembung-gelembung udara. Gelembung-gelembung udara inilah yang akan mengikat zat-zat yang ada di elektrolit atau air limbah. Kemudian zat-zat yang terikat pada gelembung-gelembung udara itu akan terangkat ke permukaan dan mengapung, berbentuk seperti lumpur yang biasanya disebut flok. Terjadinya flok pada sel elektrolisis ini merupakan penerapan dari proses flotasi. Susunan sel elekrtrolisis dapat dilihat pada Gambar 2.1 dan contoh gambar zat yang mengapung karena proses flotasi dapat dilihat pada Gambar 2.2.
commit to user
Gambar 2.1 Susunan Sel Elektrolisis
(Sumber : Zulfikar, 2010)
Gambar 2.2 Contoh Pengapungan Zat dari Proses Flotasi
2.2.2 Deret Volta
Deret Volta adalah urutan logam-logam dari reduktor terkuat sampai reduktor terlemah. Setiap logam mempunyai sifat reduktor, sebab cenderung melepaskan elektron atau mengalami oksidasi. Umumnya deret volta yang sering dipakai adalah :
commit to user
Pada deret volta, unsur logam dengan potensial elektroda lebih negatif ditempatkan dibagian kiri H, sedangkan unsur dengan potensial elektroda yang lebih positif ditempatkan dibagian kanan H.
Semakin ke kiri kedudukan suatu logam dalam deret tersebut, maka: 1. Logam semakin reaktif (semakin mudah melepas elektron).
2. Logam merupakan reduktor yang semakin kuat (semakin mudah mengalami oksidasi).
Sebaliknya, semakin ke kanan kedudukan suatu logam dalam deret tersebut, maka:
1. Logam semakin kurang reaktif (semakin sulit melepas elektron).
2. Logam merupakan oksidator yang semakin kuat (semakin mudah mengalami reduksi)
2.2.3 Hukum Faraday
Faraday mempelajari hubungan antara jumlah listrik yang digunakan pada elektrolisis dengan massa produk yang dihasilkan. Hukum Faraday pertama mengenai elektrolisis menyatakan bahwa jumlah perubahan kimia yang terjadi pada proses elektrolisis bergantung pada jumlah muatan listrik yang melalui sel elektrolisis tersebut. Hukum Faraday kedua menyatakan bahwa elektrolisis jumlah muatan listrik yang sama akan menghasilkan jumlah ekuivalen yang sama pula tanpa bergantung pada jenis zat yang terlibat dalam reaksi elektrolisis. (Bird,
Tony. 1987)
Hukum Faraday mengenai elektrolisis adalah sebagai berat (w) logam yang terelektrolisis di permukaan katoda sebanding dengan jumlah muatan yang dilewatkan (q : columb) yang sebanding dengan kuat arus (I : ampere) di kali waktu (t : detik) untuk jumlah muatan (lt) berat logam yang terelektrolisis sebanding dengan ekuivalen massa molar logam tersebut (M/nF).
commit to user
...Persamaan 2.1
Keterangan :
W : Berat logam terlarut (g) M : Massa Atom Relativ (g/mol) I : Arus (ampere)
ne : Valensi logam t : Waktu (detik)
2.2.4 Flotasi
Flotasi adalah dasar dari proses pemisahan. Flotasi menurut bahasa asing berasal dari kata float yang berarti apung atau kambang. Sehingga flotasi dapat diartikan sebagai fenomena pangapungan atau pengambangan suatu zat yang ada dalam suatu zat cair maupun gas. Seperti halnya sedimentasi, flotasi atau pengapungan digunakan untuk memisahkan padatan dari air. Unit flotasi digunakan jika massa jenis partikel lebih kecil dibandingkan dengan massa jenis air sehingga cenderung mengapung. Flotasi biasa digunakan pada industri metalurgi dan pertambangan, tetapi dapat juga digunakan untuk pengolahan air selokan dan pemurnian air, seperti untuk proses pemisahan lemak dan minyak (oil and grease removal), pemisahan padatan pada pengolahan awal dan pengolahan lanjutan, pemindahan
flok setelah pengolahan kimia, dan pengentalan lumpur (sludge thickening). (Siregar, Sakti A. 2005)
2.2.5 Adsorpsi
Secara umum peristiwa adsorpsi yang terjadi pada larutan terbagi atas dua bagian yaitu adsorpsi fisika dan adsorpsi kimia. Adsorpsi fisika merupakan adsorpsi yang disebabkan oleh gaya Van der Waals yang ada pada permukaan adsorben, panas adsorben biasanya rendah dan terjadi di lapisan pada permukaan adsorben yang umumnya lebih besar dari satu mol. Sedangkan adsorpsi kimia adalah adsorpsi yang terjadi karena adanya reaksi antara zat yang diserap dan adsorben, lapisan molekul pada permukaan adsorben hanya satu lapis dan panas adsorpsinya tinggi.
commit to user
Adsorpsi adalah proses penyerapan suatu zat di permukaan zat lain. Zat yang diserap disebut fase terserap (adsorpat), dan zat yang menyerap disebut adsorben. Adsorpsi terjadi karena gaya tarik molekul-molekul pada permukaan adsorben. Pemanfaatan adsorpsi dalam kehidupan sehari-hari antara lain :
1. Proses pemutihan gula pasir,
2. Penyembuhan sakit perut dengan serbuk karbon atau norit, 3. Penjernihan air keruh dengan menggunakan tawas (Al2(SO4)3),
4. Penggunaan arang aktif,
5. Penggunaan arang halus pada masker, berfungsi untuk menyerap gas yang beracun,
6. Filter pada rokok, yang berfungsi untuk mengikat asap nikotin dan tar.
Kinetika adsorpsi menyatakan adanya proses penyerapan suatu zat oleh adsorben dalam fungsi waktu. Adsorpsi terjadi pada permukaan zat padat karena adanya gaya tarik molekul pada permukaan zat padat atau zat cair. Molekul-molekul pada permukaan zat padat atau zat cair, mempunyai gaya tarik ke arah dalam, karena tidak ada gaya-gaya lain yang mengimbangi. Adanya gaya-gaya ini menyebabkan zat padat dan zat cair, mempunyai gaya adsorpsi. Adsorpsi berbeda dengan absorbsi. Pada absorbsi zat yang diserap masuk ke dalam absorben sedangkan pada adsorpsi zat yang diserap hanya terdapat pada permukaannya. Monolayer adalah lapisan tipis setebal ukuran molekul dan mempunyai kualitas dua dimensi yang unik. (Sukardjo, 1990)
Syarat adsorpsi yaitu:
a. Adsorben harus memiliki luas permukaan yang besar
b. Adsorben harus memiliki micropores dan macropores (misal: karbon aktif dan zeolit)
c. Adsorpsi selektif (harus menghindari kelembaban)
d. Memerlukan waktu kontak yang cukup untuk terjadi pemisahan yang baik e. Perlakuan awal untuk komposisi gas yang rendah
f. Distribusi aliran dalam tumpukan adsorben yang baik g. Adsorben harus mudah diregenerasi
commit to user
Proses adsorpsi yang terjadi pada adsorbsi kimia (kemisorpsi), partikel melekat pada permukaan dengan membentuk ikatan kimia (biasanya ikatan kovalen), dan cenderung mencari tempat yang memaksimumkan bilangan koordinasinya dengan substrat. Peristiwa adsorpsi disebabkan oleh gaya tarik molekul-molekul di permukaan adsorben. Dimana adsorben yang biasa digunakan dalam percobaan adalah kabon aktif, sedangkan zat yang diserap adalah asam asetat. (Keenan,
1999)
Jenis- jenis adsorpsi dapat dilihat pada Tabel 2.1.
Tabel 2.1 Jenis jenis adsorpsi
Adsorpsi Fisika Adsorpsi Kimia
Ikatan lemah antara molekul
gas-padatan Ikatan kimia dengan reaksi
Eksotermis (~0,1 kcal/mol) Eksotermis (> 10 kcal/mol) Tidak ada perubahan fisika atau kimia Perubahan karakteristik adsorben
Reversibel Irreversibel
Adsorpsi multilayer Hampir semua monolayer Tidak menyertai katalis Katalis
(Sumber: Atkins, P. W. 1990)
Peristiwa adsorpsi yang terjadi jika berada pada permukaan dua fase yang bersih ditambahkan komponen ketiga, maka komponen ketiga ini akan sangat mempengaruhi sifat permukaan. Komponen yang ditambahkan adalah molekul yang teradsorpsi pada permukaan. Jumlah zat yang terserap setiap berat adsorben, tergantung konsentrasi dari zat terlarut. Namun demikian, bila adsorben sudah jenuh, konsentrasi tidak lagi berpengaruh. Adsorpsi dan desorpsi (pelepasan) merupakan kesetimbangan. (Atkins, P. W. 1990)
Jika Partikel sol padat ditempatkan dalam zat cair atau gas, maka partikel zat cair atau gas akan terakumulasi. Fenomena ini disebut adsorpsi. Jadi adsorpsi terkait dengan penyerapan partikel pada permukaan zat. Partikel koloid sol memiliki kemampuan untuk mengadsorpsi partikel pendispersi pada permukaanya. Sifat ini telah digunakan dalam berbagai proses seperti penjernihan air. Adsorpsi dengan
commit to user
absorbsi itu berbeda. Bedanya adalah absorbsi terkait dengan penyerapan partikel sampai ke bawah permukaan zat. Ilustrasi adsorpsi dapat dilihat pada Gambar 2.3.
(Sumber: Kharisma W, Dewi. 2009)
Gambar 2.3 Ilustrasi Adsorpsi
2.2.6 Reaktor Batch
Reaktor batch adalah wadah atau tempat yang digunakan untuk mengolah limbah. Biasanya digunakan untuk reaksi fase cair, terutama jika kapasitas produksi kecil, sehingga sangat bermanfaat untuk industri yang membuat bermacam- macam hasil misalnya pabrik obat- obatan atau pabrik zat warna. (Anonim1, 1985)
Ditinjau dari segi biaya pembeliannya, reaktor batch lebih murah sehingga untuk industri dengan kapasitas produksi yang kecil lebih baik. Keuntungan lain penggunaan reaktor batch yaitu, lebih mudah untuk memulai mengoperasikannya dan menghentikannya, juga lebih mudah dikontrol. (Anonim1, 1985)
Kerugian penggunaan reaktor batch diantaranya (Anonim1, 1985):
1. Banyak waktu yang terbuang untuk pengisian, pemanasan air limbah yang diolah, kenaikan suhu yang terjadi, pendinginan hasil olahan, waktu pembersihan reaktor, ditambah dengan waktu tinggal pengolahan yang diperlukan untuk batch.
2. Tidak baik untuk reaksi fase gas, mudah terjadi kebocoran pada lubang pengaduk, jadi packing harus kuat.
commit to user
2.2.7 Raiso Elektroda CairanRasio elektroda cairan merupakan perbandingan antara luasan kedua sisi suatu elektroda dibandingkan dengan volume cairan yang merendamnya. Kontak antara elektroda dengan cairan menimbulkan reaksi. Di dalam sel elektrolisis terjadi reaksi pada elektroda, yakni reduksi pada katoda dan oksidasi pada anoda. Pada proses ini perbandingan luasan elektroda dengan volume cairan elektrolit sangat mempengaruhi kinerja reaktor. Nilai dari rasio elektroda cairan dapat dilihat pada Persamaan 2.2 berikut : (Utomo, Budi dkk. 2012)
...Persamaan 2.2
Dengan :
REC = rasio elektroda cairan Aelektroda = luasan seluruh sisi elektroda
Vcairan = volume cairan elektrolit
Dengan demikian rasio elektroda cairan berbanding lurus dengan luasan elektroda yang digunakan pada komponen suatu reaktor. Pada reaktor elektrokimia batch, elektroda yang digunakan berupa pelat tipis yang memiliki luasan dari kedua sisi pelat. Sedangkan volume cairan yang diperhitungkan merupakan volume cairan yang memiliki kontak langsung dengan pelat. (Utomo, Budi dkk. 2012)
Rasio elektroda cairan mempengaruhi penggunaan arus listrik. Sehingga penggunaan arus listrik dapat dijadikan indikator penggunaan daya yang berkaitan dengan biaya operasional reaktor.
Daya listrik dapat diperoleh dari Persamaan 2.3 berikut :
P = V x I ...Persamaan 2.3
Dengan :
P = daya listrik (watt) V = tegangan (volt) I = kuat arus (ampere)
commit to user
2.2.8 SpektrofotometriSpektrofotometri merupakan metode analisis yang didasarkan pada adsorpsi radiasi elektromagnet. Cahaya terdiri dari radiasi terhadap kepekaan mata manusia, gelombang dengan panjang berlainan akan menimbulkan cahaya yang berlainan sedangkan campuran cahaya dengan panjang panjang ini akan menyusun cahaya putih. Cahaya putih meliputi seluruh spektrum nampak 400nm 760 nm. (Anonim 2, 1979)
Spektrofotometri adalah suatu metode analisis yang didasarkan pada pengukuran serapan sinar monokromatis oleh suatu lajur larutan berwarna pada panjang gelombang yang spesifik dengan menggunakan monokromator prisma atau kisi difraksi dan tabung foton hampa. Alat yang digunakan adalah spektrofotometer, yaitu suatu alat yang digunakan untuk menentukan suatu senyawa baik secara kuantitatif maupun kualitatif dengan mengukur transmitan ataupun absorban dari suatu cuplikan sebagai fungsi dari konsentrasi.
Spektrofotometer menghasilkan sinar dari spektrum dengan panjang gelombang tertentu. Pada spektrometer panjang gelombang dari sinar putih dapat lebih terseleksi dan ini diperoleh dengan alat pengurai seperti prisma, grating, atau celah optis. Spektrofotometer tersusun dari sumber spektrum tampak yang kontinyu, monokromator, sel pengabsorbsi untuk larutan sempel dan suatu alat untuk mengukur perbedaan absorbsi antara sampel dan blanko ataupun pembanding. Spektrofotometri ini hanya terjadi bila terjadi perpindahan elektron dari tingkat energi yang rendah ke tingkat energi yang lebih tinggi. Perpindahan elektron tidak diikuti oleh perubahan alat spin, hal ini dikenal dengan sebutan tereksitasi singlet. (S. M. Khopkar. 2003)
Efisiensi kinerja REB-BA diukur berdasarkan serapan gelombang cahaya dengan teori spektrofotometri. Efisiensi REB-BA dapat diperoleh berdasarkan Persamaan 2.4 berikut : (Utomo, Budi dkk. 2012)
...Persamaan 2.4
Dimana : = Absorbansi sebelum (ketetapan alat = 0,85) = Warna sesudah
commit to user
2.3 Penelitian yang RelevanPengolahan air limbah batik bertujuan untuk mengurangi kadar zat pewarna yang berbahaya, serta untuk mendapatkan metode pengolahan air limbah batik yang efektif dan efisien.
Menurut penelitian (Purwaningsih, Indah. 2008), menggunakan metode elektrokoagulasi secara batch. Dari variasi yang dilakukan, yakni kuat arus, jarak elektroda, dan waktu kontak, yang paling signifikan menurunkan kadar COD dengan efisiensi penurunan rata- rata konsentrasinya 15,03% dan efisiensi rata- rata penurunan konsentrasi warna 55,36% yaitu variasi jarak elektroda 1,5 cm dengan kuat arus 12 volt dan waktu kontak antara 30-45 menit.
Menurut penelitian (Budi S, Hanif. 2013), tentang pengolahan air limbah batik
Home Industri batik di Kelurahan Sondakan menggunakan Unit Pengolahan Air
Limbah Reaktor Elektrokimia (UPAL-RE), diperoleh efisiensi penyisihan COD dan warna berturut-turut 85% dan 79% selama 40 menit dan arus listrik sebesar 20 Volt.
Penelitian yang lainnya adalah penelitian yang dilakukan oleh (Utomo, Budi dkk.
2012), yang berjudul Optimasi Kinerja UPAL-RE untuk Melayani Home Industry
Batik. Penelitian tersebut menyimpulkan bahwa berdasarkan data yang sudah diperoleh, proses penyisihan dengan reaktor elektrokimia dengan variasi Alumunium-Stainless Steel (AS) menghasilkan efisiensi serapan yang lebih baik.
Berdasarkan komunikasi lisan dengan Afif Muchshon tentang Tugas Akhirnya yang berjudul Kinerja Reaktor Elektrokimia Batch Alumunium-Besi (REB-AB) dengan Variasi Rasio Elektroda Cairan (REC) untuk Pengolahan Air Limbah Batik,di dalam penelitian tersebut disimpulkan bahwa Reaktor Elektrokimia Batch Aluminium-Besi (REB-AB) dengan REC 7,2 dan jarak elektroda 1,5 cm diperoleh efisiensi terbesar, yaitu 83,16 %. Efisiensi terendah adalah 51,09 % dengan REC 4,8 dan jarak elektroda 1,5 cm. Arus listrik terbesar adalah 4,9 ampere, yaitu pada REC 9,6 dan terendah pada REC 4,8 sebesar 3,3 ampere. Suhu tertinggi adalah
commit to user
78 C, yaitu pada REC 9,6 dan jarak elektroda 1,5 cm, sedangkan suhu terendah adalah 39 C pada REC 7,2 dan jarak elektroda 2 cm.
Berdasarkan komunikasi lisan dengan Suci Alfian Flurianti yang melakukan penelitian serupa tetapi menggunakan elektroda Alumunium- Stainless Steel (REB-AS), diperoleh variasi yang paling efektif dan efisien yaitu variasi dengan kode sampel 2AS12-5 memiliki efisiensi sebesar 90,97% serta penggunaan arus dan timbulan suhu masing- masing 5,3 Ampere dan 63 C.