DETOKSIFIKASI SIANIDA OLEH MIKROBA RUMEN
(BIOPLUS RACUN)
(Cyanide Detoxification by Rumen Microbes (Toxic Bioplus))
M. WINUGROHO1, ARFAN ABRAR2danK. G. WIRYAWAN31Balai Penelitian Ternak, PO Box 221, Bogor 2Mahasiswa PPS IPB dan 3Staf Pengajar PPS IPB, Bogor
ABSTRACT
Cassava leaf can be used as feed for ruminants. However, there is cyanide toxic that can cause death to the ruminants if it consumed excessively. Ruminants has ability to detoxify toxic compound in their feed, this related with microbes in its rumen. Rumen fluid as inoculum was taken from cassava leaf adapted-sheep in Ciampea, Bogor. This rumen fluid then processed through Balitnak method (WINUGROHO et al., 1993) with
Potassium cyanide (KCN) as substrates. This adapted rumen fluid then cultured through Hungate method in modified Brain Heart Infusion Agar (BHIA) medium to study its detoxification activity and product in vitro. Sampling were taken sequentially in 48 hours then these adapted fluid rumen were identified its morphology and gram staining reactions. The isolates were called B1, B2 and B3. Detoxification test shows that these three isolates can decrease cyanide concentration before and after incubation by; 37.50 vs. 9.50 (B1), 35.50 vs. 10.50 (B2) and 26.75 vs. 2.88 (B3) with rate of cyanide degradation were; 0.58 ppm/h (B1), 0.52 ppm/h (B2) and 0.50 ppm/h (B3). Detoxification product was ammonia with concentration; 0.054 mM (B1); 0.047 mM (B2) and 0.1mM (B3). Morphology and gram staining reaction shows that these isolates has cocci shapes and gram negative reaction. Fermentation product with cyanide as substrate were acetic, propionic, isobutyric, butyric, isovaleric and valeric acid, except for isolate B1 has no valeric acid.
Key words: Cyanide, toxic bioplus
ABSTRAK
Daun singkong berpotensi sebagai pakan ternak ruminansia. Kelemahan daun singkong yaitu adanya senyawa toksik asam sianida (HCN) yang dapat menyebabkan kematian dan penyakit subklinis bila dikonsumsi dalam jumlah besar. Ternak ruminansia memiliki kemampuan untuk bertahan terhadap senyawa-senyawa toksik yang terdapat dalam pakannya, hal ini berhubungan dengan mikroba yang hidup dalam rumen. Cairan rumen sebagai sumber inokulum diperoleh dari domba di Kecamatan Ciampea Bogor yang telah teradaptasi dengan daun singkong dalam ransumnya. Cairan rumen tadi kemudian diproses melalui metode Balitnak (Winugroho et al., 1993) dengan KCN sebagai sumber substratnya untuk mendapatkan mikroba rumen terseleksi. Mikroba rumen yang telah terseleksi ditumbuhkan dalam media Brain Heart Infussion Agar (BHIA) dan dilakukan pemurnian untuk memperoleh kultur murni. Cairan rumen teradaptasi tadi kemudian ditumbuhkan dengan metode Hungate dalam media BHIA yang dimodifikasi untuk diuji aktivitas dan produk detoksifikasinya secara in vitro selama 48 jam dan dilakukan identifikasi mikroba rumen teradaptasi secara morfologis dan sifat pewarnaan gram. Mikroba rumen yang terpilih selanjutnya disebut isolat B1, B2 dan B3. Hasil pengujian aktivitas detoksifikasi menunjukkan penurunan konsentrasi sianida sebelum dan sesudah inkubasi masing-masing 37,50 vs 9,50 (B1), 35,50 vs 10,50 (B2) dan 26,75 vs 2,88 (B3) dengan laju penurunan konsentrasi sianida masing-masing 0,58 ppm/jam (B1), 0,52 ppm/jam (B2) dan 0,50 ppm/jam (B3). Produk detoksifikasi yang dianalisa adalah amonia dengan hasil masing-msaing yaitu; 0,054 mM (B1); 0,047 mM (B2) dan 0,1mM (B3). Hasil identifikasi bakteri rumen secara morfologis menunjukkan bentuk-bentuk campuran batang dan kokus dengan sifat pewarnaan gram negatif. Produk fermentasi dengan substrat sianida menghasilkan asam asetat, propionat, isobutirat, butirat, isovalerat dan valerat, kecuali untuk isolat B1 tidak terdapat asam valerat.
PENDAHULUAN
Tanaman singkong dapat menghasilkan daun sebanyak 7-15 ton/ha (K
HAJAREN,1977) dengan
kandungan protein kasar berkisar antara 18-35% dari bahan kering (R
OGERSdan
M
ILNER, 1963).
Oleh karena itu, tanaman ini sangat berpotensi dalam menyediakan daun singkong sebagai pakan
untuk ternak ruminansia. Namun, daun singkong mengandung senyawa toksik asam sianida (HCN)
yang dapat menyebabkan kematian dan penyakit subklinis bila dikonsumsi secara berlebihan.
Ternak ruminansia memiliki kemampuan untuk bertahan terhadap senyawa-senyawa toksik yang
terdapat dalam pakannya. Hal ini berhubungan dengan mikroba yang hidup dalam rumen.
Komposisi dan populasi mikroba yang hidup dalam rumen ditentukan oleh jenis pakan yang
dikonsumsi dan interaksi antar mikroba rumen (P
RESTONdan
L
ENG, 1987). Hasil penelitian yang
dilakukan oleh J
ONES(1981) berhasil mengidentifikasi bakteri pendetoksifikasi mimosin yang
diperoleh dari rumen kambing di Hawaii tetapi tidak terdapat pada kambing yang ada di Australia.
Sehubungan dengan hal-hal di atas maka dalam penelitian ini akan dieksplorasi bakteri pada ternak
ruminansia yang memiliki kemampuan mendegradasi sianida.
MATERI DAN METODE
Seleksi mikroba yang memiliki kemampuan mendegradasi sianida
Cairan rumen sebagai sumber inokulum diperoleh dari domba yang telah teradaptasi
mengkonsumsi daun singkong. Dengan menggunakan substrat KCN dari Merck, cairan rumen
tersebut diadaptasikan dalam kondiisi anaerob suhu 39
oC selama 96 jam menggunakan metode
Balitnak (W
INUGROHOet al., 1993). Produksi gas sebagai indikator terjadinya fermentasi dicatat.
Pada akhir masa inkubasi dari total produksi gas terbanyak diambil cairan rumen yang telah
teradaptasi tadi sebanyak 0,5 ml untuk ditumbuhkan secara anaerob suhu 39
oC pada medium Brain
Heart Infusion Agar (BHIA) yang telah dimodifikasi dengan KCN. Koloni bakteri yang terbentuk
kemudian dimurnikan dan disiapkan sebagai inokulum untuk uji detoksifikasi sianida secara in
vitro.
Uji detoksifikasi sianida secara in vitro
Fermentasi in vitro dilakukan dengan menggunakan metode T
HEODOROUdan
B
ROOKS(1990)
yang telah dimodifikasi pada tabung reaksi dengan tutup karet. Media yang digunakan adalah 10 ml
media basal, 1 ml larutan sianida dengan konsentrasi 75 ppm dan 3 inokulum bakteri terpilih (B1,
B2 dan B3) yang telah teradaptasi sebanyak 0.2 ml. Fermentasi dilakukan selama 48 jam dengan
pengambilan sampel pada 0; 6; 12; 24 dan 48 jam sebanyak 1 ml untuk dianalisa konsentrasi
sianidanya.
Identifikasi bakteri
Inokulum bakteri (B1, B2 dan B3) diuji secara morfologis, sifat pewarnaan gram dan produk
asam lemak terbangnya dengan sianida sebagai substrat.
HASIL DAN PEMBAHASAN
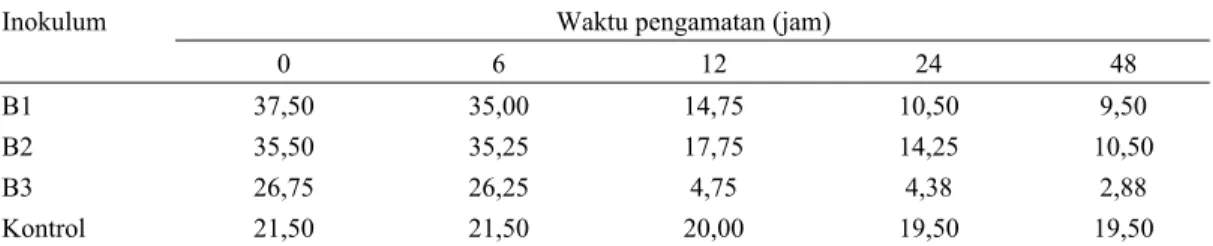
Hasil analisa konsentrasi sianida selama waktu pengamatan (0; 6; 12; 24 dan 48 jam)
menunjukkan penurunan konsentrasi yang dapat dilihat pada tabel 1.
Tabel 1. Rataan konsentrasi sianida (ppm) pada waktu pengamatan berbeda
Inokulum Waktu pengamatan (jam)
0 6 12 24 48
B1 37,50 35,00 14,75 10,50 9,50
B2 35,50 35,25 17,75 14,25 10,50
B3 26,75 26,25 4,75 4,38 2,88
Kontrol 21,50 21,50 20,00 19,50 19,50
Dari Tabel 1, terlihat bahwa penurunan konsentrasi sianida dari tiga inokulum secara nyata
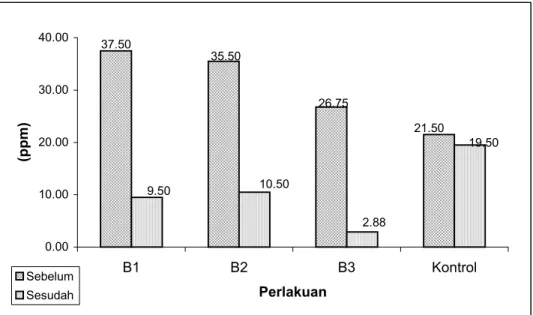
berbeda dibandingkan kontrol (P<0,05). Lebih jauh penurunan konsentrasi tersebut dapat dilihat
pada Gambar 1.
Penurunan konsentrasi sianida yang didapat dari tiap inokulum B1, B2 dan B3 masing-masing
sebesar 74,67%, 70,42% dan 89,25% dengan rataan laju penurunan sianida selama masa inkubasi
48 jam masing-masing 0,58 ppm/jam, 0,52 ppm/jam dan 0,50 ppm/jam untuk B1, B2 dan B3 secara
berurutan. Penurunan konsentrasi sianida menunjukkan inokulum yang diperoleh memiliki
kemampuan mendegradasi sianida walaupun produk fermentasi sianida masih belum diketahui.
Jalur hidrolisis sianida secara anaerob menurut F
ALLON(1992) dapat terjadi melalui reaksi berikut ;
HCN + 2H
2O HCOOH + NH
3Analisa terhadap konsentrasi amonia sebagai produk detoksifikasi dapat dilihat pada Tabel 2.
Konsentrasi amonia berbanding terbalik dengan konsentrasi sianida selama inkubasi, hal ini diduga
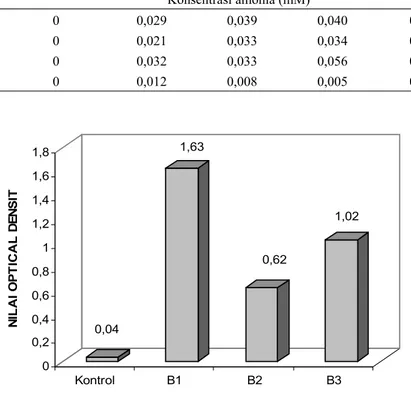
berhubungan dengan proses detoksifikasi sianida. Pertumbuhan isolat pada media yang sudah
dimodifikasi dengan sianida juga terlihat dengan meningkatnya nilai optical density pada media
yang sebelum dan sesudah inkubasi. Peningkatan nilai optical density menunjukkan pertumbuhan
isolat Gambar 3. Hasil identifikasi isolat dapat dilihat pada Tabel 3.
37.50 35.50 26.75 21.50 19.50 10.50 2.88 9.50 0.00 10.00 20.00 30.00 40.00 B1 B2 B3 Kontrol Perlakuan (ppm) Sebelum Sesudah
Gambar 1. Rataan konsentrasi sianida (ppm) sebelum dan sesudah inkubasi
Laju penurunan konsentrasi sianida untuk tiap isolat juga berbeda-beda seperti terlihat pada
Gambar 2.
0.00 0.50 1.00 1.50 2.00 2.50 3.00 3.50 4.00 0 - 6 6 - 12 12 - 24 24 - 48masa inkubasi
(ppm/jam)
B1 B2 B3 KontrolTabel 2. Rataan produksi Amonia (mM) hasil inkubasi dengan mikroba rumen terseleksi (B1-B3) Waktu (jam) 0 6 12 24 48 Isolat Konsentrasi amonia (mM) B1 B2 B3 Kontrol 0 0 0 0 0,029 0,021 0,032 0,012 0,039 0,033 0,033 0,008 0,040 0,034 0,056 0,005 0,054 0,047 0,100 0,007 0,04 1,63 0,62 1,02 0 0,2 0,4 0,6 0,8 1 1,2 1,4 1,6 1,8 N ILA I O P TI C A L D E N S IT Y Kontrol B1 B2 B3
Gambar 3. Nilai optical density sebelum dan sesudah inkubasi tiap isolat
Tabel 3. Karakterisasi mikroba rumen terseleksi yang mampu mendegradasi sianida
Karakteristik B1 B2 B3 Morfologi Pewarnaan gram Produk Fermentasi asetat propionat isobutirat butirat isovalerat valerat NH3 Kokus Gram negatif ++ + + ++ + - + Kokus Gram negatif ++ + + ++ + + + Kokus Gram negatif ++ + + ++ + + +
KESIMPULAN
Bakteri rumen yang teradaptasi memiliki kemampuan mendegradasi sianida secara in vitro
dengan produk detoksifikasinya berupa amonia.
DAFTAR PUSTAKA
AMERICAN PUBLIC HEALTH ASSOCIATION. 1985. Standard Methods for the Examination of Water and
Wastewater. American Public Health Association. Washington DC.
FALLON, R. D. 1992. Evidence of a hydrolitic route for anaerobic cyanide degradation. Applied and
Environmental Microbiology 58: 9. pp 3163-3164
JONES, R. J. 1981. Does ruminal metabolism of mimosine explain the absence of leucaena toxicity in Hawaii. Aust. Vet. J. 57 : 55-56
KHAJAREN, S., J.M. KHAJAREN, N. KITPANIT andZ. O. MULLER. 1977. Cassava in the Nutrition of Swine.
Proceedings of a Workshop Held at the University of Guelph, Ottawa
PRESTON, T. R. and R. A. LENG. 1987. Matching Ruminant Production System with Available Sources in
Tropics. Penabul Book. Armidale
ROGERS, D. J. and MILNER. 1963. Amino acid profile of minioc leaf protein in relation to nutritive value. Econ. Bot. 17:211
THEODOROU, M.K. and A. E. BROOKS. 1990. Evaluation of a New Laboratory Procedure for Estimating the
Fermentation Kinetics of Tropical Feeds. AFRC Institute for Grassland and Environmental Research. Hurley. Maidenhead, Berkshire, SL6 5LR, UK
WINUGROHO, M., M. SABRANI, P. PUNARBOWO, Y. WIDIAWATI and A. THALIB. 1993. Non-genetic approach for selecting rumen fluid contain specific microorganisms (balitnak method). Ilmu dan Peternakan 6(2) :5-9 Pusat Penelitian dan Pengembangan Peternakan. Bogor