1Program Studi Biologi, Fakultas MIPA, Universitas Tanjungpura, Jl. Prof. Dr. H. Hadari Nawawi, Pontianak
Jamur Rizosfer Sebagai Agen Antagonis Pengendali Penyakit Lapuk Fusarium
Pada Batang Tanaman Karet (
Hevea brasiliensis
MuellArg)
Wiwin Kamila Putri1 , Siti Khotimah1,Riza Linda1Email : wiwin.putri93@gmail.com Abstract
The stem rot disease caused by the Fusarium sp. fungus is one of the diseases found on the rubber tree (Hevea brasiliensis). This plant disease can be controlled by using a biological agent namely the rhizosphere fungus which is antagonistic to pathogenic fungi. This research aimed to find out the types of fungi from the rhizosphere of rubber tree and to find out the ability of those fungi to inhibit the growth of Fusarium sp. The
Fusarium sp. fungus was isolated using the direct planting method, the rhizosphere fungus was isolated using the dilution method, the antagonistic test was conducted using the paired method. The rhizosphere fungi successfully isolated were Trichoderma sp. W1, Penicillium sp.1 W2, Penicillium sp.2 W3, Chaetomium sp. W4. The research findings showed that there was inhibition of the growth of Fusarium sp. by Trichoderma
sp. with the highest antagonistic percentage by 51.08%.
Keywords: Antagonistic, Rubber, Fusarium sp., Weatheret trunk, Rhizosphere PENDAHULUAN
Tanaman karet (Hevea brasiliensis MuellArg) merupakan tanaman perkebunan penghasil getah yang bernilai ekonomi tinggi untuk bahan industri karet. Tanaman ini menjadi salah satu komoditi unggulan yang berkembang di Kalimantan Barat. Menurunnya produksi tanaman karet dapat disebabkan oleh serangan penyakit, salah satu penyakit yang menyerang tanaman karet adalah penyakit lapuk batang.Penyakit lapuk batang dapat disebabkan oleh jamur Fusarium sp. yang mengakibatkan kerusakan pada kulit cabang dan batang. Penyakit ini juga dapat mengakibatkan kematian pada tanaman. Gejala awal yang ditimbulkan penyakit lapuk batang pada tanaman karet, dengan adanya bercak-bercak berwarna coklat kehitaman yang terdapat pada kulit batang tanaman karet (Djafaruddin, 2004).
Pengendalian secara biologi (hayati) merupakan alternatif pengendalian yang dapat dilakukan tanpa harus memberikan pengaruh negatif terhadap lingkungan dan sekitarnya, salah satunya adalah sistem pengendalian menggunakan agen hayati seperti jamur yang bersifat antagonis. Beberapa mikroorganisme antagonis dapat digunakan sebagai pengendali penyakit tanaman yang disebabkan oleh jamur patogen. Penelitian Aldjas (2010) menginformasikan bahwa pada daerah rizosfer tanaman nanas (Ananas comosus
(L) Merr.) ditemukan jamur yang berpotensi antagonis terhadap jamur patogen Fusarium moniliforme seperti jamur Aspergilus fumigatus,
A. niger, Curvularia sp., Trichoderma harzianum
dan T. viride.Hasil penelitian Meiniwati et al. (2014) juga menginformasikan bahwa pada daerah rizosfer tanaman padi (Oryza sativa L.) terdapat jamur yang berpotensi antagonis terhadap jamur patogen Pyiricularia grisea seperti jamur
A.flavus, A. fumigatus, A. niger, Curvularia sp. dan Trichoderma harzianum.
Berdasarkan potensi yang dimiliki jamur rizosfer dalam menekan perkembangan beberapa jamur patogen, maka perlu dilakukan penelitian untuk melihat kemampuan jamur rizosfer dalam mengendalikan jamurFusarium sp. hasil diisolasi dari batang tanaman karet yang terserang penyakit lapuk batang di daerah perkebunan karet Kalimantan Barat.
BAHAN DAN METODE Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan selama 5 bulan, yaitu bulan Maret sampai Juli 2015. Pengambilan sampel tanah untuk mendapatkan jamur rizosfer isolat lokal dan pengambilan batang tanaman karet yang terserang penyakit lapuk batang dilakukan di areal perkebunan karet milik petani desa, Kecamatan Batang Tarang, Kabupaten Sanggau. Tahap isolasi, identifikasi dan uji antagonis dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan IlmuPengetahuan Alam Universitas Tanjungpura Pontianak
Bahan
Bahan yang digunakan dalam penelitian ini adalah sampel tanah rizosfer tanaman karet (Hevea brasiliensis Muell Arg), tanaman karet yang memperlihatkan gejala lapuk batang, media
PotatoDextrose Agar (PDA), akuades steril, alkohol 70%, asam laktat, kloramfenikol dan spirtus.
Cara Kerja
Pengambilan Sampel
Sampel tanah yang diambil adalah tanah yang ada disekitar perakaran tanaman karet yang sehat. Lokasi sampling ditentukan secara acak pada 3 titik tanaman karet dengan 3 kali pengulangan pada setiap titik. Pengambilan sampel tanah ±100 gram dilakukan dengan kedalaman 0-20 cm disekitar perakaran tanaman karet. Batang tanaman karet yang menunjukan gejala penyakit lapuk batang disayat, kemudian dimasukan ke dalam kantong plastik.
Isolasi Jamur
Isolasi jamur rizosfer tanaman karet dilakukan dengan menggunakan metode pengenceran. Sampel tanah dari lokasi sampling ditimbang sebanyak 1 g dan dimasukan ke dalam tabung reaksi yang telah berisi akuades steril sebanyak 9 ml dan dihomogenkan. Sampel tanah yang telah dihomogenkan kemudian diencerkan hingga tingkat pengenceran 10-5. Hasil dari tiap-tiap pengenceran 10-3, 10-4 dan 10-5 dipipet sebanyak 1 ml, kemudian dituang ke dalam media PDA dengan metode pourplate. Media yang telah padat diinkubasi pada suhu 28oC selama 3-7 hari. Setiap seri pengenceran diulang sebanyak 3 kali (Purwantisari dan Rini, 2009).Setelah jamur tumbuh, koloni masing-masing jamur diambil dengan ose, kemudian ditumbuhkan pada mediaPDA baru untuk memperoleh biakan murni (Samsonet al., 2010).
Isolasi jamur Fusarium sp. dari batang tanaman karet dilakukan dengan metode tanam langsung. Kulit batang diletakan pada media PDA kemudian diinkubasi pada suhu 28°C selama 7 hari (Malloc, 1997 dalam Purwantisari dan Rini, 2009). Setelah jamur tumbuh, koloni jamur diambil dengan ose, kemudian ditumbuhkan pada media PDA yang baru untuk memperoleh biakan murni (Samson et al., 2010).
Identifikasi Jamur
Biakan murni sel jamur dipulaskan secara aseptis menggunakan jarum preparat di atas permukaan gelas objek yang telah ditetesi asam laktat. Setelah
itu, preparat ditutup dengan cover glass dan diamati dibawah mikroskop (Pohan, 2011 dalam
Ningsih et al., 2012).
Setiap jamur yang tumbuh diidentifikasi berdasaarkan pada karakter koloni secara makroskopis seperti warna koloni, bentuk dan tekstur permukaan koloni, serta secara mikroskopis meliputi struktur hifa, sel kaki dan struktur reproduksi. Identifikasi jamur hasil isolasi mengacu pada buku identifikasi jamur Taxonomy of Fungi (Bessey, 1950), A Guide to Tropical Fungi (Sutton, 1990), Illustrated Genera of Fungi
(Barnet dan Hunter, 1998),Introductory Mycology
(Alexopoulos et al., 1996), Pictorial Atlas of Soil and Seed Fungi (Watanabe, 2002), dan Food and Indoor Fungi (Samson et al., 2010).
Uji Antagonis
Uji antagonis secara invitro dilakukan terhadap jenis jamur yang dominan ditemukan dari ketiga titik rizosfer tanaman karet. Pengujian dilakukan dengan cara menumbuhkan koloni jamur secara berpasangan. Biakan murni Fusarium sp. dan jamur hasil isolasi dari rizosfer karet masing-masing diambil sebanyak 1 ose dan diinokulasi pada cawan petri yang telah berisi PDA perlakuan kontrol negatif Fusarium sp. diinokulasikan ke permukaan media PDA pada bagian tengah media tanpa perlakuan (Rianti,2010). Pengukuran diameter jamur dilakukan dengan membuat garis horizontal, vertikal dan diagonal pada permukaan cawan petri yang terlihat pertumbuhan jamur
Fusarium sp.
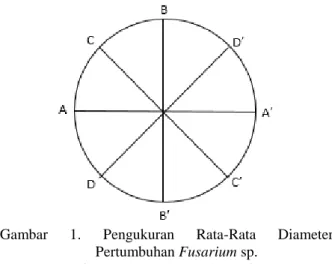
Pengukuran diameter jamur dilakukan dengan membuat garis horizontal (AA’), vertikal (BB’), dan diagonal (CC’ dan DD’) pada permukaan cawan petri yang terlihat pertumbuhan jamur
Fusarium sp.
Gambar 1. Pengukuran Rata-Rata Diameter Pertumbuhan Fusarium sp.
Rata-rata diameter pertumbuhan jamur yang diisolasi dari organ bergejala lapuk batang (d)
dihitung dengan rumus (Davis, 1965 dalam
Nawawi 2001):
Perhitungan persentase antagonis jamur Fusarium
sp. yang bersinggungan dengan agen antagonis hingga hari ke-7, menggunakan rumus (Muksin et al, 2013):
Keterangan :
PA =Persentase antagonis (%)
d1 =Rerata diameter pertumbuhanFusarium sp., sebagai kontrol (mm)
d2 =Rerata diameter pertumbuhan Fusarium
sp.pada perlakuan uji antagonis (mm) HASIL DAN PEMBAHASAN
Hasil
Pertumbuhan jamur rizosfer Tricoderma sp. W1,
Penicillium sp.1 W2, Penicillium sp.2 W3,
Chaetomium sp. W4 menunjukan adanya diameter pertumbuhan yang berbeda-beda pada setiap diameter pertumbuhan koloni Tricoderma sp. W1lebih cepat dibandingkan jamur lainnya. Koloni jamur Tricoderma sp. W1mencapai diameter Pertumbuhan sebesar 90mm pada hari ke-4 dan hari ke-7 (Gambar 2).
Gambar 2. Grafik Pertumbuhan Jamur Antagonis dan
Fussarium sp. Trichoderma sp. W1
Penicillium sp.1 W2 Penicillium sp.2 W3 Chaetomium sp. W4
Fusarium sp.
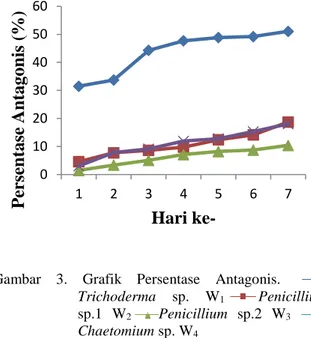
Rerata persentase antagonis (%) masing-masing jamur rizosfer terhadap Fusarium sp. mulai hari ke-1 sampai hari-7 dapat dilihat pada Gambar 3.
Gambar 3. Grafik Persentase Antagonis.
Trichoderma sp. W1 Penicillium sp.1 W2 Penicillium sp.2 W3
Chaetomium sp. W4
Morfologi koloni jamur Fusarium sp. yangditumbuhkan berpasangan dengan jamur antagonis dapat dilihat pada gambar 4.
Gambar 4. Morfologi koloni Jamur pada Uji Antagonis Hari ke-7. (A)Kontrol negatif (B)
Trichoderma sp. vs Fusarium sp. (C)
Penicillium sp.1 vs Fusarium sp. (D)
Penicillium sp.2 vs Fusarium sp. (E)
Chaetonium sp. vs Fusarium sp.
Keterangan : A : Antagonis P:Patogen Pembahasan
Hasil Isolasi jamur dari tanah rizosfer tanaman karet ditemukan 4 jenis jamur yaitu Trichoderma
sp. W1, Penicillium sp.1 W2, Penicillium sp.2 W3 dan Chaetomium sp.W4. Jamur yang diisolasi dari rizosfer tanaman karet memiliki karakteristik yang berbeda-beda. Jamur Trichoderma sp. W1 memiliki koloni berwarna hijau dengan tekstur permukaan seperti kapas. Hal ini sesuai dengan Rianti (2010) yang menyatakan bahwa jamur
0 20 40 60 80 100 1 2 3 4 5 6 7
Diam
ete
r
P
er
tum
b
u
h
an
(m
m
)
Hari
ke-0 10 20 30 40 50 60 1 2 3 4 5 6 7P
er
se
n
tase
Antagon
is
(%
)
Hari
ke-Trichoderma sp. tumbuh dengan cepat, membentuk koloni berwarna hijau pada bagian media, dan memiliki tekstur seperti kapas.
Trichoderma sp. W1 tampak memiliki konidia dan konidiofor. Konidia tampak berbentuk bulat dan berwarna hijau. Konidifor memiliki sekat dan bercabang. Percabangan utama konidiofor timbul langsung dari ketiak utama. Percabangan konidiofor memanajang di sepanjang konidiofor (Samson, et al., 2010).
Jamur Penicillium sp.1 W2 memiliki karakteristik koloni berwarana merah muda, permukaan koloni licin dan padat, dan bentuk tepi koloni rata. Pengamatan secara mikroskopis menunjukan
Penicillium sp.1 W2 memiliki bentuk konidia bulat berwarna merah muda, dan fialid berbentuk lanset. Menurut Samsonet al., (2010), terdapat jamur penicillium yang memiliki warna koloni merah muda dengan permukaan koloni padat dan memiliki konidia berwarna merahmuda.
Jamur Penicillium sp.2 W3 memiliki karakteristik koloni berwarna putih kehijauan, memiliki tekstur seperti kapas. Pengamatan secara mikroskopis menunjukan bahwa Penicillium sp.2 W3 memilikikonidia berwarna hijau, fialid berbentuk silindris dan terdapat metula. Menurut Samsonet al., (2010), Penicillium memiliki warna koloni putih kehijauan dengan permukaan koloni seperti kapas dan memiliki konidia berwarna hijau. Jamur Chaetomium sp. W4 membrntuk koloni berwarna merah muda, tekstur permukaan koloni seperti kapas dengan bentuk tepi rata. Secara mikroskopis jamur Chaetomium sp. W4 memilikiascomata berbentuk oval dan terdapat rambut ascomata. Menurut Hasanuddin (2003), jamur Chaetomium sp. memiliki koloni berwarna merah dan merah muda, dan memiliki rambut ascomata.
Daya antagonis yang tinggi pada Trichoderma sp. W1 diduga karena jamur tersebut menghasilkan enzim yang mampu merusak dinding sel jamur patogen dan menghambat pertumbuhan jamur patogen. Dinding sel Fusarium sp. diduga mengalami lisis akibat adanya aktivitas enzim yang dihasilkan oleh jamur antagonis.
Trichoderma sp. menghasilkan enzim kinase dan β 1-3 glukanase yang mampu merombak lapisan utama penyusun dinding sel jamur yaitu kitin dan glukan (Soesanto, 2008). Antagonisme
Trichoderma sp. dengan cara melisiskan dinding sel jamur patogen dapat diamati dari besarnya persentase antagonis. Hal ini mengindikasikan
dinding sel Fusarium sp. mengalami lisis sehingga pertumbuhannya terhambat.
Penicillium sp.1 W2 memiliki persentase antagonis 18,76% lebih tinggi dibandingkanPenicillium sp.2 W3 sebesar 10,43%.Hal ini karena adanya perbedaan kemampuan tumbuh dari masing-masing genus
Penicillium. Penicillium sp.1 W2 lebih mampu menguasai ruang tumbuh dan nutrisi lebih cepat dibandingkan Penicillium sp.2 W3 sehingga menghambat pertumbuhan Fusarium sp. Meskipun Penicillium sp.1 W2 memiliki persentase antagonis lebih tinggi dibandingkan
Penicillium sp.2 W3 akan tetapi genus Penicillium
ini memiliki daya antagonis yang relatif lambat. Hal ini karena adanya perbedaan kemampuan tumbuh dari masing-masing jenis jamur
Penicillium. Menurut Deacon (2006) dalam
Arisanti et al. (2012), mekanisme penghambatan oleh genus Penicilliumjuga diduga olehadanyasenyawa antibiotik yang mampu menghambat pertumbuhan jamur patogen.
Rerata diameter pertumbuhan jamur patogen pada perlakuan Chaetomium sp. W4 sebesar 18,07%. Hal ini menunjukan bahwa Chaetomium sp. W4 memiliki kemampuan antagonis relatif rendah dalam menekan pertumbuhan Fusarium sp. Sunarwati dan Yoza (2010) mengategorikan jamur antagonis yang memiliki daya hambat 26-50% termasuk dalam golongan jamur yang memiliki kemampuan antagonis rendah. Kemampuan yang dimiliki Chaetonium sp. dalam menghambat pertumbuhan jamur Fusarium sp. diduga karena Chaetomium sp. dapat menghasilkan senyawa metabolit sekunder berupa antibiotik. Menurut hasil penelitian Hasanuddin (2003) Chaetomium sp. menghasilkan antibiotik yang mampu menekan pertumbuhan jamur
Phytophthora sp.
DAFTAR PUSTAKA
Aldjas, FH, 2010, Uji Antagonis Jamur Rizosfer Isolat Lokal Rasau Jaya Terhadap Fusarium moniliforme (Sheldon) Penyebab Penyakit Busuk Buah Nenas
(Ananas comosus (L) Merr.), Skripsi, Universitas Tanjungpura, Pontianak Alexopoulos, CJ, Mims, CW, & Blackwell, M,
1996,Introductory Mycology, Fourth Edition, John Wiley and Sons, Canada
Arisanti, S, Kuswytasari, ND & Shovitri, M, 2012, ‘Uji Antimikroba Isolat Kapang Tanah Wonorejo Surabaya’
Barnett, HL & Hunter, BB, 1998,‘Illustrated Genera of Imperfect Fungi’,Fourth Edition, Burgess Publishing Company Bessey, EA, 1950, Morphology dan Taxonomy Of
Fungi, Edisi ke-3, Vikas Publishing House PVT LTD, New Delhi
Djafaruddin, 2004, Dasar-Dasar Pengendali Penyakit Tanaman, Penerbit Bumi Aksara, Jakarta
Hasanuddin. 2003. Peningkatan peranan mikroorganisme dalam sistem pengendalian penyakit tumbuhan secara terpadu. Medan: Jurusan Hama dan Penyakit Tumbuhan, Fakultas Pertanian, Universitas Sumatera Utara. USUdigital library. Diakses pada 15 Agustus 2015,http://library.usu.ac.id/download/fp/f p-hasanuddin.pdf.
Meiniwati, Khotimah, S & Mukarlina, 2014, Uji Antagonis Pyricularia grisea sacc. Penyebab Blas pada Tanaman Padi Menggunakan Jamur Rizosfer Isolat lokal, Protobiont Vol 3 (1) : 17-24, diakses pada 18 Agustus 2015, http://jurnal.untan.ac.id/index.php/jprb/art icle/view/4576/4665
Muksin, R, Rosmini, & Panggeso, J, 2013, ‘Uji Antagonisme Trichoderma sp. Terhadap Jamur Patogen Alternaria porri Penyebab Penyakit Bercak Ungu pada Bawang Merah Secara In-Vitro’, Agrotekbis, Vol. 1, no. 2, hal 140-144, diakses pada 16 Juli 2015,http://jurnal.untan.ac.id/jurnal/index. php/Agrotekbis/article/view/1513
Nawawi, G, 2001, Mengukur Jarak dan Sudut, Modul Program Keahlian Mekanisme Pertanian, Departemen Pendidikan Nasional, Direktorat Pendidikan Menengah Kejuruan, Jakarta
Ningsih, R, Mukarlina & Linda, R, 2012, ‘Isolasi dan Identifikasi Jamur dari Organ Bergejala Sakit Pada Tanaman Jeruk Siam (Citrus nobilis var. microcarpa)’, Protobiont, vol. 1, hal 73-79, diakses pada
12 Oktober 2014,
http://jurnal.untan.ac.id/index.php/jprb/art icle/view/586/608
Purwantisari, S & Rini, BH, 2009, ‘Uji Antagonis Jamur Patogen Phytoptora infestant
Penyebab Penyakit Busuk Daun dan Umbi Tanaman Kentang Dengan Menggunakan Trichoderma spp. Isolat Lokal’, Bioma, vol. 11, no. 1, hal. 24-32, diakses pada 26 September 2014, http;//eprints.undip.ac.id/
2000/1/Bioma_Susiana_Juni_2009_.pdf Rianti, R, 2010, Uji Antagonis Trichoderma
harzianum Terhadap Fusarium spp. Penyebab Penyakit Layu pada Tanaman Cabai (Capsicum annum) Secara In Vitro,
Skripsi, Universitas Tanjungpura, Pontianak
Samson, RA, Houbraken, J, Thrane, JC, Frisvad& Andersen, F, 2010, Food and Indoor Fungi, Fungal Biodiversity Centre Utrech, Netherlands
Soesanto, L.,2008, Pengantar Pengendali Hayati Penyakit Tanaman, Rajawali Press, Jakarta
Sunarwati, D, & Yoza, 2010, ‘Kemampuan
Trichoderma dan Penicillium Dalam Menghambat Pertumbuhan Cendawan Penyebab Penyakit Busuk Akar Durian (Phytophthora palmivora) Secara In Vitro’, Seminar Nasional Program dan Strategi Pengembangan Buah Nusantara Balai Penelitian Tanaman Buah Tropika, hal. 176-189, diakses pada 1 April 2014, http://balitbu.litbang.pertanian.go.id/ind/i mages/filepdf/26.pdf
Sutton, BC, 1990, A Guide to Tropical Fungi,
Singapore Science Centre, Singapore
Watanabe, T, 2002, Pictorial Atlasvof Soil and Seed Fungi, Edisi ke 2, CRC press, USA