LAPORAN PRAKTIKUM
OPERASI TEKNIK KIMIA II
ACARA :
HETP
Disusun oleh :
Nama : Janice Nathania
NIM : 011200312
Prodi : TEKNOKIMIA NUKLIR
Semester : IV
Kelompok : 2
Teman Kerja : 1. Ahmad Roisus Syifa 2. Siti Hanna
Asisten : Bangun Wasito
SEKOLAH TINGGI TEKNOLOGI NUKLIR BADAN TENAGA NUKLIR NASIONAL
YOGYAKARTA 2014 HETP
A. TUJUAN
Menentukan nilai Height Equivalent of Theoritical Plate (HETP) atau tinggi bahan isian dalam suatu kolom yang memberikan perubahan
komposisi sama dengan perubahan komposisi yang dicapai oleh satu plate teoritis atau ekivalen dengan satu plat teoritis.
B. DASAR TEORI Distilasi
Distilasi adalah suatu operasi untuk memisahkan larutan yang relatif volatil menjadi komponen-komponen penyusunnya atas dasar perbedaan titik didih dengan jalan menambahkan panas ke dalam campuran yang akan
dipisahkan. Pada operasi distilasi fase cair berada pada titik didihnya, sedangkan fase uap berada dalam kesetimbangan pada titik embunnya. Perpindahan massa dari fasa cair terjadi dengan penguapan dan dari fasa uap terjadi dengan pengembunan yang berlangsung secara simultan. Masing-masing komponen campuran umpan terdapat di dalam kedua fase itu, hanya berbeda jumlah relatifnya. Pada larutan ideal volatilitas dapat dikaitkan langsung dengan tekanan uap murni masing-masing.
Distilasi banyak digunakan untuk memisahkan campuran cairan agar menjadi campuran yang lebih murni. Keuntungan pemisahan secara distilasi adalah tidak diperlukannya komponen tambahan, sehingga tidak diperlukan komponen tambahan, sehingga tidak diperlukan proses lebih lanjut untuk menghitung senyawa yang ditambahkan tersebut. Alat yang diperlukan untuk operasi distilasi dapat berupa kolom berplat dengan sieve tray atau bubble cap tray, atau dapat pula menggunakan kolom dengan bahan isian (packing).
Refluks Lo.Xo
Faktor-faktor penting dalam merancang dan mengoperasikan kolom plat adalah jumlah plat yang diperlukan untuk mendapatkan pemisahan yang
dikehendaki, diameter kolom, kalor yang diperlukan dalam pendidihan, kalor yang dibuang pada kondensor, jarak antar plat yang dipilih, dan konstruksi plat.
Gambar di bawah menunjukkan diagram neraca bahan untuk contoh umum fasilitas distilasi kontinyu. Neraca massa untuk sistem tersebut adalah :
Neraca bahan total F = D + B
Neraca komponen F XF = D XD + B XB
Dengan mengeliminasi B dari kedua persamaan di atas, diperoleh :
B X D X B X F X F D
Dan eliminasi D menghasilkan :
B X D X F X D X F B
Umpan F.XF Hasil atas D.XD Hasil bawah B.XB Pemanas Pendingin K o lo m D is til a si
Gambar 1. Fasilitas destilasi secara kontinyu
Pengertian HETP
Bahan isian padat dan inert yang memiliki luas permukaan per satuan volume kolom dapat digunakan sebagai pengganti bubble cap plate. Berapa tinggi bahan isian dalam kolom yang bisa memberikan suatu komposisi produk pemisahan campuran tertentu harus dievaluasi.
Suatu kolom dengan bahan isian dibagi-bagi dalam unit-unit atau satuan-satuan tinggi bahan isian, dimana setiap satuan-satuan tinggi bahan isian mampu menghasilkan uap dan cairan keluar dari satuan ini dalam keadaan setimbang. Menurut definisi, pada satu plat edeal, uap dan cairan yang meninggalkan plat ideal juga pada keadaan kesetimbangan fase atau kesetimbangan termodinamik. Berarti satu satuan unit kolom tersebut ekivalen dengan satu plat ideal. Inilah konsep HETP. Karena itu dapat dinyatakan bahwa :
Tinggi bahan isian (Z) = jumlah plat ideal atau teoritis (N) x HETP
Tentu saja pernyataan ini berlaku untuk sesuatu operasi pemisahan tertentu, seperti kolom isian pada operasi penyulingan, absorpsi, dan ekstraksi.
Penggunaan pernyataan HETP diperlukan, karena dapat menggantikan proses bertingkat berlawanan arah, meskipun dari segi teoritis dipandang kurang fundamental. HETP harus dievaluasi secara eksperimen, karena HETP berubah oleh tipe, jenis, ukuran bahan isian, sangat dipengaruhi pula oleh kecapatan aliran kedua fluida (uap, cairan) maupun kisaran konsentrasi. Karena itu diperlukan banyak data eksperimen.
Evaluasi Jumlah Plat Teoritis (N)
Tinggi bahan isian (Z) ditentukan oleh nilai N atau jumlah plat teoritis dan nilai HETP. Jumlah plat teoritis N dapat dievaluasi menurut metode McGabe-Thiele (campuran biner) atau persamaan Fenske-Underwood.
Metode McGabe-Thiele Persyaratan :
1. Dalam diagram entalpi-komposisi, garis uap jenuh dan cairan jenuh keduanya berupa garis lurus dan sejajar
2. Kecepatan aliran molal tetap
3. Panas laten penguapan mendekati tetap 4. Campuran biner, ideal
Untuk evaluasi jumlah plat teoritis (N) diperlukan data kesetimbangan termodinamik atau y versus x, pada suhu tekanan operasi tertentu. Biasanya mol fraksi i dalam umpan, produk atas dan bawah dan kondisi termal umpan diketahui. Kita masih perlu melukiskan garis-garis operasi berikut :
1. 1 D R D X n X 1 D R D R 1 n Y
Garis operasi atas
1 D R D X
Garis operasi atas ini akan memotong sumbu y pada :
2. q 1 F X X q 1 q Y Garis q
q adalah panas untuk menguapkan 1 mol umpan semula menjadi uap, dibagi panas laten penguapannya. Dari nilai q yang didapat, bisa dihitung lereng garis q yaitu -q/(1-q) sehingga garis q dapat dilukis dengan lereng ini melalui titik umpan (ZF) di diagonal. Beberapa harga q untuk berbagai
kondisi umpan dapat diketahui sebagai berikut : q > 1, umpan dingin
q = 1, umpan pada titik gelembung (zat cair jenuh) 0 < q < 1, umpan sebagian berwujud uap
q = 0, umpan pada titik embun (uap jenuh) q < 0, umpan uap panas lanjut
3. B m L B BX m X B m L m L 1 m Y
Garis Opersasi Bawah
Jika langsung digunakan persamaan ini kita memerlukan data panas di sekitar reboiler. Supaya mudah, kita cari saja titik potong antara garis operasi atas dan garis q, misalnya titik P. kemudian hubungkan titik P dengan titik XB. Jika ketiga garis tersebut sudah dapat dilukis, maka jumlah plat teoritis dapat dievaluasi.
1 D R D X q XB XD Zf
Gambar 2. Evaluasi N secara grafik
Metode Fenske-Underwood Persyaratan :
1. Refluks total
2. Nilai sifat penguapan relatif tetap
1 avg logα ) D X (1 B X ) B X (1 D X log min N
Jika dipakai refluks total, garis operasi atas dan bawah berimpit dengan garis diagonal, dan jumlah plat teoritis minimal (Nm). Menurut Fenske-Underwood berikut :
avg adalah volatilitas relatif rata-rata =
D α B α o B P o A P AB α
untuk campuran biner ideal AB dapat ditentukan dengan persamaan
dengan :
o A P
: tekanan uap murni zat A pada suhu tertentu
o B P
: tekanan uap murni zat B pada suhu tertentu
1 2 3 4 5 6 7 3
C. ALAT DAN BAHAN
- Bahan
1. Alkohol (Etanol) 2. Aquadest
- Alat
1. Rangkaian alat destilasi 2. Piknometer
3. Neraca analitik 4. Alat-alat gelas
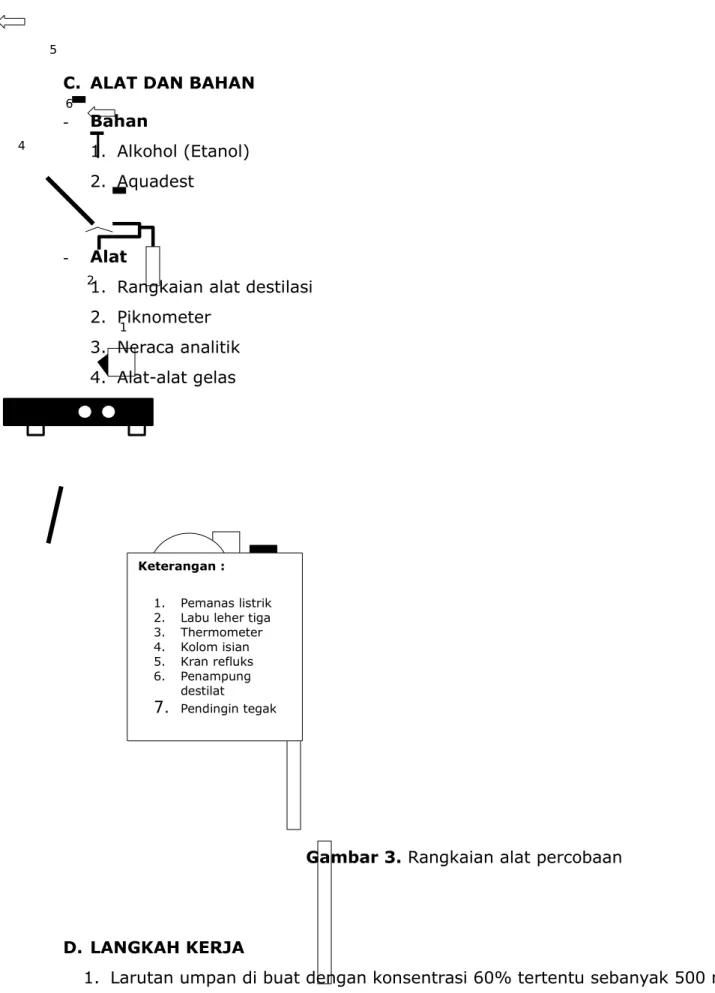
Gambar 3. Rangkaian alat percobaan
D. LANGKAH KERJA
1. Larutan umpan di buat dengan konsentrasi 60% tertentu sebanyak 500 ml 2. Komposisi campuran biner dievaluasi dengan cara mengukur densitasnya
Keterangan :
1. Pemanas listrik 2. Labu leher tiga 3. Thermometer 4. Kolom isian 5. Kran refluks 6. Penampung destilat 7. Pendingin tegak
3. Larutan umpan sebanyak 450 mL dimasukkan labu leher tiga, kemudian didistilasi dengan refluks total, sampai keadaan steady. Kondisi ini ditandai oleh suhu atas dan bawah yang konstan.
4. Destilat sebanyak 2-3 ml diambil, dan penyulingan dilanjutkan, juga dengan refluks total
5. Pengambilan destilat, penyulingan dengan refluks total dilanjutkan dengan cara sama. Suhu atas dan bawah dan waktu saat pengambilan destilat supaya dicatat.
6. Destilat dan residu diukur densitasnya dan dengan tabel densitas sehingga konsentrasi dapat diketahui kadarnya.
E. DATA PERCOBAAN 1. Komposisi campuran
Alkohol (methanol) = 385 ml Aquadest = 115 ml Total volume umpan = 500 ml 2. Tinggi kolom = 52 cm 3. Tinggi packing = 42 cm 4. Suhu T aquadest = 300 C T alkohol = 280 C T campuran = 300 C 5. Penentuan densitas
Massa piknometer kosong = 8,1685 gr Massa pikno + aquades = 14,1810 gr Massa pikno + alkohol = 12,4952 gr Massa pikno + campuran = 13, 4208 gr 6. Standar alkohol
% Alkohol Massa (gr)
100 % 3,8753
90 % 3,8845
60% 4,0851 40% 4,2970 20% 4,3673 0% 4,7710 7. Setelah destilasi Massa pikno +
destilat (gr) T destilat (0C) Waktu
Massa pikno + residu T residu (0C) 12,8633 31 6 men. 3 det 13,2626 45 12,8762 31 2 men. 52 det 13,2743 46 12,8863 31 3 men. 59 det 13,2950 49 12,8572 31 2 men. 38 det 13,2104 48 12,8134 31 2 men. 23 det 13,3183 48 F. PERHITUNGAN 1. Menentukan densitas (ρ)
Massa aquades = (Massa piknometer + aquades) – massa piknometer kosong Massa aquades = (14,1810 – 8,1685) gr Massa aquades = 6,0125 gr Volume piknometer = ) 30 (T aquades aquades massa 0 C
= ml 0387 , 6 gr/ml 995646 , 0 gr 0125 , 6 Massa campuran = (massa pikno + campuran) – massa piknometer kosong = (13,4208 – 8,1685) gr = 5,2523 gr Densitas (ρ) campuran =
gr/ml
0,89956
ml
6,0387
gr
2523
,
5
Massa alkohol = (massa pikno + alkohol) – massa piknometer kosong Massa alkohol = (12,4952 – 8,1685) gr
Densitas (ρ) alkohol = piknometer volume alkohol massa =
gr/ml
0,716495
ml
6,0387
gr
3267
,
4
Dengan cara yang sama untuk deret standar alkohol maka diperoleh hasil sebagai berikut:
% Alkohol Massa (gr) Volume piknometer (ml) Densitas (gr/ml) 100 % 3,8753 6,0387 0,641744084 90 % 3,8845 6,0387 0,643267591 80% 3,9886 6,0387 0,6605064 60% 4,0851 6,0387 0,676486661 40% 4,2970 6,0387 0,711576995 20% 4,3673 6,0387 0,723218574 0% 4,7710 6,0387 0,790070711
Dengan cara yang sama untuk data setelah destilasi diperoleh hasil sebagai berikut: Massa pikno + destilat (gr) Densitas destilat Massa pikno + residu Densitas residu 12,8633 0,804083 13,2626 0,843576 12,8762 0,806292 13,2743 0,845513 12,8863 0,808022 13,2950 0,848941 12,8572 0,803038 13,2104 0,834931 12,8134 0,795537 13,3183 0,852799 2. Menentukan kadar ρ umpan = 0,89956 gr/ml T umpan = 300C
Kadar berat alkohol dihitung berdasarkan tabel 2-112 (Perry’s Chemical
Hand Book)
Interpolasi pada suhu 300C
%
737
,
52
x
0,737
52
89896
.
0
90125
,
0
89956
,
0
90125
,
0
53
52
52
x
x
0,898 53 0,90125 52%Dengan cara yang sama untuk data setelah destilasi diperoleh hasil sebagai berikut:
Densitas destilat
Kadar destilat Densitas residu Kadar residu 0,804083 93,507% 0,843576 76,4% 0,806292 92,707% 0,845513 75,6% 0,808022 91,971% 0,848941 74,2% 0,803038 90,217% 0,834931 79,92% 0,795537 96,253% 0,852799 72,6%
3. Menentukan fraksi mol
Fraksi mol umpan (Xf) secara praktek
Xf =
)
Air
Mr
%)
kadar
-(1
pikno
vol
umpan
(
)
Alkohol
Mr
%
kadar
pikno
vol
umpan
(
)
alkohol
Mr
%
kadar
pikno
vol.
umpan
(
=)
18
)
52737
,
0
1
(
0387
,
6
89956
,
0
(
)
07
,
46
52737
,
0
0387
,
6
89956
,
0
(
)
07
,
46
52737
,
0
0387
,
6
89956
,
0
(
=303
,
0
mol
2047
,
0
mol
0621
,
0
Fraksi mol destilat (Xd)
Xd =
)
Air
Mr
%)
kadar
-(1
pikno
vol
destilat
(
)
Alkohol
Mr
%
kadar
pikno
vol
destilat
(
)
alkohol
Mr
%
kadar
pikno
vol.
destilat
(
x 0,89956=
)
18
)
93507
,
0
1
(
0387
,
6
804083
,
0
(
)
07
,
46
93507
,
0
0387
,
6
804083
,
0
(
)
07
,
46
93507
,
0
0387
,
6
804083
,
0
(
=849095
,
0
mol
110668
,
0
mol
09855
,
0
Dengan cara yang sama untuk data setelah destilasi diperoleh hasil sebagai berikut: Densitas destilat Kadar destilat Xd 0,804083 93,507% 0,849095 0,806292 92,707% 0,832401 0,808022 91,971% 0,817369 0,803038 90,217% 0,782753 0,795537 96,253% 0,909392
Fraksi mol residu (Xb)
Xb=
)
Air
Mr
%)
kadar
-(1
pikno
vol
residu
(
)
Alkohol
Mr
%
kadar
pikno
vol
residu
(
)
alkohol
Mr
%
kadar
pikno
vol.
residu
(
=)
18
)
764
,
0
1
(
0387
,
6
843567
,
0
(
)
07
,
46
764
,
0
0387
,
6
843567
,
0
(
)
07
,
46
764
,
0
0387
,
6
843567
,
0
(
=558
,
0
mol
15125
,
0
mol
08447
,
0
Dengan cara yang sama untuk data setelah destilasi diperoleh hasil sebagai berikut:
Densitas residu
Kadar residu Xb
0,845513 75,6% 0,547626 0,848941 74,2% 0,529117 0,834931 79,92% 0,608619 0,852799 72,6% 0,508657 Menentukan α avg Suhu destilat 310C
Tekanan dihitung berdasarkan tabel 2-10 (Perry’s Chemical Hand Book) Alkohol Aquadest α destilat (αd) αd =
038
,
5
mmHg
15
,
34
mmHg
05
,
172
0
aquadest
P
alkohol
P
o Suhu residu 47,20C Alkohol 21,20C 100 mmHgmmHg
05
,
172
x
x
-100
05
,
72
200
100
100
8
,
34
2
,
21
31
2
,
21
x
310C 34,80C 200 mmHg 300C 31,8 mmHgmmHg
15
,
34
x
x
-31,8
35
,
2
3
,
55
8
,
31
8
,
31
40
30
31
30
x
310C 55,3 mmHg 400C 34,80C 200 mmHgmmHg
38
,
364
x
x
-200
38
,
164
400
200
200
9
,
49
8
,
34
2
,
47
8
,
34
x
47,20C 49,90C 400 mmHgAir α residu (αb) αb =
536
,
4
mmHg
42
,
80
mmHg
83
,
364
aquadest
P
alkohol
P
o o α avg =78
,
4
536
,
4
038
,
5
b d
log α avg = log 4,78 = 0,679
Menentukan jumlah plat teoritis minimal (Nmin) dan HETP
Nmin =
1
log
)
1
(
)
1
(
log
avgXd
Xb
Xb
Xd
=1
679
,
0
)
8490951
,
0
1
(
558468
,
0
)
558468
,
0
1
(
849095
,
0
log
= 0,45 HETP = cm cm 3 , 93 45 , 0 42 N isian bahan Tinggi min 470C 79,6 mmHgmmHg
42
,
80
x
x
-79,6
82
,
0
7
,
83
6
,
79
6
,
79
48
47
2
,
47
47
x
480C 83,7 mmHg 47,20CG. PEMBAHASAN
Pada praktikum ini dilakukan dengan tujuan untuk menentukan besarnya nilai Height Equivalent of Theoritical Plate (HETP). Nilai HETP ini merupakan nilai yang menunjukkan besarnya tinggi bahan isian dalam suatu kolom yang memberikan perubahan komposisi sama dengan perubahan komposisi yang dicapai oleh satu plate teoritis atau ekivalen dengan satu palte teoritis.
Pertama, alat di rangkai sesuai dengan gambar di alat di petunjuk praktikum, jika telah di susun, larutan umpan dengan konsentrasi 50% .Umpan yang digunakan dalam percobaan ini adalah campuran antara alkohol dengan aquadest dengan volume alkohol 385 ml dan aquadest 115 ml. Dipilihnya bahan alkohol karena bahan tersebut mempunyai titik didih yang lebih rendah dibandingkan dengan aquadest sehingga dapat dilakukan destilasi karena adanya perbedaan titik didih tersebut.
Dalam menentukan HETP, harus diketahui tinggi bahan isian yang digunakan serta jumlah plat teoritis. Jumlah plat teoritis (N) dapat dievaluasi menurut metode Mc. Cabe-Thiele dan metode Fenske-Underwood. Dalam percobaan ini digunakan metode Fenske-Underwood karena dalam percobaan ini dilakukan refluks total , sifat penguapan tetap (suhu tetap), dan kecepatan aliran molal tetap.
Dari hasil perhitungan diperoleh bahwa nilai HETP dalam kolom yang memberikan perubahan komposisi sama dengan perubahan komopsisi yang dicapai oleh satu plat teoritis adalah 93,33 cm.
Dalam percobaan penentuan besarnya nilai HETP ada beberapa hal yang perlu diperhatikan, diantaranya adalah:
1. Pada saat proses destilasi berlangsung, dipastikan tidak ada alkohol yang keluar melalui sambungan karena alkohol sangat volatil. Hal ini dapat dicegah dengan memberikan vaselin pada setiap sambungan.
2. Isian kolom diusahakan dalam kondisi kering sebelum digunakan, agar tidak mempengaruhi destilat dan residu.
3. Pengukuran densitas destilat dan residu pada suhu kamar. Tidak dilakukan pengukuran pada saat destilat dan residu masih panas karena akan mempengaruhi hasil penimbangan.
1. Nilai HETP berdasarkan percobaan adalah 93,33 cm.
I. DAFTAR PUSTAKA
1. Wasito, Bangun. 2014. Petunjuk Praktikum Operasi Teknik Kimia II. Yogyakarta: STTN-BATAN.
2. Poling, Bruce E, dkk. 2008. Perry’s Hand Book: Section 2 Chemical and Physical Data 8th Edition. Mc. Graw Hill.
3. Perry R. H., Green D., Perry’s Chemical Engineer’s Hand Book, Sixth Edition, 1988, McGraw-Hill, Tokyo
Yogyakarta, 05 Juni 2014
Asisten, Praktikan,