176
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari analisis data dan pembahasan secara deskriptif dan statistik, hasil penelitian dapat disimpulkan sebagai berikut:
1. Penerapan pendekatan saintifik efektif pada materi pokok laju reaksi siswa kelas XI IPA-3 SMA Negeri 5 Kupang adalah efektif. Secara rinci dapat disimpulkan sebagai berikut:
a. Guru mampu dalam mengelola kegiatan pembelajaran dengan menerapkan pendekatan saintifik pada materi pokok laju reaksi yang ditunjukkan dengan skor rata-rata sebesar 3,88 termasuk dalam kategori baik.
b. Ketuntasan indikator hasil belajar dengan menerapkan pendekatan saintifik meliputi:
1) Ketuntasan indikator hasil belajar sikap spiritual (KI-1) diperoleh dari rata-rata proporsi indikator angket dan observasi sebesar 0,83 dan 0,97 dinyatakan tuntas.
2) Ketuntasan indikator hasil belajar sikap sosial (KI-2) diperoleh dari rata-rata proporsi indikator angket dan observasi sebesar 0,86 dan 0,85 dinyatakan tuntas.
3) Ketuntasan indikator hasil belajar kognitif (KI-3) diperoleh dari rata-rata proporsi indikator THB sebesar 0,81 dinyatakan tuntas.
177
portofolio dan THB proses sebesar 0,89, 0,92, 0,86, dan 0,83 dinyatakan tuntas.
c. Ketuntasan hasil belajar dengan menerapkan pendekatan saintifik meliputi:
1) Ketuntasan hasil belajar sikap spiritual (KI-1) dinyatakan tuntas dengan nilai rata-rata sebesar 89,53.
2) Ketuntasan hasil belajar sikap sosial (KI-2) dinyatakan tuntas dengan nilai rata-rata sebesar 85,71.
3) Ketuntasan hasil belajar pengetahuan (KI-3) dinyatakan tuntas dengan nilai rata-rata sebesar 80,72.
4) Ketuntasan hasil belajar keterampilan (KI-4) dinyatakan tuntas dengan nilai rata-rata sebesar 88,91.
2. 2. Kreativitas aptitude siswa kelas XI IPA-3 SMA Negeri 5 Kupang
dengan presentase rata-rata tes kreativitas aptitude sebesar 76,56% termasuk dalam kategori tinggi.
3. 3. Kemampuan berpikir tingkat tinggi siswa kelas XI IPA-3 SMA
Negeri 5 Kupang dengan presentase rata-rata tes kemampuan berpikir tingkat tinggi sebesar 71,16% termasuk kategori tinggi.
4. 4. a. Ada hubungan kreativitas aptitude dengan hasil belajar siswa yang
menerapkan pendekatan saintifik pada materi pokok laju reaksi siswa kelas XI IPA-3 SMA Negeri 5 Kupang tahun ajaran
178
b. Ada hubungan kemampuan berpikir tingkat tinggi dengan hasil belajar siswa yang menerapkan pendekatan saintifik pada materi pokok laju reaksi siswa kelas XI IPA-3 SMA Negeri Kupang tahun ajaran 2016/2017 dengan korelasi Pearson Product Moment rx2y= 0,47.
c. Ada hubungan kreativitas aptitude dan kemampuan berpikir tingkat tinggi dengan hasil belajar siswa yang menerapkan pendekatan saintifik pada materi pokok laju reaksi siswa kelas XI IPA-3 SMA Negeri 5 Kupang tahun ajaran 2016/2017 dengan korelasi ganda rx1x2y = 0,55.
5. 5. a. Ada pengaruh kreativitas aptitude terhadap hasil belajar siswa
dengan menerapkan pendekatan saintifik pada materi pokok laju reaksi siswa kelas XI IPA-3 SMA Negeri 5 Kupang tahun ajaran 2016/2017 yang diperoleh dari persamaan garis regresi sederhana .
b. Ada pengaruh kemampuan berpikir tingkat tinggi terhadap hasil belajar siswa dengan menerapkan pendekatan saintifik pada materi pokok laju reaksi siswa kelas xi ipa-3 SMA Negeri 5 Kupang tahun ajaran 2015/2016 yang diperoleh dari persamaan regresi sederhana .
c. Ada pengaruh kreativitas aptitude dan kemampuan berpikir tingkat tinggi terhadap hasil belajar siswa dengan menerapkan pendekatan
179
persamaan garis regresi ganda
B. Saran
Berdasarkan hasil penelitian yang diperoleh, maka dapat dikemukakan beberapa saran sebagai berikut:
1. Bagi Siswa
Diharapkan untuk meningkatkan kreativitas aptitude dan kemampuan berpikir tingkat tinggi yang dimiliki sehingga dapat meningkatkan hasil belajar.
2. Bagi Guru
a. Pendekatan saintifik sangat baik dan efektif dalam pembelajaran kimia, oleh karena itu disarankan agar guru mata pelajaran kimia dapat menerapkannya dalam pembelajaran, pada materi pokok lain yang sesuai.
b. Bagi guru perlu memperhatikan dan meningkatkan kreativitas aptitude dan kemampuan berpikir tingkat tinggi siswa agar siswa lebih aktif dalam kegiataan pembelajaran di kelas.
3. Bagi Peneliti Selanjutnya
Yang ingin melakukan penelitian dengan menggunakan pendekatan saintifik agar benar-benar melaksanakan langkah-langkah pembelajaran
180 dapat meningkatkan hasil belajarnya.
Amaria dan Hendriyanto, Jefta . 2013. Unesa Journal Of Cemical Education Penerapan Model Pembelajaran Inkuiri. Untuk Melatih Kemampuan Berpikir Tinggi Siswa Pada Materi Pokok Laju Reaksi Impelementation Inquiry Learning Model For Training High Thinnking Skills Of The Studentes On Main Material Of Reaction Rate. Vol.2. No.2 Pp.151-18 ISSN 2252-9454.
Budiningsih, Asri .2005. Belajar dan Pembelajaran .Jakarta: PT Asdi Mahasastya
Daryanto,2014. Pendekatan Pembelajaran Saintifik Kurikulum 2013. Yogyakarta:Gava Media.
Dewizt, Peter. 2006. Jurnal padjono dan wardana.
Dewizt, Peter. 2006. Promoting High Order Thinking: Ptoward a More Comperhensive Chomperhensin Curiculum.
Dhiu, Margaretha. 2012. Pengantar Pendidikan. Nusa Indah:Flores.
Gunawan.W. Adi. 2013. Genius Learning Strategi.. Jakara: Gramedia Pustaka Utama.
Letuna, Agustina. 2015. Penerapan Konsep Diri dan Kreativitas Terhadap Hasil Belajar Dengan Menerapkan Pendekatan Scientific Siswa Kelas XI IPA SMAK Sint Carolus Penfui-Kupang Tahun Ajaran 2014/2015. Kupang Unwira
Lewi, Krathwal.2009.jurnal pendidikan Hayati Vol 1 No 1240.
Mangunharjana.1993. Usaha Dalam Membangun Kreativitas. Jakarta.
Munandar, Utami. 2012. Pengenbamgan dan Kreativitas Anak Berbakat. Jakarta: Rinekacipta.
Munandar, Utami. 1992. Pengenbamgan dan Kreativitas Anak Berbakat. Jakarta: Rinekacipta.
Dengan Menerapkan Pendekatan Inkuiri Terbimbing Pada Materi Pokok Koloid Siswa Kelas XI IPA 2 SMA Negeri 6 Kupang Tahun Pelajaran 2015/2016. Kupang Unwira.
Purba, Mickhael. 2006. Kimia untuk SMA Kelas XI.Surabaya.Erlangga. Riduwan dkk.2013. Pengantar Statistika. Bandung. Alfabeta.
Sanjaya, Wina.2006. Strategi Pembeajaran Berorientasi Standar Proses Pendidikan. Jakarta: Kencana Prenada Media Group.
Slameto. 2002. Belajar dan Faktor-faktor Yang Mempengaruhi Belajar. Bandung:PT Rosdakarya.
Sugiyono. 2014. Metode Penelitian Pendidikan. Bandung Alfabeta.
Supardi.2013. Aplikasi Statistika dan penelitian. Jakarta Selatan :Change Publication.
Unwira. 2012. Pedoman Akademik Tata Krama Dan Kegiatan Kemahasiswaan Universitas Katolik Widya Mandira Kupang.. Unwira:Kupang.
L
A
M
P
I
R
A
N
181
SILABUS MATA PELAJARAN KIMIA Satuan Pendidikan : SMA Negeri 5 Kupang
Kelas/Semester : XI IPA 1/1 Tahun Pelajaran : 2016/2017 Kompetensi Inti
KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya
KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia
KI 3 : Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah
182
KI 4 : Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metoda sesuai kaidah keilmuan
Kompetensi Dasar Materi
Pokok Pembelajaran Penilaian
Alokasi Waktu Sumber Belajar 1.1 Menyadariadanyaketera turandarisifathidrokarbo n, termokimia, lajureaksi, kesetimbangankimia, larutandankoloidsebaga iwujudkebesaranTuhan YME danpengetahuantentang adanyaketeraturanterseb utsebagaihasilpemikiran kreatif manusia yang kebenarannyabersifatte ntatif. Teori tumbukan Faktor-faktor penentu laju reaksi Orde reaksi dan persamaa n laju reaksi Mengamati(Observing) Mencariinformasidengancaramem baca/ melihat/ mengamatireaksi yang berjalan sangat cepat dan reaksi yang berjalan sangat lambat, contoh petasan, perkaratan (korosi)
Menanya(Questioning)
Mengajukan pertanyaan terkait hasil observasi mengapa ada reaksi yang lambat dan reaksi yang cepat
Mengumpulkan data (Eksperimenting)
Mendiskusikan pengertian laju reaksi
Mendiskusikan faktor-faktor yang mempengaruhi laju reaksi
Merancang dan mempresentasikan
Tugas Merancang percobaan faktor-faktor yang mempengaruh i laju reaksi Observasi Sikap ilmiah dalam melakukan percobaan dan presentasi, misalnya: melihat skala volume dan suhu,cara menggunakan 3 mgg x 4 jp - Buku kimia kelas XI - Lembar kerja - Berbagai sumber lainnya 2.1 Menunjukkan perilaku ilmiah (memiliki rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet,
183 Kompetensi Dasar Materi
Pokok Pembelajaran Penilaian
Alokasi Waktu
Sumber Belajar teliti, bertanggung
jawab, kritis, kreatif, inovatif, demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari.
hasil rancangan faktor-faktor yang mempengaruhi laju reaksi (ukuran, konsentrasi, suhu dan katalis) untuk menyamakan persepsi
Melakukan percobaan faktor-faktor yang mempengaruhi laju reaksi.
Mengamati dan mencatat data hasil percobaan
Mengasosiasi(Associating)
Mengolah data untuk membuat grafik laju reaksi
Mengolah dan menganalisis data hasil percobaan faktor-faktor yang mempengaruhi laju reaksi.
Mengolah dan menganalisis data hasil percobaan untuk menentukan orde reaksi dan persamaan laju reaksi
Menghubungkan faktor katalis dengan pengaruh katalis yang ada dalam industri pipet, cara menimbang, keaktifan, kerja sama, komunikatif, tanggungjawa b, dan peduli lingkungan, dsb) Portofolio Laporan percobaan Tes tertulis uraian Menganalsisd ata hasil percobaan faktor-faktor yang mempengaruh i laju reaksi Membuat 2.2 Menunjukkanperilaku kerjasama, santun, toleran, cintadamai dan peduli lingkungan serta hemat dalam
memanfaatkan sumber daya alam.
2.3 Menunjukkan perilaku responsive dan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan
184 Kompetensi Dasar Materi
Pokok Pembelajaran Penilaian
Alokasi Waktu Sumber Belajar 3.6 Memahami teori tumbukan (tabrakan) untuk menjelaskan reaksi kimia.
3.7 Menganalisis faktor-faktor yang
memengaruhi laju reaksi dan menentukan orde reaksi berdasarkan data hasil percobaan.
Mengkomunikasikan (Communicating)
Membuat laporan hasil percobaan dengan menggunakan tata bahasa yang benar.
Mempresentasikan hasil
percobaandengan menggunakan tata bahasa yang benar.
grafik laju reaksi berdasarkan data menganalisis data hasil percobaan untuk menentukan orde reaksi dan persamaan laju reaksi 4.6 Menyajikan hasil pemahaman terhadap teori tumbukan (tabrakan) untuk menjelaskan reaksi kimia. 4.7 Merancang, melakukan, dan menyimpulkan serta menyajikan hasil percobaan faktor-faktor yang memengaruhi laju reaksi dan orde reaksi.
(RPP 01)
Sekolah : SMA NEGERI 5 KUPANG Mata Pelajaran : Kimia
Kelas /Semester : XI IPA/3 Tahun Ajaran : 2016/2017 Materi Pokok : Laju Reaksi Alokasi Waktu : 2 x 45 Menit
A. Kompetensi Inti (KI)
KI 1 Menghayati dan mengamalkan ajaran agama yang dianutnya
KI 2 Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia
KI 3 Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah
KI 4 Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metoda sesuai kaidah keilmuan
B. Kompetensi Dasar
Kompetensi Dasar Indikator Pencapaian Kompetensi 1.1 Menyadari adanya keteraturan dari
sifat larutan sebagai wujud
1.1.1 Menyadari adanya keteraturan sifat larutan sebagai wujud kebesaran Tuhan Yang
186 kebesaran Tuhan YME dan pengetahuan tentang adanya keteraturan tersebut sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
Maha Esa dengan berdoa sebelum pembelajaran.
1.1.2 Menyadari adanya keteraturan sifat larutan sebagai wujud kebesaran Tuhan Yang Maha Esa dengan berdoa sesudah pembelajaran.
1.1.3 Bersyukur adanya keteraturan sifat laju reaksi dengan menunjukkan sikap doa yang baik
1.1.4 Bersyukur adanya keteraturan sifat laju reaksi dengan berdoa sesuai agama yang dianut.
2.1 Menunjukkan perilaku ilmiah (memiliki rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreatif, inovatif, demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari.
2.1.1 Disiplin dengan hadir, mengumpulkan kuis dan tugas rumah tepat waktu. 2.1.2 Rasa ingin tahu dengan mengamati
demonstrasi, memberikan dan menjawab pertanyaan.
2.1.3 Jujur dalam mengerjakan kuis dan menggunakan data percobaan (menggunakan data apa adanya dan hasilnya sesuai dengan data percobaan) 4.7.1 Teliti dalam mengamati pembuatan
larutan dengan konsentrasi tertentu, dan mengencerkan larutan, serta menyelesaikan soal kuis, dan tugas. 2.1.4 Bertanggung jawab dalam menjaga
alat-alat praktikum, presentasi, dan menyelesaikan soal diskusi. 2.2 Menunjukkan perilaku kerjasama,
santun, toleran, cinta damai dan peduli lingkungan serta hemat dalam memanfaatkan sumber daya alam.
4.7.2 Menunjukkan perilaku kerja sama dalam mengerjakan soal diskusi dan melakukan praktikum pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
187 2.3 Menunjukkan perilaku responsif
dan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan
2.3.1 Menunjukkan perilaku pro-aktif dengan mengamati hasil praktikum, mencatat hasil pengamatan, mencari sumber belajar, memberi pertanyaan dan menyampaikan ide dalam mengerjakan soal diskusi.
3.7 Menganalisis faktor-faktor yang mempengaruhi laju reaksi dan menentukan orde reaksi berdasarkan data hasil percobaan.
3.7.1 Menjelaskan pengertian molaritas
3.7.2 Menentukan konsentrasi (molaritas) suatu larutan
3.7.3 Menjelaskan tentang konsep laju reaksi 3.7.4 Menjelaskan hubungan laju reaksi dan
koefisien reaksi dalam kaitannya dengan pengertian laju reaksi
4.8 Merancang, melakukan, dan menyimpulkan serta menyajikan hasil percobaan faktor-faktor yang memengaruhi laju reaksi dan orde reaksi.
4.8.1 Merancang percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
4.8.2 Melakukan percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
4.8.3 Menyimpulkan hasil percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
4.8.4 Menyajikan data hasil percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
C. Tujuan Pembelajaran KI 1 (Sikap spiritual)
Selama proses pembelajaran siswa dapat:
1. Menunjukkan sikap doa sebelum pembelajaran dimulai 2. Menunjukkan sikap doa sesudah pembelajaran
3. Menunjukkan sikap doa yang baik
188 KI 2 (Sikap sosial)
Selama proses pembelajaran siswa dapat :
1. Menunjukkan perilaku disiplin dengan hadir, mengumpulkan kuis, dan tugas rumah tepat waktu.
2. Menunjukkan rasa ingin tahu dengan mengamati demonstrasi, memberikan dan menjawab pertanyaan.
3. Menunjukkan perilaku jujur dalam mengerjakan kuis dan menggunakan data percobaan (menggunakan data apa adanya dan hasilnya sesuai dengan data percobaan)
4. Menunjukkan perilaku teliti dalam mengamati pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan, serta menyelesaikan soal kuis, dan tugas
5. Menunjukkan perilaku bertanggung jawab dengan menjaga alat-alat praktikum, presentasi, dan menyelesaikan soal diskusi.
6. Menunjukkan perilaku kerjasama dalam mengerjakan soal diskusi dan melakukan praktikum pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
7. Menunjukkan perilaku pro-aktif dengan mengamati hasil praktikum, mencatat hasil pengamatan, mencari sumber belajar, memberi pertanyaan dan menyampaikan ide dalam mengerjakan soal diskusi.
KI 3 (Pengetahuan)
Setelah selesai pembelajaran siswa dapat :
1. Menjelaskan pengertian molaritas dan penggunaannya.
2. Menentukan konsentrasi (molaritas) larutan dari zat padat, zat cair dan campuran. 3. Membuat berbagai konsentrasi (M) larutan dari zat cair dan zat padat.
4. Menjelaskan tentang konsep laju reaksi.
5. Menjelaskan hubungan laju reaksi dan koefisien reaksi dalam kaitannya dengan pengertian laju reaksi.
KI 4 (Keterampilan) Siswa dapat :
1. Merancang percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
2. Melakukan percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
189
3. Menyimpulkan hasil percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
4. Menyajikan data hasil percobaan pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
D. Materi Pembelajaran
kemolaran
Konsep laju reaksi
E. Pendekatan dan metode pembelajaran
Pendekatan : Scientific
Metode : Praktikum, Diskusi, Kuis, dan Penugasan F. Kegiatan Pembelajaran
Langkah pembelajaran
Deskripsi kegiatan Alokasi
Waktu Kegiatan
Pendahuluan
o Guru menyapa siswa
o Guru meminta salah seorang siswa untuk memimpin doa sebagai wujud syukur atas kebesaran Tuhan YME.
o Guru menilai sikap doa siswa (sebelum kegiatan pembelajaran, sikap doa yang baik, dan sesuai dengan agama yang dianutnya). o Guru mengecek kehadiran siswa
o Guru menilai sikap disiplin (hadir tepat waktu) siswa
o Sebagai apersepsi guru memberikan informasi yang memancing rasa ingin tahu siswa dengan mengajukan pertanyaan :
“Mengapa dilaboratorium ada larutan dengan berbagai konsentrasi yang berbeda ?
o Guru menilai rasa ingin tahu siswa yang mengamati slide dan mencoba menjawab pertanyaan.
o Guru menyampaikan topik dan tujuan pembelajaran
o Guru menyampaikan penilaian yang akan
5 menit
190
diambil selama kegiatan pembelajaran kepada siswa
Kegiatan inti Mengamati
o Guru melakukan demonstrasi awal tentang larutan HCl dengan konsentrasi yang berbeda
o Siswa mengamati 2 botol yang berisi larutan HCl dengan konsentrasi yang berbeda
o Guru menilai rasa ingin tahu siswa dari sikap memperhatikan demonstrasi
Menanya
o Siswa diharapkan mengajukan pertanyaan:
- Bagaimana cara membuat larutan dengan
konsentrasi yang berbeda ?
o Guru menjelaskan secara singkat konsep laju reaksi.
o Guru menilai rasa ingin tahu siswa yang bertanya maupun yang menjawab pertanyaan yang diajukan
Mengumpulkan Data
o Guru membagi siswa kedalam kelompok diskusi. o Siswa membaca dan menelaah LKS yang telah
diberikan oleh guru.
o Siswa melakukan praktikum sesuai dengan langkah kerja pada LKS.
o Guru membimbing siswa mencatat hasil pengamatan.
o Siswa mengerjakan soal-soal pada LKS berdasarkan hasil praktikum.
o Guru menilai sikap kerja sama, teliti, pro-aktif, jujur dan tanggung jawab siswa dalam melakukan percobaan dan membaca data percobaan.
o Guru melakukan penilaian psikomotor (KI 4).
65 menit
191
o Guru memberikan kesempatan kepada siswa menganalisis data hasil percobaan yang mereka peroleh dengan membandingkan literatur atau sumber belajar yang ada untuk membuktikan hipotesis yang mereka buat.
o Guru membimbing siswa membuat kesimpulan sementara dari percobaan yang telah dilakukan. o Guru menilai sikap jujur, pro-aktif dan kerja
sama siswa dalam berdiskusi kelompok. Mengkomunikasikan
o Guru meminta salah satu kelompok untuk
mempresentasikan hasil kerja kelompok di depan kelas dan memberi kesempatan kepada kelompok lain untuk menanggapinya.
o Guru menilai sikap pro-aktif dan presentasi siswa.
o Guru mempertegas jawaban siswa
o Guru meminta siswa mengumpulkan hasil diskusi
Kegiatan penutup
o Guru memberikan kesempatan kepada siswa untuk menanyakan materi pembelajaran yang masih belum jelas.
o Siswa bersama guru menyimpulkan materi pembelajaran.
o Guru memberikan kuis kepada siswa
o Guru menilai sikap jujur saat mengerjakan kuis dan disiplin dalam mengumpulkan kuis tepat waktu.
o Guru memberi tugas untuk membuat laporan hasil percobaan yang telah dilakukan untuk dikumpulkan pada pertemuan selanjutnya serta membaca mengenai faktor-faktor yang mempengaruhi laju reaksi
15 menit 20 menit
192 o Siswa berdo’a.
o Guru menilai sikap doa siswa (Sesudah kegiatan pembelajaran, sikap doa yang baik, dan sesuai dengan agama yang dianutnya).
o Salam penutup.
G. Alat/ Bahan/ Sumber Belajar
Sumber belajar : Buku-buku Kimia SMA Kelas XI semester ganjil Bahan Ajar
Alat dan Bahan : LCD, Spidol, LKS, alat dan bahan praktikum H. Penilaian Hasil Pembelajaran
No. Aspek Teknik Bentuk Instrumen
1. Sikap sikap spiritual Observasi Angket
Lembar observasi aspek spiritual Lembar angket aspek spiritual 2. sikap aspek sosial Observasi
Angket
Lembar observasi aspek sosial Lembar angket aspek sosial 3. Pengetahuan tes tertulis Kuis
4. Keterampilan Observasi Lembar observasi psikomotor Lembar penilaian portofolio Lembar penilaian presentasi Lembar penilaian proses
193
RENCANA PELAKSANAAN PEMBELAJARAN (RPP 02)
Sekolah : SMA Negeri 5 KUPANG Mata Pelajaran : Kimia
Kelas /Semester : XI IPA/ 3 Tahun Ajaran : 2016/2017 Materi Pokok : Laju Reaksi Alokasi Waktu : 2 x 45 Menit
A. Kompetensi Inti (KI)
KI 1 Menghayati dan mengamalkan ajaran agama yang dianutnya
KI 2 Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia
KI 3 Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah
KI 4 Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metoda sesuai kaidah keilmuan.
194 B. Kompetensi Dasar
Kompetensi Dasar Indikator Pencapaian Kompetensi
1.1. Menyadari adanya keteraturan dari sifat larutan sebagai wujud kebesaran Tuhan YME dan pengetahuan tentang adanya keteraturan tersebut sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
1.1.1 Berdoa sebelum pelajaran dimulai sebagai tanda syukur kepada Tuhan yang Maha Esa.
1.1.2 Berdoa setelah pelajaran selesai sebagai tanda syukur kepada Tuhan Yang Maha Esa
1.1.3 Berdoa dengan cara/ sikap yang baik. 1.1.4 Berdoa seuai dengan ajaran agama yang
dianut. 2.1 Menunjukkan perilaku ilmiah
(memiliki rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreatif, inovatif, demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari.
2.1.1 Disiplin dengan hadir, mengumpulkan kuis dan tugas rumah tepat waktu. 2.1.2 Rasa ingin tahu dengan mengamati
demonstrasi, memberikan dan menjawab pertanyaan.
2.1.3 Jujur dalam mengerjakan kuis dan menggunakan data percobaan (menggunakan data apa adanya dan hasilnya sesuai dengan data percobaan) 2.1.4 Teliti dalam mengamati pembuatan
larutan dengan konsentrasi tertentu, dan mengencerkan larutan, serta
menyelesaikan soal kuis, dan tugas. 2.1.5 Bertanggung jawab dalam menjaga
alat-alat praktikum, presentasi, dan menyelesaikan soal diskusi. 2.3 Menunjukkan perilaku kerjasama,
santun, toleran, cinta damai dan peduli lingkungan serta hemat dalam memanfaatkan sumber daya alam.
2.3.1 Menunjukkan perilaku kerja sama dalam mengerjakan soal diskusi dan
melakukan praktikum pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
195 3.1. Menunjukkan perilaku responsif
dan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan
3.1.1 Menunjukkan perilaku pro-aktif dengan mengamati hasil praktikum, mencatat hasil pengamatan, mencari sumber belajar, memberi pertanyaan dan menyampaikan ide dalam mengerjakan soal diskusi.
3.7 Menganalisis faktor-faktor yang mempengaruhi laju reaksi dan menentukan orde reaksi berdasarkan data hasil percobaan.
3.7.5 Menjelaskan pengaruh konsentrasi terhadap laju reaksi.
3.7.6 Menjelaskan pengaruh suhu terhadap laju reaksi
3.7.7 Menjelaskan pengaruh luas permukaan bidang sentuh terhadap laju reaksi 3.7.8 Menjelaskan pengaruh katalis terhadap
laju reaksi
3.7.9 Menganalisis faktor-faktor yang mempengaruhi laju reaksi
4.8 Merancang, melakukan, dan menyimpulkan serta menyajikan hasil percobaan faktor-faktor yang memengaruhi laju reaksi dan orde reaksi.
4.8.1 Merancang percobaan 4 faktor yang mempengaruhi laju reaksi
4.8.2 Melakukan percobaan 4 faktor yang mempengaruhi laju reaksi
4.8.3 Menyimpulkan hasil percobaan 4 faktor yang mempengaruhi laju reaksi
4.8.4 Menyajikan data hasil percobaan 4 faktor yang mempengaruhi laju reaksi
C. Tujuan Pembelajaran KI 1 (Sikap spiritual)
Selama proses pembelajaran siswa dapat:
1. Berdoa sebelum pelajaran dimulai sebagai tanda syukur kepada Tuhan yang Maha Esa.
2. Berdoa setelah pelajaran selesai sebagai tanda syukur kepada Tuhan Yang Maha Esa.
3. Berdoa dengan cara/ sikap yang baik.
196 KI 2 (Sikap sosial)
Selama proses pembelajaran siswa dapat :
1. Menunjukkan perilaku disiplin dengan hadir, mengumpulkan kuis, dan tugas rumah tepat waktu.
2. Menunjukkan rasa ingin tahu dengan mengamati demonstrasi, memberikan dan menjawab pertanyaan.
3. Menunjukkan perilaku jujur dalam mengerjakan kuis dan menggunakan data percobaan (menggunakan data apa adanya dan hasilnya sesuai dengan data percobaan)
4. Menunjukkan perilaku teliti dalam mengamati 4 faktor yang mempengaruhi laju reaksi, serta menyelesaikan soal kuis, dan tugas
5. Menunjukkan perilaku bertanggung jawab dengan menjaga alat-alat praktikum, presentasi, dan menyelesaikan soal diskusi.
6. Menunjukkan perilaku kerjasama dalam mengerjakan soal diskusi dan melakukan praktikum 4 faktor yang mempengaruhi laju reaksi
7. Menunjukkan perilaku pro-aktif dengan mengamati hasil praktikum, mencatat hasil pengamatan, mencari sumber belajar, memberi pertanyaan dan menyampaikan ide dalam mengerjakan soal diskusi.
KI 3 (Pengetahuan)
Setelah selesai pembelajaran siswa dapat :
1. Menjelaskan pengaruh konsentrasi terhadap laju reaksi melalui percobaan. 2. Menjelaskan pengaruh suhu terhadap laju reaksi melalui percobaan.
3. Menjelaskan pengaruh luas permukaan bidang sentuh terhadap laju reaksi melalui percobaan.
4. Menjelaskan pengaruh katalis terhadap laju reaksi melalui percobaan 5. Menganalisis faktor-faktor yang mempengaruhi laju reaksi.
KI 4 (Keterampilan) Siswa dapat :
1. Merancang percobaan 4 faktor yang mempengaruhi laju reaksi Melakukan percobaan 4 faktor yang mempengaruhi laju reaksi
2. Menyimpulkan hasil percobaan 4 faktor yang mempengaruhi laju reaksi 3. Menyajikan data hasil percobaan 4 faktor yang mempengaruhi laju reaksi D. Materi Pembelajaran
197 E. Pendekatan dan metode pembelajaran
Pendekatan : Saintifik
Metode : Praktikum, Diskusi, Kuis, dan Penugasan F. Kegiatan pembelajaran :
Langkah
Pembelajaran Deskripsi kegiatan
Alokasi Waktu Kegiatan
Pendahuluan
o Guru menyapa siswa
o Guru meminta salah seorang siswa untuk memimpin doa sebagai wujud syukur atas kebesaran Tuhan YME.
o Guru menilai sikap doa siswa (sebelum kegiatan pembelajaran, sikap doa yang baik, dan sesuai dengan agama yang dianutnya).
o Guru mengecek kehadiran siswa
o Guru menilai sikap disiplin (hadir tepat waktu) siswa
o Sebagai apersepsi guru memberikan informasi yang memancing rasa ingin tahu siswa dengan mengajukan pertanyaan :
1. Sebuah pesawat , terbang dengan kecepatan 2000 km/jam. Apa arti dari angka 2000 km/ jam ?
Jawab : arti dari angkan 2000 km/ jam adalah pesawat tersebut telah berpindah sejauh 2000 km dalam waktu satu jam.
2. Perubahan kimia merupakan perubahan yang terjadi pada pereaksi dan hasil reaksinya. Apa yang yang berubah pada pereaksi dan hasil reaksi dalam suatu reaksi ?
Jawab : dalam reaksi kimia, perubahan yang terjadi pada pereaksi dan hasil reaksi adalah perubahan konsentrasinya
o Guru menilai rasa ingin tahu siswa yang mengamati slide dan mencoba menjawab
5 Menit
198 pertanyaan.
o Guru menyampaikan topik dan tujuan pembelajaran
o Guru menyampaikan penilaian yang akan diambil selama kegiatan pembelajaran kepada siswa Kegiatan Inti Mengamati
o Guru melakukan demonstrasi awal tentang kecepatan reaksi kimia
o Siswa mengamati 2 paku yang berkarat dan yang tidak berkarat serta pembakaran kembang api yang berukuran kecil
o Siswa diberikan fakta bahwa suatu reaksi kimia ada yang berlangsung cepat, seperti penyulutan kembang api, dan ada yang berlangsung lambat, seperti proses perkaratan besi.
o Guru menilai rasa ingin tahu siswa dari sikap memperhatikan demonstrasi
Menanya
o Siswa diharapkan mengajukan pertanyaan:
- Mengapa ada reaksi yang berlangsung cepat dan
ada reaksi yang berlangsung lambat?
- Apa yang menyebabkan suatu reaksi berlangsung
cepat atau lambat?
o Guru menjelaskan secara singkat konsep laju reaksi. o Guru menilai rasa ingin tahu siswa yang bertanya
maupun yang menjawab pertanyaan yang diajukan Mengumpulkan Data
o Setiap kelompok siswa dibagi menjadi 4 kelompok besar, untuk menerima LKS praktikum (Lampiran 4), dengan pembagian judul praktikum sebagai berikut: o Siswa membaca dan menelaah LKS yang telah
diberikan oleh guru.
o Siswa melakukan praktikum sesuai dengan langkah
65 menit
199 kerja pada LKS.
o Guru membimbing siswa mencatat hasil pengamatan. o Siswa mengerjakan soal-soal pada LKS berdasarkan
hasil praktikum.
o Guru menilai sikap kerja sama, teliti, pro-aktif, jujur dan tanggung jawab siswa dalam melakukan percobaan dan membaca data percobaan.
o Guru melakukan penilaian psikomotor (KI 4). Mengasosiasi
o Guru memberikan kesempatan kepada siswa menganalisis data hasil percobaan yang mereka peroleh dengan membandingkan literatur atau sumber belajar yang ada untuk membuktikan hipotesis yang mereka buat.
o Guru membimbing siswa membuat kesimpulan sementara dari percobaan yang telah dilakukan.
o Guru menilai sikap jujur, pro-aktif dan kerja sama siswa dalam berdiskusi kelompok.
Mengkomunikasikan
o Guru meminta salah satu kelompok untuk
mempresentasikan hasil kerja kelompok di depan kelas dan memberi kesempatan kepada kelompok lain untuk menanggapinya.
o Guru menilai sikap pro-aktif dan presentasi siswa. o Guru mempertegas jawaban siswa
o Guru meminta siswa mengumpulkan hasil diskusi Kegiatan
penutup
o Guru memberikan kesemptan kepada siswa untuk menanyakan materi pembelajaran yang masih belum jelas.
o Guru memberikan kuis kepada siswa
o Guru menilai sikap jujur saat mengerjakan kuis dan disiplin dalam mengumpulkan kuis tepat waktu. o Siswa bersama guru menyimpulkan materi
20 menit 20 menit
200 pembelajaran.
o Guru memberi tugas rumah dan tugas untuk membuat laporan hasil percobaan yang telah dilakukan untuk dikumpulkan pada pertemuan selanjutnya
o Siswa berdo’a.
o Guru menilai sikap doa siswa (sesudah kegiatan pembelajaran, sikap doa yang baik, dan sesuai dengan agama yang dianutnya).
o Salam penutup.
G. Alat/ Bahan/ Sumber Belajar
Sumber belajar : Buku-buku Kimia SMA Kelas XI semester ganjil Bahan Ajar
Alat dan Bahan : LCD, Spidol, LKS, alat dan bahan praktikum H. Penilaian Hasil Pembelajaran
No. Aspek Teknik Bentuk Instrumen
1. Sikap sikap spiritual Observasi Angket
Lembar observasi aspek spiritual Lembar angket aspek spiritual 2. Sikap aspek social observasi
Angket
Lembar observasi aspek sosial Lembar angket aspek sosial
3. Pengetahuan Tes tertulis Soal penugasan individu, Soal penugasan kelompok, kuis
4. Keterampilan Observasi Lembar observasi psikomotor Lembar penilaian portofolio Lembar penilaian presentasi lembar penilaian proses
201
RENCANA PELAKSANAAN PEMBELAJARAN (RPP 03)
Sekolah : SMA Negeri 5 KUPANG Mata Pelajaran : Kimia
Kelas /Semester : XI IPA/3 Tahun Ajaran : 2016/2017 Materi Pokok : Laju Reaksi Alokasi Waktu : 2 x 45 Menit A. Kompetensi Inti (KI)
KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya
KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia
KI 3 : Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah
KI 4 : Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metoda sesuai kaidah keilmuan.
B. Kompetensi Dasar
Kompetensi Dasar Indikator Pencapaian Kompetensi
1.1Menyadari adanya keteraturan dari sifat larutan sebagai wujud kebesaran
1.1.1 Berdoa sebelum pelajaran dimulai sebagai tanda syukur kepada Tuhan
202 Tuhan YME dan pengetahuan tentang adanya keteraturan tersebut sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
Yang Maha Esa
1.1.2 Berdoa setelah pelajaran selesai sebagai tanda syukur kepada Tuhan Yang Maha Esa
1.1.3 Berdoa dengan cara yang baik 1.1.4 Berdoa sesuai dengan ajaran agama
yang dianut. 2.1 Menunjukkan perilaku ilmiah (memiliki
rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreatif, inovatif, demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari.
2.1.1 Disiplin dengan hadir ,
mengumpulkan kuis dan tugas rumah tepat waktu yang telah ditentukan. 2.1.2 Rasa ingin tahu dengan mengamati
demonstrasi, memberikan dan menjawab pertanyaan.
2.1.3 Jujur dalam mengerjakan kuis dan menggunakan data percobaan (menggunakan data apa adanya dan hasilnya sesuai dengan data
percobaan)
2.1.4 Teliti dalam mengamati pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan, serta menyelesaikan soal kuis, dan tugas. 2.1.5 Bertanggung jawab dalam menjaga
alat-alat praktikum, presentasi, dan menyelesaikan soal diskusi.
2.3 Menunjukkan perilaku kerjasama, santun, toleran, cinta damai dan peduli lingkungan serta hemat dalam memanfaatkan sumber daya alam.
2.3.1 Menunjukkan perilaku kerja sama dalam mengerjakan soal diskusi dan melakukan praktikum pembuatan larutan dengan konsentrasi tertentu, dan mengencerkan larutan
2.4 Menunjukkan perilaku responsif dan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan
2.4.1 Menunjukkan perilaku pro-aktif dengan mengamati hasil praktikum, mencatat hasil pengamatan, mencari
203
masalah dan membuat keputusan sumber belajar, memberi pertanyaan dan menyampaikan ide dalam mengerjakan soal diskusi.
3.6 Memahami teori tumbukan (tabrakan) untuk menjelaskan reaksi kimia.
3.7.10 Menentukan orde reaksi berdasarkan analisis data yang diperoleh melalui percobaan
3.7.11 Menentukan harga dan satuan tetapan laju reaksi berdasarkan analisis data yang diperoleh meluai percobaan
3.7.12 Menggambarkan grafik orde reaksi 3.7.13 Menjelaskan grafik orde reaksi 3.7.14 Menjelaskan keterkaitan teori
tumbukan dengan faktor-faktor yang mempengaruhi laju reaksi berdasrkan teori tumbukan.
4.6 Menyajikan hasil pemahaman terhadap teori tumbukan (tabrakan) untuk menjelaskan reaksi kimia.
4.6.1 Merancang percobaan faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
4.6.2 Melakukan percobaan faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
4.6.3 Menyimpulkan hasil percobaan faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
4.6.4 Menyajikan data hasil percobaan faktor mempengaruhi laju reaksi berdasarkan teori tumbukan
C. Tujuan Pembelajaran KI 1 (Sikap spiritual)
Selama proses pembelajaran siswa dapat:
204
2. Menunjukkan sikap doa sesudah pembelajaran 3. Menunjukkan sikap doa yang baik
4. Menunjukkan sikap doa sesuai dengan ajaran agama yang dianutnya KI 2 (Sikap sosial)
Selama proses pembelajaran siswa dapat :
1. Menunjukkan perilaku disiplin dengan hadir, mengumpulkan kuis, dan tugas rumah tepat waktu.
2. Menunjukkan rasa ingin tahu dengan mengamati demonstrasi, memberikan dan menjawab pertanyaan.
3. Menunjukkan perilaku jujur dalam mengerjakan kuis dan menggunakan data percobaan (menggunakan data apa adanya dan hasilnya sesuai dengan data percobaan)
4. Menunjukkan perilaku teliti dalam mengamati 4 faktor yang mempengaruhi laju reaksi, serta menyelesaikan soal kuis, dan tugas
5. Menunjukkan perilaku bertanggung jawab dengan menjaga alat-alat praktikum, presentasi, dan menyelesaikan soal diskusi
6. Menunjukkan perilaku kerjasama dalam mengerjakan soal diskusi dan melakukan praktikum 4 faktor yang mempengaruhi laju reaksi
7. Menunjukkan perilaku pro-aktif dengan mengamati hasil praktikum, mencatat hasil pengamatan, mencari sumber belajar, memberi pertanyaan dan menyampaikan ide dalam mengerjakan soal diskusi.
KI 3 (Pengetahuan)
Setelah selesai pembelajaran siswa dapat :
1. Menentukan orde reaksi berdasarkan analisis data yang diperoleh melalui percobaan
2. Menentukan harga dan satuan tetapan laju reaksi berdasarkan analisis data yang diperoleh meluai percobaan
3. Menggambarakan grafik orde reaksi 4. Menjelaskan grafik orde reaksi
5. Menjelaskan keterkaitan teori tumbukan dengan faktor-faktor yang mempengaruhi laju reaksi..
KI 4 (Keterampilan) Siswa dapat :
205
1. Merancang percobaan faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
2. Melakukan percobaan faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
3. Menyimpulkan hasil percobaan faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
4. Menyajikan data hasil percobaan faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
D. Materi pembelajaran
Orde reaksi
Grafik orde reaksi
Teori tumbukan
Hubungan antara faktor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan
E. Pendekatan dan metode pembelajaran
Pendekatan : Saintifik
Metode : Praktikum, Diskusi, Kuis, dan Penugasan F. Kegiatan Pembelajaran
Langkah
Pembelajaran Deskripsi kegiatan
Alokasi Waktu Kegiatan
pendahuluan
o Guru menyapa siswa
o Guru meminta salah seorang siswa untuk memimpin doa sebagai wujud syukur atas kebesaran Tuhan YME.
o Guru menilai sikap doa siswa (sebelum kegiatan pembelajaran, sikap doa yang baik, dan sesuai dengan agama yang dianutnya).
o Guru mengecek kehadiran siswa
o Guru menilai sikap disiplin (hadir tepat waktu) siswa
o Sebagai apersepsi guru memberikan informasi yang memancing rasa ingin tahu siswa dengan mengajukan pertanyaan :
5 menit
206
suatu hari, Lora dan Mia ingin membuat kolak dan salah satu bahan yang igunakan adalah Gula. Gula yang digunakan oleh lora dan Mia adalah gula lempeng, kira – kira bagaiamana caranya agar gula lempeng yang digunakan oleh Lora dan Mia untuk membuat kolak bisa cepat larut ?”
Jawab :
o Cara agar gula lempeng cepat larut dalam air
kolak tersebut adalah Gula tersebut diiris menjadi halus, karena dengan ukuran yang lebih kecil luas bidang sentuh air terhadap gula semakin besar yang menyebabkan gula cepat larut
o Guru menilai rasa ingin tahu siswa yang mengamati slide dan mencoba menjawab pertanyaan.
o Guru menyampaikan topik dan tujuan pembelajaran
o Guru menyampaikan penilaian yang akan diambil selama kegiatan pembelajaran kepada siswa Kegiatan inti Mengamati
o Guru melakukan demonstrasi awal tentang teori tumbukan
o Guru melakukan demonstrasi tentang teori tumbukan menggunakan plastisin yang dibuat bulat kemudian dirapatkan satu sama lain lalu dikutik dengan kelereng dengan kekuatan yang sama dri smping dan dari depan.
o Siswa diminta mengamati demonstrasi tersebut. o Guru menilai rasa ingin tahu siswa dari sikap
memperhatikan demonstrasi Menanya
o Siswa diharapkan mengajukan pertanyaan:
Mengapa ketik dikutik dari depan plastisin lebih
207
mudah terlepas sedangkan ketika dikutik dari samping tidak terpisah walaupun dikutik dengan kekuatan yang sama.
Apa yang menyebabkan Plastisin lebih mudah terpisah satu sama lain walaupun dikutik dengan kekuatan yang sama.
o Guru menjelaskan secara singkat tentang teori tumbukan.
o Guru menilai rasa ingin tahu siswa yang bertanya maupun yang menjawab pertanyaan yang diajukan. Mengumpulkan Data
o Setiap kelompok siswa dibagi menjadi 4 besar, untuk menerima LKS praktikum (Lampiran 4), dengan pembagian judul praktikum sebagai berikut:
o Siswa membaca dan menelaah LKS yang telah diberikan oleh guru.
o Siswa melakukan praktikum sesuai dengan langkah kerja pada LKS.
o Guru membimbing siswa mencatat hasil pengamatan. o Siswa mengerjakan soal-soal pada LKS berdasarkan
hasil praktikum.
o Guru menilai sikap kerja sama, teliti, pro-aktif, jujur dan tanggung jawab siswa dalam melakukan percobaan dan membaca data percobaan.
o Guru melakukan penilaian psikomotor (KI 4). Mengasosiasi
o Guru memberikan kesempatan kepada siswa menganalisis data hasil percobaan yang mereka peroleh dengan membandingkan literatur atau sumber belajar yang ada untuk membuktikan hipotesis yang mereka buat.
o Guru membimbing siswa membuat kesimpulan sementara dari percobaan yang telah dilakukan.
208
o Guru menilai sikap jujur, pro-aktif dan kerja sama siswa dalam berdiskusi kelompok.
Mengkomunikasikan
Guru meminta salah satu kelompok untuk
mempresentasikan hasil kerja kelompok di depan kelas dan memberi kesempatan kepada kelompok lain untuk menanggapinya.
o Guru menilai sikap pro-aktif dan presentasi siswa. o Guru mempertegas jawaban siswa
o Guru meminta siswa mengumpulkan hasil diskusi Kegiatan
penutup
Guru memberikan kesempatan kepada siswa untuk menanyakan materi pembelajaran yang masih belum jelas.
Siswa bersama guru menyimpulkan materi pembelajaran
Guru memberikan kuis kepada siswa
Guru menilai sikap jujur saat mengerjakan kuis dan disiplin dalam mengumpulkan kuis tepat waktu. Guru memberi tugas rumah dan tugas untuk membuat
laporan hasil percobaan yang telah dilakukan untuk dikumpulkan pada pertemuan selanjutnya
Siswa berdo’a.
Guru menilai sikap doa siswa (sesudah kegiatan pembelajaran, sikap doa yang baik, dan sesuai dengan agama yang dianutnya).
Salam penutup.
15 menit 20 menit
209 G. Penilaian Hasil Pembelajaran
No. Aspek Teknik Bentuk Instrumen
1. Sikap sikap spiritual Observasi Angket
Lembar observasi aspek spiritual Lembar angket aspek spiritual 2.
Sikap aspek sosial
Observasi Angket
Lembar observasi aspek sosial Lembar angket aspek sosial
3.
pengetahuan Tes tertulis
Soal penugasan individu, Soal penugasan kelompok, kuis
4. Keterampilan Observasi Lembar observasi psikomotor Lembar penilaian portofolio Lemba penilaian presentasi Lembar penilaian proses
210
BAHAN AJAR SISWA (Rpp 01 )
Kemolaran (M)
Kemolaran atau molaritas menyatakan konsentrasi (kepekatan) dari suatu larutan yang menggambarkan jumlah mol zat terlarut dalam setiap liter larutan. Kemolaran diberi notasi M, dengan satuan mol/liter.
Kemolaran berkaitan dengan jumlah mol dan volume larutan.
Keterangan: M = Kemolaran (M)
N = jumlah mol zat (mol)
V = volume larutan (liter atau L)
Jika zat terlarut dinyatakan dalam satuan gram dan volume larutan dinyatakan dalam mL atau cm3 , kemolaran dapat dirumuskan sebagai berikut:
x
Keterangan : M = kemolaran (M)
m = massa zat terlarut (gram atau g)
Mr = massa molekul realatif zat terlarut
211 Contoh Soal:
1. Hitunglah konsentrasi larutan jika 15 g ureua (Mr = 60) dilarutkan dalam air hingga volumenya menjadi 500 mL !
Jawab: Cara I: 0,25mol Cara II: M = Cara III: x x x = Konsentrasi larutan 0,5 M.
Jika konsentrasi larutan dinyatakan dalam bentuk presentase (P):
Massa (m)
212 M = Keterangan : M = Kemolaran (M)
P = Persen fase larutan (%)
V = Volume larutan (mL)
Mr = Massa molekul relatif
= massa jenis larutan (g mL-1) Contoh soal:
Terdapat 100 mL larutan NaOH 4% dengan massa jenis ( ) = 1,1 gr.cm3 . jika Mr NaOH = 40, tentukan kemolaran larutan NaOH tersebut.
Penyelesaian :
Massa larutn NaOH = x V = 1.1 gr. Cm3 x 100 mL = 110 gr
Massa NaOH terlarut =
Jadi, kemolaran larutan NaOH = 1,1 M.
Membuat Larutan Baku:
- Tentukan kemolaran dan volume larutan yang diinginkan - Hitunglah massa zat dan timbang dengan tepat
- Larutkan zat yang ditimbang dengan air pada labu ukur - Tambahkan air sampai tanda batas labu ukur.
213 - Mengencerkan Larutan Pekat
Perhitungan yang digunakan dalam proses pengenceran dirumuskan sebagai berikut:
Keterangan:
= jumlah mol zat sebelum diencerkan jumlah mol zat setelah diencerkan Langkah-langkah Pengenceran : - Hitung kemolaran larutan zat
- Hitung volume zat yang harus dipipet
- Pipet zat dan masukkan ke dalam labu ukur berisi air sambil terus dikocok - Tambahkan air sampai tanda batas labu ukur.
Contoh soal:
1. Hitung kemolaran larutan H2SO4 pekat . Jika H2SO4 yang tersedia memiliki kadar 98% dan massa jenis ( ) = 1,8 mL-1
, kemolaran H2SO4 pekat adalah: ` M H2SO4 =
214
2. Hitung volume H2SO4 yang harus dipipet menggunakan rumus pengenceran.
V1 x M1 = V2 x M2
V1 x 18 M = 100 mL x 0,3 M = 1.67 mL
Jadi, volume H2SO4 pekat yang harus dipipet adaalah 1, 67 mL.
Jika dua atau lebih larutan yang mengandung zat yang sama, tetapi kemolarannya berbeda dicampurkan larutan tersebut akan memiliki kemolaran yang baru. Kemolaran campuran tersebut dapat dihitung dengan menggunakan rumus berikut:
M M =
Contoh soal:
Jika anda mencampurkan 150 mL larutan NaCl 0,2 M dan 250 mL larutan NaCl 0,6 M, berapakah kemolaran NaCl setelah dicampurkan?
Jawab: M M M M Konsep Laju Reaksi
215
Reaksi-reaksi kimia berlangsung dengan kecepatan reaksi yang berbeda-beda, ada yang sangat cepat ada pula yang sangat lambat.
Misalnya:
Kertas (terbakar) menjadi abu adalah reaksi yang sangat cepat, sebaliknya besi menjadi karat besi memerlukan waktu bertahun-tahun.
“kecepatan reaksi atau laju reaksi adalah perubahan konsentrasi pereaksi atau hasil reaksi persatuan waktu”.
“Konsentrasi pereaksi dalam suatuu reaksi kimia semakin lama semakin berkurang, sedangkan hasil reaksi semakin lama semakin bertambah”.
Hasil reaksi (C+D)
Pereaksi (A+B)
Waktu
Pereaksi Hasil reaksi
(konsentrasi semakin berkurang) (konsenttrasi semakin bertambah) Maka :
Laju reaksi terhadap A adalah : VA =
Laju reaksi terhadap B adalah : VB =
Laju reaksi terhadap C adalah : VC =
216 Laju reaksi terhadap D adalah : VD =
Keterangan:
VA , VB = Laju perubahan konsentrasi pereaksi
Tanda (-) dan perubahan konsentrasi negatif hanya menunjukkan pengurangan konsentrasi sehingga laju reaksinya tetap positif.
VC, VD = laju perubahan konsentrasi hasil reaksi
Tanda positif (+) menunjukkan penambahan konsentrasi
Dengan demikian, laju reaksi dapat dinyatakan sebagai pengurangan konsentrasi pereaksi per satuan waktu, atau penambahan konsentrasi hasil reaksi per satuan waktu.
Laju reaksi memiliki satuan Ms-1 (M = Molar dan s = sekon = detik). Contoh soal:
1. Ke dalam tabung reaksi yang berisi 200 mL larutan HCl 2 M dimasukan 8 gram serbuk seng. Jika setelah 2 menit masih tersisa sebanyak 1,5 gram. Tentukan laju pengurangan seng? (Ar ; Zn = 65) Jawab:
Persamaan reaksi : Zn (s) + 2HCl (aq) + H2 (g) Massa Zn yang bereaksi = 8 gr – 1,5 gr = 6,5 gr
nA =
217
[A] yang bereaksi =
t = 2 menit =2 x 60 sekon = 120 sekon
Zn = 10 -3 Ms-1
Jadi, laju pengurangan logam Zn adalah 10-3 Ms-1 2. Daalam ruang 10 Liter terjadi reaksi : A + B 2C
Setelah 5 detik dihasilkan 0,3 mol C. Nyatakan laju reaksi terhadap A, b dan C.
Penyelesaian:
A + B 2C
½ . 0,3 3/2 . 0,3 0,3 = 0,15 mol 0,45 mol
Dalam waktu 5 detik zat A yang bereaksi 0,15 mol; [A] =
= -0,015 M Dalam waktu 5 detik zat B 0,45 mol;
[B] =
= -0,045 M Dalam waktu 5 detik zat C 0,3 mol;
[C] =
= -0,03 M Laju reaksi terhadap A adalah:
vA =
= 0,003 M/s Laju reaksi terhadap B adalah:
218 vB =
= 0,009 M/s Laju reaksi terhadap A adalah:
vC =
= 0,006 M/s
Hubungan Laju Reaksi dan Koefisien Reaksi
Dalam stoikiometri, perbandingan koefisien reaksi menyatakan perbandingan jumlah molpereaksi atau hasil reaksi.
Perhatikan reaksi berikut:
Tanda (+) dan (-) hanya menunjukkan sifat perubahan sehingga dalam perbandingan tdapat dihilangkan. Dalam perbandingan, waktu reaksi dianggap sama sehingga:
= [A] : [B] : [C] : [D].
Satuan konsentrasi adalah mol L-1 sehingga
Dalam perbandingan, volume setiap zat dianggap sama sehingga:
Dalam stoikiometri, perbandingan mol berbanding lurus dengan perbandingan koefisien reaksi.
Jadi, dalam suatu reaksi kimia, laju reaksi suatu zat berbanding lurus dengan perbandingan koefisian reaksi zat tersebut.
219
Contoh soal:
1. Diketahui persamaan reaksi penguraian senyawa SO3 adalah 2SO3 2SO2 + O2. Tentukan perbandingan laju perubahan konsentrasi SO3 : SO2 : O2.
Jawab:
2 : 2 : 1
220
BAHAN AJAR SISWA RPP 02
FAKTOR FAKTOR YANG MEMPENGARUHI LAJU REAKSI
1. Pengaruh Konsentrasi (C).
Konsentrasi berkaitan dengan jumlah partikel makin besar konsentrasi berarti makin banyak partikel sehingga makin banyak partikel sehingga makin banyak yang bergerak dan makin banyak yang bertumbukan dan dengan banyaknya partikel yang bertumbukkan laju reaksinya makin besar.
Jadi :
221 2. Pengaruh Temperatur (T)
Kenaikan temperature berpengaruh besar terhadap kenaikan pergerakan partikel, sehingga laju reaksinya semakin besar.Disamping itu, perubahan temperatur akan mempengaruhi (konsentrasi) juga pada harga konstanta laju reaksi. Temperatur makin besar maka harga k makin besar. Jadi temperature makin besar, maka laju reaksi makin besar, begitu juga sebaliknya.
Jadi :
Jika T ↑ maka V ↑ dan T ↓ maka V ↓ Contoh :
Untuk laju reaksi adalah dengan proses melarutkan bahan. Kalau kita melarutkan gula maka akan lebih cepat larut pada air mendidih daripada air yang dinging.
222
Pengaruh luas permukaan terhadap laju reaksi sama seperti pengaruhnya terhadap tumbukkan. Untuk itu makaluas permukaan makin besar akan menyebabkan jumlah tumbukan makin besar, sehingga diharapkan laju reaksi semakin besar.
Misalnya :
Kita melarutkan gula merah dalam air, maka akan semakin cepat larut kalau gula tersebut diiris-iris terlebih dahulu. Pengirisan gula/ penghalusan bahan merupakan cara memperbesar permukaan bahan.
Jadi :
Jika A ↑ maka V ↑ dan A ↓ maka V ↓
223
Katalis adalah suatu zat yang dapat mempercepat atau memperlambat laju reaksi.
Katalis yang sifatnya mempercepat suatu reaksi disebut katalisator sedangkan katalis yang memperlambat suatu reaksi disebut inhibitor.
Contoh :
Katalis NO2(g) digunakan pada reaksi SO2 dan O2(g) Reaksi :
2SO2 + O2 tanpa katalis 2SO3 (lambat) NO
2
2SO2 + O2 2SO3 (cepat) Mekanisme Reaksi :
2SO2+ 2NO2 2SO3 + 2NO
Persamaan Laju Reaksi dan Orde Reaksi a. Persamaan Laju Reaksi
Laju reaksi menyatakan perubahan konsentrasi zat-zat yang terlibat
224
Laju reaksi sangat dipengaruhi oleh konsentrasi pereaksi. Semakin besar konsentrasi pereaksi laju reaksinya semakin besar dengan demikian persamaan reaksi bergantung pada konsentrasi pereaksi. Persamaan laju reaksi:
x A + y B = o C V = k . Dengan :
V = laju Reaksi (Ms-1) [A] = konsentrasi zat A (M) [B] = konsentrasi zat B (M) K = konstanta laju reaksi x = orde reaksi zat A y = orde reaksi zat B x + y = orde reaksi total b. Orde Reaksi
Orde reaksi adalah bilangan pangkat konsentrasi pada persamaan laju reaksi. Orde reaksi selalu ditentukan oleh konsentrasi reaktan (pereaksi) bukan produk (hasil reaksi).
Jenis-jenis orde reaksi : 1. Reaksi Orde Nol
225
Persamaan Reaksi Persamaan Laju Reaksi
CH3COOH + H2O CH3COOH + CH3OH
v = k [CH3COOH3] [H2O]0 Catatan: orde nol untuk H2O
NO2 + H2 H2O+ NO v = k [NO2]2 [H2]0
Catatn: orde nol untuk H2
2. Reaksi Orde Satu
V = k [A]...(2)
Persamaan Reaksi Persamaan Laju Reaksi 2NO2 4NO2 + O2 V = k [N2O5]
2H2O2 2H2O + O2 V = k [H2O] SO2Cl2 SO2 + Cl2 V = k [SO2Cl2] C2H5Cl C2H4 + HCL V = k [C2H5Cl]
226 3. Reaksi Orde Dua
V = k [A]2 atau v = k [A] [B] ...(3)
Persamaan Reaksi Persamaan Laju Reaksi NO + O3 NO2 + O2 V = k [NO] [O3]
O2 2NO + CO2 V = k [NO2]2 NO2 + CO NO + O2 V = k [NO2][CO] 2H2 + SO2 2H2O + S V = k [H2][SO2] H2 + I2 2HI V = k [H2][I2]
4. Reaksi Orde Tiga
v = [A]2 [B], v = k [A] [B]2, v = k [C]3, atau v = [A] [B] [C] Persamaan Reaksi Persamaan Laju Reaksi 2NO + 2H2 N2 + 2H2O V = k [NO]2 [H2] 2NO + Br2 2NOBr V = k [NO]2 [Br] 2NO + Cl2 2NOCl V = k [NO]2 [Cl2]
227 5. Reaksi Orde Pecahan
Persamaan reaksi Persamaan laju Reaksi CO + Cl2 COCl2 v = k [ CO] [Cl2]3/4 CHCl3 + Cl2 CCl4 + HCl v = k [ CHCl3] [Cl2]1/4
2. Penentuan Orde Reaksi dan Persamaan Laju Reaksi
Orde reaksi dapat ditentukan dengan cara membandingkan data laju reaksi sebagai fungsi dari konsentrasi pereaksi. Contohnya pada reaksi pembentukan NO2.
Reaksi yang terjadi adalah : 2NO + O2 → 2NO2
Pada percobaan ini diperoleh data sebagai berikut :
No [NO](M) [O2](M) v (Ms-1) 1 2 3 4 5 0,1 0,2 0,3 0,2 0,3 0,1 0,1 0,2 0,3 0,3 1,20 x 10-3 4,80 x 10-3 2,16 x 10-3 1,44 x 10-3 3,24 x 10-3
Berdasarkan data tersebut diatas, dapat ditentukan orde reaksi dan persamaan laju reaksi dengan langkah-langkah sebagai berikut :
228
Dimisalkan persamaan laju reaksi v = k [NO]x [O2]y. untuk mencari orde reaksi NO(x), maka dipilih konsentrasi O2 yang sama, yaitu data (1) dan (2) atau data (4) dan (5) sehingga faktor O2 dapat dihilangkan dalam perbandingannya.
Berdasarkan data nomor (1) dan (2) : y x O O NO NO k k V V ) 2 ( 2 ) 1 ( 2 ) 2 ( ) 1 ( ) 2 ( ) 1 ( ) 2 ( ) 1 (
, harga k(1) = k(2) (karena suhu tetap) dan O2(1)
= O2(2) sehingga ) 2 ( 2 ) 1 ( 2 O O dapat dihilangkan. x y x M M x M M Ms x Ms x 2 , 0 1 , 0 1 , 0 1 , 0 2 , 0 1 , 0 10 80 , 4 10 20 , 1 1 3 1 3 2 , 2 1 4 1 x x
. Jadi orde reaksi NO = 2
b) Menentukan orde reaksi O2
Untuk menentukan orde reaksi O2(y), pilih data [NO] yang sama, yaitu data nomor (2) dan (4) atau data nomor (3) dan (5). Berdasarkan data nomor (2) dan (4) : 1 , 3 1 3 1 3 , 0 1 , 0 10 44 , 1 10 80 , 4 1 2 1 3 ) 4 ( 2 ) 2 ( 2 ) 4 ( ) 2 ( y M M Ms x Ms x O O V V y y
Jadi orde reaksi O2 = 1 c) Menentukan orde reaksi total
229 = 2 + 1 = 3
Persamaan laju reaksi dapat dituliskan sebagai berikut : v = k [NO]2 [O2]
230
BAHAN AJAR SISWA (BAS RPP 03)
I. Teori Tumbukan
Berdasarkan teori kinetik-molekuler, reaktan harus bertumbukan agar dapat bereaksi, mereka harus bertumbukan dengan energi yang cukup dan orientasi yang tepat, sehingga dapat memutuskan ikatan lama untuk membentuk ikatan baru;
“Bila temperatur naik, maka energi kinetik rata-ratanya bertambah – laju reaksi juga bertambah. Bila konsentrasi dinaikkan, maka jumlah tumbukan akan bertambah sehingga laju reaksipun meningkat.
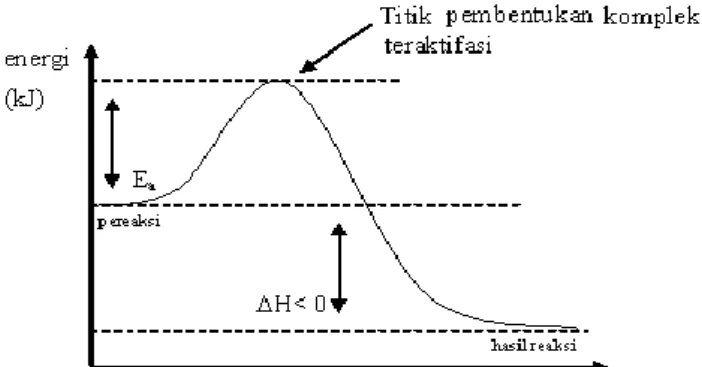
Reaksi antara molekul-molekul pereaksi terjadi apabila terjadi tumbukan. Untuk saling bertumbukan, molkul-molekul pereaksi harus mempunyai energi kinetik minimum tertentu. Energi minimum yang harus dimiliki oleh partikel pereaksi untuk menghasilkan tumbukan yang efektif disebut energi aktivasi (Ea). Jadi, jika enrgi aktivasi terlampaui, reaksi dapat berlangsung. Sebaliknya, jika energi aktivasi tidak terlampaui, reaksi kimia tidak akan berlangsung.
II. Energi Pengaktifan
Tidak semua tumbukan menghasilkan reaksi. Misalnya,kertas dan kayu tidak terbakar ketika bersentuhan dengan oksigen pada suhu kamar.Namun,setelah dibakar dengan korek api,kayu dan kertas akan terbakar. Pembakaran itu akan menghasilkan energi yang jauh lebih besar
231
dari pada energi yang diberikan oleh korek api. Reasi seperti itu disebut reaksi eksoterm. Dengan demikian,kertas dan kayu dapat bereaksi dengan oksigen di udara jika mendapat energi tambahan dari luar.
Reaksi kebalikan dari reaksi eksoterm adalah reaksi endoterm. Reaksi endoterm memerlukan energi yang lebih besar daripada energi yang dibebaskan. Dengan kata lain energi yang dibebaskan tidak cukup untuk mengaktifkan molekul lain agar terjadi reaksi. Oleh karna itu, pada reaksi endoterm harus ditambahkan energi secara terus menerus.
Gambar grafik: E Keadaan transisi produk Energi pengaktifan Ea +∆H reaksi pereaksi
232 jalan reaksi
Energi pengaktifan bergantung pada suhu reaksi. Reaksi yang bergantung pada suhu rendah berarti memiliki energi pengaktifan rendah. Reaksi yang hanya dapat berlangsungpada suhu tinggi memiliki energi pengaktifan besar.
III. Faktor-faktor yang mempengaruhi laju reaksi berdasrkan teori tumbukan
a. Konsentrasi Pereaksi
Berhubungan dengan teori tumbukan menyatakan bahwa: semakinb besar konsentrasi, semakin besar kemungkinan terjadinya tumbukan antarmolekul yang bereaksi sehingga laju reaksi semakin cepat berlangsung.
Contoh: 3M HCl lebih cepat bereaksi dari pada 2M HCl. b. Suhu
Dengan menggunakan teori tumbukan, jelas bahwa semakin tinggi suhu, maka molekul-molekul yang mencapai energi aktivasi semakin banyak, sehingga laju reaksi semakin cepat berlangsung.
Contoh: suhu 35oC lebih ncepat beraksi dari pada suhu 25oC. Nilai peningkatan laju reaksi dapat dihitung dengan menggunakan rumus berikut:
Vt= ( )
XVo