PENGEMBANGAN METODE ANALISIS
SENYAWA MARKER SPESIFIK
PIPER RETROFRACTUM
VAHL
DAN
PIPER NIGRUM
L
.
DALAM CAMPURAN
MENGGUNAKAN KLT-DENSITOMETRI DAN
VISUALIZER
M. REZKI DWITYA
FAKULTAS FARMASI UNIVERSITAS AIRLANGGA
DEPARTEMEN FARMAKOGNOSI DAN FITOKIMIA
SURABAYA
2014
PENGEMBANGAN METODE ANALISIS
SENYAWA MARKER SPESIFIK
PIPER RETROFRACTUM
VAHL
DAN
PIPER NIGRUM
L
.
DALAM CAMPURAN
MENGGUNAKAN KLT-DENSITOMETRI DAN
VISUALIZER
M. REZKI DWITYA
050911289
FAKULTAS FARMASI UNIVERSITAS AIRLANGGA
DEPARTEMEN KIMIA FARMASI
SURABAYA
2014
PUBLIKASI KARYA ILMIAH
Demi perkembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya, dengan judul :
PENGEMBANGAN METODE ANALISIS
SENYAWA MARKER SPESIFIK PIPER RETROFRACTUM VAHL DAN PIPER NIGRUM L. DALAM CAMPURAN MENGGUNAKAN
KLT-DENSITOMETRI DAN VISUALIZER
Untuk dipublikasikan atau ditampilkan di internet atau media yang lain yaitu Digital Library Perpustakaan Universitas Airlangga untuk kepentingan akademik sebatas sesuai dengan Undang – Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi karya ilmiah ini saya buat dengan sebenarnya.
Surabaya, September 2014
M. Rezki Dwitya
NIM. 050911289
Saya yang bertanda tangan dibawah ini,
Nama : M. Rezki Dwitya
NIM : 050911289
Fakultas : Farmasi
menyatakan dengan sesungguhnya bahwa hasil tugas akhir yang saya tulis dengan judul:
PENGEMBANGAN METODE ANALISIS
SENYAWA MARKER SPESIFIK PIPER RETROFRACTUM VAHL DAN PIPER NIGRUM L. DALAM CAMPURAN MENGGUNAKAN
KLT-DENSITOMETRI DAN VISUALIZER
adalah benar – benar merupakan hasil karya sendiri. Apabila di kemudian hari diketahui bahwa skripsi ini menggunakan data fiktif atau merupakan hasil dari plagiarisme, maka saya bersedia menerima sanksi berupa pembatalan kelulusan dan atau pencabutan gelar yang saya peroleh.
Demikian surat ini saya buat untuk dipergunakan sebagaimana mestinya.
Surabaya, September 2014
M. Rezki Dwitya
NIM. 050911289
PENGEMBANGAN METODE ANALISIS
SENYAWA MARKER SPESIFIK PIPER RETROFRACTUM VAHL DAN PIPER NIGRUM L. DALAM CAMPURAN MENGGUNAKAN
KLT-DENSITOMETRI DAN VISUALIZER
SKRIPSI
Dibuat Untuk Memenuhi
Syarat Mencapai Gelar Sarjana Farmasi Pada
Fakultas Farmasi Universitas Airlangga
Surabaya
2014
Oleh :
M. REZKI DWITYA
NIM : 0510911289
Skripsi ini telah disetujui oleh :
Pembimbing Utama Pembimbing Serta
Dr. Idha Kusumawati, S.Si., M.Si., Apt. Prof. Dr. Gunawan Indrayanto, Apt.
NIP. 197004081995122001 NIP. 194707031976031001
vii
Segala puji dan syukur saya panjatkan kehadirat Allah SWT. atas segala berkat dan rahmat-Nya, sehingga saya dapat menyelesaikan skripsi yang berjudul “PENGEMBANGAN METODE ANALISIS SENYAWA
MARKER SPESIFIK PIPER RETROFRACTUM VAHL. DAN PIPER
NIGRUM L. DALAM CAMPURAN DENGAN MENGGUNAKAN KLT – DENSITOMETRI DAN VISUALIZER” ini dengan baik.
Dalam menyusun skripsi ini tidak lepas dari bantuan berbagai pihak baik moril maupun materiil. Oleh karena itu pada kesempatan ini perkenankanlah saya menyampaikan rasa terima kasih yang sedalam-dalamnya kepada:
1. Ibu Dr. Idha Kusumawati, S.Si., M.Si., Apt. selaku pembimbing
utama yang berkenan meluangkan waktunya untuk membimbing saya dengan penuh kesabaran dan keikhlasan, serta memberi semangat kepada saya sehingga skripsi ini dapat diselesaikan dengan baik.
2. Bapak Prof. Dr. Gunawan Indrayanto, Apt.selaku pembimbing serta
yang berkenan meluangkan waktunya untuk membimbing saya dengan penuh kesabaran dan keikhlasan, serta memberi semangat kepada saya sehingga skripsi ini dapat diselesaikan dengan baik.
3. Bapak Drs. Abdul Rahman, M.Si., Apt. selaku penguji yang
memberikan saran serta masukan yang membangun untuk skripsi yang saya kerjakan.
viii
memberikan saran serta masukan yang membangun untuk skripsi yang saya kerjakan.
5. Dekan Fakultas Farmasi Universitas Airlangga Dr. Umi Athiyah,
MS., Apt yang telah memberikan kesempatan kepada saya untuk mengikuti pendidikan program sarjana di Fakultas Farmasi Universitas Airlangga.
6. Mama, papa, kakak, adik dan seluruh keluarga saya yang dengan
penuh kesabaran selalu mendoakan, memberikan semangat serta dukungan dalam berbagai hal sehingga saya dapat menyelesaikan skripsi ini dengan baik.
7. Whina Puti Rum Kirana Banse yang selalu mendukung, memberi
saran dan memberi semangat, sehingga saya dapat menyelesaikan skripsi ini dengan baik.
8. Teman-teman seperjuangan anak bimbing Bu Idha: Rizki, Subhan,
Lendra, Imam, Vrian, Rohman, Faris, Mas Aji, Mas Tito, Mbak Icha.
9. Teman-teman angkatan 2009, 2010 dan semua pihak yang tidak
dapat saya sebutkan satu-persatu yang telah membantu baik langsung maupun tidak langsung dalam menyelesaikan skripsi ini.
ix
Fakultas Farmasi Universitas Airlangga dengan harapan semoga bermanfaat bagi kita semua.
Surabaya, September 2014
Penyusun,
M. Rezki Dwitya
x
PENGEMBANGAN METODE ANALISIS
SENYAWA MARKER SPESIFIK PIPER RETROFRACTUM VAHL.
DAN PIPER NIGRUM L. DALAM CAMPURAN DENGAN MENGGUNAKAN KLT – DENSITOMETRI DAN VISUALIZER
M. Rezki Dwitya
Kontrol kualitas obat herbal, dalam beberapa kasus, memungkinkan untuk melakukan identifikasi senyawa spesifik, yang biasa disebut senyawa marker yang dapat digunakan untuk membantu pembuatan produk yang konsisten. Senyawa marker adalah senyawa atau golongan senyawa yang dapat digunakan untuk mengontrol konsistensi tiap batch produk jadi tanpa harus mengetahui adanya aktifitas atau tidak senyawa tersebut.
Senyawa marker diklasifikasikan menjadi dua, yang pertama adalah senyawa marker aktif, yaitu senyawa atau golongan senyawa yang diketahui secara umum mempunyai kontribusi dalam aktifitas terapetik. Yang kedua adalah senyawa marker analisis yaitu senyawa atau golongan senyawa yang digunakan untuk tujuan analisis tanpa perlu mengetahui adanya kontribusi aktifitas terapetik atau tidak (Natural Health Product Directorate’s Canada, 2012).
Untuk evaluasi gel polyherbal yang mengandung Terminalia
arjuna, Centella asiatica dan Curcuma longa, dilakukan identifikasi
senyawa marker setiap tanaman pada gel tersebut. Untuk Curcuma longa,
digunakan standard reference curcumin sebagai senyawa marker, yang kita
ketahui bahwa curcumin merupakan main component didalam tanaman
tersebut (Patel et al., 2011).
Prasaplai merupakan salah satu produk obat herbal tradisional di Thailand yang mengandung empat tanaman yang berada pada dua genus
yang sama, yaitu Piper retrofractum Blume dan P. nigrum L., serta
Zingiber cassumunar Roxb. dan Z. officinale Roscoe. Sehingga untuk melakukan identifikasi senyawa spesifik tanaman yang berada pada genus yang sama, tidak bisa dilakukan mengunakan senyawa utama / senyawa
xi
berdasarkan senyawa marker karakteristik / senyawa marker spesifik
menggunakan instrumen KLT-Densitometri dan Visualizer.
Dengan demikian, tujuan dari penelitian ini adalah Mendapatkan metode analisis yang valid untuk penentuan senyawa marker pada formula
campuran menggunakan KLT-Densitometri dan Visualizer.
Konsentrasi sampel yang digunakan adalah 10.000 ppm dan jumlah larutan yang akan ditotolkan pada plat KLT adalah 35,0 µL. Sedangkan fase gerak yang terpilih adalah n-Heksan, kloroforom (0.5:3.5). Kondisi ini dapat menampakkan senyawa marker spesifik dari tiap tanaman dan memiliki pemisahan yang baik antara senyawa marker spesifik dan senyawa lainnya. Dari hasil eluasi dengan fase gerak terpilih tersebut, senyawa marker spesifik merica hitam memiliki resolusi 0,84, sedangkan senyawa marker spesifik cabe jawa memiliki resolusi 3,60.
Pada penelitian ini, ditentukan senyawa marker spesifik merica hitam berada pada Rf 0,09, sedangkan senyawa marker spesifik pada cabe
jawa berada pada Rf 0,52. Dari hasil scanning profil spektra, diketahui
panjang gelombang maksimum senyawa marker spesifik tanaman merica hitam dan cabe jawa berada pada 340 nm. Selanjutnya, untuk analisis kuantitatif akan dilakukan scanning senyawa marker spesifik masing-masing tanaman pada panjang gelombang tersebut.
Validasi metode analisis merupakan persyaratan utama untuk membuktikan kehandalan dan kesesuaian suatu metode untuk digunakan (Renger, 2006). Pada penelitian ini, validasi yang dilakukan meliputi : Uji stabilitas, presisi, batas deteksi dan batas kuantifikasi, peak identity dan
peak purity, linearitas dan akurasi.
Berdasarkan penelitian yang telah dilakukan, diperoleh kesimpulan yaitu : Dengan menggunakan KLT-Densitometri, dapat diperoleh metode
analisis yang valid untuk menentukan senyawa marker spesifik Piper
retrofractum Vahl.dan Piper nigrum L. dengan nilai %KV pada tanaman merica hitam adalah 1,12 – 3,96%, untuk cabe jawa adalah 1,12 – 3,91%. Nilai r dari senyawa marker spesifik merica hitam adalah 0,99869 dan untuk senyawa marker speisifk cabe jawa adalah 0,99921. Kemudian %akurasi yang didapatkan untuk tanaman merica hitam adalah 103,87 – 110,80% sedangkan untuk tanaman cabe jawa adalah 102,92 – 106,50%.
xii
Analytical Method Development Specific Marker Compounds
Piper retrofractum Vahl. and Piper nigrum L. in mixture using TLC - Densitometry and Visualizer
M. Rezki Dwitya
Piper retrofractum Vahl. and Piper nigrum L. are two plants that are in the same genus, which is often used in an herbal remedy. To detect or identify the plants that are in the same genus in a herbal medicine formula, required specific markers that could indicate the existence in a formula. This study aims to obtain a valid analytical method for the determination of specific markers in the mix formula using TLC - densitometry and Visualizer. Concentration of the sample used was 10,000 ppm and application volume injected on TLC plates was 35.0 μL. While the selected mobile phase is
n-Hexane, Kloroforom (0.5: 3.5). Specific markers of Piper nigrum L. Rf
values was found to be 0.09, and for specific markers of Piper
retrofractum Vahl. was 0.52. The method was found to be precise, specific and accurate and can also be used for identitify both two plants of piper in the one mixture or formulation.
Keywords: analytical method development, method validation, compound specific markers, identification, Piper retrofractum Vahl., Piper nigrum L, thin layer chromatography, densitometry.
xiii
Halaman LEMBAR PERSETUJUAN PUBLIKASI KARYA ILMIAH
LEMBAR PERNYATAAN BUKAN HASIL PLAGIARISME
LEMBAR PENGESAHAN 1.1 Latar Belakang Masalah... 1
1.2 Rumusan Masalah... 5
1.3 Tujuan Penelitian... 5
1.4 Manfaat Penelitian... 5
BAB II. TINJAUAN PUSTAKA 2.1 Tinjauan tentang Tanaman Piper retrofractum Vahl... 6
2.1.1 Klasifikasi tanaman... 6
2.1.2 Penyebaran dan tempat tumbuh... 7
2.1.3 Nama daerah... 7
2.1.4 Kandungan tanaman... 8
2.2 Tinjauan tentang Tanaman Piper nigrum L... 9
2.2.1 Klasifikasi tanaman... 9
2.2.2 Penyebaran dan tempat tumbuh... 10
xiv
2.2.4 Kandungan tanaman... 12
2.2.4 Manfaat cabe jawa dan merica hitam... 12
2.3 Tinjauan Umum Kromatografi Lapis Tipis (KLT)... 13
2.3.1 Definisi KLT... 13
2.3.2 Keuntungan metode KLT... 13
2.3.3 Prinsip pemisahan pada KLT... 14
2.3.4 Metode deteksi pada KLT... 15
2.4 Tinjauan Umum Densitometri... 17
2.5 Tinjauan Ekstraksi dengan Microwave... 17
2.6 Validasi Metode... 18
2.6.1 Uji Stabilitas... 18
2.6.2 Presisi... 18
2.6.3 Peak identity dan peak purity... 19
2.6.4 Batas deteksi dan batas kuantitasi... 19
2.6.5 Linearitas... 20
2.6.6 Akurasi... 21
BAB III. KERANGKA KONSEPTUAL 3.1 Uraian Kerangka Konseptual... 22
3.2 Kerangka Konseptual... 25
3.3 Hipotesis... 26
BAB IV. METODE PENELITIAN 4.1 Bahan dan Alat Penelitian... 27
4.1.1 Bahan tanaman... 27
4.1.2 Bahan kimia dan bahan lain... 27
4.1.3 Alat-alat... 28
xv
4.2.1 Pembuatan serbuk simplisia... 21
4.2.2 Penentuan kadar air serbuk simplisia... 21
4.2.3 Pembuatan formula campuran... 21
4.2.4 Preparasi sampel... 21
4.2.5 Optimasi kondisi... 21
4.2.6 Penentuan senyawa marker spesifik... 21
4.2.7 Validasi metode... 21
4.2.7.1 Stabilitas... 12
4.2.7.2 Presisi... 12
4.2.7.3 Peak purity dan peak identity... 12
4.2.7.4 Batas deteksi dan batas kuantitasi... 12
4.2.7.5 Linearitas... 12
4.2.7.6 Akurasi... 12
4.3 Skema Metode Penelitian... 22
BAB V. Hasil Penelitian 5.1 Penentuan Kadar Air... 27
5.2 Optimasi Kondisi... 27
5.3 Penentuan Senyawa Marker Spesifik... 27
5.4 Hasil Validasi Metode... 27
5.4.1 Uji Stabilitias... 21
5.4.2 Presisi... 21
5.4.3 Peak purity dan peak identity... 21
5.4.4 Batas deteksi dan batas kuantitasi... 21
5.4.5 Linearitas... 21
5.4.6 Akurasi... 21
xvi
BAB VII KESIMPULAN DAN SARAN... 80 DAFTAR PUSTAKA... 82
xvii
Tabel halaman
IV.1 Spesifikasi tanaman yang diperoleh……….27 IV.2 Komposisi tanaman untuk pembuatan formula campuran………...29 IV.3 Preparasi pembuatan kurva kalibrasi masing-masing tanaman……33 V.1 % Kadar air pada serbuk simplisia merica hitam dan cabe jawa….36 V.2 Rf senyawa marker spesifik dari tiap tanaman……….39 V.3 Rasio area senyawa marker spesifik pada tiap formula campuran...43 V.4 %KV rasio area masing-masing senyawa marker spesifik pada
tiap formula (n=3)………....43
V.5 Peak purity senyawa marker spesifik merica hitam………...44
V.6 Peak purity senyawa marker spesifik cabe jawa………..44
V.7 Batas deteksi dan batas kuantitasi pada merica hitam………….….47
V.8 Batas deteksi dan batas kuantitasi pada cabe jawa………...47
V.9 Linearitas senyawa marker spesifik merica hitam………….……...48
V.10 Linearitas senyawa marker spesifik cabe jawa……….49 V.11 Homogenity test konsentrasi terendah dan tertinggi yang
digunakan untuk kurva kalibrasi pada sampel merica hitam………50 V.12 Homogenity test konsentrasi terendah dan tertinggi yang
digunakan untuk kurva kalibrasi pada sampel cabe jawa………....51 V.13 Akurasi kadar merica hitam pada tiap formula ( n = 3 )…………..52 V.14 Akurasi kadar cabe jawa pada tiap formula ( n = 3 )…………...53
xviii
DAFTAR GAMBAR
Gambar halaman
2.1 Piper retrofractum Vahl………...6
2.1 Piper nigrum L………..………...9
3.1 Skematik kerangka konseptual………...25
4.1 Skematik arah eluasi uji stabilitas pada plat KLT………...31
4.2 Skematik peak purity...32
4.3 Skematik metode penelitian………...35
5.1 Hasil visualisasi sampel merica hitam, formula campuran, cabe jawa pada 366 nm menggunakan CAMAG TLC – Visualizer…………...37
5.2 Kromatogram masing-masing tanaman dan formula campuran pada 366 nm………38
5.3 Hasil visualisasi uji stabilitas dalam pelarut pada 366 nm………….40
5.4 Kromatogram uji stabilitas dalam pelarut pada 366 nm…….……...41
5.5 Hasil visualisasi uji stabilitas pada 366 nm selama 2 jam…………..42
5.6 Hasil visualisasi uji stabilitas pada 366 nm selama 3 jam…………..42
5.7 Peak identity senyawa marker spesifik merica hitam………45
5.8 Peak identity senyawa marker spesifik cabe jawa...45
5.9 Kurva kalibrasi merica hitam………...48
5.10 Kurva kalibrasi cabe jawa………..49
1
PENDAHULUAN
1.1 Latar Belakang
Dalam beberapa tahun terakhir, produk bahan alam semakin
sering digunakan sebagai produk obat-obatan, nutraceuticals dan juga
kosmetik. Sekitar 80% dari populasi manusia di dunia, masih menggunakan tanaman obat dan obat tradisional lainnya untuk kebutuhan utama dalam menjaga kesehatan mereka. Berdasarkan definisi WHO, ada tiga macam pengobatan herbal: simplisia, ekstrak, dan produk jadi. Pengobatan herbal telah meningkat tajam sejalan dengan tren global dari
masyarakat dunia yang “back to nature”. Produk herbal kini dijual dalam
bentuk tablet, kapsul, serbuk, teh, ekstrak dan tanaman segar atau kering. Hal ini menyebabkan kekhawatiran karena semakin banyaknya orang yang mengkonsumsi obat herbal tanpa menggunakan resep. Selain itu, beberapa obat herbal juga dapat menyebabkan masalah kesehatan apabila pemakaiannya tidak tepat. Beberapa obat herbal juga dianggap tidak efektif dan dapat berinteraksi dengan obat lain (Sekhon, 2011).
Obat herbal, baik single herbal maupun poly herbal, mengandung banyak senyawa dalam matriks yang kompleks dimana tidak ada senyawa aktif tunggal yang bertanggung jawab atas efektifitas obat secara
keseluruhan (Ip et al., 2010). Kuantitas dan kualitas keamanan dan
efektifitasnya jauh dari cukup untuk memenuhi kriteria yang dibutuhkan dalam penggunaannya secara luas. Alasan utamanya adalah kurangnya metodologi penelitian yang dapat diterima untuk evaluasi obat tradisional (Liang et al., 2004). Selalu ada kekhawatiran tentang komposisi yang tidak
konsisten dari obat-obatan herbal dan sering terjadi intoksikasi oleh
adulterant dan / atau komponen beracun. Kontrol kualitas obat herbal bertujuan untuk memastikan konsistensi, keamanan dan efektifitasnya (Li
et al., 2008).
Ada kesulitan yang besar dalam menetapkan metode untuk kontrol kualitas yang disebabkan oleh kompleksitas dari obat herbal. Teknik untuk membuktikan keaslian bahan, tidak cukup kuat untuk mengidentifikasi semua bahan yang terkandung dalam produk. Berdasarkan hal tersebut,
semakin banyak bermunculan “adulteration” dan obat dengan kualitas
rendah (Yongyu et al., 2011).
Obat herbal dengan kandungan senyawa multikomponen (multiple
compund) berbeda dengan obat sintesis atau obat yang hanya terdiri dari
satu komponen (single compund). Obat herbal memiliki banyak komponen
kimia yang terkandung didalamnya, seperti komponen yang mempunyai aktivitas terapetik, komponen yang tidak mempunyai aktivitas, komponen
kimia yang belum teridentifikasi, dsb. Sehingga untuk menerapkan current
Good Manufacturing Practices (cGMP) pada obat herbal multikomponen lebih sulit (Lazarowych, 1998).
Identifikasi dan uji kualitas bahan baku tanaman merupakan syarat penting yang harus dilakukan oleh industri ketika berurusan dengan obat herbal. Dan perlu diperhitungkan pula bahwa tanaman yang akan diuji memiliki komposisi yang kompleks dan tidak konsisten berdasarkan kandungan metabolit sekundernya. Oleh karena itu, batas analitis tidak setepat saat kita berurusan dengan senyawa kimia tunggal. Hal ini adalah fakta yang dapat diterima bahwa analisis kualitatif dan kuantitatif senyawa kimia dari tanaman merupakan bagian penting dan dapat diandalkan dari
uji kontrol kualitas (Mukherjee et al., 2007). Evaluasi fitokimia adalah
salah satu cara untuk menilai kualitas obat herbal, meliputi screening
fitokimia, chemoprofiling, dan analisis senyawa marker menggunakan
teknik analisis modern. Kromatografi lapis tipis (KLT) banyak digunakan sebagai metode analisis cepat dan sederhana untuk berbagai bahan kimia
organik seperti obat-obatan, produk bahan alam dan biomolekul (Kim et
al., 2010).
Kontrol kualitas obat herbal, dalam beberapa kasus, memungkinkan untuk melakukan identifikasi senyawa spesifik, yang biasa disebut senyawa marker yang dapat digunakan untuk membantu pembuatan produk yang konsisten. Senyawa marker adalah senyawa atau golongan senyawa yang dapat digunakan untuk mengontrol konsistensi tiap batch produk jadi tanpa harus mengetahui adanya aktifitas atau tidak senyawa tersebut.
Senyawa marker diklasifikasikan menjadi dua, yang pertama adalah senyawa marker aktif, yaitu senyawa atau golongan senyawa yang diketahui secara umum mempunyai kontribusi dalam aktifitas terapetik. Yang kedua adalah senyawa marker analisis yaitu senyawa atau golongan senyawa yang digunakan untuk tujuan analisis tanpa perlu mengetahui adanya kontribusi aktifitas terapetik atau tidak (Natural Health Product Directorate’s Canada, 2012). Karena hanya sejumlah kecil senyawa kimia yang terbukti memiliki aktifitas farmakologis yang jelas, sehingga senyawa kimia lainnya juga dapat digunakan sebagai marker. Senyawa marker dapat menjadi indikator kualitas obat herbal (Li et al., 2008).
Pada jurnal yang di tulis oleh Li (2008), dikatakan bahwa terdapat delapan kategori senyawa yang bisa dikatakan senyawa marker dalam uji
kontrol kualitas obat herbal, yaitu therapeutic components, bioactive components, synergistic components, characteristic components, main
components, correlative components, toxic components, and general
components (Li et al., 2008).
Pada penelitian Patel (2011) Untuk evaluasi gel polyherbal yang
mengandung Terminalia arjuna, Centella asiatica dan Curcuma longa,
dilakukan identifikasi senyawa marker setiap tanaman pada gel tersebut.
Untuk Curcuma longa, digunakan standard reference curcumin sebagai
senyawa marker, yang kita ketahui bahwa curcumin merupakan main
component didalam tanaman tersebut (Patel et al., 2011).
Prasaplai merupakan salah satu produk obat herbal tradisional di
Thailand yang berkhasiat untuk mengurangi dysmenorrhea dan mengatur
siklus mesntruasi. Obat ini mengandung sepuluh bahan tanaman mentah, yaitu Acorus calamus L., Allium sativum L., Citrus hystrix DC., Curcuma zedoaria Roscoe., Eleutherine palmifolia (L.) Merr., Nigella sativa L.,
Piper retrofractum Blume, P. nigrum L., Zingiber cassumunar Roxb. dan
Z. officinale Roscoe (Gritsanapan and Tangyuenyongwatana, 2009). Dari formula tersebut, terkandung empat tanaman yang berada pada dua genus
yang sama, yaitu Piper retrofractum Blume dan P. nigrum L., serta
Zingiber cassumunar Roxb. dan Z. officinale Roscoe. Sehingga untuk melakukan identifikasi senyawa spesifik tanaman yang berada pada genus yang sama, tidak bisa dilakukan mengunakan senyawa utama / senyawa mayor nya. Oleh karena itu, pada penelitian ini akan dilakukan identifikasi
tanaman Piper retrofractum Blume dan P. nigrum L. pada campuran nya
berdasarkan senyawa marker karakteristik / senyawa marker spesifik
menggunakan instrumen KLT-Densitometri dan Visualizer. Keuntungan
menggunakan KLT untuk penentuan senyawa marker spesifik tanaman dalam obat herbal: lebih sederhana, fleksibel, lebih cepat, kepekaan tertentu dan preparasi sampel yang lebih sederhana (Liang et al., 2004).
1.2 Rumusan Masalah
Apakah dapat dikembangan metode analisis yang valid untuk penentuan senyawa marker pada formula campuran menggunakan KLT-Densitometri dan Visualizer?
1.3 Tujuan Penelitian
Mendapatkan metode analisis yang valid untuk penentuan senyawa marker pada formula campuran menggunakan KLT-Densitometri dan Visualizer.
1.4 Manfaat Penelitian
Untuk memberikan data ilmiah mengenai metode analisis yang valid untuk penentuan senyawa marker pada formula campuran dan bisa dimanfaatkan oleh industri untuk uji kontrol kualitas produk herbal.
6
BAB II
TINJAUAN PUSTAKA
2.1 Tinjauan tentang Tanaman Piper retrofractum Vahl.
Gambar 2.1Piper retrofractum Vahl. (Tropicalplantbook)
2.1.1 Klasifikasi tanaman
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivision : Spermatophyta
Division : Magnoliophyta
Class : Magnolipsida
Subclass : Magnoliidae
Order : Piperales
Family : Piperaceae
Genus :Piper L.
Species : Piper retrofractum Vahl
(United States Department of Agriculture, 2014).
2.1.2 Penyebaran dan tempat tumbuh
Cabe jawa memiliki beberapa nama daerah, yaitu: di Sumatera disebut lada panjang, cabai jawa, cabai panjang. Di jawa, namanya cabean, cabe alas, cabe areuy, cabe jawa, cabe sula. Di Madura dinamai cabhi jhamo, cabhi ongghu, cabhi solah, sedangkan di Makassar dikenal dengan nama cabai. Tumbuh di tempat-tempat yang tanahnya tidak lembap dan berpasir seperti di dekat pantai, daerah datar sampai 600 meter di atas permukaan laut (dpl). Tanaman ini dapat tumbuh dan menghasilkan dengan baik di semua jenis lahan kering atau semua jenis tanah di pulau Jawa (Nuraini, 2003).
2.1.3 Nama daerah
Madura : cabhi jhamo, cabhi ongghu, cabhi solah Jawa : cabean, cabe alas, cae areuy
Sumatera : cabai panjang Makasar : cabai
(Nuraini, 2003).
2.1.4 Kandungan tanaman
Senyawa kimia yang terkandung dalam cabe jawa antara lain asam amino bebas, damar, minyak atsiri, beberapa jenis alkaloid seperti piperine, piperidin, piperatin, piperlonguminine, β-sitosterol, sylvatine, guineensine, piperlongumine, filfiline, sitosterol, methyl piperate, minyak atsiri (terpenoid), n-oktanol, linalool, terpinil asetat, sitronelil asetat, sitral, alkaloid, saponin, polifenol, dan resin (kavisin). Alkaloid utama yang terdapat di dalam buah cabe jawa adalah piperin (Isnawati et al., 2002).
Cabe jawa merupakan salah satu tanaman yang diketahui memiliki efek stimulan terhadap sel-sel syaraf sehingga mampu meningkatkan stamina tubuh. Efek hormonal dari tanaman ini dikenal sebagai afrodisiaka. Berdasarkan penelitian secara ilmiah, cabe jawa digunakan sebagai afrodisiaka karena mempunyai efek androgenik, untuk anabolik, dan sebagai antivirus. Dari suatu tinjauan pustaka dikatakan bahwa secara umum kandungan kimia atau senyawa kimia yang berperan sebagai afrodisiak adalah turunan steroid, saponin, alkaloid, tannin dan senyawa lain yang dapat melancarkan peredaran darah. (Nuraini, 2003).
2.2 Tinjauan tentang Tanaman Piper nigrum L.
Gambar 2.2Piper nigrum L. (US Departemen of Agriculture)
2.2.1 Klasifikasi tanaman
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivision : Spermatophyta
Division : Magnoliophyta
Class : Magnolipsida
Subclass : Magnoliidae
Order : Piperales
Family : Piperaceae
Genus :Piper L.
Species : Piper nigrum L.
(United States Department of Agriculture, 2014).
2.2.2 Nama daerah
Sumatera : Koro-koro,lada,lado ketek Madura :Sakang
2.2.3 Penyebaran dan tempat tumbuh
Merica hitam (Piper nigrum) berasal dari pantai barat Ghats, Malabar, India. Lada dibawa oleh para pendatang Hindu ke Pulau Jawa antara tahun 100 SM dan 600 M. Daerah awal pemasukan tanaman lada di Indonesia tidak diketahui dengan jelas, namun diperkirakan bahwa tanaman lada pertama kali ditanam di daerah Karesidenan Banten (Wahid, 1996).
Penyebaran tanaman lada dari daerah Banten mula-mula mengarah ke timur Pulau Jawa. Di daerah Banten, Jakarta, Cirebon, Jepara, Surakarta dan Yogyakarta, lada pada mulanya diusahakan dalam bentuk perkebunan sampai dengan abad ke-18. Bersamaan dengan itu pengusahaannya dalam
bentuk perkebunan rakyat dimulai di Sumatera (Aceh, Bengkulu, Bangka, Lampung,Sumatera Barat, Sumatera Timur, dan Jambi) serta ke Kalimantan (Pontianak,Banjarmasin, dan Pangkalan Bun di Kalimantan Tengah) (Wahid 1996).
Daerah pengembangan lada saat ini adalah Lampung yang terkenal dengan lada hitamnya (Lampong black pepper), dan Bangka yang lebih dikenal dengan lada putihnya (Muntok white pepper). Selain itu, banyak pengembangan pertanaman lada baru di Kalimantan Barat, Kalimantan Tengah dan Kalimantan Timur, serta Sulawesi Selatan dan Sulawesi Tenggara (Manohara et al, 2005).
Merica hitam merupakan tanaman memanjat dari keluarga Piperaceae yang dalam pertumbuhannya dipengaruhi oleh faktor lingkungan. Batang tanaman lada berbuku-buku dan berbentuk sulur. Sulur panjat tumbuh lebih baik dalam keadaan nisbi udara kurang cahaya (fototrof negatif) sedangkan sulur buah dalam keadaan cukup cahaya (fototrof positif). Intensitas cahaya yang dibutuhkan berkisar dari 50% sampai 75%. Lada dapat tumbuh dengan baik di daerah dengan ketinggian 0-500 m dpl. Curah hujan yang paling baik untuk tanaman lada adalah 2000 - 3000mm/tahun dengan hari hujan 110-170 hari,dan musim kemarau 2-3 bulan/tahun. Kelembapan nisbi udara yang sesuai dari 70% sampai
90% dengan kisaran suhu 25-350C. Tanaman lada dapat tumbuh pada
semua jenis tanah, terutama tanah berpasir dan gembur dengan unsur hara yang cukup. Tingkat kemasaman tanah (pH) yang sesuai berkisar 5-6.5. Penggunaan tiang panjat hidup (tajar) dalam budi daya lada akan membantu mengurangi intensitas cahaya yang berlebihan dan akan membuat tanaman berumur lebih panjang karena tanaman tidak didorong
berproduksi lebih sementara input yang diberikan terbatas. Penanaman tanaman penutup tanah akan mengurangi cekaman kekeringan akibat
kemarau dan menghambat penyebaran Phytophthora capsici selama musim
hujan. Pembuatan saluran drainase yang cukup dan terasering yang disesuaikan dengan kondisi lahan diperlukan untuk menghindari genangan air selama musim hujan (Wahyuno, 2009).
2.2.4 Kandungan tanaman
Senyawa kimia yang terkandung dalam tanaman Piper nigrum
antara lain 1,8-Cineol, Acetophenone, Alpha-Pinene, Alpha-Terpineol,
Ascorbic-Acid Borneol, Caff eic-Acid, Camphor, Carvone, Caryophyllene, Citral, Citronellal, Citronellol, Eugeno, Eugenol-Methyl-Ether, Gaba, Geranyl-Acetate, Hyperoside, Limonene, Linalool, Linalyl-Acetate, Magnesium, Methyl-Eugenol, Myrcene, Myristicin, Niacin, P-Cymene, Perillaldehyde, Piperidine, Piperine, Quercetin, Quercitrin, Safrole, Stigmasterol, Thiamin, Tocopherol, Zinc (Anonim, 2009).
2.2.5 Manfaat cabe jawa dan merica hitam
Buah, daun dan akar tanaman Cabe Jawa dapat digunakan untuk pengobatan. Buah yang sudah tua dapat digunakan untuk pengobatan perut kembung, mulas, muntah-muntah, diaforetik, karminatif, merangsang nafsu makan, demam, influenza, migren, peluruh keringat, encok, infeksi pada hati, tekanan darah rendah, urat saraf lemah, sukar bersalin, dan sebagai afrodisiaka. Akar dapat digunakan untuk sakit gigi, luka, dan kejang, sedangkan daunnya untuk obat kumur. Di India, Afrika Utara, Afrika
Timur, dan Asia Tenggara, Cabe Jawa juga digunakan untuk bumbu masak.
2.3 Tinjauan Umum Kromatografi Lapis Tipis (KLT)
2.3.1 Definisi KLT
KLT adalah metode yang baik untuk memisahkan campuran senyawa yang berbeda polaritas nya (Gabriela, 2010). KLT merupakan metode kromatografi cair dimana sampel diberikan berbentuk spot kecil atau garis pada plat penyerap pada kaca, plastik atau plat logam. Fase gerak migrasi melalui fase diam melalui lubang kapiler, kadang dibantu oleh gravitasi tekanan. Fase gerak pada metode KLT dapat terdiri dari pelarut tunggal atau campuran pelarut organik. Saat ini, telah banyak penyerap yang dapat digunakan antara lain silika gel, selulosa, alumina, poliamida, penukar ion dan ikatan kimia yang dilapisi pada kaca atau polyester atau lembaran aluminium (Fried dan Sherma, 1999). KLT juga dapat
dikembangkan menjadi fingerprinting kromatografi yang digunakan untuk
identifikasi (Gabriela, 2010; Wagner et al., 1996) dan kontrol kualitas
ekstrak tanaman (Liang et al., 2004).
2.3.2 Keuntungan metode KLT
Keuntungan menggunakan KLT sebagai penentuan senyawa marker spesifik tanaman pada obat herbal : lebih sederhana, fleksibel, lebih cepat, kepekaan tertentu, dan preparasi sampel yang lebih sederhana (Liang
et aL., 2004).
2.3.3 Prinsip pemisahan pada KLT
Pemisahan senyawa pada kromatografi dipengaruhi oleh kombinasi sifat kinetik dan termodinamik. Sifat termodinamik bertanggung jawab atas nilai retensi dan selektifitas. Sedangkan sifat kinetik menentukan pelebaran zona selama pemisahan (Spangenberg, 2011; Poole, 1992).
Pada saat pemisahan campuran komponen, setiap senyawa terdistribusi dan berinteraksi pada kedua fase, yakni fase diam dan fase gerak. Interaksi komponen senyawa dengan kedua fase meliputi dua mekanisme yakni adsorpsi dan partisi (Spangenberg, 2011).
Adsorpsi merupakan fenomena permukaan. Adsorpsi pada KLT terjadi pada permukaan partikel fase diam yang kontak dengan fase gerak.
Dalam mekanisme adsorpsi dapat terjadi ikatan van der waal’s interaksi
dipol-dipol dan interaksi ion komplek seperti ikatan hidrogen. Penerapan pemisahan pada kromatografi, mekanisme adsorpsi harus bersifar
reversible dan hanya interaksi fisika. Sedangkan, pada kromatografi partisi, pemisahan tergantung pada kelarutan senyawa pada dua eluen yang tidak saling larut (Spangenberg, 2011).
Parameter yang digunakan untuk menunjukkan letak noda adalah
Rf, didapatkan dari rasio perbandingan :
Harga Rf mulai dari 0 (solut berada di titik penotolan) sampai
0,999 (solute berada digaris akhir fase gerak).
2.3.4 Metode deteksi pada KLT ( Wall, 2005) 1. Teknik non-destructive
a.Deteksi visible
Deteksi ini digunakan untuk senyawa yang mempunyai warna, misalnya pewarna alami dan sintesis dan senyawa nitrofenol. b. Deteksi UV
Dalam membantu metode deteksi ini, plat mengandung indikator senyawa inorganik fosforesensi atau indikator senyawa organik fluoresensi. Proses fluoresensi diakibatkan gelombang elektromagnetik yang memancarkan energi yang dibawa transisi elektron dari ground state yang eksitasi singlet state. Eksitasi
elektron kembali pada ground state mengemisikan energi pada
panjang gelombang visible. Fosforesensi memiliki perbedaan
dengan fluoresensi, elektron kembali pada keadaan ground state
melalui keadaan triplet.
2. Reaksi reversible
a. Iodin
Iodin merupakan reagent yang sangat berguna untuk mendeteksi keberadaan berbagai analit organik pada plat.
b. Amonia
Reagen amonia sering digunakan bersama reagen lain untuk
meningkatkan deteksi noda, antara lain bromocresol green dan
bromocresol blue.
3. Reaksi non-reversible
a. Fluoresen
Metode ini digunakan untuk mendeteksi senyawa organik substansial, salah satu reagen yang sering digunakan adalah
fluorescein digunakan untuk mendeteksi Lipid, purin, pyrimidin, barbiturate, senyawa tak jenuh, klorinasi hidrokarbon dan heterosiklik.
b. Indikator pH
Indikator ini hanya digunakan untuk mendeteksi keberadaan senyawa asam dan basa. Reagen yang sering digunakan adalah
sulfonthalein. 4. Teknik destructive
a.Reaksi Charring
Metode reaksi charring biasanya digunakan reagen yang sesuai
kemudian diikuti dengan pemanasan pada temperatur tinggi untuk merusak beberapa senyawa organik.
b. Aktivasi thermochemical
Metode ini membutuhkan pemanasan pada suhu tinggi untuk merubah senyawa agar dapat berfluoresensi pada paparan lampu UV.
5. Derivatisasi
Metode ini menggunakan reagen untuk mereaksikan analit agar noda pada plat dapat terlihat. Metode ini terbagi menjadi dua: analit direaksikan setelah dikromatografi dan direaksikan sebelum dikromatografi.
2.4 Tinjauan Umum Densitometri
Densitometri merupakan metode analisis instrumental yang berdasarkan interaksi radiasi elektromagnetik dengan analit ditentukan adalah absorbs, transmisi, pantulan (refleksi) pendar fluor atau pemadaman pendar fluor dari radiasi semula. Perajah dari densitometri akan mengubah noda yang dibacanya menjadi kromatogram yang terdiri dari deretan puncak. Letak noda sesuai dengan jarak tempuh noda dan tinggi atau luas puncak sebanding dengan kadar analit pada noda yang bersangkutan (Mulya dan Suharman, 1995).
Densitometer dioperasikan dengan sistem optis transmisi dan reflektan. Komponen – komponen yang berwarna yang tidak menyerap sinar ultraviolet dapat dianalisis dengan pantulan absorbs pada panjang gelombang sinar tampak (visible) menggunakan sistem optis reflektan dan transmisi. Komponen – komponen tidak berwarna akan menyerap ultraviolet, dapat dianalisis dengan mengukur absorbansi sinar ultraviolet yang direfleksikan (Touchstone dan Dobbins, 1983)
2.5 Tinjauan Ekstraksi dengan Microwave
Apabila dibandingkan dengan ekstraksi sonikasi, ekstraksi dengan microwave memiliki beberapa kelebihan:
1. Mengurangi penggunaan pelarut
2. Tingkat efisiensi yang lebih tinggi
3. Mengurangi waktu ekstraksi
4. Peningkatan kemampuan analisis seperti: %perolehan kembali dan
keterulangan.
2.6 Validasi Metode
Pengembangan metode analisis memerlukan syarat yang menyatakan bahwa metode yang digunakan untuk analisis harus tervalidasi. Validasi analisis merupakan persyaratan utama untuk membuktikan kehandalan dan kesesuaian suatu metode untuk digunakan (Renger et al, 2006). Pada penelitian ini, validasi yang dilakukan meliputi : Uji stabilitas, presisi, peak identity dan peak purity, batas deteksi dan batas kuantitasi, linearitas dan akurasi.
2.6.1 Uji stabilitas
Untuk memulai membuat prosedur analisis menggunakan KLT tahap terpenting adalah mengecek kestabilan senyawa dalam setiap step prosedur (Renger et al., 2006). Stabilitas yang perlu diuji adalah stabilitas dalam pelarut dan dalam plat KLT. Parameter yang digunakan sebagai uji stabilitas dalam pelarut, apabila tidak ada perbedaan noda pada sampel larutan yang ditotolkan dengan penyimpanan dengan sampel yang baru dilarutkan dan segera ditotolkan. Sedangkan uji stabilitas plat, jika noda yang terbentuk dengan KLT bidimensional membentuk garis longitudinal (Riech et al., 2008).
2.6.2 Presisi
Presisi dibagi menjadi tiga kategori: repeatability, intermediate precision, dan reproducibility. Repeatability ditentukan ketika analisis dilakukan di satu laboratorium oleh satu analis, dengan peralatan kerja
yang sama dan dilakukan dalam satu hari kerja. Intermediate precision
diperoleh ketika analisis dilakukan dalam satu laboratorium yang sama
oleh analis yang berbeda selama beberapa hari atau minggu, dengan
peralatan kerja yang berbeda. Reproducibility diperoleh dari hasil yang
diukur dalam laboratorium yang berbeda dengan tujuan memverifikasi metode, apakah dapat memperoleh hasil yang sama dengan fasilitas yang
berbeda. Kriteria penerimaan (nilai RSD) uji presisi adalah ≤ 2%.
(Indrayanto dan Yuwono, 2005).
2.6.3 Peak identity dan peak purity
Untuk mendeteksi interaksi dari senyawa lain, kemurnian puncak analit harus ditentukan. Konsekuensi dari persyaratan ini adalah bahwa resolusi analit dari komponen lain harus lebih dari 1,5-2,0. Spektrum UV-Vis dari puncak dapat digunakan untuk menentukan kemurnian dari puncak tersebut, dalam hal ini koefisien korelasi “r” (istilah ini digunakan oleh software DAD System Manager Hitachi dan WinCATS dari CAMAG). Jika nilai r adalah 0.0000-0.8900 maka puncak tersebut tidak murni, dan apabila nilai r adalah 0.9000-0.9500 berarti peak tersebut terkontaminasi. Untuk menentukan identitas puncak, maka data seluruh puncak standar dan analit harus dibandingkan, nilai r atau Match Factor dapat dihitung dengan menggunakan perangkat lunak dari KCKT/KLT-Densitometer. (Indrayanto dan Yuwono, 2005).
2.6.4 Batas deteksi dan batas kuantitasi
Batas deteksi didefinisikan sebagai konsentrasi terendah dari sebuah analit yang dapat dideteksi dalam kondisi analisis yang digunakan. Keberadaan analit dapat dilihat pada batas deteksi, namun konsentrasi batas deteksi tidak dapat diukur secara kuantitatif. Batas kuantifikasi adalah
konsentrasi terendah yang bisa ditentukan dengan akurasi yang diterima dan presisi dalam kondisi analisis. Umumnya, batas kuantifikasi dapat diperkirakan sebagai tiga kali lipat batas deteksi. Dengan menggunakan analisis regresi linear pada konsentrasi analit yang relatif rendah dan menghitung nilai Xp, batas deteksi dapat ditentukan sebagai ¼ dari Xp. Disarankan menggunakan 5-10 sampel pada konsentrasi analit yang relatif rendah untuk menentukan Xp dengan cara pengenceran sampai tidak ada respon terdeteksi dari analit tersebut. Dalam hal ini, persyaratan parameter linearitas (Vx0, r, nilai Xp, dll) dari garis regresi harus dipenuhi sebelum batas deteksi dapat diperkirakan dengan menggunakan nilai Xp. (Indrayanto dan Yuwono, 2005).
2.6.5 Linearitas
Penentuan liniearitas dilakukan dengan menggunakan minimal lima macam konsentrasi dimana kelima macam konsentrasi tersebut berkisar antara 80-120% dari kadar analit yang diperkirakan. Sebagai parameter adanya hubungan linear atau tidak digunakan koefisien korelasi r pada analisis regresi linear,
y = bx + a, harga r yang diharapkan lebih besar dari r tabel (Carr, 1990). Parameter yang perlu ditentukan adalah deviasi rata-rata dari garis regresi (Sy), standar deviadi fungsi (Sxo), dan koefisien variasi dari fungsi
(Vxo). Persamaan yang mempunyai nilai Vxo paling kecil dapat dipilih
untuk analisis selanjutnya. Harga Vxo sebaiknya tidak lebih dari 5%. Harga r lebih besar dari r tabel tidak menjamin bahwa kurva linear yang diperoleh
mempunyai harga Vxo yang baik (Indrayanto dan Yuwono, 2005)
Persamaan-persamaan tersebut dapat dihitung dengan
ICH mendefinisikan akurasi prosedur analisis sebagai kedekatan antara nilai sebenarnya yang diketahui dan nilai yang diperoleh. Akurasi juga dapat digambarkan sebagai sejauh mana hasil dari metode yang digunakan dengan nilai sebenarnya yang diketahui. Penilaian akurasi dapat dilakukan dengan beberapa cara. Salah satunya adalah dengan membandingkan hasil dari metode yang dibuat dengan hasil dari metode referensi yang sudah ditetapkan. Pendekatan ini mengasumsikan bahwa ketidakpastian dari metode referensi diketahui. Kedua, akurasi dapat dinilai dengan menganalisis sampel yang sudah diketahui konsentrasi nya (misalnya, sampel kontrol atau material referensi yang terjamin) dan membandingkan nilai yang terukur dengan nilai yang sebenarnya seperti yang terdapat pada material (Huber, 2007).
22 BAB III
KERANGKA KONSEPTUAL
3.1 Uraian kerangka konseptual
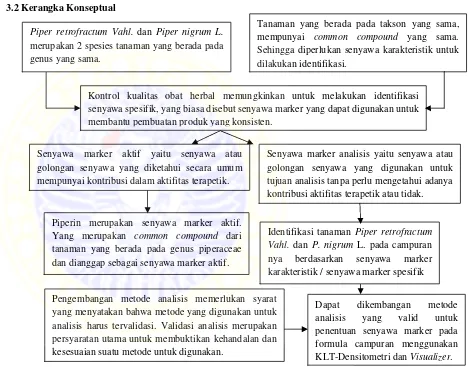
Piper nigrum L. dan Piper retrofractum Vahl. merupakan 2 tanaman yang berada pada genus yang sama yaitu Piperaceae. Spesies piper tersebar luas di wilayah tropis dan subtropis dunia, dan biasanya digunakan sebagai obat dengan berbagai macam cara. Tanaman dengan genus piper, terkenal dalam sistem pengobatan ayuverda di India.
Kontrol kualitas obat herbal, dalam beberapa kasus, memungkinkan untuk melakukan identifikasi senyawa spesifik, yang biasa disebut senyawa marker yang dapat digunakan untuk membantu pembuatan produk yang konsisten. Senyawa marker adalah senyawa atau golongan senyawa yang dapat digunakan untuk mengontrol konsistensi tiap batch produk jadi tanpa harus mengetahui adanya aktifitas atau tidak senyawa tersebut.
Senyawa marker diklasifikasikan menjadi dua, yang pertama adalah senyawa marker aktif, yaitu senyawa atau golongan senyawa yang diketahui secara umum mempunyai kontribusi dalam aktifitas terapetik. Yang kedua adalah senyawa marker analisis yaitu senyawa atau golongan senyawa yang digunakan untuk tujuan analisis tanpa perlu mengetahui adanya kontribusi aktifitas terapetik atau tidak (Natural Health Product Directorate’s Canada, 2012). Karena hanya sejumlah kecil senyawa kimia yang terbukti memiliki aktifitas farmakologis yang jelas, sehingga senyawa kimia lainnya juga dapat digunakan sebagai marker. Senyawa marker dapat menjadi indikator kualitas obat herbal.
Terdapat delapan kategori senyawa yang bisa dikatakan senyawa
marker dalam uji kontrol kualitas obat herbal, yaitu therapeutic
components, bioactive components, synergistic components, characteristic
components, main components, correlative components, toxic components,
and general components (Li et al., 2008).
Pada penelitian Patel (2011) Untuk evaluasi gel polyherbal yang
mengandung Terminalia arjuna, Centella asiatica dan Curcuma longa,
dilakukan identifikasi senyawa marker setiap tanaman pada gel tersebut.
Untuk Curcuma longa, digunakan standard reference curcumin sebagai
senyawa marker, yang kita ketahui bahwa curcumin merupakan main
component didalam tanaman tersebut (Patel et al., 2011).
Piperin adalah salah satu senyawa mayor yang dimiliki oleh beberapa spesies tanaman yang berada pada genus Piperaceae dan merupakan senyawa amida pertama yang diisolasi dari spesies piper. Dari hasil studi farmakologi, dilaporkan bahwa piperin mempunyai aktivitas sebagai depresan sistem saraf pusat, anti piretik, analgesik, dan anti inflamasi (Parmar et al, 1997).
Prasaplai merupakan salah satu produk obat herbal tradisional di
Thailand yang berkhasiat untuk mengurangi dysmenorrhea dan mengatur
siklus mesntruasi. Dari formula tersebut, terkandung empat tanaman yang
berada pada dua genus yang sama, yaitu Piper retrofractum Blume dan P.
nigrum L., serta Zingiber cassumunar Roxb. dan Z. officinale Roscoe. Sehingga untuk melakukan identifikasi senyawa spesifik tanaman yang berada pada genus yang sama, tidak bisa dilakukan mengunakan senyawa utama / senyawa mayor nya.
Oleh karena itu, peneliti melakukan identifikasi tanaman Piper retrofractum Vahl. dan Piper nigrum L. pada campuran nya berdasarkan senyawa marker karakteristik / senyawa marker spesifik menggunakan
instrumen KLT-Densitometri dan Visualizer. Keuntungan menggunakan
KLT untuk penentuan senyawa marker spesifik tanaman dalam obat herbal: lebih sederhana, fleksibel, lebih cepat, kepekaan tertentu dan preparasi sampel yang lebih sederhana (Liang et al., 2004).
Pengembangan metode analisis memerlukan syarat yang menyatakan bahwa metode yang digunakan untuk analisis harus tervalidasi. Validasi analisis merupakan persyaratan utama untuk membuktikan kehandalan dan kesesuaian suatu metode untuk digunakan (Renger, 2006). Pada penelitian ini, validasi yang dilakukan meliputi : Uji stabilitas, presisi, peak identity dan peak purity, batas deteksi dan batas kuantitasi, linearitas dan akurasi.
22
3.2 Kerangka Konseptual 25
Piperin merupakan senyawa marker aktif.
Yang merupakan common compound dari
tanaman yang berada pada genus piperaceae dan dianggap sebagai senyawa marker aktif.
Kontrol kualitas obat herbal memungkinkan untuk melakukan identifikasi senyawa spesifik, yang biasa disebut senyawa marker yang dapat digunakan untuk membantu pembuatan produk yang konsisten.
Senyawa marker aktif yaitu senyawa atau golongan senyawa yang diketahui secara umum mempunyai kontribusi dalam aktifitas terapetik.
Senyawa marker analisis yaitu senyawa atau golongan senyawa yang digunakan untuk tujuan analisis tanpa perlu mengetahui adanya kontribusi aktifitas terapetik atau tidak.
Piper retrofractum Vahl. dan Piper nigrum L.
merupakan 2 spesies tanaman yang berada pada genus yang sama.
Identifikasi tanaman Piper retrofractum Vahl. dan P. nigrum L. pada campuran nya berdasarkan senyawa marker karakteristik / senyawa marker spesifik
Pengembangan metode analisis memerlukan syarat yang menyatakan bahwa metode yang digunakan untuk analisis harus tervalidasi. Validasi analisis merupakan persyaratan utama untuk membuktikan kehandalan dan kesesuaian suatu metode untuk digunakan.
Dapat dikembangan metode analisis yang valid untuk penentuan senyawa marker pada formula campuran menggunakan KLT-Densitometri dan Visualizer. Tanaman yang berada pada takson yang sama,
mempunyai common compound yang sama.
Sehingga diperlukan senyawa karakteristik untuk dilakukan identifikasi.
Gambar 3.1 Skematik kerangka konseptual
22 3.3 Hipotesis
Dapat dikembangan metode analisis yang valid untuk penentuan senyawa marker pada formula campuran menggunakan KLT-Densitometri dan Visualizer.
27
BAB IV
METODOLOGI PENELITIAN
4.1 Bahan dan Alat Penelitian
4.1.1 Bahan Tanaman
Bahan yang digunakan dalam penelitian ini adalah buah dari tanaman cabe jawa dan merica hitam. Kedua tanaman tersebut diperoleh dan diidentifikasi dari Balai penelitian tanaman rempah dan obat (Balittro) Bogor.
Tabel IV.1 Spesifikasi buah tanaman yang diperoleh
Tanaman Umur saat
panen
Musim
panen Cara pengeringan
Cabe jawa 4 bulan Kemarau Menggunakan Oven 50
0 C
Merica hitam 6 bulan Kemarau Menggunakan Oven 50
0 C
4.1.2 Bahan kimia dan bahan lain
Bahan kimia yang digunakan untuk penelitian ini adalah n-Heksan p.a (merck), kloroform p.a (malinckorf), Plate TLC Silica Gel GF 254 merck.
4.1.3 Alat-alat
Moisture Analyzer HB43-S Mettler Toledo, Microwave Sharp
R230-R(S), Ayakan No. 13 mm; 2-μm pore; PTFE syringe filter, Linomat
5, Automatic Development Chamber 2, Camag TLC Visualizer, Camag TLC scanner 3, software WinCATS versi 1436336, software VMA solution versi 1.2.0b.
4.2 Metode Penelitian
4.2.1 Pembuatan serbuk simplisia
Buah cabe jawa dan merica hitam dalam kondisi kering. Kedua buah tanaman tersebut kemudian dibuat menjadi serbuk simplisia menggunakan blender. Setelah itu diayak menggunakan ayakan No. 100.
4.2.2 Penentuan kadar air serbuk simplisia
Pengukuran kandungan air yang berada di dalam serbuk simplisia tanaman cabe jawa dan merica hitam. Dengan menimbang 500,0 mg masing-masing serbuk simplisia, kemudian pengukuran menggunakan alat Moisture Analyzer. Simplisia dinilai cukup aman bila mempunyai kadar air kurang dari 10% (Departemen Kesehatan Republik Indonesia, 1985).
4.2.3 Pembuatan Formula Campuran
Tabel IV.2 Komposisi tanaman untuk pembuatan formula campuran
BAHAN TANAMAN F1 F2 F3
Merica Hitam 75% 50% 25%
Cabe Jawa 25% 50% 75%
Membuat 3 formula campuran sebanyak 100,0 gram tiap formulanya. Serbuk simplisia buah cabe jawa dan merica hitam ditimbang sesuai dengan komposisi dari tiap formula campurannya. (Komposisi tanaman untuk pembuatan formula campuran dilihat pada tabel IV.1). Setelah itu, diaduk dan diayak menggunakan ayakan No. 100.
4.2.4 Preparasi Sampel
Serbuk sampel formula campuran ditimbang 50,0 mg, dimasukkan kedalam labu ukur 5 mL, lalu ditambahkan n-Heksan p.a 3,0 mL, diekstraksi menggunakan Microwave. Kemudian dalam labu ukur tersebut
ditambahkan n-Heksan ad 5 mL atau sampai garis tanda. Tiap sampel
disaring dengan menggunakan 13 mm, 2-μm pore, PTFE syringe filter.
4.2.5 Optimasi kondisi
Pada tahap ini dilakukan penentuan fase gerak, penentuan konsentrasi sampel, penentuan jumlah larutan sampel yang ditotolkan dan penentuan panjang gelombang pada analisis menggunakan densitometri. Larutan sampel ditotolkan menggunakan Linomat-5 pada plat KLT silika gel 60 F254. Setelah totolan kering plat dieluasi menggunakan ADC-2.
Noda yang diperoleh diamati di TLC Scanner-3 pada panjang gelombang 254 nm dan 366 nm. Fase gerak yang terpilih adalah fase gerak yang dapat memisahkan peak terpilih dengan peak lain, dengan pemisahan paling baik berdasarkan nilai resolusi > 0,8 serta panjang gelombang sinar UV yang dapat menampakkan senyawa marker spesifik dari masing-masing tanaman.
4.2.6 Penentuan senyawa marker spesifik
Penentuan senyawa marker spesifik dengan memilih salah satu senyawa pada masing-masing tanaman, yang hanya dimiliki tanaman itu saja. Senyawa yang terpilih harus memiliki resolusi > 0,8 dan memiliki
peak purity ≥ 0,9900. Sehingga dengan adanya senyawa marker spesifik didalam formula campuran, dapat menandakan keberadaan tanaman tersebut
4.2.7 Validasi metode
4.2.7.1 Stabilitas
Pertama stabilitas dalam pelarut, sampel pertama adalah formula campuran yang dilarutkan pada 8 jam sebelum penotolan, sampel kedua adalah formula campuran yang dilarutkan satu jam sebelum penotolan, sampel ketiga adalah formula campuran yang dilarutkan segera sebelum penotolan. Ketiga larutan sampel tersebut kemudian ditotolkan sebesar 35,0 µL menggunakan Linomat-5 pada satu plat KLT yang sama. Selanjutnya, dieluasi menggunakan fase gerak terpilih pada ADC-2, noda hasil pemisahan dilihat menggunakan Camag TLC Visualizer.
Kedua, stabilitas dalam plat. Larutan sampel ditotolkan menggunakan Linomat-5 sebesar 35,0 µL pada plat KLT 10x10 cm sebanyak satu kali disalah satu sudut. Kemudian dieluasi menggunakan fase gerak yang terpilih pada ADC-2. Kemudian dilakukan eluasi kedua pada sisi yang tegak lurus pada sisi yang kedua setelah 2 jam dan 3 jam. Setelah eluasi, divisualisasikan menggunakan Camag TLC Visualizer.
Gambar 4.1 Skematik arah eluasi uji stabilitas pada plat KLT
4.2.7.2 Presisi
Ketiga sampel formula campuran ditotolkan menggunakan
Linomat-5 sebanyak 35,0 µl pada plat KLT silika gel 60 F254 10x10 cm. Masing-masing sampel dilakukan replikasi sebanyak 3 kali. Selanjutnya, dieluasi menggunakan fase gerak terpilih dalam ADC-2, kemudian dilakukan analisis menggunakan Camag TLC Scanner-3 dan software WinCATS. Hal ini dilakukan 3 kali di 3 hari yang berbeda dengan komposisi eluen yang sama. Lalu nilai rasio area dari peak senyawa marker spesifik akan dibandingkan dengan peak yang sama tiap replikasinya sehingga diperoleh variabilitas interday dan intraday.
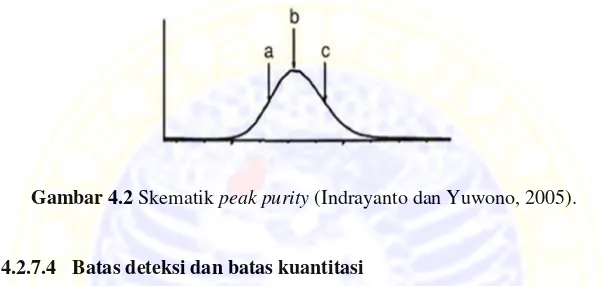
4.2.7.3 Peak purity dan peak identity
Pada tahap ini dilakukan scanning spektra pada masing – masing
peak senyawa marker spesifik pada tiap tanaman. Untuk peak identity
dilakukan dengan mengkorelasikan peak yang digunakan untuk standard
dengan peak yang sama pada track yang berbeda. Sedangkan peak purity
dilakukan dengan mengkorelasikan spektra pada awal peak dengan maksimum peak (r s,m) dan spektra pada maksimum peak dengan spektra pada akhir peak (r m,e). Peak identity dan peak purity diterima apabila memiliki nilai correlation limit > 0,9900.
Gambar 4.2 Skematik peak purity (Indrayanto dan Yuwono, 2005).
4.2.7.4 Batas deteksi dan batas kuantitasi
Untuk menentukan batas deteksi dan batas kuantitasi, masing-masing larutan sampel tanaman tunggal ditotolkan sampai di konsentrasi senyawa marker spesifik tidak tampak. Kemudian diambil 5 tingkat konsentrasi yang akan dilakukan perhitungan regresi linear dengan
menggunakan software VMA Solution. Sehingga akan diketahui batas
deteksi dan batas kuantifikasi dari masing – masing larutan sampel tanaman tunggal.
4.2.7.5 Linearitas
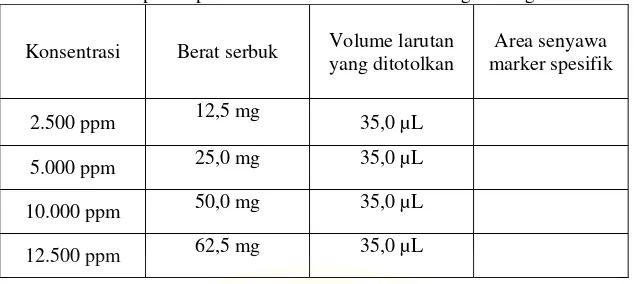
Tabel IV.3 Preparasi pembuatan kurva kalibrasi masing-masing tanaman
Konsentrasi Berat serbuk Volume larutan
yang ditotolkan
Area senyawa marker spesifik
2.500 ppm 12,5 mg 35,0 µL
5.000 ppm 25,0 mg 35,0 µL
10.000 ppm 50,0 mg 35,0 µL
12.500 ppm 62,5 mg 35,0 µL
Serbuk simplisia merica hitam dan cabe jawa ditimbang sebanyak 5 kali dengan berat serbuk yang sesuai pada tabel 4.3. Kemudian masing – masing serbuk yang sudah ditimbang dimasukkan kedalam labu ukur 5 mL, lalu ditambahkan n-Heksan p.a 3,0 mL, diekstraksi menggunakan
Microwave. Kemudian dalam labu ukur tersebut ditambahkan n-Heksan ad
5 mL atau sampai garis tanda. Tiap sampel disaring dengan menggunakan
13 mm, 2-μm pore, PTFE syringe filter. Langkah berikutnya adalah
menotolkan 5 tingkat konsentrasi larutan sampel tersebut pada plat KLT. Kemudian dianalisis menggunakan densitometri pada lambda maksimum masing-masing senyawa marker spesifik. Setelah itu dilakukan perhitungan regresi linear antara area senyawa marker spesifik dengan berat serbuk simplisia.
4.2.7.6 Akurasi
Tiap formula campuran dilakukan penimbangan sebanyak 3 kali seberat 50,0 mg. Kemudian masing-masing dimasukkan kedalam labu ukur 5 mL, lalu ditambahkan n-Heksan p.a 3,0 mL, diekstraksi menggunakan
Microwave. Kemudian dalam labu ukur tersebut ditambahkan n-Heksan ad
5 mL atau sampai garis tanda. Tiap sampel disaring dengan menggunakan 13 mm, 2-μm pore, PTFE syringe filter.
Langkah berikutnya adalah menotolkan tiap larutan sampel formula campuran yang telah dibuat sebanyak 35,0 µL dengan menggunakan Camag-Linomat 5 bersamaan dengan 4 tingkat konsentrasi larutan sampel tanaman tunggal yang digunakan sebagai kurva kalibrasi pada plat KLT ukuran 20 x 10 cm. Kemudian dieluasikan dengan heksan:kloroform (0,5:3,5) menggunakan Camag ADC-2. Lalu setelah eluasi, plat dianalisis menggunakan densitometri pada lambda maksimum dari masing-masing senyawa marker spesifik. Area dari senyawa marker spesifik tiap tanaman pada masing-masing formula akan dimasukkan kedalam persamaan regresi yang didapat dari perhitungan regresi linear antara area senyawa marker spesifik pada tanaman tunggal dengan berat penimbangan masing-masing tingkat konsentrasinya. Selanjutnya dilakukan perbandingan antara berat sebenarnya masing-masing tanaman pada tiap formula dengan berat yang diperoleh dari hasil analisis menggunakan densitometri.
4.3 Skema Metode Penelitian
Gambar 4.3 Skematik metode penelitian Pembuatan serbuk simplisia
masing – masing tanaman
Penentuan kadar air serbuk
simplisia masing – masing tanaman Pembuatan formula campuran
Preparasi sampel
Optimasi Kondisi
Penentuan senyawa marker spesifik
Validasi Metode
Stabilitas, Presisi, Peak identity dan purity, batas deteksi dan kuantitasi, linearitas,
akurasi
F1 : MH 25% CJ 75%
F2 : MH 50% CJ 50%
F3 : MH 75% CJ 25%
36
BAB V
HASIL PENELITIAN
5.1 Penentuan Kadar Air
Sebelum serbuk simplisia masing-masing tanaman dibuat formula campuran, perlu dilakukan uji kadar air. Penentuan kadar air menggunakan
Moisture Analizer. Dari hasil pengamatan ditentukan kadar air pada serbuk simplisia pada masing – masing tanaman :
Tabel V.1 % Kadar air pada serbuk simplisia merica hitam dan cabe jawa.
TANAMAN KADAR AIR
Serbuk simplisia merica hitam 7,24 ± 0,28 %
Serbuk simplisia cabe jawa 8,18 ± 0,26 %
Pada tabel V.1 diketahui bahwa kadar air serbuk simplisia merica hitam dan serbuk simplisia cabe jawa memenuhi persyaratan FHI kurang dari 10%. Setiap penimbangan yang dilakukan, serbuk tanaman tunggal maupun formula campuran harus dilakukan perhitungan berat kering dari berat serbuk yang ditimbang untuk menjamin kuantitasi yang hasil didapatkan.
5.2 Optimasi Kondisi
Konsentrasi sampel yang digunakan adalah 10.000 ppm dan jumlah larutan yang akan ditotolkan pada plat KLT adalah 35,0 µL. Sedangkan fase gerak yang terpilih adalah n-Heksan, kloroforom (0.5:3.5). Kondisi ini dapat menampakkan senyawa marker spesifik dari tiap tanaman
dan memiliki pemisahan yang baik antara senyawa marker spesifik dan senyawa lainnya. Dari hasil eluasi dengan fase gerak terpilih tersebut, senyawa marker spesifik merica hitam memiliki resolusi 0,84, sedangkan senyawa marker spesifik cabe jawa memiliki resolusi 3,6. Persyaratan nilai resolusi yang diterima adalah > 0,8. Kemudian dari hasil scanning,
masing-masing peak senyawa marker spesifik mempunyai nilai peak purity ≥
0,9900.
5.3 Penentuan Senyawa Marker Spesifik
Gambar 5.1 Hasil visualisasi sampel merica hitam, formula campuran dan cabe jawa pada 366 nm menggunakan Camag TLC – Visualizer. a)cabe jawa, b) formula campuran, c) merica hitam.
Gambar 5.2 Kromatogram masing-masing tanaman dan formula campuran pada 366 nm.
1)peak marker merica hitam, 2) peak marker cabe jawa.
Penentuan senyawa marker spesifik dilakukan dengan memilih satu senyawa dari tiap tanaman tunggal merica hitam dan cabe jawa, yang hanya dimiliki oleh salah satu tanaman itu saja. Sehingga dengan adanya senyawa tersebut, bisa menandakan keberadaan tanaman tunggal di formula campuran. Terlihat pada gambar 5.1, di Rf 0,09 sampel tanaman tunggal merica hitam sama-sama noda dengan warna yang sama, sedangkan noda tersebut tidak tampak pada sampel cabe jawa. Pada gambar 5.2 juga membuktikan bahwa pada kromatogram sampel merica hitam dan formula campuran sama-sama terdapat peak pada Rf 0,09 dan peak tersebut tidak tampak di kromatogram sampel cabe jawa. Maka dapat disimpulkan bahwa senyawa marker spesifik merica hitam terdapat pada Rf 0,09.
Sedangkan untuk senyawa marker spesifik cabe jawa, terlihat pada gambar 5.1, pada Rf 0,52 baik sampel cabe jawa dan formula
campuran terdapat noda dengan warna yang sama tetapi noda tersebut tidak tampak di sampel merica hitam. Pada gambar 5.2 juga membuktikan bahwa pada kromatogram sampel cabe jawa dan formula campuran sama-sama terdapat peak pada Rf 0,52 dan peak tersebut tidak tampak di kromatogram sampel merica hitam. Maka dapat disimpulkan bahwa senyawa marker spesifik merica hitam terdapat pada Rf 0,52.
Tabel V.2 Rf senyawa marker spesifik dari tiap tanaman
TANAMAN Rf
Merica Hitam 0,09
Cabe Jawa 0,52
5.4 Hasil Validasi Metode
5.4.1 Uji stabilitas
Pertama uji stabilitas pada pelarut. Untuk menguji ekstrak formula
campuran dalam pelarut Heksan p.a, dilakukan 3 sampel : sampel recenter
paratus (rp), sampel dengan waktu kontak 1 jam dan sampel dengan waktu kontak 8 jam.
Gambar 5.3 Hasil visualisasi uji stabilitas dalam pelarut pada 366 nm; a. Sampel rp; b. Sampel dengan kontak pelarut dan serbuk simplisia formula campuran selama 1 jam; c. Sampel dengan kontak pelarut dan serbuk simplisia formula campuran selama 8 jam.
Gambar 5.4 Kromatogram uji stabilitas dalam pelartu pada 366 nm.
Dari gambar 5.3 tersebut menunjukkan tidak adanya perbedaan noda dari ketiga sampel dan pada gambar 5.4 juga menunjukkan tidak terdapat perbedaan kromatogram dari ketiga sampel. Hal tersebut
menunjukkan sampel dapat stabil dalam penyimpanan suhu ruangan (250
C) selama 8 jam.
Selanjutnya uji stabilitas dalam plat KLT, untuk menguji stabilitas serbuk simplisia dalam pelarut Heksan p.a, dilakukan menggunakan 2 sampel (sampel kontak dengan plat 2 jam dan 3 jam).
Gambar 5.5 Hasil visualisasi uji Gambar 5.6 Hasil visualisasi uji stabilitas pada 366 nm selama 2 jam stabilitas pada 366 nm selama 3 jam
Pada gambar 5.5 menunjukkan sampel stabil selama 2 jam, hal tersebut ditunjukkan dengan noda yang terbentuk berupa garis longitudinal. Sedangkan pada gambar 5.6 menunjukkan bahwa terdapat noda diluar garis longitudinal (degradan). Dari gambar tersebut dapat disimpulkan bahwa serbuk simplisia formula campuran stabil dalam plat KLT selama 2 jam.
5.4.2 Presisi
Pada uji validasi presisi, dilakukan 3 kali replikasi tiap formula dan dilakukan selama 3 hari. Kemudian area senyawa marker spesifik cabe jawa akan dibagi dengan area senyawa marker spesifik merica hitam pada tiap formulanya, sehingga didapatkan nilai rasio area dari senyawa marker spesifik cabe jawa. Begitu juga sebaliknya untuk area senyawa marker merica hitam, dibagi dengan area senyawa marker cabe jawa tiap formulanya sehingga akan didapatkan nilai rasio area dari senyawa marker
spesifik merica hitam. Kemudian dihitung %KV dari rasio area pada masing-masing intraday dan interday.
Tabel V.3 Rasio area senyawa marker spesifik pada tiap formula campuran
MH F1 MH F2 MH F3 CJ F1 CJ F2 CJ F3
Tabel V.4 %KV rasio area masing-masing senyawa marker spesifik pada tiap formula (n=3)
Pada tabel V.4 menunjukkan bahwa KV area senyawa marker spesifik kedua tanamanan, baik intraday dan interday ≤ dari 5%.
5.4.3 Peak purity dan peak identity
Pada tahap ini dilakukan scanning pada masing-masing peak senyawa marker spesifik. Peak discan dengan menggunakan lambda 200 nm – 500 nm.
Tabel V.5 Peak purity senyawa marker spesifik merica hitam
Tabel V.6 Peak purity senyawa marker spesifik cabe jawa
Gambar 5.7 Peak identity senyawa marker spesifik merica hitam
Gambar 5.8 Peak identity senyawa marker spesifik cabe jawa
Pada tabel V.4, menunjukkan bahwa peak purity dari peak
senyawa marker spesifik cabe jawa memiliki nilai correlation limit ≥
0,9900 dan panjang gelombang maksimum senyawa tersebut berada disekitar 340 nm. Pada gambar 5.7 dilakukan overlay profil spektra antara peak senyawa marker spesisik cabe jawa pada formula dengan senyawa marker spesifik cabe jawa pada serbuk simplisianya. Nilai correlation limit
dari overlay kedua profil spektra tersebut adalah ≥ 0,9900.
Sedangkan pada tabel V.5 menunjukkan bahwa peak purity dari
peak senyawa marker spesifik merica hitam memiliki nilai correlation limit
≥ 0,9900 dan panjang gelombang maksimum senyawa tersebut berada
disekitar 340 nm. Terlihat pada gambar 5.8 dilakukan overlay profil spektra antara peak senyawa marker spesisik merica hitam pada formula dengan senyawa marker spesifik merica hitam pada serbuk simplisianya. Nilai
correlation limit dari overlay kedua profil spektra tersebut adalah ≥ 0,9900.
5.4.4 Batas deteksi dan batas kuantitasi
Untuk mengetahui batas deteksi dan batas kuantitasi dari masing-masing senyawa marker tiap tanaman, dilakukan perhitungan regresi linear dari 5 level konsentrasi sampel yang ditotolkan yang masih menampakkan noda senyawa marker spesifik. Kemudian akan dilakukan perhitungan regresi linear antara berat sampel dengan area yang didapatkan
menggunakan software VMA Solution.
Tabel V.7 Batas deteksi dan batas kuantitasi pada merica hitam
Konsentrasi sampel Volume totolan Berat sampel Area
186 ppm 35,0 µL 0,93 mg 356,56
Dari tabel V.7 terlihat bahwa senyawa marker spesifik merica hitam memiliki batas deteksi pada 0,92 mg dan batas kuantitasi pada 2,76 mg.
Tabel V.8 Batas deteksi dan batas kuantitasi pada cabe jawa
Konsentrasi sampel Volume totolan Berat sampel Area
460 ppm 35,0 µL 2,30 mg 240,56
Dari tabel V.8 terlihat bahwa senyawa marker spesifik cabe jawa memiliki batas deteksi pada 1,29 mg dan batas kuantifikasi pada 3,86 mg.