LAMPIRAN
Lampiran 2. Gambar tumbuhan dan daun kelor (Moringa oleifera Lam.)
Gambar 1. Tumbuhan kelor (Moringa oleifera Lam.)
Lampiran 3. Gambar simplisia dan serbuk daun kelor
Gambar 3. Panjang dan LebarDaun kelor
Lampiran 4. Gambar mikroskopik daun kelor segar dan serbuk simplisia daun kelor
Keterangan :
Penampang melintang daun kelor segar Perbesaran 10x40
1. Kutikula (Lapisan lilin) 2. Epidermis atas
3. Jaringan palisade (jaringan tiang) 4. Jaringan spons (jaringan bunga karang) 5. Kristal oksalat bentuk druse
6. Epidermis bawah 7. Rambut penutup 8. Berkas pembuluh 9. Stoma
1
2 3
4
6 5
Lampiran 4. (Lanjutan)
Keterangan :
Mikroskopik serbuk simplisia daun kelor Perbesaran 10x40
1. Stomata tipe anomositik pada epidermis bawah 2. Rambut penutup
3. Sel minyak 4. Berkas pembuluh
5. Kristal oksalat bentuk druse
1
2
3
4
Lampiran 5. Perhitungan hasil pemeriksaan karakterisasi simplisia daun kelor
1. Perhitungan penetapan kadar air
a. Berat sampel = 5,026 g
Volume air = Vt-Vo = 2,2 ml - 1,8 ml = 0,40 ml
Kadar air = 0,40
5,026x 100% = 7,958%
b. Berat sampel = 5,015 g
Volume air = Vt-Vo = 2,15 ml - 1,8 ml = 0,35 ml
Kadar air = 0,35
5,015 x 100% = 6,979%
c. Berat sampel = 5,013 g
Volume air = Vt-Vo = 2,15 ml - 1,8 ml = 0,35 ml
Kadar air = 0,35
5,013 x 100% = 6,981%
Kadar air rata-rata = (7,958+6,979+6,981)%
3 = 7,306%
Kadar air simplisia = volume air
Lampiran 5. (Lanjutan)
2. Perhitungan penetapan kadar sari larut dalam air
a. Berat sampel = 5,011 g
Kadar sari rata-rata = (31,361 +28,074 +27,018)%
3 = 29,717%
Kadar sari = berat sari
berat sampel x 100
Lampiran 5. (Lanjutan)
3. Perhitungan penetapan kadar sari larut dalam etanol
a. Berat sampel = 5,012 g
Kadar sari rata-rata = (17,877+23,270+21,128)%
3 = 20,573%
Kadar sari = berat sari
berat sampel x 100
Lampiran 5. (Lanjutan)
4. Perhitungan penetapan kadar abu total
a. Berat sampel = 2,016 g
Berat abu = 0,187 g
Kadar abu = 0,187
2,016 x 100% = 9,27%
b. Berat sampel = 2,012 g
Berat abu = 0,175 g
Kadar abu = 0,175
2,012 x 100% = 8,69%
c. Berat sampel = 2,020 g
Berat abu = 0,188 g
Kadar abu = 0,188
2,020 x 100% = 9,30%
Kadar abu total rata-rata = (9,27+8,69+9,30)%
3 = 9,08%
Kadar abu total = berat abu
Lampiran 5. (Lanjutan)
5. Perhitungan penetapan kadar abu tidak larut asam
a. Berat sampel = 2,016 g
Berat abu = 0,017 g
Kadar abu = 0,017
2,016 x 100% = 0,84%
b. Berat sampel = 2,012 g
Berat abu = 0,016 g
Kadar abu = 0,016
2,012 x 100% = 0,79%
c. Berat sampel = 2,020 g
Berat abu = 0,021 g
Kadar abu = 0,021
2,020 x 100% = 1,03%
Kadar abu total rata-rata = (0,84 + 0,79 + 1,03)%
3 = 0,88%
Kadar abu tidak larut asam = berat abu
Lampiran 6. Gambar biji kelor (Moringa oleifera Lam.)
Gambar 6. Biji kelor yang terdapat di dalam buah
Lampiran 6. (Lanjutan)
Gambar 8. Biji kelor segar dengan Gambar 9. Biji kelor kering dengan kulit biji kulit biji
Gambar 10. Simplisia biji kelor
Lampiran 7. Gambar mikroskopik biji kelor segar dan serbuk simplisia biji kelor
Keterangan:
Penampang melintang biji kelor segar Perbesaran 10x40
1. Lapisan kutikula 2. Lapisan lendir 3. Epidermis atas
4. Jaringan palisade (jaringan tiang) 5. Parenkim dengan minyak atsiri 6. Embrio
7. Berkas pembuluh 8. Sel batu
9. Sklerenkim
1
Lampiran 7. (Lanjutan)
Keterangan:
Mikroskopik serbuk simplisia biji kelor Perbesaran 10x40
1. Parenkim dengan minyak atsiri 2. Sklerenkim
3. Berkas pembuluh 4. Sel batu
1
2
3
Lampiran 8. Perhitungan hasil pemeriksaan karakterisasi simplisia biji kelor
1. Perhitungan penetapan kadar air
a. Berat sampel = 5,013 g
Volume air = Vt-Vo = 2,0 ml - 1,8 ml = 0,20 ml
Kadar air = 0,20
5,013 � 100% = 3,989%
b. Berat sampel = 5,015 g
Volume air = Vt-Vo = 2,0 ml - 1,8 ml = 0,20 ml
Kadar air = 0,20
5,015 x 100% = 3,988%
c. Berat sampel = 5,018 g
Volume air = Vt-Vo = 2,05 ml - 1,8 ml = 0,25 ml
Kadar air = 0,25
5,018 x 100% = 4,982%
Kadar air rata-rata = (3,989+3,988+4,982)%
3 = 4,319%
Kadar air simplisia = volume air
Lampiran 8. (Lanjutan)
2. Perhitungan penetapan kadar sari larut dalam air
a. Berat sampel = 5,018 g
Kadar sari rata-rata = (18,732 +18,342+19,669)%
3 = 18,914%
Kadar sari = berat sari
berat sampel x 100
Lampiran 8. (Lanjutan)
3. Perhitungan penetapan kadar sari larut dalam etanol
a. Berat sampel = 5,023 g
Kadar sari rata-rata = (16,98+11,99+17,97)%
3 = 14,997%
Kadar sari = berat sari
berat sampel x 100
Lampiran 8. (Lanjutan)
4. Perhitungan penetapan kadar abu total
a. Berat sampel = 2,013 g
Berat abu = 0,1750 g
Kadar abu = 0,1750
2,013 x 100% = 8,693%
b. Berat sampel = 2,017 g
Berat abu = 0,1761 g
Kadar abu = 0,1761
2,017 x 100% = 8,730%
c. Berat sampel = 2,022 g
Berat abu = 0,1814 g
Kadar abu = 0,1814
2,022 x 100% = 8,971%
Kadar abu total rata-rata = (8,693+8,730+8,971)%
3 = 8,978%
Kadar abu total = berat abu
Lampiran 8. (Lanjutan)
5. Perhitungan penetapan kadar abu tidak larut asam
a. Berat sampel = 2,013 g
Berat abu = 0,0171 g
Kadar abu = 0,0171
2,013 x 100% = 0,849%
b. Berat sampel = 2,017 g
Berat abu = 0,0184 g
Kadar abu = 0,0184
2,017 x 100% = 0,912%
c. Berat sampel = 2,022 g
Berat abu = 0,0199 g
Kadar abu = 0,0199
2,022 x 100% = 0,984%
Kadar abu total rata-rata = (0,849 + 0,912 + 0,984)%
3 = 0,915%
Kadar abu tidak larut asam = berat abu
Lampiran 9. Bagan kerja penelitian untuk daun kelor
Dipisahkan dari pengotornya Dicuci, ditiriskan dan dikeringkan Ditimbang
Dikeringkan pada suhu ± 40ºC Ditimbang
Diblender/dihaluskan Daun kelor 3,0 kg
Simplisia 395 g
Serbuk daun kelor
Uji karakterisasi simplisia Penetapan kadar
magnesium dan besi dengan metode AAS Daun kelor yang
telah di ambil
Pemeriksaan makroskopik
Penetapan kadar air Pemeriksaan mikroskopik
Penetapan kadar sari larut dalam air
Penetapan kadar sari larut etanol
Penetapan kadar abu total
Lampiran 10. Bagan alir proses destruksi kering (simplisia daun kelor)
Ditimbang 5 g di dalam krus porselen
Ditambahkan 5 tetes Asam Nitrat 65% (b/v)
Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100°C dan perlahan-lahan temperatur dinaikkan hingga suhu 500°C dengan interval 25°C setiap 5 menit
Dilakukan selama 75 jam dan dibiarkan hingga dingin di dalam tanur
Ditambahkan 5 ml Asam Nitrat (1:1)
Diuapkan pada hot plate sampai kering Serbuk daun kelor
Sampel yang telah mengarang
Sampel yang telah mengabu
Lampiran 11. Bagan kerja penelitian untuk biji kelor
Dikeluarkan bijinya
Dicuci, ditiriskan dan dikeringkan Ditimbang
Dikeringkan pada suhu ± 40ºC Dibuang kulit bijinya
Ditimbang
Diblender/dihaluskan Biji kelor 2,0 kg
Simplisia 235 g
Serbuk biji kelor Buah Kelor
Uji karakterisasi simplisia Penetapan kadar
magnesium dan besi dengan metode AAS Pemeriksaan makroskopik
Penetapan kadar air Pemeriksaan mikroskopik
Penetapan kadar sari larut dalam air
Penetapan kadar sari larut etanol
Penetapan kadar abu total
Lampiran 12. Bagan alir proses destruksi kering (simplisia biji kelor)
Ditimbang 5 g di dalam krus porselen
Ditambahkan 5 tetes Asam Nitrat 65% (b/v)
Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100°C dan perlahan-lahan temperatur dinaikkan hingga suhu 500°C dengan interval 25°C setiap 5 menit
Dilakukan selama 92 jam dan dibiarkan hingga dingin di dalam tanur
Ditambahkan 5 ml Asam Nitrat (1:1)
Diuapkan pada hot plate sampai kering Serbuk biji kelor
Sampel yang telah mengarang
Sampel yang telah mengabu
Lampiran 13. Bagan alir pembuatan larutan sampel
Dilarutkan dalam 5 ml Asam Nitrat (1:1)
Dimasukkan ke dalam labu tentukur 100 ml
Dibilas krus porselen sebanyak tiga kali dengan 10 ml akuademineralisata
Dicukupkan dengan akuademineralisata hingga garis tanda
Disaring dengan kertas saring Whatman No.42
Dibuang 10 ml untuk menjenuhkan kertas saring
Dimasukkan ke dalam botol
Dilakukan analisis kualitatif
Dilakukan analisis kuantitatif dengan spektrofotometer
serapan atom pada λ 285,2 nm (lampu katoda magnesium)
untuk magnesium, λ 248,3 nm (lampu katoda besi) untuk besi
Sampel hasil dekstruksi
Filtrat
Larutan sampel
Lampiran 14. Gambar hasil analisis kualitatif magnesium dan besi
Gambar 12. Hasil Reaksi Magnesium + NaOH + Titan Yellow menghasilkan larutan berwarna merah terang
Lampiran 15. Data kalibrasi magnesium dengan spektrofotometer serapan atom, perhitungan persamaan garis regresi dan koefisien korelasi (r)
No Konsentrasi (µg/ml) (X)
Lampiran 15. (Lanjutan)
r = ∑XY− [
(∑X )(∑Y )
n ]
��∑X²–(∑X)² / n � (∑Y²−(∑Y)² / n )
r = 0,36482 –�
(3,0000 )(0,4943 )
6 �
��2,2000−(3,0000 )2
6 ��0,06051213−
(0,4943 )2
6 �
r = 0,11767
0,11769
r = 0,999830062
Lampiran 16. Data kalibrasi besi dengan spektrofotometer serapan atom, perhitungan persamaan garis regresi dan koefisien korelasi (r)
No Konsentrasi (µg/ml) (X)
Lampiran 16. (Lanjutan)
r = ∑XY− [
(∑X )(∑Y )
n ]
��∑X²–(∑X)² / n � (∑Y²−(∑Y)² / n )
r =
1,6610 –�(30,0000 )(0,2279 )
6 �
��220,0000−(30,0000 )2
6 ��0,01254347−
(0,2279 )2
6 �
r = 0,5215
0,5216
r = 0,999808282
Lampiran 17. Rekapitulasi data kadar magnesium dan besi dalam simplisia daun dan biji kelor sebelum uji t
Lampiran 18. Rekapitulasi data kadar magnesium dan besi dalam simplisia daun dan biji kelor setelah uji t
Lampiran 19. Contoh perhitungan kadar magnesium dan besi dalam sampel
1. Contoh perhitungan kadar magnesium dalam simplisia daun kelor
Berat sampel yang ditimbang = 5,0753 g
Absorbansi (Y) = 0,0829
Persamaan garis regresi: Y = 0,1681 X
−
0,00175X = 0,0829 + 0,00175
0,1681 = 0,5030 µg/ml
Konsentrasi magnesium = 0,5030 µg/ml
Kadar (µg/g) = Konsentrasi (µg/ml ) x Volume (ml ) x Faktor pengenceran
2. Contoh perhitungan kadar besi dalam simplisia daun kelor
Berat sampel yang ditimbang = 5,0753 g
Absorbansi (Y) = 0,0238
Lampiran 19. (Lanjutan)
3. Contoh perhitungan kadar magnesium dalam simplisia biji kelor
Berat sampel yang ditimbang = 5,0865 g
Absorbansi (Y) = 0,0877
Persamaan garis regresi: Y = 0,1681 X
−
0,00175X = 0,0877 + 0,00175
0,1681 = 0,5320 µg/ml
Konsentrasi magnesium = 0,5320 µg/ml
Kadar (µg/g) = Konsentrasi (µg/ml ) x Volume (ml ) x Faktor pengenceran
4. Contoh perhitungan kadar besi dalam simplisiaa biji kelor
Berat sampel yang ditimbang = 5,0865 g
Absorbansi (Y) = 0,0162
Lampiran 20. Perhitungan statistik kadar magnesium dalam sampel
1. Perhitungan statistik kadar magnesium dalam simplisia daun kelor
No Xi
Data diterima jika t hitung < t tabel
Lampiran 20. (Lanjutan)
t hitung 3 = | −3,6181 |
2,6479 / √6
= 3,346
t hitung 4 = | −1,2152 |
2,6479 / √6 = 1,123
t hitung 5 = | −0,2152 |
2,6479 / √6 = 0,198
t hitung 6 = | 2,4188 |
2,6479 / √6
= 2,237
Kadar magnesium dalam simplisia daun kelor:
µ = X ± (t (α / 2, dk) x SD / √�)
= 615,7956 mg/100 g ± (4,0321 x 2,6479 mg/100 g / √6 )
= (615,7956 ± 4,3595) mg/100 g
Kadar magnesium pada simplisia daun kelor sebenarnya terletak antara:
Lampiran 20. (Lanjutan)
2. Perhitungan statistik kadar magnesium dalam simplisia biji kelor
No Xi
Data diterima jika t hitung < t tabel
Lampiran 20. (Lanjutan)
t hitung 3 = | −0,0634 |
0,7507 / √6
= 0,207
t hitung 4 = | −0,0593|
0,7507 / √6 = 0,193
t hitung 5 = | −1,231|
0,7507 / √6 = 4,022
t hitung 6 = | −0,0553 |
0,7507 / √6
= 0,180
Kadar magnesium dalam simplisia biji kelor:
µ = X ± (t (α / 2, dk) x SD / √�)
= 208,0895 mg/100 g ± (4,0321 x 0,7507 mg/100 g / √6 )
= (208,0895 ± 1,234) mg/100 g
Kadar magnesium pada simplisia biji kelor sebenarnya terletak antara:
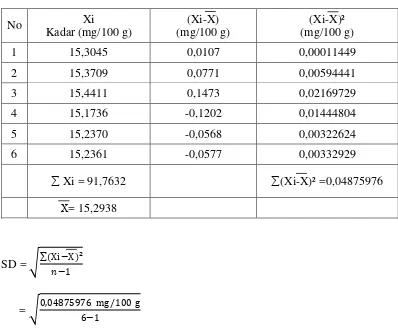
Lampiran 21. Perhitungan statistik kadar besi dalam sampel
1. Perhitungan statistik kadar besi dalam simplisia daun kelor
No Xi
Data diterima jika t hitung < t tabel
Lampiran 21. (Lanjutan)
t hitung 3 = | 0,1473 |
0,0987 / √6
= 3,6825
t hitung 4 = |−0,1202 |
0,0987 / √6
= 3,005
t hitung 5 = |−0,0568 |
0,0987 / √6
= 1,420
t hitung 6 = |−0,0577 |
0,0987 / √6
= 1,4425
Kadar besi dalam simplisia daun kelor:
µ = X ± (t (α / 2, dk) x SD / √�)
= 15,2938 mg/100 g ± (4,0321 x 0,0987 mg/100 g / √6 )
= (15,2938 ± 0,161284) mg/100 g
Kadar besi pada simplisia daun kelor sebenarnya terletak antara:
Lampiran 21. (Lanjutan)
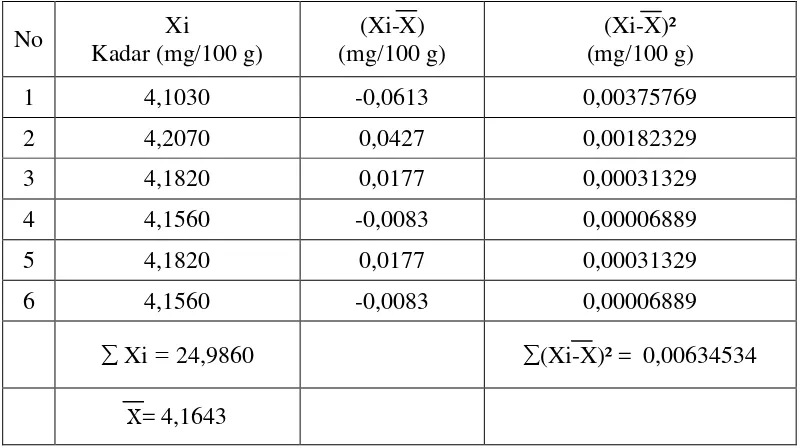
2. Perhitungan statistik kadar besi dalam simplisia biji kelor
No Xi
Data diterima jika t hitung < t tabel
Lampiran 21. (Lanjutan)
Data pertama ditolak karena t hitung lebih besar dari t tabel, untuk itu perhitungan
diulangi dengan cara yang sama tanpa mengikutsertakan data pertama
Lampiran 21. (Lanjutan)
Pada interval kepercayaan 99% dengan nilai α = 0,01; dk = 4 diperoleh nilai t
tabel = α/ 2 = 4,6041.
Data diterima jika t hitung < t tabel
t hitung = |��−�| �� / √�
t hitung 2 = | 0,0304 |
0,0214 / √5 = 3,166
t hitung 3 = | 0,0054 |
0,0214 / √5 = 0,562
t hitung 4 = |−0,0206 |
0,0214 / √5
= 2,145
t hitung 5 = | 0,0054 |
0,0214 / √5 = 0,5625
t hitung 6 = |−0,0206 |
0,0214 / √5
= 2,145
Kadar besi dalam simplisia biji kelor:
µ = X ± (t (α / 2, dk) x SD / √�)
= 4,1766 mg/100 g ± (4,6041 x 0,0096 mg/100 g / √5 )
= (4,1766 ± 0,0442) mg/100 g
Kadar besi pada simplisia biji kelor sebenarnya terletak antara:
Lampiran 22. Pengujian beda nilai rata-rata kadar magnesium pada simplisia daun dan biji kelor
No Daun Biji
1. X1 = 615,7956 X2 = 208,0895
2. S1 = 2,6479 S2 = 0,7507
Dilakukan uji F dengan taraf kepercayaan 99% untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2) atau berbeda (σ1 ≠ σ2).
- H0: σ1= σ2
H1: σ1≠ σ2
- Nilai kritis F yang diperbolehkan dari tabel (F 0,01/2, (5,5)) adalah = 14,94
- Daerah kritis penolakan: hanya jika F0 ≥ 14,94
disimpulkan bahwa σ1 = σ2. Berarti tidak terdapat perbedaan yang signifikan
rata-rata kadar magnesium dalam simplisia daun dan biji kelor.
- Dilanjutkan dengan uji beda rata–rata menggunakan distribusi t
- Simpangan bakunya adalah:
Lampiran 22. (Lanjutan)
- H0 : µ1 = µ 2
H1 : µ1≠ µ 2
- Dengan menggunakan taraf kepercayaan 99% dengan nilai α = 1%
t 0,01/2 = ± 3,1693 untuk df = 6 + 6 -2 = 10
- Daerah kritis penerimaan: - 3,1693 ≤ t0≤ 3,1693
- Daerah kritis penolakan: t0< -3,1693 dan t0> 3,1693
t0 =
(X1−X2)
���11+1
�2
= (615 ,7956 − 208,0895)
1,9461 �1
6+ 1 6
= 407,7061
1,1235
= 362,8892
- Karena t0 = 362,8892 > 3,1693 maka hipotesis H0 ditolak. Berarti terdapat
Lampiran 23. Pengujian beda nilai rata-rata kadar besi pada simplisia daun dan biji kelor
No Daun Biji
1. X1 = 15,2938 X2 = 4,1766
2. S1 = 0,0987 S2 = 0,0214
Dilakukan uji F dengan taraf kepercayaan 99% untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2) atau berbeda (σ1 ≠ σ2).
- H0: σ1= σ2
H1: σ1≠ σ2
- Nilai kritis F yang diperbolehkan dari tabel (F 0,01/2, (5,4)) adalah = 22,46
- Daerah kritis penolakan: hanya jika F0 ≥ 22,46
disimpulkan bahwa σ1 = σ2. Berarti tidak terdapat perbedaan yang signifikan
rata-rata kadar besi dalam simplisia daun dan biji kelor.
- Dilanjutkan dengan uji beda rata–rata menggunakan distribusi t
- Simpangan bakunya adalah:
Lampiran 23. (Lanjutan)
- H0 : µ1 = µ 2
H1 : µ1≠ µ 2
- Dengan menggunakan taraf kepercayaan 99% dengan nilai α = 1%
t 0,01/2 = ± 3,2498 untuk df = 6 + 5 - 2 = 9
- Daerah kritis penerimaan: - 3,2498 ≤ t0≤ 3,2498
- Daerah kritis penolakan: t0< -3,2498 dan t0> 3,2498
t0 =
(X1−X2)
���11+1
�2
= (15,2938− 4,1766 ) 0,0749 �16+15
=
11,1172 0,0453= 245,4128
- Karena t0 = 245,4128 > 3,2498 maka hipotesis H0 ditolak. Berarti terdapat
Lampiran 24. Hasil analisis kadar magnesium dan besi sebelum dan sesudah penambahan masing-masing larutan baku pada simplisia daun kelor
1. Hasil analisis kadar magnesium (Mg) sebelum ditambahkan larutan baku
Sampel Berat Sampel (g)
Rata-rata 5,0747 615,7956
2. Hasil analisis kadar magnesium (Mg) setelah ditambahkan larutan baku
Sampel
∑ 30,3485 4095,4233 653,7182
Lampiran 24. (Lanjutan)
3. Hasil analisis kadar besi (Fe) sebelum ditambahkan larutan baku
Sampel Berat Sampel (g)
Rata-rata 5,0747 15,2938
4. Hasil analisis kadar besi (Fe) setelah ditambahkan larutan baku
Sampel
Lampiran 25. Perhitungan jumlah baku yang ditambahkan untuk persen perolehan kembali magnesium dan besi pada simplisia daun kelor
Jumlah baku yang ditambahkan dapat dihitung menggunakan rumus berikut:
C*A = 10 % x X
V =
C∗A x BSKonsentrasi baku yang digunakan
Keterangan:
C*A = Kadar larutan baku yang ditambahkan (µg/g)
X = Kadar rata–rata logam pada sampel (mg/100 g)
V = Jumlah larutan baku yang ditambahkan (ml)
BS = Berat rata–rata sampel untuk uji persen perolehan kembali (g)
1. Magnesium
Berat rata–rata sampel untuk uji persen perolehan kembali (BS) = 5,0581 g
Kadar rata–rata magnesium pada daun kelor yang dikeringkan (X) = 615,7956
mg/100 g
Konsentrasi baku yang digunakan
= 615,7956 µg/g x 5,0581 g
1000 µg/ml
= 3,114755724 ml
Lampiran 25. (Lanjutan)
2. Besi
Berat rata–rata sampel untuk uji persen perolehan kembali (BS) = 5,0581 g
Kadar rata–rata besi pada daun kelor (X) = 15,2938 mg/100 g
C*A = 10 % x X
= 10
100 x 15,2938 mg/100 g
= 1,52938 mg/100 g = 15,2938 µg/g
V
= C∗A x BSKonsentrasi baku yang digunakan
= 15,2938 µg/g x 5,0581 g
10 µg/ml
Lampiran 26. Perhitungan uji perolehan kembali kadar magnesium dan besi dalam simplisia daun kelor
1. Perhitungan uji perolehan kembali kadar magnesium
Sampel 1
Persamaan regresi : Y = 0,1681 X
−
0,00175X = 0,0909 + 0,00175
0,1681 = 0,5511 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5511 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5511 µg/ml
5,0578 g x 100 ml x 625
= 6810,0260 µg/g
= 681,0026 mg/100 g
Kadar sampel 1 setelah ditambah larutan baku (CF) = 681,0026 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari keenam sampel
CA =
(619,4215 + 614 ,5925+612 ,1775 +614,5804 +615 ,7878 +618 ,2144 ) mg /100 g
6 = 615,7956 mg/100g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Maka % perolehan kembali magnesium = CF−CA
�∗�
x 100%
= (681 ,0026 − 615,7956) mg /100 g
61,2878 mg /100 g
x 100%
Lampiran 26. (Lanjutan)
Sampel 2
Persamaan regresi : Y = 0,1681 X
−
0,00175X = 0,0913 + 0,00175
0,1681 = 0,5535 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5535 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5535 µg/ml
5,0583 g x 100 ml x 625
= 6839,0071 µg/g
= 683,9007 mg/100 g
Kadar sampel 2 setelah ditambah larutan baku (CF) = 683,9007 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari keenam sampel
CA=
(619,4215 + 614 ,5925+612 ,1775 +614 ,5804 +615,7878 +618 ,2144 ) mg /100 g
6 = 615,7956 mg/100g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Maka % perolehan kembali magnesium = CF−CA
�∗�
x 100%
= (683 ,9007 − 615,7956) mg /100 g
61,2878 mg /100 g x 100%
Lampiran 26. (Lanjutan)
Sampel 3
Persamaan regresi : Y = 0,1681 X
−
0,00175X = 0,0919 + 0,00175
0,1681 = 0,5571 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5571 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5571 µg/ml
5,0586 g x 100 ml x 625
= 6883,0802µg/g
= 688,3080 mg/100 g
Kadar sampel 3 setelah ditambah larutan baku (CF) = 688,3080 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari keenam sampel
CA =
(619,4215 + 614 ,5925+612 ,1775 +614,5804 +615 ,7878 +618 ,2144 ) mg /100 g
6 = 615,7956 mg/100g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Maka % perolehan kembali magnesium = CF−CA
�∗�
x 100%
=(688,3080 − 615,7956) mg/100 g61,2878 mg/100 g x 100%
Lampiran 26. (Lanjutan)
Sampel 4
Persamaan regresi : Y = 0,1681 X
−
0,00175X = 0,0910 + 0,00175
0,1681 = 0,5517 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5517 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5517 µg/ml
5,0580 g x 100 ml x 625
= 6817,1708 µg/g
= 681,7170 mg/100 g
Kadar sampel 4 setelah ditambah larutan baku (CF) = 681,7170 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari keenam sampel
CA =
(619,4215 + 614 ,5925+612 ,1775 +614,5804 +615 ,7878 +618 ,2144 ) mg /100 g
6 = 615,7956 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Maka % perolehan kembali magnesium = CF−CA
�∗� x 100% =(681,7170 − 615,7956) mg/100 g
61,2878 mg/100 g x 100%
Lampiran 26. (Lanjutan)
Sampel 5
Persamaan regresi : Y = 0,1681 X
−
0,00175X = 0,0904 + 0,00175
0,1681 = 0,5481 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5481 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5481 µg/ml
5,0576 g x 100 ml x 625
= 6773,2224 µg/g
= 677,3222 mg/100 g
Kadar sampel 5 setelah ditambah larutan baku (CF) = 677,3222 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari keenam sampel
CA =
(619,4215 + 614 ,5925+612 ,1775 +614,5804 +615 ,7878 +618 ,2144 ) mg /100 g
6 = 615,7956 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Maka % perolehan kembali magnesium = CF−CA
�∗� x 100% =(677,3222 − 615,7956) mg/100 g
61,2878 mg/100 g x 100%
Lampiran 26. (Lanjutan)
Sampel 6
Persamaan regresi : Y = 0,1681 X
−
0,00175X = 0,0912 + 0,00175
0,1681 = 0,5529 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 0,5529 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 0,5529 µg/ml
5,0582 g x 100 ml x 625
= 6831,7286 µg/g
= 683,1728 mg/100 g
Kadar sampel 6 setelah ditambah larutan baku (CF) = 683,1728 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari keenam sampel
CA =
(619,4215 + 614 ,5925+612 ,1775 +614,5804 +615 ,7878 +618 ,2144 ) mg /100 g
6 = 615,7956 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
C*A =
Maka % perolehan kembali magnesium = CF−CA
�∗� x 100%
= (683 ,1728 − 615,7956) mg /100 g
61,2878 mg /100 g x 100%
Lampiran 26. (Lanjutan)
2. Perhitungan uji perolehan kembali kadar besi
Sampel 1
Persamaan regresi: Y = 0,00745 X + 0,00065
X = 0,0262 − 0,00065
0,00745 = 3,4295 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,4295 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 3,4295 µg/ml
5,0578 g x 100 ml x 2,5
= 169,5154 µg/g
= 16,9515 mg/100 g
Kadar sampel 1 setelah ditambah larutan baku (CF) = 16,9515 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari ke enam sampel
CA =
(15,3045+ 15,3709+15,4411 + 15,1736 +15,2370 +15,2361) mg/100 g
6 = 15,2938 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
Lampiran 26. (Lanjutan)
Sampel 2
Persamaan regresi: Y = 0,00745 X + 0,00065
X = 0,0264 − 0,00065
0,00745 = 3,4563 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,4563 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 3,4563µg/ml
5,0583 g x 100 ml x 2,5
= 170,8232 µg/g
= 17,0823 mg/100 g
Kadar sampel 2 setelah ditambah larutan baku (CF) = 17,0823 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari ke enam sampel
CA = (15,3045 + 15,3709+15,4411 + 15,1736 +15,2370 +15,2361 ) mg /100 g6 = 15,2938 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
Lampiran 26. (Lanjutan)
Sampel 3
Persamaan regresi: Y = 0,00745 X + 0,00065
X = 0,0265 − 0,00065
0,00745 = 3,4697 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,4697 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 3,4697µg/ml
5,0586 g x 100 ml x 2,5
= 171,4753 µg/g
= 17,1475 mg/100 g
Kadar sampel 3 setelah ditambah larutan baku (CF) = 17,1475 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari ke enam sampel
CA =
(15,3045 + 15,3709+15,4411 + 15,1736 +15,2370 +15,2361 ) mg /100 g
6 = 15,2938 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
Lampiran 26. (Lanjutan)
Sampel 4
Persamaan regresi: Y = 0,00745 X + 0,00065
X = 0,0263 − 0,00065
0,00745 = 3,4429 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,4429 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 3,4429µg/ml
5,0580 g x 100 ml x 2,5
= 170,1710 µg/g
= 17,0171 mg/100 g
Kadar sampel 4 setelah ditambah larutan baku (CF) = 17,0171 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari ke enam sampel
CA =
(15,3045 + 15,3709+15,4411 + 15,1736 +15,2370 +15,2361 ) mg /100 g
6 = 15,2938 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
Lampiran 26. (Lanjutan)
Sampel 5
Persamaan regresi: Y = 0,00745 X + 0,00065
X = 0,0262 − 0,00065
0,00745 = 3,4295 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,4295 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 3,4295 µg/ml
5,0576 g x 100 ml x 2,5
= 169,5221 µg/g
= 16,9522 mg/100 g
Kadar sampel 5 setelah ditambah larutan baku (CF) = 16,9522 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari ke enam sampel
CA =
(15,3045 + 15,3709+15,4411 + 15,1736 +15,2370 +15,2361 ) mg /100 g
6 = 15,2938 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
Lampiran 26. (Lanjutan)
Sampel 6
Persamaan regresi: Y = 0,00745 X + 0,00065
X = 0,0261 − 0,00065
0,00745 = 3,4161 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,4161 µg/ml
CF =
Konsentrasi (µg/ml )
Berat sampel x Volume (ml) x Faktor pengenceran
= 3,4161µg/ml
5,0582 g x 100 ml x 2,5
= 168,8397 µg/g
= 16,8839 mg/100 g
Kadar sampel 6 setelah ditambah larutan baku (CF) = 16,8839 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan lautan baku (CA) adalah kadar
rata-rata dari ke enam sampel
CA =
(15,3045 + 15,3709+15,4411 + 15,1736 +15,2370 +15,2361 ) mg /100 g
6 = 15,2938 mg/100 g
Berat sampel rata-rata uji recovery = 5,0581 g
Kadar larutan standar yang ditambahkan (C*A) adalah
Lampiran 27. Perhitungan simpangan baku relatif (RSD) kadar magnesium dan besi dalam sampel
1. Perhitungan simpangan baku relatif (RSD) kadar magnesium dalam sampel
Lampiran 27. (Lanjutan)
2. Perhitungan simpangan baku relatif (RSD) kadar besi dalam sampel
No. Persen perolehan kembali (Xi) (%)
6. 100,5374 -7,70576 59,37873718
∑Xi = 649,4495 ∑(Xi - X)2
SD = 6,113504219%
RSD = ��
� X 100%
RSD = 6,113504219 %
108,2415 % X 100%
Lampiran 28. Perhitungan batas deteksi (LOD) dan batas kuantitasi (LOQ) 1. Perhitungan batas deteksi dan batas kuantitasi magnesium
Lampiran 28. (Lanjutan)
2. Perhitungan batas deteksi dan batas kuantitasi besi
Lampiran 31. Gambar alat spektrofotometer serapan atom dan tanur
Gambar 14. Alat spektrofotometer serapan atom (Hitachi Z-2000)
Lampiran 32. Gambar alat destilasi air dan oven
Gambar 16. Alat destilasi (Boeco) Gambar 17. Tabung Penerima
Lampiran 33. Gambar Hotplate dan Mikroskop
Gambar 19. Hotplate (Fisions)