Informasi Dokumen
- Penulis:
- Beata Ratnawati
- Pengajar:
- Ir. Mochtar Hadiwidodo
- M. Arief Budiharjo, ST. MEng
- Wiharyanto Oktiawan ST, MT
- Sri Hapsari Budisulistiorini, ST, M.Eng
- Sri Sumiyati, ST, MSi
- Sekolah: Universitas Diponegoro
- Mata Pelajaran: Teknik Lingkungan
- Topik: Penurunan COD Limbah Tahu Dengan Biofilter Media Kerikil
- Tipe: laporan tugas akhir
- Tahun: 2010
- Kota: Semarang
Ringkasan Dokumen
I. PENDAHULUAN
Bagian ini menjelaskan latar belakang penelitian yang berfokus pada pengolahan limbah tahu, khususnya mengenai kandungan Chemical Oxygen Demand (COD) yang tinggi. Penelitian ini bertujuan untuk menemukan metode pengolahan yang efektif dan ekonomis, dengan menggunakan biofilter media kerikil. Penulis juga mengidentifikasi masalah yang ada, seperti pencemaran lingkungan akibat limbah tahu, dan menetapkan tujuan penelitian untuk menurunkan konsentrasi COD melalui biofilter anaerob dan aerob.
1.1 Latar Belakang
Latar belakang penelitian ini menggarisbawahi pentingnya pengolahan limbah tahu yang dihasilkan dari industri. Dengan meningkatnya permintaan akan tahu, limbah yang dihasilkan juga meningkat, mengakibatkan pencemaran lingkungan. Penelitian ini berfokus pada pengurangan COD yang tinggi dalam limbah tahu, yang mencapai 12.390 mg/l, melalui penggunaan biofilter.
1.2 Identifikasi Masalah
Identifikasi masalah mencakup pencemaran yang dihasilkan oleh limbah tahu yang dibuang langsung ke sungai. Konsentrasi COD yang tinggi menjadi masalah utama yang perlu diatasi, dan penelitian ini bertujuan untuk menemukan cara untuk menurunkan konsentrasi tersebut dengan menggunakan biofilter.
1.3 Pembatasan Masalah
Pembatasan masalah ditetapkan untuk fokus pada penyisihan COD dari limbah tahu. Penelitian ini akan mengukur efisiensi pengolahan menggunakan biofilter anaerob dan aerob, dengan konsentrasi efluen yang dihasilkan sebagai parameter utama.
1.4 Perumusan Masalah
Rumusan masalah dalam penelitian ini mencakup tiga pertanyaan utama: Seberapa besar konsentrasi COD yang dapat diturunkan? Apakah ada pengaruh waktu tinggal terhadap penurunan COD? Dan seberapa besar efisiensi pengolahan biofilter anaerob dibandingkan dengan aerob?
1.5 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui efisiensi penurunan COD pada biofilter dengan media kerikil, serta pengaruh lama kontak terhadap penurunan COD. Penelitian ini juga bertujuan untuk membandingkan efisiensi pengolahan antara biofilter anaerob dan aerob.
1.6 Ruang Lingkup
Ruang lingkup penelitian ini mencakup aspek keilmuan, lokasi penelitian, dan pembahasan yang akan dilakukan. Penelitian ini akan dilakukan di laboratorium dengan menggunakan miniatur sistem pengolahan limbah.
1.7 Manfaat Penelitian
Manfaat dari penelitian ini diharapkan dapat memberikan kontribusi bagi pengembangan ilmu pengetahuan dalam bidang pengolahan limbah cair, serta memberikan solusi bagi masyarakat dalam mengelola limbah tahu secara efektif.
II. TINJAUAN PUSTAKA
Tinjauan pustaka memberikan dasar teori mengenai pengolahan limbah, khususnya melalui proses biologis. Penelitian ini membahas berbagai mikroorganisme yang berperan dalam pengolahan limbah, serta karakteristik limbah cair industri tahu yang menjadi fokus penelitian.
2.1 Pengolahan Biologis
Pengolahan biologis merupakan metode yang digunakan untuk mengurangi konsentrasi komponen organik dalam air limbah. Tinjauan ini mencakup peran mikroorganisme, sumber karbon dan energi, serta kinetika pertumbuhan bakteri yang penting dalam proses pengolahan.
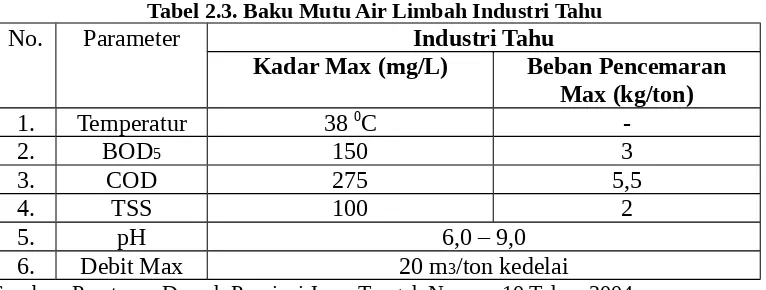
2.2 Limbah Cair Industri Tahu
Bagian ini menjelaskan tentang karakteristik limbah cair dari industri tahu, termasuk bahan baku dan proses pembuatan tahu. Limbah ini mengandung banyak bahan organik yang dapat mencemari lingkungan jika tidak dikelola dengan baik.
2.3 Parameter Dalam Air Limbah
Parameter yang diukur dalam air limbah mencakup padatan total, suhu, COD, dan pH. Setiap parameter memiliki pengaruh terhadap kualitas air dan proses pengolahan limbah.
2.4 Proses Pengolahan Biologi Secara Aerob
Proses aerobik dalam pengolahan limbah melibatkan penggunaan oksigen untuk menguraikan bahan organik. Penjelasan tentang biofilter dan proses pengolahan yang dilakukan dalam kondisi aerobik dijelaskan di sini.
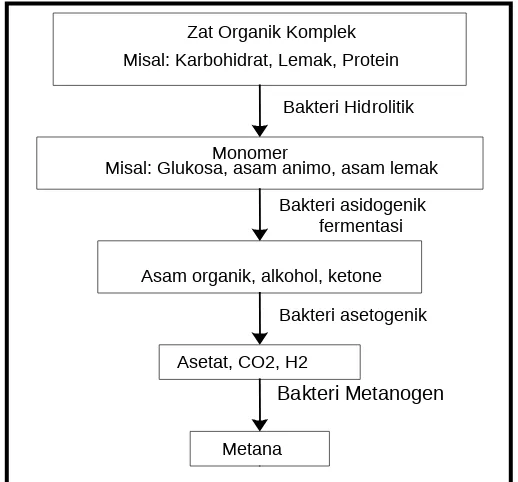
2.5 Biofilter
Biofilter adalah media yang digunakan untuk mengolah air limbah dengan menumbuhkan mikroorganisme di atas media tersebut. Proses ini dapat dilakukan dalam kondisi aerobik, anaerobik, atau kombinasi keduanya, dengan tujuan untuk mengurangi konsentrasi COD.
III. METODOLOGI PENELITIAN
Metodologi penelitian ini menjelaskan langkah-langkah yang diambil untuk mencapai tujuan penelitian, termasuk pengaturan variabel, alat dan bahan yang digunakan, serta tahapan penelitian yang dilakukan.
3.1 Tujuan Operasional Penelitian
Tujuan operasional penelitian ini adalah untuk menguji efisiensi penurunan COD dengan menggunakan biofilter media kerikil, serta mengevaluasi pengaruh waktu tinggal terhadap proses pengolahan.
3.2 Metode dan Jenis Penelitian
Penelitian ini menggunakan metode eksperimen dengan pendekatan kuantitatif. Data yang diperoleh akan dianalisis untuk menentukan efisiensi penurunan COD pada biofilter anaerob dan aerob.
3.3 Variabel Penelitian
Variabel yang diteliti terdiri dari variabel bebas yaitu waktu tinggal dan jenis proses pengolahan, serta variabel terikat yaitu efisiensi penurunan COD.
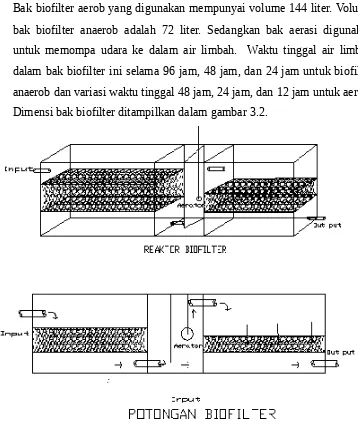
3.4 Alat dan Bahan
Alat dan bahan yang digunakan dalam penelitian ini meliputi reaktor biofilter, media kerikil, dan alat ukur untuk menentukan konsentrasi COD dalam air limbah.
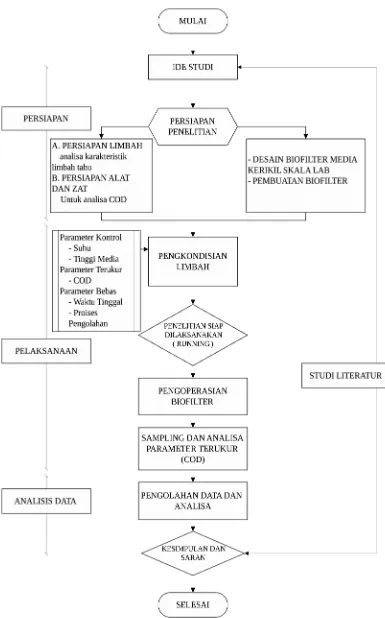
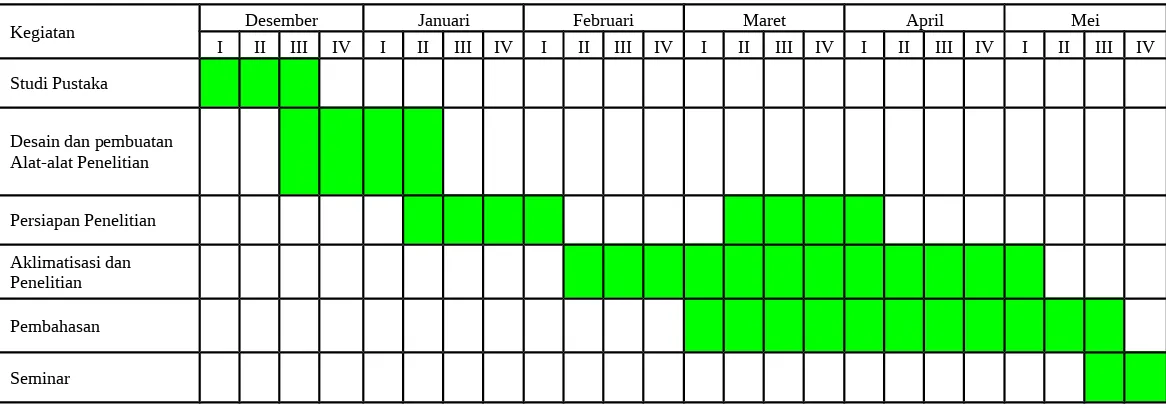
3.5 Tahapan Penelitian
Tahapan penelitian terdiri dari persiapan, pelaksanaan, dan analisis data. Setiap tahap akan dilakukan dengan seksama untuk memastikan hasil yang valid dan dapat diandalkan.
IV. ANALISIS DATA DAN PEMBAHASAN
Bagian ini menyajikan hasil penelitian yang diperoleh dari pengujian efisiensi penurunan COD pada biofilter anaerob dan aerob, serta analisis data yang mendukung temuan tersebut.
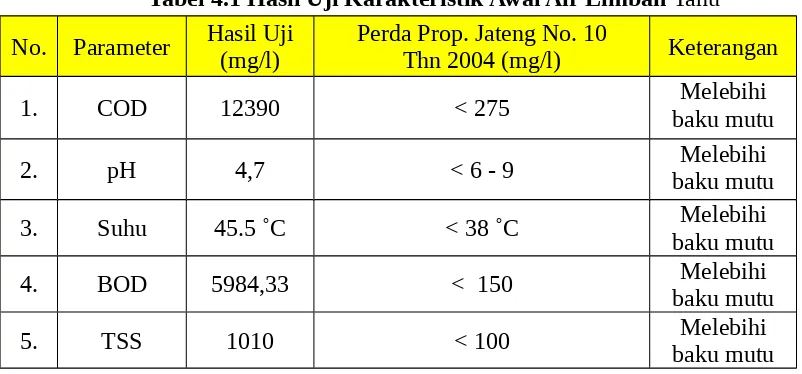
4.1 Karakteristik Air Limbah
Analisis karakteristik air limbah dilakukan untuk memahami komposisi dan konsentrasi COD sebelum dan setelah pengolahan. Data ini penting untuk menilai efisiensi pengolahan yang dilakukan.
4.2 Tahap Penelitian
Tahap penelitian mencakup pengujian yang dilakukan pada biofilter dengan variasi waktu tinggal yang berbeda. Hasil dari setiap pengujian akan dibandingkan untuk menentukan waktu tinggal yang paling efektif.
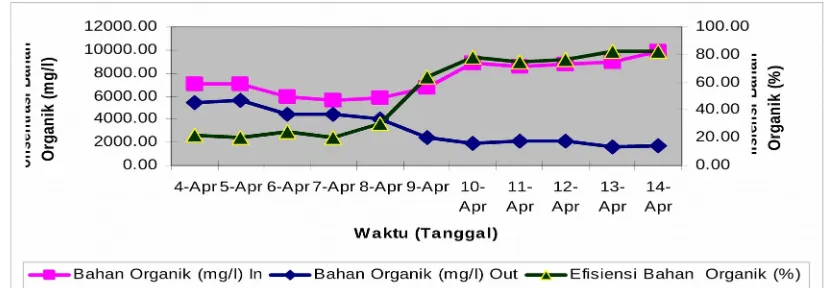
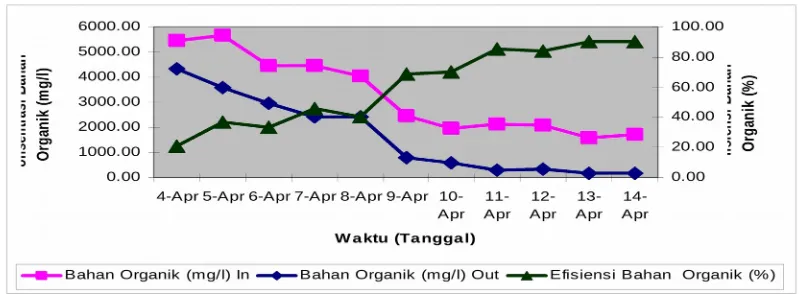
4.3 Hasil dan Pembahasan Penelitian
Hasil penelitian menunjukkan bahwa waktu tinggal yang lebih lama berpengaruh positif terhadap penurunan COD. Efisiensi pengolahan biofilter aerob lebih tinggi dibandingkan anaerob, dengan angka efisiensi yang signifikan.
4.4 Analisa dan Pembahasan Hasil Penelitian
Pembahasan hasil penelitian mengaitkan data yang diperoleh dengan teori yang ada, serta memberikan rekomendasi untuk aplikasi biofilter dalam pengolahan limbah tahu di industri.
V. KESIMPULAN DAN SARAN
Kesimpulan dari penelitian ini merangkum temuan utama mengenai efisiensi penurunan COD menggunakan biofilter. Saran untuk penelitian lebih lanjut dan aplikasi praktis juga diberikan.
5.1 Kesimpulan
Kesimpulan penelitian ini menegaskan bahwa penggunaan biofilter media kerikil efektif dalam menurunkan COD limbah tahu, dengan efisiensi yang lebih tinggi pada proses aerob dibandingkan anaerob.
5.2 Saran
Saran yang diberikan meliputi perlunya penelitian lebih lanjut untuk mengoptimalkan desain biofilter dan mengeksplorasi kombinasi metode pengolahan lainnya untuk limbah tahu.
Referensi Dokumen
- Perbandingan Efisiensi Teknologi Pengolahan Limbah Cair Industri Tahu Secara Aerasi; Flokulasi; Biofilter Anaerob Dan Biofilter Anaerob-Aerob Ditinjau Dari Parameter Bod 5 & Cod ( Pujiastuti, Peni )
- Buku Latihan SPSS Statistik Parametrik ( Santoso, Singgih )
- Pengembangan dan Uji Coba Peralatan Pengolahan Air Limbah Industri Tempa dan Tahu ( Sola, Laban )
- Dasar-dasar Pengelolaan Air Limbah ( Sugiarto )
- Wastewater Treatment ( Sundstrom, Donald W dan Herbert E Klei )